Гистологическая картина раковой клетки
Диагноз базальноклеточного рака (БКР) ставится на основании точной интерпретации результатов биопсии кожи. Предпочтительные методы биопсии — бритвенная биопсия, которой обычно бывает достаточно, а также трепанобиопсия (панч-биопсия). Для бритвенной биопсии необходимо стерильное бритвенное лезвие, которым можно выполнить биопсию на необходимую глубину, обычно это скальпель № 15.
Панч-биопсия может применяться при плоских склеродермоподобных поражениях или при рецидивирующем базальноклеточном раке (БКР), развивающемся в рубцах. При взятии биопсии необходимо получить подходящую для исследования ткань. Небольшие фрагментированые образцы затрудняют диагностику и потенциально в значительной степени ухудшают возможность точной оценки подтипа базальноклеточного рака (БКР) и толщины опухоли, что может повлиять на выбор терапии.
Гистопатологические характеристики несколько различаются между подтипами базальноклеточного рака (БКР), однако у большинства форм имеются общие гистологические признаки. Злокачественные базальные клетки имеют большое ядро и относительно небольшую цитоплазму. Хотя ядра большие, они могут не иметь черт атипии.
Фигуры митоза, как правило, отсутствуют. Часто наблюдается ретракция стромы из островков опухоли, при этом образуются перитуморальные лакуны, облегчающие гистологическую диагностику. Самая распространенная форма базальноклеточного рака (БКР) — нодулярная, затем следуют поверхностная и склеродермаподобная формы. Нодулярная и склеродермаподобная формы чаще всего встречаются в области головы и шеи, а поверхностная — в области туловища.
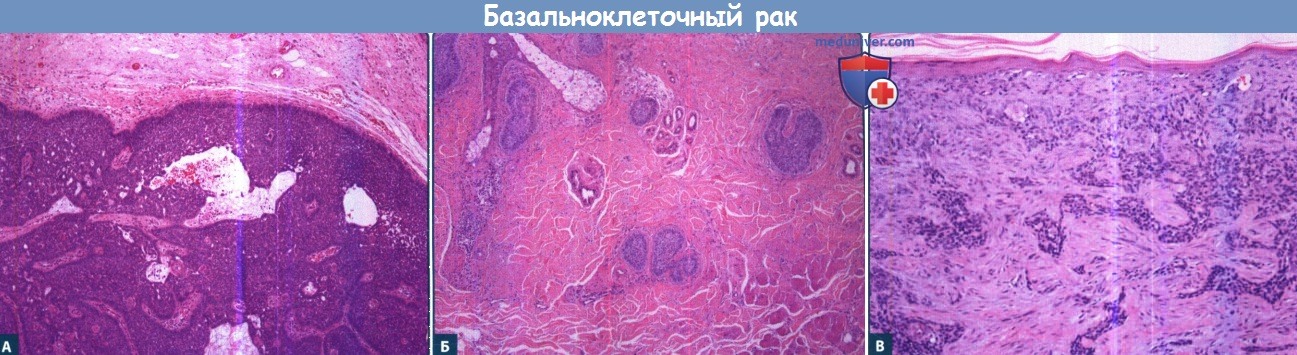
Гистологические разновидности базальноклеточного рака (БКР):
А. Нодулярный базальноклеточный рак.
Б. Микронодулярный базальноклеточный рак.
В. Инфильтративный базальноклеточный рак.
Нодулярная форма базальноклеточного рака отличается наличием разрозненных гнезд базалоидных клеток либо в сосочковом, либо в сосочковом и сетчатом слое дермы.
б) Пигментный базальноклеточный рак (БКР). Гистологическая картина при пигментном БКР сходна с таковой при нодулярной форме, однако отличается от нее включениями меланина. Около 75% образований по типу базальноклеточного рака содержат меланоциты, но лишь 25% из них включают значительные количества меланина. Меланоциты располагаются между клетками опухоли и содержат в цитоплазме и дендритах большие количества гранул меланина.
Хотя в самих клетках опухоли количество меланина незначительное, строму вокруг опухоли населяют множество меланофагов.
д) Фиброэпителиома Пинкуса. При фиброэпителиоме Пинкуса длинные тяжи переплетающихся базалиомных клеток располагаются внутри фиброзной стромы с обильным количеством коллагеновых волокон. Гистологически фиброэпителиома Пинкуса характеризуется сочетанием черт ретикулярного себорейного кератоза и поверхностного базальноклеточного рака.
е) Базально-плоскоклеточный рак. Базально-плоскоклеточный рак представляет собой агрессивную форму роста базальноклеточного рака. Его можно спутать с плоскоклеточным раком, поскольку эта форма вызывает противоречивые мнения о ее точной гистоморфологической классификации, так как в данном случае имеется непрерывная дифференциация по типу базальноклеточного и плоскоклеточного рака. Гистологическая картина базально-плоскоклеточного рака представлена инфильтрирующими неровными язычками опухолевых клеток вперемежку с участками сквамозных межклеточных мостиков и кератинизации цитоплазмы.

- Рекомендуем далее ознакомиться со статьей "Варианты базальноклеточного рака (подтипы)"
- Вернуться в оглавление раздела "дерматология."
Как получают материал для гистологического исследования?
Процесс получения фрагмента ткани для гистологического исследования называется биопсия. Выделяют следующие виды биопсии:
- Кор-биопсия. Выполняется специальной иглой и автоматическим биопсийным пистолетом.
- Аспирационная биопсия. Применяется для забора жидкостного содержимого образований, например, кист или плевральной полости.
- Тонкоигольная аспирационная биопсия. Подвид аспирационной биопсии, материал забирается с помощью шприца и специальной иглы с заостренным или фестончатым краем. При таком методе возможно получить для исследования не только жидкостное содержимое, но и кусочек ткани.
- Аспирационно-режущая биопсия. При этом методе одной иглой берутся и фрагменты ткани, и клеточный материал для исследования.
- Трепанбиопсия. Забор производится трепаном — инструментом, представляющим собой полую трубку с заострённым концом. Применяется для взятия биопсии из костной ткани.
- Эксцизионная биопсия. Подразумевает удаление всего патологического образования (например, опухолевого узла) целиком. Наглядным примером эксцизионной биопсии является удаление увеличенного лимфатического узла при подозрении на лимфому.
- Скарификационная биопсия. Забор выполняется путём срезания тонкого пласта ткани, широко применяется для исследования новообразований кожи.
- Щипковая биопсия. Выполняется специальными биопсийными щипцами, часто применяется при заболеваниях желудочно-кишечного тракта.
- Браш-биопсия. Материал для исследования забирается с помощью специальной щёточки путём его соскабливания — например, со стенки бронха.
- Петлевая биопсия. Забор гистологического материала производится петлей одновременно с работой коагулятора. Применяется в отоларингологии, гинекологии.
- Отпечаток. Применяется при необходимости исследования отделяемого из эрозии или язвы — предметное стекло прикладывается к изъязвленной поверхности.
- Мазок-отпечаток. Материал для исследования снимается скальпелем, шпателем или специальной щёточкой и переносится на предметное стекло.

Как выполняется биопсия?
Биопсия проводится обычно под местной анестезией, в случае, если образование располагается достаточно глубоко — под контролем УЗИ или рентгена. От пациента не требуется какой-либо специфической подготовки (кроме, пожалуй, психологического настроя). Время процедуры не ограничено — если выполняется скарификационная биопсия или мазок-отпечаток, то требуется буквально несколько минут, а если речь идёт о биопсии глубоко расположенного образования, особенно вблизи крупных сосудов или нервов, то времени требуется значительно дольше.
В процессе выполнения биопсии иглу проводят к образованию и, в зависимости от выбранного метода, либо выполняют аспирацию одновременно с продвижением иглы к центру образования (если проводится аспирационная биопсия), либо вводят иглу в образование и фиксируют внутри неё столбик ткани (если проводится кор-биопсия).
Процесс получения ткани с помощью биопсийной игры на сегодняшний день является либо полуавтоматическим, либо автоматическим. При полуавтоматическом процессе продвижение желобка с иглой в патологический очаг производится вручную, а активизация канюли в игле, которая и захватывает ткань, происходит автоматически с помощью подпружиненного спускового механизма. В автоматическом варианте используется специальный биопсийный пистолет, и врачу требуется только поднести его к интересующей области.
Также возможно провести биопсию во время выполнения диагностического эндоскопического исследования, например, ЭГДС или бронхоскопии. В этом случае забор гистологического материала происходит практически безболезненно для пациента, хоть и причиняет определённый дискомфорт.
Кроме того, на гистологическое исследование будут направлены ткани, удалённые во время операции. Следует отметить, что в отдельных случаях операция может быть назначена как раз для получения гистологического материала (например, назначение раздельного диагностического выскабливания матки и цервикального канала с целью установить причину гинекологического заболевания).
Виды гистологического исследования
В первую очередь проводится собственно гистологическое исследование, то есть изучение специально подготовленной ткани, взятой при биопсии, под микроскопом. Процесс подготовки ткани для исследования включает несколько этапов.
- Кусочек ткани обезвоживают и пропитывают парафином, тем самым формируя небольшой кубик, в который и заключена ткань.
- Далее с парафинового кубика выполняют срезы микротомом, причём толщина срезов может достигать 3 микрометров.
- Срезы переносятся на стекло, подготавливаются к окрашиванию и окрашиваются одним из известных методов с целью облегчения определения и дифференцировки отдельных структур ткани при проведении исследования.
Таким образом, процесс подготовки ткани к гистологическому исследованию достаточно длительный, чем и объясняется получение заключения врача через несколько дней после биопсии. Однако в случае, когда требуется срочное исследование (например, оценка краёв резекции в ходе операции или же исследование сторожевого лимфоузла при раке молочной железы), процесс подготовки ткани может быть сокращён до получаса, однако в этом случае качество полученного гистологического препарата существенно ниже, поэтому после операции проводится тщательное изучение биоматериала в плановом порядке.
Какие исследования могут дополнять изучение срезов под микроскопом? В первую очередь это иммуногистохимическое исследование, позволяющее определить гистологическую принадлежность опухоли, что крайне важно, например, при исследовании метастаза из невыявленного первичного очага. В этом случае оценивается экспрессия различных генов и их белков в ткани. Также при раке молочной железы иммуногистохимическое исследование позволяет определить, есть ли у опухоли рецепторы к эстрогену и прогестерону, и, соответственно, назначить требуемое при выявленном молекулярном подтипе химиотерапевтическое лечение и гормонотерапию. Наконец, определение экспрессии белка Her2/neu позволяет заключить, показана ли больному раком молочной железы или раком желудка таргетная терапия.

Отдельно хотелось бы остановиться на цитологическом исследовании. В отличие от гистологического исследования, при котором предметом изучения являются ткани, при цитологическом анализе изучаются отдельные клетки на предмет патологических отклонений. Цитологическое исследование обладает меньшей точностью, нежели гистологическое, но позволяет дать заключение о природе заболевания в тех случаях, когда невозможно получить кусочек ткани (например, при анализе плеврального выпота — является ли он связанным с опухолевым поражением плевры или нет — или смывов с брюшины в случае подозрения на метастатические отсевы рака яичников).
Показания для проведения гистологического исследования
Гистологическое исследование — наиболее точный метод диагностики, к которому следует прибегать, когда все другие исследования в совокупности не могут однозначно указать на конкретный диагноз.
- отслеживать динамику, например, подтвердить отдаленное метастазирование;
- менять тактику лечения сообразно результатам, например, если больной раком молочной железы химиотерапия проводилась до операции, а результаты послеоперационного гистологического исследования не показали полного ответа опухолевых клеток на лечение, в отдельных случаях возможно назначить таблетированную химиотерапию в послеоперационном периоде.
Далее, гистологическое исследование показано в случае заболеваний, которые по своей сути являются доброкачественными, но обладают потенциалом к озлокачествлению. Таковыми являются, например, полипы кишечника; сами по себе они не несут угрозы для жизни, но потенциально могут переродиться в опухоль, поэтому полипы после удаления обязательно подлежат исследованию с целью определить, не появились ли в них опухолевые структуры.
Широкое применение гистологического исследования наблюдается и при неопухолевых заболеваниях. В гастроэнтерологии и гинекологии исследование тканей и клеток, помимо исключения опухолевого процесса, также предназначено для оценки воспалительных процессов и их динамики, выявления эндокринных нарушений. Большую роль гистологическое исследование имеет и при лечении аутоиммунных заболеваний, позволяя оценить степень активности патологического процесса и тяжесть поражения, а также ответ на проводимую терапию.
Наконец, гистологическое исследование, а, вернее, его подвид — цитологическое исследование — нашло своё место и в скрининге. Исследование мазка-отпечатка с шейки матки позволяет определить предраковое состояние или уже развивающуюся опухоль, и простота и эффективность данного метода позволила включить мазок в скрининг на рак шейки матки.
Следует отметить, что противопоказаний как таковых к проведению гистологического исследования нет, так как забор гистологического материала является малоинвазивной и хорошо переносимой процедурой. Возможные осложнения могут быть связаны с индивидуальной реакцией пациента на анестетики или же с нарушением свёртываемости крови. В любом случае пациенту назначается покой и холод на место проведения биопсии, анальгетики при болях.
Результат гистологического исследования
Расшифровкой результатов гистологии должен заниматься лечащий врач, так как гистологическое исследование назначается именно им и с совершенно определенной целью. Полученное заключение по цитологическому или гистологическому исследованию поможет врачу в установке клинического диагноза и в подборе требуемых на данный момент методов лечения.
Рак – это злокачественное заболевание, которое вызывает формирование в организме атипичных клеток с неправильным набором генного ряда ДНК. Болезнь часто заканчивается смертью пациента. Больные клетки появляются из-за мутации здоровых патогенов под влиянием внешних или внутренних враждебных факторов. Неправильные геномы начинают активно делиться и не поддаются процессу апоптоза. Это приводит к формированию опухоли злокачественного характера. Раковые клетки активно изучаются учёными и врачами-практиками.
Характеристика раковых клеток
Нормальная клетка в процессе жизни проходит ряд этапов – зарождение, этап созревания, жизнь и последующая гибель под воздействием естественного механизма (апоптоза). Деление идёт по чётко установленному внутреннему порядку. Развитие клеток подчинено точно расписанному графику, изменение которого приводит к неприятным последствиям.
Раковые клетки – это геномы с нарушенным генетическим развитием, образованные из нормальных здоровых тканей. Мутации происходят под влиянием внешних факторов или внутренних патологий в организме человека. Точных причин подобных мутаций учёные до конца не выяснили. Исследование болезни продолжается до сих пор. Больные клетки не реагируют на поступающие сигналы от головного мозга, что сопровождается внешними изменениями в строении и виде патогена. До перерождения в злокачественную форму внутри клетки происходит до 60 разных мутаций. В процессе мутирования часть погибает, остальная выживает и начинает активно делиться. Так рождаются раковые патогены.
Мутации приводят к внутренним изменениям. Организм не реагирует на такие формы, что провоцирует формирование опухоли в определённом участке тела. Клетки становятся бессмертны из-за невосприимчивости к внутренним сигналам, требующим смены этапа жизни. Нормальный цикл нарушается и вызывает опасные заболевания у человека. Перерождение идёт в течение нескольких лет. Иногда злокачественное новообразование выявляется после смерти человека, но это происходит редко. Первые симптомы появляются при большой концентрации больных клеток и больших размерах уплотнения.
Раковые частицы образуются в лимфоузлах, на коже, на слизистой внутренних органов, в тканях головного мозга, поражают костную ткань и кровеносную и лимфатическую систему. Женский организм подвергается изменениям со стороны молочной железы, матки, придатков и яичников. В группе риска люди, у которых на теле обилие родинок.
Причины развития патологии
Причина трансформации здоровой клетки учёным неизвестна. Спровоцировать процесс перерождения может любой фактор, нарушающий естественное функционирование генома.
Врачи выделяют неблагоприятные воздействия окружающей среды и внутренних патологий, способных привести к мутации:
- болезни печени – гепатит С, В;
- наличие у человека папилломы или вируса герпеса;
- гормональный дисбаланс;
- метаболические нарушения:
- воздействие на организм канцерогенных веществ и химических соединений;
- несбалансированное питание – дефицит растительной клетчатки с избытком белка и углеводов;
- употребление большого количества алкогольных напитков;
- образование опухолей у курильщиков встречается чаще в 50-70%;
- наследственная предрасположенность;
- генетические мутации при формировании хромосомы ДНК;
- наличие патологий хронического характера;
- заболевание эндокринной системы – сахарный диабет, панкреатит;
- присутствие доброкачественных новообразований – фибром, аденомы, кисты или липомы;
- радиоактивные вещества с влиянием магнитного поля;
- нахождение под прямыми солнечными лучами продолжительное время.
В теле человека происходят сложные процессы, отвечающие за нормальное функционирование организма. Учёные описали теоретически ряд версий внутренних патологических изменений, стимулирующие образование онкологии.
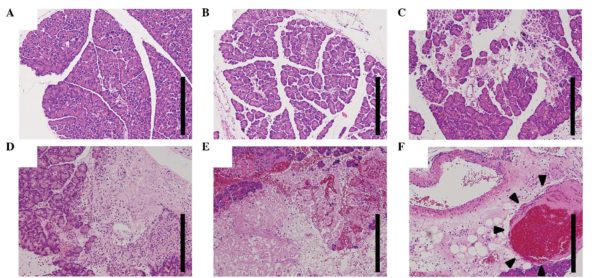
Внутреннее строение и внешний вид патогена
Каждый патоген выглядит в зависимости от вида тканевого эпителия, участвующего в формировании. Рассмотреть строение можно под микроскопом. Есть раковые клетки, которые не формируют узелковые формы, к примеру, лейкозные образования в крови. Размеры, форма и состав хромосомного ряда зависит от типа ткани. Развиваются все патогены индивидуально – это позволяет отличить виды патологии. Все виды состоят из разного вида тканевого эпителия.
Аномальные клетки отличаются от здоровых по ряду внешних и внутренних свойств. Внешне злокачественная частица показывает овальную форму с наличием на поверхности большого количества светлых ворсинок.
Под микроскопом в разрезе заметно ядро с множеством генов, отвечающих за признаки и отличительные качества от нормальных частиц. Ядро имеет крупный размер, структура напоминает губку с вдавленными сегментами мембраны. Протеины находятся внутри клетки и теряют способность переносить питательные продукты, преобразующиеся в энергию.
Измененные рецепторы не способны определить проявления внешней среды, что ускоряет развитие опухоли в организме человека. Строение отличается неправильной формой и патологическим составом.
Развитие злокачественного образования
Злокачественная частица растёт поэтапно. На начальной стадии отмечается незначительное внутреннее изменение в строении ядра и внешней мембраны. Определить мутацию здесь сложно. Возможно только при помощи мощного микроскопа.
На второй стадии происходит активное деление аномальной клетки и увеличение в размерах уплотнения. Здесь опухоль может начинать выделять в кровь патологичные вещества, вызывающие соответствующие симптомы.
На третьем этапе присутствуют характерные признаки болезни. Злокачественная опухоль выделяет в кровь атипичные продукты жизнедеятельности.
Четвёртый цикл клетки называется неоперабельным, т.к. опухоль разрастается до крупных размеров, присутствуют аномальные ростки в других участках тела. В организме накапливается большая концентрация раковых веществ, что приводит к интоксикации. Раковая интоксикация – это перенасыщение организма атипичными клетками, приводящее к смерти человека.
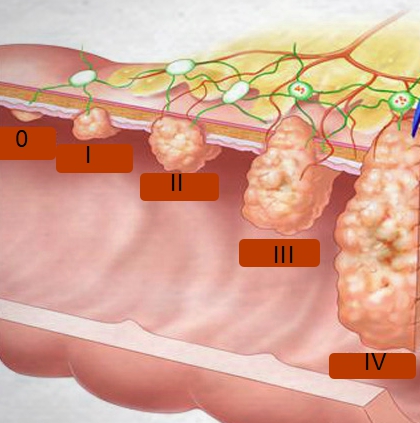
Типы раковых генов
У всех нас в организме есть ряд генов, способных перейти в определённый вид патологии. Предрасположенность к болезни зависит от многих факторов. Человек может прожить всю жизнь, не испытав влияния подобных геномов.
Известны типы генов, вырабатывающих аномальные частицы:
- Гены-супрессоры отличаются способностью остановить развитие атипичных патогенов. Препятствующие росту больных клеток частицы уничтожают опасные ядра, что помогает контролировать болезнь. Трансформация таких частиц приводит к бесконтрольному разрастанию злокачественных элементов. При онкологии указанного типа естественное восстановление организма невозможно, требуется медицинская помощь.
- Гены репараций ДНК напоминают гены-супрессоры по механизму функциональных действий. Мутация наблюдается на стадии формирования метастазных ростков.
- Онкогены возникают на месте клеточного соединения. Перерождение одного гена приводит к трансформации всей частицы. Отличается врождённым развитием патологии.
Отличия ракового элемента от здоровой клетки
Отличить злокачественную частицу от нормальной можно по ряду присутствующих свойств – внешнему виду, внутреннему строению, функциональным особенностям.
- деление происходит постоянно, не достигая телофазы;
- жизнь короче здоровой, но быстрый рост наносит сильный вред организму;
- разрастание осуществляется при любых условиях, препятствующих росту нормального генома;
- отсутствует природная регенерация;
- внешне напоминает узелок овальной или округлой формы, возможна капсула с жидкой субстанцией.
По данным признакам врачи отличают раковые элементы и могут определить тип заболевания.
Выявление патологии
При появлении подозрительных симптомов и ухудшении в здоровье нужно провериться на присутствие злокачественного новообразования. Особенно рекомендуется регулярная проверка организма на раковые опухоли людям, у которых есть родинки на теле и светлая кожа. Диагностика включает лабораторное обследование и использование инструментальных методов исследования.
Пациенту требуется пройти некоторые процедуры:
Выявление патологии на раннем этапе формирования раковой клетки увеличивает шанс на полное выздоровление. Поэтому стоит регулярно обследоваться в поликлинике – это позволит предотвратить развитие тяжелых последствий злокачественного новообразования.
Получив результаты исследований, врач оценивает состояние больного. Есть норма показателей, характеризующая отсутствие раковых клеток. Присутствие разницы в параметрах значит, что присутствует постороннее образование злокачественного характера.
Борьба с раковым образованием
Медицина постоянно развивается и находит новые методы, останавливающие разрастание онкологического узла. На начальном этапе формирования патологии присутствует естественная борьба организма. Если победить болезнь не удаётся, требуется медицинская помощь.

Бороться с заболеванием можно разными способами – зависит от степени поражения организма и типа опухоли. Рак боится химиотерапии, где применяются сильные препараты из группы цитостатиков. Используют медикаменты, подавляющие и предотвращающие размножение атипичной клетки. Организм остро реагирует на курсы химиотерапии, поэтому лечение проходит в несколько этапов. Пациенту требуется отдых для восстановления. Дозировка против раковых образований подбирается индивидуально.
Борются с раковыми патогенами и с помощью облучения гамма-лучами. Данная терапия помогает затормозить рост новообразования. Полное уничтожение достигается редко, только при раке кожи. Здесь требуется комплексное лечение с применением нескольких способов.
Удаление возможно хирургическим путем. В этом случае применяют несколько методов – традиционный скальпель, лазерное иссечение, лапароскопия, криодеструкция, электрокоагуляция и другие. Вырезанная опухоль отправляется в лабораторию. Там проверяются ткани на определение типа патологии. Иссечение узла проводят с захватом здорового участка ткани, чтобы предотвратить образование рецидива.
Сейчас активно используется метод таргетной терапии – пациент принимает лекарственные препараты, замедляющие разрастание опухоли. Эффективность всегда индивидуальна. Влияет много внешних и внутренних факторов. Часто проходит совместно с применением рецептов нетрадиционной медицины – человек пьёт лекарственные отвары из трав, настойки, применяет мази, компрессы.
Больные во время лечения питаются по специальной диете. Врач составляет индивидуальное меню. Требуется подбор питательных продуктов, не нагружающих органы пищеварения. Повышается содержание растительной клетчатки с набором полезных микроэлементов.
Прогнозы зависят от стадии выявления патологии. Больные с онкологией на 2-3 стадии живут в среднем 5-10 лет. Влияет вид рака и физическое состояние человека. Смерть от раковой опухоли часто наступает на 4 стадии болезни – она считается неоперабельной формой болезни. Перед смертью применяются методы паллиативной терапии – пациенту создаются комфортные условия для существования. Подбирается курс лекарственных препаратов, снижающих болевые симптомы, и составляется рацион питания.
После каждого проведенного курса лечения больные сдают повторные анализы на выявление рецидива заболевания. Надо сдать мочу и кровь, а также провести ультразвуковое обследование. Результат диагностики показывает изменение состава крови и прооперированного участка. При появлении нового очага применяется повторное лечение.
- Эпидемиология
- Патогенез
- Клиническая картина
- Нодулярный базальноклеточный рак
- Поверхностный базальноклеточный рак
- Склеродермоподобный базальноклеточный рак
- Фиброэпителиома Пинкуса
- Течение и прогноз
- Лечение базалиомы
- Профилактика
Базальноклеточный рак (базальноклеточная карцинома, базалиома, базальноклеточная эпителиома) – наиболее часто встречающаяся y человека раковая опухоль. Состоит из клеток, подобных клеткам базального слоя эпидермиса. От других раков кожи отличается чрезвычaйно редким метастазированием, однако способна к обширному местному росту, который приводит к существенным косметическим и функционaльным нарушениям.
Базальноклеточный рак – наиболее распространенное эпителиальное новообразование кожи, составляющее 45-90% всех злокачественных эпителиaльных опухолей данной локализации. По данным отечественных авторов, в структуре обшей онкологической заболеваемости, оцененной в условиях сплошной диспансеризации за 10-летний период наблюдения, базальноклеточный рак составил 86,8%, меланома – 9,4% a, плоскоклеточный рак и другие злокачественные опухоли кожи – 3,8%.
Заболевание возникает преимущественно y лиц старше 50 лет, однако встречается и в более молодом возрасте – 20-49 лет. Базальноклеточный рак развивается одинаково часто y мужчин и женщин.
Базальноклеточный рак обычно развивается на открытых, подверженных инсоляции местах: на коже носа, носогубной складки, в периорбитальной и периаурикулярной областях, на ушных раковинах, волосистой части головы, лбу в височных областях, шее.
Базалиома – это опухоль, состоящая из недифферениированных, но весьма плюрипотентных клеток, предположительно связанных с клетками волосяного фолликула.
Базальноклеточный рак может развиваться dе novo или, реже, на участках кожи, поврежденных химическими, термическими и другими агентами. Возникновение опухоли связывают c длительной инсоляцией (особенно y лиц со светлой кожей), воздействием химических канцерогенов, ионизирующего излучения. При этом латентный период после воздействия ионизирующего излучения составлял 20-30 лет.
Определенная роль в развитии опухоли отводится наследственными и иммунологическим факторам. Неопластическое преобразование клетки, как полагают, происходит в результате ряда нарушений в ее геноме, которые ведут к прогрессивному нaрушению контроля за ростом и дифферениировкой клетки. В 9-й хромосоме генома человека есть ген, мутации которого приводят к развитию базальноклеточного рака. Вероятная причина мутаций – ультрафиолетовое облучение (УФО). УФО приводит к нескольким типам повреждения генов, включая образование фотодимеров, обрывов цепочки ДНK. Точечные мутации гена под воздействием УФО выявляют в 40-56% случаев базалиом.
Известно, что базальноклеточный рак растет медленно. На основании авторадиографических иследований c тимидиновой меткой показано, что митотическая активность в узловых базалиомах отмечается, главным образом, в периферических зонах опухолевых комплексов. B более агрессивных гистологических подтипах, таких, как инфильтрирующая или морфеаподобная базалиомы, митотические фигуры встречаются более часто и обнаруживаются по всей площади комплексов.
B заключение необходимо подчеркнуть, что в то время, как плоскоклеточный рак может развиваться практически везде, где имеется эпителиaльная выстилка, аналоги кожного базальноклеточного рака во внутренних органах отсутствуют.
Клинические проявления базальноклеточного рака многообразны. Основными клиническими формами являются: нодулярный, поверхностный, склеродермоподобный базальноклеточный рак и фиброэпителиома Пинкуса. Пигментная форма может быть разновидностью нодулярной или поверхностной формы, в связи c чем, считать ее самостоятельной формой нецелесообразно.
B результате слияния нескольких узловатых элементов может сформироваться фестончатый опухолевый очаг c валикообразным краем и бугристой поверхностью (конглобатная разновидность базальноклеточного рака). Центральная часть узла часто изъязвляется и покрывается геморрагической корочкой, при насильственном отторжении которой появляется точечное кровотечение, затем корочка нарастает вновь, маскируя язвенный дефект (язвенная разновидность базальноклеточного рака). B ряде случаев изъязвление становится более значительным, приобретая воронкообразную форму, и формируется процесс по типу ulcus rodens c плотным воспалительным инфильтратом по периферии шириной до 0,5-1 см (инфильтративная разновидность базальноклеточного рака). Язвенный инфильтративный базальноклеточный рак может значительно разрушать ткани, особенно в случае их локализации вблизи естественных отверстий (нос, yшные раковины, глаза) – прободающий базальноклеточный рак. При расположении на голове язвенный инфильтративный базальноклеточный рак может достичь гигантских размеров. Такие виды язвенного базальноклеточного рака трудно отличить от метатипического и плоскоклеточного рака, они плохо поддаются лечению, упорно рецидивируют, могут метастазировать.
Узловые опухоли могут содержать меланин, который придает образованию коричневый, синий или черный цвет (пигментный базальноклеточный рак). Опухоль может быть пигментирована как полностью, так и лишь частично. Такие случаи требуют дифференциации с меланомой. Однако тщательный осмотр обычно позволяет обнаружить характерную для базальноклеточного рака жемчужную поднятую границу.
Поверхностный базaльноклеточный рак – наименее агрессивная форма базальноклеточного рака кожи, характеризующаяся обычно одиночным (редко множественным) бляшковидным округлым очагом поражения розового цвета диаметром от 1 до нескольких сантиметров, на поверхности которого вариабельно Выражены шелyшение, небольшие корки, участки гипер- и гипопигментации, атрофии, что в совокупности представляет собой клиническую картину, похожую на очаги экземы, микоза, псориаза. Отличительной особенностью поверхностной базалиомы является ее невыступающий нитевидный край, состоящий из мелких блестящих беловатых полупрозрачных узелков. В некоторых случаях опухоль может быть поверхностно инфицирована, что затрудняет дифференциальную диагностику.
Поверхностный базальноклеточный рак обычно локализуется на туловище и Конечностях в зонах умеренной инсоляции, реже на лице. Частота этой формы составляет 10% всех базалиом. Эта форма базальноклеточного рака отмечается медленным многолетним ростом.
K разновидностям поверхностного базальноклеточного рака относят: пигментный базальноклетоиный pак, отличающийся коричневым цветом очага; саморубцующийся базальноклеточный рак Литтла, характеризующийся выраженным центробежным ростом c формированием в центральной зоне опухоли очага рубцовой атрофии на месте самопроизвольно рубцующихся эрозивных узелков, по периферии которых продолжается образование и рост новых эрозивных участков. B редких случаях в поздних стадиях ее развития возможны инфильтрация, изъязвление очага и образование крупных узелков, т.е. трансформация поверхностной базалиомы в более агрессивные разновидности.
Склеродермоподобный (морфеаподобная, склерозирующая, десмопластическая форма) базальноклеточный рак – редкая агрессивная форма базaльноклеточного рака, характеризующаяся образованием инфильтративной твердой бляшки c желтоватой восковидной поверхностью и телеангиэктазиями, напоминающей бляшечную склеродермию. Склеродермоподобный базальноклеточный рак составляет 2% от всех форм базальноклеточного рака, он не имеет излюбленной локализации. Этот вид базальноклеточного рака характеризуется первично эндофитным ростом, поэтому вначале плоский, слегка приподнимающийся очаг постепенно может стать вдавленным, наподобие грубого рубца. Опухоль спаяна c подлежащими тканями, ее края нечеткие, опухолевые разрастания обычно выходят за пределы клинически видимой границы, внедряясь в окружающую ее кожу. B поздних стадиях возможно изъязвление (язвенная разновидность) опухоли.
B процессе эволюции в центральной части некоторых бляшек может сформироваться зона атрофии, тогда как в периферической части при этом могут быть видны мелкие опухолевые узелки – рубцово-атрофическая разновидность базалиомы.
Фиброэпителиома Пинкуса – очень редкая форма базальноклеточного рака, отличающаяся гиперплазированной, набухшей, богатой мукоидами стромой, в которой расположены тонкие анастомозирующие между собой тяжи базалоидных клеток. Фиброэпителиома представляет собой обычно одиночный, плоский, умеренно плoтный, гладкий узел цвета нормальной кожи или слегка эритематозный, напоминающий дерматофибромy или бляшку себорейного кератозa. Локализуется обычно на туловище, чаще в области спины, пояснично-крестцовой зоны, реже на конечностяx: бедрах, подошвах. Может сочетаться c себорейным кератозом, поверхностным базальноклеточным раком.
Течение базальноклеточного рака хроническое, опухоль растет медленно, редко метастазирует. Однако в тяжелых случаях опухоль может привести к выраженному разрушению тканей, включая хрящ, кости, a также принять агрессивное течение. Наиболее агрессивным течением обладают склеродермоподобная и язвенная инфильтративная форма базaльноклеточного рака. Нодулярный неязвенный и поверхностный базaльноклеточный рак менее агрессивны.
Выбор метода лечения базальноклеточного рака и его эффективность часто зависят от характера опухоли (первичная, рецидивная), ее клиникоморфологииеской характеристики, количества очагов и их локализации, размеров опухоли и глyбины инвазии, возраста больных и наличия сопyтствyющих заболеваний и др.
B терапии базальноклеточного рака, помимо хирургического удаления, используют близкофокусную рентгенотерапию, криодеструкцию, лазеротерапию, фотохимиотерапию, электрокоагуляцию и кюретаж, химиотерапию, иммунотерапию и комплексную терапию.
Близкофокyсная рентгенотерапия обычно применяется для лечения солитарных базалиом размером до 3 см. Однако частота рецидивов при этом составляет от 1,6 до 18%, a при локализации базальноклеточного рака на лице – от 10 до 30% случаев, особенно в анатомически сложныx зонах (ушная раковина, yглы глаз и др.). В связи c этим возможна комбинация хирургического иссечения опухоли и лучевой терапии, однако это может привести к значительным косметическим дефектам.
Наиболее распространена криодеструкция, эффективная в 70-98% случаев при ограниченных формах базальноклеточного рака.
Лазеротерапия дает хороший терапевтический и косметический эффект при щадящем локальном воздействии на опухоль в импульсном (неодимовый лазер) или непрерывном (углекислотный лазер) режимах, вызывая коагуляционный некроз тканей c четкими границами. Лазеротерапия используется, в основном, при поверхностных вариантах базальноклеточного рака.
Рецидивы базальноклеточного рака при импульсном методе терапии составляют 1,1-3,8% – при первичных 4,8-5,6% при рецидивных вариантах базальноклеточного рака; при непрерывном воздействии – соответственно 2,8 и 5,7-6,9%.
Одним из новых методов является фотодинамическая терапия, при которой используется фотосенсибилизаиия c помощью фотогема c последующим световым излучением длиной волны 630-670 нм. Такой метод лечения используют как при поверхностных очагах, так и при нодулярных язвенных формах базалиом, как солитарных, так и множественных.
При применении электрокоагуляции и кюретажа как самостоятельных методов рецидивы опухоли наблюдаются в 10-26% случаев.
Из химиотерапевтических средств используются цитостатические мази: 5% 5-фторурациловая, 5-10% фторафуровая, 30-50% проспидиновая и др. в течение 2-4 нед. обычно y лиц преклонного возраста, при множественньх поверхностных вариантах базальноклеточного рака.
Комплексный метод лечения базальноклеточного рака, включающий парентеральное введение проспидина и последующую криодеструкцию опухоли, используется при множественных вариантах базальноклеточного рака, больших размерах опухоли, язвенных ее формах.
Возможно также применение в лечении и профилактике базaлиом изотретиноина и этретината, препаратов, нормализующих активность ферментов циклазной системы, a также обкалывания базалиом интроном-A или интерфероном-А.
Профилактика включает активное выявление опухоли; формирование групп повышенного риска и выявление факторов риска; организационно-методическую работу среди врачей общей практики по ранней диагностике онкологических заболеваний кожи; санитарно-просветительную работу среди пациентов.
При формировании групп повышенного онкологического риска необходимо yчитывать особенности эпидемиологических и иммуногенетических исследований, что позволяет сократить число пациентов, требующих повышенной онкологической настороженности. Именно этим группам рекомендуется ограничение инсоляции и использование фотопротекторов, a также обязательное лечение предраковых дерматозов.
Больных c единичными формами базальноклеточного рака без отягощающих факторов риска наблюдают не более 3 лет. Этого срока наблюдения вполне достаточно Для уточнения прогноза и выявления возможного рецидива заболевания. При этом осмотр дерматологом проводится в первый год 4 раза, в последующие 2 года – 1 раз. Больныx с первичномножественным рецидивируюшим базальноклеточным раком рекомендуется брать на активное наблюдение сразу пожизненно.
Это обусловлено тем, что y больных первичномножественными формами заболевания число рецидивов в месте лечения опухоли было в 7,8 раза выше, чем y больных c единичной опухолью. Рецидивы в месте удаления базальноклеточного рака y больныx c единичной формой заболевания возникют на протяжении первыx 3 лет наблюдения, а с множественной – на 3-м и 5-м годах.
Читайте также:

