Лучевая терапия что это такое и последствия при раке костей
Выбор тактики лечения и прогноз определяются типом рака кости, который диагностирован у пациента, и некоторыми другими факторами.
Разновидности рака костей
Остеосаркома — наиболее распространенная разновидность первичного рака костей. Чаще всего встречается в возрасте 10–30 лет, как правило, возникает в костях рук и ног, таза. Мужчины болеют чаще по сравнению с женщинами. Менее 10% случаев остеосаркомы приходится на людей старше 60 лет.
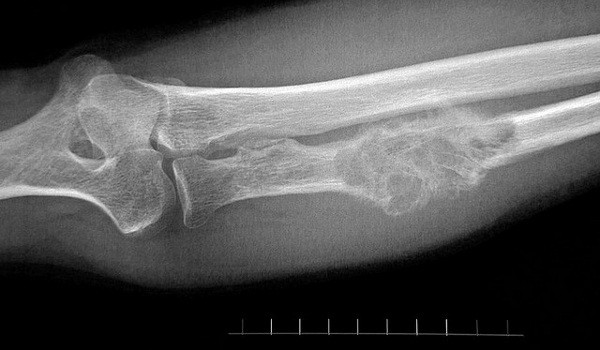
Хондросаркомы происходят из хрящевой ткани, это второй по распространенности тип первичного рака костей. Молодые люди до 20 лет болеют очень редко. С 20 до 75 лет риск возникновения хондросаркомы постепенно нарастает, мужчины и женщины болеют примерно одинаково часто. Хондросаркомы могут возникать в костях рук и ног, таза, черепа, в лопатке. Они могут начать расти и во внутренних органах, в которых присутствует хрящевая ткань, например, в гортани, трахее.
Саркома Юинга — третий по распространенности тип рака костей. Поражает детей, подростков, молодых людей. После 30 лет заболевание встречается крайне редко. Чаще всего опухоль локализуется в костях таза, нижних и верхних конечностях, лопатках, ребрах.
Злокачественная фиброзная гистиоцитома обычно локализуется в мягких тканях, в редких случаях — в костях. Заболевание преимущественно встречается в среднем и пожилом возрасте. При костной локализации чаще всего поражаются кости ног в области колена. Злокачественная фиброзная гистиоцитома склонна к локальному росту, но иногда может давать метастазы, например, в легких.
Фибросаркома также чаще встречается в мягких тканях. У людей среднего и пожилого возраста может поражать кости рук, ног.
Хордома — опухоль, которая чаще всего находится в основании черепа или позвоночном столбе. Обычно диагностируется после 30 лет, у мужчин примерно вдвое чаще, чем у женщин. Хондромы склонны к медленному локальному росту, в редких случаях дают метастазы в лимфатические узлы, печень.
Лечение рака костей
Лечением пациента со злокачественной опухолью костной ткани занимается команда врачей, в которую могут входить: онколог, хирург, специализирующийся в сфере ортопедии, химиотерапевт, врач лучевой терапии, ортопед, реабилитолог, психоонколог.
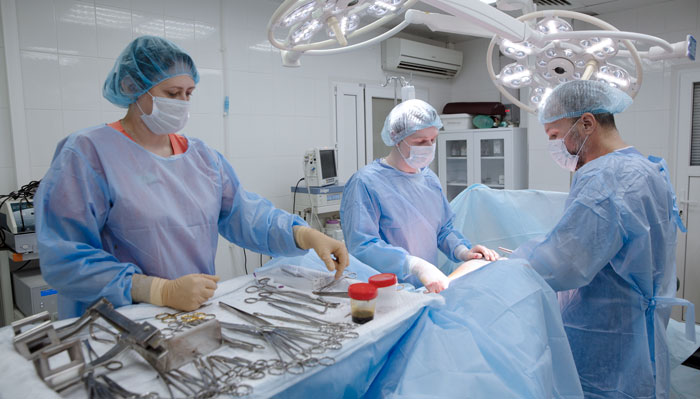
Хирургическое лечение рака костной ткани
Хирургия — основной радикальный метод лечения рака костей. В прошлом у большинства пациентов прибегали к ампутации — удалению всей конечности или ее части, пораженной опухолью. В настоящее время хирурги стараются отдавать предпочтение органосохраняющим вмешательствам. Удаленную часть кости заменяют костным трансплантатом или эндопротезом из металла, других материалов. Если приходится удалять фрагмент бедренной или плечевой кости, нижележащую часть конечности можно сохранить. При этом рука или нога станет короче, но сможет ограниченно выполнять свои функции.
Иногда в качестве альтернативы хирургическому вмешательству применяют криодеструкцию (разрушение опухолевой ткани низкой температурой), кюретаж (выскабливание специальным инструментом), введение в отверстие в кости цемента из полиметилметакрилата (при затвердевании он нагревается и разрушает опухолевые клетки).
Лучевая терапия при раке костей
Для того чтобы уничтожить опухолевые клетки в кости, требуются высокие дозы излучения, которые приводят к серьезным побочным эффектам. Поэтому лучевая терапия при раке костей находит ограниченное применение:
- Если опухоль невозможно полностью удалить хирургически.
- При положительном крае резекции по данным биопсии после операции.
- В качестве паллиативного метода лечения при рецидиве, чтобы уменьшить боль и отек.
Наиболее широкое применение лучевая терапия находит при саркомах Юинга.

Химиотерапия при раке костей
Химиотерапию чаще всего применяют для лечения остеосарком и сарком Юинга. Другие виды рака костей реагируют на нее плохо. Применяют различные химиопрепараты: цисплатин, доксорубицин, ифосфамид, этопозид, метотрексат, циклофосфамид, винкристин.
Иногда применяют таргетные препараты — лекарственные вещества, которые блокируют молекулы, необходимые для роста и выживания злокачественных опухолей.
Лечение при метастазах рака в костях
При лечении метастазов в костной ткани используют химиопрепараты, которые эффективны против первичной опухоли. Применяют лучевую терапию. Если метастатические очаги приводят к значительному разрушению костной ткани, назначают бисфосфонаты. Эти препараты вводят внутривенно каждые 3–4 недели, они помогают предотвратить патологические переломы, уменьшить боль, снизить уровень кальция в крови.

Хирургическое лечение носит паллиативный характер. При патологических переломах кости укрепляют с помощью винтов, стержней и других металлических конструкций. Иногда прибегают к радиочастотной аблации: в опухоль вводят иглу и подают на нее ток высокой частоты, который разрушает опухолевые клетки.
Реабилитация после лечения рака костей
После ампутации конечности показано протезирование. При правильно спланированных реабилитационных мероприятиях пациенты, перенесшие ампутацию нижней конечности, обычно могут снова ходить спустя 3–6 месяцев.
После органосохраняющих операций реабилитационный период продолжается дольше. Способность ходить восстанавливается примерно через год. Если не проводить реабилитационное лечение, возникает стойкая утрата функции конечности. При инфицировании, смещении или разрушении эндопротеза требуется повторное хирургическое вмешательство. Некоторым пациентам в последующем приходится выполнять ампутацию.
После наступления ремиссии и завершения лечения пациент должен находиться под наблюдением врача. При возникновении любых симптомов нужно посетить клинику и пройти обследование. Это помогает вовремя диагностировать рецидив рака в кости, метастазов в других органах.
Прогноз выживаемости
На прогноз влияют такие факторы, как тип и стадия рака кости, локализация и размер опухоли, возраст пациента. В среднем пятилетняя выживаемость (процент пациентов, которые остаются живы в течение 5 лет с момента диагностики заболевания) при всех типах злокачественных опухолей костей составляет 70%.
Стадии рака костей
Выделяют 4 стадии развития опухолей кости:
- 1 стадия: опухоль ограничена костью, не прорастает в соседние ткани, не распространяется в лимфатические узлы, отдаленные метастазы отсутствуют. Опухоль является высокодифференцированной и отличается низкой степенью агрессивности.
- 2 стадия: опухоль также ограничена костью, не прорастает в соседние ткани, но является низкодифференцированной (опухолевая ткань практически утратила черты нормальной ткани) и более агрессивной.
- 3 стадия: в кости имеется 2–3 очага, они могут быть высоко- или низкодифференцированными.
- 4 стадия: опухоль, которая распространилась за пределы кости в другие органы и ткани.

Причины и факторы риска рака костей
Точные причины возникновения злокачественных опухолей костей неизвестны. Некоторые факторы риска повышают вероятность развития заболевания:
- Остеосаркомы чаще диагностируют у людей, которые перенесли курс лучевой терапии и/или химиотерапии по поводу других типов рака.
- Риски остеосаркомы повышает применение металлических фиксирующих устройств (скоб, спиц, пластин, винтов) при переломах костей.
- Играют роль некоторые наследственные заболевания: наследственная ретинобластома (редкая злокачественная опухоль глаза), синдром Ли-Фраумени.
- У пожилых людей возникновению рака костей может предшествовать Болезнь Педжета — заболевание, при котором нарушается процесс естественного обновления костной ткани, и кости становятся хрупкими.
Симптомы злокачественных опухолей костей
Зачастую первым проявлением рака костей становится боль. Поначалу она возникает лишь во время сна и физических нагрузок, затем становится постоянной, мучительной. Если пораженный участок кости не прикрыт массивными мышцами и находится близко к коже, опухоль можно увидеть при визуальном осмотре, прощупать. Возникает отек.
Рак разрушает нормальную костную ткань, ослабляет кости, в итоге происходят патологические переломы от небольшого усилия. Во время перелома в кости возникает сильная острая боль. Если опухоль сдавливает нерв, в пораженной части тела появляется онемение, покалывание, слабость мышц (парезы, вплоть до паралича).
Похожие симптомы могут возникать и при других заболеваниях, например, при артритах, остеомиелите, после перенесенных травм. Рак костей встречается редко, но при возникновении болей в костях без видимой причины лучше сразу посетить врача и провериться.
Методы диагностики
Компьютерная томография помогает уточнить размеры, расположение, количество опухолевых очагов, степень прорастания в окружающие ткани, обнаружить метастазы в лимфатических узлах и внутренних органах. По показаниям назначают МРТ: она помогает лучше визуализировать опухоль, оценить состояние мягких тканей, головного и спинного мозга.
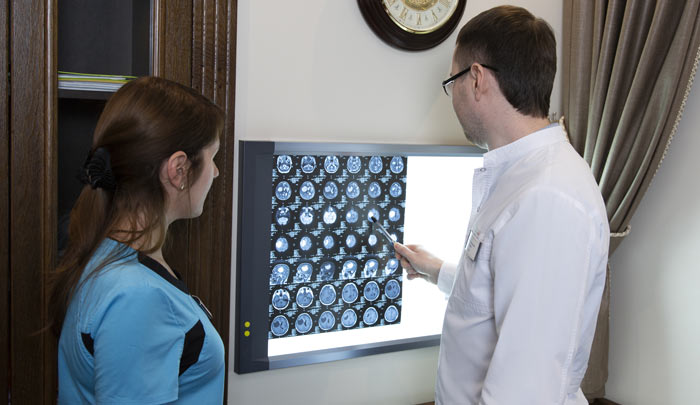
В поиске мелких метастазов помогает позитронно-эмиссионная томография. Во время исследования в организм вводят молекулы сахара с радиоактивной меткой. Опухолевые клетки поглощают радиофармпрепарат и становятся видимыми на снимках, выполненных специальным аппаратом.
Наиболее точный метод диагностики онкологических заболеваний — биопсия. Во время исследования получают фрагмент предположительно опухолевой ткани и отправляют в лабораторию для изучения внешнего вида клеток, строения ткани, молекулярно-генетических характеристик. Биопсию можно провести разными способами:
- При тонкоигольной биопсии используют шприц с иглой. Если кость находится глубоко, скрыта мышцами, процедуру проводят под контролем компьютерной томографии.
- При трепан-биопсии используют толстую иглу диаметром примерно полтора миллиметра. Считается, что этот метод лучше, чем тонкоигольная биопсия, он позволяет установить более точный диагноз.
- Иногда для исследования нужен большой фрагмент кости. В таких случаях проводят эксцизионную или инцизионную биопсию: выполняют хирургическое вмешательство, удаляют всю опухоль или ее часть.
Онкологические заболевания могут развиваться стремительно, распространяясь и поражая соседние органы. Все применяемые сегодня способы лечения рака достаточно агрессивны для организма и имеют побочные эффекты. Радиолучевая терапия – это один из способов борьбы с раковой опухолью, стоящий на втором месте по эффективности после хирургического вмешательства. По отчету Королевского колледжа радиологов (Великобритания) среди успешно пролеченных от рака пациентов 49 % из них удалили опухоли хирургически, 40 % прошли успешное радиологическое лечение, 11 % излечились благодаря химиотерапии.

Что это такое
Рентгено-, радио-, телегамма-, протоно-, нейтронная терапия и др. – это направленное действие пучков элементарных частиц или жесткого электромагнитного излучения на раковые клетки. Жесткое излучение вызывает разрывы цепочек ДНК и хромосомные мутации, размножение и деление клеток угнетается, из-за чего опухоли значительно уменьшаются либо разрушаются полностью. Расположенные вблизи здоровые клетки также повреждаются, но они обладают способностью к восстановлению. Крайне важно, чтобы интенсивность и направленность излучения были заранее точно просчитаны, так как даже относительно небольшое превышение терапевтической дозы может вызвать очень серьезные, а в некоторых случаях необратимые последствия.
Чувствительность опухолей и здоровых тканей к лучевой терапии
Лучевая терапия применяется для лечения разных видов рака. Здоровые клетки органов и опухолей имеют различную радиочувствительность и способность к регенерации. От различия этих параметров напрямую зависит успешное уничтожение раковых клеток при помощи облучения. Чем более радиочувствительны клетки опухоли, тем меньшие дозы облучений можно применять.
Радиочувствительность здоровых тканей. Высокочувствительными принято считать костный мозг, гонады, кишечник, лимфотоки, глаза (хрусталик). К среднечувствительным относятся печень, легкие, почки, кожа, молочные железы, стенки кишечника, нервная ткань. Относительно нечувствительными считают кости, мышечную и соединительную ткани.
Радиочувствительность опухолей. К высокочувствительным новообразованиям относятся лимфомы, лейкемии, семинома, саркома Юинга, эмбриональные опухоли. К среднечувствительным – мелкоклеточный рак легкого, молочной железы, плоскоклеточные карциномы, аденокарцинома кишечника, глиома. К относительно нечувствительным относятся саркома костной и соединительной тканей, меланома.
Организация лечения
Для успеха применения радиолечения крайне важна правильная организация процесса лучевой терапии, начиная с планирования и заканчивая реабилитацией после лечения. Современные отделения радиационной терапии оснащены разнообразным оборудованием как для поверхностного облучения, так и для воздействия на глубоко залегающие злокачественные новообразования. В подготовке к лучевой терапии принимают участие терапевты-радиологи и физики.
Подбор оборудования для облучения. В зависимости от размещения источника излучения относительно тела, различают следующие их разновидности:
- внутритканевый – его вводят непосредственно в больной участок в виде раствора, игл, зондов;
- внутриполостной – когда он помещен в какую-либо полость тела;
- дистанционный – соответственно находится на расстоянии от тела.
В настоящее время уже применяется техника, позволяющая использовать множественные поля облучения, что позволяет индивидуально и точно выбирать режимы облучения конкретных пациентов.
Планирование процесса лечения. Процесс расчета оптимальных доз, временных периодов и участков воздействия лучевой терапии называется планированием. Эти сложные расчеты проводятся совместно высококвалифицированными радиологами, физиками, дозиметристами, математиками. При использовании современных компьютерных технологий создаются карты изодозных кривых. На данных картах определяются районы тела, получающие эквивалентные поглощенные дозы, а также проводится необходимая коррекция поглощенной дозы для органов и тканей с нерегулярной плотностью, таких как легкие и кости. Пациент также принимает участие в планировании. При помощи специального рентгеновского аппарата на теле лежащего пациента медики определяют поле облучения и проводят маркировку соответствующих участков. Эти маркировочные линии остаются до конца курса лучевой терапии. В довершение планирования проходит обсуждение возможных способов фиксации для того, чтобы пациент не мог пошевелиться во время экспозиции.
Изготовление защитных экранов и фиксирующего оборудования. При радиологических отделениях больниц работают специальные мастерские, в которых специалисты изготавливают для пациентов различные индивидуальные иммобилизирующие устройства. Такие, как, например, шлем из оргстекла для фиксации головы в определенном положении при облучении опухолей мозга и шеи. А также вырезают защитные экраны сложной формы из свинцовых пластин для создания индивидуального поля облучения на различных частях тела.

Возможные последствия
Последствия лучевой терапии делятся на острые побочные явления во время и после процедуры и отложенные (хронические) эффекты. На вероятность возникновения осложнений влияет физическое состояние и возраст пациента, тип онкологии и стадия развития патологии.
Побочные явления во время и после облучения. Часто во время и после процедур могут наблюдаться следующие симптомы:
- болевые ощущения и воспалительные процессы в облучаемых органах;
- чувство усталости и эмоциональной подавленности;
- снижение аппетита, тошнота;
- локальные ожоги кожи;
- нарушение в работе желудочно-кишечного тракта, диарея, спазмы.
Чаще всего побочные явления, развивающиеся во время лечения, нетяжелые. Они поддаются медикаментозному лечению или проходят благодаря коррекции рациона. Через две-три недели после окончания лучевой терапии они исчезают. У части пациентов побочные явления не возникают.
Отложенные последствия. Иногда пациенты чувствуют ухудшение состояния через полгода, год, несколько лет после окончания лучевой терапии. Поздние осложнения могут быть вызваны запуском механизмов тканевого нарушения, связанного с радиоповреждением эндотелия – внутреннего покрытия кровеносных сосудов. Закупорка мелких сосудов и последующая тканевая гипоксия приводят к фиброзу пораженных тканей. Среди отложенных последствий, в зависимости от места облучения, встречаются:
- радиационный некроз мягких тканей;
- снижение емкости мочевого пузыря, гематурия;
- кишечная непроходимость;
- образование свищей;
- утрата способности к зачатию;
- образование вторичных опухолей.
Некоторые из этих состояний поддаются хирургическому лечению.
Причины возникновения тяжелых последствий
Доказано, что радиация обладает канцерогенным, мутагенным и тератогенным воздействием, нарушая ядерные связи в структуре ДНК и повреждая генетический материал. Рассмотрим механизм возникновения вторичных опухолей. После облучения в высокой дозе ткань раковой опухоли исчезает, а окружающие нормальные ткани остаются. Но в них сохраняются однажды привнесенные радиацией изменения. Здоровая клетка, постоянно обновляясь, может устранить такие повреждения, но до определенного уровня. При подходящих условиях они все-таки передаются последующим поколениям клеток. Существует вероятность, что повреждения будут накапливаться, и спустя десятки лет это приведет к возникновению вторичной опухоли. Такие случаи известны медицине, хоть и достаточно редки. Следует также помнить, что остаточные лучевые повреждения обязательно должны учитываться при проведении лечебных процедур на данных частях тела в будущем, так как облученные ткани в целом хуже заживают.
Влияние на плод
Лучевая терапия запрещена у беременных из-за тератогенного свойства радиации. Среди причин:
- самопроизвольное патологическое прерывание беременности;
- перинатальная и неонатальная смертность;
- возникновение у плода серьезных пороков развития, включая микроцефалию и замедленное умственное развитие.
Если больная в период от 10 дней до 26 недель беременности подвергалась лучевой терапии, следует рассмотреть вопрос об искусственном прерывании беременности.
Новые методы
Медицинская наука не стоит на месте. Десятки ведущих ученых в развитых странах занимаются разработкой новых и совершенствованием существующих видов лечения онкологических заболеваний. В некоторых клиниках уже внедряются новейшие достижения в области лучевой терапии. Перечислим некоторые из них.
Интраоперационное облучение. В операционной, открыв доступ к больному органу и четко различая зону поражения, врачи направляют на нее воздействие пучка электронов, максимально отодвигая в сторону кишечник и другие чувствительные органы, чтобы не нанести им вреда.
Трехмерная конформная лучевая терапия. Данные компьютерной томографии в цифровом виде связывают с лечебным аппаратом таким образом, что на выходе создается форма пучка, соответствующая конфигурации опухоли-мишени. Врач корректирует направление в случае необходимости. При данном методе очень важна дополнительная иммобилизация пациента.
Стереотаксическая лучевая терапия. Данный метод по принципу действия схож с двумя предыдущими. Специальный модифицированный линейный ускоритель применяется точечно для подведения высокой дозы излучения к небольшой по размерам опухоли или метастазам. Чаще всего применяется при лечении опухолей головного мозга.
Иммунная терапия с радиоактивными метками. Новейшее достижение медицинской микробиологии – терапия при помощи моноклональных антител. Моноклональными называют антитела, вырабатываемые иммунными клетками, полученными из одной плазматической клетки с заданными свойствами, действующие против любых природных антигенов. В клинической онкологии уже применяют инфузии препарата, содержащего моноклональные антитела, меченные радионуклидами. Этим способом радиоактивный изотоп подводится к строго определенной мишени антитела. Метод успешно применяют в лечении лимфом. Ведется разработка препаратов для лечения онкогинекологических заболеваний.

Реабилитация
После облучения человеческому организму требуется продолжительный период восстановления. Процесс реабилитации – это заключительный и очень важный этап лучевой терапии. Он может проходить дома или в тяжелых случаях в условиях стационара. Врач дает подробные рекомендации, обязательно включающие в себя индивидуальный рацион, распорядок дня, легкие физические нагрузки, режим трудовой деятельности и отдыха. Особо отмечается необходимость беречь облученные участки кожи от прямых солнечных лучей не менее года. Неукоснительное выполнение больным всех рекомендаций поможет его организму восстановить нормальную работу всех своих систем. По окончании периода реабилитации пациенту назначаются даты обязательных контрольных осмотров. При ухудшении состояния больному следует обратиться к лечащему врачу, не дожидаясь установленных сроков. Примерный перечень таких симптомов:
- повышение температуры тела, кашель;
- боль, не проходящая в течение 3–5 дней;
- потеря аппетита, тошнота, понос;
- появление опухоли или отека в области облучения;
- появление кожных высыпаний.
Последние исследования результатов лечения онкологических больных с применением лучевой терапии показывают, что с 90-х годов прошлого века риск осложнений значительно снизился благодаря применению качественно новых целенаправленных техник облучения. Все больше и больше пациентов, прошедших лучевую терапию, полностью восстанавливаются и сохраняют здоровье на долгие годы.

Химиотерапия – целенаправленное воздействие на очаг мутировавших клеток в организме пациента путем введения специальных медикаментов.

Этот метод избавления от онкопроцесса подразумевает цели:
- максимальное подавление активности раковых элементов;
- формирование необходимых условий для дальнейшего оперативного иссечения очага;
- послеоперационное подавление не устраненных мутировавших клеток.
Механизм лечебного воздействия медикаментозных средств – химии – на ткани и органы онкобольного достаточно прост. Оно осуществляется на молекулярном уровне – разрушается сама внутриклеточная структура, подавляется активный рост мутировавших элементов.
Введение противоопухолевых препаратов осуществляться различными путями. Часто используют:
- пероральный;
- внутривенный;
- введение препарата непосредственно в опухоль.
Чаще применяется первый из-за системного влияния, так как он самый удобный. Второй способ быстрее доставляет препарат непосредственно к очагу. Оба способа отличаются сильными побочными эффектами из-за воздействия не только на раковые, но и здоровые клетки. Эффективнее и безопасней предыдущих третий метод, так как вещества действуют непосредственно на новообразование.

Показания к применению
Курс химиотерапии при раке молочной железы необходим в следующих случаях:
- нужно уменьшить размеры новообразования, чтобы впоследствии удалить его хирургическим путем;
- нужно предупредить распространение метастазов;
- как дополнительное медикаментозное воздействие по отношению к лучевому или к хирургическому вмешательству;
- если диагностировано поражение регионарных (близлежащих) лимфоузлов.

Побочные эффекты
От агрессивного химического воздействия, как уже было отмечено, страдают клетки кровеносной системы, ЖКТ, волосяных луковиц и ногтей, кожи, слизистых оболочек. Отсюда и следующие негативные последствия:
- выпадение волос — частичное или полное. После остановки лечения рост восстанавливается;
- остеопороз — ослабление костной ткани; тошнота, диарея, рвота — результат воздействия на ЖКТ;
- анемия и, следовательно, повышенная утомляемость;
- инфекционные заболевания. К ним приводит общее снижение иммунитета;
- нарушение репродуктивной функции, вплоть до временного или полного бесплодия (касается мужчин и женщин).
В чересчур ослабленном организме могут возникнуть серьезные осложнения: к примеру, тифлит (воспаление слепой кишки), аноректальная инфекция, пневмония. Поэтому, прежде чем назначить лечение, врач оценивает риски. Побочные эффекты должны быть такими, чтобы пациент смог их перенести.

Как проводится химиотерапия?
Этот метод может быть рекомендован в качестве монотерапии, либо в сочетании с иными способами лечения радиотерапией;
- хирургией;
- гормонотерапией;
- таргетной терапией;
- сочетанием любых из этих методов.
Возможно проведение высокодозной химиотерапии в рамках трансплантации костного мозга или стволовых клеток.

Эффективность использования химиотерапии
- красная химиотерапия. Самая тяжелая форма терапии. Проводят её с применением Антациклинов – растворов выраженного красного цвета. Такой вид терапии угнетает иммунные силы организма.
- желтая терапия. Также является действенной, но переносится немного легче;
- синяя терапия. Оказывает положительный эффект при прогрессировании патологии;
- белая терапия. Назначается на начальных этапах.
В большинстве случаев пациенту назначают минимальные дозы препаратов, но, если болезнь не будет поддаваться лечению, их придется увеличить. Опасность такого подхода заключается в том, что повышенные дозировки химиопрепаратов губительно сказываются не только на атипичных, но и на здоровых клетках.
Самой эффективной химиотерапия терапия будет тогда, когда произойдет значительное увеличение доз подобных средств. Высокие дозировки способствуют преодолению устойчивости раковых клеток, но при этом повышается риск причинения вреда клеткам нормальным. К увеличению доз прибегают, если опухоль слишком большая и нельзя обойтись без ее хирургического удаления. Ведь чем больше размер злокачественного образования, тем более устойчивы пораженные клетки. Поэтому, для предотвращения поражения других областей организма, невозможно обойтись без химиотерапии.

Что собой представляет лучевая терапия
Один из широко применяемых и эффективных направлений в онкологии для лечения рака – лучевая терапия. Опухолевые клетки отличаются высокой чувствительностью, последствия, как правило, минимальны, ведь здоровые клетки не страдают. Суть заключается в воздействии особым ионизирующим излучением, создаваемым современной аппаратурой, основанной на источнике радиации.
Воздействие на новообразование ионизирующим излучением именуется специалистами лучевой терапией. Целенаправленное облучение проекции очага раковых клеток приводит к их обратному развитию и гибели.
Определить точно локализацию и размеры новообразования помогают современные диагностические методы исследования. Пациента тщательно подготавливают к каждой лечебной процедуре. Избежать тяжелых последствий помогают современные аппараты – с направленным излучением.
Курс, как правило, состоит из 3–4 сеансов, продолжительность каждого определяется специалистом-онкологом.

Для каких видов рака применяется лучевая терапия?
Лучевая терапия применяется для лечения разнообразных видов рака. В настоящее время более половины больных, страдающих тем или иным видам рака, успешно лечатся с помощью облучения.
Облучение может использоваться в виде самостоятельного метода лечения. Иногда ЛТ проводят перед операцией для уменьшения размеров опухоли или после нее для уничтожения оставшихся раковых клеток. Довольно часто для разрушения опухоли врачи применяют облучение совместно с противоопухолевыми лекарствами (химиотерапия).
Даже у тех пациентов, которым нельзя удалить опухоль, ЛТ позволяет уменьшить ее размеры, ослабить боль и улучшить общее состояние.
Лучевая терапия показана при раке:
- носоглотки и кольца глоточных миндалин,
- шейки матки,
- гортани,
- кожи,
- молочной железы,
- легкого,
- языка,
- тела матки,
- некоторых других органов.

Виды лучевой терапии
Дистанционная терапия – вид лечения, при котором источник излучения располагается вне пределов тела больного, на некотором расстоянии. Предшествовать дистанционной терапии может компьютерная томография, дающая возможность в трехмерном виде спланировать и смоделировать операцию, что позволяет более точно воздействовать лучами на пораженные опухолью ткани.
Брахитерапия – метод лучевой терапии, при котором источник излучения располагается в непосредственной близости от опухоли или в ее тканях. Среди достоинств данной методики можно назвать уменьшение негативного воздействия облучения на здоровые ткани. Помимо этого, при точечном воздействии имеется возможность увеличить дозу излучения.

Сколько времени длится курс лучевой терапии?
Длительность курса радиотерапии зависит от многих факторов, которые оцениваются у каждого пациента в отдельности. В среднем 1 курс длится около 3 – 7 недель, в течение которых процедуры облучения могут выполняться ежедневно, через день или по 5 дней в неделю. Количество сеансов в течение дня также может варьировать от 1 до 2 – 3.

При каких заболеваниях назначают ЛТ?
Радиотерапия широко применяется в медицине для лечения рака и некоторых других болезней. Доза облучения зависит от тяжести недуга и может быть разбита на неделю или более. Один сеанс длится от 1 до 5 минут. Используют облучение радиацией в борьбе с опухолями, которые не содержат жидкость или кисты (рак кожи, рак шейки матки, предстательной и молочной железы, рак мозга, лёгких, а также при лейкемии и лимфомах).
Чаще всего назначается лучевая терапия после операции или до неё с целью уменьшить опухоль в размерах, а также убить остатки раковых клеток. Помимо злокачественных образований с помощью радиоизлучений лечат также болезни нервной системы, костей и некоторые другие. Дозы облучения в таких случаях отличаются от онкологических доз.

Побочные эффекты
Химиотерапию нельзя назвать безопасной процедурой, поэтому нужно знать всё о процедуре, чем опасна для организма химия, какие последствия может повлечь прием противоопухолевых средств и методы их устранения.
Наиболее распространенными побочными реакциями являются:
- Тошнота и рвота;
- Облысение и ухудшение состояния ногтей;
- Общее недомогание;
- Ухудшение слуха;
- Плохой аппетит;
- Шум в ушах;
- Изменение состава крови;
- Нарушение координации;
- Сбои в работе кишечника.
Побочные симптомы могут проявляться по-разному. У кого-то они явно выраженные, у кого-то проявляются слабо. Рвотный синдром может проявиться сразу после применения средства, а выпадение волос наблюдается через пару недель после завершения сеансов.

Разница между химиотерапией и лучевой терапией
Предназначение химиотерапии и радиотерапии – нарушать ДНК раковых клеток, что приводит к прекращению их размножения и уничтожению раковой опухоли. Хоть суть этих методов в одном, но применяются они в разных ситуациях.
- Химиотерапия применяется, когда опухоль распространена по организму. Она вводится или непосредственно в кровь, или принимается в виде таблеток.
- Радиотерапия применяется для более локального лечения опухоли.
Например, для лечения рака простаты на ранней стадии бывает достаточно применить только радиотерапию. А при лечении лейкемии часто обходятся только химиотерапией.
Выбор лечебной тактики при выявленном у человека злокачественном новообразовании – приоритет лучевой, химиотерапии, рекомендуется доверить высококвалифицированному специалисту. Каждый из них имеет свои особенности, преимущества и недостатки. В чем же разница, и какой метод будет наилучшим можно уточнить у лечащего врача во время консультации.
- Можно ли вылечить лейкемиюЛейкоз – это злокачественное заболевание, которое часто называют раком крови.
Врач с 36 летним стажем работы. Медицинский блогер Левио Меши. Постоянный обзор животрепещущих тем по психиатрии, психотерапии, зависимостям. Хирургии, онкологии и терапии. Беседы с ведущими врачами. Обзоры клиник и их врачей. Полезные материалы по самолечению и решению проблем со здоровьем. Посмотреть все записи автора Левио Меши
Читайте также:

