Комбинированное лечение рака молочной железы это
Достигнутые в последние годы успехи в лечении рака молочной железы относятся главным образом к ранним формам заболевания. Почти у половины оперированных больных раньше или позже появляются отдаленные метастазы, местные или регионарные рецидивы. Если диссеминация в организме и перенос опухолевых клеток и их комплексов в отдаленные органы и ткани может происходить уже в самых ранних фазах развития новообразования (безусловно до начала лечения), то причина местных и регионарных рецидивов кроется в невозможности удаления во всех случаях опухолевых змболов, пораженных лимфангитом кожных и субфасциальных лимфатических сосудов, а также лимфатических узлов. Опухолевая инвазия регионарных лимфатических узлов, по данным Института онкологии, установлена у 58,3%, по наблюдениям МНИОИ им. П. А. Герцена, — у 54,8% поступивших в стационар больных (Баженова А. П., Барвитенко П. Г., 1978).
Таким образом, лечение больных раком молочной железы в меньшей степени связано с решением хирургической проблемы, а представляет собой сложные и пока еще твердо не установленные сочетания, комбинации и комплексы хирургических, лучевых, химиогормональных и в последнее время иммунологических воздействий.
Прежде чем перейти к конкретным обоснованиям методов лечения, остановимся на самих понятиях сочетанного, комбинированного и комплексного лечения.
Под сочетанным методом лечения в Институте онкологии, как и в других лечебных учреждениях (Петерсон Б. Е. и др., 1978), понимается применение нескольких одинаковых методов воздействия, взаимно усиливающих друг друга или действующих параллельно. Примером сочетанного лечения могут служить одновременное использование при предоперационном лучевом лечении гамма- и электронотерапии, а при лечении метастазов — нескольких химиотерапевтических препаратов разнонаправленного действия (например, алкилирующих агентов и антиметаболитов и пр.).
В понятие комбинированного лечения вкладывается представление о различных, но принципиально одинаковых по направленности методах, используемых как последовательно, так и одновременно. Примером комбинированного лечения могут быть предоперационная лучевая терапия и последующая мастэктомия, направленные на разрушение и удаление первичного очага и регионарных метастазов. Одновременное применение химио- и гормональной терапии при лечении больных с отдаленными метастазами, появившимися в разные сроки после мастэктомии, обусловлено комбинированным воздействием на обменные процессы в опухоли и организме, изменение которых на разных уровнях может препятствовать росту отдаленных метастазов.
Наконец, в последние годы появилось представление о комплексном лечении. Под ним, как справедливо отмечают Б. Е. Петерсон и соавт. (1978), понимают использование всех видов воздействия как на первичную опухоль и регионарные лимфатические узлы, так и на метастатические очаги в отдаленных органах. С этой целью могут быть предложены комплексы мероприятий, состоящие из местнорегионарных оперативно-лучевых воздействий (их сочетаний и комбинаций) и общих — химиогормональных и иммунотерапевтических методов.
Поскольку исторически сложилось мнение о главенствующем месте в лечении рака молочной железы оперативного удаления первичного очага и регионарных коллекторов, все остальные методы, входящие в комплексное лечение, принято называть дополнительными.
Нельзя не указать, что, по мнению авторитетных специалистов, приведенные группировки разных методов лечения в принципе лишены практического смысла, поскольку в каждом конкретном случае все равно перечисляются все компоненты, составляющие комбинацию или комплекс. В связи с тем что большинство специалистов все же пользуются указанными группировками, нередко вкладывая в них различные понятия, мы считаем целесообразным, чтобы практический врач имел представление не только об основополагающих принципах лечения, но и о существующей терминологии.

Рак молочной железы занимает первое место в структуре заболеваемости женщин, а частота его неуклонно растет особенно в пожилом возрасте. Статистические данные последних лет свидетельствуют о неуклонном, интенсивном росте заболеваемости и смертности от рака молочной железы в различных странах.
Усилия онкологов, направленные на борьбу с раком молочной железы, еще не дают ожидаемого эффекта. В связи с тем, что более 50 % больных злокачественными новообразованиями обращаются в медицинские учреждения при распространенном процессе, а общепринятые методы лечения недостаточно эффективны, в структуре смертности населения Казахстана, как впрочем, и в других странах мира, онкологические заболевания продолжают занимать второе место после сердечно-сосудистых заболеваний. Это обусловливает актуальность разработки новых и совершенствование существующих методов диагностики и лечения рака молочной железы.
Чрезвычайная сложность канцерогенеза и трудности ранней диагностики рака молочной железы ставят задачу первостепенной важности – выбор оптимального варианта лечения рака молочной железы у каждой больной. Это трудная задача, так как при лечении рака молочной железы применяются все современные методы онкологии: хирургический, лучевой, цитостатический, гормональный, иммунологический и различные способы коррекции функции отдельных органов и систем.
При раке молочной существуют различные варианты хирургического, комбинированного и комплексного лечения. Однако результаты современных методов лечения остаются неудовлетворительными. Пятилетняя относительная выживаемость колеблется в пределах 55–61 % (Березкин Д.П., Литягин В.П., Есенкулов А.Е.). Больные наиболее часто погибают в первые два года от генерализации процесса. Большие перспективы возлагаются на проведение послеоперационной химиотерапии (Павлов А.С., Доценко В.С., Давыдов М.И. и др.). При применении комплексной терапии, операция остается важнейшим звеном при лечении РМЖ.
Поиски путей улучшения выживаемости больных при РМЖ с учетом вышеизложенного приобретают научную значимость в области онкологии и являются актуальными на современном этапе. В программе лечения злокачественных новообразований (в частности молочной железы), в последние 10–15 лет наметились новые подходы. Связаны они в основном с пересмотром хирургических принципов в сторону уменьшения объема оперативного вмешательства без нарушения принципов радикализма.
Целью проведенной работы является улучшение ближайших и отдаленных результатов лечения больных РМЖ путем ступенчатого рассечения грудной мышцы и удаления малой грудной мышцы с фасцией, единым блоком, лимфодессекция подключичных, подлопаточных, подмышечных, сторожевых и не сторожевых лимфоузлов при экономном хирургическом вмешательстве, и в процессе комбинированного лечения. Лимфодессекция проводились на основании данных анализа наиболее распространенных путей лимфагенного метастазирования рака молочной железы после хирургического лечения различными методами и проведение химиолучевой терапии. После хирургического лечения различными методами и проведения химиолучевой терапии осуществлен анализ пятилетней выживаемости больных РМЖ.
На протяжении пяти лет мы наблюдали и анализировали результаты комбинированного лечения больных с локализованными формами РМЖ II А стадии, лечившихся в Талдыкорганском Областном онкологическом диспансере. Больные в количестве 77 человек были распределены на 2 группы:
1 группа (27 человек) – получившие широкую секторальную резекцию с лимфодисекцией аксилярной зоны.
При широкой секторальной резекции удаляются только лимфатические узлы аксилярной зоны. Однако некоторые авторы говорят о необходимости удаления не только лимфатических узлов, но и клетчатки подключичной зоны. Мы нисколько не умоляем достоинства данной методики, но считаем, что удаление клетчатки подключичной зоны представляется не выполнимым при сохранении малой грудной мышцы, так как лимфатические узлы настолько малы, что через мышцу их определить не удается.
Преимущество нашей методики заключается в свободном доступе к подключичной вене, и абластичной лимфодессекции с медиальных концов ключицы не разрывая лимфатический аппарат, тем самым не открывая путь к выходу опухолевых клеток в операционном поле, и не нарушая принцип абластичности.
2 группа (50 человек). Эти больные получили радикально -секторальную резекцию РМЖ со ступенчатым рассечением большой грудной мышцы, удалением единым блоком с фасцией и лимфодисекцией подключичных, подлопаточных, подмышечных зон.
Послеоперационное облучение было проведено всем больным 1 и 2 группы. В зону лучевого воздействия включалась молочная железа с подлежащей грудной стенкой и 2–3 см легочной ткани, СОД 20 гр.
Пациенты были распределены не только по стадиям заболевания, но и по видам рака молочной железы. Процентное соотношение видов РМЖ отражено в рис. 1.
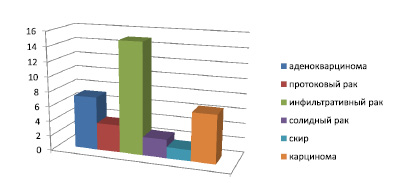
Рис. 1. Процентное соотношение видов РМЖ у экспериментальных больных
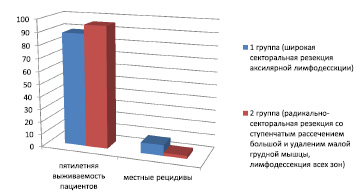
Рис. 2. Пятилетняя выживаемость больных после хирургического лечения рака молочной железы – I–II стадии
Из рис. 1 один видно, что у 7,2 % пациентов был поставлен диагноз аденокварцинома; у 3,7 % – протоковый рак; инфильтративный рак у 15 % пациентов; солидный рак – у 2,5 % пациентов; скир – у 1,5 % и кварцинома – у 6,5 % пациентов с раком молочной железы.
К первой группе, были отнесены больные, к которым был применен вид хирургического лечения под названием широкая секторальная резекция аксилярной лимфодессекции. Таких больных было 27 человек (1стадия РМЖ – 12 человек; 2 стадия РМЖ – 15 человек). Пятилетняя выживаемость у 24 женщин из 27.
Ко второй группе был применен метод под названием радикально-секторальная резекция со ступенчатым рассечением и удалением малой грудной мышцы, лимфодессекцией всех зон. Таких больных было 50 человек (1 стадия РМЖ – 20 человек; 2 стадия РМЖ – 30 человек). Пятилетняя выживаемость у 48 женщин.
Местные рецидивы у данной категории пациентов незначительные.
Результаты лечения РМЖ отражены в рис. 2.
Как видно из рис. 2 пятилетняя выживаемость в 1 группе I–II А стадии составляет 88,7 %. Местные рецидивы в послеоперационный период проявились у 8,4 % пациентов с РМЖ.
Во второй группе I-II А стадии пятилетняя выживаемость составляет 95,6 %. Местные рецидивы в послеоперационный период проявились у 2,4 % пациентов с РМЖ.
Общая пятилетняя выживаемость составила 90,2 %.
Таким образом, мы видим преимущество ступенчатого рассечения большой грудной мышцы, в стадии выживаемости пациентов и проявлении местных рецидивов в послеоперационный период.
Втрое преимущество заключается в том, что в данном виде хирургического лечения осуществляется свободный доступ к подключичной вене и абластичной лимфодессекции всех зон.
Мы считаем, что именно этот технический прием и обусловил улучшение результатов лечения у наших пациентов с различными стадиями рака молочной железы.
Апробация изложенных в статье положений проводилась на научно-практических и научно-методических республиканских и международных конференциях, посвященных вопросам онкологии. Статья является логическим продолжением опубликованных статей в международных научных журналах [3] и сборниках международных и республиканских научных конференций [1; 2].

В настоящее время, в онкологии выделяют три базовых вида лечения опухоли в молочной железе:
- радикальное — при котором достигается полное удаление опухоли;
- паллиативное – проводимое, когда радикально избавиться от патологии невозможно, но практическое воздействие на опухоль (хирургическое, лучевое, химиотерапия) существует.
- симптоматическое – нацеленное на максимальное устранение симптомов и улучшение самочувствия больного.
Лечение рака груди наиболее перспективно на ранних стадиях заболевания, при которых вполне обоснованно можно ожидать полного выздоровления.
К основным направлениям лечения рака молочной железы относятся:
- Хирургическое вмешательство в форме резекции (частичного удаления), либо полного удаления тканей железы (мастэктомия).
- Системная терапия, воздействующая на весь организм в целом. В схему включают: химиотерапию, гормонотерапию, таргетную (целенаправленную) терапию. В последние годы появились новые методы, разработанные на основе достижений иммунологии и генетики – иммунотерапия и генотерапия.
- Лучевая терапия.
До выбора метода лечения определяется стадия болезни.
Лучевая терапия или радиотерапия
Это компонент лечения направленный на уменьшение количества рецидивов опухоли (после операции), уменьшение объёма опухолевой массы (до операции) и подавления потенциального развития раковых клеток.

При обработке больного участка (ложа опухоли) рентгенологическим облучением или гамма-лучами оставшиеся после операции атипичные клетки уничтожаются полностью. Лечение проводят курсами с перерывами, чтобы за это время здоровые клетки могли восстановиться после воздействия облучения.
На практике применяют 2 вида радиотерапии:
- Контактная, при которой на ткань воздействует внешний источник (линейный ускоритель ионного излучения).
- Дистанционная (брахитерапия), предусматривающее поступление радиоактивного вещества прямо внутрь ткани. При этом его количество рассчитывают отдельно для каждой пациентки в точных дозах.
- в составе комплексной терапии после органосохраняющей операции;
- риск повторного развития опухоли после мастэктомии (большие размеры, вовлечение в процесс лимфоузлов);
- множественные раковые очаги;
- инвазия (внедрение) атипичных клеток в микроскопические кровеносные и лимфатические сосуды;
- разрастание опухли за границы лимфатических узлов;
- распространение атипичных клеток в область соска, ареолы, кожи, большой грудинной мышцы;
- некроз тканей, интенсивные костные боли на любой стадии в рамках паллиативного лечения с целью снятия болевого синдрома.
Более подробно про лучевую терапию при раке молочной железы можно прочитать, перейдя по ссылке.
Химиотерапия
Суть метода состоит в назначение специальных препаратов (цитостатиков, противораковых антибиотиков и других средств), тормозящих агрессию опухоли и разрушающих атипичные клетки. Применяют как отдельный метод и в комплексе с другими, до и после хирургического лечения.
Выделяют 2 формы:
- Неоадъювантная химиотерапия, которая проводится до операции. Увеличение опухоли останавливается, что позволяет максимально точно удалить образование, не травмируя здоровые ткани.
- Адъювантная химиотерапия проводится после операции, с целью разрушения оставшихся раковых клеток, в частности, если метастатический процесс уже начался.
- III стадия онкопатологии;
- отсутствие клеточных рецепторов, чувствительных к эстрогенам и прогестерону (новообразование не реагирует на лечение гормонами);
- высокая скорость деления раковых клеток (низкодифференцированный рак);
- первично нерезектабельные опухоли, при которых возможность проведения хирургического вмешательства отсутствует.
Распространенные препараты этой группы, используемые чаще, в комбинациях для взаимного усиления терапевтического действия:
Циклофосфан, Метотрексад, Фторурацил, Адрибластин, Доцетаксел, Паклитаксел, Доксорубицин, Эпирубицин (значительно меньше воздействует на миокард), Винорельбин, Гемзер (из новых).
Схемы лечения врач подбирает индивидуально. В некоторых случаях препараты сочетают с таргетными (прицельными) средствами (Бевацизумаб).
В результате грамотного применения схем химиотерапии улучшение наблюдаются у 50 – 70 пациенток из 100.
Беременность, грудное вскармливание;
- Индивидуальная непереносимость препаратов с развитием острых аллергических реакций;
- Интоксикация;
- Высокий билирубин крови.
Гормонотерапия
Гормональные средства используют при лечении гормонозависимого рака молочной железы.
- Антиэстрогены: Тамоксифен (Нолвадекс). Назначается до менопаузы, и в основном — на ранней стадии рака.
- Ингибиторы ароматазы, включая Анастразол (Аримидекс), Экземестан (Аромазин), Летрозол (Фемара), Аминоглутетимид (при метастазирующем раке груди, устойчивом к другим гормональным средствам), применяемые у пациенток после менопаузы.
- Аналоги гонадолиберина: Лейпрорелин, Гозорелин (Золадекс) у женщин в пременопаузе. Причем их сочетание с Тамоксифеном более эффективно, чем у каждого из них в отдельности.
Гормональное лечение рака молочной железы показано при развитии гормонозависимых опухолей для снижения риска рецидивов, обычно после химиотерапии и удаления злокачественного очага.
Таргетная терапия
Показания: рак груди с активным белком HER2 на II — IV стадии.
Средства, подавляющие активность особого онкопротеина HER2, который влияет на рост карциномы: Трастузумаб (Герцептин), Ритуксимаб, Нератиниб, Лапатиниб (Тайкерб)
Другие препараты: Фазлодекс (антиэстроген), Иресса, ингибитор белка PARP Инипариб и Олапариб проходят испытания.
Хирургическое лечение
Хирургическое удаление массива пораженной раком ткани — основной метод избавления от раковой опухоли в груди.

Большинство пациенток подвергается щадящей органосохраняющей операции, когда иссекается только опухоль с окружающей тканью, но грудная железа сохраняется (лампэктомия).
При метастазах или крупной опухоли требуется выполнение мастэктомии (полное удаление железы).
- Прорастание опухоли в грудную стенку.
- Тяжелая недостаточность миокарда и сосудистой системы.
- Серьезные нарушения кровоснабжения мозга.
- Сахарный диабет в стадии декомпенсации, недостаточность почек, печени в тяжелой форме.
Лечебная тактика определяется стадией развития карциномы:
- Лечение рака молочной железы 1 стадии предусматривает резекцию органа, плюс радиотерапию коротким курсом для предупреждения рецидивов, и при необходимости — назначения гормонов и химиопрепаратов.
- Лечение рака молочной железы 2 стадии предполагает мастэктомию (при больших опухолях) или резекцию железы и адъювантную терапию. Сегодня онкологи чаще проводят резекцию.
- На III стадии проводят химиотерапию с последующей мастэктомией и облучением.
- На IV стадии лечение считается симптоматическим, когда основной задачей считают не ликвидацию ракового процесса, а устранение симптомов и продление жизни.
Лечение первично нерезектабельных опухолей
При первично нерезектабельной карциноме программа лечения включает:
Полихимиотерапию, которая проводится с целью:
- уменьшения объема первичного очага;
- снижения агрессивности злокачественных клеток;
- уменьшение величины пораженных лимфоузлов;
- создания условий для возможности выполнения облучения и оперативного вмешательства;
- снижения вероятности рецидивов и метастазирования.
Лучевое воздействие с целью максимального разрушения опухолевых тканей.
Комбинированная химиолучевая терапия усиливает местное воздействие на опухоль, почти в 70 % обеспечивая возможность проведения хирургического вмешательства
Паллиативное лечение
Целью паллиативной помощи является повышение качества жизни пациента при малой вероятности излечения рака в распространенной форме, на поздних стадиях, когда не имеется возможности использовать радикальный метод. Такое лечение уменьшает страдания больного, и позволяет продлить жизнь.
Паллиативное лечение включает:
Паллиативную хирургию
Под паллиативной операцией в онкологии понимают такое вмешательство, при удаляются не все опухолевые массы, а те, которые возможно удалить. Целью такой операции является устранение не болезни, а последствий опухолевого процесса. Необходимость в таких операциях возникает почти у 40% женщин на III — IV стадиях.
При этом предполагается удаление первичной опухоли, но при этом остаются раковые очаги, например, для рака молочной железы — метастазы в костной ткани.
Также может проводиться мастэктомия, резекция смежных тканей, пораженных лимфоузлов, иссечение нежизнеспособных тканей вокруг опухолевой язвы (некрэктомия).
Такие операции создают благоприятные условия для последующей противоопухолевой лекарственной терапии, эффективность которой зависят от объема оставшейся опухоли.
Химиотерапию
Вливание химиопрепаратов в сниженных дозах (супрессивная химиотерапия) дает возможность за короткий срок остановить активное деление аномальных клеток и разрушить уже существующие. Чаще используется в сочетании с хирургией.
Радиотерапию
Лучевая терапия в паллиативном режиме проводится:
- если поражены 4 и более лимфоузлов;
- при широком распространении рака, что иногда позволяет преобразовать нерезектабельную опухоль в форму, при которой возможна операция.
Используется для снижения интенсивности болей при распространении метастазов в кости позвоночника и таза.
Гормональную терапию
Подавляет активность половых гормонов, способных ускорять рост карциномы. Базовое показание для назначения гормональных средств — повышенная чувствительность к эстрогену клеток раковой опухоли. Как правило, гормонотерапия назначается уже после лучевой или химиотерапии, кроме случаев агрессивного развития рака.
Своевременное проведение паллиативного лечения нередко продлевает жизнь на несколько лет. Выраженную положительную реакцию на паллиативные виды терапии наблюдают у 60 — 80% пациентов, при этом почти 30% больных отмечают серьезное улучшение общего состояния.
Симптоматическое лечение
Направлено на устранение или смягчение симптоматики от развития ракового процесса и применения лучевой и химической терапии.
Симптоматическое лечение при раке груди необходимо:
- на терминальной стадии, либо, когда пациенту по каким-то причинам отказали в радикальном и паллиативном лечении, и он не способен пережить операцию и введение наркоза из-за истощения (кахексия), сопутствующей патологии;
- при распространении метастатического процесса с целью снятия болей.
- медикаменты для борьбы с болью, тошнотой, лихорадкой, одышкой;
- радиационное облучение, проводимое для устранения болевого синдрома, сдавления нервных узлов;
- симптоматические операции, которые выполняют для устранения нарушений, вызванных распространением метастазов.
В рамках медикаментозной помощи больному назначаются следующие группы препаратов:
- Обезболивающие нестеройдной группы.
- Наркотические анальгетики.
- Психотропные средства, транквилизаторы, антидепрессанты, необходимые при лечении невралгий, тика, болей при низком пороге чувствительности и усиленных эмоциональным компонентом, чрезмерном возбуждении.
- Препараты от тошноты и рвоты, которые чаще используют в сочетании, чтобы усилить их действие.
- Жаропонижающие при опухолевой лихорадке, которые помогают избежать резких изменений температуры и быстрого истощения пациента. Терапию начинают с максимальных разовых доз, подбирая оптимальные.
Злокачественная опухоль в груди является одной из основных причин ранней смерти женщины от онкологии. Лечение рака молочной железы наиболее эффективно при выявлении заболевания на 1 стадии, когда нет метастазов и можно без последствий удалить злокачественное новообразование. Важно комплексно подходить к терапии: правильный выбор лечебной тактики позволяет надеяться на благоприятный прогноз для жизни.
При обнаружении опухоли на начальном этапе роста шансы на выздоровление максимальны
Основные факторы, влияющие на эффективность терапии
Выявление злокачественной опухоли в груди – это рубеж, разделяющий жизнь женщины на до и после: борьба с раком становится повседневной действительностью, а прошлая жизнь кажется утерянным счастьем. Эффективное лечение рака молочной железы зависит от следующих факторов:
- своевременность выявления (стадия онкологии);
- гистологический вариант опухоли;
- вид клеточных изменений (дифференцировка тканей);
- состояние иммунной системы (способность собственных защитных сил противостоять раку);
- наличие общих хронических заболеваний.
Онкология груди относится к наследственно программируемым болезням – важно знать о болезнях молочных желез у близких родственниц: наличие генетического риска становится фактором онконастороженности. Возможность предотвратить опухоль или выявить рак вовремя значительно выше при постоянном наблюдении у врача.
Лечение рака молочной железы – основные методы
Вне зависимости от прогноза врач будет использовать все виды и варианты терапии. Лечение рака молочной железы включает следующие методы:
- Хирургическое удаление злокачественного новообразования;
- Применение лекарственных препаратов (химиотерапия, гормональные средства);
- Лучевая терапия.
Важно точно и последовательно выполнять все назначения врача, чтобы результатом комбинированного воздействия стало избавление от опухоли с сохранением жизни.
Основа успешной борьбы с онкологией груди – хирургическая операция. В зависимости от стадии и величины опухоли используют следующие варианты вмешательств:
- простая мастэктомия;
- радикальная мастэктомия (удаление железы вместе с мышцами и клетчаткой груди);
- широкая резекция (квадрантэктомия) – экономный вариант оперативного лечения с сохранением части груди;
- секторальная резекция (удаление опухоли) при малых размерах новообразования и низком риске метастазирования.
Важно учитывать противопоказания для органосохраняющих видов операций. Нельзя использовать резекцию в следующих случаях:
- размер новообразования 30 мм и более;
- двухсторонний онкологический процесс;
- отсутствие четких границ опухолевой ткани на маммограмме;
- инфильтративная форма;
- внутрипротоковый вариант рака;
- центральное расположение новообразования;
- подмышечная локализация опухоли;
- невозможность проведения радиотерапии;
- наличие выраженного иммунодефицита.
Для каждой пациентки объем операции подбирается индивидуально: если имеются показания для полного удаления груди, то следует прислушаться к мнению специалиста (шансы на выживание повышаются при тотальном удалении злокачественной опухоли).
Своевременная диагностика – основа успеха лечения рака молочных желез
Важный этап комплексной терапии – применение лекарственных препаратов. Комбинированное лечение рака молочной железы включает следующие медикаментозные средства:
- гормонотерапия (молочная железа – гормоночувствительна);
- химиотерапия (для подавления оставшихся раковых клеток).
- Важными факторами успешной терапии являются:
- длительность приема медикаментов (подбирается индивидуально);
- возраст (в постменопаузе надо использовать несколько лекарственных препаратов);
- вовлечение в онкопроцесс подмышечных лимфоузлов.
Медикаментозная терапия проводится в течение 2-3 лет, что позволяет значительно улучшить прогноз при 1-2 стадии онкологии.
Основная цель курсового лучевого воздействия – предотвращение рецидива опухолевого роста. Радиотерапия проводится до операции и после хирургического вмешательства. При использовании органосохраняющей методики облучение является обязательным элементом комбинированной терапии.
Прогноз для жизни
При выявлении опухоли в груди на начальных этапах роста шансы на выздоровление максимальные: после операции и курсовой терапии 85% женщин живут 5 лет и более. При 1 стадии заболевания 75% пациенток имеют шанс умереть от старости, а не от болезни. При обнаружении метастазов в подмышечные лимфоузлы лечение рака молочной железы позволяет продлить жизнь до 10 лет 40% женщин. При 4 стадии 10% смогут прожить около 10 лет.
Рак молочной железы — болезнь настолько распространенная, что с ней, к сожалению, сталкивается каждая десятая женщина независимо от возраста. При этом в половине случаев это заболевание в нашей стране выявляется уже на поздних стадиях, и потому болезнь часто побеждает.
Рак молочной железы: бороться — значит победить!
К основным факторам риска возникновения рака молочной железы можно отнести:
- ожирение;
- отягощенный семейный анамнез (онкозаболевания у кровных родственников). Например, если у матери или ее сестер был рак молочной железы, у дочери риск заболевания повышается в девять раз;
- курение (особенно ― с юного возраста).
Существуют и другие провоцирующие факторы.
Медицинский факт
Неблагоприятный прогноз рака молочной железы заключается в том, что многие пациентки узнают о своем заболевании уже на третьей–четвертой стадии, когда клетки рака распространились за пределы железы и требуется сложное и многоступенчатое лечение. Поэтому ученые продолжают разрабатывать новые методы диагностики, позволяющие заметить начало болезни на самых первых этапах, а также методы лечения, способные без выраженных побочных эффектов привести к устойчивому выздоровлению.
Важна и эстетическая сторона лечения. В прошлом хирургические операции, направленные на удаление опухоли молочной железы, были крайне травмирующими, что приводило к косметическому изъяну во внешнем облике пациенток. Сегодня мастэктомия (полное удаление груди) в клиниках проводится только по строгим показаниям, к тому же хирурги в основном стремятся к максимально органосохраняющему лечению. Если мастэктомии все же не избежать, врач предложит пациентке одномоментную или двухэтапную реконструкцию груди ― когда полностью удаляется молочная железа (в большинстве случаев возможно подкожное удаление с сохранением сосково-ареолярного комплекса) и устанавливается имплантат.
В зависимости от симптомов выделяют две формы рака молочной железы: узловая и диффузная (диффузно-отечная).
Узловые, как это следует из названия, характеризуются наличием одного или более образований в молочной железе. Эта форма рака чаще встречается, проще диагностируется на ранних стадиях и потому лучше поддается лечению.
Диффузная (диффузно-отечная) форма не имеет четкого очага, распространяется по всей толще железы и инфильтрирует кожу. Встречается гораздо реже, отличается высоким риском метастазирования и труднее поддается лечению.
По тому, из каких структур и клеток молочной железы исходит опухоль, различают следующие морфологические типы:
- Инвазивная протоковая карцинома — самый распространенный вид злокачественного новообразования (80% всех случаев рака молочной железы). Этот вид рака развивается внутри молочных протоков и постепенно прорастает (инвазирует) в окружающие здоровые ткани железы, что приводит к появлению опухолевых эмболов в лимфатических и кровеносных сосудах и впоследствии ― метастазов в лимфоузлах и других органах. При своевременном обнаружении хорошо поддается лечению.
- Инвазивная дольковая карцинома встречается всего в 15% случаев.
- Воспалительный рак молочной железы — редкий, но крайне агрессивный тип рака, относится к диффузной группе. Симптомами могут быть повышение температуры, покраснение и отечность груди, а в некоторых случаях — скопление гноя в тканях молочной железы. В такой ситуации требуется незамедлительное начало химиотерапии.
Стадирование рака груди призвано помочь врачам объяснить друг другу и пациентам, насколько далеко зашло заболевание. Ключевыми параметрами определения стадии являются размеры опухоли, обнаружение злокачественных клеток в ближайших и отдаленных лимфоузлах, а также наличие метастазов.
Так, 0-я стадия при раке молочной железы говорит о том, что рак неинвазивный, то есть опухоль не вышла за пределы той анатомической области, где она возникла. Прогноз при выявлении такого новообразования всегда благополучный.
1-я стадия означает, что рак распространился на ткани молочной железы, но при этом максимальный размер опухоли не более 2 см, а в лимфатических узлах нет раковых клеток. Пятилетняя средняя выживаемость женщин с этой стадией рака близка к 100%. В России на этой стадии выживаемость составляет до 95%.
При 2-я стадии рака молочной железы онкологи ориентируются на размер опухоли (2–5 см) и/или на вовлечение в процесс ближайших подмышечных лимфоузлов. Средняя пятилетняя выживаемость составляет около 93%, в России — до 80%.
3-я стадия определяется или большими размерами опухоли (более 5 см) и вовлечением лимфоузлов, или прорастанием новообразования за пределы тканей молочной железы, в кожу, мышцы или внутригрудные лимфоузлы. Эту же стадию выставляют пациенткам с воспалительным раком молочной железы. Пятилетняя относительная выживаемость для рака молочной железы 3-й стадии в мире составляет около 72%, в России — до 50%.
4-я стадия подразумевает появление метастазов — очагов опухоли в костях, легких, головном мозге, печени и других органах тела. Пятилетняя выживаемость составляет 22–27%, в России — не более 10%.
На 1-й и 2-й стадиях заболевание протекает бессимптомно и не причиняет болевых ощущений. Обнаружить рак в этот период можно либо по данным маммографии, либо методом пальпации (ощупывания), иногда женщина находит уплотнение в груди при самообследовании.
На 3-й и 4-й стадиях опухоль уже видна, может иметь вид язвы или большой шишки. Может появиться уплотнение в подмышечной ямке или над ключицей — эти симптомы свидетельствуют о поражении лимфоузлов.
С развитием процесса возможно появление болевого синдрома, который связан с прорастанием опухоли в ткани грудной стенки. Женщина может замечать прозрачные или кровянистые выделения из груди, втяжение соска, изменение цвета или структуры кожи молочной железы.
Это важно!
Тревожными сигналами могут стать:
- наличие уплотнений или опухолевидных образований в одной или обеих молочных железах;
- выделения из соска любого характера, не связанные с беременностью или лактацией;
- эрозии, корочки, чешуйки, изъязвления в области соска, ареолы;
- беспричинно возникающая деформация, отек, увеличение или уменьшение размеров молочной железы;
- увеличение подмышечных или надключичных лимфоузлов.
Какие методы обычно применяются в лечении рака молочной железы?
Вне зависимости от формальных стадий необходимо помнить, что каждый случай рака — уникальная ситуация, поэтому прогноз может отличаться от усредненных статистических показателей. Главное — своевременно обратиться за помощью, найти клинику и авторитетного врача, а после ― неукоснительно следовать предписаниям специалистов. Рак — это не приговор, а только сложная медицинская проблема, для решения которой нужен грамотный подход.
Когда онколог подтверждает самые страшные опасения, все дела и жизненные приоритеты уступают место мыслям о болезни. Но не стоит поддаваться панике. Надо найти в себе силы и изучить достоверную информацию о раке молочной железы, современных возможностях и способах лечения заболевания. Обращение к врачу на ранних стадиях болезни позволяет надеяться на счастливый результат.
Этот вопрос мы адресовали врачу-онкологу Европейского медицинского центра (г. Москва) Анне Маховой:
«При таком диагнозе, как рак молочной железы, стоит отнестись со всей серьезностью к выбору лечебного учреждения, но не затягивать с принятием решения, поскольку в вопросе лечения онкозаболеваний время играет существенную роль.
Очень важно выработать тактику лечения в каждом конкретном случае рака молочной железы — этим должна заниматься мультидисциплинарная команда врачей, работающая в многопрофильном госпитале и осуществляющая свою деятельность по международным протоколам.
Институт онкологии ЕМС — это многопрофильное медицинское учреждение международного уровня, объединившее под одной крышей все необходимое для лечения онкологических больных. Мы прошли аккредитацию Joint Commission International (JCI), а лечение рака молочной железы проводим по европейским и американским протоколам. Это означает, что клиника работает по мировым стандартам, а уровень технического обеспечения и профессионализм врачей не уступают госпиталям США или Израиля.
Лечение рака молочной железы осуществляется в нашем госпитале силами команды врачей различных специальностей: онкологов, маммологов, радиологов, радиотерапевтов, онкопсихологов. Совместно принимается решение о выборе тактики лечения и подбираются щадящие (насколько это возможно) методики лечения.
Мы оказываем весь комплекс процедур для лечения рака молочной железы:
- осмотр (консультация) врачом-онкологом, хирургом, радиотерапевтом;
- комплекс исследований для диагностики злокачественных новообразований молочной железы;
- иммуноцитохимическое исследование с моноклональными антителами материала из различных тканей и органов для выявления метастазов опухоли (онкомаркеры-цитокератины, nm23, SCC, РЭА и другие;
- молекулярно-генетическое исследование мутаций в генах BRCA1 и BRCA2 в крови;
- молекулярно-генетическое исследование мутаций в гене BRCA1 в биопсийном (операционном) материале;
- назначение лекарственных препаратов при онкологическом заболевании (химиотерапия, таргетная и иммунотерапия);
- хирургическое лечение;
- лучевая терапия, в том числе интраоперационная лучевая терапия;
- медицинская реабилитация пациентов, перенесших операцию по причине онкологического заболевания, химиотерапию, лучевую терапию;
- прием (осмотр, консультация) врача по паллиативной медицинской помощи (первичный и повторный).
Центр лучевой терапии EMC имеет в своем распоряжении единственную в России сверхточную систему для проведения лучевой терапии и радиохирургии. Установка выполняет облучение опухолей различного размера в любой части тела с субмиллиметровой точностью. Это достигается за счет того, что во время сеанса аппарат ориентируется на КТ-изображения высокого качества и контролирует положение пациента и отклонение мишени облучения в режиме онлайн.
В Институте онкологии мы осуществляем различные виды хирургических операций. Операции проводит хирург-онкомаммолог с опытом работы в ведущих европейских онкологических центрах. В большинстве случаев мы рекомендуем органосохраняющее лечение при раке молочной железы. Если удаление груди неизбежно, может быть проведена кожесохраняющая мастэктомия и мастэктомия с сохранением сосково-ареолярного комплекса. Мы предлагаем нашим пациентам современные возможности для немедленной или отсроченной реконструкции груди, в том числе с помощью липофилинга (коррекции собственной жировой тканью пациента).
Состояние лимфоузлов ― важнейший показатель для определения стадии заболевания и выбора тактики лечения. Удаление и проверка первых подмышечных лимфоузлов позволяет доктору оценить, насколько объемной должна быть операция. Если в сторожевых лимфоузлах нет метастазов, можно избежать подмышечной лимфодиссекции (удаления всех лимфоузлов), которая часто сопровождается серьезными побочными эффектами, в частности, развитием лимфедемы.
- медицинскую деятельность на основании лицензии ЛО-77-01-019876, выданной Департаментом здравоохранения города Москвы 10 апреля 2020 года;
- высокотехнологичную медицинскую деятельность на основании лицензии ФС-99-01-009514, выданной Федеральной службой по надзору в сфере здравоохранения 25 апреля 2018 года.
** Аккредитация Объединенной международной комиссии (Joint Commission International), полученная Европейским медицинским центром (госпиталь на ул. Щепкина, 35), распространяется на период с 7 апреля 2018 года по 6 апреля 2021 года.
Читайте также:

