Вакцина от рака мыши
Меланома — самая опасная из опухолей кожи и одно из самых злокачественных онкологических заболеваний. Основная беда в том, что болезнь метастазирует (распространяется) через лимфу и кровь на ранних стадиях и зачастую ее диагностируют уже на поздних стадиях (III, IV), когда оперативное лечение бессильно. Часто через годы заболевание возвращается метастазами даже в тех случаях, когда рак был диагностирован до появления метастазов и иссечен целиком.
До недавних пор эффективного лечения метастатической меланомы фактически не существовало. Назвать интерферон эффективным можно только с очень большой натяжкой.
Но с появлением таргетных (биологических) препаратов и иммунотерапии ситуация в корне поменялась. К сожалению, иммунотерапия помогает только в 40% случаев, что само по себе огромный прорыв в лечении этого страшного заболевания. Но что делать остальным 60% пациентов?
И вот новое открытие: израильские ученые из Университета Тель-Авива разработали новую нановакцину от меланомы, и она оказалась эффективной при исследовании на мышах. Эта разработка, по мнению исследователей, может проложить путь к эффективному лечению и даже профилактике этого заболевания. Результаты исследования были опубликованы в серьезном научном издании Nature Technology.
Исследованием руководила профессор Ронит Сатчи-Финаро, заведующая кафедрой фармакологии и физиологии, глава лаборатории по онкологическим исследованиям и наномедицине факультета Саклера Тель-Авивского университета. Научную работу выполнили Анна Скомпарин и постдокторант Жоао Конниот.
Были проведены три группы экспериментов:
- Здоровым мышам вводили вакцину, а затем клетки меланомы. Опухоль у мышей не развилась, это означает, что вакцина обладает профилактическим действием. Механизм ее действия схож с механизмом давно и хорошо известных вакцин: против кори, ветрянки, краснухи, гриппа и т. д.
- Затем наночастицы вакцины ввели больным меланомой мышам вместе с препаратом иммунотерапии группы ингибиторов PDL-1. К этой группе относятся такие, например, препараты, как Опдиво и Кейтруда. Совместное действие препаратов дало лучший результат, чем монотерапия ингибитором PDL-1. А при добавлении препарата Ибрутиниб (Ibrutinib), использующегося сегодня для лечения рака крови, результаты были еще лучше. Дело в том, что Ибрутиниб способствует выработке специфических лейкоцитов, которые уничтожают опухоли.
- Использование нановакцины было проверено на мышах с метастазами в мозгу и дало положительный результат, значит, данное лечение может использоваться и для лечения больных с отдаленными метастазами, включая мозг. Надо заметить, что лечение метастаз в мозге всегда является самой большой проблемой, т. к. большинство препаратов не проникают в мозг через гематоэнцефалический барьер.
Эта научная работа дала начало совершенно новому подходу в лечении меланомы даже на самых поздних стадиях злокачественного процесса. Более того, существует надежда, что этот подход может использоваться для создания вакцин и для других видов рака, таких как рак почек, легких, мочевого пузыря, поджелудочной железы, рака груди.
В ближайшее время начнутся испытания вакцины на людях. Этот процесс обычно занимает 5–10 лет. Но в некоторых случаях, если результаты очень убедительны, в последнее время комиссия FDA дает ускоренное разрешение на использование препаратов в клинической практике, как это было, к примеру, с первым препаратом Kymriah технологии CAR-T, о котором я уже писал.
Воистину, чудеса происходят на наших глазах. И я с нетерпением жду лицензирования нового препарата, чтобы применять его для пациентов своей клиники.

Не зная иммунной системы человека, Имхотеп обнаружил существенную связь между опухолями и инфекциями, которая не появлялась в научной литературе вплоть до начала 20-го века, пока костный хирург и исследователь рака Уильям Коли (William Coley) не начал вводить живые бактерии, а позже бактериальные токсины людям с саркомой.
- Хотя методика Коли показала некоторый успех в лечении рака пациентов, она была забыта в пользу новой химиотерапии и лучевой терапии, говорит Злоза.
Теперь, когда иммунотерапия привлекает внимание исследователей рака, Злоза и другие начали осознавать, что Имхотеп и Коли могли совершить большой прорыв в иммунотерапии: они использовали инфекции, чтобы дать толчок собственной иммунной системе больных раком, для уничтожения своих опухолей.
Злоза и его коллеги недавно добавили доказательства этого подхода исследованием мышей с опухолями, которых лечили вакциной против сезонного гриппа: инъекция вакцины, состоящей из инактивированных вирусов гриппа, введенных непосредственно в опухоли кожи мышей резко замедлила рост образований и в некоторых случаях их размер уменьшался, сообщили исследователи в январе в PNAS.
«Наличие такой довольно мягкой вакцины оказывает такое глубокое влияние на опухолевый иммунитет, и это удивительно, - говорит Томас Куппер, дерматолог, который изучает лечение опухолей кожи в Институте рака Дана - Фарбер в Бостоне (Dana-Farber Cancer Institute in Boston) и не принимал участия в исследовании.
По его словам, если результаты подтвердятся в клинических исследованиях на людях, это может положить начало инновационному способу нацеливания на определенные типы опухолей, которые были чрезвычайно сложными для лечения, а также на раковые клетки, которые перемещаются в другие части тела.
- Злоза и его команда сосредоточились только на тех видах трудно поддающихся лечению опухолей, известных как "холодные опухоли", потому что у них не так много иммунных клеток, проникающих в них. По сравнению с другими опухолями, при холодных опухолях меньше шансов для иммунной системы определить наличие раковых клеток, которые отличаются от нормальных клеток в организме, и любые присутствующие иммунные клетки имеют тенденцию подавлять, а не активировать иммунную систему.
Исследователи подозревают, что инъекция белков, ассоциированных с гриппом, в опухоли кожи мыши сигнализирует врожденной иммунной системе мышей о том, что инородный материал попал в организм.
- Полученный иммунный ответ, как предположили ученые, превращает холодные опухоли в "горячие".
В соответствии с этой идеей, специалисты обнаружили, что лечение работало только тогда, когда белки гриппа вводились непосредственно в опухоли кожи. Инъекция живого вируса гриппа в опухоли не повлияла на раковые клетки, вероятно потому, что вирус не способен реплицироваться и продуцировать вирусные белки в этих клетках, предположили исследователи в своей статье.
Инъекция инактивированного теплом вируса или вирусных белков за пределы опухоли - например, в мышцы мышей - также не влияла на опухоли.

Когда команда ввела вакцину против гриппа в опухоли, дендритные клетки, "пехотинцы" врожденной иммунной системы, заполнили раковые клетки. Эти дендритные клетки начали собирать кусочки вируса гриппа, называемые патоген - ассоциированными молекулярными структурами (PAMP), которые помогают вызвать иммунный ответ и поглощают части опухолей.
Когда дендритные клетки экспрессируют (активизируют) вирусные и опухолевые антигены на своих поверхностях, чтобы привлечь Т-клетки, они могут инициировать атаки как на грипп, так и на раковые клетки.
Исследователи обнаружили увеличение количества Т-киллеров, несущих рецепторы для специфического опухолевого антигена, и предположили, что эти клетки действительно были нацелены на опухолевые клетки.
Ученые также показали, что когда у мыши было две опухоли, как обработанная, так и необработанная, она росла медленнее после инъекции прививки от гриппа по сравнению с опухолями у нелеченных мышей.
Чтобы увидеть, произойдет ли нечто подобное с человеческими опухолями, команда Злоза имплантировала клетки рака молочной железы человека в жировые прослойки мышей. Как и при этой форме рака человека, опухоли жировой ткани метастазировали в легкие мышей.
Так же, как команда обнаружила при работе с опухолями мыши, прививка от гриппа в первичную опухоль в жировой прокладке привела к снижению роста как этой опухоли, так и любых метастатических опухолей легких, которые начали формироваться.
Однако между мышами и людьми существует важное различие, которое интригует и Злоза, и Масопусту. Лабораторные мыши никогда не подвергались воздействию гриппа, но люди заражаются этим вирусом, и многие ежегодно получают прививки от него. Это означает, что могут существовать медлительные Т-клетки, которые готовы реагировать на инактивированный вирус, если он вводится в опухоли человека.
Куппер отмечает, что исследования также показывают, что врачи могут использовать вирусную иммунотерапию для повышения эффективности другой формы лечения рака - ингибиторов контрольных точек, которые, как известно, менее эффективны при холодных опухолях.

Сотрудники Стэнфордского университета при помощи стволовых клеток создали вакцину от рака, доказавшую эффективность против опухолей молочной железы, легких и кожи у мышей.
Для производства вакцины ученые использовали индуцированные плюрипотентные стволовые клетки (iPSC), которые генерируются из зрелых клеток определенного типа.
Более 10 лет назад в Японии было впервые доказана возможность генетического перепрограммирования зрелых клеток таким образом, чтобы они вели себя подобно плюрипотентным стволовым клеткам.
Плюрипотентные клетки способны принимать любую форму и выполнять всевозможные функции, приобретая нужную организму хозяина специализацию.
Доктор Джозеф Ву (Joseph Wu) из Института биологии стволовых клеток и регенеративной медицины в Стэнфордском университете утверждает, что иммунизация животных эмбриональной тканью позволяет предотвратить развитие злокачественных опухолей. Такое предположение было высказано почти сто лет назад, и ученые из разных стран длительное время пытались использовать эмбриональные стволовые клетки в качестве вакцины от рака.
Но основная проблема противораковых вакцин заключалась в ограниченном количестве антигенов, чужеродных агентов для активации иммунного ответа.
В публикации на страницах Cell Stem Cell говорится, что использование iPSC из собственного генетического материала пациентов дает целый ряд иммуногенных преимуществ, открывая нам дорогу к реальной иммунопрофилактике рака.
Тренировка иммунной системы против рака
Доктор Ву и его коллеги взяли клетки мышей и создали из них iPSC, которые затем вводили обратно в организм животных, уже в составе комплексной вакцины от рака. Вакцина была поливалентной, то есть защищала сразу от нескольких типов рака. Как поясняют авторы, основным преимуществом iPSC является универсальность – нет нужды искать идеальные антигены для нацеливания на определенный тип опухолевых клеток.
Дело в том, что многие из антигенов плюрипотентных стволовых клеток можно обнаружить в злокачественных клетках при раке легких, кожи, молочной железы и др.
Но вернемся к результатам эксперимента.
Когда животные получили инъекции iPSC, их тело отреагировало выработкой антител против злокачественных опухолей разных типов. Вакцина фактически сделала лабораторных животных неуязвимыми к онкозаболеваниям!
Чтобы подтвердить эффект, ученые ввели iPSC грызунам с раком молочной железы. Из 75 животных 70% полностью победили опухоль, а у 30% животных удалось добиться значительного уменьшения размеров в течение 4 недель после введения вакцины. Аналогичными были результаты на мышах с раком легких и кожи (меланомой).
Если изобретение войдет в клиническую практику, в скором будущем собственные стволовые клетки будут не только лечить рак, но и предотвращать его в группах риска.
Быть может, скоро мы перестанем бояться смертельной болезни?
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
МИНСК, 2 фев — Sputnik. Вакцина от рака, созданная учеными Стэндфордского университета, успешно проходит испытания на мышах. Ученые рассказали, что разработанное ими вещество активирует Т-лимфоциты в клетках опухоли и удаляет метастазы. Причем вакцина обещает быть недорогой и воздействовать направленно на клетки опухоли, не поражая весь организм.

Вакцина состоит из двух типов антител. Использование одного из них уже протестировано и одобрено для использования на человеческом организме. Второй тип прошел испытание еще только в нескольких независимых друг от друга клиниках. Вакцину протестировали на мышах. Профессор онкологии Рональд Леви отметил, что эффект, который они наблюдали у мышей, удивителен.
"Сами по себе эти антитела и молекулы никак не будут действовать на рак, но их комбинация имеет радикально иные свойства. Мы предполагаем, что их смесь будет столь же эффективно работать и при лечении пациентов, а также при борьбе с другими типами рака", — рассказывает Леви.
Ученый отметил, что для борьбы с опухолью у мышей было достаточно небольшого количества антител. Ученые ввели антитела в опухоль у мышей, и она практически полностью исчезла за десять дней, причем уменьшаться начали и соседние опухолевые образования. Дальнейшие наблюдения показали, что подобная "вакцина" защитила мышей от повторного появления очагов рака груди, даже учитывая предрасположенность.
Профессор Рональд Леви является одним из ведущих ученых, занимающихся разработкой вакцины от рака. Проводимые в его лаборатории исследования привели к созданию противоопухолевого средства "Ритуксимаб".
МИНСК, 15 июл - Sputnik. Россия исключена из списка стран, после посещения которых белорусам нужно находиться на карантине, сообщили в Минздраве республики.
МИНСК, 15 июл – Sputnik. Результаты централизованного тестирования по английскому языку стали известны в среду. Абитуриенты активно делятся набранными баллами в тематических группах в соцсетях, эмоционально обсуждают допущенные ошибки.
Большинство результатами довольно: Sputnik расспросил вчерашних выпускников о сложности тестов, глупых ошибках, переживаниях и том, как они оценивают свои шансы во время вступительной гонки.

"Я получила 100 баллов! Не ждала такого результата: когда я только вышла с испытания, начала проверять какие-то моменты в интернете и общаться с другими абитуриентами, стала сомневаться в некоторых пунктах. Поэтому была уверена, что написала на 90-95", – делится столичная абитуриентка Женя Шленкова, которая намерена поступить в БГУИР на экономику электронного бизнеса.
Девушке достался пятый вариант, самыми сложными она называет задания Б5 и Б6. Говорит, что за английский стоит браться как можно раньше: она и репетиционное тестирование писала выше, чем на 90 баллов.
"Английский стоит начинать учить уже в начальной школе. Вообще, стоит уделять больше времени не тестам, а чтению книг на английском или просмотру интересных роликов от носителей языка. Мне это очень помогло. И конечно, главное – найти хорошего преподавателя, который будет повышать уровень, а не просто поддерживать его", – советует стобалльница.
По ее словам, большинство ребят довольны результатами ЦТ по английскому языку (почти все написали минимум на 80): "Этот предмет дался легче, чем математика или русский".
"Конечно, 100 баллов по любому предмету очень повышают шанс на поступление. Но на специальность, куда я планирую попасть, довольно высокие баллы – 358; а у меня даже с учетом результатов английского получается 357. Надеюсь, баллы немного снизятся, и я смогу пройти на бюджет, потому что платное даже не рассматриваю", – откровенничает Женя.
"Я получила 94 балла: сразу появились сомнения, но в целом была достаточно уверена в своих знаниях. Даже не могу вспомнить конкретные задания, которые показались сложными, все было достаточно понятно. Ошибки допустила по глупости, например, во временах, которые прекрасно знаю – на ЦТ, видимо, подзабыла или перенервничала", – рассказывает еще одна столичная абитуриентка Меланья Канаш.
Девушка говорит, что выложилась "по максимуму", нужно было лучше справляться с волнением. Отзывы ее знакомых по поводу результатов ЦТ по английскому языку разнятся.
"Кто-то наугад набрал 40 баллов и вполне доволен результатом, кто-то готовился год-два, получил свои 70+ и тоже рад. Есть те, кто также готовился, получил достаточно высокие результаты (85+), но не доволен собой, поскольку ждал лучшего и писал РТ минимум на 90 баллов", - делится она.

Меланья Канаш набрала 350 баллов в сумме: раздумывает над поступлением на международное право в БГУ или государственное управление и право в президентскую Академию.
"В БГУ по баллам спокойно прохожу на платное, в Академию прохожу на бесплатное. Пока буду выбирать, но считаю так: что бы я ни выбрала - пройду. Предполагаю, что кроме меня будет большое количество абитуриентов с высокими баллами, создастся сильная конкуренция, но я даже рада: приятно быть в числе сильнейших", – откровенничает собеседница агентства.
Другой собеседник Sputnik, абитуриент Богдан Левчук из Кобрина, планирует поступить в Институт бизнеса БГУ, он набрал 83 балла – столько и хотел.
"Сложнее всего дались задания, связанные с текстом, я допустил пару ошибок с артиклями, думаю, их можно было избежать. Считаю, что написал не на свой максимальный балл: скорее всего, мне нужно было больше повторять правила в последнюю неделю перед ЦТ", – говорит парень и добавляет, что свои шансы на поступление в любом случае оценивает довольно высоко.

Примерно такой же балл получила на ЦТ абитуриентка из Витебска Яна, которая планирует поступить на юрфак.
"Получила 85 баллов - не считаю, что это плохой результат, но я надеялась получить больше, так что расстроилась, когда узнала. На ЦТ мне было легко выполнять задания, видимо, допустила ошибки по невнимательности или из-за волнения – у меня так часто, и это очень обидно. Всем было сложно: я одна из немногих людей в своей компании с баллом выше 80", – делится она.
Яна советует приступать к углубленной подготовке уже в девятом классе и стараться не переживать: волнение очень мешает сконцентрироваться.
Таня Калашникова из городка Высокое в Брестской области набрала 92 балла: она во время подготовки ежедневно общалась с иностранцами – это очень помогло.
"Моя главная ошибка – исправлять правильное на неправильное в конце теста. В Б-части я сделала одну ошибку, недобрала только из-за стресса и долгой дороги до города, где сдавала ЦТ. Считаю, что у меня довольно неплохие результаты: надеюсь, что история Беларуси, которая будет на следующей неделе, не подведет", – делится девушка.

А минчанка Екатерина Крищанович набрала 71 балл, английский сдавала четвертым предметом и не возлагала на него больших надежд (хотя на ДРТ набрала 86).
"ЦТ по английскому достаточно объемное, много текста, надо внимательно вчитываться и улавливать смысл, чтобы не допустить ошибки. Думаю, что в этом году при поступлении большой конкуренции будет – абитуриентов в этом году значительно меньше. Но весь этот процесс все равно волнительный", – говорит Катя.
Лабораторных мышей с одним из самых агрессивных видов рака удалось вылечить
![]()

Раковые клетки. Фото: Matthew Daniels / wellcomecollection.org
Ученые из Исследовательского института Скриппса в Сан-Диего разработали новую вакцину против меланомы (рака кожи). Она показала стопроцентный результат в ходе испытаний на лабораторных мышах. Лекарство в сочетании с уже существующей терапией может не просто лечить агрессивные формы меланомы, но и даже предотвращать ее рецидивы.
Меланома – злокачественная опухоль, которая развивается из меланоцитов – пигментных клеток, занимающихся производством меланинов. Рак локализуется в коже, иногда – в сетчатке глаза или слизистых оболочках. Это одно из самых агрессивных онкологических заболеваний, с частыми рецидивами и высоким риском развития метастазов почти во всех органах. Главная опасность этой опухоли в том, что организм слабо реагирует на ее развитие в начальном этапе, поэтому человек может не заметить болезнь. После этого меланома стремительно прогрессирует и часто приводит к смерти.
Модель пропаганды — теория Эдварда Хермана и Ноама Хомского, утверждающая наличие систематических перекосов в средствах массовой информации и объясняющая их экономическими причинами.
С точки зрения модели пропаганды, СМИ рассматриваются как предприятия, продающие товар — читателей и аудиторию (а не новости) — другим предприятиям (рекламодателям, правительствам).
То есть, если вы не заплатили за то, что читаете, значит кто-то другой заплатил за то, чтобы вы это прочитали.
Зарплата авторов и редакторов Republic формируется только за счет денег подписчиков.
![]()
\u0414\u0430! ","nick":"Yulia Smagina","userId":96154,"voteUp":null,"voteDn":null,"createdAt":"2018-09-13 11:01:54","updatedAt":"2018-09-13 11:01:54","parentId":55884,"edited":0,"deleted":0,"avatar":"006698c6a27f2cb79c2575a1030267e0.png","userVote":"","twitterPage":null,"vkPage":null>,"55911":<"id":"55911","comment":"
\u0412\u043e\u0442 \u0431\u044b \u043e\u0431\u043e\u0440\u043e\u043d\u043d\u044b\u0439 \u0431\u044e\u0434\u0436\u0435\u0442 \u043f\u0435\u0440\u0435\u043d\u0430\u043f\u0440\u0430\u0432\u0438\u0442\u044c \u043d\u0430 \u0437\u0434\u0440\u0430\u0432\u043e\u043e\u0445\u0440\u0430\u043d\u0435\u043d\u0438\u0435, \u043d\u0443 \u0438 \u043d\u0435\u043c\u043d\u043e\u0436\u043a\u043e \u043d\u0430 \u043e\u0431\u0440\u0430\u0437\u043e\u0432\u0430\u043d\u0438\u0435 \u043f\u043e\u0434\u043a\u0438\u043d\u0443\u0442\u044c. ","nick":"\u041c\u0430\u043a\u0441 \u041c\u0430\u043a\u0441\u043e\u0432","userId":7216,"voteUp":null,"voteDn":null,"createdAt":"2018-09-13 15:02:31","updatedAt":"2018-09-13 15:02:31","parentId":0,"edited":0,"deleted":0,"avatar":"f24f37f0b15a8559605da387626eac26.png","userVote":"","twitterPage":null,"vkPage":null>,"55977":<"id":"55977","comment":"
\u041e\u0442\u043b\u0438\u0447\u043d\u0430\u044f \u0441\u0442\u0430\u0442\u044c\u044f. \u041f\u043e\u0447\u0438\u0442\u0430\u043b \u0441 \u0443\u0434\u043e\u0432\u043e\u043b\u044c\u0441\u0442\u0432\u0438\u0435\u043c. \u041d\u0430\u0434\u0435\u044e\u0441\u044c \u0430\u0432\u0442\u043e\u0440 \u0431\u0443\u0434\u0435\u0442 \u043e\u043f\u043e\u0432\u0435\u0449\u0430\u0442\u044c \u043e \u043f\u0440\u043e\u0434\u043e\u043b\u0436\u0435\u043d\u0438\u0438 \u043e\u043f\u044b\u0442\u043e\u0432 \u0438 \u0432\u044b\u0445\u043e\u0434\u0430 \u043b\u0435\u043a\u0430\u0440\u0441\u0442\u0432\u0430 ","nick":" ","userId":46676,"voteUp":null,"voteDn":null,"createdAt":"2018-09-14 12:49:13","updatedAt":"2018-09-14 12:49:13","parentId":0,"edited":0,"deleted":0,"avatar":null,"userVote":"","twitterPage":null,"vkPage":null>>,"viewedComments":[]>">

Срез лимфоузла под микроскопом
Wikimedia Commons
Американские ученые разработали метод эффективной доставки пептидных антигенных вакцин для персонализированной терапии рака. В эксперименте применение этого метода вызвало полное излечение большинства подопытных мышей. Результаты работы опубликованы в журнале Nature Materials.
Пептидные вакцины от рака представляют собой антигены, специфичные для опухоли конкретного пациента (неоантигены) и, соответственно, производимые персонально на основании результатов секвенирования опухолевой ДНК. В силу высокой безопасности применения и сравнительной простоты производства их исследованиями занимаются многие научные коллективы, однако добиться достаточной эффективности в клинических испытаний пока не удавалось. Причина этого заключается в плохом проникновении пептидных неоантигенов и адъювантов (препаратов, усиливающих их действие) в лимфоузлы и, как следствие, недостаточной активации цитотоксических Т-лимфоцитов под их действием.
Сотрудники Мичиганского университета с коллегами из других научных центров предложили доставлять антигены с адъювантами наночастицы, напоминающие по строению липопротеиды высокой плотности (ЛПВП). Это одна из разновидностей белково-липидных комплексов, служащих для транспорта жиров (в частности, холестерина) в крови.
Разработанные учеными наночастицы состоят из трех компонентов: первый — аналог аполипопротеина А (компонента ЛПВП) — служит материалом наночастицы; второй — связаный с холестерином динуклеотид CpG — обеспечивает ее продвижение к лимфоузлам и третий — это персонализированные неоантигены, вызвающие иммунную реакцию. Подобная наночастица имеет форму диска диаметром около 10 нанометров.
Как показали эксперименты, такой метод доставки вызывает устойчивую презентацию неоантигена дендритными клетками и их созревание, что, в свою очередь, приводит к появлению большого числа активированных цитотоксических Т-лимфоцитов, специфичных к антигену опухоли (в 47 раз больше, чем при применении растворимых пептидных неоантигенов).

Принцип действия методики
Rui Kuai et al., Nature Materials, 2016
Эти Т-лимфоциты эффективно распознавали и уничтожали раковые клетки в периферических тканях мышей. Добавление к подобной иммунотерапии ингибиторов иммунных контрольных точек CTLA-4 и PD-1 через 10 дней привело к полному рассасыванию аденокарциномы толстой кишки примерно у 88 процентов животных (против примерно 25 процентов в случае растворимых антигенов) и меланомы у около 90 процентов животных (против примерно 38 процентов при применении растворимых антигенов). Повторное введение аналогичных раковых клеток через 70 дней к развитию опухолей не привело, то есть к ним развился иммунитет.
В настоящее время ученые занимаются воспроизведением технологии у более крупных животных, чтобы в случае успеха перейти к клиническим испытанием. Для разработки и вывода технологии на рынок университет учредил спин-офф EVOQ Therapeutics.
Иммунотерапия в настоящее время является наиболее перспективным направлением в экспериментальном лечении рака. Помимо неоантигенов разработаны и проходят испытания вакцины в виде РНК-липоплексов, а также различные генетически модифицированные кроветворные клетки и Т-лимфоциты. Про лимфоциты с химерными антигенными рецепторами, которые уже полностью излечили несколько десятков пациентов с неоперабельными опухолями, можно почитать в нашем материале.

Меланома. Саркома. Рак прямой кишки. Каждый из этих диагнозов звучит как приговор. Традиционные методы лечения не помогают. Девять из десяти больных погибают в первый же год после диагноза. Остановить прогрессирование болезни – значит спасти жизнь. Пусть на время, пусть на 10–15 лет, но всё-таки…
Иммунная система пациента с агрессивной формой рака словно вывешивает белый флаг и в упор не видит опасные для жизни клетки. Но научить её распознавать клетки новообразования и бороться с ними всё-таки возможно.
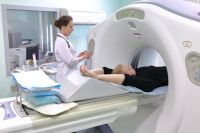
Лаборатория в составе отделения биотерапии опухолей была создана в НИИ онкологии имени Н. Н. Петрова в 1998 году. Уже через пять лет учёные получили свой первый патент – на иммунотерапию костномозговыми дендритными клетками больных солидными опухолями. Ещё через пять лет, в 2003 году, запатентована аутологичная вакцина на основе костномозговых дендритных клеток в сочетании с фотодинамической терапией для лечения химиорезистентных диссеминированных солидных опухолей. В 2010 году специалисты НИИ получают разрешение применять своё изобретение в клинической деятельности. В 2014‑м создаётся научный отдел онкоиммунологии.
А если иммунитет очнётся?
Новое – это хорошо забытое старое. Уникальные противоопухолевые вакцины учёные из НИИ онкологии имени Н. Н. Петрова создают в конце XX – начале XXI века. Но мало кто помнит, что ещё в XIX веке медицинская наука обратила внимание на интересную закономерность: пациенты, у которых есть опухоль, заболевают инфекцией и… выздоравливают. Опухоль разрушается!

А почему разрушается опухоль? Впоследствии выяснилось: потому что активируется иммунная система. Она как будто приходит в сознание и начинает видеть не только вирусы или бактерии, но и опухолевые клетки, которые до поры до времени успешно уклонялись от иммунного надзора. Новое направление в медицине начало развиваться, но вскоре изобрели лучевую терапию, а затем химиотерапию. Эти методы стали давать результаты, и об иммунной системе на время забыли.
Но прошло много лет, и стало понятно, что химиотерапия и лучевая терапия – ещё не панацея. Необходимы дополнительные методы лечения, которые восстановят противоопухолевый иммунный ответ. К исследованию клеток иммунной системы вернулись вновь.
Когда опухоль сильнее лимфоцита
Кстати, а почему иммунитет оказывается беспомощным перед опухолевой клеткой? Наш организм похож на общество: наиболее активно и эффективно отстаивают свои права те, у кого они не так уж и нарушены.
Из-за мутаций и быстрого роста опухоли иммунная система перестаёт узнавать опасные клетки, которые когда-то были родными, а теперь стали чужеродными. Есть даже теория, что опухолевым клеткам помогают… нормальные, здоровые клетки, расположенные по соседству. Они начинают синтезировать факторы роста, благодаря которым развивается новообразование.

Надо успеть
У каждого пациента своя вакцина. Та, которая подействует именно на его опухоль. Для этого учёные тщательно изучают опухолевые клетки, взятые у больного. Измельчив биоматериал с помощью специальной автоматической машины, пытаются полностью охарактеризовать опухоль – выявить все особенности её поведения, все иммуносуппрессирующие факторы, которые она продуцирует. Нет, это совсем не опечатка.
Опухолевые клетки в отличие от многих из нас всеми силами цепляются за жизнь. Не сработал один механизм подавления иммунной системы – она вырабатывает другой. Не сработал другой – создаёт третий. На экране клеточного видеокомпьютера видно, как стремительно делятся клетки рака толстой кишки. Специальные ножи лабораторной автоматической машины, раскрошившие опухоль на отдельные клетки, новообразованию, кажется, нипочём.

Чтобы успеть, необходимо приготовить вакцинный препарат и ввести больному человеку его первую инъекцию. На создание препарата требуется десять дней – если процесс пройдёт удачно с первой же попытки.
За два первых месяца лечения пациент получит вакцину четырежды. В препарате будут активированные дендритные клетки, которые научат лимфоциты распознавать опухоль. Так стартует иммунный ответ.
Как рождается вакцина
Противоопухолевая вакцина создаётся из собственных клеток иммунной системы больного. Со стороны начало работы очень похоже на обычный анализ крови из вены. В биоматериале учёные по специальным методикам выделят предшественников периферических дендритных клеток – моноциты. А потом начнётся самое сложное. Моноциты необходимо дифференцировать в дендритные клетки. Для этого нужны специальные факторы роста клеток человека (никак не факторы роста для экспериментальных животных), в частности, интерлейкин‑4, гранулоцитарно-макрофагальный колониестимулирующий фактор и особая бессывороточная питательная среда (без ксеногенных факторов лабораторных животных) для получения индивидуальной вакцины человека. В такие условия моноциты помещаются на десять дней. Через неделю их забирают на анализ – проточную цитометрию. Если процесс прошёл правильно, лаборатория обнаружит в материале предшественников – незрелые дендритные клетки. Если же нет, придётся начинать всё сначала. И дай бог успеть вовремя. Так бывает у начинающих учёных без опыта работы, наличия импортных ростовых факторов и специальной дендритноклеточной питательной среды.
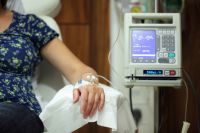
Созревшая дендритная клетка, уже представляющая частицы опухоли на своей поверхности, становится основным компонентом противоопухолевой вакцины.

Надо просто любить эти клеточки…
Приготовление вакцинного препарата – процесс не только и не столько химический. Если не любить отдельные живые клетки, если не относиться к ним бережно и заботливо, как к маленьким детям, лекарство не получится. И пациент не выздоровеет.
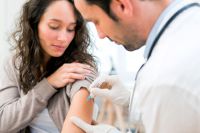
Доктор медицинских наук Ирина Александровна Балдуева, разрабатывающая противоопухолевые вакцины в НИИ онкологии им. Н. Н. Петрова с 1998 года, замечает: важен не только настрой больного на выздоровление, но и настрой специалиста, который создаёт вакцинный препарат. И пусть это кажется странным, но клетки иммунной системы получаются активными и жизнеспособными только тогда, когда к ним относятся с особой любовью.
Одиночество опасно для жизни
Наши клетки – это мы сами в миниатюре. Сегодня в науке уже известно: когда человек в депрессии, по-другому работает не только мозг, но и все без исключения органы и системы. Возможности нашего организма безграничны – и многое вопреки всем достижениям медицинской науки зависит от того, какой приказ отдаст подсознание.
Другой случай из практики врачей НИИ онкологии им. Н. Н. Петрова. На сей раз печальный. Молодую женщину спасти не удалось. А всё началось с того, что во время медового месяца её муж случайно задел наручными часами родинку у неё на спине. На месте содранной родинки началось кровотечение. Несомненно, кровотечение остановили. Но вскоре развилась агрессивная форма меланомы. Далее было всё очень банально – пациентку бросил муж, ставший невольным виновником заболевания. Это подкосило женщину ещё больше. Не помогли ни поддержка родителей, ни усилия врачей. Красивая и очень молодая женщина с онкологическим диагнозом твёрдо решила, что жить ей незачем.

На стенах кабинета Ирины Александровны Балдуевой – прекрасные картины. Многие из них создал её пациент – художник, капитан 2-го ранга в отставке. Несмотря на ампутированную руку, Борис Матвеевич пишет новые пейзажи, руководит Фондом культуры и учит рисованию маленьких детей из неполных семей. Денег за уроки он не берёт.
Читайте также:

