Стентирование при опухолях кишечника
+7(925)191-50-55
В Европейской клинике хирургии и онкологии уже много лет проводится лечение пациентов с раковыми заболеваниями. У многих из них опухоль обнаруживают на поздних стадиях развития, когда возможности излечения и прогноз выживаемости существенно ухудшаются. В этом случае практикуют паллиативные мероприятия, которые облегчают существование таких людей и улучшают качество жизни. Часто самым оптимальным решением является установка стента в пораженный онкологическим процессом участок кишечника, что восстанавливает его проходимость и не дает развиться опасным для жизни осложнениям. Процедура введения стента хорошо освоена врачами Европейской клиники и их профессиональное мастерство позволяет проводить подобную манипуляцию с минимумом побочных эффектов.
+7(925)191-50-55
г. Москва, Духовской переулок, 22б
Рак толстого кишечника очень распространен в человеческой популяции и его частота очень высока в странах Запада, но заметно ниже в Азии и Африке, что несомненно связано со спецификой рациона питания в этих частях Света. У мужчин рак ободочной кишки составляет 5,8% в структуре общей онкологической заболеваемости, а у женщин эта цифра равна 7%. Вероятность заболеть раком сигмовидной, прямой кишки или ануса для мужчин и женщин равна примерно 5%. Благодаря особенностям строения кишечной стенки и лимфатической системы чаще наблюдается рак левых отделов толстого кишечника. По той же причине здесь обычно локализуется такое осложнение, как кишечная непроходимость, смертность от которой варьирует от 7% до 22%.
Экстренная помощь при острой кишечной непроходимости еще недавно не имела альтернатив и заключалась в деструктирующей резекции толстого кишечника и наложения колостомы. Это приводило к неблагоприятным последствиям для психики пациента, его замыканию и уходу в себя. Восстановление толстого кишечника посредством пластики происходило примерно через 8-12 месяцев и все это время больной, как правило, был потерян для нормальной социальной жизни. Другим неприятным фактом экстренной резекции толстого кишечника служит отсутствие возможности качественной лимфодиссекции, что увеличивает вероятность рецидива опухоли и распространение ее на другие анатомические области. Вероятность развития кишечной непроходимости при опухоли толстого кишечника колеблется от 26% до 69% и эта патология в практике любого отделения хирургии и онкологии наблюдается очень часто.
Появление методики стентирования позволило быстро и эффективно устранять кишечную непроходимость и подготовить пациента к полноценной операции по поводу основного заболевания. Сами стенты изготавливаются из прочного никелид-титанового сплава, который обладает памятью металла, позволяющей ему расправляться после установки в проблемном участке. Современные стенты покрывают специальным составом, который не дают прорасти тканям сквозь сетчатую стенку. Биоинертная оболочка сплава предотвращает развитие реакции со стороны иммунной системы. Стент хорошо переносится организмом, а осложнения возникают в основном не из-за качества исполнения протеза, а за счет прогрессирования основного заболевания.
Перед стентированием пациент сдает ряд анализов крови, мочи, коагулограмму, тест на ряд инфекций, снимают ЭКГ: все это необходимо для выявления оценки общего состояния, так как противопоказаний к установке протеза в случае острой кишечной непроходимости нет. Стентирование в толстом кишечнике проходит достаточно безболезненно и часто удается обойтись лишь внутримышечным введением сибазона. Как правило, накануне делают клизму для лучшей визуализации стенки кишечника, но иногда, в острой ситуации, обходятся без нее. Общие принципы проведения данной манипуляции примерно такие же, как и при других локализациях.
Стентирование проводят под двойным контролем: колоноскопическим и рентгеноконтрастным телевидением. Для того, чтобы правильно локализовать место протезирования, на уровне нижнего края опухоли, перекрывающей кишечник, вводят так называемую рентгеноконтрастную клипсу и по ней в дальнейшем ориентируются. Доступ осуществляется через прямую кишку. С помощью колоноскопической визуализации в кишечник проводят металлическую струну с атравматическим наконечником. Затем по этой струне проводят контейнер, содержащий стент в скрученном состоянии. Когда он достигает рентгеноконтрастной клипсы, его вводят вглубь еще на 2 см и после этого извлекают стент и расправляют его. Контейнер удаляют из кишечника, а стент постепенно принимает свою необходимую форму и открывает просвет толстой кишки для каловых масс. После этого кишечная непроходимость устраняется и связанные с ней симптомы нивелируются. При неоперабельном раке стентирование позволяет сохранить нормальный стул на всё оставшееся время жизни.
Первую операцию по стентированию в пищеварительном тракте осуществили еще в 1979 году и к настоящему времени метод доказал свою эффективность, способность быстро устранять проблемы пациента, восстанавливать утраченные функции, улучшать качество жизни. В Европейской клинике хирургии и онкологии применяют стенты от ведущих мировых производителей, обладающих самыми удачными механическими и биологическими характеристиками. Высокие технологии в сочетании с исключительным профессионализмом персонала клиники дают возможность добиваться прекрасных результатов не только в лечении, но и в оказании паллиативной помощи больным.
+7(925)191-50-55
г. Москва, Духовской переулок, 22б
+7(925)191-50-55 - европейские протоколы лечения в Москве
Рак кишечника даже при наличии современных методов обследования часто диагностируют на поздних стадиях заболевания. Пациенты, поступившие в клинику онкологии с запущенной формой рака кишечника, требуют особого подхода, длительного комбинированного лечения. Часто онкологи не имеют возможности удалить сразу опухоль. В большинстве онкологических отделений пациентам выполняют паллиативную операцию – наложение колостомы. Каловый свищ доставляет пациентам неудобства, требует постоянного ухода и защиты кожи вокруг стомы. Сам факт существования свища вынуждает человека вести изолированный образ жизни.
Можно ли поставить стент в кишечнике? Онкологи Юсуповской больницы вместо операции наложения калового свища выполняют стентирование кишечника. Процедура заключается в подведении к месту сужения кишки через эндоскопический зонд в сложенном виде полого сетчатого цилиндра. Затем стент расправляется и расширяет просвет кишки, создавая каркас.
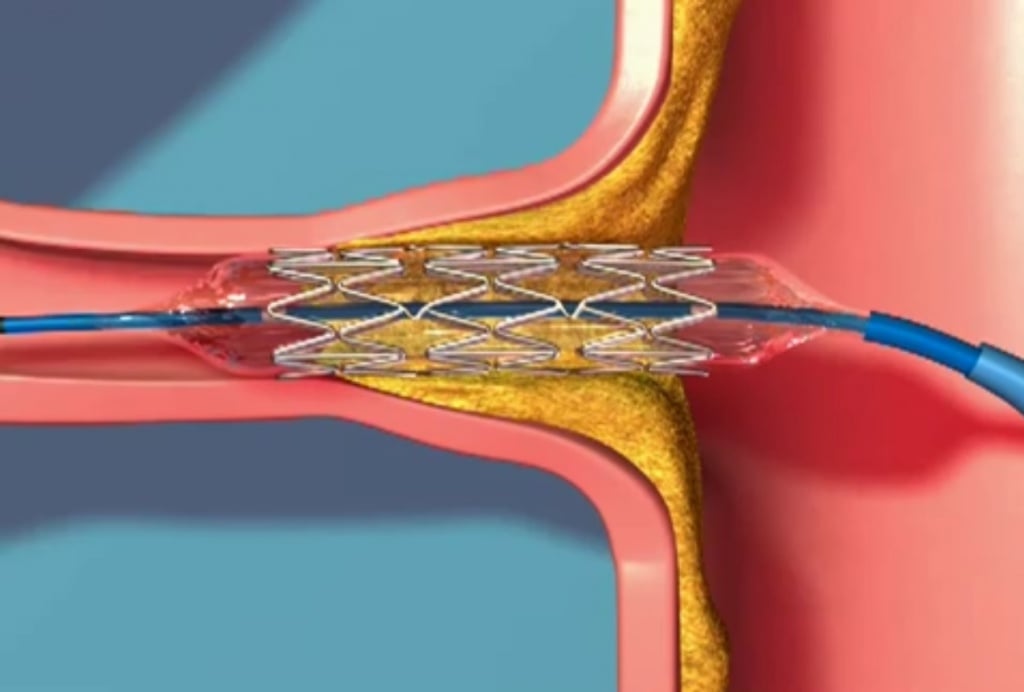
В Юсуповской больнице созданы все условия для оказания паллиативной помощи пациентам с запущенной формой рака кишечника. Врачи клиники онкологии индивидуально подходят к выбору оперативного вмешательства, учитывают возраст больного раком, стадию опухоли, наличие сопутствующих заболеваний. Медицинский персонал внимательно относится к пожеланиям пациента. Все тяжёлые случаи рака кишечника обсуждаются на заседании экспертного совета с участием профессоров и врачей высшей категории. Ведущие онкологи коллегиально принимают решение о выборе метода лечения.
Показания и противопоказания к стентированию кишечника
Стентирование толстой кишки – это восстановление просвета при его грубом стойком сужении. Процедура является одним из наиболее эффективных и востребованных способов лечения пациентов с неоперабельными новообразованиями этих органов, которые доставляют ощутимый физический дискомфорт, существенно меняют привычный образ жизни. Стентирование толстой кишки – малоинвазивная процедура, которая обычно хорошо переносится больными, ослабленными онкологическим заболеванием.
Стентирование кишечника может быть окончательным способом лечения пациентов, которым не показано по различным причинам радикальное оперативное вмешательство. Установку стента также выполняют с целью предоперационной подготовки к радикальной операции. Противопоказаний для стентирования толстой кишки нет.
Техника установки стента в кишечник
Стент-эндопротез – это самораскрывающийся металлический проволочный каркас или пористая трубка. Диаметр устройства онкологи подбирают исходя из размеров просвета, для которого он предназначен. Скрученный в спираль стент устанавливают под эндоскопическим контролем в суженный участок кишечника. После этого он расправляется, раздвигает стенки кишки. Проходимость суженного участка кишечника восстанавливается.
Стентирование рака толстой кишки позволяет избежать выведения колостомы (концевого отрезка кишки на переднюю брюшную стенку). В клинике онкологии представлен большой выбор стентов из различного материала и различных технологических решений:
- с нитями для удаления стента;
- с внутренней пластиковой оболочкой;
- со специальным покрытием, не допускающим прорастания тканей опухоли через стенку стента.
При расположении злокачественного новообразования в прямой кишке онкологи устанавливают стент под рентгенологическим контролем. При другой локализации опухоли используют колоноскоп с рабочим каналом для проведения инструментов. Если до установки стента не удаётся провести эндоскоп за область обтурации, врачи предварительно проходят проводником через область сужения, а в последующем проводят по нему доставочное устройство со стентом. Проведение проводника через зону сужения выполняют с помощью манипуляционного катетера с рентгеноконтрастной меткой на конце.
После прохождения манипуляционным катетером-проводником через область сужения, комплекс удаляют, а через просвет катетера контрастируют отдел кишки, расположенный выше сужения, и зону стеноза. Этот метод позволяет онкологам получить представление о протяженности стриктуры и выбрать нужную длину стента. В дальнейшем через просвет манипуляционного катетера в кишечник заводят жёсткий проводник за верхний край сужения. Под постоянным рентгенологическим контролем по жёсткому проводнику в область стриктуры устанавливают стент. Наличие рентгеноконтрастных меток позволяет легко ориентироваться при установке стента в области сужения. Расправление стента контролируют рентгенологически. После этого доставочное устройство извлекают.
Осложнения после стентирования кишечника
Стентирование, как и любое хирургическое вмешательство, связано с риском развития осложнений. Они могут возникнуть в процессе подготовки, во время установки стента или быть связаны с анестезиологическим способом. У большинства пациентов установка стента в кишечник проходит успешно. Все больные после стентирования при раке кишечника отмечают улучшение состояния, связанное с восстановлением продвижения газов и каловых масс. В раннем послеоперационном периоде для купирования умеренно выраженного болевого синдрома врачи назначают неопийные анальгетики.
Редко происходит миграция стента. В таком случае онкологи устройство удаляют и устанавливают новый стент. Существует риск перфорации толстой кишки ниже уровня опухолевого стеноза в результате выраженных супрастенотических изменений стенки кишки. В процессе выведения оптимальной позиции для установки стента редко происходит прободение непосредственно новообразования толстой кишки. Причиной осложнения является фиксация кишки опухолью, что не позволяет оптимально позиционировать стент в просвете кишечника.
Использование стентирования при раке кишечника позволяет онкологам Юсуповской больницы оказать пациентам полноценную квалифицированную медицинскую помощь в кратчайшие сроки. Стентирование выполняется опытным высококвалифицированным персоналом при наличии необходимого инструментария, RG- и эндоскопического оборудования. Получить консультацию вы можете по телефону клиники.

- Команда врачей, проводящих эндоскопические вмешательства
- Стентирование желудочно-кишечного тракта (ЖКТ)
- Как лучше перенести стентирование?
Стентирование — это способ восстановления просвета полого органа при помощи специального устройства — стента, который представляет собой тончайший металлический каркас, как правило, в форме цилиндра, способный восстанавливать форму трубчатых органов, измененную сдавлением либо врастанием опухоли.
Преимуществом эндоскопических методик является их высокая эффективность, минимальное количество осложнений, максимально быстрая реабилитация пациентов и существенное улучшение качества жизни за счет уменьшения количества дней, необходимых для реабилитации и сохранением физиологических функций стентируемого органа.
Команда врачей, проводящих эндоскопические вмешательства
Эндоскопическая хирургия в лечении онкологических пациентов требует от хирурга высокой точности, виртуозного владения методиками стентирования и немалого опыта. Нашим коллективом врачей под руководством доктора медицинских наук М. С. Бурдюкова выполнено:
- Более 1000 эндоскопических операций на желчных протоках;
- Более 200 эндоскопических стентирований при опухолях пищевода;
- Более 100 стентирований при опухолях желудка;
- Более 150 стентирований по поводу опухолей двенадцатиперстной кишки;
- Более 100 стентирований при опухолях толстой кишки;
- Более 50 эндоскопических операций у пациентов, ранее перенесших серьезное хирургическое вмешательство.
Эндоскопическое лечение отличает высокая эффективность с минимумом осложнений. Пациенты максимально быстро восстанавливаются, существенно улучшается качество их жизни, а функции стентируемого органа сохраняются.

Далее мы остановимся чуть подробнее на стентировании желудочно-кишечного тракта, стентировании желчевыводящих путей, а также трахеобронхиального дерева.
Стентирование желудочно-кишечного тракта (ЖКТ)
Стентирование желудочно-кишечного тракта — это малоинвазивный способ восстановления проходимости желудочно-кишечного тракта за счет установки стента. Это вмешательство проводится под двойным контролем: эндоскопическим и рентгенологическим, что позволяет максимально контролировать процесс и выполнять прецизионные, уникальные по своей точности операции.
Стентирование — это оптимальный способ помощи пациентам с опухолевыми и доброкачественными стриктурами (сужениями) ЖКТ, которым хирургическое лечение не показано в виду распространенности опухолевого процесса или при наличии противопоказаний к его проведению, а также, в некоторых случаях — как метод временной помощи перед предстоящим оперативным вмешательством.
Чаще всего стентирование применяется при следующих заболеваниях:
- опухоли пищевода, пищеводно-желудочного перехода, желудка, двенадцатиперстной кишки, толстой кишки;
- прорастание (компрессия) злокачественными опухолями смежных органов (при опухолях легкого);
- рецидив опухоли в области анастомоза после оперативного лечения;
- пищеводно-респираторные свищи;
- несостоятельность анастомозов после операции;
- доброкачественные стриктуры пищевода и анастомозов;
- перфорации пищевода, в том числе ятрогенные.

В этом случае цель вмешательства — улучшение качества жизни пациента за счёт восстановления пассажа пищи, жидкости и лекарственных препаратов по ЖКТ; возможность полноценного питания и приёма химиопрепаратов естественным способом. А также подготовка пациента к оперативному лечению, проведению химиотерапии и другим специфическим методам лечения.
Всю необходимую информацию о подготовке к стентированию в каждом конкретном случае пациент получает от лечащего врача. Но общим правилом является следующее: воздерживаться от приема пищи в течение определенного времени перед вмешательством.
Установка стента проводится в условиях медикаментозного сна, поэтому, никаких болезненных ощущений и дискомфорта пациент не испытывает. Время, затрачиваемое на выполнение стентирования, зависит от уровня расположения сужения, типа выбранного для установки стента и обычно составляет 15–45 минут. После выполнения эндоскопического стентирования пациенту выдается документ, содержащий протокол исследования и заключение. Протокол содержит детальное описание хода вмешательства. Врач, выполнявший стентирование, подробно пояснит о дальнейшем режиме питания, выдаст на руки краткую памятку. По желанию ход исследования может быть записан на диск, о чем необходимо предупредить медицинский персонал заранее.
В течение 30 минут после процедуры не следует пить. После выполнения вмешательства пациенту (либо его родственникам) выдается памятка, в которой указаны все необходимые рекомендации по течению послеоперационного периода, особенностях диеты и состояниях, которые возникают у пациента после стентирования. Рекомендуется проинформировать врача-эндоскописта при появлении необычных симптомов и любых тревожащих обстоятельствах в первые часы и дни после исследования.
Для избавления пациента от дисфагии (невозможности употреблять пищу) и обеспечения адекватного уровня качества жизни используется множество методов. Среди них хирургические, сопряженные с высокой частотой осложнений, летальностью, длительностью стационарного лечения и более высокой его стоимостью. Часто такие вмешательства не приводят к улучшению качества жизни. Использование других эндоскопических методов для реканализации просвета (например,электро- и лазерной коагуляции, бужирования, баллонной дилатации) требует длительного лечения с повторением сеансов, при этом их эффективность является кратковременной.
Поскольку стентирование это малоинвазивный метод восстановления проходимости желудочно-кишечного тракта, имеется риск возникновения как обычных, связанных с выполнением эндоскопического исследования, так и своих специфических осложнений. Частота серьёзных осложнений при проведении диагностического исследования достаточно низка и не превышает 0,01%. Подавляющее большинство осложнений могут быть скорректированы эндоскопическим или медикаментозным способом.
Стентирование желчевыводящих путей
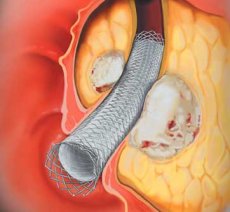
Стентирование желчевыводящих путей — малоинвазивный эндоскопический способ восстановления проходимости желчных путей при механической желтухе путем установки в желчные протоки на уровень сужения стента, который открывает просвет протоков и восстанавливает беспрепятственный отток желчи из печени в двенадцатиперстную кишку. Это вмешательство позволяет сохранить естественный желчеотток, что, во-первых, резко повышает качество жизни (не нужно ходить с выходящими наружу дренажами), кроме того, естественное поступление желчи не приводит к потере важных веществ, а также стимулирует нормальную работу кишечника.
Вмешательство проводится под двойным контролем: эндоскопическим и рентгенологическим, поскольку необходима точность движений и навигации даже большая, чем при стентировании ЖКТ.
Билиодуоденальное стентирование является оптимальным способом восстановления желчеоттока у пациентов с механическим блоком желчных протоков. Пациентам с опухолевыми и доброкачественными стриктурами ЖКТ, которым хирургическое лечение не показано в виду распространенности опухолевого процесса или при наличии противопоказаний к его проведению, а также, в некоторых случаях, как метод временной помощи перед предстоящим оперативным вмешательством.
Стентирование желчных протоков применяется при следующих заболеваниях, вызывающих затруднение желчеоттока и механическую желтуху:
- Опухоль поджелудочной железы, большого дуоденального сосочка, внепеченочных желчных протоков, двенадцатиперстной кишки;
- Метастатическое поражение печеночно-двенадцатиперстной связки;
- Желчекаменная болезнь, осложненная холедохолитиазом;
- Хронический панкреатит;
- Кисты поджелудочной железы;
- Постхолецистэктомический синдром;
- Стриктуры желчных протоков после различных операций на желчном пузыре и печени.
Методы лечения механической желтухи включают в себя восстановление оттока желчи, а также медикаментозную терапию, направленную на восстановление функции печени, избавление органов и тканей от накопленного избыточного билирубина.
Цель стентирования желчных протоков — это улучшение качества жизни пациентов за счёт восстановления пассажа желчеоттока наиболее физиологическим и безопасным способом — эндоскопическим. Способом, после которого в максимально быстрые сроки происходит восстановление функции печени. Стентирование желчных протоков, а также другие виды операций на желчном дереве, выполняемые эндоскопически являются либо самостоятельным и окончательным методом оказания помощи пациентам, либо подготовительным этапом перед операцией или проведением других, специфических методов лечения, например, таких как химиотерапия.
Установка билиодуоденального стента проводится в условиях медикаментозного сна и не вызывает никаких болезненных ощущений. Время, затрачиваемое на выполнение стентирования, зависит от уровня расположения, анатомических особенностях пациента, в частности анатомии панкреатобилиарной зоны, особенностей выполняемого вмешательства, типа и количества выбранных стентов. Обычно это 45–60 минут.
В течение суток после вмешательства пациенту рекомендуется соблюдать постельный режим и воздержаться от приема пищи. После выполнения вмешательства пациенту (либо его родственникам) выдают памятку, в которой указаны все необходимые рекомендации по течению послеоперационного периода, особенностях диеты и состояниях, которые возникают у пациента после стентирования. Рекомендуется проинформировать врача-эндоскописта при появлении необычных симптомов и любых тревожащих обстоятельствах в первые часы и дни после исследования.
Чрескожное дренирование внутрипечёночных желчных протоков или желчного пузыря это альтернативный метод лечения, который применяют при высоких блоках желчеотведения, когда имеются технические ограничения для эндоскопического стентирования.
Преимущества эндоскопического метода:
- малая инвазивность,
- статистически доказанная большая безопасность по сравнению с другими альтернативными способами восстановления желчеоттока,
- возможность удаления камней при холедохолитиазе,
- обеспечение физиологичного оттока желчи у большинства пациентов.
Осложнения также редки как и при других вариантах эндоскопического стентирования. Подавляющее большинство осложнений могут быть скорректированы эндоскопическим или медикаментозным способом.
Стентирование трахеобронхиального дерева
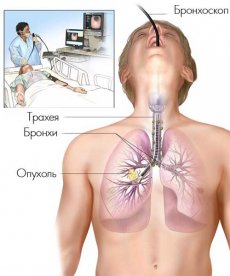
Стентирование трахеобронхиального дерева — это малоинвазивный способ восстановления проходимости трахеи и главных бронхов, обеспечивающий доступ воздуха к легочной ткани путем установки на уровень сужения стента. Вмешательство проводится под двойным контролем: эндоскопическим и рентгенологическим.
Стентирование является одним из способов помощи пациентам с опухолевыми и доброкачественными стриктурами трахеи и бронхов, страдающих выраженной дыхательной недостаточностью, которым хирургическое лечение не показано в виду распространенности опухолевого процесса или при наличии противопоказаний к его проведению. В некоторых случаях стентирование применяется для временной помощи перед предстоящим оперативным вмешательством, либо, при наличии перспективы от планируемой химиотерапии, как временный этап оптимизации дыхательной деятельности до момента ответа опухоли на химиотерапию.
Применяется при следующих заболеваниях:
- центральный рак лёгкого с вовлечением трахеи или главных бронхов,
- стриктуры трахеи или бронхов после длительного нахождения пациента на искусственной вентиляции легких,
- компрессия трахеи и главных бронхов увеличенными лимфатическими узлами,
- пищеводно-респираторные свищи,
- несостоятельность анастомозов после операции.
Целью вмешательства является улучшение качества жизни пациентов за счёт обеспечения доступа кислорода к легочной ткани путём восстановления просвета обтурированного бронха либо трахеи; подготовка пациента к оперативному лечению, проведению химиотерапии и другим специфическим методам лечения, реабилитация пациентов после длительного нахождения в условиях искусственной вентиляции лёгких, осложненной формированием стриктуры в месте стояния интубационной трубки, либо трахеостомы.

Установка стента проводится в условиях медикаментозного сна, поэтому, никаких болезненных ощущений и дискомфорта пациент не испытывает. Время, затрачиваемое на выполнение стентирования зависит от уровня расположения сужения, типа выбранного для установки стента и обычно составляет 15–45 минут.
Для избавления пациента от асфиксии и обеспечения адекватного уровня качества жизни используется множество методов:
- Хирургический метод в виду либо распространенности опухолевого процесса, либо морфологическим особенностям строения опухоли не всегда показан.
- Использование других эндоскопических методов для реканализации просвета — электро- и лазерной коагуляции, бужирования, баллонной дилатации — требует длительного лечения с повторением сеансов, при этом их эффективность является кратковременной.
- Выжидательная тактика направлена на получение ответа от проведения химиотерапии, однако, при выраженных симптомах дыхательной недостаточности, химиотерапевты могут отказаться от её проведения до коррекции дыхательной недостаточности.
Осложнения крайне редки и в случае возникновения могут быть скорректированы эндоскопическим способом.
Как лучше перенести стентирование?
Чтобы комфортно себя чувствовать во время стентирования, пациенту необходимо быть морально настроенным к исследованию, быть к нему подготовленным, знать, что исследование для него безопасное, знать, что он доверяет свое здоровье профессионалам.
Моральный настрой пациента может складываться из следующих факторов:
- вмешательство все равно необходимо сделать,
- от результатов вмешательства зависит здоровье,
- в Европейской клинике исследование выполняют только высококвалифицированные доктора.
В таком случае, во время проведения стентирования вы будете максимально расслаблены, что является одним из наиболее важных факторов, влияющих на успешность и эффективность проведения вмешательства.
Мерзляков М. В., Грачев А. В., Богачев Е. Г., Шапкин А. А., Перминов А. А., Хапаева Т. Н.
ГБУЗ Кемеровская областная клиническая больница
ГБОУ ВПО Кемеровская государственная медицинская академия
г. Кемерово
В соответствии с данными ВОЗ в 2010 году, рак толстой кишки занимает третье место в структуре онкологической патологии, а количество больных с запущенными формами заболевания достигает 70 %. Эта локализация рака составляет 15 % от всех первично диагностированных опухолей. Заболеваемость колоректальным раком составила около 19 случаев на 100000 населения, а смертность — около 9 на 100000 населения. [Ties Boerma & Carla AbouZahr et all, 2010].
Ежегодно в мире регистрируется более полумиллиона случаев заболевания раком толстой и прямой кишки и заболеваемость им увеличивается с течением последних десятилетий. Наибольшая заболеваемость отмечается в США, Канаде, странах Западной Европы и России. Менее выражен рост заболеваемости в странах Азии и Африки.
В общей (оба пола) структуре заболеваемости злокачественными новообразованиями населения России в 2011 году опухоли ободочной кишки составили 6,5 %, прямая кишка, ректосигмоидный отдел и анус 4,9 %. У мужского населения опухоли ободочной кишки составили 5,8 %. Значителен удельный вес злокачественных новообразований прямой кишки, ректосигмоидного соединения, ануса 5,2 %. Среди женского населения опухоли ободочной кишки в структуре заболеваемости злокачественными новообразованиями составили 7,0 %, прямой кишки, ректосигмоидного соединения, ануса 4,7 %. От 20 до 50 % больных колоректальным раком при первичном обращении имеют метастазы в печень [Ю. И. Патютко, 2005; А. М. Агавелян, 2010; В. И. Русин, 2011; В. И. Чиссов, В. В. Старинский, Г. В. Петрова 2013].
В Кемеровской области многолетняя динамика смертности от злокачественных опухолей ободочной и прямой кишки аналогична динамике заболеваемости. С 1995 по 2000 г. наблюдался период уменьшения смертности с последующим ее ростом с 2001 по 2010 г. За период с 1995 по 2000 г. смертность от колоректального рака в среднем составила 20,25 на 100 тыс. населения [18,65–21,94], а за период с 2001 по 2010 год — 25,56 на 100 тыс. населения [95 %ДИ=23,68–27,43]. Смертность от колоректального рака у мужчин и женщин в 2010 г. достигла показателя 31,16 на 100 тыс. населения (95 %ДИ=29,12–33,31), [А. С. Животовский, А. Г. Кутихин, Ю. А. Магарилл, Е. Б. Брусина 2012].
Несмотря на достижения современной медицины в диагностике заболеваний желудочно-кишечного тракта и, в частности патологии ободочной и прямой кишки, до 60–70 % больных к моменту обращения за медицинской помощью и постановки диагноза имеют осложнённое течение, требующее неотложного хирургического вмешательства.
Обтурационная кишечная непроходимость является самым частым осложнением рака толстой кишки. Она развивается у 26,4–69 % пациентов. Наиболее характерно это осложнение для опухолей левых отделов толстой кишки (67–72 %), что связано с особенностями местного роста и спецификой интрамурального лимфооттока.
На современном этапе развития хирургии основная цель большинства оперативных вмешательств заключается не только в ликвидации патологического процесса и его осложнений, но и в максимальном восстановлении утраченных функций резецированного органа. Отсутствие единой доктрины лечения, частые послеоперационные осложнения, а главное — высокая летальность — являются причиной постоянного внимания специалистов к этому разделу ургентной хирургии и делают эту проблему актуальной.
Общепризнанным стандартом тактики лечения опухолевой острой кишечной непроходимости левой половины толстой кишки является обструктивная резекция толстой кишки с наложением колостомы. По данным литературы до 65 % операций на толстой кишке завершаются формирование колостомы, а при острой кишечной непроходимости с левосторонней локализации опухоли этот показатель достигает почти 100 %.
Экстренная хирургическая резекция по поводу острой толстокишечной обструкции злокачественной природы связанна с летальностью, варьирующей от 7,2 % до 22,4 %.
Оперативное лечение, выполняемое по неотложным показаниям чаще всего, не сопровождаются адекватной лимфодиссекцией в результате чего, с позиций современной онкологии данное хирургическое лечение не может считаться радикальным. Восстановление непрерывности толстой кишки осуществляется вторым этапом через 8–12 месяцев.
Альтернативным способом разрешения острой обтурационной непроходимости кишечника у больных колоректальным раком на современном этапе развития хирургии является стентирование зоны обструкции металлическим саморасширяющимся стентом. Эта методика может быть использована как с целью предоперационной подготовки, так и в качестве окончательного способа лечения больных, которым операция не показана вследствие распространенности опухолевого процесса либо из-за тяжести сопутствующих заболеваний. Установка толстокишечного стента дает возможность проведения подготовки, стабилизации пациента и выполнения плановой, одноэтапной хирургической операции. [В. В. Веселов, А. В. Васильченко, А. Н. Кузнецов 2006 г.]
В 2012 году в клинике хирургии ГБУЗ КОКБ наблюдались 6 пациентов, жителей Кемеровской области, с клиническими проявлениями толстокишечной непроходимости злокачественной природы, с преимущественным поражением левых отделов толстой кишки (сигмовидная и прямая). Среди пациентов было две женщины и четыре мужчины. Возраст варьировал от 42 до 86 лет. Срок госпитализации от установления диагноза рака сигмовидной и прямой кишки от 2 недель до 2 месяцев.
У четырех пациентов морфологическая картина заболевания была установлена ранее, при гистологическом исследовании биопсийного материала, характер непроходимости был интермиттирующий. Все они поступили в клинику для планового оперативного вмешательства. Стентирование прямой и сигмовидной кишки было проведено как этап подготовки к одномоментной операции по поводу наличия злокачественной опухоли толстой кишки.
Один пациент не подозревал о наличии у себя онкологического заболевания и был доставлен машиной скорой медицинской помощи с клиникой острой толстокишечной непроходимости. При клиническом обследовании у него был выявлен генерализованный процесс с развитием канцероматоза брюшной полости, с вовлечением тонкой кишки в опухолевый конгломерат в области сигмовидной кишки и развитием тонкокишечной непроходимости через четыре дня лечения в стационаре.
Ещё один пациент страдал заболеванием более шести месяцев, в оперативном лечении ему было отказано, по причине наличия множественных метастазов в отдаленные органы, трижды прошел курс химиотерапии по поводу данного заболевания. Установка саморасправляющегося покрытого стента данному пациенту была показана как паллиативное разрешение интермиттирующей толстокишечной обтурационной непроходимости.
Всем пациентам в первые сутки госпитализации были установлены саморасправляющиеся покрытые стенты SX- ELLA Stent из никелид-титанового сплава. Имплантация проводилась в рентгеноперационной, без предварительной подготовки толстой кишки, вариантом выбора премедекации было внутримышечное введение раствора сибазона, по показаниям. Дистальный край опухоли отмечали наложением рентгеноконтрастной эндоскопической клипсы. По инструментальному каналу в просвет опухоли, под контролем рентгеноскопии проводили жесткую струну — проводник с атравматическим наконечником, аппарат извлекали. По струне проводнику проводили доставочное устройство, устанавливали рентгеноконтрастными метками дистальной части выше на 2,0 см. наложенных клипс маркеров. Полному раскрытию стента предшествовало введение водорастворимого контрастного вещества по катетеру доставочного устройства. После раскрытия стента доставочное устройство извлекалось. Стул у всех пациентов состоялся на операционном столе. Полное расправление стентов достигнуто на первые сутки после имплантации. Нормализация стула получена на вторые сутки. Четверо пациентов оперированы в сроки две недели после стентирования толстой кишки.
Пациент с неоперабельным раком сигмовидной кишки, в течение 6 месяцев дважды обращался в клинику для повторной имплантации стента, вследствие его миграции. Первая миграция через 1 месяц, затем следовал период мнимого благополучия 1 месяц с нормальным стулом. Вторая миграция через 2 месяца от первичной имплантации, стент установлен, толстокишечная непроходимость ликвидирована. Смерть пациента через 5 месяцев, до последнего дня жалоб на нарушения стула не было.
Пациенту с канцероматозом брюшной полости наложена илеостома. Больной выписан для симптоматического лечения по месту жительства, без нарушения пассажа по толстой кишке.
Выводы:
Установка никелид-титановых саморасправляющихся покрытых колоректальных стентов является эффективным, малотравматичным и элегантным методом решения острой обтурационной непроходимости кишечника опухолевого генеза, способным улучшить качество жизни пациентам перед радикальной операцией.
Читайте также:

