Рак у детей лекарства
МОСКВА, 5 февраля. /ТАСС/. Перебои с поставками в Россию некоторых лекарств для лечения онкозаболеваний у детей связаны с временным прекращением поставок фармацевтической субстанции цитарабина. Ситуация находится под контролем Минздрава РФ, сообщили в среду в пресс-службе министерства.
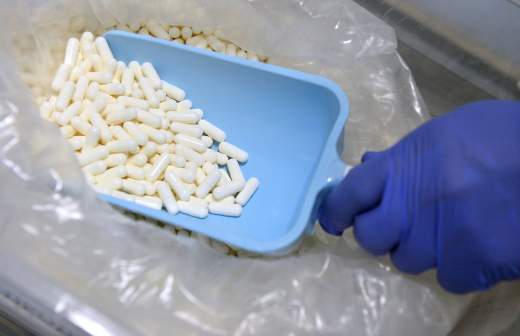
Ранее газета "Известия" сообщила, что детские онкологи и благотворительные фонды обеспокоены тем, что в клиниках заканчивается запас самых необходимых и эффективных препаратов для лечения рака у детей. Самая большая проблема возникла с препаратами "Онкаспар" и "Цитарабин", которые применяются при терапии лейкозов. По данным врачей и общественников, препараты не могут закупить уже несколько месяцев.
"В целях бесперебойного обеспечения онкологическими лекарственными препаратами Минздравом России было проведено совещание с представителями производителей лекарственных препаратов, содержащих действующее вещество цитарабин. По данным производителей, перебои с поставками вышеуказанных лекарственных препаратов связаны с временным прекращением поставок фармацевтической субстанции цитарабина, - говорится в сообщении.
В пресс-службе пояснили, что препарат по международному непатентованному наименованию (МНН) цитарабин представлен в России в нескольких наименованиях "Алексан", "Цитозар НоваМедика", "Цитарабин-ЛЭНС", "Цитарабин". По итогам совещания были достигнуты договоренности с производителями о поставках данных препаратов для обеспечения потребности на несколько месяцев, а также возобновить прекращенные поставки лекарств в страну. "Вопрос лекарственного обеспечения цитарабином и пэгаспарагиназом находятся на контроле Минздрава РФ", - говорится в сообщении.
По данным Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Д. Рогачева Минздрава РФ, потребность в препаратах с цитарабином составляет порядка 57 тыс. флаконов в различной дозировке. В то же время, по данным Росздравнадзора, с октября 2019 года в РФ было выпущено более 85 тыс. флаконов с данным действующим веществом. "На текущий год запланирован выпуск около 370 тыс. флаконов этого препарата", - следует из сообщения министерства.
У другого препарата, применяемого при лечении детских лейкозов, "Онкаспар" (МНН: пэгаспарагиназа), регистрация на территории РФ была отменена в августе 2019 года по решению производителя. "Лекарственный препарат "Аспарагиназа медак" начнет поставляться в 2020 году, а также зарегистрированы лекарственные препараты с наименованиями "Аспарагиназа" и "Веро-Аспарагиназа", - говорится в сообщении.
Дженерики
Как сообщил "Известиям" директор Института гематологии, иммунологии и клеточных технологий Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Д. Рогачева, профессор Алексей Масчан, врачам нужны оригинальные препараты, так как дженерики (воспроизведенные лекарства) подходят и помогают не всем.
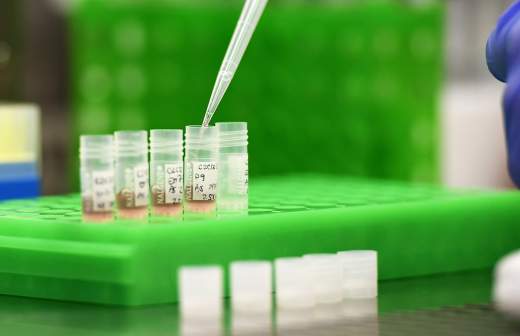
"Анализ данных по эффективности и безопасности зарегистрированных в РФ воспроизведенных лекарственных препаратов аспарагиназы и циторабина, поступающих в Росздравнадзор в ходе фармаконадзора, показывает, что выявляемые нежелательные реакции являются осложнениями терапии, описанными в инструкциях по применению данных лекарственных препаратов. По нежелательным реакциям на данные препараты проводились проверки Росздравнадзора, подтвердившие качество данных препаратов", - отмечают в пресс-службе.


Он подчеркнул, что для закупки онкаспара необходимо выделить федеральное финансирование. Кроме того, требуется распоряжение правительства о ввозе обезличенной партии препарата (то есть не для конкретных пациентов).
— Предвидя сложности, мы заранее закупили онкаспар, пока он был в России, поэтому прожили в спокойном режиме первую половину 2019-го. К концу года все стали понимать, что вопрос с регистрацией не решается. А этот препарат нужно принимать сразу после постановки диагноза, тратить время на заполнение документов и ожидание ответов никак нельзя. К сожалению, ни с одним лекарством нельзя разобраться по щелчку пальцев. Если власти ускорятся, то в течение года проблему возможно решить, — считает Екатерина Шергова.

В Минздраве ответили, что на 18 декабря 2019 года заявление о государственной регистрации онкаспара в ведомство не поступало. Решение о регистрации должны принимать разработчики и производители лекарственных средств.
Не та форма
— После публикации в Минздраве было несколько совещаний на эту тему. Проблему услышали и осознали, но никаких законодательных и правовых инициатив пока так и не было озвучено, — сказал Алексей Масчан.
По словам врача, с сентября ситуация с препаратом не изменилась, и онкоцентры по-прежнему остро нуждаются в нем.
— Производитель нужной больницам формы цитарабина, уже ушедший с рынка, сделал большую партию для детей, но препарат сразу раскупили, поскольку он нужен не только детям, но и взрослым. В итоге препарата снова не хватает и тем, и другим, — пояснил он.

Отечественные производители цитарабина есть, но они изготавливают препарат в количествах, формах и дозировках, которые подойдут не каждому. Между тем без этого лекарства многие пациенты просто не имеют шанса выжить.
Становитесь в очередь
Регионы испытывают дефицит препаратов для лечения онкозаболеваний у детей, признала и главный научный сотрудник НПЦ специализированной медицинской помощи детям им. В.Ф. Войно-Ясенецкого департамента здравоохранения Москвы, доктор медицинских наук Ольга Желудкова. Эксперт добавила, что в московских учреждениях проблем с препаратами нет.
По ее словам, в регистрации нуждается куда больший ряд препаратов. Так, стоит внести в госреестр препарат для высокодозной химиотерапии с аутотрансплантацией Тепадина, считает эксперт. Это лекарство применяется при эмбриональных опухолях головного и спинного мозга (медуллобластоме и нейробластоме центральной нервной системы и другими), а также для лечения рецидивов медуллобластомы. Сегодня он закупается за счет фондов, и его необходимо сделать более доступным.

— Мы сталкиваемся в проблемой ввоза, заполнением документов и регистрацией, что не позволяет своевременно проводить адекватное лечение. Это еще один препарат, который, на мой взгляд, требует регистрации. Замена таких препаратов влечет за собой снижение эффективности и излечиваемости пациентов, — заключила Ольга Желудкова.
Более того, в последнее время онкологи стали скрывать проблему от фондов.

Какой прогноз на выздоровление у малышей? Если в семье заболел один ребёнок, есть ли риск возникновения рака у его братьев или сестёр?
Чудо? Зафиксируйте!
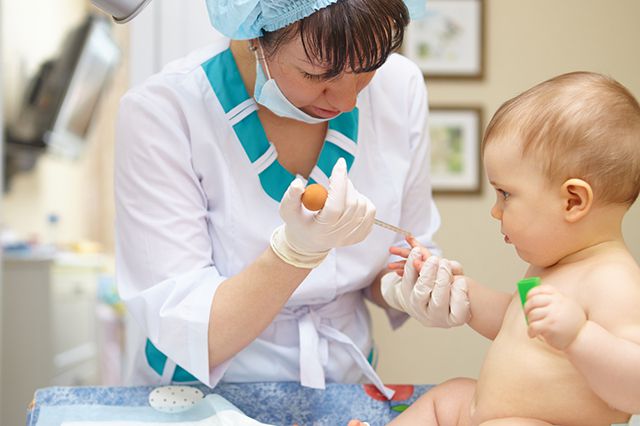
Маргарита Белогурова: Больше всего детей заболевают на первом году жизни. Далее заболеваемость падает – и второй пик приходится на подростковый возраст. Больше всего маленьких пациентов с острым лимфобластным лейкозом (рак крови), с опухолями центральной нервной системы (главным образом с опухолями головного мозга) и лимфомами (заболевания лимфатической ткани).
– С какими заболеваниями детские онкологи уже научились справляться?
– Прорыв в лечении детей со злокачественными новообразованиями произошёл в 90‑е годы прошлого века, когда в Россию пришли западные протоколы и методы интенсивного лечения детских опухолей. Сегодня в крупных центрах онкологи достигли впечатляющих результатов лечения: при лимфобластных лейкозах – 80% излечения, при некоторых его видах – больше 90%, при лимфоме Ходжкина – почти 95%, при опухоли Вилмса (почки) – почти 90%.
– Правда ли, что шанс на излечение у детей выше, чем у взрослых?
– У детей другая биология опухолей, благодаря которой эти опухоли хорошо отвечают на лечение. Поэтому прогнозы на излечение от рака у детей более благоприятные. Нередко мы видим, что детская опухоль (даже на запущенной четвёртой стадии заболевания, с распространёнными метастазами) тает, как снег, буквально на глазах. И речь идёт не о продлении жизни (как у взрослых), а о полном излечении от рака.
У детей также фиксируются случаи спонтанного исцеления от рака. Например, если ребёнок заболел нейробластомой до года, есть вероятность того, что опухоль исчезнет независимо от того, лечили его или нет. Такое чудо происходило в практике любого детского онколога, в том числе и в моей. Все они описаны, задокументированы и подтверждены снимками и результатами исследований.

Родные в группе риска
– Если ребёнок благополучно вылечился, могут ли родители выдохнуть и навсегда забыть о болезни?
– Это зависит от того, чем ребёнок болел. Например, если ребёнок вылечился от лимфомы Беркитта и с момента выздоровления прошёл год – о болезни можно забыть, поскольку рецидивов после года этой агрессивной опухоли не бывает. После опухоли костей выдохнуть можно только спустя 6–8 лет. Однако нужно помнить, что онкологи лечат ребёнка, который растёт, тяжёлыми препаратами, негативно влияющими на сердце, почки, рост, половое развитие. Поэтому наши пациенты нуждаются в пожизненном наблюдении. В первые годы оно нужно, чтобы вовремя выявить и ликвидировать рецидив, в последующие – чтобы своевременно корректировать возможные последствия перенесённого лечения.

– На родительских форумах самая обсуждаемая тема – вероятность возникновения рака у родных братьев и сестёр заболевшего ребёнка?
– Раньше мы успокаивали родителей, говоря, что в одну воронку бомба два раза не падает. Современные исследования показывают, что раковые бомбы – исключение. Поскольку рак – болезнь генов, то чем ближе генетический материал детей, тем выше вероятность того, что болезнь возникнет и у другого ребёнка. Наивысшая степень риска у близнецов. У родных братьев и сестёр заболевшего ребёнка вероятность возникновения рака на 25% выше, чем в семьях, где нет онкобольных. Наблюдаться у врача они тоже должны пожизненно, поскольку рак может возникнуть не только в детстве, но и спустя 20–40 лет.
Везде и повсеместно
– Везде ли врачи лечат одинаково успешно? Зависит ли прогноз на выздоровление от места, где ребёнок живёт?
– Если наш пациент живёт там, где у него нет возможности полноценно лечиться (а центров, где представлены не все спектры возможностей современной онкологии в России, к сожалению, немало), то местные врачи должны отправить его в федеральную клинику. Другое дело, что из-за нехватки мест там его могут не принять на лечение. Но даже в таких случаях ребёнок возвращается на лечение по месту жительства с конкретными рекомендациями, а процесс контролируется врачами из федеральной клиники.
Кстати, федеральные центры в Москве и Санкт-Петербурге не берут на лечение местных малышей, поскольку нацелены на лечение детей из регионов. Но всех они принять, к сожалению, не могут.

– Когда говорят, что в России лечат так же и с тем же результатом, что и на Западе, это часто воспринимается как лукавство.
– Между тем это правда. В России лечат по западным протоколам и теми же лекарствами, что и в европейских и американских клиниках. Поэтому результаты лечения полностью сопоставимы. Другое дело, что это хрупкое равновесие. Если лекарства наших пациентов попадут под ответные санкции и мы будем вынуждены работать с неизвестными препаратами, удержать эту планку нам вряд ли удастся.
Почему у детей возникает рак?
У детей опухоли преимущественно эмбриональной природы. Если при закладке произошёл какой-то сбой или ошибка (порок сердца, неопущение яичка, удвоение почки) или ребёнок – носитель патологического гена, за ним нужно пристально следить: вовремя проходить врачей-специалистов (узкие специалисты знают ассоциативные связи патологии и видов опухолей) и дважды в год делать УЗИ.
Лекарственное лечение злокачественных опухолей у детей является относительно новым, но очень перспективным направлением комплексной терапии, что связано с высокой чувствительностью большинства новообразований у детей к противоопухолевым препаратам. Лишь менее 9 % из них не реагирует положительно на это лечение. Разнообразие злокачественных опухолей практически исключает возможность создания препарата, одинаково эффективного для всех новообразований. В связи с этим проводится широкий поиск препаратов различного механизма действия, что имеет важнейшее значение для комбинированной химиотерапии опухолевых заболеваний.
Все препараты, используемые в настоящее время в химиотерапии опухолей, делятся на две группы — гормональные и собственно химиотерапевтические синтетического и природного происхождения. Первые используются для лечения новообразований, сохранивших способность тканей, в которых они развиваются, реагировать на гормоны, в норме регулирующие их рост. К ним относятся андрогены, эстрогены, прогестероны, кортикостереоиды.
Терапевтический эффект большинства химиопрепаратов связан с подавлением ими различных этапов обмена нуклеиновых кислот в опухолевых клетках. Препарат может непосредственно взаимодействовать с нуклеиновыми кислотами, нарушая их способность нормально функционировать, и может взаимодействовать с ферментами, ответственными за биосинтез и функционирование нуклеиновых кислот.
Группы химиопрепаратов
Алкилирующие препараты, способные реагировать с нуклеофильными центрами, нарушая синтез ДНК и в меньшей степени РНК, в результате чего наступают изменения структуры дезоксирибонуклеопротеидов, и клетки становятся нежизнеспособными. В эту группу входят эмбихин, новэмбихин, допан, циклофосфан, сарколизин, фторбензотэф и др.
Антиметаболиты, т. е. вещества, сходные по химической структуре с витаминами, которые включаются вместо них в процессы обмена, действуя при этом как конкурентные ингибиторы важных метаболических процессов. Так, фолиевая кислота принимает участие в синтезе пуринов и пиримидинов и соответственно в синтезе нуклеотидов. Антифолиевые препараты, аналоги пурина и пиримидинов, имеют, таким образом, большое значение в химиотерапии. Такие препараты из этой группы, как метотрексат, 6-меркаптопурин, 5-фторурацил, фторафур, цитозинарабинозид, относятся к числу лучших из известных противоопухолевых средств.
Противоопухолевые антибиотики (дактиномицин, хризомалин, аурантин, брунеомицин, рубомицин, карминомицин, митоцин С, стрептонигрин, блеомицин, адриамицин), состоящие из различных аминокислот, соединенных с хромоформной группой, нашли широкое применение в лечении многих системных и солидных новообразований у детей.
Препараты растительного происхождения (винкристин, винбластин) являются митотическими ядами, блокирующими митозы клеток.
Прочие противоопухолевые препараты с неуточненным механизмом действия (аспарагиназа, имидазол-карбоксамид (ДТIС), хлодитан (орто-пара-ДДД), прокарбазин (натулан), производные нитрозомочевины (BCL, CCL).
Выбор препарата обычно основывается на знании его эффективности при том или другом морфологическом виде опухоли. Некоторые из противоопухолевых агентов метаболически инертны, пока они не активированы нормальной тканью организма. Применение циклофосфана не дает местного эффекта, так как он метаболически инертен до тех пор, пока не метаболизируется в печени.
Одним из существенных ограничений при применении химиотерапии является устойчивость в некоторых анатомических регионах злокачественных клеток, где концентрация препаратов недостаточна для достижения их гибели.
Так, большинство противоопухолевых препаратов не проникает через гематоэнцефалический барьер, что является причиной последующего развития нейролейкоза. Для его профилактики применяют эндолюмбальное введение метотрексата и лучевую терапию.
Таким образом, до начала химиотерапии необходимо комплексное обследование больного для выяснения состояния ряда органов и систем, в частности костномозгового кроветворения, печени, почек и др.
В настоящее время в детской онкологии в большинстве случаев химиопрепараты применяют внутривенно (системная химиотерапия). В ряде случаев химиопрепараты вводят эндолюмбально. В последние годы при лечении рада злокачественных опухолей широкое применение получила регионарная (в частности, внутриартериальная) химиотерапия, проводимая с помощью современных инфузаторов. Этот метод с успехом применяется при саркомах мягких тканей и костей. Проводятся исследования по использованию этого метода при раках печени и нефробластомах.
Метод основан на гипотезе создания в очаге поражения высокой и постоянной концентрации лекарственного препарата с одновременным снижением токсического действия лекарственного агента.
В настоящее время общепризнано, что наибольший эффект следует ожидать от полихимиотерапии. Обычно в комбинацию включают препараты, в той или иной степени активные при данной опухоли.
Теоретически целесообразно включение препаратов: 1) обладающих разным механизмом действия, т. е. имеющих разные точки приложения на обмен опухолевых клеток; 2) действующих на разные фазы клеточного цикла, на чем основан принцип синхронизации клеточной популяции (применение препарата, блокирующего определенную фазу клеточного цикла для обеспечения последующего максимального воздействия через определенный промежуток времени другого препарата, действующего в этой фазе); 3) оказывающих различное побочное действие с тем, чтобы избежать суммации токсических эффектов; 4) обладающих различной быстротой действия с тем, чтобы более медленно действующий закрепил ремиссию, достигнутую быстродействующим препаратом.
Лекарственная противоопухолевая терапия применяется как самостоятельно, так и в комбинации с хирургическим и лучевым методами лечения.
Предоперационная химиотерапия предполагает выполнение грех основных задач:
- уменьшение размеров опухоли для создания благоприятных условий при операции и абластики;
- определение биологической чувствительности опухоли к химиопрепаратам;
- профилактика потенциально имеющихся метастазов в доклинической стадии и лечение имеющихся отдаленных метастазов.
Это важно для решения вопроса о целесообразности применения данной комбинации препаратов в послеоперационном периоде с целью профилактики рецидивов и метастазов.
Профилактическая и поддерживающая химиотерапия показала свою целесообразность при многих новообразованиях у детей — нефробластоме, нейробластоме, рабдомиосаркоме, не говоря уже о системных поражениях (лимфосаркома, лимфогранулематоз, лейкоз). При назначении профилактической химиотерапии необходимо руководствоваться степенью лечебного (лекарственного) патоморфоза в удаленной или подвергшейся биопсии опухоли после проведения предоперационной химиотерапии. При наличии III—IV степени патоморфоза профилактическое лечение проводят по той же схеме; при I—II степени необходимо провести замену химиопрепаратов.
Наконец, при диссеминированных новообразованиях химиотерапия является ведущим, а в большинстве случаев и единственным методом лечения.
При оценке эффективности химиотерапии учитывают рекомендации, предложенные ВОЗ в 1977 г.:
а) полный эффект. Исчезновение всех опухолевых образований, определяемое дважды в течение срока не менее 4 нед;
б) частичный эффект. Уменьшение всех измеряемых опухолей не менее чем на 50 %, определяемое дважды в срок не менее 4 нед. При этом не должно обнаруживаться появление новых опухолевых очагов;
в) без эффекта. К этой категории относятся те больные, у которых отмечается уменьшение опухолей менее чем на 50 % или увеличение их менее чем на 25 %. При этом не должно констатироваться появление новых опухолевых очагов;
г) прогрессирование. Увеличение размеров опухолей на 25 % или больше, появление новых опухолевых очагов. Уменьшение опухоли менее чем на 50 % не оценивается как улучшение, а увеличение ее менее чем на 25 % не рассматривается как ухудшение.
Продолжительность общего эффекта отсчитывается от даты начала лечения до даты первого наблюдения прогрессирования болезни. Продолжительность полного объективного эффекта измеряется от даты, когда этот полный эффект впервые зарегистрирован, до даты, когда отмечены первые признаки прогрессирования заболевания. Для частичного эффекта отсчет ведется от начала лечения.
При проведении химиотерапии часто наблюдаются различные проявления токсичности препаратов, т. е. изменение нормальной биологической деятельности живой клетки в патологическом направлении. Оказывая подавляющее действие на быстро размножающиеся клетки злокачественной опухоли, препараты воздействуют и на такие нормальные клетки и их ткани, как кроветворные органы, слизистая оболочка кишечника, нервная ткань. Отмечены токсические воздействия многих препаратов на определенные органы и ткани. Так, препараты винкоалкалоидов воздействуют на нервную ткань, антрациклины — на сердечную мышцу. Комбинируя препараты с различными токсическими воздействиями, можно получить дополнительный эффект воздействия на опухолевые клетки, не усиливая побочные эффекты химиотерапии.
Различают немедленные побочные реакции, возникающие в 1-е сутки введения препаратов (тошнота, рвота), ранние, развивающиеся в пределах 1-й недели и представленные разнообразными токсическими явлениями со стороны кроветворения, нервной системы, печени, почек, и поздние побочные реакции, аналогичные ранним, но наблюдающиеся в более поздние сроки в процессе дальнейшего лечения. Нередко последние являются результатом кумуляции длительно применяющихся препаратов.
При выраженности побочных проявлений химиотерапию прерывают, а в ряде случаев и прекращают. Наиболее частой причиной прерывания лечения являются нарушения кроветворения, характеризующиеся уменьшением числа лейкоцитов и тромбоцитов. Проведение лекарственного лечения с учетом возможных побочных эффектов и своевременным принятием профилактических мер может предупредить возникновение серьезных осложнений.
Даже короткое перечисление методов лечения, применяемых в детской онкологии, показывает, какой значительный арсенал терапевтических средств имеется в настоящее время в руках детского онколога. В последние десятилетия разработаны наиболее эффективные программы комплексного лечения многих злокачественных новообразований, учитывающие возможности хирургического, лучевого и лекарственного методов. Комбинации их и удельный вес каждого из них существенно колеблются в зависимости от морфологического вида, распространенности опухоли, ее чувствительности к химиолучевой терапии и, наконец, от возраста больного ребенка.
В течение последних двух десятилетий произошли существенные сдвиги в детской онкологии в виде совершенствования методов диагностики и комплексного лечения злокачественных новообразований у детей.
Наиболее значительные результаты в лечении многих злокачественных новообразований в локализованной стадии получены в последнее десятилетие (1970—1980). Достигнутые успехи объясняются главным образом большим вниманием многих исследователей к проблеме детской онкологии, интенсивной разработкой и внедрением в практику новых методов диагностики, химиолучевой терапии.
В настоящее время с учетом неудовлетворительных результатов лечения ряда нозологических форм злокачественных заболеваний у детей, таких как забрюшинная нейробластома (5-летняя выживаемость не более 20 %), тератобластомы (5-летняя выживаемость не более 15 %), для улучшения результатов лечения стала применяться так называемая высокодозная полихимиотерапия. Этот вид лечения проводится одновременно с трансплантацией костного мозга и дает обнадеживающие предварительные результаты. Однако оно должно проводиться только в специализированных отделениях на базе детских онкогематологических учреждений.
Вместе с тем необходимо подчеркнуть, что чем своевременнее диагностирована опухоль, тем больше шансов добиться выздоровления ребенка даже при применении менее агрессивной терапии.

Детская онкология — это то, что окружает нас каждый день. Со всех сторон мы слышим о сборе средств на лечение очередного заболевшего малыша. Болезнь не щадит детей любого возраста, от новорождённых малышей, до подростков.
Благодаря недавним достижениям в медицине более 80% больных могут прожить более пяти лет после постановки диагноза по сравнению только с 58% в 1970-х годах.
Наиболее распространённые виды детских онкологических заболеваний.
Лейкоз — это рак костного мозга и крови, он наиболее распространён. Примерно 1/3 всех детских онкологических диагнозов приходятся на лейкозы. Существует много типов лейкозов, но два наиболее часто встречающихся у детей: острый миелолейкоз (ОМЛ) и острый лимфолейкоз.
Рак костей — существует два типа рака костей, и вместе они составляют около трёх процентов детских онкологических заболеваний. Первый тип — остеосаркома, наиболее распространён у молодых людей и подростков. Опухоли обычно локализуются в руках или ногах. Саркома Юинга является вторым основным типом рака кости и встречается реже. Этот тип саркомы встречается у подростков и наиболее распространён в костях таза и грудной клетки.
Нейробластома — шесть процентов детских онкологических заболеваний являются нейробластомами. Этот рак образуется в нервных клетках развивающихся эмбрионов. Опухоли появляются у младенцев и маленьких детей, в основном в возрасте до десяти лет. Опухоли нейробластомы обычно начинаются в брюшной полости, но могут начинаться где угодно.
Опухоли головного/спинного мозга — чуть более четверти всех детских раковых заболеваний являются опухолями головного мозга. Эти опухоли обычно локализуются низко в головном мозге, в отличие от взрослых опухолей мозга, которые обычно обнаруживаются выше. Опухоли спинного мозга или головного мозга являются второй по распространённости формой рака.
Рабдомиосаркома — рак скелетной мышцы, рабдомиосаркома может начинаться в любом месте организма и является наиболее распространённым раком мягких тканей у детей, на долю которого приходится 3% всех детских раковых заболеваний.
Опухоль Вильмса растёт в одной из почек и очень редко присутствует в обеих почках. Опухоли Вильмса чаще всего выявляются в возрасте от трёх до четырёх лет и составляют только пять процентов детских раковых заболеваний.
Лимфомы — этот рак поражает иммунную систему и обычно начинается в лимфатических узлах. Лимфома может также распространиться на костный мозг и другие органы. Лимфомы Ходжкина и Неходжкина могут возникать как у взрослых, так и у детей. Лимфома Ходжкина — это три процента детского рака, а неходжкинская — пять процентов.
Лечение детской онкологии.
План лечения детского рака варьируется в зависимости от типа и стадии. Наиболее распространённые методы лечения включают хирургию, химиотерапию и радиацию. Другие методы лечения рака включают трансплантацию стволовых клеток, иммунотерапию и другие.
Наиболее эффективным методом лечения детской онкологии в целом является химиотерапия. Это лекарство направлено на то, чтобы повлиять на быстрорастущие раковые клетки, а большинство детских онкологических заболеваний весьма агрессивны. Но дети лучше чем взрослые отвечают на лечение, легче переносят более высокие дозировки лекарств, и быстрее, и легче восстанавливаются. Хотя реакции на химиотерапию могут быть весьма интенсивными, облучение может быть худшим выбором для детей. Серьёзные долгосрочные побочные эффекты от радиации, больше, чем от химиотерапии.
В идеале у ребёнка, заболевшего онкологическим заболеванием, должна быть целая команда врачей и специалистов, которые бы следили и лечили ребёнка, а также оказывали ему и его семье всестороннюю поддержку. Это:

Детская онкология — это то, что окружает нас каждый день. Со всех сторон мы слышим о сборе средств на лечение очередного заболевшего малыша. Болезнь не щадит детей любого возраста, от новорождённых малышей, до подростков.
Благодаря недавним достижениям в медицине более 80% больных могут прожить более пяти лет после постановки диагноза по сравнению только с 58% в 1970-х годах.
Наиболее распространённые виды детских онкологических заболеваний.
Лейкоз — это рак костного мозга и крови, он наиболее распространён. Примерно 1/3 всех детских онкологических диагнозов приходятся на лейкозы. Существует много типов лейкозов, но два наиболее часто встречающихся у детей: острый миелолейкоз (ОМЛ) и острый лимфолейкоз.
Рак костей — существует два типа рака костей, и вместе они составляют около трёх процентов детских онкологических заболеваний. Первый тип — остеосаркома, наиболее распространён у молодых людей и подростков. Опухоли обычно локализуются в руках или ногах. Саркома Юинга является вторым основным типом рака кости и встречается реже. Этот тип саркомы встречается у подростков и наиболее распространён в костях таза и грудной клетки.
Нейробластома — шесть процентов детских онкологических заболеваний являются нейробластомами. Этот рак образуется в нервных клетках развивающихся эмбрионов. Опухоли появляются у младенцев и маленьких детей, в основном в возрасте до десяти лет. Опухоли нейробластомы обычно начинаются в брюшной полости, но могут начинаться где угодно.
Опухоли головного/спинного мозга — чуть более четверти всех детских раковых заболеваний являются опухолями головного мозга. Эти опухоли обычно локализуются низко в головном мозге, в отличие от взрослых опухолей мозга, которые обычно обнаруживаются выше. Опухоли спинного мозга или головного мозга являются второй по распространённости формой рака.
Рабдомиосаркома — рак скелетной мышцы, рабдомиосаркома может начинаться в любом месте организма и является наиболее распространённым раком мягких тканей у детей, на долю которого приходится 3% всех детских раковых заболеваний.
Опухоль Вильмса растёт в одной из почек и очень редко присутствует в обеих почках. Опухоли Вильмса чаще всего выявляются в возрасте от трёх до четырёх лет и составляют только пять процентов детских раковых заболеваний.
Лимфомы — этот рак поражает иммунную систему и обычно начинается в лимфатических узлах. Лимфома может также распространиться на костный мозг и другие органы. Лимфомы Ходжкина и Неходжкина могут возникать как у взрослых, так и у детей. Лимфома Ходжкина — это три процента детского рака, а неходжкинская — пять процентов.
Лечение детской онкологии.
План лечения детского рака варьируется в зависимости от типа и стадии. Наиболее распространённые методы лечения включают хирургию, химиотерапию и радиацию. Другие методы лечения рака включают трансплантацию стволовых клеток, иммунотерапию и другие.
Наиболее эффективным методом лечения детской онкологии в целом является химиотерапия. Это лекарство направлено на то, чтобы повлиять на быстрорастущие раковые клетки, а большинство детских онкологических заболеваний весьма агрессивны. Но дети лучше чем взрослые отвечают на лечение, легче переносят более высокие дозировки лекарств, и быстрее, и легче восстанавливаются. Хотя реакции на химиотерапию могут быть весьма интенсивными, облучение может быть худшим выбором для детей. Серьёзные долгосрочные побочные эффекты от радиации, больше, чем от химиотерапии.
В идеале у ребёнка, заболевшего онкологическим заболеванием, должна быть целая команда врачей и специалистов, которые бы следили и лечили ребёнка, а также оказывали ему и его семье всестороннюю поддержку. Это:
Читайте также:


