Причины заболевания раком молочной железы и возможности его профилактики
Процесс развития любого онкологического отклонения происходит по одинаковой схеме. Начало процесса – неконтролируемое организмом деление клеток органов и тканей, где происходит локализация новообразования. Раковые клетки носят злокачественный характер и меняют структуру настолько сильно, что без специальных медицинских тестов невозможно определить первоначальную структуру клетки. Рак – это появление новообразования злокачественного характера, при котором рост атипичных клеток повышен, он прорастает в органы и ткани. Идёт распространение раковых клеток по организму через лимфатическую систему и систему кровоснабжения. В случае метастазирования онкологии в жизненно важные органы может наступить смерть пациента. Запущенный онкологический процесс – всегда опасный.
Исходя из этого, происходит расчёт стадийности болезни. Первая стадия – прогноз на выздоровление и сохранение жизни приближен к 100%. Лечение на четвёртой стадии не даёт практического результата и призвано продлить жизнь и облегчить состояние. Хирургическое вмешательство нецелесообразно по причине глубокого повреждения метастазами всего организма без отношения к локальному месту произрастания опухоли. Статистика неумолимо подтверждает, насколько важна ранняя диагностика.
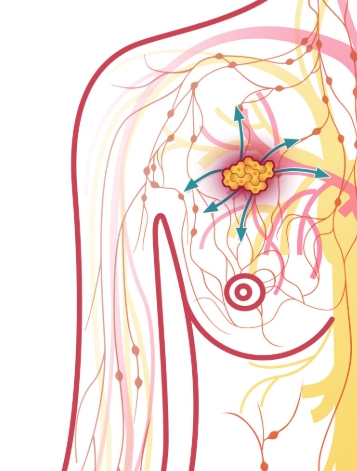
Развитие онкологических патологий – серьёзная проблема в современном обществе. Они возникают у детей и взрослых, у мужчин и женщин. Статистические показатели развития рака говорят: если брать в расчёт онкологию среди женщин, рак молочной железы – на лидирующих позициях. Это опасное заболевание, вовремя принятые медицинские меры спасут жизнь пациентки. Полагается соблюдать врачебные рекомендации по профилактическим мерам для сокращения риска развития этой патологии. Профилактика рака молочной железы – комплекс действий, направленных на минимизацию риска возникновения патологии и на своевременное обнаружение онкологии.
Особенности профилактики
Профилактика рака груди у женщин сокращает смертность. Она призвана уменьшить риск развития онкологи, а при ремиссии – рецидива болезни. Профилактика рака молочных желёз:
- первичная;
- вторичная;
- третичная.
Профилактический комплекс мероприятий, призванных определить начальные процессы формирования злокачественных опухолей. Раннее выявление болезни – основной фактор простого и быстрого лечения в сравнении с запущенными стадиями.
Профилактические меры начальной группы:
- здоровый образ жизни;
- достаточная подвижность каждый день;
- отсутствие вредных привычек и зависимостей;
- физические упражнения, направленные на укрепление мышц груди;
- борьба с проявлениями стресса;
- снижение массы тела;
- отказ от гормональных препаратов после наступления менопаузы;
- потребление достаточного витаминного комплекса;
- правильное питание;
- правильно подобранные продукты;
- регулярная самодиагностика.
Самодиагностика проводится регулярно перед наступлением месячных. Первые проявления рака замечаются при пальпации и визуальном осмотре груди. Диагностика предупреждает развитие патологических процессов. Памятка, выпущенная министерством здравоохранения, содержит перечень основных симптомов, на которые нужно обратить внимание, а также способы самостоятельного диагностирования патологии.
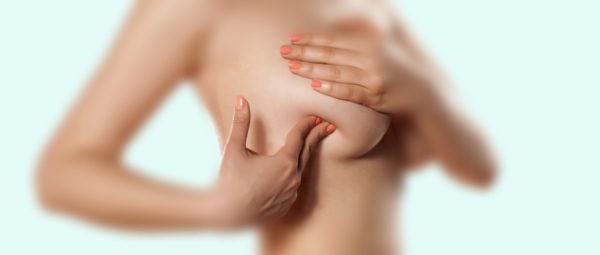
Для выполнения диагностики женщине нужно встать перед зеркалом и осмотреть область грудной клетки. Первичное внимание уделить форме груди, форме ореолы и соска. Поднять обе руки вверх, провести визуальный осмотр в таком положении. Произвести пальпацию груди, положив три пальца на область ореолы и совершать круговые движения по всей площади груди. На наличие выделений самодиагностика производится с помощью зажатия соска между указательным и большим пальцем руки. Повторить процедуру пальпации в положении лежа. Проверить область подмышек, где расположены лимфоузлы, на предмет их увеличения.
При обнаружении любых признаков проявления стоит обратиться к врачу. На рак могут указывать:
- появление выделений крови или гноя из соска;
- изменение формы груди;
- изменение цвета кожных покровов;
- сухость кожи;
- шелушение соска;
- увеличение в районе лимфоузла;
- уплотнения в молочной железе;
- боль при пальпации в области груди.
Этот комплекс профилактических действий начинается при установлении в ходе самодиагностики признаков начала онкологии. Женщина должна обратиться к маммологу для проведения диагностических мероприятий под контролем дипломированных специалистов.
Женщине назначают ультразвуковое исследование и маммографию. Ультразвуковое исследование молочных желёз призвано установить наличие опухоли размером от 2,5 миллиметров. Процедура полностью безопасна, не влияет на жизненные процессы, не причиняет боли и нет необходимости в стационарном нахождении. Всё можно выполнить амбулаторно. В профилактических целях это исследование назначается при употреблении пациенткой гормональных препаратов, которые могут спровоцировать рост опухоли.

Маммография – скрининговое исследование молочных желёз на специальном рентгеновском оборудовании. Процедуру рекомендовано проходить раз в год женщинам старше 50 лет. Для молодых женщин назначается при явном наличии признаков онкологического процесса.
Вторичная профилактика включает прохождение обследований у маммолога, онколога и гинеколога. Дополнительные исследования назначаются по прямому назначению специалистов узкого профиля при наличии соответствующих показаний к ним.
Основная задача производимых действий при этом виде профилактики заключается в своевременном определении возникновения метастазирования. Диагностические мероприятия назначаются специалистом-онкологом при чётко разработанном плане лечения больного. Обязательно выполнять все предписанные клинические рекомендации лечащего врача. Онкологом могут быть назначены следующие виды диагностики:
- Анализ крови на онкомаркеры.
- Биопсия повреждённой ткани под контролем ультразвукового исследования.
- Биопсия повреждённой ткани под контролем магнитно-резонансной томографии.
- Биопсия повреждённой ткани под контролем маммографии.
- Иные исследования по усмотрению врача.
Для прохождения специальных диагностических процедур можно посетить онкологический диспансер. Это необходимая мера для наибольшей диагностической достоверности.
К сожалению, при современном уровне развития медицины невозможно полностью исключить риск развития онкологического процесса. Профилактика позволяет только минимизировать возможные риски. При постоянном проведении самодиагностики повышается шанс своевременного врачебного вмешательства, что повышает шансы на полное избавление от недуга.
Обследование у врача в обязательном порядке должны проходить женщины, уже проходившие лечение от рака молочной железы, и у которых болезнь находится в стадии ремиссии.
Частота профилактической диагностики зависит от времени после проведённого лечения. В первый год после онкологии проверка проводится раз в 4 месяца. Один раз в полгода на второй год. Затем раз в год.

Диета при профилактике
По статистике, соблюдение диеты – одно из ключевых правил профилактики онкологии молочной железы. Высокая калорийность продуктов при неумеренном употреблении их в пищу вызывает развитие опухолевых новообразований в организме человека. Дополнительно снижается уровень защиты организма, общее состояние здоровья, работа сердца и сосудов.
Приведённые выше утверждения подтверждаются статистически. Более 75% женщин, проходящих лечение от онкологии груди, страдает от повышенного веса. Статистика выживаемости в 10-летний период указывает на необходимость сохранения стройной фигуры. Правильно подобранная для пациента диета и строгое соблюдение предписаний по части продуктов обеспечат женщине возможность сохранить свою жизнь и здоровье.
Жиры продуцируют гормоны, сильно влияющие на рост опухоли. При повышенном содержании жиров гормонов вырабатывается больше – следовательно, повышается риск развития патологии.
Соблюдение диеты рекомендовано и для полноценного развития и восстановления деятельности иммунной системы человека, обеспечивающее общие защитные функции организма.
Диета включена в комплекс общеукрепляющих мер при проведении противоопухолевой терапии. Издаётся соответствующий буклет, в котором подробно расписываются основные принципы диетического питания, о которых мы сейчас и поговорим.
Принципы построения рациона в период проведения профилактических мероприятий заключаются в выполнении следующих рекомендаций:
- Рацион питания делится на 4-6 приёмов пищи с соблюдением режима приёма продуктов. Еда должна происходить примерно в одно и то же время.
- Сахар, его заменители, соли и иные специи должны быть дозированы либо по возможности исключены из рациона.
- Суточная норма употребления питьевой воды должна быть на уровне не ниже 2-х литров для полноценной работы почек по выведению из организма вредных химических элементов.
- Блюда должны быть свежими и употребляться непосредственно после приготовления.
- Рацион наполнен витаминизированными компонентами, такими как овощи и травы.
- Рацион должен содержать обилие клетчатки.
- Рацион гармоничен по принципу верного содержания белков, жиров и углеводов на 100 граммов продукта.

При низкотемпературных сезонах желательно регулярно употреблять мультивитаминные комплексы для поддержания работы организма.
При нахождении пациентки на диете присутствует прямой запрет на употребление списка продуктов:
- алкогольные напитки;
- продукты с высоким содержанием жира (жирное мясо или рыба, жирное молоко, сыр, майонез);
- покупные полуфабрикаты;
- напитки: крепкий чёрный чай, кофе, какао;
- газированные напитки сладкие и пресные;
- запрещено употреблять продукты типа быстрое питание (фаст-фуд);
- фабричные соки из пакетов.
С осторожностью и дозировано употребляют:
- яйца кур и перепёлок;
- сливочное масло;
- картофель;
- кефир обезжиренный;
- макаронные изделия;
- мёд;
- варенье;
- зефир.
В перечень продуктов, рекомендованных к употреблению в период профилактики, относят:
- нежирное мясо, к примеру, мясо курицы, кролика;
- зелень (укроп, петрушка, лук, сельдерей);
- овощи (свёкла, чеснок, капуста);
- ягоды;
- тыквенные семена;
- семена подсолнуха;
- нежирные кисломолочные продукты;

- грибы;
- морепродукты нежирные;
- орехи;
- каши (овсяная, перловая, гречневая);
- отвары из трав, шиповника;
- некрепкий чай;
- некрепкий кофе;
- горох;
- чечевица.
При таком разнообразии компонентов не составляет труда составить правильный, питательный и вкусный набор блюд. Для перестройки на новый рацион организму не требуется много времени. Наоборот, возврат к старым пищевым привычкам окажется затруднителен.
Для закрепления эффекта диеты желательно постоянно поддерживать необходимый уровень физической активности.
Основы физических упражнений
Физические нагрузки в умеренных количествах благотворно влияют на жизнедеятельность организма. При регулярности занятий происходит выброс гормонов счастья (эндорфинов), что укрепляет моральное состояние женщины, необходимое для полноценной жизни. Вес тела остаётся в заданных пределах и не переходит в ожирение.
Помимо этого, спорт благоприятно сказывается на таких видах жизнедеятельности организма, как:
- улучшение работы иммунитета;
- нормализация сна;
- выносливость;
- снижение утомляемости;
- укрепление мышечного тонуса;
- укрепление скелета;
- укрепление стенок сердечной мышцы.
Главное при занятиях спортом соблюдать меру и не перенапрягать организм, так как спорт в избыточных количествах влечёт вред. В целях профилактики рака груди рекомендованы регулярные легкоатлетические упражнения для насыщения организма кислородом.
К числу видов спорта, рекомендованных для профилактики, относятся:
- бег трусцой;
- велосипедные прогулки;
- плавание;
- йога;
- фитнес.
Перед применением диеты и физических упражнений желательно проконсультироваться с врачом для достижения результата.
Выдержки из статьи
Нелюбина Л.А., к.м.н.; Лактионов К.П., профессор
ФГБУ "Российский онкологический научный центр им. Н.Н.Блохина" РАМН
"Вестник РОНЦ им. Н. Н. Блохина РАМН, т. 24, №2, 2013
Заболеваемость
Рак молочной железы (РМЖ) стоит на первом месте по распространенности у женщин во всем мире, включая Российскую Федерацию, и служит основной причиной смерти женщин от онкологической патологии. В 2008 г. в мире диагностировано 1,38 млн новых случаев заболевания по сравнению с 500 тыс. в 1975 г., что составило 23% всех случаев злокачественных новообразований и 16% смертельных исходов у женщин [Jemal A. et al., 2011]. К 2030 г. число заболевших РМЖ предположительно составит 2,1 млн человек [http://glo-bocan.iarc.fr].
Самая высокая заболеваемость – 75–110 случаев на 100 тыс. женщин – наблюдается в странах с высоким уровнем социально-экономического развития – в Северной Америке, Австралии и Западной Европе; в большинстве стран Африки и Азии заболеваемость самая низкая – менее 20 на 100 тыс. женщин [http://glo-bocan.iarc.fr] . Государства Северной и Восточной Европы, включая Россию, где, по данным на 2009 г., число новых случаев составило 45,5 на 100 тыс. женщин, занимают промежуточное положение [Давыдов М.И., Аксель Е.М., 2011].
Обследование мигрантов из регионов с низкой заболеваемостью показало, что заболеваемость среди них достигает уровня страны местонахождения в течение одного-двух поколений, что свидетельствует о значительном влиянии окружающей среды и образа жизни [McPherson K. et al., 2000].
В последние 15–20 лет в ряде экономически развитых стран наряду с высокой заболеваемостью РМЖ наблюдается сокращение смертности от него вследствие распространения инновационных медицинских технологий диагностики и адъювантной терапии опухоли [Coleman M.P. et al., 2008]. Так, по данным ВОЗ, в странах Евросоюза с 1995 г. смертность от РМЖ снизилась на 21% [http://glo-bocan.iarc.fr]. В России, начиная с 2003 г., можно наблюдать относительную стабилизацию смертности, ранее быстро нараставшей.
Заболеваемость и смертность повышаются с возрастом: до 75% всех случаев РМЖ приходится на период постменопаузы [Pegram M.D. et al., 2012]. У женщин моложе 35 лет заболеваемость низкая – менее 5% всех случаев.
У мужчин также возможно развитие РМЖ, хотя наблюдается это крайне редко. Поэтому РМЖ можно назвать женской опухолью.
Причины РМЖ
Помимо возраста и пола выделен ряд факторов, которые ассоциируются с повышением риска РМЖ, в их числе наследственная предрасположенность, РМЖ в семейном и индивидуальном анамнезе, эндокринные влияния, перенесенные пролиферативные заболевания и облучение молочных желез (МЖ), повышенная плотность ткани МЖ, а также отдельные факторы образа жизни.
Существует общепринятое мнение о том, что рак – генетическое заболевание, возникающее в результате прогрессивного накопления в геноме соматических клеток молекулярных повреждений [Bell D.W., 2010; Wood L.D. et al., 2007] . По современным данным, развитие типичной опухоли определяют от 50 до 80 различных соматических мутаций [Wood L.D. et al., 2007]. Среди них одни возникают в результате нарушений репликации ДНК, другие – вследствие воздействия комплекса экзо- и эндогенных мутагенов. Мутационные изменения могут быть как наследственными, так и приобретенными – спорадическими.
Наследственная предрасположенность
Это один из самых значимых факторов риска (ФР). Выделяют два вида наследственного РМЖ: семейный и наследуемый.
Семейный РМЖ составляет 20–30% всех случаев, его связывают с комплексом генетических изменений в разнообразных низкопенетрантных генах [Lichtenstein P. et al., 2000].
Наследуемый рак составляет 5–10% всех случаев РМЖ и обусловлен наследуемыми мутациями определенных генов – BRCA1, BRCA2, ТР53, РТЕN или др. Для наследуемых форм характерны высокая вероятность рака, вертикальная передача от матери или отца и сочетание с опухолями других локализаций. Наследуемый РМЖ часто возникает в молодом возрасте и характеризуется аутосомно-доминантным типом наследования (т. е. возникает при наличии терминальных мутаций только в одной копии генов) [Lichtenstein P. et al., 2000; Turnbull C., Rahman N., 2008].
Риск семейного рака зависит от числа заболевших членов семьи, близости их родственной связи и их возраста в момент заболевания: чем моложе заболевший родственник, тем выше вероятность наследственной составляющей. Наличие в семье одной родственницы I степени родства (мать, родная сестра, дочь), болевшей РМЖ, увеличивает риск заболевания в 1,8 раза, 2 родственников – в 3 раза, 3 родственников или более – в 4 раза [Collaborative Group on Hormonal Factors in Breast Cancer, 2001].
Доминантные герминальные мутации генов супрессоров опухолевого роста BRCA1 и BRCA2 отвечают почти за 50% всех случаев наследуемого РМЖ [Foulkes W.D., 2008].
Нарушение функции этих генов приводит к нестабильности генома и повышенной вероятности злокачественной трансформации. В генах BRCA выявлено более 1000 герминальных мутаций.
Генетическое обследование позволяет выявить носительниц мутаций генов BRCA1 и BRCA2, у которых риск РМЖ в 10–30 раз превышает общепопуляционный и достигает 85%. При этом у мужчин – носителей мутаций генов ВRСА1и ВRСА2 повышен риск РМЖ, рака предстательной железы и ряда других опухолей.
Носители мутаций генов ВRСА в общей популяции встречаются очень редко – с частотой менее 1 %, и в большинстве случаев семейного рака их выявить не удается. При этом наличие у заболевших моложе 50 лет родственника, болевшего РМЖ в возрасте до 50 лет, увеличивает вероятность данных мутаций на 25%. Риск данных мутаций повышается при наличии рака яичников у кого-либо из родственниц I степени родства, двустороннего РМЖ или сочетания РМЖ и рака яичников.
Значительное повышение риска РМЖ (в 8–10 раз) отмечается при двух очень редких наследственных синдромах – Ли-Фраумени и Коудена, обусловленных герминальными мутациями в генах ТР53 и РТЕN соответственно. Синдромы характеризуются развитием множественных опухолей различных локализаций, в том числе РМЖ [Turnbull C., Rahman N. et al., 2008].
Эндокринные факторы
Эндогенные гормональные влияния. Результаты эпидемиологических и других исследований свидетельствуют о взаимосвязи между риском РМЖ и репродуктивным анамнезом женщин. Основные периоды роста и развития МЖ – пубертатный, беременность и лактация – проходят под влиянием стероидных гормонов яичников: эстрадиола и прогестерона, а также инсулина и факторов роста. Стимулируя пролиферацию клеток эпителия МЖ, стероидные гормоны повышают вероятность случайных генетических повреждений клеток в процессе их деления, выступая активаторами или промотерами опухолевого роста.
Репродуктивные факторы, которые увеличивают продолжительность действия и/или уровни стероидных гормонов яичников, повышают риск РМЖ. К таким факторам относятся длительный менструальный период с ранним началом менструаций (до 12 лет) и поздней менопаузой (после 55 лет) и отсутствие в анамнезе родов или поздние первые роды (после 30 лет) [Hulka B.S., Moorman P.G., 2001; Kelsey J.L., Gammon M.D. et al., 1993] . Риск РМЖ у родивших первого ребенка в возрасте 30–34 лет равен риску нерожавших, а у родивших первого ребенка после 35 лет риск выше, чем у нерожавших. У женщин с менопаузой, наступившей после 55 лет, риск РМЖ в 2 раза выше, чем у женщин с менопаузой до 44 лет. У женщин с высокими уровнями эндогенного эстрогена и тестостерона в период постменопаузы риск заболевания повышен в 2 раза по сравнению с женщинами, имеющими низкие уровни этих гормонов [Tamimi R.M., Byrne C. et al., 2007; Key T., Appleby P. et al., 2002].
При этом выполнение овариэктомии в возрасте до 35 лет значительно снижает риск РМЖ – более чем на 60%. Первые роды в раннем возрасте (до 28 лет), большое количество родов, позднее половое созревание и ранняя менопауза снижают риск и могут рассматриваться как защитные факторы [Kelsey J.L., Gammon M.D. et al., 1993; Lambe M., Hsieh C. et al., 1994]. У женщин, родивших первого ребенка до 20 лет, риск РМЖ почти в 2 раза ниже, чем у женщин, впервые родивших после 30 лет. Риск снижается соответственно числу родов. Так, при наличии 5 родов или более риск РМЖ в 2 раза ниже, чем у нерожавших.
Длительное грудное вскармливание (в течение года или более) также снижает риск РМЖ, причем тем сильнее, чем продолжительнее период лактации. Суммарный анализ данных 47 эпидемиологических исследований с включением 30 стран (более 50 000 наблюдений) позволил выявить статистически значимое уменьшение риска на 4,3% после каждых 12 мес грудного вскармливания [Collaborative Group on Hormonal Factors in Breast Cancer, 2002].
Беременность, как и лактация, уменьшает число менструальных циклов и, соответственно, кумулятивное воздействие эндогенных гормонов. Кроме того, беременность и лактация оказывают непосредственное влияние на клетки эпителия МЖ, способствуя их истинной дифференцировке (зрелости), которая достигается только с лактацией. Предполагают, что дифференцированные клетки более устойчивы к канцерогенезу по сравнению с недифференцированными [Russo J., Moral R. еt al., 2005; Britt K., Ashworth A. et al., 2007].
В ряде проспективных исследований не выявлено причинно-следственной связи между искусственным абортом и повышением риска РМЖ [Beral V., Bull D. et al., 2004; Committee on Gynecologic Practice, 2009].
Длительное использование комбинированных пероральных контрацептивов дает небольшое повышение риска РМЖ (относительный риск 1,24), который снижается через 5 лет после прекращения приема препаратов [Collaborative Group on Hormonal Factors in Breast Cancer. 1996; Marchbanks P.A., McDonald J.A. et al., 2002].
Длительное (на протяжении 5 лет или более) применение комбинированных препаратов, содержащих эстрогены и прогестагены, с целью заместительной гормональной терапии (ЗГТ) для смягчения симптомов возрастной утраты эстрогенной функции яичников повышает риск РМЖ и смерти от него, при этом более длительный прием препаратов ассоциируется с большим риском [Rossouw J.E., Anderson G.L. et al., 2002; Chlebowski R.T., Anderson G.L. et al., 2010; Beral V., Reeves G. Et al., 2011]. По данным ряда рандомизированных плацебо-контролируемых исследований, выполненных в рамках Women`s Health Initiative (1993—2003 гг.) с участием 161 809 женщин в возрасте 50–79 лет, установлено повышение заболеваемости инвазивным РМЖ на 24% среди женщин с интактной маткой, получавших комбинированные препараты ЗГТ на протяжении 7 лет [Rossouw J.E., Anderson G.L. et al., 2002]. У другой группы женщин, входивших в исследование: ранее перенесших гистерэктомию и поэтому получавших монотерапию эстрогенами (конъюгированный лошадиный эстроген), – повышения риска РМЖ не выявлено. Следует отметить, что у 41% женщин из этой группы наряду с гистерэктомией была выполнена двусторонняя овариэктомия.
В нескольких других исследованиях [Beral V., Reeves G. Et al., 2011; Calle E.E., Feigelson H.S et al., 2009] выявлено небольшое повышение риска РМЖ, связанное в том числе с монотерапией эстрогенами, особенно у женщин пониженного питания.
Публикация материалов исследования Women`s Health Initiative повлекла значительное ограничение применения ЗГТ в США в период с 2001 по 2003 гг., что привело к быстрому снижению заболеваемости РМЖ (на 7%).
Как было показано, что у женщин, начавших ЗГТ сразу после наступления менопаузы, риск РМЖ выше по сравнению с теми, кто начал прием препаратов позже [Beral V., Reeves G. еt al., 2011]. При этом риск быстро снижался в течение 5 лет после отмены препаратов [Chlebowski R.T., Anderson G.L. et al., 2010; Beral V., Reeves G. еt al., 2011; Calle E.E., Feigelson H.S et al., 2009].
Поскольку не ясно, в течение какого периода можно безопасно принимать препараты ЗГТ, рекомендуемая в настоящее время длительность приема составляет не более 1–2 лет.
Ожирение и возрастная прибавка массы тела
В эпидемиологических исследованиях получены статистически достоверные данные о сильной связи ожирения и возрастной прибавки массы тела в период менопаузы с риском РМЖ [Food, nutrition, physical activity, and the prevention of cancer: a global perspective. Washington, 2007] . По данным противоракового общества США, у женщин с увеличением массы тела после наступления менопаузы на 10 кг или более риск РМЖ почти на 20% больше, чем у тех, кто сохранил массу тела на прежнем уровне.
Эндогенный гормональный фон представляется доминирующим механизмом во взаимосвязи ожирения и риска РМЖ. В постменопаузе эстрогены образуются в первую очередь в жировой ткани. Таким образом, избыточное количество жировой ткани становится причиной гиперэстрогении и, соответственно, повышенного риска РМЖ.
У молодых женщин в пременопаузе избыточная масса тела не является ФР РМЖ. При этом установлено, что повышенная физическая активность снижает риск РМЖ. Защитный эффект в большей степени выражен в период постменопаузы [Food, nutrition, physical activity, and the prevention of cancer: a global perspective. Washington, 2007; Friedenreich C.M., Cust A.E. et al., 2008] . Снижение риска отмечено как при умеренных, так и при выраженных физических нагрузках. Механизм снижения риска предположительно связан с благоприятным влиянием на массу тела, гормональный фон и энергетический баланс [Neilson H.K., Friedenreich C.M. et al., 2009].
Употребление алкоголя
Положительная и статистически достоверная связь между употреблением алкоголя даже в небольших количествах (один прием ежедневно) и риском РМЖ подтверждена результатами целого ряда исследований [Hamajima N., HiroseK. Et al., 2002; Key J., Hodgson S. et al., 2006; Zhang S.M., Lee I.M. et al., 2007]. При этом риск зависит от дозы и сохраняется независимо от вида употребляемого алкоголя Причины заболевания раком молочной железы и возможности его профилактики. Как показывает метаанализ данных более 40 эпидемиологических исследований, у женщин, употребляющих 2 порции алкоголя 2 раза в день (24 г алкоголя), вероятность возникновения РМЖ повышается на 21% [Singletary K.W., Gapstur S.M., 2001]. У женщин, употребляющих от 2 до 5 порций алкоголя в день, риск РМЖ увеличивается до 50%.
В исследовании с участием 51 847 женщин в постменопаузе выявлено повышение частоты эстрогенположительного РМЖ при употреблении алкоголя. Наиболее вероятный механизм повышения риска в данном случае состоит в увеличении уровня эстрогенов и андрогенов [Singletary K.W., Gapstur S.M., 2001].
Пролиферативные заболевания МЖ
Непролиферативные заболевания МЖ, такие, как кисты, фиброаденомы, эктазия протоков, не ассоциируются с избыточным ростом ткани МЖ и не повышают риск РМЖ. Пролиферативные же заболевания МЖ, подтвержденные данными биопсии, повышают риск РМЖ. Пролиферативные заболевания без атипии – гиперплазия, склерозирующий аденоз, радиальный рубец, внутрипротоковая папиллома – характеризуются избыточным ростом ткани МЖ и повышают риск РМЖ в 1,5–2 раза [Hartmann L.C., Sellers T.A. et al., 2005; Wang J., Costantino J.P. et al., 2004]. Пролиферативные заболевания с атипией – атипическая протоковая и атипическая дольковая гиперплазии – характеризуются избыточным ростом атипичных клеток в протоках и дольках МЖ и значительно повышают риск РМЖ – в 4–5 раз. Дольковая карцинома in situ повышает риск инвазивного рака обеих МЖ в 8–10 раз [Hartmann L.C., Sellers T.A. et al., 2005; Ashbeck E.L., Rosenberg R.D. et al., 2007].
Как установлено, у женщин, перенесших РМЖ, повышен риск второй опухоли. Если лечение проводилось в возрасте моложе 40 лет, риск второй опухоли любой локализации выше в 3 раза, а риск рака второй МЖ – в 4,5 раза. У лечившихся по поводу РМЖ повышен риск рака яичников и рака эндометрия из-за сходных ФР – гормональных и генетических [American Cancer society. Cancer Facts & Figures 2011-2012].
Ионизирующие излучения
Облучение грудной клетки в возрасте от 10 до 30 лет, предпринятое с лечебной целью (например, при лимфоме Ходжкина), резко повышает риск РМЖ – до 35% в возрасте 40–50 лет [Preston D.L., Mattsson A. et al., 2002] . Самый высокий риск отмечается у лиц, получивших облучение в период полового созревания. В период роста и развития, когда еще не завершена дифференцировка терминальных протоков и долек МЖ, ее ткань особенно чувствительна к действию канцерогенов. РМЖ развивается латентно, через 8 лет или более после завершения терапии, в среднем – через 23 года [Russo J., Hu Y.F., 2000] .
Высокая плотность ткани МЖ
Плотность ткани МЖ – маммографический показатель соотношения железистой и жировой тканей, который в значительной степени отражает состояние эндогенного гормонального фона. Высокая плотность ткани МЖ служит независимым ФР РМЖ. Плотность паренхимы – индивидуальная особенность; при этом уменьшение плотности наблюдается с возрастом, после родов и в период менопаузы [Ursin G., Lillie E.O. et al., 2009]. Жировая ткань прозрачна и на маммограмме выглядит темной, а соединительная и железистая ткани – плотные, и на снимках они выглядят белыми. У женщин с длительно сохраняющейся высокой плотностью МЖ риск РМЖ в 4–6 раз выше, чем у женщин с менее плотной тканью [Ginsburg O.M., Martin L.J. et al., 2008; Boyd N.F., Guo H. et al., 2007; McCormack V.A., dos Santos Silva I., 2006].
Не доказано влияние курения на повышение риска РМЖ.
Изучается влияние на риск РМЖ таких факторов, как содержание жиров в продуктах питания, употребление большого количества овощей и фруктов, а также употребление других продуктов питания. Окончательные данные пока не получены [Michels K.B., Mohllajee A.P. et al., 2007].
В таблице суммированы ФР РМЖ с указанием степени относительного риска (ОР) [Singletary S.E., 2003].
Таблица. Факторы риска РМЖ
Читайте также:

