Новые патенты для рака
в этой теме будут выложены патенты, научные статьи по лечению разных видов рака с описанием методик.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУ
Изобретение относится к медицине, а именно к онкологии, и может быть использовано при противоопухолевой иммунотерапии больных раком легкого с множественным метастатическим поражением единственного легкого.
Известен "Способ лечения рака легкого" (см. Патент РФ № 2107494, опубликованный от 27.03.1998 г., бюл. № 9.) путем внутривенного введения лимфы, инкубированной с химиопрепаратами, отличающийся тем, что вместо аутолимфы используют донорскую лимфу, в ситуациях, когда больные лишены возможности забора собственной лимфы из-за метастазирования опухоли в лимфатические узлы средостения в зоне грудного лимфатического протока и его компрессии, а также анатомических особенностей шейного отдела грудного лимфатического протока, когда последний представлен в виде множественных мелких разветвлений, недоступных для дренирования.
Известен "Способ лечения местно-распространенного рака легкого" (см. Патент РФ № 2348420, опубликованный от 10.03.2009 г., бюл. № 7), отличающийся от аутолимфохимиотерапии тем, что больным после дренирования грудного лимфатического протока собранную лимфу инкубируют в течение 24 часов при температуре 37°С с 1 млн ME Ронколейкина (рекомбинантного интерлейкина-2), затем проводят сочетанное воздействие аутолимфоиммунотерапией и аутолимфохимиотерапией.
Данный способ позволяет стимулировать противоопухолевый клеточный иммунный ответ, способствуя цитотоксическому лизису опухолевых клеток клетками-эффекторами иммунной системы, не увеличивая частоты и тяжести побочных токсических реакций проводимого лечения.
Однако известный способ имеет ряд недостатков: 1) малоэффективен у больных с приобретенным иммунодефицитом вследствие ранее проведенной химио- или химиолучевой терапии; 2) малоэффективен у больных с генерализацией опухолевого процесса вследствие иммуносуппрессивного действия самой опухоли и ее множественных метастазов; 3) неосуществим у больных с блокированным грудным лимфатическим протоком после расширенных пневмонэктомий с медиастинальной лимфодиссекцией.
Целью изобретения является улучшение результатов противоопухолевого лекарственного лечения больных с множественным метастатическим поражением единственного легкого, перенесших ранее комбинированное или комплексное лечение рака легкого.
Поставленная цель достигается тем, что во время проведения аутогемохимиотерапии выполняют аллогенную трансплантацию-трансфузию лимфолейкоцитарной массы, полученной от одногруппного донора, после стимуляции донора нейпогеном (филграстим: гранулоцитарно-макрофагальный колоностимулирующий фактор) в дозе 2,5 мг/кг веса в течение 2-3 дней до достижения уровня лейкоцитов в периферческой крови 20-25×10/9/л, проводят 2 сеанса аппаратного лимфлейкоцитафереза. Полученные, в процессе лимфлейкоцитафереза, донорские клетки собирают в стерильные пластикатные контейнеры и разделяют на 2 равные порции. Первую порцию инкубируют с Ронколейкином (рИЛ-2) в дозе 500.000 ME, вторую порцию инкубируют с Лейкифероном (рИНФ-альфа) в дозе 300.000 ЕД при температуре 37°С в течение 3 часов и непосредственно после завершения инкубации вводят внутривенно капельно реципиенту-больному. Аналогичную трансфузию проводят через 24 часа, используя 2 порции донорской лимфолейкоцитарной массы, полученной в результате второго сеанса цитафереза.
Изобретение "Способ лечения рака легкого "является новым, так как оно неизвестно в онкологии при противоопухолевой лекарственной терапии больных с множественным метастатическим поражением единственного легкого.
Новизна изобретения заключается в том, что при проведении противоопухолевой иммунотерапии на лимфолейкоцитарной взвеси одногруппного донора после стимуляции лейкопоэза нейпогеном в дозе 2,5 мг/кг массы донора в течение 2-3 дней до достижения уровня лейкоцитов в периферической крови 20-25×109/л проводят сеанс лимфлейкоцитафереза на сепараторе крови МСS+"НЕМОNЕТIСS" объем крови = 4,5 объема циркулирующей крови в режиме протокола LDP. Полученные и собранные в стерильные пластиковые контейнеры донорские клетки в количестве 3
10 /л делят на четыре порции. 1-я порция, инкубированная с Ронколейкином в дозе 500.000 ME, 2-я порция, инкубированная с Лейкинфероном в дозе 300.000 ЕД в течение 3 часов при температуре 37°С, непосредственно после инкубации вводятся врутривенно капельно больному-реципиенту. Аналогичная процедура проводится через 24 часа с использованием 2 новых порций донорской клеточной массы, полученной в результате второго сеанса цитафереза.
Изобретение является промышленно применимым, так как может быть использовано в здравоохранении при противоопухолевой иммунной терапии больных раком легкого в различных медицинских учреждениях преимущественно онкологического профиля - в НИИ онкологии, онкологических диспансерах.
Больной Б., 1951 г.р., история болезни № С-10051/ч, поступил в торакальное отделение 24.07.2008 г. с диагнозом: Рак левого легкого центральная форма T3N2M0 3А стадия, состояние после комплексного лечения в 2007 г., множественное метастатическое поражение единственного правого легкого (гистологический анализ № 181178-84 - плоскоклеточная ороговевающая карцинома).
С 1.08 по 11.08.2008 г. проведено 2 аутогемохимиотрансфузии, суммарно введено: цисплатины - 200 мг, гемзара - 2000 мг 4.08 и 12.08.2008 г. от одногруппного донора на фоне стимуляции его лейкопоэза подкожным введением гранулоцитарно-макрофагального колониестимулирующего фактора роста (филграстим - 300 мкг) при лейкоцитозе периферической крови донора 18-20 10/л проведено 2 сеанса лейкоцитафереза 4,5 ОЦК с получением лимфолейкоцитарной взвеси в объеме 440 и 510 мл. Каждый объем полученной лимфолейкоцитарной взвеси разделен на 2 равные порции, одна из которых инкубирована с рекомбинантным интерлейкином-2 (ронколейкин - 500.000 ME), другая - с интерфероном-альфа (лейкинферон - 300.000 ЕД). После инкубации в течение 180 мин с иммунными препаратами проведены трансфузии аллогенной лимфолейкоцитарной взвеси реципиенту-больному.
Оценка результатов химиоиммунотерапии проведена через 2 недели. При контрольной компьютерной томографии органов грудной полости от 2.09.2008 г. отмечена положительная динамика в виде значительного уменьшения размеров ранее выявленных метастатических очагов с 12 до 8 мм, с 10 до 5 мм, снижения их интенсивности, новых очагов не выявлено. Далее с 10.09 по 16.09.2008 г. проведен второй курс химиоиммунотерапии по описанной выше методике. При контрольном компьютерном томографическом исследовании, выполненном через 21 день после окончания лечения, в правом легочном поле метастатические очаги не визуализируются, лимфатические узлы корня правого легкого и средостения не увеличены.
Продолжительность полной ремиссии до момента повторного обнаружения метастазов в паренхиме единственного правого легкого составила по результатам компьютерной томографии около 6 мес. Продолжена паллиативная химиотерапия, на фоне которой продолжительность жизни больного от момента завершения химиоиммунотерапии с трасплантацией аллогенных клеток к настоящему времени составила 19 мес. при стабилизации опухолевого процесса. Наблюдение за больным продолжено.
Способ лечения рака легкого, включающий противоопухолевую иммунотерапию, отличающийся тем, что больным с метастатическим поражением единственного легкого во время проведения аутогемохимиотерапии выполняют трансфузию аллогенной лимфолейкоцитарной массы, полученной от одногруппного донора; после стимуляции лейкопоэза донора нейпогеном в дозе 2,5 мкг/кг массы тела в течение 2-3 дней до достижения уровня лейкоцитов в периферической крови 20·109 /л проводят 2 сеанса лимфолейкоцитафереза 4,5 ОЦК, собирая взвесь в стерильные пластиковые контейнеры; полученную в результате сеанса цитафереза разделяют на 2 равные порции: 1-ю порцию инкубируют с ронколейкином в дозе 500.000 ME, 2-ю порцию инкубируют с лейкинфероном в дозе 300.000 ЕД при температуре 37°С в течение 180 мин и внутривенно капельно вводят больному-реципиенту; аналогичную процедуру проводят через 24 ч, используя аллогенную лимфолейкоцитарную массу, полученную в результате второго сеанса цитафереза
СПОСОБ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ
Имя заявителя:
Имя изобретателя: Козлов Сергей Васильевич (RU); Золотарёва Татьяна Геннадьевна (RU)
Имя патентообладателя: Государственное учреждение Самарский государственный медицинский университет (RU)
Адрес для переписки: 443099, г.Самара, ул. Чапаевская, 89, ГУ СамГМУ
Дата начала действия патента: 2004.02.24
Изобретение относится к медицине, в частности к онкологии, и может быть использовано при комплексном лечении рака молочной железы. Для этого вводят имунофан 0,05% - 1 мл 5 дней ежедневно тремя курсами: после лучевой терапии, после радикальной операции и между вторым и третьим циклами полихимиотерапии. Способ позволяет увеличить длительность периода иммунологической стимуляции с повышением иммунологических показателей до нормы и отсутствием метастазирования и рецидивов на период до 12 месяцев.
Изобретение относится к медицине, а именно к онкологии, и может быть использовано при комплексном лечении рака молочной железы для повышения иммунологической реактивности.
Известны способы лечения больных раком молочной железы путем введения в организм различных иммуномодуляторов, например интерферона [1], левамизола [2].
Однако известные способы создают нестойкое увеличение иммунологической реактивности, после которой наступает выраженный спад, сопровождающийся рецидивом заболевания или метастазированием опухоли.
Целью изобретения является удлинение периода стимуляции иммунологической реактивности у больных раком молочной железы.
Эта цель достигается тем, что после окончания лучевой терапии проводится первый курс введения 0,005% раствора имунофана по 1 мл, внутримышечно, ежедневно, в течение 5 дней. После радикальной операции назначается второй курс введения 0,005% раствора имунофана по 1 мл, ежедневно, внутримышечно, в течение 5 дней. Затем 0,005% раствор имунофана по 1 мл внутримышечно вводится в течение 5 дней между вторым и третьим циклами профилактической полихимиотерапии.
Сравнение заявляемого способа с другими, известными в области медицины способами лечения рака молочной железы, показало его соответствие критериям изобретения.
Способ реализуется следующим образом.
Больным с установленным диагнозом рака молочной железы местно-распространенной формы IIB-IIIB стадий проводится лучевое лечение, радикальная операция, 6 циклов профилактической полихимиотерапии, которые дополняются 3 курсами введения 0,005% раствора имунофана по 1 мл внутримышечно, ежедневно, в течение 5 дней. Первый курс введения имунофана осуществляется после лучевой терапии. Второй курс проводится после радикальной операции. Заключительный, третий курс назначается в перерыве между вторым и третьим циклами полихимиотерапии и проводится также в течение 5 дней путем внутримышечного введения 0,005% раствора имунофана по 1 мл, ежедневно.
Пример 1. Больная Р., 39 лет, поступила с диагнозом: рак правой молочной железы IIБ стадии. До начала противоопухолевого лечения больной было проведено иммунологическое обследование, в котором выявлено снижение относительного содержания Т-лимфоцитов с фенотипом CD3+ до 40,6%, абсолютного - 650 в 1 куб.мм, CD4+ - 18,6% и 300 в 1 мм3 крови соответственно (определение проводилось методом проточной цитометрии с использованием моноклональных антител по рекомендациям ВОЗ, Ройт А., 1991, Хаитов и соавт., 1995). Больной проводилось комплексное лечение (предоперационная лучевая терапия, радикальная операция, профилактическая химиотерапия). Учитывая резкое снижение содержания субпопуляций Т-лимфоцитов, больной назначен первый курс имунофана - 0,005% раствор по 1 мл в мышцу 1 раз в день в течение 5 дней после лучевой терапии. Второй курс иммуностимулирующего лечения был проведен после операции путем внутримышечного введения имунофана 0,005% раствора по 1 мл ежедневно в течение 5 дней. Проведенное контрольное исследование иммунологических показателей показало повышение уровня лимфоцитов CD3+ до 54%, абсол. - до 820 в 1 мм3, лимфоцитов CD4+ до 24%, абс. - до 490 в 1 мм3. Третий курс имунофана был проведен в перерыве между 2 и 3 циклами химиотерапии. Режим введения имунофана был аналогичен двум предыдущим. Через 6 месяцев от начала противоопухолевого лечения больной по данным контрольного исследования иммунологических показателей уровень лимфоцитов CD3+ составил 65%, абсолютное число клеток - 1200 в 1 мм 3, CD4+ - лимфоцитов составил 38% и 630 в 1 мм3 . Таким образом, в процессе противоопухолевого лечения, сопровождающегося иммуностимуляцией, отмечался постоянный рост иммунологических показателей, приближаясь к таковым у здоровых лиц. Общее состояние пациентки весь период лечения было удовлетворительное, данных за рецидив или метастазирование через 12 месяцев не выявлено.
Пример 2. Больная А., 46 лет, поступила с диагнозом: рак правой молочной железы IIIB стадии. До операции получила курс лучевого лечения, после чего проведено иммунологическое обследование, выявлено снижение относительного содержания Т-лимфоцитов с фенотипом CD3+ до 37%, абсолютного - 520 в 1 мм3, CD4+ - 22,6% и 290 в 1 мм3 крови. Выявленное снижение содержания субпопуляций Т-лимфоцитов послужило основанием для проведения первого курса лечения имунофаном - 0,005% раствором по 1 мл в мышцу 1 раз в день в течение 5 дней после лучевой терапии. Второй курс иммуностимулирующего лечения был проведен после радикальной операции путем внутримышечного введения имунофана 0,005% раствора по 1 мл ежедневно в течение 5 дней. Проведенное контрольное исследование иммунологических показателей показало повышение уровня лимфоцитов CD3+ до 59%, абсол. - до 800 в 1 мм3, лимфоцитов CD4+ до 26%, абс. - до 430 в 1 мм3. Третий курс имунофана был проведен в перерыве между 2 и 3 циклами химиотерапии. Режим введения имунофана был аналогичен двум предыдущим. По окончании противоопухолевого лечения в результатах иммунологического обследования пациентки выявлено повышение уровня лимфоцитов CD3+ до 68%, абсолютное число клеток - 1700 в 1 мм3, CD4+ -лимфоцитов - до 38% и 590 в 1 мм3 соответственно, что соответствует нормальным физиологическим значениям. Таким образом, в процессе противоопухолевого лечения, в сочетании с иммуностимуляцией, отмечалось повышение иммунологических показателей до нормы. По окончании лечения и через 12 месяцев пациентка осмотрена, данных за рецидив или метастазирование не выявлено, состояние удовлетворительное.
Положительный эффект от использования предлагаемого способа выражается в повышении процентного и абсолютного числа лимфоцитов, Т-лимфоцитов и их субпопуляций в периферической крови, приближаясь к уровню здоровых лиц в течение всего периода противоопухолевого лечения, дозы и режим введения имунофана не вызывают побочных и токсических реакций, эффект сохраняется до 12 месяцев.
Изобретение целесообразно использовать в медицине, а именно в онкологии, при лучевой терапии, после радикальной операции и в процессе профилактической полихимиотерапии у больных раком молочной железы для повышения иммунологической реактивности с целью повышения длительности безрецидивного периода и появления метастазов.
1. Российский онкологический журнал, 1996, № 3, с.60-64.
2. Иммунотерапия при злокачественных новообразованиях. Москва, Медицина, 1999, с.136.
Способ лечения молочной железы путем лучевой терапии, радикальной операции и профилактической полихимиотерапии, отличающийся тем, что после лучевой терапии проводят первый курс введения 0,05%-ного раствора имунофана в течение 5 дней по 1 мл ежедневно, после радикальной операции проводят второй курс введения 0,05%-ного раствора имунофана в течение 5 дней по 1 мл, ежедневно в течение 5 дней, затем проводят профилактические циклы полихимиотерапии, после чего проводят заключительный третий курс введения 0,05%-ного раствора имунофана 1 раз в день в течение 5 дней между вторым и третьим циклами полихимиотерапии.
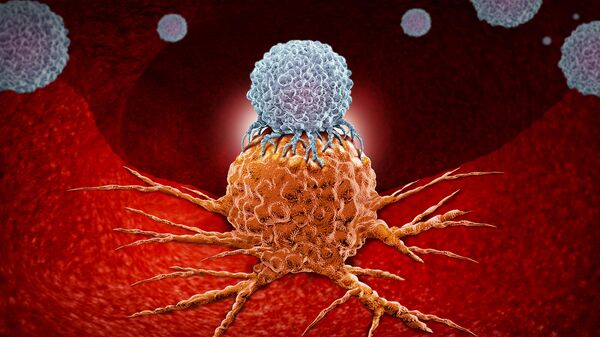

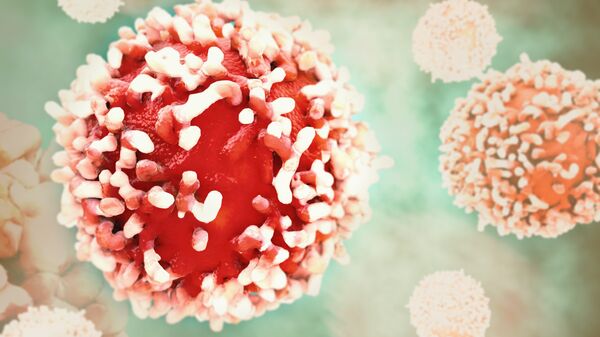
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
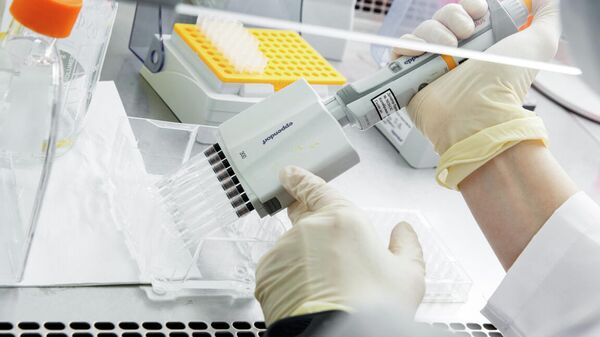
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
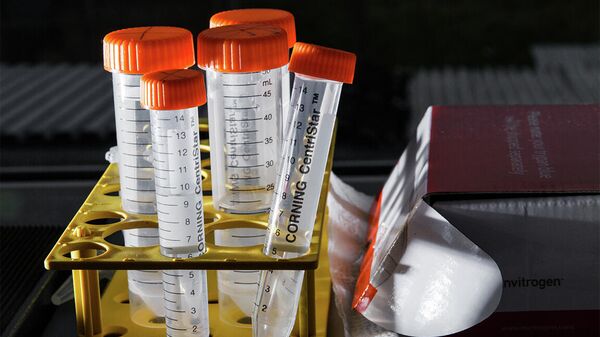
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела

С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела
Из бактерий выделяют генетический материал и расшифровывают
Из бактерий выделяют генетический материал и расшифровывают
Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека

Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела
Из бактерий выделяют генетический материал и расшифровывают
Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека
За последние десятилетия наука серьезно продвинулась вперед в лечении рака. И хотя полная победа над этим заболеванием еще довольно далека, у врачей с каждым годом становится все больше эффективных инструментов для борьбы с опухолями.
Один из них – активизация собственного иммунитета человека против раковых клеток. Именно в иммуноонкологии сегодня проводится максимальное количество исследований и разрабатывается наибольшее число противоопухолевых препаратов.
В чем плюсы и методы механизма, за открытие которого была присвоена Нобелевская премия, беседуем с заведующей дневным стационаром №3 Алтайского краевого онкологического диспансера, кандидатом медицинских наук Еленой Россохой.

Заведующая дневным стационаром №3 Алтайского краевого онкологического диспансера, кандидат медицинских наук Елена Россоха. Фото: Юлия КОРЧАГИНА
- Елена Ивановна, расскажите, как в норме действует иммунный ответ на возникновение злокачественных клеток?
- Иммунитет – это уникальная способность организма защищать себя от губительного воздействия внешних и внутренних потенциально опасных факторов, каковыми являются, в том числе, и раковые клетки.
Давайте разберемся, что такое рак? В норме все клетки организма проходят строго определенные стадии развития, выполняют заданные функции, размножаются по установленным правилам, а со временем стареют и умирают. Эта запрограммированная обязательная смерть нормальных клеток называется апоптоз. Но иногда у обычной клетки в силу ряда причин происходит сбой в программе деления – она приобретает способность делиться очень быстро и бесконечное количество раз, становится потенциально бессмертной - злокачественной.
Опухолевые клетки ежедневно появляются в организме любого человека и отличаются от здоровых наличием аномального белка - ракового антигена. Но в норме иммунитет вовремя распознает угрозу и уничтожает чужеродные элементы с помощью Т-лимфоцитов и других компонентов.
Кстати
Доказано, что если иммунитет подавлен ( ВИЧ , терапия иммуносупрессорами после пересадки органов), то риск развития онкологических заболеваний высок. И наоборот, раковые опухоли могут проходить сами собой без какого-либо специального лечения. Это явление получило название синдрома Перегрина по имени молодого священника, жившего в Италии в конце XIII века. У него была саркома (костная опухоль), требующая ампутации ноги. Хирургия тех времен не могла ему помочь, и юноше оставалось только уповать на Бога. Спустя некоторое время опухоль чудесным образом исчезла, а Святой Перегрин прожил долгую жизнь и умер в возрасте 80 лет без признаков рецидива.
- Почему же в какой-то момент иммунитет ослабляет свою защиту?
-В настоящее время механизмы взаимодействия опухолей и иммунной системы активно изучаются.

В иммуноонкологии сегодня проводится максимальное количество исследований и разрабатывается наибольшее число противоопухолевых препаратов. Фото: Юлия КОРЧАГИНА
Кстати
За открытие иммунных контрольных точек PD-1 и CTLA-4, американцу Джеймсу Эллисону и японцу Тасуко Хондзё в 2018 году была вручена Нобелевская премия. Это открытие позволило совершить прорыв в лечении некоторых ранее смертельных опухолей.
- В чем отличие иммунотерапии от других видов лекарственного противоопухолевого лечения?
- Можно сказать, что открытие принципов иммунотерапии изменило саму парадигму противоопухолевой терапии. Раньше в ее основе лежало воздействие на опухолевую клетку. Сейчас в центре внимания онкологов находится иммунная система человека, возможности ее перепрограммирования и восстановления способности самостоятельно противостоять злокачественным опухолям.
- Какие виды опухолей можно лечить с помощью иммунотерапии, и какова эффективность такого лечения?
- В первую очередь, это распространенные метастатические процессы, 3 и 4 стадии рака, когда удалить злокачественное новообразование с помощью операции невозможно. Что касается видов опухолей, то иммунотерапию можно применить практически ко всем из них. Рак легкого, мочеполовой системы у мужчин и женщин, молочной железы, различные виды лимфом, опухоли головы и шеи, меланома.
Кстати, впервые подобные препараты начали использовать именно при меланоме. Это очень агрессивные опухоли, характеризующиеся быстрым ростом и метастазированием. Еще несколько лет назад такие пациенты, даже получая специальное противоопухолевое лечение, жили максимум шесть месяцев. Сейчас благодаря иммунотерапии, медиана выживаемости для них выросла до нескольких лет.
В лечении злокачественной меланомы достигнут самый высокий прогресс. Пожалуй, самый известный онкобольной, излечившийся благодаря иммунотерапии, бывший презедент США Джимми Картер. В возрасте 90 лет он сообщил об успешно перенесенной операции по удалению опухоли печени. Однако вскоре стало известно, что это - метастаз меланомы, тогда же были выявлены и метастазы в головной мозг. Немедленно начатая иммунотерапия дала результаты - уже через год лечения сообщалось, что у экс- президента не обнаружено никаких следов онкологических образований.
Вообще, в последние годы темпы появления новых лекарств для борьбы с опухолями, ускорились в геометрической прогрессии. Сейчас любая уважающая себя фармацевтическая компания одновременно разрабатывает десятки молекул. Не факт, что из каждой из них на выходе появится новый противоопухолевый препарат, но, тем не менее, благодаря такой высокой заинтересованности производителей, в мире регулярно появляются новые эффективные лекарства.
- Если механизм иммунотерапии так эффективен, прост и органичен замыслу самой природы, почему одним пациентам назначают такие препараты, а другим, с таким же диагнозом, - нет?
- Рак настолько сложное заболевание, что вряд ли когда-нибудь будет придумано универсальное лекарство от этой болезни. Поэтому и иммунотерапия – это не панацея, а всего лишь еще одна очень хорошая лекарственная опция.
Почему мы не назначаем одинаковые препараты пациентам с одинаковыми диагнозами - а что вы считаете одинаковым диагнозом? Это раньше мы лечили рак легкого, рак груди, рак почки и так далее. Сейчас пациента с таким определением статуса болезни ни один врач не сможет лечить эффективно.

Иногда у обычной клетки в силу ряда причин происходит сбой в программе деления – она приобретает способность делиться очень быстро и бесконечное количество раз, становится потенциально бессмертной - злокачественной. Фото: Юлия КОРЧАГИНА
Ученые давно доказали, что не существует абсолютно одинаковых раков. Поэтому мы сейчас лечим не опухоли, а их особенности - наличие определенных биомаркеров. В иммунотерапии это уровень экспрессии рецептора PD-L1 на опухолевых клетках. И чем этот уровень этот выше, тем более результативным будет лечение. Вот почему персонализация - тренд современной онкологии.
Онкологи уже научились применять иммунопрепараты не только в монорежиме, но и эффективно использовать их в сочетании с химиопрепаратами, таргетными и даже другими иммунными препаратами. Причем, комбинация двух или нескольких средств, как правило, имеет синергетический эффект, они многократно усиливают действие друг друга.
Полностью излечить метастатический процесс, к сожалению, нельзя. Наша задача, чтобы пациент жил долго и в хорошем качестве. И сегодня мы научились переводить рак в длительное хроническое течение, назначая последовательную терапию при прогрессировании заболевания.
- Может ли человек сам, не дожидаясь лечения в стационаре, купить иммунологический препарат и начать его использовать самостоятельно? Ведь многие из них выпускаются в форме таблеток – ничего сложного.
- Ни в коем случае! Любой иммунологический препарат должен приниматься под контролем врача, имеющего опыт работы с подобными средствами.
Иммунологические препараты при неграмотном применении могут вызывать тяжелые побочные явления. Например, у пациента появилась высокая температура, кашель одышка. Что это – аутоиммунная или обычная пневмония? Знать это крайне важно, ведь при схожем названии тактика лечения будет принципиально различной.
Токсичная реакция на иммунологический препарат может развиться как через несколько дней, так и через несколько лет после его применения, может пройти почти сразу, а может сохраняться годами. Понимание первопричин каждого из явлений крайне важно для его успешного лечения.
Конечно, такие тяжелые побочные эффекты развиваются редко, поэтому мы успешно лечим наших пациентов в условиях дневного стационара, однако быть готовыми к ним просто необходимо. Тем более не понятно, зачем так рисковать собственным здоровьем, ведь все препараты есть в наличии в диспансере, и пациенты получают их абсолютно бесплатно. А это отнюдь немалые деньги – одно введение такого препарата может стоить 500 тысяч рублей, а общий курс составляет до 18 процедур.
- Почему так дорого?
- Разработка нового иммунологического препарата стоит порядка миллиарда долларов. Это многоуровневый процесс, в ходе которого сначала изучаются общие и специфические свойства препарата, потом его тестируют на животных, затем на добровольцах, следующим этапом изучают степень его токсичности, и так далее.
На входе может стартовать десять потенциальных лекарств, а лет эдак через двадцать к финишу придет лишь один препарат. И только семь лет после разработки формула защищается патентом, по истечении этого срока буквально на следующий день заранее скопированный препарат начинает продаваться гораздо дешевле. Вот производители и успевают отбить затраты и заработать на своем изобретении.
- Можно ли профилактически укрепить иммунитет конкретно против онкологии?
- К сожалению, это невозможно. Иммунитету все равно, против кого бороться, для него и раковая клетка и вирус гриппа – одинаково опасны. Он либо работает, либо нет. Чтобы увереннее противостоять, в том числе развитию злокачественных патологий, нужно укреплять свой иммунный ответ в целом. Рекомендации тут стандартные: здоровый образ жизни, отказ от вредных привычек, правильное питание, постоянный контроль за хроническими болезнями высокого онкориска. Кроме этого существуют и специфические меры профилактики, например, вакцинация против рака шейки матки.
Ну а если есть выраженные проблемы с иммунитетом – частые простуды, головные боли, усталость, упадок сил, сонливость, раздражительность – то лучше обратиться к врачу.
- Ваше мнение: действительно ли иммунотерапия – это прорыв в онкологии, как об этом сейчас говорят?
- Это несомненный прорыв. Появление современных иммунных препаратов коренным образом изменило подход к терапии злокачественных опухолей. У этой категории лекарств есть важная особенность: однажды получив полный ответ на иммунотерапию, мы сохраняем его на годы. У цитостатиков и таргетных препаратов такого нет, там этот эффект длится в среднем от полугода до года. То, что новые препараты дают возможность превратить ра нее считавшееся смертельным заболевание в контролируемую хроническую болезнь или полностью от нее излечиться, вселяет надежду в миллионы больных.
Да, мы пока не можем вылечить всех. Но можем выделить иммунозависимую популяцию и полечить ее. Например, для рака легкого это около 25% всех пациентов. Это уже немало!
Бывает, что опухоли уходят полностью, как в случае со Святым Перегрином, однако следует признать, что это случается крайне редко. Чаще – они значительно уменьшаются в размерах или полностью регрессируют и такое состояние при назначении иммунотерапии может длиться очень долго. Сейчас все эти эффекты изучаются более активно, и я уверена, что ученых ждет еще масса революционных открытий.
Читайте также:

