Молекулярный рак что это такое
Идентификация молекулярных механизмов, принимающих участие в возникновении новообразований, позволила изменить характер подходов к поиску новых лечебных средств: если раньше в этой области превалировал эмпирический компонент, то за последние годы попытки терапевтической модификации биологически важных мишеней стали принимать целенаправленный, патогенетически обоснованный характер.
Под онкологической химиопрофилактикой понимается длительный прием нетоксичного лекарственного препарата, который существенно снижает риск возникновения злокачественной патологии (по стилю своего применения онкохимиопрофилактические средства похожи на фармацевтические формы витаминов).
К настоящему моменту уже подведены первые итоги клинических испытаний антагониста эстрогенов - тамоксифена; показано, что регулярное употребление последнего существенно снижает риск возникновения рака молочной железы.
Недостатком тамоксифена является эпизодическое появление побочных эффектов. Сейчас проходят испытания более специфического антиэстрогенового препарата - ралоксифена. Предполагается, что применение ралоксифена не будет сопровождаться отрицательными последствиями. В отношении профилактики рака легкого большие надежды связываются с применением антагонистов ретиноидных рецепторов. Интересными представляются эксперименты на животных, в которых удалось предотвратить возникновении опухолей толстой кишки посредством назначения ингибиторов циклооксигеназы.
Если до 1990-х гг. поиск антираковых химиопрепаратов базировался на феноменологических критериях - например, подбирались вещества, преимущественно поражающие быстроделящиеся клетки, то за прошедшее десятилетие появился принципиально новый алгоритм разработки терапевтических средств. В качестве мишени выбирается не свойство раковой клетки (по понятным причинам оно не может обладать высокой специфичностью), а биологическая молекула (чаще всего фермент), лежащая в основе злокачественной трансформации.
Особый интерес вызывают попытки индивидуализации терапии опухолей, основанные на уточнении ее молекулярно-генетических особенностей. Например, хорошие шансы на внедрение имеет тест на микросателлитную нестабильность, который может свидетельствовать не только о наследственном характере заболевания, но и о хорошей чувствительности новообразования к препаратам группы фторпиримидинов (5-фторурацил, кселода и т. д.). Молекулярно-генетические методы в онкологии всегда используются в комплексе (рис. 19).

Рис. 19. Протоколы молекулярно-генетической диагностики в нейроонкологии
Интерес вызывают также подходы, направленные на выявление индивидуальной картины метаболизма химиотерапевтических препаратов. В частности, многие опухоли характеризуются гиперэкспрессией фермента тимидинфосфорилазы. Именно в этих случаях представляется оправданным назначение кселоды - нетоксичного предшесгвенника 5-фторурацила. Данное направление медицины пока еще находится на начальных этапах своего развития, однако есть все основания полагать, что молекулярные подходы к индивидуализации противоопухолевой терапии получат дальнейшее развитие в самое ближайшее время.
В настоящее время предпринимаются интенсивные попытки, направленные на выявление предиктивных маркеров противоопухолевой терапии.
Исследования подобного рода ставят две задачи:
1) молекулярно-генетическая характеристика пациента, позволяющая индивидуализировать дозировку препаратов и уменьшить риск появления токсических реакций;
2) мутационный и экспрессионный анализ опухолевой ткани с целью предсказания чувствительности новообразования к лекарственным средствам (рис. 20).

Рис. 20. Молекулярные маркеры ответа на противоопухолевую терапию
Результат лечения онкологического заболевания зависит от так называемого терапевтического индекса, т. е. от разницы между ингибирующим воздействием препарата на трансформированные и нормальные клетки. Как противоопухолевые, так и побочные эффекты зависят от активной концентрации препарата в средах организма, что, в свою очередь, определяется индивидуальным набором полиморфных вариантов гена.
Чувствительность опухоли к лекарственному средству определяется приобретенными молекулярными событиями (мутациями, изменениями экспрессии генов), которые отражаются на внутри-опухолевой концентрации препарата, присутствии и доступности соответствующих биохимических мишеней и т. д.
Таблица 7. Молекулярные маркеры эффективности и токсичности противоопухолевой терапии

В табл. 7 обобщены сведения о молекулярных предикторах эффективности и токсичности препаратов, используемых при противоопухолевой терапии.
Несколько полиморфных вариантов генов, ассоциированных с повышенной чувствительностью к цитостатикам, уже идентифицированы. В частности, носители мутантных аллелей гена TPMT плохо метаболизируют меркаптопурин и нуждаются в 10-15-кратном уменьшении дозировки этого препарата. Существенно, что мутации в гене TPMT консервативны, поэтому для определения функционального состояния соответствующего фермента достаточно провести всего три анализа полимеразной цепной реакции (ПЦР).
Некоторые варианты гена UGT1A1 ассоциированы с повышенной чувствительностью к иринотекану. Лабораторный тест, направленный на выявление подобных индивидов и влекущий за собой необходимость снижения стартовой дозировки препарата на 20-25%, прошел регистрацию FDA. Вероятно, применение метотрексата также требует пересмотра ряда количественных аспектов, в зависимости от полиморфизма гена MTHFR. Носительство мутантных аллелей гена DPD сопряжено с риском летальных реакций в ответ на введение 5-фторурацила.
Тимидинфосформилаза (ТР) является фактором ангиогенеза, поэтому повышенная экспрессия соответствующего гена ассоциирована с плохим прогнозом. Однако ТР обладает способностью активировать предшественник 5-фторурацила капецитабин, поэтому опухолеспецифическое увеличение активности фермента может способствовать локальному увеличению концентрации цитостатика.
Повышенная экспрессия генов ферментов репарации ДНК позволяет опухоли нейтрализовать воздействие терапевтических средств. Подобный эффект подтвержден для препаратов платины и алкилирующих агентов. Положительный результат при назначении антрациклинов более вероятен, когда в опухоли активирована мишень препаратов этой группы - топоизомераза II-a. Высокая продукция одной из молекул тубулинов, а именно Р-тубулина класса III, может снизить лечебный эффект таксанов и винкаалкалоидов.
Определение состояния рецепторов гормонов и гена HER2 для подбора таргетной терапии рака молочной железы (РМЖ) уже стало классическим примером молекулярной индивидуализации терапии. Назначение ритуксимаба (Мабтеры) и иматиниба (Гливека) также производят исключительно на основании результатов молекулярного теста.
Хорошей воспроизводимостью отличаются работы, выявляющие высокую чувствительность к цетуксимабу (Эрбитуксу) опухолей толстой кишки, содержащих повышенную копийность гена EGFR. Напротив, присутствие мутаций в онкогене KRAS свидетельствует о бесперспективности применения антагонистов EGFR.
Выявление единичных опухолевых клеток посредством молекулярно-биологических методов
Выявление единичных опухолевых клеток в различных тканях и средах организма представляет клинический интерес по целому ряду причин. Во-первых, подобные технологии могут быть направлены на определение риска метастазирования первичной опухоли и, следовательно, на уточнение целесообразности и интенсивности адъювантного лечения.
Во-вторых, выявление диссеминированных злокачественных клеток может оказаться пригодным для мониторинга эффективности послеоперационной терапии, а также для прогнозирования рецидива. И, наконец, в-третьих, на молекулярные методы возлагаются огромные надежды в плане ранней диагностики новообразований.
Объекты исследования, как правило, варьируются в зависимости от локализации опухоли и путей ее метастазирования. Для новообразований в тех органах, которые граничат с окружающей средой, источником биологического материала обычно выступают выделяемые жидкости и среды организма.
Так, разработка методов ранней диагностики рака легкого подразумевает анализ мокроты, толстой кишки - фекалий, мочевыводящих путей - мочи. Исследования опухолей молочной железы обычно включают ткани региональных лимфатических узлов, кровь и костный мозг. При изучении ранних этапов метастазирования новообразований желудочно-кишечного тракта целесообразно анализировать биопсии печени.
Адекватный выбор биологического материала для исследований в значительной мере осложняется разнообразием биологического поведения опухолей. Например, карциномы молочной железы могут метастазировать как лимфогенным, так и гематогенным путем, причем эти альтернативные пути распространения опухолевых клеток зачастую реализуются вне зависимости друг от друга.
Другая критическая проблема - правильный выбор метода молекулярной детекции опухолевых клеток. Наиболее традиционным является применение иммуноцитохимии. К ее достоинствам следует отнести возможность визуальной оценки строения окрашенных клеток, а также пригодность для внедрения в любой морфологической лаборатории. Главный недостаток данного метода - его достаточно высокая трудоемкость.
Для неинвазивной детекции минорных фракций ДНК можно использовать ряд методов в комбинациях и модификациях:
1. Обогащающие:
• фракционирование при выделении; обогащающая гибридизация;
• AS-PCR (аллель-специфичная ПЦР) и Proof-reading PCR;
• Wild-Type Blocking PCR;
• LM-PCR;
• COLD-PCR;
• рестрикционные методы.
2. Высокочувствительные:
• выделение с помощью сорбентов, задерживающих фракции всех размеров;
• ПЦР-амплификация фрагментов минимальной длины (
План лечения составляют с учётом стадии опухолевого процесса, морфологической структуры опухоли, возраста больной, сопутствующих заболеваний, общего состояния пациентки. Применяют следующие методы лечения: хирургический, комбинированный (сочетание операции с лучевой или лекарственной терапией) и ком.
По данным многочисленных публикаций, этиология и патогенез РМЖ сложны и определяются сочетанием многих факторов. Гормональная регуляция функции молочных желез значительно сложнее, чем эндометрия. Помимо эстрогенов и прогесторона, развитие молочных желез в пубертатном периоде, их функция во время бер.
Гистологическую градацию рака молочной железы впервые ввел R.B. Greenough из Бостона, который в 1925 г. опубликовал анализ 73 случаев рака молочной железы. Несмотря на то что прошло много времени и опубликовано большое количество работ о применении гистологической градации рака молочной железы, ниче.
При анализе данных, получаемых с помощью ультразвукового исследования, целесообразно выделить ряд диагностических задач, решение которых позволит получить полный комплекс эхографических признаков рака молочной железы и метастатических лимфатических узлов, по которым в дальнейшем будет производиться .
Патологические процессы в молочной железе отличаются многообразными клиническими проявлениями, что норой создает серьезные дифференциально-диагностические трудности. Для гипеколога важнее всего заметить (не пропустить!) патологию молочных желез, что приведет в движение систему методов уточня.
Доброкачественные изменения молочных желез относятся к наиболее распространенным заболеваниям и включают различные по клиническим, морфологическим и этиологическим признакам процессы. Отличительной особенностью молочной железы является сложность четкой дифференцировки физиологических и патологически.
Рак молочной железы развивается из эпителия млечных протоков и альвеол. Патоморофологическая характеристика рака молочной железы включает такие параметры, как размер первичного очага, его локализацию в молочной железе, тип роста, морфологическое строение, степень дифференцировки, наличие регионарных.
Молекулярные процессы в опухоли
Каждая здоровая клетка содержит молекулу ДНК, из которой она считывает информацию, какую форму и специальность получить, какие белки и ферменты производить, а главное, когда делиться и умирать. Подробнее о том, как это происходит почитайте в нашем первом материале .
Мутации в протоонкогенах и генах-супрессорах, отвечающие за деление и смерть клетки, приводят к тому, что клетка перестает следовать инструкции и синтезирует белки и ферменты неправильно. Молекулярные процессы выходят из-под контроля: клетка постоянно делится, отказывается умирать и копит генетические и эпигенетические мутации. Поэтому злокачественные новообразования часто называют болезнью генома.
Драйверные мутации создают различные популяции клеток, что обеспечивает разнообразие опухоли. Эти популяции или клоны по-разному реагируют на лечение: некоторые из них устойчивы и приводят к рецидиву. К тому же разная чувствительность клонов к терапии может привести к радикальному изменению молекулярного профиля в ходе лечения: даже незначительные в начале популяции клетки могут получить преимущество и стать доминирующими в конце лечения, что приведет к устойчивости и развитию опухоли.

Источник: Cell .
Иллюстрации: Майкл Ковальски .
Молекулярная диагностика
Драйверные мутации, изменения в количестве или структуре белков используют в качестве биомаркеров — мишеней, по которым подбирают лечение. Чем больше мишеней известно, тем более точным может быть выбор из потенциально эффективных схем лечения.
Отделить драйверные мутации от остальных и определить молекулярный профиль опухоли непросто. Для этого применяется технология секвенирования, флуоресцентной гибридизации in situ (FISH), микросателлитного анализа и иммуногистохимии.
Методы секвенирования нового поколения позволяют выявить драйверные мутации, включая те, что делают опухоль чувствительной к таргетной терапии.
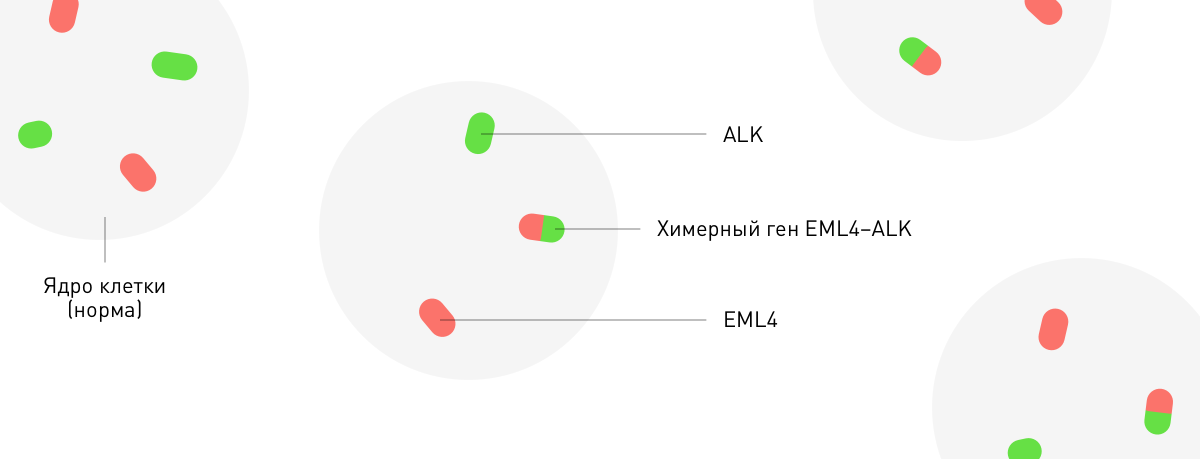
Флуоресцентная гибридизация in situ (FISH).
Микросателлитный анализ показывает степень нарушения системы репарации ДНК, а иммуногистохимия — белковые биомаркеры, расположенные на поверхности, в цитоплазме и ядрах опухолевых клеток.
Специалисты Solo исследуют до 450 генов и биомаркеров, чтобы оценить, как опухоль может ответить на применение более таргетных препаратов для лечения онкологических заболеваний. Для некоторых из них анализ биомаркера продиктован производителем. Для других используют данные клинических исследований и рекомендации международных сообществ онкологов.
Помимо выбора мишеней для таргетной терапии, молекулярное профилирование помогает обнаружить мутации, которые напротив, делают опухоль устойчивой к определенному лечению, или генетические особенности, которые связаны с повышенной токсичностью и требуют индивидуального подбора дозы лекарства.
Для исследований используется материал биопсии или парафинизированные блоки послеоперационного материала.
Молекулярное профилирование дает дополнительную информацию о заболевании, но она не всегда применима для выбора лечения. Например, в ситуациях, когда стандартная терапия обладает достаточной эффективностью или показано хирургическое лечение. Можно определить клинические ситуации когда такое исследование может быть наиболее полезно:
- Редкий вид опухоли;
- Опухоли с неустановленным первичным очагом (неизвестно, где изначально появилась опухоль, давшая метастазы);
- Тех случаев, когда требуется выбор из нескольких вариантов применения таргетной терапии;
- Исчерпаны возможности стандартной терапиии требуется экспериментальное лечение или включение пациента в клинические исследования.
Специалисты проекта Solo консультируют онкологов или пациентов и подсказывают, нужен ли тест в данном случае.
Результат диагностики также включает рекомендации по клиническим исследованиям с подходящим тестируемым препаратом. У пациента есть возможность принять в них участие.
Прецизионная медицина и клинические исследования
Обычно в медицинской практике применяют общие стратегии для лечения пациентов с определенным диагнозом. Для мелкоклеточного рака легкого используется одна стратегия, для немелкоклеточного — другая. Для онкологических заболеваний этот метод подходит не всегда. Из-за различий на молекулярном уровне даже при одном и том же типе опухоли пациенты могут получить неэффективное или лишнее лечение.
С увеличением исследований и изобретением таргетных препаратов, подход к лечению онкологических заболеваний начал меняться. Чтобы увеличить безрецидивный период и продолжительность жизни пациента, нужно учитывать молекулярный профиль опухоли, ответ организма на лекарственные препараты и химиотерапию (фармакогеномика), знать главные биомаркеры.
Прецизионная медицина позволяет существенно улучшить прогноз конкретного пациента, избежать серьезных побочных эффектов онкологических препаратов и значительно повысить качество жизни больного. Но и у этого метода существуют недостатки.
Таргетных препаратов становится все больше, и они имеют два основных ограничения: большинство молекулярно-направленных агентов обеспечивают лишь частичное подавление сигнальных путей и многие из них слишком токсичны для использования в комбинации.
Представьте, что вы архитектор Москвы. Перед вами стоит непростая задача — решить проблему с пробками в час пик, построив один мост. Молекулярные механизмы можно сравнить с движением машин, а мост — главный препарат, который должен решить основную проблему. Кажется, что несколько лекарств (серия мостов), направленные на главные молекулярные нарушения, могут решить эту проблему. Но токсичность препаратов при этом увеличивается и может быть непредсказуемой.
Мы стали лучше понимать молекулярные процессы злокачественных опухолей, но текущие методы внедрения точной онкологии в клиническую практику сильно отстают. Чтобы ускорить изучение таргетной терапии, ученые разработали два новых подхода — Basket и Umbrella.

Суть метода Basket в том, что для исследования выбирают пациентов с определенным биомаркером, независимо от расположения и названия опухоли. В мае 2017 года FDA одобрила такой метод лечения для биомаркера под названием высокая микросаттелитная нестабильность (MSI-H) или дефект восстановления несоответствия (dMMR).
Молекулярные нарушения отличаются не только у разных пациентов, но и в пределах одной опухоли. Гетерогенность — большая проблема в онкологии, для решения которой был разработан дизайн исследования Umbrella. Для метода Umbrella пациентов сначала отбирают по типу злокачественных новообразований, а потом учитывают генетические мутации.
Такие исследования помогают не только собрать информацию о действии таргетных препаратов — иногда это единственная возможность для пациентов, которые не отвечают на стандартное лечение зарегистрированными препаратами.
Клинический пример
Мы решили привести наглядный пример, как может выглядеть использование расширенного молекулярного профилирования.
Пациент с меланомой кожи и метастазами в печени обратился к онкологу. Врач и пациент приняли решение сделать молекулярное профилирование, чтобы получить более полную информацию о заболевании. Пациенту провели биопсию и отправили образцы ткани на исследование. В результате диагностики в опухоли обнаружили несколько важных генетических нарушений:

Ориентируясь на результаты клинических исследований и рекомендации можно прийти к следующим выводам:
- Потенциально эффективными могут быть препараты класса BRAF-ингибиторов (Вемурафениб), более того, наличие мутации NRAS может служить дополнительным основанием для назначения двойной блокады сигнального каскада — комбинацией с MEK-ингибиторами (Траметиниб).
- Несмотря на то что нет одобренной терапии, направленной непосредственно на онкоген NRAS, известно, что мутации в нем повышают вероятность успешного лечения при назначении иммунотерапии (Ипилимумаб и Пембролизумаб).
- Наследственный генетический вариант в гене TPMT указывает на повышенную индивидуальную токсичность Цисплатина, что требует коррекции дозы при назначении платиносодержащих режимов терапии.
Таким образом, врач получает возможность ориентироваться среди возможных вариантов лечения отталкиваясь не только от клинических параметров пациента, но и учитывая молекулярные особенности опухоли.
Молекулярная диагностика — это не панацея для всех онкологических заболеваний. Но это важный инструмент для онколога, который позволяет подойти к лечению злокачественных опухолей с новой стороны.
Спасибо, что читали и комментировали наши материалы об онкологии. Вот полный список статей:
Последние научные разработки в области ядерной медицины предусматривают альтернативы дополнительного лечения, особенно для больных неоперабельным раком. Подобное лечение имеет свойство целенаправленного на раковую ткань лечения и позволяет продлить жизнь и повысить её качество.
Лечение отталкиваясь от свойства раковых клеток
Современный подход к лечению рака чаще всего оценивается под названием "целенаправленное лечение". Цель этого лечения это раковые клетки. Имеющие свойство анормального размножения, раковые клетки отличаются от здоровых клеток в связи с разными белками которые находятся на оболочки клетки или с некоторыми молекулами которые находятся внутри клетки. В последние годы, с помощью специальных молекул, которые способны определить характеристику или слабые стороны раковых клеток, разрабатываются новые целенаправленные (умные) методы лечения. Эти специальные молекулы, которые способны находить раковые образования, вводятся в организм через рот или через вену.
Молекулярные технологии нацелены на раковую ткань
Если имеется молекула которая имеет свойство целевого направления на раковую клетку, отталкиваясь от назначенного лечения возможно загрузить в молекулу лекарство, атом или другие уничтожающие агенты. С помощью лечебных агентов загруженных в молекулу-носителя возможно будет целенаправленно уничтожить зараженную ткань на клеточном уровне. Таким образом возможно будет использовать более высокие дозы с минимальным повреждением здоровых тканей.
Новые альтернативы лечения для неоперабельных больных
Молекулярное лечение является новым оружием в борьбе с раком. Подобное лечение даёт ещё один шанс неоперабельным пациентам или пациентам, которые испробовали все остальные методы лечения. Для болезней на более распространённых стадиях, подобное лечение используется в качестве последнего удара по раковым клеткам. Но по мере накопления опыта, в дальнейшем возможно будет использовать подобное лечение на более ранних стадиях заболевания.
Использование молекулы-носителя при сканирование
Сканирование раковых клеток распространенных по всему организму происходит на основании той же логики что и при лечении. Загруженные в молекулу-носителя специальные агенты, которые добываются отталкиваясь от свойства раковых клеток, направляются в область ракового распространения и таким образом позволяют определить распространение заболевания по всему организму. Если сравнивать с предыдущими методами сканирования, молекулярное сканирование позволяет добиться более успешных результатов в качестве анализирования распространения заболевания. С помощью одного и того же метода, возможно использовать агенты позволяющие определять распространение заболевания и одновременно лечить его. Подобные агенты называются тераностические агенты (латинское сочетание слова лечение и диагностика). Подобные агенты помимо лечения так же позволяют более эффективно определить распространение лекарственного препарата по организму и ход заболевания.
Метод эффективно используется при раке простаты (предстательной железы)
Новые молекулярные методы лечения и диагностики начали использоваться, и со временем будут чаще использоваться, при лечении и диагностики рака простаты. В крови имеется раковый показатель более известный как ПСА. После установления диагноза рака простаты, с помощью методов сканирования определяется стадия заболевания. Методы сканирование при раке простаты используют один и тот же путь что и молекулярные целенаправленные методы лечения. Используя белок ПСМА, который специфичен для рака простаты, был создан метод сканирования под названием ПЭТ-КТ. ПСМА ПЭТ-КТ позволяет определить наличие метастазов и таким образом предотвратить ненужные вмешательства и лечения больным с раком простаты. Помимо этого, пациентам с метастазирующим и невосприимчивыми к стандартному лечению заболеванием, возможно провести целенаправленное лечение с использованием высоко энергичного атома лютеций 177. При раке простаты помимо лютеция недавно начали использовать молекулярное лечение с радием 223. С радием 223, возможно нацеливаться на костные метастазы гормонально устойчивого рака простаты. Исследования доказали, что с помощью лечения радием 223 возможно продлить срок выживаемости больным раком простаты с распространенными костными метастазами.
Атомные шарики при лечении рака
При раке печени возможно уничтожить раковую ткань с помощью радиоактивных микрошариков которые внутривенно запускаются в зараженную область. Подобный метод лечения называется радиоэмболизация или лечение радио-микрошариками и проводится совместно со специалистами таких областей медицины как, ядерная медицина, радиология и медицинская онкология. Лечение возможно использовать, как и при раке печени так же и при метастазах в печень от другой первичной опухоли. В лечении используются микрошарики начиненные радиоактивным веществом с высокой энергией; yttrium-90. Радиоактивные микрошарики внутривенно вводятся в область, питающую раковую опухоль с помощью ангиографии. Таким образом, микрошарики способны уничтожить раковые клетки и областные распространения с помощью радиоактивных лучей. Подобное лечение способно остановить рост заболевания, сократить опухоль в размерах и повысить срок выживаемости. Лечение больше всего предпочитается в случаях, когда больной испробовал все имеющиеся лечения и когда опухоль не подлежит хирургическому вмешательству. Для проведения лечения радиоактивными микрошариками такие показатели как возраст, физическое состояние больного, состояние печени, распространение заболевания имеют очень важное значение.
Лечение продлевает продолжительность жизни при нейроэндокринным типе рака
При лечении нейроэндокринных разновидностей рака, так же возможно использовать радиоактивные методы лечения. Подобное лечение называется пептид-рецепторная радионуклидная терапия (ПРРТ). Нейроэндокринные опухоли (НЭО) состоят из пептид рецепторов соматостатина и могут образоваться в таких органах как желудок, поджелудочная железа, кишечник, щитовидная железа и лёгкие. Перед началом лечения с помощью ПЭТ-КТ определяется распространение рецепторов по опухоли и их количество. Помимо этого так же определяется распространение заболевания (метастазирование) по всему организму и устанавливается доза лечения. Во время лечения, радиоактивные пептиды внутривенно вводятся в организм и целенаправленно прикрепляясь к раковым клеткам, уничтожают их за счёт радиоактивных лучей. После лечения пациентам возможно будет необходимо несколько дней остаться в больнице. Обычно подобное лечение продолжается 3-5 курсов. Подобное лечение проводится при неоперабельных, обширно метастазирующих и не подлежащим химиотерапевтическому лечению опухолях. С помощью подобного лечения, из трёх пациентов у одного бывает возможно получить положительный эффект и у половины пациентов бывает возможно остановить рост заболевания.
Лечение радиоактивным йодом рака щитовидной железы
Лечение радиоактивным йодом (атомное лечение) является самым известным и часто используемым радионуклидным лечением при раке щитовидной железы. Лечение используется уже долгие годы и является лечением, чья надежность и эффективность была неоднократно доказана. Подобное лечение проводится после оперативного лечения пациентам с диагноз рака щитовидной железы. После того как вся щитовидная железа удаляется хирургическим вмешательством, радиоактивный йод накопляется в остаточных раковых клетках и с помощью радиоактивных лучей позволяет уничтожить оставшиеся микроскопические клетки. Так же при рецидиве заболевания, при необходимости лечение проводится с более высокими дозами. Радиоактивный йод применяется оральным путём в качестве капсулы или жидкости.
Радиоактивные лечения бывают эффективны при некоторых опухолей детского возраста
Возможно использовать вещества связанные с радиоактивным йодом под названием МИБГ, для лечения одной из опухолей детского возраста, невробластомы. МИБГ имеет похожие свойства с пептидом под названием норепинефрин, который используется раковыми клетками. МИБГ связывается с радиоактивным йодом и вводится в организм внутривенным путём. Подобное лечение, целенаправленно уничтожая раковые клетки, помогает 1/3 пациентам с неоперабельным заболеванием на распространенной стадии. Лечение МИБГ так же может быть эффективным у подходящих пациентов с диагнозом нейроэндокринного рака.
Использование при лимфоме (рак лимфатических узлов)
При раке лимфатических узлов (лимфоме) который не реагирует на другие онкологические методы лечения, радионуклидная терапия может быть альтернативным методом лечения. Подобное лечение возможно применить для подходящих больных лимфомой низкой степени. Связанные с Yttrium-90 или Йод-131 антикоры под названием CD20, целенаправленно направляются к антикорам находящимся в раковых клетках и на микроскопическом уровне уничтожают их методом высокодозными радиоактивными лучами. С помощью данного метода больше чем у половины пациентов, чьё заболевание сопротивляется другим методам онкологического лечения, возможно добиться положительный ответ.
Не травмирует больных
Атомные методы лечения не наносят сильный вред здоровым тканям и таким образом не травмируют больных как химиотерапия и радиотерапия. Во время лечения радиотерапией, радиоактивные лучи помимо раковой ткани так же затрагивают и приносят вред здоровым тканям. При атомных лечениях облучение не затрагивает весь организм. С помощью свойства целенаправленного влияния, только раковая опухоль и её окружность подвергается облучению и таким образом возможно в значительной степени защитить здоровые ткани организма. Но важно принять меры защиты тех мест откуда будет выходить не использованная часть атома.
Видимая часть айсберга
Ядерная медицина не используется при каждой разновидности рака. Ядерная медицина является быстро развивающийся областью медицины и используется при лечении таких заболеваний как; нейроэндокринные опухоли, некоторые разновидности лимфомы, рак печени, диффузный токсический зоб, рак щитовидной железы, некоторые разновидности опухолей детского возраста, специально выбранные больные раком простаты. Для того что бы правильно принять решение о лечении, пациент начиная с диагностики должен оценивается многопрофильной командой состоящей из специалистов разных областей медицины. Учитывая достигнутые успехи, будет правильно назвать сегодняшние достижения видимой частью айсберга.
Читайте также:

