Обходной гастроэнтероанастомоз при раке
При раке желудка выполняют два типа паллиативных операций. При первом типе вмешательств операция, не устраняя очага поражения, направлена на улучшение питания и общего состояния больного. Такими операциями являются обходной анастомоз между желудком и тонкой кишкой - гастроэнтероанастомоз, гастро- и еюностомии. При втором типе операций удаляется первичный очаг опухоли или метастазы. К таким операциям относятся паллиативные резекции, паллиативные гастрэктомии и удаление метастазов.
Гастроэнтеростомия (наложение гастроэнтеростомоза)
Желудочно-кишечный анастомоз накладывается при иноперабельном раке выходного отдела желудка, и эта операция является наиболее частым паллиативным вмешательством. Смысл операции заключается в создании соустья между желудком и тощей кишкой. В настоящее время выполняют заднюю - позадиободочную, реже переднюю - впередиободочную гастроэнтеростомию. В первом случае через отверстие в брыжейке поперечно-ободочной кишки выводят заднюю стенку желудка и соединяют анастомозом с петлей тонкой кишки. Во втором варианте, петлю кишки проводят впереди от поперечно-ободочной кишки, прикладывают к передней стенке желудка и соединяют с ним соустьем. В 8-10 см ниже гастроэнтероанастомоза обычно накладывается межкишечный брауновский анастомоз.
Операцию применяют при неоперабельном раке проксимального отдела желудка и пищевода, сопровождающемся нарушением проходимости пиши. Предложено более ста модификаций этой операции. Наибольшее распространение получила гастростомия по Кадеру и Витцелю.
Кишечный свищ или энтеростому накладывают для обеспечения питания больного при раке желудка и создания проходимости пищеварительного тракта. Операция также производится при обширном поражении желудка с нарушением проходимости и невозможности наложить гастростому. Подобная операция является единственным средством помочь неоперабельному больному раком резецированного желудка. Чаще искусственный свищ создается в начальном отделе кишечника (еюностомия).
Однао еюностомия не пользуется популярностью среди хирургов. Это связано с тем, что введение зонда, значительно суживающего просвет кишки, вызывает застой и создает условия для вытекания кишечного содержимого.
Ко второму типу паллиативных операций относятся паллиативные резекции. Эти операции, в основном, выполняются при невозможности полного удаления метастазов в лимфатических узлах или в органах при удалимости первичной опухоли. Паллиативную резекцию желудка производят главным образом в целях увеличения эффективности последующей лучевой и химиотерапии.
Противопоказаниями к проведению паллиативной резекции являются: метастазы в брюшину, брыжейку, сальник, асцит; отдаленные метастазы в кости, головной мозг, легкие и т.д., тяжелое общее состояние больного.
Паллиативное удаление первичного очага позволяет уменьшить массу опухоли и, тем самым, снизить токсическое ее влияние на организм больного, устранить источник непроходимости и кровотечения, что позволяет больному жить некоторое время с метастазами. В основном паллиативные резекции выполняются с целью дальнейшего проведения химио- и лучевой терапии Обходные анастомозы, гастро- и еюностомы также облегчают проведение лекарственного лечения, поскольку ослабленный голодом больной не в состоянии выдержать лечение. Улучшение состояния пациента после начала питания через стому в дальнейшем позволит применить химиотерапию. Техника таких операций такая же, как и обычной резекции желудка, но без удаления лимфатических узлов или метастазов.Химиотерапию в чистом виде применяют только при неоперабельных формах рака. Попытки продлить жизнь этих больных с помощью полнили монохимиотерапии показали эффективность 5-фторурацила и фторафура. 5-Фторурацил вводят внутривенно из расчета 15 мг/кг через день в суммарной дозе на курс лечения 4—5 г. Фторафур назначают по 30 мг/кг внутривенно или внутрь, рекомендуется суточную дозу делить на 2 приема, ориентировочная суммарная доза — 20—30 г. Повторные курсы химиотерапии проводят через 4—6 нед.
Химиотерапия позволяет добиться частичной регрессии опухоли у 20—30% больных. Средняя продолжительность жизни больных, перенесших паллиативную дистальную резекцию желудка, при проведении им химиотерапии составляет 23,3±3,6 мес, а если химиотерапия не назначалась — только 12,9±2,8 мес.
Профилактическая химиотерапия может проводиться у радикально оперированных больных раком желудка. Дополнительное лечение 5-фторурацилом в дозе 15 мг/кг через день (по 3 г суммарно) назначают через 1 и 3 мес после радикальной операции. Это лечение уменьшает частоту рецидивов и метастазов.
Химиотерапия перечисленными препаратами может сопровождаться рядом побочных явлений, среди которых основное значение имеет угнетение кроветворения (особенно белого ростка и тромбоцитов) и поражение слизистых оболочек желудочно-кишечного тракта. В этих случаях ограничивается возможность длительного лечения или применения высоких доз.
Дата добавления: 2016-07-18 ; просмотров: 3552 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Рак желудка — это диагноз, который пугает каждого человека. С современной экологией и принципами образа жизни, количество людей с подобным диагнозом растет с каждым годом. В 90% случаев — причина развития злокачественного процесса – хронический гастрит ассоциированный с Helicobacter Pylori.
Как любая онкологическая патология, заболевание имеет 3 типа лечебного воздействия:
3. Симптоматическое лечение – лечение направленно на устранение симптомов заболевания, без удаления первичной опухоли. Выполняется пациентам с 4 стадией заболевания, либо при больших местнораспространённых опухолях.

Выбор оперативного вмешательства всегда решается индивидуально для каждого пациента, исходя из множества факторов.
Радикальные хирургические вмешательства
Эндоскопические методики – это одни из самых современных направлений в желудочной хирургии рака, которые впервые совершили прорыв в лечении в Японии. Суть метода заключается в том, что врач — эндоскопист во время проведения ФГДС иссекает опухоль в пределах жизнеспособных тканей. И пациент без выполнения больших и травматичных операций продолжает жить дальше! Но у данного метода существуют значительные ограничения: он показан пациентам только с самым ранним раком желудка, на том этапе, пока опухоль локализуется только в поверхностных слоях эпителия. К сожалению, на данной стадии рак абсолютно не имеет никаких симптомов, а подобные операции в России носят скорее казуистический характер.
Резекция (удаление части органа) – является органосохраняющей операцией. Суть состоит в удалении части органа с опухолью и окружающими опухоль лимфоузлами (лимфодиссекция). Резекции желудка бывают двух видов: дистальная и проксимальная. Выбор вида резекции зависит от того в какой части органа растёт опухоль.
Операция завершается восстановлением непрерывности желудочно-кишечного тракта при помощи подшивания тонкой кишки к стенке резецированного органа с формированием анастомоза (искусственного соустья).
Самая объёмная операция на желудке при раке — гастрэктомия. Она заключается в полном удалении органа. Эту операцию выполняют, при наличии хотя бы одного из следующих условий:
- рак тела желудка;
- диффузно-инфильтративный характер роста опухоли;
- недифференцированные формы рака (перстневидноклеточный).
Восстановление непрерывности желудочного – кишечного тракта после удаления органа заключается в подшивании к пищеводу тонкой кишки.
Резекцию желудка и гастрэктомию выполняют также и в качестве паллиативных операций при развитии жизнеугрожающих состояниях для пациента.
Симптоматические хирургические вмешательства
Как уже было сказано, основная цель симптоматического лечения – это повышение качества жизни пациента, вылечить которого уже по тем или иным причинам невозможно. Опухоль на этом этапе разрастается настолько сильно, что перекрывает просвет органа, делая невозможным питание пациента. Наиболее частые жалобы: тошнота, ощущение переполнения желудка даже при приёме незначительного количества пищи, рвота съеденной едой. Главная миссия врачей – восстановить возможность питания.
Итак, рассмотрим наиболее типовые операции.
Гастростомия – операция, суть которой сводится к формированию соустья (гастростома) между желудком и внешней средой. Показанием для такого вида лечения являются неудалимые опухоли пищеводно-желудочного перехода. Гастростома позволяет пациенту принимать пищу не через рот, а сразу в желудок, что спасает его от истощения.
Гастроэнтероанастомоз – это обходной анастомоз, который формируется между непоражённой частью органа и тонкой кишкой при больших опухолях выходного отдела. Таким образом, пища сначала попадает в желудок, затем эвакуируется сразу в тонкую кишку, минуя опухоль.
Этот вид симптоматической операции является наиболее физиологичным для пациента.
Это, пожалуй, самый последний предел хирургического лечения, применяемый при тотальном поражении желудка раковой опухолью, когда стенка проросла новообразованием во всех отделах, и нет возможности выполнить какую-либо другую операцию. В таком случае начальный участок тонкой кишки подшивается к передней брюшной стенке и формируется соустье между кишкой и внешней средой (еюностома). Питание пациент получает непосредственно в кишку, что позволяет ему не умереть от мучительной голодной смерти.
Одним из самых современных видов симптоматического лечения является расширение опухолевого стеноза. При этом методе врач — эндоскопист раздвигает участок ракового сужения при помощи стента (своеобразная каркасная распорка), позволяя пациенту питаться через рот достаточно длительное время. К сожалению, в настоящее время метод практикуется не во всех лечебных учреждениях.
Консультации врача при появлении первых жалоб и ежегодный скрининг органов ЖКТ помогут выявить рак на начальной стадии. Это сэкономит потраченное на лечение время, деньги, здоровье. И нужно всегда помнить, что рак излечим при своевременном обращении. Необходимость удаления всего органа (или другая операция при раке желудка) и срок жизни после операции напрямую зависит от стадии процесса, когда началось лечение. Рак желудка после операции требует от пациента особого подхода, который заключается в радикальном изменении образа жизни, принципов питания и трудового режима.
Анастомоз может быть наложен на передней(anastomosis anterior)и на задней (anastomosis posterior)стенке желудка. В обоих случаях к желудку подводится двойная петля тощей кишки, одна из них —оральная —будет приводящей, вторая —каудальная —отводящей. Согласно этому, может быть наложено четыре способа га строэнтероа на стомозов :
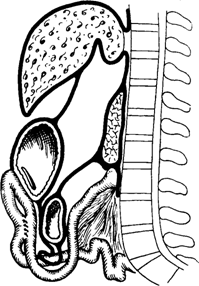
Рис. 5-162. Oastroenteroanastomosis antecolica anterior
1. gastroenteroanastomosis antecolica anterior (Wolfler, 1881),(рис. 5-162)-,
2. gastroenteroanastomosis antecolica posterior (Монастырский, 1885);
3. gastroenteroanastomosis retrocolica anterior (Billroth, 1885),(-рис. 5-163)-,
4. gastroenteroanastomosis retrocolica posterior (Hacker, 1885),(рис. 5-164).
На практике распространены только первый и четвертый способы, третий способ используется только в исключительных случаях. Второй способ анастомоза распространения не получил, мы его никогда не накладываем.
Особой формой гастроэнтероанастомоза является Y-анастомозпо Roux (1893);при нем имеется только отводящая петля кишки, так как к желудку подводится только одна петля тощей кишки. В принципе и этот анастомоз может иметь четыре вышеназванных варианта.
Y-образныйанастомоз по Rouxкак самостоятельная операция не производится, его используют для восстановления пищеварительного канала после резекций или повторных резекций желудка(рис. 5-165).
Gastroenteroanastomosis antecolica anterior
Производится верхняя левосторонняя трансректальная лапаротомия. Сальник и поперечнообо-дочная кишка оттягиваются ассистентом кверху и кпереди, благодаря чему открывается двенадца-типерстно-тощекишечный изгиб (flexura duodeno-jejunalis).Нужно убедиться в том, что именно этот участок кишки обнаружен хирургом, потому что уже случалось, что хирург принимал за первую петлю тощей кишки приросшую к этому месту нижнюю петлю подвздошной кишки. Если гастро-
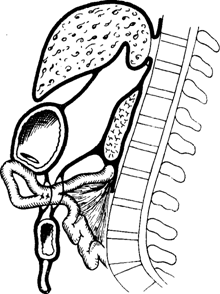
Рис. 5-163. Oastroenteroanastomosis retrocolica anterior
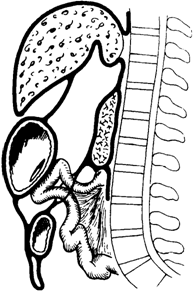
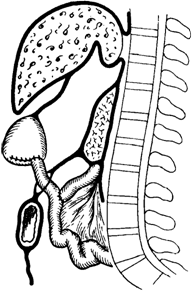
Рис. 5-164. Oasti-oenteroanastomosis retrocolica posteriorРис. 5-165. Y-образный гастроэнтероанастомоз по Roux
энтероанастомоз накладывается на эту последнюю петлю подвздошной кишки, больной в скором времени может погибнуть.
Если нет сращений, то первую петлю тощей кишки легко распознать по тому, как она появляется из забрюшинного пространства. Возможные сращения разделяются ножницами лишь настолько, чтобы отдельные кишечные петли приняли свое первоначальное положение. Верным признаком того, что перед нами двенадцатиперстно-то-щекишечный изгиб, является то, что вправо от него (к правой стороне тела больного) проходит перед последним отделом двенадцатиперстной кишки, вертикально—верхняя брыжеечная артерия и вправо от нее —одноименная вена. Слева от изгиба, за задней париетальной брюшиной проходит снизу вверх нижняя брыжеечная вена. Следовательно, этот изгиб располагается между нижней брыжеечной веной (слева от изгиба) и верхней брыжеечной артерией (справа от изгиба).
Петля тощей кишки берется в 20—25смот двенадцатиперстно-тощекишечного изгиба и поднимается впереди от сальника и поперечноободоч-ной кишки в верхний отдел брюшной полости, где помещается рядом с желудком.
Место для наложения анатомоза выбирается далеко от привратника, чтобы в случае опухоли в области привратника сужение анастомоза происходило как можно позднее. Место для анастомоза выбирается на бессосудистом участке по продольной оси желудка. Принято сшивать тонкую кишку с желудком изоперистальтически, однако и антиперистальтическое расположение не сопровождается никакими последствиями.
Часть желудка, подлежащая вскрытию, поднимается и зажимается в поперечном направлении у ее основания мягким зажимом, чтобы, сильно ин-
фицированное желудочное содержимое (опухоль, анацидность) не попало на брюшину.
Желудок сшивают с тонкой кишкой непрерывными серо-серозными швами на протяжении примерно 10см.На расстоянии около полусантиметра от ряда швов на желудке на протяженииб—8>см рассекается серо-мускулярный слой. На сосуды, проходящие в субмукозном слое, накладываются москитные зажимы, после чего они по линии разреза перевязываются. Затем рассекается слизистая. Просвет кишки вскрывается на такую же длину. В случае опухоли из стенки желудка выкраивается овальный лоскут, чтобы на гипертрофически уплотненной стенке образовалась щель, которую длительное время не сможет закрыть растущая опухоль.
После рассечения слизистой желудка и кишки отсасывается содержимое этих органов и их внутренняя поверхность вытирается салфетками. Накладывается непрерывный прошивной ряд кетгу-товых швов, затем передний непрерывный ряд кет-гутовых швов и, наконец, передним непрерывным серо-серозным швом завершается наложение анастомоза.
После наложения анастомоза по данному способу содержимое двенадцатиперстной кишки (желчь, панкреатический сок, кишечное отделяемое) должно сначала по приводящей петле кишки попасть от двенадцатиперстно-тощекишечного изгиба к месту анастомоза, а уже потом по отводящей петле —в нижний отдел кишечника. Чтобы содержимому кишки не нужно было преодолевать такой обходной путь, обычно между нижележащими частями приводящей и отводящей петель тощей кишки накладывается анастомоз поBraun,илиеюно-еюнальный анастомоз (рис. 5-166).
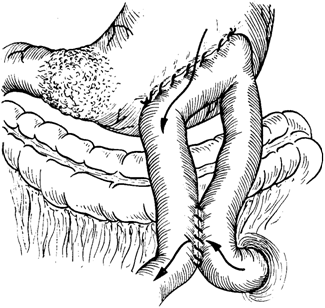
Рис. 5-166. Gastroenteroanastomosis antecolica anterior. Законченныйанастомоз. Между приводящей и отводящей петлями кишки накладывается межкишечный анастомоз по Braun
При гастроэнтероанастомозе, наложенном не при резекции желудка, а в особенности при обычной гастроэнтеростоме, случается, что содержимое желудка попадает не в отводящую, а в приводящую петлю кишки и оттуда —через двенадцатиперстную кишку, если привратник еще несколько открыт, —совершает обратный путь в желудок. Возникаетпорочный круг.Короткий анастомоз между петлями тощей кишки по Braun служит для предупреждения этого осложнения.
Однако многие авторы, в том числе и автор этой главы, не считают обязательным наложение анастомоза по Braunпри gastroenteroanastomosis antecolica anterior.После завершения наложения гастроэнтероанастомоза брюшная полость послойно закрывается наглухо, без дренирования.
Gastroenteroanastomosis retrocolica posterior
Производится верхняя левосторонняя трансректальная лапаротомия. Большой сальник и попе-речноободочная кишка отводятся ассистентом кверху и кпереди. На нижней поверхности натянутой брыжейки поперечноободочной кишки, на ее бессосудистом участке скальпелем наносится разрез в направлении спереди назад, этот разрез затем расширяется тупым путем двумя пальцами до 10см.
Левой рукой желудок отодвигается книзу. После этого в отверстии брыжейки поперечноободочной кишки появляется задняя поверхность же-
лудка. Желудок отводится книзу. Рядим с ним помещается первая после двенадцатиперстно-тоще-кишечного изгиба петля тощей кишки. С этой петлей будет образован анастомоз на н. т. короткой петле. Линия анастомоза может быть выбрана на участке желудка между большой и малой кривизной как по его продольной оси, так и по поперечной.
Как правило, анастомоз накладывается в изопе-ристальтическом направлении, но может быть без неблагоприятных последствий наложен и антиперистальтически. Если анастомоз наложен по поперечнику желудка, то он изоперистальтичен, если приводящая петля обращена к малой кривизне, а отводящая к большой кривизне желудка, то анастомоз наложен антиперистальтично. Четыре ряда швов накладываются, как и при предыдущем варианте анастомоза.
После наложения последнего ряда серо-серозных швов края разреза на брыжейке поперечно-ободочной кишки несколькими серозными швами прикрепляют к задней стенке желудка, чтобы через это отверстие не могла проскользнуть и ущемиться петля тощей кишки (рис. 5-167).
Брюшная полость закрывается послойно, наглухо, дренажная трубка в брюшную полость не вводится.
При иноперабильной карциноме привратники желудка из двух вариантов применяемых анастомозов рекомендуетсяgastroenteroanastomosis antecolica anterior санастомозом по Braunили без него. Дело в том, что раковая опухоль часто распространяется и на брыжейку поперечноободочной кишки и может полностью закрыть gastroenteroanastomosis retrocolica posterior.От наложения

Рис. 5-167. Gastroenteroanastomosis retrocolica posterior под высоко поднятой поперечноободочной кишкой
Дата добавления: 2018-06-27 ; просмотров: 807 ;
Паллиативные операции при раке желудка включают в себя симптоматические операции, временно облегчающие состояние пациентов, и направленные на устранение тех или иных тяжелых или опасных для жизни симптомов онкологического заболевания, а также циторедуктивные операции, которые существенно уменьшают размер первичной опухоли и метастазов, уменьшая степень опухолевой интоксикации.
В каких ситуациях проводятся паллиативные операции при раке желудка?
В лечении рака желудка главная роль до сих пор принадлежит хирургическому методу, однако, на поздних стадиях рака желудка при распространенных поражениях окружающих тканей с вовлечением регионарных лимфатических узлов и наличием отдалённых метастазов, тяжелом состоянии пациента, проведение радикальных операций невозможно. Радикальные операции при раке желудка (субтотальная резекция желудка, гастрэктомия, проксимальная резекция) – это всегда обширные операции, которые помимо вмешательства собственно на желудке сопровождаются удалением большого и малого сальника, а во время комбинированных операций одновременно удаляют полностью или частично пораженные раковым процессом соседние органы (поджелудочную железу, печень, поперечно-ободочную кишку, селезенку).
Радикальная операция при раке желудка является серьезным хирургическим вмешательством, которое требует существенной компенсации функций организма. Многим больным отказывают в операции из-за высокой степени операционного риска. Между тем при раке желудка на 4-й стадии на фоне специфической терапии 5-летняя выживаемость достигает 15-20%, а с развитием высокотехнологичных методов лечения можно рассчитывать и на большее продление жизни пациентов. Поэтому сейчас активно разрабатываются хирургические методики, позволяющие облегчить состояние и значительно улучшить качество жизни пациентов с раком желудка, радикальная операция у которых невозможна.
Выполнение паллиативных операций у пациентов с раком желудка делают возможным проведение лучевой и химиотерапии, введение индивидуальных противоопухолевых вакцин и моноклональных антител (SU11248), что позволяет добиться стойкой стабилизации течения заболевания и увеличить ожидаемую продолжительность жизни.
Когда необходимо паллиативное хирургическое вмешательство?
Диагноз 4 стадии рака желудка устанавливается при инвазивном поражении опухолью соседних органов, близлежащих лимфатических узлов, или при наличии метастазов в отдаленные органы и ткани. Хирургическое лечение в таких ситуациях применяется преимущественно для лечения жизнеугрожающих состояний – кровотечения из опухоли, прободения (перфорации) стенки желудка, стенозе желудка с развитием тяжелых водно-электролитных расстройств и невозможностью питания, желтухе при поражении опухолью печени и желчевыводящих путей.
В хирургическом стационаре лечение начинают с попытки остановки кровотечения с помощью кровоостанавливающих средств и установке зонда Блэкмора для прекращения желудочного кровотечения. Одновременно начинается инфузия препаратов плазмы крови с целью профилактики ДВС-синдрома, а при массивной кровопотере также проводится переливание эритроцитарной массы. Малоинвазивные вмешательства выполняются с целью поиска источника кровотечения и точечной ликвидации кровотечения, для чего проводится эндоскопическое вмешательство, позволяющее выполнить клипирование и прошивание кровоточащего сосуда, провести электро- или плазменную коагуляцию. Все эти методики остановки желудных кровотечений при раке желудка и других осложнениях онкологических заболеваний используются в Европейской онкологической клинике.
При неэффективности предпринятых мер по устранению желудочного кровотечения проводится экстренная хирургическая операция.
Желтуха - прямое противопоказание для проведения плановых химио- и лучевой терапии. Единственным радиальным методом снижения высокого уровня билирубина является восстановления оттока желчи из печени путем проведения рентгенохирургического вмешательства. Дренирование позволяет наладить временный отток наружу на поверхность кожи (наружный дренаж) или как наружу, так и в естественном направлении в кишечник (наружно-внутренний дренаж). В некоторых случаях, когда опухолевое сдавление изолирует несколько разных сегментов желчного дерева, например, как левую, так и правую доли печени, может потребоваться установка нескольких дренажей.
После снижения уровня билирубина до нормальных величин и уменьшения явлений холангита дренаж заменяется на стент или стенты – специальные эндопротезы, которые поддерживают желчный проток в открытом состоянии. Выполнение одномоментного дренирования и стентирования проводится только по строгим медицинским показаниям, чаще всего эти операции разделены по времени. В целом, дренирование и стентирование желчных протоков существенно улучшает качество жизни больных.

У 10-15% пациентов раком желудка развивается требующий хирургического вмешательства стеноз (сужение просвета) кардиального или пилорического отдела желудка. Симптомами этого состояния служат затруднение при проглатывании пищи при поражении верхних (кардиальных) отделов, тяжесть, чувство переполнения и рвота давно съеденной пищей при вовлечении перехода из желудка в 12-перстную кишку(пилоростеноз).
Стеноз при раке желудка чреват развитием опасных для жизни водно-электролитных расстройств и усугублением кахексии (истощения). Для восстановления прохождения пищи по желудочно-кишечному тракту, коррекции и профилактики водно-электролитных нарушений при иноперабельном раке желудка со стенозом пилорического отдела проводят операцию гастроэнтеростомии, т.е. наложение соустья между желудком и тощей кишкой.
C целью коррекции стеноза при неоперабельном раке проксимального (кардиального) отдела желудка c переходом на пищевод при нарушении прохождения пищи может использоваться стентирование желудка – установка специальных стентов, которые восстанавливают нормальное прохождение пищи через желудок в кишечник. Альтернативным способом хирургического лечения является наложение гастростомы – гастростомия - формирование отверстия в желудке и передней брюшной стенке, для обеспечения питания больного через зонд. В результате уменьшаются симптомы интоксикации и обеспечение питание больного.
Операции раке с метастазами
Рак желудка в большинстве случаев довольно рано дает метастазы. Из числа наиболее часто поражаемых метастазами органов следует указать печень, поджелудочную железу, легкие, яичники (метастаз Крукенберга), а также брюшину, которая покрывается множественными раковыми узелками, что сопровождается выпотом жидкости в брюшную полость (асцитом). Помимо того, что метастазы могут приводить к развитию острых осложнений, требующие экстренной хирургической помощи (сдавление нижней полой вены), они существенно нарушают функционирование пораженных органов, значительно ухудшают общее состояние, нередко сопровождаясь нестерпимыми болями, требующими постоянного обезболивания.
Как в ведущих, в т.ч. зарубежных клиниках, так и в Европейской онкологической клинике для лечения метастазов рака желудка, в частности в печень, используется чрескожная чреспеченочная радиочастотная абляция (РЧА) – методика, вызывающая контролируемый асептический некроз метастатического очага, без повреждения окружающих тканей. Результатом такого некроза становится полная гибель опухолевых клеток метастаза. При ее выполнении, которое проводится под общим обезболиванием, под ультразвуковым контролем сквозь кожу вводится монополярный радиоволновой электрод, разогревающий именно нужный участок печени и вызывающий локальный некроз метастаза. РЧА может также проводится во время открытой операции на желудке и органах брюшной полости. РЧА метастазов печени дает возможность надолго продлить жизнь пациента без возникновения рецидивов. У нас накоплен опыт неодократного проведения РЧА для полного устранения множества мелких метастазов печени, а также в случае появления новых метастатических очагов.
В отделении интервенционной онкологии и эндоваскулярной хирургии Европейской онкологической клиники выполняется химиоэмболизация артерий, питающих крупные метастазы, преимущественно в печени, с целью уменьшения негативного влияния метастазов рака на организм пациента. Прекращение кровотока в опухоли уже само по себе оказывает лечебное воздействие. Одновременная доставка в ткань опухоли химиопрепаратов разрушает ее изнутри, избавляя пациента от токсического действия лекарства на весь организм в целом.
В мире используется также такая методика лечения метастазов печени, как радиоэмболизация метастазов рака желудка в печень. Она проводится под контролем ангиографа с помощью внутрисосудистой селективной катеризации сосудов печени. В сосуд, питающий опухоль, вводятся эмболизирующие частицы с радиоактивным изотопом иттрий-90, которые в последующие после операции 64 часа продолжают изнутри воздействовать на опухоль. К сожалению, в нашей стране данная методика не доступна. Для этих целей мы направляем пациентов в клиники Израиля и Германии.
Малотравматичные резекции печени, включая радиочастотную аблацию метастазов рака в печень, в нашей клинике проводятся учеником профессора, д.м.н. Юрия Ивановича Патютко, заместителем главного врача клиники, к.м.н. Андреем Львовичем Пылёвым. Кроме того, наиболее сложные операции выполняются самим Юрием Ивановичем Патютко, руководителем хирургического отделения опухолей печени РОНЦ им. Н. Н. Блохина.
При распространении опухолевого процесса – диссеминации метастазов опухоли желудка по брюшине (т.н. канцероматоз брюшины) может происходить накопление жидкости в брюшной полости. Это состояние называется асцит, оно довольно мучительно для пациента. В основном, оно обусловлено механическим препятствием обратному всасыванию жидкости из брюшной полости, в норме происходящему очень интенсивно (до 1,5 л в сутки) и закупоркой лимфатических сосудов. При метастатическом поражении паренхимы печени, в основе развития асцита лежит, кроме того, препятствие венозному оттоку крови.
Когда жидкости становится больше 5 л и больше сдавление внутренних органов, нарушение экскурсии диафрагмы, повышение внутрибрюшного давления приводят к смещению органов вверх, в грудную полость, вызывают дыхательную недостаточность и нарушение нормального крово- и лимфотока. При этом создаются благоприятные условия для быстрого и обширного метастазирования опухоли. Однако одномоментное удаление большого количества асцитической жидкости может привести к возникновению тяжелых осложнений, поэтому в Европейской онкологической клинике для дренирования асцитов применяются современные методики лапароцентеза с использованием специальных помп для постепенного и дозированного удаления серозной жидкости.
Параллельно проводится инфузионная терапия для коррекции водно-электролитных нарушений, инфузии альбумина, коллоидов и объёмо-замещающих растворов. Для предотвращения возникновения асцита, после первичной эвакуации асцитической жидкости, мы активно используем цитостатические препараты, т.е. лекарственные вещества, способствующие уменьшению объема выпота и более медленному накоплению жидкости, в том числе внутриполостное введение лекарственных препаратов. Внутриполостная химиотерапия эффективна в 40-60% случаев и позволяет сохранить положительный эффект брюшинной пункции на срок более 2 месяцев. Лапароцентез производится под ультразвуковой навигацией и при необходимости завершается установкой дренажа для длительной эвакуации жидкости.
Применяемые в нашей клинике катетеры не ограничивают естественную двигательную активность и обеспечивают возможность возвращения пациента к привычной деятельности. При рефрактерных и массивных асцитах возможно проведение паллиативных операций (установка перитонеовенозного шунта, частичная деперитонизация стенок брюшной полости, оментогепатофренопексия и другие). При таком комплексном подходе процедуру лапароцентеза требуется делать в 2-3 раза реже, чем при классическом проведении пункции брюшинной полости.
Насколько оправданы вмешательства в 4 стадии рака желудка, ведь они не приводят к излечению?
Философия оказания медицинской помощи в Европейской онкологической клинике заключается в том, что пациенту надо стараться помочь всегда. Человеческая жизнь бесценна, и ее нужно продлить на максимально больший срок при поддержании максимально возможного качества жизни. Вмешательства на поздней стадии онкологического заболевания, включая 4-ю стадию рака желудка, должны предприниматься, поскольку они позволяют существенно улучшить качество жизни пациентов, уменьшить интоксикацию и выраженность болевого синдрома, продлить жизнь и возможность общения с родными и близкими на существенный срок. Например, проведение перитонэктомии в сочетании с гипертермической внутрибрюшной химиотерапией у больных с канцероматозом брюшины при раке желудка позволяет увеличить продолжительность жизни до 18 месяцев. При единичных изолированных метастазах рака желудка в печень ее резекция позволяет достичь 5-летней выживемости у 18–34% больных.
Для лечения 4 стадии рака желудка в отделении паллиативной и симптоматической терапии используются все возможные варианты лечения онкологических больных: все виды химиотерапии, лучевая терапия, которая позволяет уменьшать болевой синдром, а также выполняются паллиативные операции. С целью облегчения введения препаратов возможна имплантация венозных и артериальных инфузионных порт-систем для химиотерапии, проводится регионарная интраартериальная инфузия химиопрепаратов, местная терапия.
— Необходима ли какая-либо особая подготовка для проведения паллиативных операций?
Безусловно, из-за тяжести болезни наши пациенты требуют особенно тщательной подготовки и ведения послеоперационного периода. Обычно предоперационная подготовка заключается в общеукрепляющем лечении, инфузионной терапии белковыми препаратами, солевыми и коллоидными растворами, витаминами, в применении тонизирующих средств. Существуют методики предоперационной инфузионной подготовки, позволяющие уменьшить кровопотерю в процессе операции, они активно используются в нашей клинике. Как правило больные нуждаются в гипералиментации – введении питательных веществ высокой энергетической ценности.
В послеоперационном периоде на несколько дней исключают прием пищи и воды через рот. Необходимые количества жидкости и питательных веществ восполняют путём внутривенных вливаний питательных растворов с инсулином, витаминами, а также крови и белковых препаратов. Пациенту назначают антибиотики, сердечные средства, наркотики и кислород. Важным компонентом является тщательный уход, дыхательная гимнастика, внимательное наблюдение за течением послеоперационного периода. В дальнейшем огромное значение имеет правильное сбалансированное дробное питание, приём необходимых препаратов и уход за больным.
Читайте также:

