Химиотерапия при плеврите при раке яичников
Другая проблема в лечении раке яичника (РЯ) — плевральный выпот. Приблизительно у 1/З пациенток с асцитом выявляют плевральный выпот, который, как правило, чувствителен к системной химиотерапии (XT). Плевральный выпот без асцита обычно указывает на наличие метастазов в плевре.
Используют те же методы лечения, что и при асците. Устойчивое повторяющееся накопление жидкости иногда можно преодолеть дренированием грудной клетки с последующим плевродезом. Облитерация плевральной полости предотвращает накопление жидкости.
С этой целью через дренажную трубку инстиллируют блеомицин (60—120 мг) или тальк. Техника плевродеза с введением суспензии талька через дренажную трубку в положении больной лежа приносит успех в 81 % случаев. Часто после этой процедуры может быть лихорадка, но нарушение дыхания наблюдается редко.
Место для торакоцентеза выбирают во время рентгеноскопии, УЗИ, КТ или физикального исследования грудной клетки. При тотальном гидротораксе лучшее место для пункции — седьмой или восьмой межреберный промежуток по задней подмышечной линии. Самая частая ошибка заключается в решении выполнить эту процедуру ниже необходимого уровня пункции.
Врач должен знать, что при пневмонии или травме происходит подъем диафрагмы и уменьшение объема легкого, поэтому следует выбрать более высокий уровень для пункции. Во время процедуры пациент находится в удобном положении сидя, слегка наклоняясь вперед и опираясь на специальную стойку с подушкой или на помощника.
Целесообразна премедикация наркотическим препаратом или диазепамом. Кожу грудной клетки обрабатывают антисептиком и закрывают стерильным бельем.
Проводят анестезию грудной стенки 5—10 мл лидокаина (Ксилокаин) с использованием шприца с иглой 22 G. Тщательно инфильтрируют кожу, ребро, надкостницу и париетальную плевру. При правильном обезболивании торакоцентез практически безболезненный. Иглу с коротким срезом (длина 7—10 см, 18—30 G) с помощью трехходового запорного крана присоединяют к шприцу объемом 20— 50 мл.
Некоторые предпочитают иглу, через которую проходит мягкий пластиковый катетер. После приложения достаточного усилия игла проникает в плевральную полость. Во избежание повреждений межреберного нерва и сосудов пункцию проводят в нижней части межреберного пространства. Для того чтобы игла занимала устойчивое положение на грудной стенке, ее можно фиксировать зажимом. При проведении процедуры воздух не должен попадать в грудную полость.
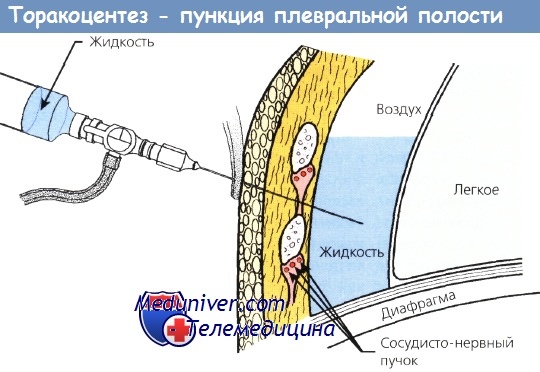
Во многих случаях за одну процедуру торакоцентеза можно удалить 2000—3000 мл жидкости. При медленной аспирации легкое успевает расправиться. Если выпот возник из-за метастазов в плевре, ткань легкого становится менее эластичной и может потребоваться дренирование плевральной полости.
На коже вокруг места пункции делают небольшой разрез и троакар вводят в плевральную полость; часто достаточно установить дренаж небольшого размера (№ 12—14). Иногда установку трубки после разреза кожи скальпелем осуществляют с помощью кровоостанавливающего зажима. Затем конец трубки, который был закрыт во время введения в полость, сразу присоединяют к дренажу с водяным затвором и фиксируют ее к грудной стенке несколькими швами. Такие дренажи часто оставляют на несколько дней и удаляют через сутки после плевродеза.
Хирургический подход к лечению рецидивирующих опухолевых выпотов был несколько ограничен. Перитонеовенозное шунтирование в качестве паллиативной процедуры при злокачественном асците, который не поддается стандартному лечению, появилось с момента разработки перитонеовенозного клапана, чувствительного кдавлению, и впервые описано LeVeen и соавт.
Qazi и Savlov сообщили об эффективной паллиативной помощи благодаря этому методу в 70 % случаев (28 из 40 пациентов). При плевральном выпоте с переменным успехом использовали декортикацию легкого и плеврэктомию. Эти процедуры заменила инстилляция химиотерапевтических препаратов и каустических веществ. Для индукции плеврита использовали гипертонический раствор глюкозы и суспензию талька.
Показатель успешного проведения того или иного подобного мероприятия в значительной мере зависит от опыта исследователя.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Патологические процессы в плевре и плевральной полости, в том числе плеврит, носят обычно вторичный характер, чаще всего –это осложнения заболеваний легких, травм грудной клетки, заболеваний органов средостения и брюшной полости. При этом нередко симптоматика плеврального выпота является ведущей в клинической картине заболевания.
| Механизм образования плеврального выпота при злокачественных новообразованиях: |
| Прямое влияние опухоли 1. Метастазы в плевру (увеличение проницаемости капилляров плевры) 2. Метастазы в плевру (обструкция лимфатических узлов) 3. Поражение лимфатических узлов средостения (cнижение лимфатического оттока из плевры). 4. Обтурация грудного протока (хилоторакс). 5. Обтурация бронха (снижение внутриплеврального давления). 6. Опухолевый перикардит. Опосредованное влияние опухоли 1. Гипопротеинемия. 2. Опухолевые пневмонии. 3. Эмболия сосудов легких. 4. Состояние после лучевой терапии. |
Плевральный выпот может быть транссудатом и экссудатом. Причиной образования транссудата обычно является застойная сердечная недостаточность, в основном у больных с левожелудочковой недостаточностью и перикардитом. При скоплении транссудата (гидротораксе) листки плевры не вовлечены в первичный патологический процесс.
Гидроторакс наблюдается в тех случаях, когда изменяется системное или легочное капиллярное или онкотическое давление плазмы (левожелудочковая недостаточность, цирроз печени).
Плеврит (скопление экссудата в полости плевры) наиболее часто образуется у больных злокачественными новообразованиями. Наиболее распространенной причиной экссудативного плеврита является метастазирование в плевру и лимфатические узлы средочтения. Плевральный выпот при опухолях имеет сложное происхождение: накопление жидкости обусловлено увеличением проницаемости капилляров вследствие их воспаления или разрыва эндотелия, а также ухудшением лимфатического дренажа из-за обструкции лимфатических путей опухолью и прорастания опухоли в плевру. Накоплению выпота у онкологических больных могут способствовать нарушение питания и снижение содержания белка в сыворотке крови [1–4].
АЛГОРИТМ ЛЕЧЕНИЯ ОПУХОЛЕВЫХ ПЛЕВРИТОВ
Схема
Опухолевый (метастатический) плеврит является частым осложнением при раке легкого, молочной железы, яичников, а также при лимфомах и лейкозах. Так, при раке легкого он встречается у 24– 50% больных, молочной железы – до 48%, при лимфомах – до 26%, а раке яичников – до 10%. При других злокачественных опухолях опухолевый плеврит выявляется у 1 – 6% пациентов (рак желудка, толстой кишки, поджелудочной железы, саркомы, меланомы и др.). Наиболее частой причиной экссудативных плевритов является метастазирование в плевру и лимфатические узлы средостения. Плеврит, как правило, свидетельствует о далеко зашедшем опухолевом процессе и является следствием опухолевых высыпаний по плевре.
Диагностика
Цитологическое исследование плевральной жидкости на опухолевые клетки (содержание эритролитов более 1 млн/мм3) является важным методом диагностики. Получение при плевральной пункции геморрагического экссудата с высокой степенью вероятности свидетельствует об опухолевой этиологии выпота. Частота обнаружения опухолевых клеток при этом достигает 80– 70%. На основании цитологического исследования плевральной жидкости часто удается определить морфологический тип первичной опухоли.
Таблица 1. Частота выпотов различной этиологии (Р. Лайт, 1986) [1]
Частота выпотов, %
Накопление жидкости в плевральной полости приводит к сдавлению легкого, смещению средостения, что в свою очередь вызывает усиление одышки, нарушение дыхательной и сердечной деятельности. Часто плеврит, являясь единственным проявлением опухолевого процесса, может быть причиной смерти больного.
Лечение больных с выпотом в плевральную полость заключается прежде всего в эвакуации жидкости, внутриплевральном введении лекарственных препаратов с целью прекращения накопления жидкости в плевральной полости и рассасывания экссудата. Это приводит к улучшению состояния больного, уменьшению одышки, болей, легочно-сердечной недостаточности и тем самым к удлинению жизни. Алгоритм диагностики и лечения опухолевых плевритов представлен на схеме.
Перед решением вопроса о введении внутриплеврально тех или иных лекарственных препаратов необходимо уточнить локализацию первичного процесса, так как при раке молочной железы, яичников, мелкоклеточном раке легкого, лимфомах проведение системной химиотерапии может привести к ликвидации плеврального выпота у 30– 60% пациентов.
Таблица 2. Препараты, используемые для плевродеза (сводные данные)
В тех случаях, когда системная химиотерапия не показана или она была неэффективной, необходимо внутриплевральное введение лекарственных препаратов. Показанием для плевральных пункций и внутриплеврального введения лекарств является наличие выпота в плевральной полости выше уровня II– III ребра спереди, выраженной одышки с явлениями легочной или легочно-сердечной недостаточности, при ожидаемой продолжительности жизни более 2 нед. При наличии выпота без клинической симптоматики нет смысла производить плевральные пункции и вводить те или иные лекарственные препараты.
Таким образом, можно отметить следующие показания для плевродеза:
1. Наличие субъективных симптомов плеврита (выраженная одышка, боли, кашель).
2. Наличие выпота, рефрактерного к современной химио- и гормонотерапии.
3. Наличие бронхиальной обструкции.
В табл. 2 представлены препараты, используемые в настоящее время для плевродеза.
Методика введения цитостатиков, их разовые и суммарные дозы, а также режим лечения:
| 1. Эмбихин 10–30 мг 1 раз в 7–14 дней, 3–4 введения, всего 40–120 мг. 2. Тиофосфамид 30–40 мг 1 раз в 7–14 дней, 3–4 введения, всего 120–160 мг. 3. Фторурацил 500–1000 мг 1 раз в 7 дней, 3–4 введения, всего 2000–3000 мг. 4. Блеомицин 15–30 мг 1 раз в 7 дней, 4–5 введений, всего 60–150 мг. 5. Адриамицин 30–40 мг 1 раз в 7 дней, 3–4 введения, всего 90–120 мг. 6. Цисплатин 50–60 мг 1 раз в 7 дней, 2–3 введения, всего 100–180 мг. 7. Митоксантрон (новантрон) по 20–25 мг, 2–3 введения. 8. Вепезид 100–150 мг 2 раза в 7 дней, 3–4 введения, всего 600 мг. 9. Тиофосфамид 30 – 40 мг + фторурацил 500 мг 1 раз в 7 дней, 3 введения. |
Эффективность внутриплеврального введения отдельных цитостатиков при раке легкого и молочной железы колеблется от 60 до 80%. В табл. 3 представлены данные РОНЦ им. Н.Н. Блохина РАМН по эффективности химиотерапии опухолевых плевритов [5].
Особого внимания заслуживают методы неспецифической терапии с использованием различных склерозирующих средств для получения химического серозита, склеивания плевральных листков и таким образом ликвидации выпота в плевральной полости. К этим веществам относятся тальк, хинакрин (акрихин), делагил и тетрациклин. Эффективность введения талька, акрихина, делагила достигает 55–60%, а тетрациклина – 80–70% [6–10].
Методика введения тетрациклина. Тетрациклина гидрохлорид наиболее эффективен в больших дозах (20 мг/кг или 1200–1600 мг -12–16 ампул по 100 мг). У больного под местной анестезией производят пункцию плевральной полости с введением тонкой силиконовой трубки, по которой с помощью вакуум-отсоса эвакуируют жидкость. После этого трубку зажимают и под рентгеновским контролем убеждаются, что легкое расправилось. В случае, если легкое не расправилось или имеется смещение средостения в сторону плеврального выпота, не следует вводить тетрациклин из-за возможности образования Тпанцирного легкогоУ. Поскольку введение тетрациклина может сопровождаться болевыми ощущениями, то его предварительно разводят в 50 мл 0,5% раствора новокаина и затем вводят в дренажную трубку. Последнюю прижимают на 2 ч, а больного просят несколько раз менять положение тела. Через 2 ч зажим снимают, а дренажную трубку подключают к вакуум-отсосу с постоянным давлением (от 15 до 20 см вод. ст.). Аспирацию продолжают не менее 24 ч, пока объем выводимой жидкости не будет менее 150–200 мл в сутки. После этого дренажную трубку удаляют.
Таблица 3. Эффективность химиотерапии опухолевых плевритов (данные РОНЦ)
Рак яичников является одной из наиболее частых злокачественных гинекологических опухолей и составляет 4-ю причину смертности от рака у женщин. Половина всех случаев заболевания приходится на возраст старше 65 лет. Приблизительно 5-10% рака яичников является семейным заболеванием в 3-х наиболее частых вариантах: только рак яичников, рак яичников и молочной железы, рак яичников и толстой кишки. В первую очередь прослеживается наследственность у родственников по 1-й степени (мать, дочь, сестра). Меньший риск существует для женщин 2-й степени родства (бабушка, тетя). При генетических исследованиях обнаруживаются мутации связей в локусе BRCA-1 хромосомы 17g21.
BRCA -2, также отвечающий за возникновение семейного рака яичников и рака молочной железы, расположен в хромосоме 13g12.
Для женщин, имеющих повышенный риск заболевания, старше 35 лет, имеющих детей, может рассматриваться вопрос о профилактической овариэктомии, однако ее значимость до сих пор окончательно не установлена. Описаны случаи заболевания после профилактической операции, первоначально начинающиеся с перитонеальных опухолевых разрастаний, подобных раку яичников.
Особенностью рака яичников являются распространение в брюшную полость путем имплантации клеток и локальная инвазия в мочевой пузырь и кишечник. Частота поражения лимфоузлов составляет 24% при стадии I, 50% — при II, 74% — при III и 73% — при IV стадии. Тазовые лимфоузлы вовлекаются так же часто, как и парааортальные. Опухоль путем трансдиафрагмального распространения может блокировать диафрагмальный лимфоотток, что является причиной асцита и плеврита.
Для больных с I стадией наиболее важна степень морфологической дифференцировки опухоли. Проточный цитометрический анализ ДНК при I и IIA стадиях может выявить группу повышенного риска.
Поскольку в ранних стадиях рак яичников является бессимптомной болезнью, он диагностируется главным образом в поздних стадиях, результатом чего является ранняя смертность примерно у 65% заболевших. При субоптимально операбельной III и IV стадиях 5-летняя выживаемость составляет менее 10% даже при использовании цисплатинсодержащих режимов химиотерапии.
После оптимальных операций при III стадии медиана выживаемости составляет 52-63 мес.
Классификация рака яичников (по FIGO)
I Опухоль ограничена яичниками
IA Опухоль ограничена одним яичником, асцита нет. Нет опухолевых проявлений на внешней поверхности яичника, капсула интактна.
IB Опухоль ограничена двумя яичниками, нет асцита. Нет опухоли на внешней поверхности, капсулы интактны.
IC Опухоль такая же, как в стадиях IA и IB, но с наличием опухоли на поверхности одного или обоих яичников, или нарушением капсулы, или имеется асцит, и/или обнаруживаются опухолевые клетки в перитонеальном смыве.
II Опухоль вовлекает один или оба яичника и распространяется в полость малого таза.
IIA Опухоль характеризуется распространением в матку и/или маточные трубы.
IIB Распространение на другие ткани малого таза.
IIC Опухоль такая же, как в стадиях IIA и IIB, но имеется опухоль на поверхности одного или обоих яичников, или отмечается разрыв капсулы, или асцит, и/или обнаруживаются опухолевые клетки в перитонеальном смыве.
IV Опухоль одного или обоих яичников с отдаленными метастазами. Плеврит с цитологически обнаруживаемыми опухолевыми клетками, паренхиматозные метастазы в печени.
Для диагностики и контроля над эффективностью лечения при эпителиальных опухолях используются такие опухолевые маркеры, как раково-эмбриональный антиген и опухолево-специфический антиген СА-125. Имеется высокая корреляция уровня СА-125 через месяц после 3 курса химиотерапии при III и IV стадиях и выживаемости. В случаях нормализации этого маркера в процессе лечения, повторное повышение маркера определяет активизацию процесса, хотя и не означает необходимость незамедлительного лечения.
Повышенный уровень СА-125 указывает на высокую вероятность рака яичников, в то же время отрицательный ответ не исключает наличие остаточной опухоли. Уровень СА-125 может быть повышен как при других злокачественных опухолях, так и при разных заболеваниях половых органов, например при эндометриозе.
Методы лечения зависят от стадии процесса. Ключевым моментом в лечении является операция. В отличие от других опухолей женских половых органов, стадия процесса при раке яичников устанавливается после хирургического вмешательства. Несмотря на то, что лишь незначительное число больных может быть излечено одной операцией, успех терапии определяется объемом первоначального вмешательства. Возможность достижения в последующем полной ремиссии, подтвержденной морфологически, зависит от размеров остаточных опухолей. Радикальной операцией при раке яичников считается двусторонняя овариосальпингэктомия с экстирпацией матки и удалением большого сальника. У молодых женщин, настаивающих на сохранении репродуктивной функции, при I стадии и 1-й степени злокачественности (G1) возможна односторонняя овариэктомия. Во время операции для уточнения стадии и морфологического варианта берут биопсию из латеральных каналов, тазовой брюшины и диафрагмы, связки, подвешивающей яичник, парааортальных, общих подвздошных, наружных и внутренних подвздошных лимфатических узлов, серозы прямой кишки и мочевого пузыря.
Тактика лечения
Больным с опухолями в IA-IB стадии с высокой или средней степенью дифференцировки (т.е. I-II степенью злокачественности G1 и G2) после операции не требуется дополнительного лечения.
При 3-й степени злокачественности (G3) IC стадии высока вероятность рецидива (до 20%), что требует дополнительных методов лечения.
Возможна системная химиотерапия; внутрибрюшинное введение радиоактивного фосфора 32Р или облучение брюшной полости малого таза. Однако введение 32Р оказалось более токсичным при одинаковой эффективности при сравнении с проведением 6 курсов цисплатина.
Экстирпация или надвлагалищная ампутация матки с придатками с резекцией большого сальника и удалением всех или большинства опухолей. При отсутствии видимых опухолей производят множественные биопсии и смывы из брюшной полости. Дальнейшее лечение включает:
-
При минимальных остаточных опухолях (
- Почему у онкологических больных возникает плеврит?
- Какие симптомы возникают при плеврите?
- Как диагностируют плеврит?
- Лечение плеврита при злокачественных опухолях
- Химиотерапия при экссудативном плеврите
- Что такое плевродез?
- Иммунопрепараты для плевродеза
- Эффективность лечения у онкологических больных с экссудативным плевритом
Плевритом называют воспаление листков плевры — тонкой оболочки из соединительной ткани, которая покрывает легкие (висцеральный листок плевры) и внутреннюю поверхность стенок грудной клетки (париетальный листок плевры).
Узкая щель между париетальным и висцеральным листками плевры называется плевральной полостью. В норме в ней содержится немного (10 мл) жидкости — она работает как смазка, уменьшая трение во время движений легких в процессе дыхания.
Существуют две разновидности плеврита:
- Экссудативный плеврит сопровождается скоплением в плевральной полости жидкости (такое состояние называют гидротораксом).
- При сухом плеврите на плевре образуются фибринозные наложения, она утолщается.
При онкологических заболеваниях чаще всего встречается первая форма — экссудативный плеврит.
Почему у онкологических больных возникает плеврит?
Существует много причин, из-за которых в плевре возникает воспаление. Например, плеврит может стать осложнением воспаления легких, сердечной недостаточности, цирроза печени и других заболеваний.
Основная причина плеврита при онкологических заболеваниях — метастазы раковых клеток в плевру и лимфатические узлы, которые находятся в грудной клетке. В итоге нарушается отток лимфы, повышается проницаемость стенок капилляров. Жидкость просачивается в плевральную полость.
Чаще всего плеврит возникает при раке легкого, молочной железы, яичников. Реже причиной становятся злокачественные опухоли желудка, толстой кишки, поджелудочной железы, мезотелиома плевры, меланома.
Какие симптомы возникают при плеврите?
Жидкость, которая скапливается в плевральной полости, сдавливает легкое, мешает ему расправляться. Чем больше объем жидкости, тем сильнее выражены симптомы плеврита:
- Слабость, плохое самочувствие.
- Невозможность глубоко вдохнуть, ощущение, что легкие расправляются не полностью.
- Сухой (иногда с небольшим количеством мокроты) кашель, который возникает из-за раздражения нервных рецепторов в плевре.
В дальнейшем все сильнее становится заметна одышка, возникает тяжесть в половине грудной клетки. Пациент старается лежать на больном боку (если плеврит носит односторонний характер), это позволяет здоровому легкому лучше расправляться.
Указанные симптомы могут быть вызваны и другими заболеваниями. Причины плеврита тоже бывают разными. Для точной диагностики обратитесь к врачу.
Как диагностируют плеврит?
Во время приема у врача вам нужно будет рассказать о ваших симптомах, о том, как и когда они возникли, как изменялись со временем. Доктор попросит перечислить заболевания, которые вы перенесли в течение жизни, особенно в последнее время. Затем будет произведен осмотр. Врач осмотрит и ощупает вашу грудную клетку, прослушает легкие и сердце при помощи фонендоскопа.
Рентгенография поможет выявить плеврит, оценить количество жидкости в грудной клетке, иногда — обнаружить метастазы опухоли в плевре и лимфатических узлах.
Компьютерная томография помогает более точно выявить причину, степень распространённости опухолевого плеврита и вызвавших его специфических изменений. В некоторых случаях врач может назначить УЗИ.
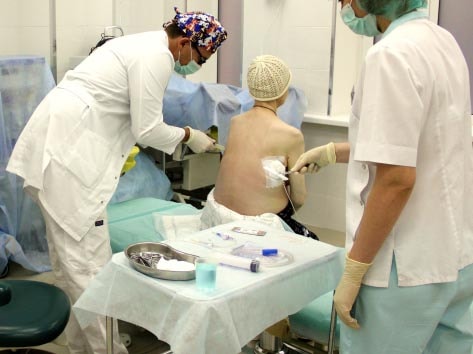
Обязательный метод диагностики — диагностическая плевральная пункция. Её проводят, если жидкости в плевральной полости не очень много, и нет состояния, угрожающего жизни. Врач вводит в грудную клетку иглу, получает некоторое количество жидкости и отправляет на исследование в лабораторию.
Если жидкости в плевральной полости много, и имеется состояние, угрожающее жизни, пациенту нужная срочная помощь. Проводят плевроцентез — процедуру, во время которой из грудной клетки удаляют как можно больше жидкости. Часть её отправляют на анализ.
Если после обследования диагноз остается неясен, врач-онколог и анестезиолог-реаниматолог могут принять решение о проведении видеоторакоскопии. В грудную клетку вводят специальный инструмент с видеокамерой — торакоскоп, — и осматривают грудную клетку изнутри. Во время видеоторакоскопии можно провести биопсию — получить фрагмент опухоли или подозрительного участка и отправить в лабораторию для изучения под микроскопом. Обычно после этого удается установить точный диагноз.
Лечение плеврита при злокачественных опухолях
В первую очередь при достаточно выраженном экссудативном плеврите нужно провести плевроцентез — эвакуацию жидкости из плевральной полости. Обычно, это помогает уменьшить одышку, боли, улучшить самочувствие и качество жизни пациента.
Плевроцентез проводят при помощи набора, в который входят:
- специальный шприц с коннектором,
- стерильный мешок для сбора жидкости,
- закрытая система, не пропускающая воздух,
- соединительная трубка.
Во время процедуры врач вводит раствор анестетика в межреберном промежутке на уровне, где находится жидкость, затем вводит иглу в плевральную полость и удаляет жидкость. В конце процедуры в плевральной полости оставляют катетер, соединенный с мешком, в который впоследствии постепенно оттекает жидкость.
Узнать подробнее о процедуре можно из отдельной статьи о плевроцентезе на нашем сайте.
В Европейской клинике, в отличие от многих других клиник, плевроцентез выполняют с помощью современного устройства Pleurocan (США) и исключительно под контролем ультразвука, что делает вмешательство максимально быстрым, эффективным и безопасным.
Врачи нашей клиники ежемесячно выполняют плевроцентез десяткам пациентов. Мы выполняем цитологическое исследование экссудата, вводим препараты интраплеврально, проводим комплексное лечение рака практически любых типов, локализаций, стадий.
Химиотерапия при экссудативном плеврите
Плевроцентез при экссудативном плеврите у онкологического больного — это симптоматическое лечение. Процедура помогает устранить сдавление легкого и улучшить состояние пациента, но не устраняет причину заболевания. После того как в лаборатории будут изучены раковые клетки, которые находятся в удаленном экссудате, врач-онколог определится с дальнейшей тактикой.
Если опухолевые клетки чувствительны к химиопрепаратам, назначают системную химиотерапию. По статистике, системная химиотерапия в сочетании с другими методами лечения помогает устранить плеврит примерно у 60% пациентов, чувствительных к химиопрепаратам.
Что такое плевродез?
Если после цитологического исследования жидкости из плевральной полости выясняется, что опухолевые клетки нечувствительны к химиопрепаратам, и если исчерпаны все виды системного лечения, прибегают к плевродезу — процедуре, во время которой листки плевры склеиваются, и между ними перестает накапливаться жидкость.
Существуют разные виды плевродеза (механический, химический, физический), при экссудативном плеврите у онкологических больных применяют химический. В плевральную полость вводят препарат, который склеивает листки плевры.
Для химического плевродеза применяют разные группы препаратов:
- Неспецифические склерозирующие препараты: антибиотики-тетрациклины, тальк. В настоящее время эти средства применяют редко, так как они плохо переносятся, после их введения возникают сильные боли.
- Цитостатики: блеомицин, доксорубицин, цисплатин, этопозид, 5-фторурацил и др. Эти лекарства относятся к группе химиопрепаратов, они способны уничтожать опухолевые клетки, но при экссудативном плеврите на первый план выступает их способность склеивать листки плевры.
- Препараты для иммунотерапии. Одновременно обеспечивают плевродез и уничтожают раковые клетки, которые находятся в плевре. Плевродез иммунопрепаратами при экссудативном плеврите у онкологических больных — наиболее прогрессивная методика. По некоторым данным, её эффективность достигает 90–94% (для других методов — редко выше 60%). Иммунотерапия эффективна при опухолях, устойчивых к химиопрепаратам, и после внутриплевральной химиотерапии. Основной и наиболее часто встречающийся побочный эффект данного вида терапии — лихорадка и состояние, напоминающее грипп, с которыми легко справиться при помощи нестероидных противовоспалительных средств (НПВС).
Иммунопрепараты для плевродеза
Перед введением иммунопрепаратов нужно, по возможности, удалить всю жидкость из плевральной полости, иначе иммунотерапия может быть неэффективна. Курс лечения в среднем составляет 14 дней (5 дней терапии, затем 2 дня перерыв — цикл повторяют дважды).
Препараты, которые применяют для иммунотерапии экссудативного плеврита:
- Рекомбинантный интерлейкин-2. Препарат вводят в дозировке 1 млн. МЕ ежедневно в течение 14-ти дней (десять рабочих дней). Метод эффективен примерно у 90% пациентов.
- LAK-клетки. Вводят по 50–100 млн. клеток ежедневно, обычно в течение пяти дней. Курс терапии продолжается 7 дней.
- Рекомбинантный интерлейкин-2 и LAK-клетки. Последовательно проводят 5 внутриплевральных введений рекомбинантного интерлейкина-2 в дозировке 1 млн. МЕ ежедневно, затем 5 введений LAK по 50–100 млн. клеток ежедневно. В среднем курс лечения продолжается 14 дней.
Во время курса лечения пациент постоянно находится под контролем медперсонала, получает поддерживающую терапию. После окончания курса пациента обследуют, затем показан перерыв 3–4 недели, затем — контрольное обследование.
Эффективность лечения у онкологических больных с экссудативным плевритом
Обычно врач-онколог отправляет жидкость, полученную из плевральной полости, на цитологическое исследование 3 раза:
- Перед началом лечения.
- Во время курса — обычно в середине.
- После завершения лечения.
В лаборатории экссудат изучают под микроскопом: определяют наличие опухолевых клеток, их количество и особенности строения. Для того чтобы оценить эффективность лечения онкологического заболевания и экссудативного плеврита, врач ориентируется на четыре основных показателя:
- Общее состояние пациента, изменение жалоб.
- Данные обследования.
- Скорость увеличения объема жидкости в плевральной полости.
- Изменение клеточного состава жидкости. Об успешном лечении говорит уменьшение количества опухолевых и преобладание лимфоидных клеток.
Диагностикой и лечением экссудативного плеврита при онкологических заболеваниях должен заниматься врач, который специализируется на данной патологии, в условиях специализированного стационара, где есть необходимое оборудование и препараты. В Европейской клинике есть всё необходимое.
Читайте также:

