Эпидемиология рака полости рта
Слизистая оболочка полости рта и подлежащие ткани представляют особую анатомическую сложность, обусловливающую специфику клинического течения и лечения развивающихся здесь опухолей. Злокачественные опухоли, возникающие в полости рта - это преимущественно различные виды плоскоклеточного рака. Среди злокачественных опухолей области головы и шеи рак органов полости рта по частоте занимает второе место после рака гортани.
Заболеваемость населения земного шара раком слизистой оболочки полости рта неравномерна, мировой стандарт составляет 9,7%ооо, в том числе у мужчин 6,4%ооо, соотношение мужчин и женщин почти 2:1, а смертность – 4,7%ооо.
В Республике Казахстан в 2005 году рак полости рта составлял 2,2% от общего числа заболевших злокачественными опухолями, составляя 3,8%ооо и занимая 18 ранговое место в структуре онкологической заболеваемости населения республики.
Рак органов полости рта развивается у мужчин в 5 – 7 раз чаще, чем у женщин. В Норвегии и Финляндии рак языка с одинаковой частотой встречается у мужчин и женщин, в то время как в Англии соотношение мужчин и женщин составляет 3:1, в США – 4:1, во Франции – 7:1. Наиболее часто болеют люди в возрасте 60 – 70 лет. Обычно в возрасте старше 80 лет. Однако рак органов полости рта нередко встречается у молодых людей, описаны заболевания у 4-летних детей.
Примерно 55% случаев рака органов полости рта локализуется на языке. Большинство авторов распределяет органы полости рта по частоте поражения в следующем порядке: язык, щека, дно полости рта, альвеолярный край верхней челюсти, альвеолярный край нижней челюсти, небо.
Среди злокачественных опухолей органов полости рта ведущее место занимают эпителиальные. Злокачественные опухоли полости рта эпителиального происхождения в большинстве случаев (90–95%) имеют строение плоскоклеточного ороговевающего рака. Другие виды рака встречаются значительно реже
Виды новооброзований челюстно-лицевой области.Эпидемиология
Международная классификация. Идея создания единой международной классификации рака с распространением по стадиям зародилась уже давно. Конкретная работа по созданию единой классификации и отчетности была начата в 1950 г. Подготовка проведена Комитетом по номенклатуре и статистике опухолей (Committee on Tumor Nomenclature and Statistics) под председательством Perry. С 1954г. Международный противораковый комитет взял на себя ответственность за разработку классификации и организовал специальный комитет под председательством профессора Р. Denoix. По настоящее время было 6 изданий разработанных и переработанных классификаций.
В основу классификации положена оценка трех элементов: первичной опухоли (Т), лимфатических узлов (N) и метастазов (М). Каждый из элементов системы ТNМ имеет несколько градаций, характеризующих степень распространения злокачественной опухоли.
В настоящее время практически все учреждения пользуются Международной клàссификацией опухолей по системе TNM 2002г.. Стадия рака устанавливается при первичном обследовании больного, а затем уточняется после операции (pTNM).
Классификация TNMрака кожи.
Клиническая (cTNM) и патоморфологическая (pTNM) классификации рака кожи идентичны.
Первичная опухоль (Т)
Tх - оценка первичной опухоли невозможна;
Т0 - первичная опухоль не обнаружена;
Tis - рак in situ;
Т1 - опухоль размерами 2 см и менее в наибольшем измерении;
Т2 - опухоль размерами 2,1-5 см в наибольшем измерении;
ТЗ - опухоль размерами более 5 см в наибольшем измерении;
Т4 - опухоль с поражением глубоких структур (хрящей, мышц или костей)
В случае множественных одновременных опухолей указывают максимальный показатель Т, а число опухолей указывают в скобках, например Т2(5).
Поражение регионарных лимфоузлов (N)
NX - состояние регионарных лимфоузлов оценить невозможно;
NO - метастазов в регионарных лимфоузлах нет;
N1 - метастазы в регионарных лимфоузлах имеются.
Отдаленные метастазы (М)
MX - наличие отдаленных метастазов оценить невозможно;
а) Эпидемиология рака полости рта и глотки. Практически все злокачественные новообразования полости рта и глотки представлены плоскоклеточным раком; заболеваемость, лечение и прогноз в целом сходны. Рак полости рта занимает 11 место в мире по количеству абсолютных случаев, рак глотки — двадцатое.
В сумме рак полости рта и ротоглотки является шестым по частоте встречаемости в мире. В 2000 году в мире отмечалось 389000 новых случаев, 2/3 из которых приходились на развивающиеся страны. Частота заболеваемости раком полости рта и глотки зависит от страны. Чаще всего им страдают жители Австралии, Франции, Венгрии, Южной Америки (Бразилии), южной Африки; реже всего болеют жители Мексики и Японии. Ежегодно от рака полости рта и глотки умирает около 200000 человек в мире.
Согласно приблизительным оценкам Американского онкологического общества, в 2008 году в США было зарегистрировано около 35310 новых случаев (25310 у мужчин, 10000 у женщин) рака полости рта (22900) и глотки (12410); около 7590 человек (5210 мужчин и 2380 женщин) умерли. В сумме они составляют около 2,5% всех злокачественных новообразований.
Из всех злокачественных заболеваний полости рта и глотки (за исключением опухолей слюнных желез и носоглотки) рак полости рта составляет 88%, рак глотки— 12%. Большая часть злокачественных новообразований полости рта поражает язык (43,1%), миндаликовые ниши (23,4%), губы (9,1%) и дно полости рта (7,8%). Также возможно поражение десен, неба, неуточненных участков полости рта.
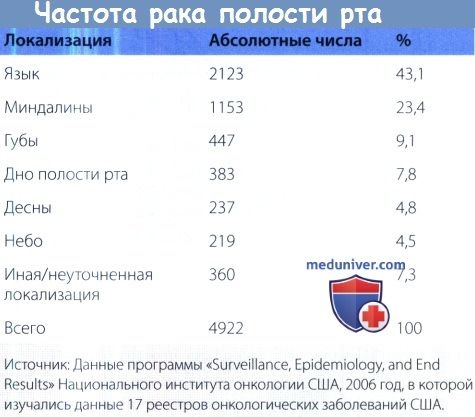
Встречаемость плоскоклеточного рака полости рта различной локализации.
Рак слюнных желез и носоглотки не учитывается.
Рак полости рта и глотки может встречаться в молодом возрасте. Среди всех пациентов, лица моложе 40 лет составляют 2,9%, моложе 50 лет— 16,2%. Заболеваемость увеличивается с возрастом и достигает максимальных значений в промежутке 70-79 лет. Далее заболеваемость у мужчин постепенно снижается, у женщин же она продолжает расти. Заболеваемость раком полости рта и глотки выше среди мужчин, чем среди женщин. Соотношение женщин и мужчин составляет 2:7 для рака полости рта, и 3:4 для рака глотки.
В течение последних 30 лет частота заболеваемости в США постепенно снижалась. Частота заболеваемости раком полости рта снизилась на 18,8% (с 8,7 на 10000 до 6,5% на 100000), рака глотки на 44% (с 1,8 до 1,0 на 100000). Но в отличие от рака других локализаций, заболеваемость раком языка среди американцев до 40 лет выросла почти на 60%. Рост продолжался вплоть до 1985 года, после чего заболеваемость сохраняется на одном уровне.
При тщательном обследовании пациентов с раком полости рта и ротоглотки примерно у 15% выявляется рак другой локализации, чаще всего гортани, пищевода или легких. Из пациентов, полностью излечившихся от рака полости рта и глотки, примерно у 10% впоследствии разовьется злокачественное новообразование одного из этих органов.
б) Факторы риска. Основными факторами риска рака полости рта и ротоглотки являются курение и употребление алкоголя. Являясь независимыми факторами риска, при сочетании они обладают синергетическим эффектом. По примерным оценкам курение является причиной 41% случаев рака полости рта и ротоглотки у мужчин и 15% у женщин во всем мире. Также, курение и алкоголь являются причиной 3/4 всех случаев рака полости рта в США.
По сравнению с некурящими людьми, у злостных курильщиков риск развития рака полости рта выше в 4-10 раз (после поправки на потребление алкоголя). После поправки на табакокурение, у лиц, употребляющих умеренные количества алкоголя, риск развития рака полости рта увеличивается в три раза, у злоупотребляющих алкоголем — в 8-9 раз. У алкоголиков и злостных курильщиков риск возрастает более чем в 35 раз. Снижение числа курящих лиц, предположительно, является причиной снижения частоты заболеваемости раком полости рта и ротоглотки в США.
У некоторых групп пациентов употребление бездымных табачных продуктов также является значимым фактором риска; увеличение риска рака и лейкоплакии полости рта так же велико, как и при табакокурении. У лиц, употребляющих нюхательный табак, новообразования чаще всего возникают на тех участках, где табак контактирует со слизистой щеки или десен.
Предполагается, что в Индии и Юго-Восточной Азии большинство случаев рака полости рта и глотки связаны с жеванием листьев бетеля. Впрочем, в США бездымные табачные продукты употребляют редко.
И хотя основными факторами риска рака полости рта и глотки являются употребление алкоголя и табака, семейный анамнез также играет определенную роль. У лиц, в семье которых имелись родственники со злокачественными новообразованиями полости рта и глотки, риск повышен в три раза (по сравнению с контрольной группой).
Предположительно, в основе заболевания лежит генетическая неполноценность механизмов репарации ДНК. После коррекции на возможные сопутствующие факторы, включая употребление алкоголя и табака, лица с отягощенным семейным анамнезом и с повышенной чувствительностью к мутагенам имеют в семь раз больший риск развития рака полости рта и глотки (по сравнению с нормальной контрольной группой). Это свидетельствует о том, что наследственность также играет роль в развитии заболевания.
Также одним из факторов риска является вирус папилломы человека (ВПЧ). Наибольшей канцерогенностью обладают ВПЧ 16 и 18 типов, их действие, по всей видимости, связано с мутацией гена, кодирующего белок ТР53. Общая частота инфицирования ВПЧ при опухолях полости рта в разных исследованиях варьирует от 14 до 91%. В тканях плоскоклеточного рака полости рта экспрессия ВИЧ повышена в четыре раза по сравнению с нормальной слизистой оболочкой.
Также, опухоли ротоглотки (особенно миндаликовых ниш) в три раза чаще оказываются ВПЧ-положительными, чем опухоли головы и шеи другой локализации. Тем не менее, точный характер связи между ВПЧ и новообразованиями полости рта, так же, как и сопутствующие факторы риска, до конца не установлены. Хорошо известно, что низкий уровень потребления овощей и фруктов также повышает риск развития рака полости рта и ротоглотки.
в) Ключевые моменты. В сумме рак полости рта и ротоглотки является шестым по частоте встречаемости в мире. Из всех злокачественных заболеваний полости рта и глотки (за исключением опухолей слюнных желез и носоглотки) рак полости рта составляет 88%, рак глотки— 12%. Большая часть злокачественных новообразований полости рта поражает язык (43,1%), миндаликовые ниши (23,4%), губы (9,1%) и дно полости рта (7,8%). Основными факторами риска является употребление алкоголя и табака.
А. И. Будовский
стоматолог-ортопед, частная практика (Санкт-Петербург)
В индустриально развитых странах рак занимает второе место после сердечно-сосудистых заболеваний как причина смерти [47]. Знание истории, распространенности, а также закономерностей его возникновения способствует лучшему пониманию этиологии, патогенеза, выработке наиболее оптимальных мер профилактики и лечения данного заболевания. Краткий исторический экскурс развития онкологии в контексте лечения опухолей области головы и шеи.
Исследование мумий и древних останков ставит серьезные вопросы о причинах возникновения, роста и развития раковых заболеваний (рис. 1) .
Рис. 1. Исследование мумии
Ученые Манчестерского университета, например, предположили, что рак вообще является современным заболеванием, вызванным антропогенными причинами, загрязнением окружающей среды, рационом питания [11, 13]. Эту теорию подтверждает тот факт, что при обследовании 100 мумий был выявлен только один случай установленного рака, сообщения в литературе античного периода о раке также крайне скудны [14]. При этом отмечается значительный рост числа раковых заболеваний в период индустриализации. Хотя данная теория представляется спорной, если учесть, что в древние времена 40 % популяции не доживало до 40 лет. То есть основная масса людей просто не жили достаточное время, чтобы получить рак [15].
Это же касалось и опухолей головы и шеи. На самом деле многие хирурги XIX века считали эти опухоли неизлечимыми заболеваниями. Описания хирургического лечения опухолей этой локализации появляются уже в начале 1800-х годов, но с большим количеством летальных исходов после такого лечения.
В 1840 году Купер (A. Cooper) обнаруживает присутствие раковых клеток опухоли груди в лимфатических сосудах и таким образом демонстрирует распространение рака.
Максимилиан фон Келиус (Maximillian von Chelius 1847) был одним из первых, кто осознал значимость метастазов в регионарные лимфоузлы.
В середине XIX века произошел огромный скачок в области хирургии головы и шеи.
Джон Коллинз Уоррен (John Collins Warren, 1778—1856), профессор анатомии и хирургии Гарвардской медицинской школы, руководитель хирургии и основатель Массачусетской больницы общей практики, оперирующий хирург, в главном госпитале Массачусетса (Massachusetts General Hospital) проводит удаление опухоли шеи под общим наркозом (рис. 2) .

Рис. 2. Robert Cutler Hinckley. Первая операция под эфиром, 1893. Холст, масло, 8′ х 10′
Что, в свою очередь, ознаменовало рождение современной анестезиологии.
Кстати, на этой же картине изображен Эбен Фрост (Ebenezer Hopkins Frost, 1824—1866), учитель музыки, получавший общую анестезию при экстракции зуба несколько ранее, 30 сентября 1846 года. Он в коричневом камзоле, стоит слева от оперирующего Уоррена.
В 1880 году Эмиль Теодор Кохер (Emil Theodor Kocher, 1841—1917) описывает Y-образный разрез для удаления лимфатических узлов шеи. Также он выступает за систематическое удаление не только основной опухоли, но и лимфатических узлов, что отличает его подход от подхода других ученых, описанного в более ранних публикациях Уоррена в 1837 году и фон Лангенбека (von Langenbeck) в 1875 году. Целью их было простое удаление опухолей. Благодаря выдающейся работе, выполняемой с 1885 г. по хирургии щитовидной железы, Эмиль Теодор Кохер стал лауреатом Нобелевской премии в 1910-м. Кстати, в 1913 г. он оперировал Крупскую Н. К.
Развитие науки в этот период идет параллельно накоплению опыта и работе практикующих хирургов.
Работу Потта продолжил Генри Батлин (Henry Butlin, 1845—1912), хирург госпиталя святого Бартоломью в Лондоне. Он провел исследование, в рамках которого установил, что случаи рака мошонки среди трубочистов континентальной Европы, Америки и даже Шотландии практически неизвестны. Рак кажется исключительно английским заболеванием. Это было связано с тем, что трубочисты других стран использовали защитную одежду.
Эти работы легли в основу получения экспериментального рака у кроликов японскими учеными в 1915 году: Katsusabur? Yamagiwa (1863—1930) и K?ichi Ichikawa (1888—1948).
Генри Батлина считают отцом британской школы хирургии в области головы и шеи [25].
В 1885 году в своей научной работе он представил серии клинических случаев хирургического лечения рака языка, где показал, что результаты лечения пациентов, перенесших резекцию подчелюстных лимфатических узлов, были лучше с точки зрения рецидивирования заболевания и выживаемости пациентов независимо от распространенности опухолевого процесса, чем у тех пациентов, у которых подобная операция не проводилась. В этой работе он активно выступал за профилактическое удаление лимфатических узлов при всех видах рака языка [21, 22, 25, 26, 28]. Генри Батлин представил свою историческую работу по раку языка в своей Хантеровской лекции в 1898 г.
Русский хирург М. Регульский (M. Regulskiy) подчеркивал в своей диссертационной работе в 1894 году необходимость удаления лимфатических узлов при раке нижней губы [28].
Первая книга по опухолям головы и шеи была опубликована Лейном в 1888.
Джордж Крайль в 1906 году публикует свою фундаментальную работу по методике иссечения регионарных шейных узлов, которая включила в себя 132 клинических случая.
Однако только к концу XVIII века рак начинают изучать систематически и интенсивно.
Развитие в области демографической статистики позволило в XIX веке изучить закономерности возникновения рака в различных странах. Уильям Фарр (William Farr, 1807—1883) в Англии в сотрудничестве с Марком Д’Эспе (Marc d’Espine) в Женеве разработали номенклатуру системы группировки болезней (Farr, 1975), которая легла в основу Международной классификации болезней.
В 1914 году появляется первая в мире Служба опухолей головы и шеи в Мемориальном онкологическом центре имени Слоуна — Кеттеринга (the Memorial Sloan Ketering Cancer Center), США.
Также большое влияние на дальнейшее изучение причин развития рака оказали труды Френсиса Рауса.
Американский ученый Фрэнсис Раус в 1911 г. доказал вирусную природу рака — саркомы Рауса. Лишь в 1966 г, спустя 55 лет, ему была вручена за это открытие Нобелевская премия по физиологии и медицине [4, 16].
Основателем российской онкологической школы можно по праву считать Н. Н. Петрова (1876—1964) (рис. 3) .

Рис. 3. Н. Н. Петров (1876—1964), основатель российской онкологической школы
Развитие онкологии подразделяют на четыре периода [12]. Работы Петрова Н. Н. и других известных ученых начала XX века (Л. А. Зильбер, М. Ф. Глазунов, Ю. М. Васильев, Н. А. Краевский и т. д.), формирование различных школ, таких как Рего (Regaud) в Париже, Бервена (Berven) в Стокгольме, Петрова в Ленинграде, Герцена в Москве, а также развитие и создание международных организаций открывают новейшую историю достаточно молодой науки.
За последние годы этого периода появилось множество открытий и исследований, посвященных генам, ответственным за появление и развитие различных опухолей. Возможно, именно эти работы будут в дальнейшем определять специфику диагностики, прогнозирования и лечения онкологических заболеваний [22].
Полный список литературы находится в редакции

это злокачественное новообразование, поражающее губы (чаще всего нижнюю губу), внутренние поверхности полости рта, а также заднюю стенку глотки, миндалины и слюнные железы. Заболевание чаще встречается у мужчин, как правило людей старше 40 лет.
Причины и факторы риска.
- Курение, в том числе жевание и нюхание табака.
- Употребление алкогольных напитков.
! При сочетании этих двух факторов - вероятность поражения ротовой полости возрастает.
- Мужской пол.
- Острые края пломбы, неудобный протез или другие факторы, оказывающие травмирующее действие на слизистую рта, могут привести к развитию раковой опухоли.
- Инфицирование полости вирусом папилломы, который относится к шестнадцатому типу, может быть причиной появления рака.
- Наличие красного плоского лишая слизистой полости рта плоский - угроза раковых образований.
- Ослабление иммунитета при системном приёме химических препаратов является фактором риска появлении онкологии.
- Неполноценное питание с недостаточным употреблением фруктов и овощей и дефицитом антиоксидантов – витаминов А, С и Е создаёт условия для роста раковых клеток.
- Частый контакт с асбестом способствует возникновению рака в полости рта. Такое же неблагоприятное влияние оказывают на человека полициклические органические соединения.
Клинические проявления.
- утолщение языка, что приводит к дискомфорту во время еды и разговора,
- онемение языка,
- онемение дёсен, некоторых зубов,
- выпадение зубов без видимой причины,
- отёк челюсти,
- боль в ротовой полости, которая принимает хронический характер,
- хроническое увеличение лимфатических узлов, расположенных в области шеи,
- изменение голоса,
- потеря веса,

- появление на губах или в полости рта образования, которое не проходит длительное время и имеет тенденцию увеличиваться в размерах, это может быть:
- красное пятно,
- беловатое пятно,
- язвочка,
- уплотнение,
- нарост.
! Эти явления могут и не быть раковыми образованиями, но переродиться в них с течением времени.
Образования проходят три фазы развития:
- Начальная ступень – человек замечает непривычные явления в состоянии здоровья ротовой полости. Случаются неясные боли, уплотнения, язвы в полости рта.
- Развитая стадия болезни — язвы становятся в виде щелей. Они могут располагаться над опухолью. Возникают болевые ощущения, которые могут отдавать в разные области головы. Раковая опухоль может развиваться и без выраженной боли.
- Запущенная ступень — заболевание активно разрушает окружающие ткани.
Формы рака полости рта (классификация по внешнему виду):
- Узловатая - во рту появляется уплотнение чёткой формы. Поверхность слизистой в этом месте либо не меняется, либо имеет белесоватые пятна. Новое образование обычно быстро увеличивает свои размеры.
- Язвенная - проявляется в виде язвы на слизистой оболочке. Она беспокоит пациента и долго не заживает. Патология в виде язвочки быстро прогрессирует. Такая форма рака ротовой полости поражает слизистые чаще других разновидностей.
- Папиллярная - выглядит как опухоль плотной структуры, которая свисает в полость рта. Покров слизистой внешне не изменяется.

(рак слизистой оболочки полости рта в начальной стадии)
Отдельные разновидности опухолей ротовой полости.
В зависимости от дислокации образования различают:
- Рак щёк - Дислокация образования часто на линии рта, на уровне его угла. Сначала может напоминать язвочку. Со временем возникают ограничения в открывании рта, дискомфорт при жевании и разговоре.
- Рак дна полости рта - Опухоль находится на мышцах донышка и может захватывать близлежащие зоны: нижнюю часть языка и в слюнные железы. Пациент жалуется на боль и усиление слюноотделения.
- Опухоль языка - Трудности, возникающие при жевании и дискомфорт во время пользования речевым аппаратом, иногда являются следствием онкологии языка. Опухоль дислоцируется на его боковых поверхностях – случаи такой патологии встречаются часто. Реже рак возникает на нижней поверхности языка или на его верхней части, затрагивает его корень или кончик.
- Опухоль в зоне альвеолярных отростков - Проблема может дислоцироваться на верхней и на нижней челюсти. Рак может поражать и зубы, что вызывает кровотечения и боли в этих местах.
- Рак в зоне нёба - В зависимости от того какая ткань подвергается заболеванию, появляется разная форма рака неба. Если охвачены мягкие ткани, то развивается рак, который называется плоскоклеточный. Твёрдое нёбо может иметь заболевание: цилиндрома, аденокарцинома, встречается и плоскоклеточный вид. Проблема обнаруживает себя появлением болей и дискомфорта во время приёма пищи.
- Метастазы:
- Раковое образование способно активно прорастать в рядом лежащие слои. Распространение опухоли зависит от её вида и локализации. Развитие заболевания происходит в продвижении раковых клеток в лимфатические узлы.
- Рак слизистой оболочки щёк и альвеолярных отростков нижней челюсти запускает метастазы в зону поднижнечелюстных узлов. Образования, возникшие в дистальных отделах, дают метастазы в узлы возле яремной вены.
- Рак языка, дислоцирующийся в районе его кончика и боковых поверхностей, прогрессирует в лимфоузлы шеи, а также может захватывать подчелюстные узлы.
- При патологии — рак ротовой полости встречаются, но нечасто отдалённые метастазы. Они распространяются во внутренние органы: печень, лёгкие, мозг, сердце, а также в костную ткань.
![]()
(рак дна полости рта)
Диагностика.
- Опухоль специалист определяет визуально.
- Лабораторный метод определения клинического анализа периферической крови позволяет оценить общее состояние больного и обнаружить анемию (малокровие), а при биохимическом анализе крови крови можно заподозрить поражение печени и костей.
- Степень разрастания болезни в мягкие ткани диагностируется методом пальпации и применением инструментальных методов визуализации:
- Биопсия – взятие кусочка ткани для исследования с целью подтверждения диагноза опухоли. Материал может быть получен в результате соскоба в области подозрительного участка, пункции тонкой иглой или хирургического удаления части опухоли.
- Рентгенография грудной клетки дает возможность выявить поражение легочной ткани, что встречается редко, но возможно при распространенном опухолевом процессе.
- Компьютерная томография (КТ), иногда с дополнительным введением контрастного вещества, помогает определить размер, форму и расположение опухоли, а также наличие увеличенных лимфатических узлов.
Лечение.
Существуют различные методы лечения раковой опухоли. Выбор способа зависит от стадии развития новообразования и его формы.
Хирургическое. Если нельзя обойтись без отсечения опухоли задействуют хирургическое вмешательство. После удаления образования могут проводиться манипуляции по восстановлению нарушенного внешнего вида пациента.

Химиотерапия. Применение лекарственных препаратов группы цитостатики (убивают раковые клетки) целесообразно в комбинации с облучением и/или с хирургическим вмешательством.
Профилактика развития рака ротовой полости.
- Лучший метод профилактики рака полости рта – это периодический осмотр своего рта и глотки. Помните, что выявление рака на ранней стадии позволяет надеяться на успех лечения!
- Необходимо расстаться с табакокурением и злоупотреблением алкоголя.
- Отказаться от жевания табака — постоянное использование бездымного табака повышает риск заболевания раком полости рта в 50 раз.
- Разумно избегать ультрафиолетовых лучей солнца, когда оно в зените.
- Подбирать рацион, богатый клетчаткой и антиоксидантами. Исключить приём очень острой и горячей пищи.
- Следить за полостью рта, чтобы не было травмирующего фактора (обломков зубов с острыми краями), разрушающего слизистую оболочку.
Люди, прекращающие использование табака даже после долгих лет курения и жевания, намного уменьшают риск заболевания раком полости рта.
Злокачественное новообразование представляет собой длительно незаживающую язву эпителиального слоя слизистой оболочки рта и ретромолярной области.
Анатомическое строение
Полость рта – это начальный отдел пищеварительного тракта, в котором пережевывается пища, вырабатывается слюна для переваривания пищи. Он задействован в процессе дыхания, глотания, артикуляции и речи.
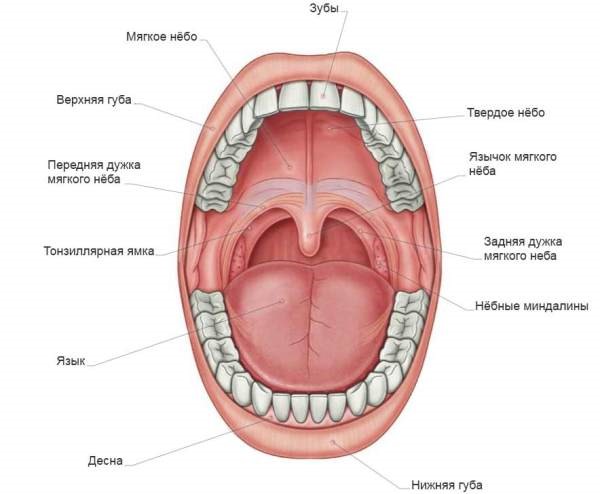
В состав ротовой полости входит:
- преддверие (губы, передняя сторона зубов, внутренняя поверхность щек);
- десны;
- дно, на котором лежит язык;
- две трети языка;
- зубы;
- позадимолярный треугольник – пространство на нижней челюсти позади третьего моляра;
- твердое и мягкое небо.
Классификация
Рак полости рта подразделяется на три вида:
- папиллярный. Узелок в слизистой оболочке увеличивается в размере и свисает в полость рта. Новообразование медленно прогрессирует;
- инфильтративный. Уплотнение на розоватой слизистой отличается белесым цветом, четкими контурами и формой, истончением оболочки вокруг. При пальпации со стороны щеки чувствуется плотный инфильтрат. Опухоль склона к быстрому росту. Больной жалуется на невыносимую боль;
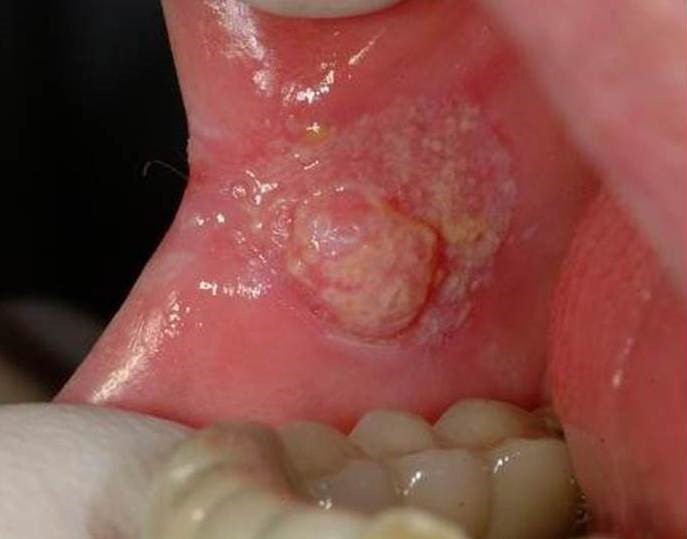
- язвенный. Наиболее распространенная форма заболевания. Язвочки на слизистой не заживают, разрастаются, а кайма вокруг них краснеет. Контур рваный, а его края кровоточат.

Метастазы опухоли появляются быстро. Злокачественные клетки прорастают в подбородочные, подчелюстные, глубокие яремные лимфатические узлы. На этот процесс влияет толщина и глубина опухоли. Так, при углублении новообразования на 4-5 мм метастазы возникают в 98% случаев. На Т1-стадии онкологии метастазирование выявляется в половине случаев, а при достижении Т4-стадии отдаленное распространение раковых клеток наблюдается в 85% случаев.
Классификация TNM
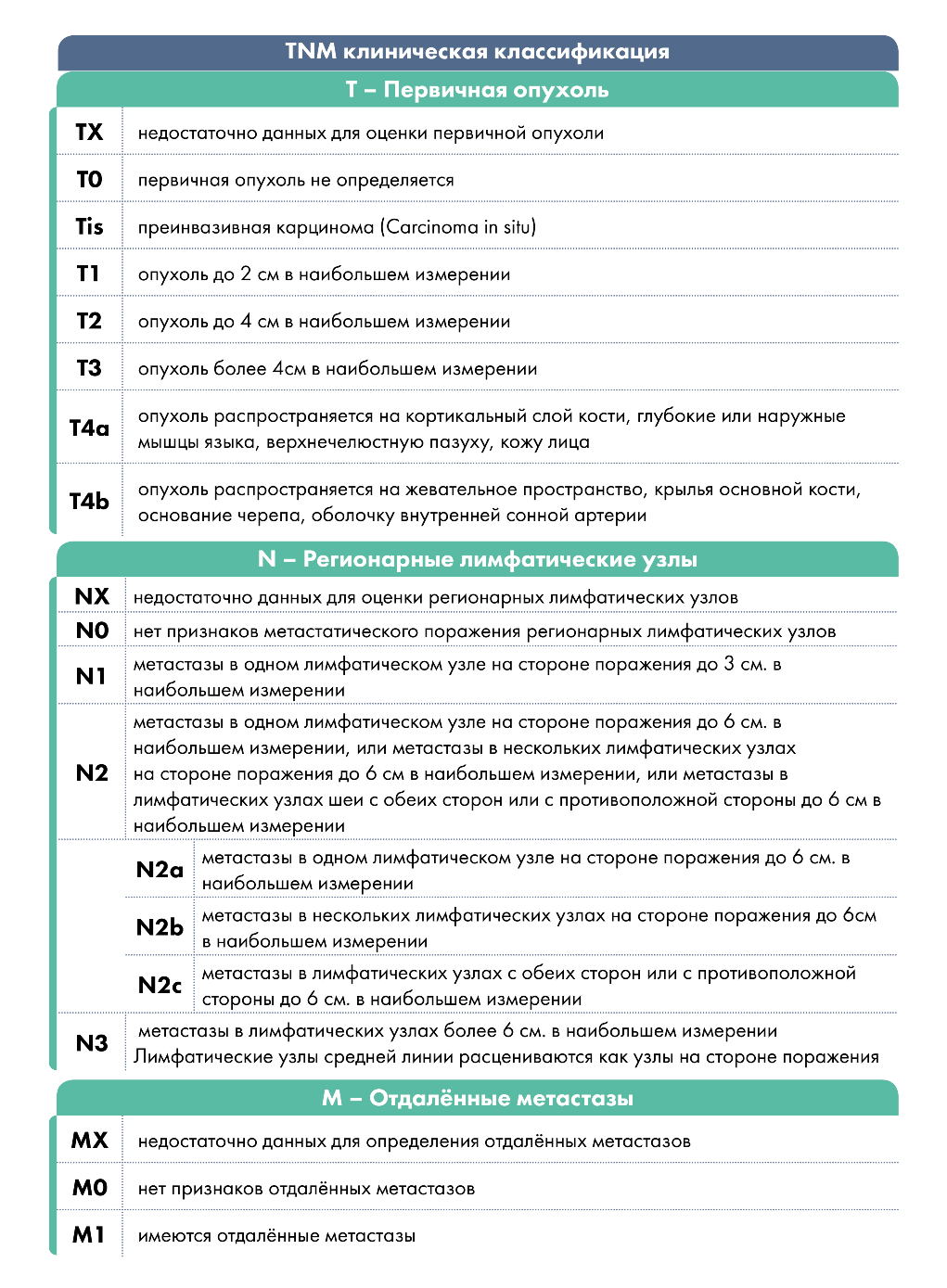
Причины возникновения
Распространенность рака полости рта растет и на сегодняшний день диагностируется у 2% больных среди общего числа заболевших. Начиная с 2009 года, заболеваемость выросла на 25%, при этом в основном выявляется плоскоклеточный рак и только в единичных случаях – аденокарцинома.
Большинство очагов онкологии наблюдается на языке. Чуть меньше злокачественных образований на дне полости рта. Рак мягкого и твердого неба, десен и щек выявляется в 20% случаев. Гораздо реже диагностируется поражение альвеол нижней челюсти – 4%, дужек неба, ретромолярной области и преддверия – 3%.
Исходя из практики, онкологии полости рта больше подвержены мужчины, чем женщины. Это связано с вредными привычками, например, злоупотребление сигаретами или разжевывание тонизирующих смесей усиливает выработку слюны, которая вымывает полезные элементы со слизистой. В группу риска входят больные ВПЧ, пожилые люди, работники вредных производств, больные красным плоским лишаем, люди, у которых систематически травмируется слизистая рта пломбой, протезом, металлическими предметами.
Симптомы
Идентифицировать злокачественную язву от обычного стоматита во рту можно по отеку и припухлости щек, болезненности и постоянному дискомфорту даже в состоянии покоя. Насторожить должно длительное незаживление раны и ее кровоточивость.
По мере развития заболевания признаки усиливаются:
- отек нарастает и распространяется на шею;
- усиливается красное или белое пятно на слизистой рта;
- неприятные ощущения при пережевывании и глотании;
- трудности при разговоре из-за трения слизистой о зубы при движении челюсти;
- появление неприятного запаха изо рта;
- чувство инородного предмета в горле;
- анемия рта.
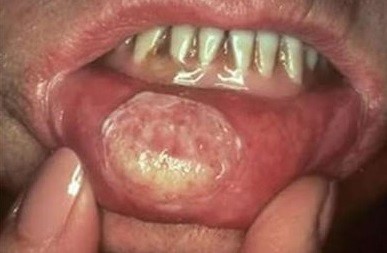 | 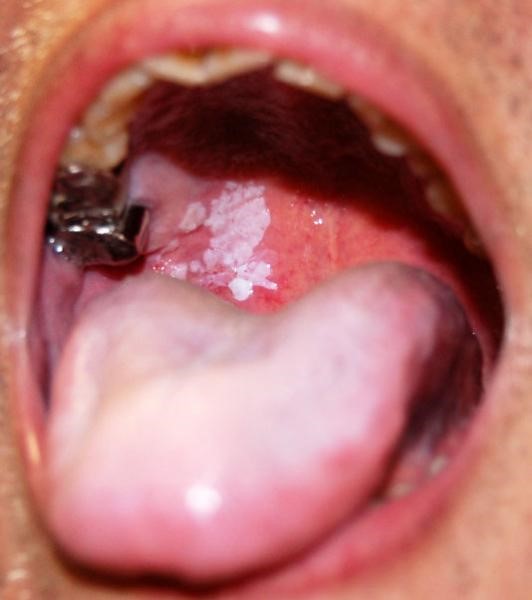 |
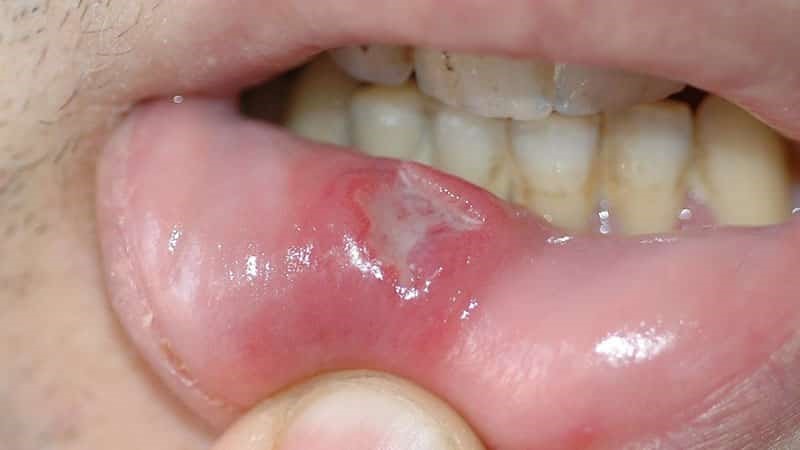 |
На поздней стадии рака выпадают зубы, стремительно снижается масса тела.
Диагностика
На первичной консультации врач осматривает полость рта, рассматривает язвы, эрозии, повреждения слизистой, а затем берет мазок для исследования. Для подтверждения воспалительного процесса больной направляется на общий и биохимический анализ крови.
Диагноз подтверждается по результатам обследования:
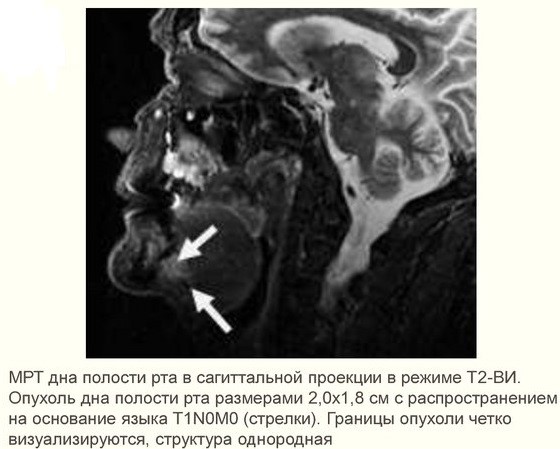
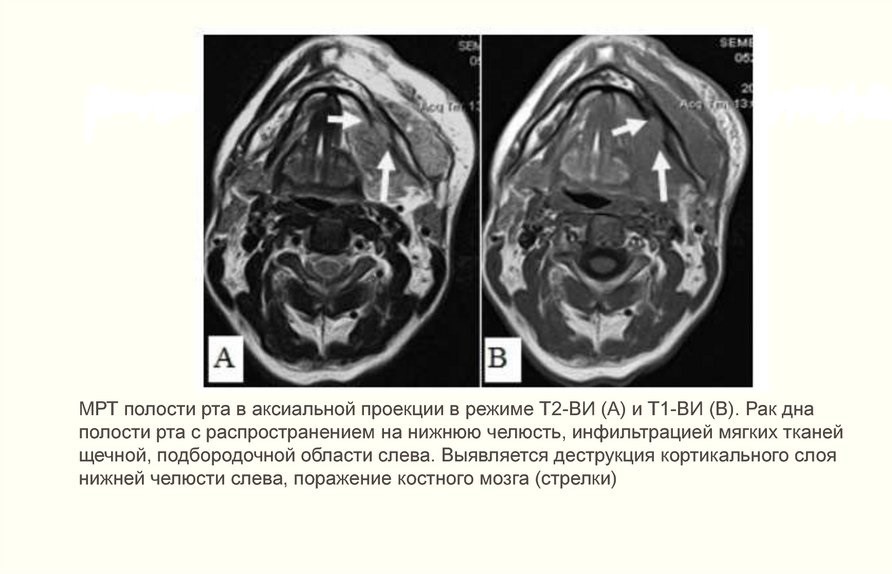
- при подозрении на метастазы проводится аспирационная биопсия тонкой иглой лимфатических узлов под подбородком, под челюстью и в верхней трети шеи;
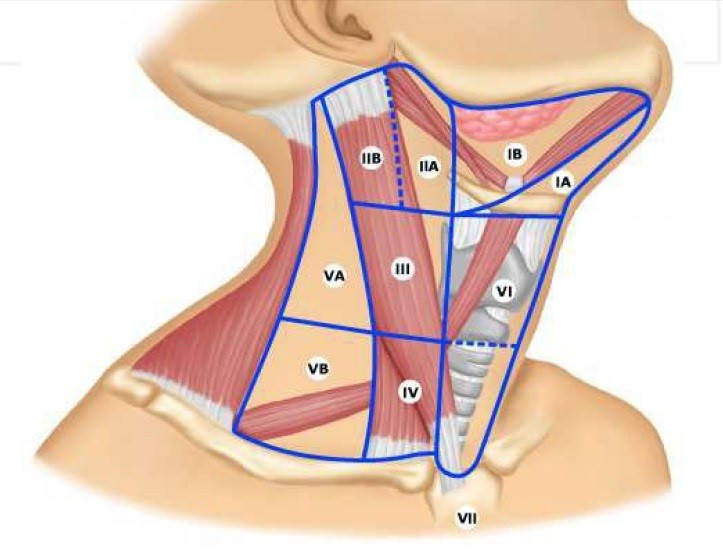
- позитронно-эмиссионная томография. Показывает глубину залегания опухоли, а также ранние метастазы;
- остеосцинтиграфия. Исследуются кости скелета для поиска перемещенных раковых клеток;
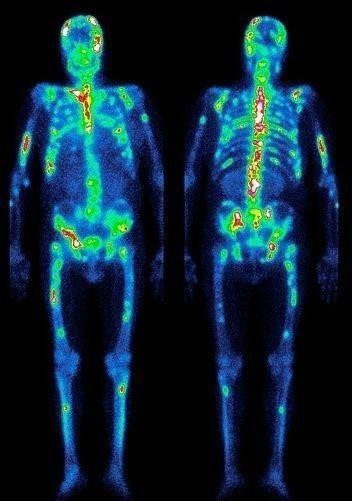
- КТ костей лица с контрастом. Снимки показывают прорастание опухоли в шейные сосуды, челюсть или основание черепа.
Лечение
Выбор тактики лечения зависит от стадии и распространенности новообразования. При быстром разрастании опухоли методы терапии комбинируются.
Принцип хирургического вмешательства врач определяет после определения стадии опухоли и ее распространения. Если раковые клетки проникли в надкостницу и окружающие ткани, проводится клиновидная, плоскостная или сагиттальная резекция челюсти. Если при обследовании выявлено прорастание раковых клеток напрямую в кость или дефект замечен уже во время операции, осуществляется сегментарная резекция нижней челюсти. Врач на месте оценивает поражение и определяет толщину иссекаемого слоя.
Следующий этап операции – это частичное или полное иссечение шейных лимфатических узлов для предотвращения метастазов при условии толщины опухоли более 4 мм или расположении очага опухоли в дне полости рта или на языке. Если новообразование расположено на срединной линии, то шейные лимфатические узлы иссекаются с двух сторон. Операция завершается одномоментным замещением поврежденных тканей.
После удаления опухоль отправляется на гистологическое исследование. Оценивается ее размер, толщина, глубина, края. На дальнейшее лечение влияет прорастание клеток за границы капсулы удаленного лимфатического узла, расхождение раковых клеток на соседние органы.
Облучение после операции назначается при диагностировании Т3, Т4, N2, Т3 стадий болезни не позже чем через шесть недель после удаления опухоли. Необходимость в лучевой терапии возрастает при периневральной инвазии в лимфатических сосудах. Суммарная очаговая доза за все сеансы – 60 гр, а разовая очаговая доза за один сеанс – 2 гр. При выявлении метастазов на шее СОД повышается до 66 гр, а при отсутствии риска метастазирования СОД уменьшается до 50 гр.
В качестве основного лечения лучевая терапия используется в суммарной очаговой дозе 60-70 гр. Процедура проводится пять дней в неделю, при этом она комбинируется с химиотерапией. Каждые три недели вводится 100 мг цисплатина.
Противоопухолевые препараты назначаются перед хирургическим вмешательством или одновременно с лучевой терапией для уменьшения размера новообразования. Иногда терапия назначается одновременно с операцией.
Лечение предполагает использование схемы 5-фторацила вкупе с цисплатином или иные средства – карбоплатин, метотрексат, блеомицин. Они вызывают ряд побочных явлений, например, рвоту или тошноту, выпадение волос, снижение аппетита, повышение кровоточивости. Симптомы исчезают после прохождения курса лечения, но после приема цисплатина иногда фиксируется стойкое нарушение слуха.
Прогноз рака полости рта зависит от стадии, на которой выявлена болезнь. Если лечение начато на нулевой стадии, то болезнь купируется. Стоит отметить, что курение провоцирует рецидив или перерождение опухоли, поэтому может потребоваться повторная операция или облучение. Оперирование на первой стадии повышает выживаемость до 80-85%, а комбинация лучевой терапии с операцией на второй стадии на 60-80%. Уже на последующих стадиях развития рака выживаемость не более 50%, при этом применяются все три метода лечения одновременно.
Диспансерное наблюдение
Поскольку опухоль может рецидивировать и дать метастазы, после пройденного курса лечения больной встает на учет в онкодиспансер. Первый год следует посещать врача каждый месяц, второй год профилактический осмотр проводится каждые 4-6 месяцев, а далее раз в год или при каких-либо недомоганиях. Осмотр предполагает прохождение обследования – УЗИ и контрастное МРТ мягких тканей шеи, ПЭТ, остеосцинтиграфию. Обязательна консультация отоларинголога, стоматолога и онколога. Доктор может сократить срок диспансеризации при высоком риске рецидива.
Список литературы по теме:
Читайте также:


