Что такое бфт в онкологии
Онкологические заболевания в современном мире встречаются все чаще. Это связано с особенностями экологии, множеством новых вирусов, а также с большим количеством канцерогенов. Ежегодно ученые вводят новые методы борьбы с раком. Однако прежние способы лечения применяются до сих пор. Одним из них является ПХТ. Расшифровка этой аббревиатуры – полихимиотерапия. Системное введение цитостатических препаратов помогает устранить атипичные клетки, из которых состоит опухоль. Несмотря на то что данный вид лечения нелегко переносится пациентами, он является одним из самых эффективных методов.
ПХТ в онкологии: расшифровка аббревиатуры
В медицинской документации людей, страдающих от раковых заболеваний, часто встречается такое понятие, как химиотерапия. Сокращенно ее называют ПХТ. В онкологии расшифровка данной аббревиатуры - полихимиотерапия, что означает сочетанное воздействие сразу нескольких цитостатических средств. Данный вид лечения направлен на полное устранение опухоли или ее уменьшение.
В большинстве случаев ПХТ сочетают с другими методами лечения. Среди них – хирургическое удаление патологического образования и лучевая терапия. Иногда полихимиотерапия является самостоятельным методом лечения. Выбор ПХТ зависит от расположения и стадии рака, а также от состояния больного. Назначать цитостатические препараты может только врач-онколог.
Виды химиотерапии в онкологии

Противоположным понятием является адъювантная ПХТ в онкологии. Расшифровка аббревиатуры проста. АПХТ – это профилактическое лечение рака после операции. Имеется в виду, что саму опухоль полностью удалили, однако для предотвращения рецидива требуется цитостатическая терапия. Перечисленные виды ПХТ относятся к комбинированному или комплексному лечению злокачественных опухолей. То есть, помимо назначения препаратов, пациенту проводится операция, а иногда – и облучение.
Отдельным видом терапии является самостоятельный (лечебный) курс ПХТ в онкологии. Расшифровка подобного медицинского термина понятна не каждому врачу. Зачастую отличить лечебный курс от профилактической терапии может только онколог. Самостоятельная ПХТ проводится в тех случаях, когда другие методы оздоровления не показаны. Например, при мелкоклеточном раке легкого или наличии метастазов в отдаленные органы.
Показания к проведению терапии
Стоит отметить, что каждая злокачественная опухоль лечится по-разному. Иногда достаточно только оперативного лечения или облучения, в других случаях – требуется химиотерапия. ПХТ назначают лишь по специальным медицинским показаниям, когда это необходимо. Если подобное лечение не было предложено после операции врачом, значит злокачественный процесс был ограничен небольшим участком и не поразил глубокие слои органа. Кроме того, некоторые типы опухолей не поддаются химиотерапии. Выделяют следующие показания для ПХТ в онкологии:
- Злокачественные образования лимфоидной ткани.
- Рак крови.
- Опухоли пищеварительного тракта.
- Мелко- и крупноклеточный рак легкого.
- Новообразования головы и шеи.
Следует отметить, что эффективность химиотерапии зависит от гистологического типа опухоли. К примеру, железистый рак поддается цитостатическому лечению лучше, чем плоскоклеточная карцинома или саркома. Зачастую ПХТ не назначают на первых стадиях болезни, если опухоль можно удалить оперативным путем. Адъювантная терапия показана пациентам, у которых после хирургического лечения была обнаружена 2 или 3 стадия рака. Если опухоль имеет большой размер и проросла в соседние органы, назначают самостоятельный курс ПХТ. Иногда данный вид лечения применяется на поздней стадии рака, когда другие методы бессильны.
Что такое курс химиотерапии?
Большинство людей знает, что химиотерапию принято назначать курсами. Это означает, что цитостатические средства вводятся в организм неоднократно, а на протяжении длительного времени - с определенными промежутками. Подобная схема лечения необходима, потому что препараты разрушают не только саму опухоль, но и другие клетки организма. Введение большой дозы единовременно невозможно, так как цитостатики обладают кардио-, нефро- и гепатотоксичным действием. Чтобы организм восстановился после курса ПХТ, требуется время. В среднем это занимает 2-4 недели. За этот период клетки крови успевают обновиться, и общее самочувствие пациента приходит в норму.
Количество курсов ПХТ в онкологии может быть различным. Оно зависит от переносимости препаратов, состояния больного и эффективности лечения. После 3 курсов проводится обследование, благодаря которому врач делает соответствующее заключение. Если опухоль полностью исчезла или частично уменьшилась, химиотерапию продолжают. В случаях, когда имеется прогрессирование злокачественного процесса, схему ПХТ меняют. При этом отсчет курсов начинается заново.
Подготовка и сопроводительная терапия
Противопоказания к назначению химиотерапии
Несмотря на то что химиотерапия относится к одним из самых эффективных методов лечения рака, ее проведение не всегда необходимо. В некоторых случаях цитостатические средства приносят больше вреда, чем пользы. Проведение ПХТ противопоказано в следующих случаях:
- Старческий возраст (от 70 лет).
- Непереносимость цитостатических средств.
- Наличие тяжелых патологий со стороны сердца.
- Почечная и печеночная недостаточность.
- Прогрессирование заболевания, несмотря на проводимую терапию.
- Наличие множественных метастазов.
- Кахексия.
Перед тем как назначить ПХТ, проводится комплекс обследований. К ним относятся: общий и биохимический анализ крови, ЭКГ, ОАМ, коагулограмма, УЗИ сердца. При выявлении декомпенсированных заболеваний лечение цитостатиками нецелесообразно.
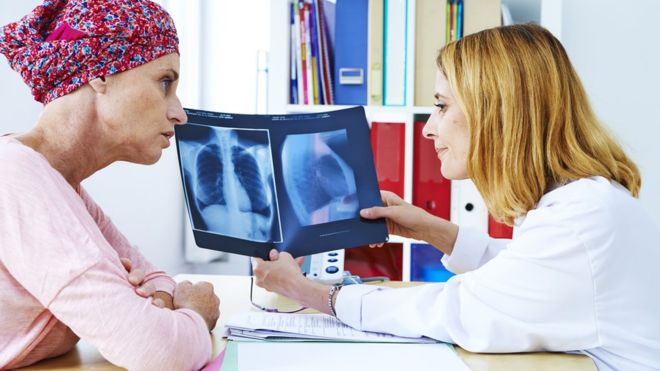
Возможные результаты химиотерапии
Для контроля эффективности ПХТ проводится повторное обследование. Благодаря этому оценивается результат терапии. К благоприятным исходам лечения относятся: полный и частичный регресс опухоли, а также стабилизация. В первом случае новообразование исчезает или уменьшается в размере в 2 раза и более. Стабилизация процесса означает, что опухоль осталась прежней. Однако это расценивается как положительный результат, ведь без лечения рак быстро прогрессирует.
Если при обследовании выявлено, что злокачественное образование растет, или появились метастазы, схему лечения меняют. При удовлетворительном состоянии пациента количество курсов химиотерапии неограниченно. Однако постоянное прогрессирование служит показателем того, что лечение не приносит результата, а только вредит организму. Это служит противопоказанием для назначения ПХТ.

Список лекарственных средств
Паллиативная химиотерапия (ПХТ)

Радикальные методы лечения поздней стадии онкологического заболевания не всегда бывают доступны. В этом случае врачи часто назначают медикаментозную терапию в виде паллиативной химиотерапии (ПХТ). Такое лечение не устраняет причину заболевания, но позволяет значительно облегчить состояние пациента. Разработаны различные схемы ПХТ, необходимые для терапии определенных форм злокачественных новообразований. Консультация онколога может пациенту получить больше информации о таком лечении.
Химиотерапией называют основной медикаментозный метод лечения злокачественных новообразований, основанный на применении противоопухолевых препаратов. Введение специальных медикаментов позволяет уменьшить размер опухоли и остановить распространение болезни в организме, однако химиотерапия редко помогает полностью избавиться от патологии. Как и лучевая терапия, противоопухолевое лечение обычно назначается после оперативного вмешательства. При терминальных стадиях, когда опухоль распространяется на другие органы, онкологи чаще назначают паллиативное лечение (ПХТ) в качестве основного метода.
Механизм действия любой формы химиотерапии, включая ПХТ, зависит от назначаемых препаратов. Одни лекарственные средства непосредственно разрушают аномальные клетки, а другие способны лишь остановить рост опухоли. Существенным недостатком такого лечения является отсутствие абсолютной селективности: лекарственные вещества также воздействуют и на здоровые ткани, что становится причиной осложнений. Тем не менее особенности деления и метаболизма злокачественных клеток делают их более легкой мишенью для противоопухолевых средств. Кроме того, ученые постоянно разрабатывают новые высокоселективные медикаменты.
Особым преимуществом ПХТ в онкологии является высокая доступность. Хирургическое лечение может быть нецелесообразным из-за неоперабельного расположения опухоли, наличия метастазов и высокого риска осложнений, однако химиотерапия почти всегда доступна даже на поздних стадиях болезни. В отличие от хирургии, медикаментозное лечение не требует полного удаления поврежденного органа и не вызывает обширную травматизацию тканей.
Как уже было сказано, ПХТ может иметь разные формы влияния на заболевание. Подбор медикаментов зависит от цели терапии, формы онкологического заболевания и состояния пациента. Обычно онкологи назначают несколько препаратов для улучшения терапевтического эффекта.
Основные виды препаратов:
- Цитотоксические лекарственные средства, нарушающие внутриклеточные процессы. Главным представителем этой группы являются антиметаболиты, по своей химической структуре напоминающие внутриклеточные протеины. Проникновение таких химических соединений в опухолевую ткань обуславливает разрушение клеток.
- Цитостатические лекарственные средства, необходимы для предотвращения дальнейшего роста злокачественного очага. Это алкилирующие препараты, растительные алкалоиды и противоопухолевые антибиотики, поражающие внутриклеточную ДНК. Такие медикаменты нарушают процесс деления клеток.
Различные схемы ПХТ предусматривают назначение комбинированной терапии, в которой представлены цитостатические и цитотоксические лекарства. Также в схемах учитывается количество циклов лечения, порядок и кратность приема лекарственных средств. Использование сразу нескольких видов химиотерапии показывает большую эффективность, чем назначение одного препарата в качестве монотерапии.
Онкологические заболевания характеризуются прогрессирующим течением. Изначально опухоль формируется из аномальных клеток определенной ткани и растет в пределах определенной области. Постепенно рост патологии затрагивает все более глубокие ткани, что приводит к распространению опухоли на соседние структуры. Проникновение злокачественных клеток в лимфатическую ткань и кровоток постепенно приводит к формированию вторичных опухолей (метастазов) в отдаленных органах. На этой стадии радикальное лечение, как правило, недоступно, поэтому главной формой терапии является облегчение состояние пациента.
Медикаментозная терапия в виде ПХТ также необходима для улучшения качества жизни онкологического больного. Введение противоопухолевых препаратов помогает устранить некоторые осложнения заболевания, включая отеки, воспалительные процессы и болевой синдром. При этом врачу необходимо учитывать влияние побочных эффектов химиотерапии, поскольку такое лечение само по себе может значительно ухудшить состояние больного. Таким образом, курс ПХТ на поздней стадии онкологии назначается только в том случае, если позитивный эффект химиотерапии перекрывает ее побочные эффекты. Часто такой метод паллиативного лечения позволяет увеличить срок жизни пациента.
Другие виды паллиативной помощи:
- Назначение обезболивающих препаратов для устранения болевого синдрома.
- Проведение психотерапии с назначением антидепрессантов и анксиолитиков.
- Терапевтическое и хирургическое лечение осложнений онкологии.
Грамотное совмещение паллиативной химиотерапии с другими видами медицинской помощи позволяет значительно облегчить тягостные симптомы болезни.

Любая форма терапии злокачественного новообразования может быть назначена только после проведения тщательной диагностики, что также касается и ПХТ. Химиотерапия является сложной медицинской процедурой, характеризующейся высоким риском возникновения побочных эффектов, поэтому врачу необходимо сразу исключить наличие противопоказаний. Перед проведением лечения проводится консультация с целью уточнения состояния больного. Онколог спрашивает пациента о жалобах, изучает анамнестические данные и проводит физикальное обследование. Для подтверждения диагноза требуются результаты инструментальных и лабораторных исследований.
- Рентгенография, компьютерная и магнитно-резонансная томография – высокоточные методы визуального обследования внутренних органов, с помощью которых врач может установить область локализации патологии и определить стадию болезни.
- Ультразвуковое обследования – способ визуализации внутренних органов, подразумевающий использование высокочастотных звуковых волн. Во время обследования врач может видеть структуру пораженного органа на экране.
- Эндоскопическое исследование полостных органов с помощью гастроскопии, колоноскопии, бронхоскопии и других процедур.
- Биопсия – забор небольшого участка злокачественного новообразования с последующим гистологическим исследованием материала. Микроскопирование клеток позволяет уточнить форму патологии и стадию болезни, что очень важно для назначения ПХТ.
- Анализ крови для обнаружения онкологических маркеров, свидетельствующих о наличии патологического процесса в том или ином органе.
- Лабораторные тесты печени, почек и других органов для оценки общего состояния организма.
После получения всех необходимых результатов врач назначает определенную схему противоопухолевой терапии.
Несмотря на то, что химиотерапия подчас является менее агрессивным методом лечения онкологии, чем оперативное вмешательство, нельзя не учитывать степень негативного влияния противоопухолевых препаратов на здоровые клетки. Даже самые высокоселективные препараты могут нарушать функции внутренних органов. Степень проявления побочных эффектов зависит от индивидуальной восприимчивости организма пациента. Для уточнения возможных рисков врачи ориентируются на противопоказания.
Абсолютные и относительные противопоказания к медикаментозному лечению:
- Тяжелая степень почечной или печеночной недостаточности.
- Непроходимость желчных путей.
- Аллергическая реакция на лекарственные средства.
- Выраженные патологии сердца и сосудов.
- Тяжелая онкологическая кахексия.
- Острый дефицит эритроцитов и гемоглобина в крови (анемия).
- Невосприимчивость опухолевых клеток к химиотерапии.
- Острая стадия системных воспалительных и инфекционных заболеваний.
Назначение противоопухолевой терапии при наличии перечисленных противопоказаний может вызвать жизнеугрожающее осложнение, в то время как основной целью паллиативного лечения является облегчение состояния пациента.
Состояние после ПХТ обычно отягощается возникновением негативной симптоматики, обусловленной влиянием цитостатических и цитотоксических препаратов на здоровые клетки. К самым распространенным побочным эффектам химиотерапии относят:
- Выпадение волос и ломкость ногтей.
- Тошноту и рвоту.
- Дефицит тромбоцитов и лейкоцитов в крови.
- Слабость и усталость.
- Потерю аппетита.
- Подавление функций иммунитета.
Таким образом, паллиативное лечение (ПХТ) онкологических заболеваний подходит далеко не всем пациентам. Для уточнения всех необходимых деталей и прохождения обследования необходимо обратиться к онкологу.
Химиотерапия в широком смысле — это воздействие токсичными препаратами на причину заболевания, коей могут являться болезнетворные микроорганизмы, паразиты или раковые клетки. Антибиотики и противоглистные препараты — это тоже химиотерапия. Но чаще всего этот термин применяют по отношению к препаратам, предназначенным для борьбы со злокачественными опухолями.
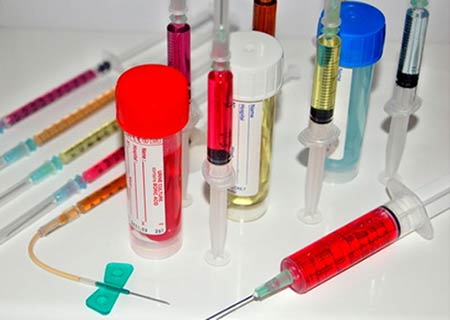
Химиотерапия вместе с хирургией и лучевой терапией входит в классическую тройку лечения онкологических заболеваний.
Как работают химиопрепараты?
Раковые клетки отличаются от здоровых способностью к бесконтрольному делению. Существуют разные группы химиопрепаратов с разными механизмами действия, но суть их работы всегда сводится к тому, что они поражают быстро размножающие клетки — не только раковые, но и здоровые, поэтому для химиотерапии зачастую характерны серьезные побочные эффекты.
Все химиопрепараты делят на две большие группы. Цитостатические (цитостатики) останавливают клеточное деление. Раковые клетки не могут размножаться, в них запускается механизм запрограммированной клеточной гибели — апоптоз. Цитотоксические препараты непосредственно вызывают гибель опухолевых клеток.
Назначением химиотерапии занимается онколог или более узкоспециализированный врач — химиотерапевт. Выбор препаратов зависит от некоторых факторов:
- Тип рака и его молекулярно-генетические характеристики. Разные опухоли чувствительны к разным лекарствам.
- Стадия рака.
- Виды лечения, которые применялись прежде.
- Возраст и общее состояние здоровья больного.
- Наличие сопутствующих заболеваний.
Можно назначать монотерапию одним препаратом, но лучшего эффекта обычно удается достичь, когда пациент получает комбинацию химиопрепаратов с разными механизмами действия. Нередко химиотерапию сочетают с другими видами лечения.
Классификация
Выделяют следующие основные разновидности химиотерапии:
- Неоадъювантная. Проводится до хирургического вмешательства. В данном случае ее основная цель — уменьшить размеры опухоли, чтобы хирургу было проще ее удалить.
- Адъювантная. Проводится после хирургического лечения. Опухоль удалена, но в организме пациента могли остаться раковые клетки. Химиотерапия помогает уничтожить их и предотвратить рецидив.
- В качестве основного вида лечения. Химиопрепараты могут стать основным методом лечения рака, когда операция противопоказана или неэффективна (на поздних стадиях).
- Химиолучевая терапия. Термин, который обозначает сочетание химиотерапии и лучевой терапии. При этом повышается эффективность, но возрастает риск побочных эффектов.
- Химиоэмболизация. Специфическая разновидность лечения, когда в артерию, питающую опухоль, вводят эмболизирующий препарат в сочетании с химиопрепаратом. Частички эмболизирующего препарата перекрывают просвет сосудов, лишая опухоль кислорода и питательных веществ, а химиопрепарат атакует раковые клетки.
Химиотерапия применяется как для радикального (с целью полного уничтожения опухоли и наступления ремиссии), так и для паллиативного (сокращение размеров опухоли, борьба с симптомами, продление жизни пациента) лечения.
Как вводят химиопрепараты?
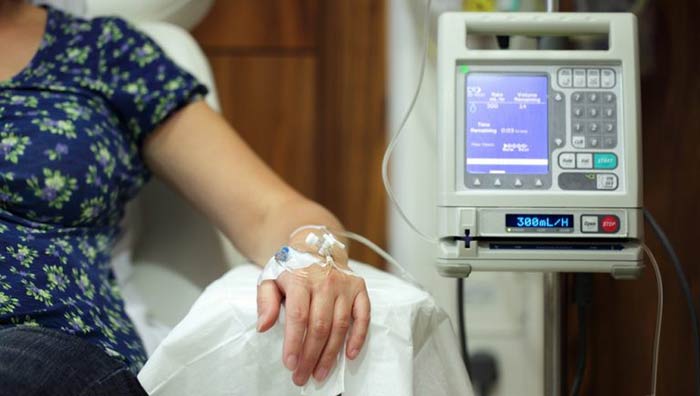
Чаще всего химиопрепараты вводят в виде растворов внутривенно, через иглу, катетер или имплантируемые порт-системы. Иногда их принимают в виде таблеток. Такая химиотерапия называется системной, потому что лекарство поступает в системный кровоток и разносится по всему организму.
В отдельных случаях проводят местную химиотерапию: препарат вводят непосредственно в место, где находится опухоль:
- Интраартериально — в питающую опухоль артерию.
- В брюшную полость.
- В плевральную полость.
- Под оболочки головного и спинного мозга.
- В желудочки головного мозга.
- В мочевой пузырь.
- Существуют препараты для втирания в кожу.
Местное введение препарата помогает предотвратить его воздействие на здоровые органы и избежать серьезных побочных эффектов.
Как подбирают дозировки?
Правильный подбор доз химиопрепаратов — ответственная задача. Если дозировка будет слишком маленькой, это снизит шансы на успешное лечение, а если слишком большой — сильно возрастут риски тяжелых побочных эффектов. Коридор между эффективностью и безопасностью, в котором приходится лавировать врачу-химиотерапевту, зачастую очень узкий.
Существуют два основных метода расчета доз химиопрепаратов: по весу пациента и по площади его тела. Для отдельных групп онкобольных дозировки нужно подбирать индивидуально:
- Пожилые люди.
- Пациенты, у которых нарушено питание, в состоянии истощения.
- Пациенты, имеющие избыточную массу тела или ожирение.
- Пациенты, которые имеют сопутствующие проблемы со здоровьем и, помимо химиопрепаратов, вынуждены принимать другие лекарства.
- Люди, страдающие анемией, иммунодефицитными состояниями, нарушением свертываемости крови, болезнями почек и печени.
- Дети.
- Пациенты, у которых химиотерапия сочетается с лучевой терапией.
Как долго длится курс лечения?
На этот вопрос сложно дать однозначный ответ. Это индивидуально. Курсы могут иметь разную продолжительность. Некоторым больным достаточно одного курса лечения, другим требуется несколько. В первую очередь это определяется типом и стадией рака, его молекулярно-генетическими характеристиками, общим состоянием здоровья пациента, разновидностью химиопрепаратов, которые было решено использовать, протоколами химиотерапии.
Что такое циклы химиотерапии?
Так как химиопрепараты атакуют все быстро размножающиеся клетки без разбора, все они в той или иной степени токсичны для организма. Поэтому их нельзя вводить постоянно в течение длительного времени. Организму нужны передышки, чтобы восстановиться.
Химиотерапию проводят циклами. Лекарство вводят однократно, либо в течение нескольких дней подряд, либо в течение нескольких дней через день, после чего следует перерыв. Продолжительность циклов бывает разной. Обычно она измеряется неделями и составляет 7, 14, 21, 28 дней.
Курс лечения может включать несколько циклов. Врач выбирает оптимальный график введения препаратов, который, с одной стороны, помогает добиться максимальной эффективности, в то же время обеспечивает минимальный риск побочных эффектов.
Что такое протоколы химиотерапии?
Правильный подбор химиопрепаратов, их комбинаций и доз — сложная задача. Для того чтобы ее эффективно решить, опыта одного врача не хватит. По всему миру проведены многочисленные исследования с участием тысяч пациентов, их результаты легли в основу протоколов химиотерапии. В этих документах подробно прописаны все нюансы назначения химиотерапии при разных типах и стадиях рака.
В разных странах врачи могут руководствоваться разными протоколами химиотерапии. Некоторые из них полностью или частично устарели, другие учитывают наиболее современные достижения в области онкологии.

Какими побочными эффектами обладают химиопрепараты?
За счет того, что химиопрепараты атакуют не только опухолевые, но и активно размножающиеся здоровые клетки, они обладают многочисленными побочными эффектами. Пациент может испытывать:
- Боли в разных частях тела.
- Тошноту и рвоту.
- Выпадение волос, изменение ногтей.
- Нарушение аппетита и извращение вкуса.
- Диарею или запоры.
- Повышенную утомляемость.

Химиотерапия может приводить к изменениям со стороны крови: повышенной кровоточивости, анемии, снижению иммунитета, при этом повышается риск инфекционных осложнений. Разные сочетания химиопрепаратов токсичны в разной степени.
Можно ли справиться с побочными эффектами химиотерапии? Существуют некоторые эффективные способы:
- В первую очередь врач даст некоторые рекомендации по поводу образа жизни, питания.
- Для защиты волос и ногтей во время введения препаратов используют охлаждающие шапочки, специальные охлаждающие пакеты для рук и ног.
- Поддерживающая терапия помогает справиться с неприятными симптомами и перенести курс химиотерапии более комфортно.
- Если эти меры не помогают, приходится снижать дозы химиопрепаратов, заменять их более безопасными. Это может негативно повлиять на эффективность лечения.
Выберите химиотерапевта и запишитесь на приём

Главный врач Европейской клиники, онколог, к.м.н.

Биологическая терапия – это лечение, которое оказывает действие на процессы в клетках. Существует несколько типов такой терапии:
- Блокирует деление и дальнейший рост злокачественных клеток.
- Находит раковые клетки и уничтожает их.
- Воздействует на иммунную систему, стимулируя ее атаковать злокачественные клетки.
Есть несколько названий биологической терапии:
- Модификаторы биологических реакций.
- Биологические агенты.
- Таргетная терапия.
- Иммунотерапия.
Будет ли рекомендована биологическая терапия, зависит от типа злокачественной опухоли, стадии болезни, примененных методов лечения. Многие типы биологической терапии все еще являются экспериментальными. Такое лечение не подходит для всех видов рака. Но в некоторых случаях биологическая терапия может быть лучшим вариантом.
Иммунотерапия – один из видов биологической терапии. Она использует вещества, вырабатываемые иммунной системой организма. Они помогают ему бороться с инфекциями и заболеваниями. Другие виды биологической терапии используют вещества, которые также имеют природную основу, но не являются частью иммунитета.
Биологические методы лечения могут быть довольно запутанными. Пока не существует простого способа их группировки, которому легко следовать. Некоторые препараты объединены в соответствии с их влиянием – к примеру, блокируют рост злокачественных клеток. Другие группы включают определенный тип лекарств – моноклональные антитела, нацеленные на специфические белки злокачественных клеток. Есть препараты, которые принадлежат к более чем одной группе. Например, лекарство, которое блокирует развитие патологической клетки, но вместе с тем является моноклональным антителом.
Для пациента важно знать задачу лечения и возможные побочные эффекты.
Виды биологической терапии
Моноклональные антитела – это вид биологической терапии. Моноклональный означает – один тип. Таким образом, каждое моноклональное антитело – это множество копий одного типа антитела. Их изготавливают в условиях лаборатории.
Антитела распознают и присоединяются к специфическим белкам, которые производят клетки. Каждое моноклональное антитело идентифицирует только один конкретный белок. Они работают по-разному в зависимости от белка, на который нацелены. Их создают для работы с различными типами рака.
В настоящее время многие моноклональные антитела доступны для лечения злокачественных опухолей, многие находятся на стадии проверки в условиях клинических испытаний. Для этих препаратов характеры разные побочные эффекты.
Моноклональные антитела действуют по-разному, некоторые из них более чем одним способом.
Запуск иммунной системы
Определенные антитела стимулируют иммунную систему атаковать и уничтожать раковые клетки. Несмотря на то, что злокачественные клетки являются аномальными, они развиваются из здоровых, таким образом, иммунной системе может быть сложно распознать их. Некоторые антитела просто присоединяются к раковым клеткам, облегчая работу иммунитета.
Блокировка молекул, останавливающих работу иммунитета
Также их называют ингибиторами контрольно-пропускного пункта. Иммунная система использует специфические молекулы, которые предотвращают разрушение здоровых клеток. Их называют контрольно-пропускным пунктом. Некоторые злокачественные клетки создают такие молекулы, они деактивируют иммунную систему в виде Т-клеток, атакующих раковые клетки. Препараты, блокирующие такие молекулы, называют ингибиторами контрольно-пропускного пункта. Они представляют собой тип иммунотерапии в онкологии и включают препараты, блокирующие CTLA-4, PD-1 and PD-L1.
Блокировка сигналов, сообщающих раковым клеткам о делении
Злокачественные клетки часто создают в большом количестве молекулы под названием рецепторы факторов роста. Они находятся на поверхности клеток и посылают сигналы, которые помогают им выживать и делиться. Некоторые моноклональные антитела препятствуют работе рецепторов факторов роста, блокируя сигнал или сам рецептор. Поэтому злокачественная клетка не получает больше сигнал, в котором нуждается.
К некоторым моноклональным антителам присоединяются химиопрепараты или радиация. Антитело находит раковую клетку и доставляет к ней непосредственно препарат или излучение.
Все моноклональные антитела в названии имеют 'mab' (monoclonal antibodies):
- Трастузумаб (Герцептин)
- Бевацизумаб (Авастин)
- Ритуксимаб (Мабтера)
Лечение, как правило, осуществляется внутривенно, через капельницу. Частота и количество процедур зависит от типа моноклонального антитела и вида опухоли.
Все препараты имеют нежелательные последствия. Они могут зависеть от типа клеток, на которые нацелены; от того, переносит ли антитело химиопрепарат или излучение.
Наиболее распространенным побочным эффектом всех моноклональных антител является аллергическая реакция на препарат. Она происходит, как правило, в начале терапии. Для предотвращения реакции используется парацетамол или антигистаминный препарат для начала лечения.
Аллергическая реакция может включать следующие симптомы:
- озноб;
- лихорадку;
- сыпь и зуд;
- тошноту;
- одышку;
- головные боли;
- обмороки;
- изменение артериального давления.
Вакцины могут помочь защитить организм от инфекций и заболеваний. Но также их применяют для лечения и профилактики некоторых видов рака. Вакцины доставляют небольшое количество белка в организм. В зависимости от вакцины белки могут быть от вирусов, бактерий или раковых клеток, но они не способны вызвать заболевание.
Иммунная система распознает, что белки вакцины отличаются от собственных белков и устанавливает атаку против них. Лейкоциты производят белки – антитела, распознающие определенные белки в вакцине. Антитела присоединяются к белкам и помогают вывести их из организма. Некоторые антитела все же остаются в организме. Если он подвергнется воздействию тех же белков в будущем, он быстро идентифицирует их и начинает создавать нужные антитела.
Существует два типа вакцин от рака – для профилактики и для лечения.
Вакцины от рака для профилактики
В настоящее время существует только одна вакцина, предотвращающая рак. Он может предупредить развитие рака шейки матки, защищая от вируса папилломы человека (ВРЧ). Как известно, этот вирус вызывает изменения, которые могут привести к данному виду онкологии. Если женщина имеет прививку, прежде чем она подвергнется воздействию вируса, риск заболеть раком шейки матки будет очень низкий.
Существует большое количество испытаний по применению вакцин, предотвращающих другие виды рака, но они еще находятся на стадии исследования.
Вакцины от рака для лечения
Данный вид вакцин направлен на обучение иммунной системы распознавать и атаковать злокачественные клетки. Они помогают:
- остановить дальнейший рост опухоли;
- предотвратить рецидив;
- уничтожить любые оставшиеся клетки после применения других методов.
Колониестимулирующие факторы известны также как факторы роста. Эти также вещества производятся организмом, существует их несколько типов. Некоторые из них стимулируют костный мозг создавать определенные типы клеток крови. В настоящее время существует возможность создавать некоторые из них в условиях лаборатории.
При лечении рака врачи могут обращаться к терапии под названием гранулоцитарный колониестимулирующий фактор (Г-КСФ) после химиотерапии, чтобы восстановить уровни клеток крови. Существуют различные типы этих препаратов:
- Ленограстим (граноцит)
- Филграстим (Нейпоген, Zarzio, Nivestim, Ratiograstim)
- Pegfilgrastim или Neulasta – форма филграстима, но продолжительного действия.
Исследователи изучают вопрос о применение некоторых факторов роста как биологической терапии. GM-CSF (гранулоцитарный и макрофагальный колониестимулирующий фактор) – фактор роста, увеличивающий количество некоторых типов лейкоцитов – нейтрофилов и моноцитов. Также он стимулирует дендритные клетки к делению. Эти клетки помогают иммунной системе распознавать и атаковать злокачественные клетки. Таким образом, исследователи применяют GM-CSF наряду с другими видами биологической терапии, чтобы увеличить количество дендритных клеток, а также в качестве вакцины для лечения некоторых видов рака.
Данная терапия проводится в рамках экспериментальных исследований. В ходе испытаний у пациентов увеличилось число дендритных клеток после вакцины. Но пока не известно, влияет ли это на рак. Испытания проводились с участием небольшого числа пациентов, в основном с меланомой.
Интерферон и интерлейкин – это вещества, создаваемые клетками организма для коммуникации друг с другом. Это белки, которые принадлежит к группе химических веществ под названием цитокины.
Интерферон и интерлейкин могут стимулировать работу иммунной системы, поэтому врачами была создана их техногенная версия для лечения рака. По принципу функционирования эти препараты называют иммунотерапией.
Интерферон и интерлейкин работают в нескольких направлениях:
- вмешиваются в способы деления и распространения рака;
- стимулируют работу иммунной системы – Т-клеток и других – атаковать злокачественные клетки;
- стимулируют раковые клетки вырабатывать вещества, которые привлекают к ним клетки иммунной системы.
Показания к применению альфа-интерферона
Врачи используют альфа-интерферон в лечении разных видов злокачественных опухолей:
- рака почки;
- меланомы;
- множественной миеломы;
- некоторых видов лейкемии.
В организм препарат поступает внутривенно с помощью капельницы, а также подкожно. Частота применения зависит от типа рака. В большинстве случаев интерферон дают 3 раза в неделю, но бывает и ежедневно в виде инъекций.
Показания для интерлейкина
Интерлейкин 2 также называют Алдеслейкин (или IL2 или Пролейкин). Чаще всего его используют для лечения рака почки. В рамках клинических испытаний его задействовали также для других видов онкологии. Для введения в организм используют подкожные инъекции, капельницы. Частота применения зависит от типа злокачественной опухоли.
Некоторые из нежелательных последствий терапии интерфероном и интерлейкином 2 могут включать:
- усталость;
- гриппоподобные симптомы;
- диарею;
- низкие уровни клеток крови;
- тошноту;
- потерю аппетита;
- интерлейкин может вызывать низкое давление крови.
Гены кодируют сообщения, которые доносят информацию клеткам, как создавать белки. Белки – это молекулы, контролирующие способы поведения клеток. Таким образом, гены решают, как будет выглядеть человек, как будет работать организм. Тело человека обладает тысячами отдельных генов.
Гены состоят из ДНК, которые располагаются в ядре клетки. Ядро – это контрольный центр клетки. Гены, объединяясь по группам, создают хромосомы. Человек наследует половину хромосом от матери, половину – от отца.
Раковые клетки отличаются от здоровых. Они имеют мутации или ошибки в нескольких генах, что приводит их к слишком частому процессу деления и образования опухоли. Гены, которые могут быть повреждены:
- гены, стимулирующие клетки размножаться (известны как онкогены);
- гены, останавливающие клеточное деление (гены-супрессоры опухолей);
- гены, восстанавливающие поврежденные гены.
Многие мутации генов, которые приводят к созданию злокачественных клеток, являются следствием окружающей среды или факторов образа жизни, таких как курение. Но некоторые люди наследуют дефектные гены, повышающие риск определенных видов рака. Наследованные поврежденные гены становятся причиной рака у 2-3 человек из 100.
Генная терапия - это один из видов лечения, который использует гены для терапии заболеваний. Исследователи надеются, что некоторые виды генной терапии смогут вылечить рак.
Внедрение генов в раковые клетки – один из наиболее сложных аспектов в генной терапии. Исследователи работают над поиском новых эффективных способов осуществления этой задачи. Гены обычно доставляются в раковую клетку с помощью носителя или перевозчика, которого также называют вектором. Наиболее распространенные типы носителя, которые используют в генной терапии – вирусы, поскольку они входят в клетку и доставляют генетический материал. Вирусы изменяют так, чтобы они не могли вызывать серьезные заболевания, лишь легкие симптомы.
Измененные вирусы могут быть направлены только на раковые клетки, а не на здоровые. Они только переносят ген в злокачественные клетки.
Исследователи тестируют и другие виды носителей, такие как инактивированные бактерии.
Ученые изучают различные способы применения генной терапии, в том числе:
- усиление иммунного ответа;
- повышение эффективности других методов лечения рака;
- блокировка процессов, защищающих раковые клетки;
- использование измененных вирусов.
Усиление иммунного ответа
Некоторые виды генной терапии направлены на повышение естественной способности организма атаковать злокачественные клетки. Иммунная система человека обладает клетками, которые распознают и убивают вредные субстанции, способные вызвать заболевания, такие как раковые клетки.
Существует много различных типов иммунных клеток. Некоторые из них производят белки, которые активизируют иммунные клетки уничтожать злокачественные. Другие добавляют гены иммунных клеток, чтобы повысить качество поиска патологических клеток или уничтожить определенные виды рака.
Повышение эффективности других методов лечения рака
Некоторые препараты генной терапии внедряют гены в злокачественные клетки, чтобы сделать их более чувствительными к конкретным процедурам – к химиотерапии или лучевой терапии. Они повышают эффективность других методов лечения.
Генная терапия препарата Pro
Некоторые виды генной терапии доставляют гены в раковые клетки, позволяющие преобразовывать лекарства из неактивной формы в активную. Неактивная форма называется препаратом Pro.
После предоставления носителя, содержащего ген, врач дает пациенту препарат в виде таблетки или капсулы, поступающей в кровоток. Он циркулирует в организме и не наносит вреда здоровым клеткам, однако, достигая раковые, ген активирует препарат и тот уничтожает клетку.
Блокировка процессов, защищающих раковые клетки
Некоторые препараты блокируют процессы, которые используют раковые клетки, чтобы выжить. Например, большая часть клеток в организме запрограммированы умереть, если их ДНК повреждена и восстановлению не подлежит. Такой процесс называется запрограммированной смертью клеток или апоптозом. Но раковым клеткам удается блокировать этот процесс. Некоторые стратегии генной терапии направлены на снятие такой блокировки. Исследователи надеются, что новые виды лечения смогут обеспечить смерть злокачественным клеткам.
Использование измененных вирусов
Определенные вирусы инфицируют и уничтожают клетки. Исследователи работают над способами изменения эти вирусов так, чтобы они были нацелены только на злокачественные клетки, не нанося вреда здоровым. При данном виде лечения не задействуется внедрение генов. Поэтому в истинном смысле слова это не генная терапия.
Один из таких примеров – вирус герпеса. Измененный вирус называют Oncovex. Его изучали в рамках клинических испытаний в лечении метастатической меланомы, рака поджелудочной и рака головы и шеи.
Вопросы, которые можно задать врачу по биологической терапии:
- Почему предлагается биологическая терапия в конкретном случае?
- Какой тип биологической терапии будет использоваться?
- Существуют ли другие варианты лечения для конкретного случая болезни?
- Будет ли проводиться другое лечение в то же время?
- Безопасны ли биологические методы терапии?
- Каковы будут преимущества биологической терапии?
- Необходима ли госпитализация во время лечения?
- Сколько займет терапия?
- Какие побочные эффекты могут быть?
- Как долго будет длиться побочные эффекты?
- Будет ли долгосрочные побочные действия?
- Есть что-нибудь, что может помочь с побочными эффектами?
Читайте также:

