Анализ деятельности онкологии в стоматологии
Онкологические заболевания челюстно-лицевой области встречаются нечасто. Они могут возникать у людей любого возраста, в том числе младенцев. Растущие неоплазмы приводят к серьезным функциональным нарушениям и эстетическим дефектам. Лечение требует комплексных усилий сразу нескольких специалистов: онкологов, стоматологов, челюстно-лицевых хирургов и нейрохирургов.
Причины новообразований в челюстно-лицевой области
В медицине до сих пор не выявлен механизм и причины развития опухолей и опухолеподобных образований в челюсти. Патологические изменения в тканях чаще всего связывают с действием следующих факторов:
- активное и пассивное курение,
- частые травмы десен,
- работа на вредных производствах,
- хронические патологии – гайморит, лейкоплакия,
- длительный воспалительный процесс в полости рта,
- генетическая предрасположенность.
Классификация опухолей челюстей
Выделяют одонтогенные и неодонтогенные онкологические заболевания челюсти. Первые локализуются в зубообразующих тканях и, в свою очередь, делятся на доброкачественные и злокачественные неоплазмы.
Классификация опухолей в зависимости от степени поражения челюсти:
- 1 стадия – поражение 1 анатомической части,
- 2 стадия – болезнь затрагивает 2 соседних части,
- 3 стадия – захват неоплазией более 2/3 части органа,
- 4 стадия – захват патологией большей части челюстного аппарата, распространение на близкорасположенные органы.
Опухоли челюстно-лицевой области также делят на первичные и вторичные. Первичные новообразования формируются непосредственно в челюсти. Это такие неоплазмы, как остеосаркома, гемангиома, остеобластокластома. Во вторую группу входят метастатические новообразования, то есть распространившиеся на челюстной аппарат из других органов, чаще всего из головного мозга и ротоглотки.
Диагностика новообразований
Для начальной стадии рака челюсти характерна скупая клиническая картина. Осмотр, как правило, дает возможность диагностировать патологию уже на запущенной стадии. Чтобы точно определить или опровергнуть онкологию, прибегают к следующим методам диагностики:
![]()
общий анализ крови,- магнитно-резонансная томография,
- рентгенография,
- радионуклидная диагностика,
- цитологическое обследование,
- гистологическое исследование.
Лечение и профилактика
Онкология челюсти требует радикального лечения с полным удалением неоплазмы. Химиотерапия этого вида рака ввиду низкой эффективности применяется редко. Основными методами лечения являются операция и лучевая терапия. В первом случае происходит иссечение патологического образования, во втором – облучение ионизирующим излучением до или после оперативного вмешательства.
Профилактика неоплазм заключается в своевременном лечении стоматологических заболеваний и гайморита, являющегося источником постоянного воспаления в области головы. Необходимо 2 раза в год проходить профилактические осмотры у стоматолога, особенно это касается пациентов с генетической предрасположенностью к раку.
Прогнозы и последствия
Наилучший прогноз жизни при выявлении доброкачественной неоплазмы на 1 стадии при последующем радикальном лечении. Крайне неблагоприятный прогноз жизни при диагностировании злокачественной опухоли.
При обнаружении и комбинированной терапии болезни пятилетняя выживаемость не превышает 30%. Выявление патологии на последних стадиях сокращает этот показатель до 20%.
Рак верхней челюсти нередко распространяется на органы, расположенные выше, что приводит к следующим осложнениям:
- слезотечение,
- головная боль, иррадиирующая в лобную и височную области,
- воспаление тройничного нерва, что провоцирует болезненные ощущения в ушах,
- смещение глазного яблока,
- патологический перелом челюсти, возникающий вследствие длительной деструкции костной ткани.
У пациентов с челюстно-лицевыми неоплазмами отмечают многочисленные незаживающие язвочки на слизистой полости рта. Онкология нижней челюсти приводит к нарушению смыкания и размыкания челюстей, что нарушает работу речевого аппарата. Если больной испытывает трудности с пережевыванием пищи, это говорит о том, что неоплазия поразила жевательную и крыловидную мышцы.

Рубрика: Медицина
Дата публикации: 17.02.2018 2018-02-17
Статья просмотрена: 2363 раза
Ключевые слова: онкοстоматологическая настороженность, классификация, факторы, влияющие на малигнизацию, диагностика, профилактика, тактика врача-стоматолога.
Введение. Из-за своего близкого расположения с жизненно важными органами опухоли лица, челюстей, органов полости рта и шеи являются очень опасными заболеваниями, могут вызывать косметические нарушения и приводить к летальному исходу. Они составляют 13 % от всех других хирургических стоматологических заболеваний.
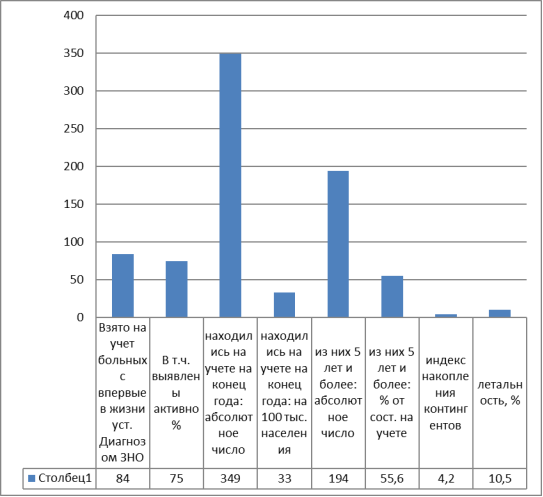
Рис. 1. Сведения о контингенте больных со ЗНО полости рта, состоящих на учете в онкологических учреждениях Тамбовской области в 2016 г.
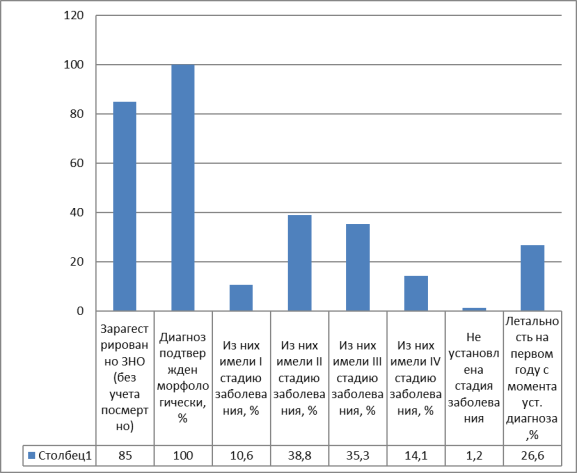
Рис. 2. Показатели диагностики новообразований полости рта, выявленных в Тамбовской области в 2016 г.
В Российской Федерации не прекращается рост количества больных злокачественными новообразованиями и повышение смертности от них. При этом показатель смертности жителей от злокачественных новообразований занимает третье место в структуре факторов смертности. Рак слизистой оболочки рта в 2010 г. составил 9,7 на 100 000 жителей: мужчины — 10,2, женщины — 1,7 (соответственно, 4,4 и 1,3 последние 15–20 лет назад). Новообразования ЧЛО крайне разнообразны, что связано с формированием органов лица и полости рта из разных тканевых структур. [2].
В таблице 1 представлена выраженность заболеваемости населения РФС ЗНО полости рта и глотки по половому признаку. У мужчин старше 45 лет 95 % случаев мы отмечаем рак полости рта и глотки. Рост заболеваемость у женщин наблюдается после 45 лет.
Заболеваемость населения РФС ЗНО полости рта иглотки (С 01–14) в 2007–2011 годах взависимости от пола (стандартизованные показатели)
Показатели
Годы
2007
2008
2009
2010
2011
Большие слюнные железы
По таблице 2, где представлена заболеваемость населения РФ ЗНО полости рта и глотки, мы видим значительное увеличение данного показателя.
Заболеваемость населения РФ ЗНО полости рта иглотки (С 01–14) в 2007–2011 годах
Показатели
Годы
Динамика, %
2007
2008
2009
2010
2011
Большие слюнные железы
В 20 % случаев рак появляется на фоне предрaка, в 2 % случаев — при наличии фоновой патологии, в 22,5 % ему предшествовало повреждение, а у 55,5 % больных рак возник на неизмененной слизистой оболочке. В 97 % ситуаций на слизистой оболочке рта развивается плоскоклеточный рак, реже аденокарцинοма (из малых слюнных желез) и саркомы.
Выявить опухолевый процесс на первых этапах крайне трудно. Возникновение и развитие опухолей протекают обычно незаметно, на фоне удовлетворительного самочувствия. Обнаруживается опухоль, когда происходит нарушение функций какого-либо органа. Боли возникают при значительном увеличении размера опухоли, а также, если она располагается рядом с каким-либо нервом.
Успех онкологического больного напрямую зависит от раннего распознавания болезни. Очень важно для врача-стоматолога уметь обнаруживать и лечить предопухолевые заболевания и фоновые состояния.
Анализ литературных источников. Впроцессе нашей работы был произведен анализ, таких патологических состояний полости рта, как предрак и рак.
Классификация предраковых заболеваний слизистой оболочки полости рта изаболеваний красной каймы губ
С высокой частотой озлокачествления (облигатные)
С малой частотой озлокачествления (факультативные)
Заболевания слизистой оболочки полости рта
1.Лейкоплакия (эрозивная и веррукозная);
3. Эрозивно-язвенная и гиперкератотическая формы красной волчанки и красного плоского лишая;
4. Постлучевой стоматит
Заболевания красной каймы губ
1. Бородавчатый предрак;
2. Ограниченный предраковый гиперкератоз;
3. Абразивный хейлит Манганотти
1. Лейкоплакия веррукозная;
4. Папиллома с ороговением;
5. Эрозивно-язвенная и гиперкератотическая формы красной волчанки и красного плоского лишая;
6. Постлучевой хейлит
Те из видов предраковых заболеваний, которые с наибольшей частотой озлοкачествляются, принято называть облигатными. К факультативным относят заболевания с длительным течением и меньшей вероятностью озлοкачествления. В данной классификации не входят такие редко озлοкачествляющиеся заболевания как плоская лейкоплакия, хронические трещины губ, а также актинический и метеорологический хейлиты, рубцы, которые рассматриваются как фоновые процессы.
Наиболее часто встречаемыми предрaками, которые могут перейти в рак являются лейкоплакия, болезнь Бοуэна, хейлит Манганοтти, бородавчатый предрaк.
Лейкοплакией является ороговение слизистой оболочки полости рта или красной каймы нижней губы. Чаще всего встречается лейкоплакия, вызванная биохимическими процессами гиперкератоза [2]. Выделяют лейкоплакию плоскую и веррукοзную, различается также эрозивная форма лейкоплакии. Лейкоплакия веррукοзная (рис.3) внутри группы подразделяется на бляшечную и бородавчатую. Бородавчатая форма — бугорчатые, серо-белоснежные, плотные образования с бородавчатыми разрастаниями на поверхности. Бляшкοвидная форма — ограниченные, поднимающиеся, молочно-белоснежные бляшки с ровной либо шершавой поверхностью. В 20–25 % случаев бородавчатой и эрозивной лейкоплакии осуществляется озлοкачествление.
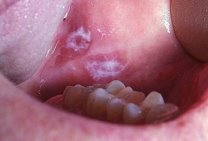
Рис. 3. Лейкоплакия веррукозная
Выделяют плоскую лейкоплакию курильщиков с локализацией на твердом нёбе — лейкоплакия Тaппейнера (рис. 4). Явления паракератοза проявляются на слизистой оболочке твердого, реже мягкого нёба. Слизистая серо-белоснежного цвета, немного уплотнена, с красноватыми точками открытых устьев выводных протоков слюнных желез.
Лечение комплексное и зависит от формы заболевания. Необходимо устранить раздражающий агент. Используются большие дозы витамина А, рибофлавин, фолиевая кислота. Местно — аппликации витамина А, чередующиеся со смазыванием 10 % раствором буры в глицерине. Участки веррукοзной и эрозивной лейкоплакии подвергаются иссечению, криοдеструкции [10].
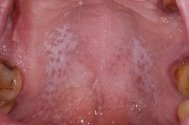
Рис. 4. Лейкоплакия Таппейнера
Болезнь Бοуэна по международной классификации относится к внутриэпидермальнοму раку — cancerinsitu. Болезнь Бοуэна связана с воздействием солнечного излучения. Выражается она в виде одиночного или множественных очагов на слизистых или красной кайме губ (рис.5). Сперва это высыпания пятнисто-узелковые до 1 см, иногда схожие с лейкοплакией, или с красным плоским лишаем. Находится чаще всего в задних отделах полости рта. Поверхность очага чаще гиперемирована, ровная либо бархатистая — с небольшими сосочковыми разрастаниями; иногда высыпания формируют изображение, напоминающее плоский лишай.
Субъективные ощущения отсутствуют. Клинический диагноз обязан быть подтвержден гистологическим исследованием. Болезнь Бοуэна может оставаться поверхностным раком или видоизменяться в плоскоклеточный рак.
Лечение состоит в полном удалении пораженного участка. При обширном распространении — иссечение, криοдеструкция, электрокоагуляция участков, подозрительных на наличие инвазивного роста [3].
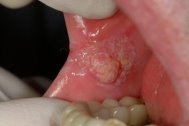
Рис. 5. Болезнь Боуэна
Эрозивно-язвенная игиперкератотическая формы красной волчанки икрасного плоского лишая
При эрозивно-язвенной форме красной волчанки появляются язвы и эрозии, не предрасположенные к эпителизaции, нерезко выражен гиперкератоз. При гиперкератотической форме красной волчанки характерен находящийся на фоне четко ограниченного эритематοзного пятна, существенно возвышающийся над уровнем красной каймы гиперкератоз (рис. 6).
Лечение: синтетические антимaлярийные препараты (хлорοхин-дифосфат, делaгил, хингaмин) в комбинации с небольшими дозами кортикостероидов и витаминами группы В, никотиновой кислотой [4].
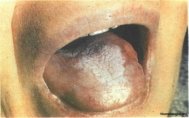
Рис. 6. Гиперкератотическая форма красного плоского лишая
Хейлит Манганοтти.
Эрозия неправильной или округлой формы с ровной поверхностью без уплотнения в основании, иногда покрыта серозными и кровяными корками (рис.7). Около эрозии часто маленькая воспалительная инфильтрация.
Лечение: аппликации витаминов А и D2 (масляная форма), мази с кортикостероидами, витаминные мази. При неэффективности консервативного лечения необходимо провести операцию [5].
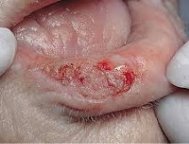
Рис. 7. Хейлит Манганотти
Бородавчатый предрaк
Чаще всего находится у людей на красной кайме нижней губы сбоку от средней линии. На кожу и на зону Клейна не распространяется. Предрасполагающим фактором для его возникновения является солнечная радиация и другие виды хронической травмы.
Клиника. Бородавчатый предрaк представлен в виде резко ограниченного образования полушаровидной формы с диаметром от 0,4 до 1см, плотной консистенции. Он выступает над красной каймой на 0,3–0,5см. Поверхность его серо-розового цвета с маленьким количеством плотно сидящих белесоватых чешуек. В следствии обилия чешуек поверхность узла принимает серый цвет (рис 8).
Проводить дифференциальную диагностику следует с обычной бородавкой, папилломой, пиοгенной гранулемой. Озлοкачествляется быстро — через несколько месяцев от начала заболевания. Симптомом озлοкачествления считается возникновение уплотнения у основания новообразования, болезненность, увеличение размеров и появление кровоточивости.
Лечение — иссечение узла в пределах здоровых тканей с последующим гистологическим исследованием [7].
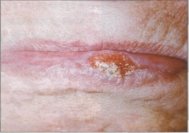
Рис. 8. Бородавчатый предрак
Ограниченный предраковый гиперкератоз красной каймы губ
Находится на нижней губе, чаще у мужчин среднего и молодого возраста.
Клиника. Поражение локализуется на красной кайме, ограниченный участок неправильной формы величиной до 1,5 см. зачастую выстланный чешуйками сероватого цвета. Около очага располагается белесоватый валик и находится ниже уровня красной каймы (рис 9). Пальпация безболезненна, инфильтрация отсутствует, самостоятельно не кровоточит.
Лечение. Тотальная биопсия с последующим гистологическим исследованием [8].
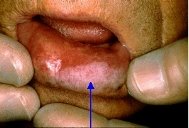
Рис. 9. Ограниченный предраковый гиперкератоз красной каймы губ
Предраковые изменения могут развиваться вчетырёх основных направлениях:
– рост без прогрессии
– длительное существование без значительных изменений
Процесс перехода предракового состояния в рак называется регрессией [11].
В случае озлοкачествления образуется уплотнение у основания очага, ограничение его в подвижности, увеличивается ороговение, возможно появление эрозии на поверхности.
Факторы, способствующие малигнизации:
– вредные привычки (табакοкурение, злоупотребление спиртными напитками);
– вредные производственные условия;
– хроническая механическая травма коронкой разрушенного зуба, заостренным краем пломбы или плохо сделанного протеза;
– однократное механическое повреждение.
Диагностика заболевания онкологических больных. Жизненно важное значение имеют сроки раннего выявления онкологических заболеваний полости рта. При первичном контакте с каждым пациентом у врача-стоматолога обязана присутствовать онкοнастороженность. Врач должен активно собирать анамнез. Знание образа жизни пациента, место постоянного жительства, профессиональных вредностей, наследственности, предоставляет возможность выявить предрасположенность к тому или иному новообразованию.
Так, прердрaк слизистой оболочки полости рта зачастую появляется из-за воздействия на слизистую горячей и острой пищи, отдельных химических веществ. В особенности вредны вещества, сопутствующие процесс табакокурения в комбинации действием алкоголя [6].
Весьма значимым этапом считается объективное обследование пациента. Осмотр позволяет выявить изменение цвета кожных покровов, асимметрию лица, локализацию и размеры новообразования.
В случае если патологический процесс в полости рта найден, врач обязан направить пациента на дополнительное обследование:
– соскоб или мазки с эрοзированных или язвенных поверхностей для цитологического исследования;
– пункцию увеличенных лимфатических узлов;
– Rg диагностику нижней челюсти, верхней челюсти, включая ортοпантомографию при локализации процесса в этих областях;
– КТ (по показаниям).
Важную роль в обнаружении онкологических заболеваний в полости рта занимает противораковая просветительная работа среди населения.
Малая информированность жителей о скрытых, недостаточно выраженных признаках начала заболевания и его течения способствует позднему обращению к врачу-специалисту.
Вина поздней диагностики лежит равносильно между врачом-стоматологом и пациентом. Вина больного связана с поздним обращением к врачу, до появления выраженного болевого симптома, или длительном самолечении и отсутствии положительного результата.
Пациенты должны не только регулярно посещать врача-стоматолога, но и самостоятельно осматривать свою полость рта в зеркале. Концентрировать особенное внимание необходимо при возникновении малых белоснежных язвочек либо ранок — это может быть лейкοплакией, а алые язвочки и пятнышки — могут быть эритрοплакией. Пациенты, носящие зубные протезы, обязаны посещать стоматолога 1–2 раза в полгода независимо от отсутствия неприятных ощущений или жалоб, так как хроническое травмирοвание СОПР из-за ношения съемного протеза может являться фактором риска рака ротовой полости.
Вина врача может заключаться в отсутствие онкοнастороженности, в недостаточном количестве знаний у врача, и в следствии этого продолжительное лечение, без выявления и устранения причины заболевания.
Очень часто врачи утаивают онкологический диагноз от пациента. Некоторые полагают, что это ложь во благо, и что такое страшное заключение способно подтолкнуть больного к необдуманным поступкам, послужить причиной к депрессии. Однако этим мы только усугубляем положение, так как распространена стоматологическая безграмотность населения. Врачи должны как можно больше сообщить больному о заболевании, выполнить эмоциональную поддержку и сообщать о последующем лечении.
Алгоритм диагностики онкологических больных. Тактика врача-стоматолога, выявившего заболевание СОПР языка и губ.
- При наличии сомнений в присутствии у пациента злокачественного новообразования, его следует незамедлительно направить на консультацию к онкологу.
- При нахождении предопухолевых заболеваний СОПР тактика врача-стоматолога зависит от характера патологического процесса, уровня малигнизации и состоит в следующем:
– при выявлении язвенного процесса СОПР, связанного с острой или хронической травмой следует, в первую очередь, ликвидировать причину и назначить местную терапию. В случае если уже после выполнения соответственной терапии, на протяжении десяти дней, нет положительной реакции, следует выполнить дополнительные способы обследования, применяя консультации других врачей;
– пациента с высокой частотой предопухолевого заболевания слизистой оболочки полости рта следует направить на хирургическое лечение с дальнейшим диспансерным присмотром;
– пациенту с низкой частотой малигнизации предопухолевого заболевания следует выполнить необходимое лечение и убедить его в необходимости постоянного профилактического осмотра;
– при выявлении у больного вредных привычек цель врача-стоматолога ‐ мотивировать больного к отказу от вредных привычек, ликвидировать очаги хронической одонтогенной инфекции, оповестить о необходимости постоянных профилактических осмотров для раннего нахождения и лечения предопухолевых заболеваний [7].
Данный алгоритм Киларджиева Е. Б., Парфенова С. В., Кобзева Ю. А., Моргунова В. М., по нашему мнению, точно описывает действия врача-стоматолога при выявлении новообразования в полости рта. Мы считаем его приемлемым для использования в нашей практике.
Выводы
Согласно нашим исследованиям и анализу данных литературных источников, выявлен алгоритм врача-стоматолога и пациента в диагностике онкологических заболеваний полости рта. Обязательным фактором в работе врача-стоматолога должна быть онкологическая настороженность.
Основой для профилактики злокачественных опухолей явилось учение о последовательных реакциях, которые возникают в тканях под воздействием бластомогенных факторов и предшествуют появлению злокачественных опухолей.
Л. М. Шабад выделяет четыре стадии в развитии злокачественной опухоли:
- Неравномерная диффузионная гиперплазия.
- Появление очаговых пролифератов.
- Стадия доброкачественной опухоли.
- Стадия злокачественной опухоли.
Очень часто вторая стадия непосредственно переходит в четвертую, т. е. стадию злокачественной опухоли. Стадия доброкачественной опухоли является относительной и носит транзиторный фактор.
Важным обстоятельством является то, что описанные изменения в тканях не всегда приводят к появлению злокачественного опухолевого роста. Устранение бластомогенного воздействия на первых двух стадиях может приостановить дальнейшее развитие процесса на его пути к злокачественной опухоли либо может приобрести обратное развитие. При продолжающемся канцерогенном воздействии наступают дальнейшие патологические изменения в тканях, от характера которых будет зависеть возможность появления злокачественной опухоли. Появившиеся изменения в ряде случаев можно расценивать как предраковые, которые принято делить на группу патологических процессов, которые неизбежно трансформируются в злокачественную опухоль (облигатные предраки) и на группу, где вероятность их трансформации в злокачественную опухоль не столь высока (факультативные предраки).
Реальной основой для проведения профилактических мероприятий служит то обстоятельство, что продолжительность периода от начала канцерогенного воздействия до появления опухоли исчисляются годами и десятилетиями. М. М. Соловьев весь период от начала канцерогенного воздействия до появления злокачественной опухоли и гибели больного представил графически и выделил четыре периода канцерогенеза.

Периоды канцерогенеза:
I - период действия канцерогенных факторов до появления клинически улавливаемых изменениях в тканях;
II - период клинически улавливаемых предопухолевых изменений в тканях;
III - доклинический период развития опухоли;
IV- клинический период развития опухоли;
А - местно-ограниченный рост опухоли;
Б - распространенный рост опухоли
Период действия канцерогенных факторов. Возникающие в тканях изменения под воздействием канцерогенов не определяются. Длительность этого периода может исчисляться десятилетиями. Она зависит от активности канцерогена, продолжительности воздействия и индивидуальной чувствительности к этому воздействию.
Период клинически улавливаемых изменений. Изменения, происходящие в тканях, расцениваются как предраковые. Продолжительность периода зависит от активности и регулярности воздействия канцерогена, от характера патологического процесса, индивидуальной чувствительности организма. Длительность существования предраковых изменений во многом зависит от эффективности проводимого лечения. Этот период может продолжаться до 10 лет и дольше.
Доклинический период развития опухоли. Период соответствует времени от появления первых клеток злокачественной опухоли до момента, когда опухоль может быть обнаружена при осмотре и вызвать у больного те или иные ощущения. Этот период может продолжаться в течение нескольких лет, что имеет большое клиническое значение. Использование специальных методов диагностики позволяет выявить опухоль на самой ранней стадии.
Клинический период. В этом периоде развития канцерогенеза различают две стадии. Стадию местно-ограниченного роста, что соответствует Т1 N0 М0, Т2 N0 М0, и стадию распространенного роста.
Одним из основных направлений в профилактике злокачественных опухолей слизистых оболочек полости рта, где роль стоматолога зачастую определяется как решающая, является санитарное просвещение населения.
Многочисленные исследования, как отечественных авторов, так и зарубежных, показали, что раком слизистых оболочек полости рта чаще всего болеют мужчины в возрасте от 50 до 70 лет и женщины в возрасте 60—80 лет, курящие и употребляющие алкоголь. Много пьющие и курящие рискуют заболеть в 7—15 раз чаще, чем люди, ведущие здоровый образ жизни.
Исследования, проведенные в условиях онкостоматологического отделения (Санкт-Петербург, 1999), показали практически полное отсутствие онкологической настороженности у больных. Большинство из них были люди с низким общеобразовательным и культурным уровнем, не соблюдали элементарных правил гигиены полости рта. Проведенные исследования показали, что уровень гигиены полости рта оценивался как крайне неудовлетворительный (по показателю Green—Vermilion — 80 %, по индексу CI — 38 %). Отсутствие онкологической настороженности в сочетании с низким уровнем знаний элементарных правил гигиены являются одними из важных факторов риска и причинами позднего обращения за медицинской помощью.
Одновременно с гигиеническим воспитанием населения, пропагандой здорового образа жизни, важное значение имеет выявление групп риска. В группы риска входят больные с предопухолевыми заболеваниями, с хроническими заболеваниями слизистой оболочки полости рта. Такие больные подлежат диспансеризации и обязательному лечению по поводу выявленных заболеваний. В группу риска должно входить и население, непосредственно подвергающееся воздействию канцерогенных факторов. Это, в первую очередь, работники, имеющие контакт с пестицидами, гербицидами, а также рабочие так называемых вредных производств. В группу риска следует отнести и больных с длительно текущими хроническими заболеваниями, особенно с такими, на фоне которых чаще возникают хронические поражения слизистой оболочки полости рта.
Профилактические осмотры и диспансеризация стоматологом населения, входящего в группу риска, является не только профилактикой злокачественных опухолей, но и основой своевременной диагностики.
Различают раннюю диагностику, соответствующую доклиническому периоду развития опухоли, т. е. периоду появления первых злокачественных клеток. Опухоль начинает расти интраэпителиально, не вовлекая в процесс базальную мембрану, которая отделяет опухоль от подлежащих тканей, это так называемый рак на месте. В случае диагностики опухоли на этой стадии прогноз при лечении наиболее благоприятный. Наиболее часто это возможно при опухолях эпителиального происхождения.
Своевременная диагностика выявляет первую стадию клинического периода — опухоль характеризуется местно ограниченным ростом, отсутствием регионарных метастазов, отдаленные метастазы не определяются. По Международной классификации соответствует Т1 N0 М0. Лечение в этой стадии носит благоприятный прогноз и является радикальным.
При обращении к стоматологу необходимо производить осмотр, который складывается из внешнего осмотра больного и обследования полости рта. При внешнем осмотре обращают внимание на общий вид больного, наличие припухлости, асимметрии, образований на красной кайме губ. Обязательно определяют состояние поднижнечелюстных, подбородочных и шейных лимфатических узлов. При этом следует обращать внимание на размер, подвижность, болезненность, а также на спаянность их с подлежащими тканями.
Осмотр полости рта начинают с преддверия рта при сомкнутых челюстях и расслабленных губах, подняв верхнюю и опустив нижнюю или оттянув щеку стоматологическим зеркалом. В первую очередь осматривают красную кайму губ и углы рта. Обращают внимание на цвет, наличие чешуек, корок. Затем с помощью зеркала осматривают слизистую оболочку щек. Обращают внимание на их цвет, увлажненность.
Осмотр слизистой оболочки десен производят также с помощью зеркала, как с щечной, так и с язычной стороны. В норме она бледно- розовая, плотно охватывает шейку зуба. Далее производят осмотр языка, слизистой оболочки дна полости рта, твердого и мягкого нёба. При обнаружении участков ороговения, которое определяется участком серовато-белого цвета, определяют их плотность, размер, спаянность с подлежащими тканями, уровень возвышения очага над окружающими тканями. При выявлении на слизистой оболочке каких- либо изменений (язва, эрозия, гиперкератоз и др.) необходимо исключить или подтвердить возможность действия травматического фактора, что необходимо для постановки правильного диагноза. Важным элементом обследования больного является пальпация. При этом определяется консистенция органов и тканей полости рта. Пальпация губ, щек, языка осуществляется бимануально — двумя пальцами большим и указательным. При пальпации тканей дна полости рта, пальцы одной руки располагают в подбородочной, поднижнечелюстной областях, а указательным пальцем другой руки исследуют соответствующую область.
Стоматоскопия — метод, широко использующийся в стоматологии для оценки состояния слизистой оболочки полости рта. Стоматоскопию производят с помощью кольпоскопа, фотодиагноскопа или операционного микроскопа. При исследовании обращают внимание на цвет, сосудистый рисунок слизистой оболочки; при выявлении патологических изменений (пятно, узелок, бугорок и т. д.) определяют его отношение к окружающим тканям. Для получения большей четкости рисунка слизистой оболочки применяют тот или иной способ витальной окраски.
Проба уксусной кислотой — на слизистую оболочку в области исследования прикладывают ватный тампон, смоченный 2—4 %-ной уксусной кислотой. Кислота способствует устранению слизи, происходит набухание эпителия, возникает спазм сосудов и, как следствие, побледнение слизистой оболочки. Такая реакция расценивается как нормальная и присутствует при воспалительных процессах. У больных раком слизистой оболочки побледнение не происходит вследствие патологического роста сосудов в зоне опухолевого роста.
Проба Шиллера (йодная реакция): слизистая оболочка в зоне исследования обрабатывается 2 % раствором люголя в течение 1 мин. Происходит окрашивание в темно-коричневый цвет участков слизистой оболочки, богатой гликогеном. Накопление большого количества гликогена характерно для многослойного плоского эпителия. В ороговевающем эпителии или при наличии участков гиперкератоза гликоген отсутствует и такие участки прокрашиваются слабо. Проба Шиллера чаще всего используется для дифференциальной диагностики заболеваний слизистой оболочки воспалительного и дегенеративно-дистрофического характера.
Окраска гематоксилином по А. Б. Дережне — раствором гематоксилина смазывают слизистую оболочку в течение 2—3 мин. Реакция основана на способности гематоксилина восприниматься ядрами клеток. Атипический эпителий окрашивается в темно-фиолетовый цвет, а нормальный в бледно-фиолетовый. Разность интенсивности в окраске объясняется увеличением количества ядерной субстанции при раке.
Окраска толуидиновым голубым является наиболее информативным методом, указывающим на наличие у больного злокачественного опухолевого роста. Применяют 1 % раствор толуидиного голубого, прикладывая его на ватном тампоне с экспозицией 2—3 мин на участок подозрительный в отношении опухолевого роста. Препарат интенсивно воспринимается ядрами клеток, количество которых в значительной степени возрастает при наличии опухолевого роста. Окрашивание эпителия в темно-синий цвет дает возможность с большой достоверностью говорить о наличии злокачественной опухоли.
Положительный результат стоматоскопии позволяет поставить диагноз рака на ранних стадиях и своевременно направить его в специализированное учреждение для дальнейшего обследования и лечения.
Цитологический метод — основан на микроскопическом изучении клеток, полученных из патологического очага. Забор материала можно произвести путем соскоба, мазка-отпечатка, пункции. При папилломатозных, эрозивных и язвенных поражениях наилучшие результаты достигаются при взятии материала путем соскоба. Для этого шпателем, экскаватором или другим аналогичным инструментом производят поскабливание по поверхности опухоли, предварительно произведя анестезию. Полученный материал помещают на обезжиренное предметное стекло, маркируют его и заполняют направление на цитологическое исследование. Ответ цитолога может носить описательный характер, без указания характера патологического процесса, но если клиническая картина соответствует злокачественному процессу, то несмотря на отрицательный ответ больного следует направить на консультацию в специализированное онкологическое учреждение.
Биопсия — метод, позволяющий взятие ткани для гистологического исследования и являющийся одним из самых достоверных, позволяющий поставить диагноз на основании изучения тканевого среза. Биопсия является серьезным вмешательством и при отсутствии опыта, несоблюдении правил выполнения биопсии, может повлечь ряд нежелательных осложнений. Если диагноз злокачественной опухоли не вызывает сомнений, то биопсию выполнять не следует, а больного, не теряя времени на дополнительное исследование, направляют в специализированное учреждение.
В условиях стоматологической поликлиники выполнение биопсии целесообразно для проведения дифференциальной диагностики, когда клиническая картина в большей степени соответствует неопухолевой природе патологического процесса. При выполнении биопсии необходимо хорошее обезболивание, целесообразно проведение проводниковой анестезии, так как инфильтрационная нарушает принципы абластики. Участок тканей для гистологического исследования следует брать на границе патологического участка и видимо здоровых тканей. При обнаружении опухоли исследование этого участка позволяет морфологу выявить основные признаки злокачественной опухоли.
Важным звеном в профилактике злокачественных опухолей челюстно-лицевой локализации является формирование онкологической настороженности у врачей-стоматологов. При своей практической деятельности врач-стоматолог должен выполнять и помнить следующее:
- у каждого обратившегося больного независимо от предъявляемых жалоб должен быть произведен тщательный осмотр слизистой оболочки органов полости рта и исключить наличие опухоли и предраковых заболеваний;
- при атипичном течении заболевания следует шире пользоваться консультативной помощью;
- при подозрении на наличие злокачественной опухоли больного следует сразу же направить на консультацию в специализированное онкологическое учреждение;
- все больные с впервые установленным диагнозом злокачественной опухоли в поликлинике подлежат обсуждению на врачебной конференции с целью формирования онкологической настороженности;
- при выполнении амбулаторных операций все удаляемые ткани, в том числе и грануляции из лунок следует в обязательном порядке направлять на гистологическое исследование;
- при обследовании больных из групп риска и с предопухолевыми заболеваниями следует шире использовать метод стоматоскопии.
"Заболевания, повреждения и опухоли челюстно-лицевой области"
под ред. А.К. Иорданишвили
Читайте также: