Для гистологической диагностики рака предстательной железы
- English
- Русский







































Главное меню
- Редакционная коллегия
- Редакционный совет журнала
- Архив
- База авторов
- Порядок рецензирования статей
- Информация для авторов
- Информация для рекламодателей
- Издательский дом
- Политика редакции
- Обратная связь
Главное меню
- Редакционная коллегия
- Редакционный совет журнала
- Архив
- База авторов
- Порядок рецензирования статей
- Информация для авторов
- Информация для рекламодателей
- Издательский дом
- Политика редакции
- Обратная связь
В настоящее время золотым стандартом диагностики рака предстательной железы (РПЖ) является гистологическая оценка биоптатов, полученных при трансректальной тонкоигольной мультифокальной биопсии предстательной железы (ПЖ) под контролем ультразвукового исследования [1,2,3]. Биоптаты ПЖ являются одним из самых сложных материалов для гистологической оценки. Морфологическая идентификация минимального фокуса аденокарциномы представляет значительную сложность в связи с необходимостью дифференциальной диагностики микрофокуса аденокарциномы с большим количеством доброкачественных состояний.
В настоящее время широко распространена биопсия из 10-14 точек [4,5]. В ряде случаев при наличии в анамнезе пациента простатической интраэпителиальной неоплазии или атипической мелкоацинарной пролиферации выполняется сатурационная биопсия ПЖ. Несмотря на то, что накоплен немалый опыт выполнения биопсии ПЖ в некоторых учреждениях биоптаты из левой и правой долей погружаются в два, отдельно маркированных, контейнера. Соответственно, при работе с гистологическим материалом в лаборатории биоптаты из одной доли помещаются в один блок и, таким образом, на микропрепарате оказывается несколько (от 3 и больше) фрагментов ткани ПЖ. Множество столбиков в одной кассете приводит к неравномерной заливке парафином биопсийного столбика и может вызвать потерю значительного количества материала для гистологического исследования и к большому количеству артефактов. Европейской и Американской ассоциациями патологов рекомендовано размещение на микропрепарате не более одного столбика ткани. Это не только позволяет сохранить длину биоптата и свести к минимуму количество артефактов, но и помогает спланировать постановку игл при брахи- и (или) криотерапии, решить вопрос об объеме предстоящей операции или спланировать ход повторных биопсий с прицельным забором большего количества фрагментов 10.
Следующим этапом работы с биопсийным материалом является макроскопическое описание столбиков тканей с последующим формированием патологоанатомического заключения. В мире приняты следующие диагнозы для оценки биоптатов ПЖ [6,7]:
- Аденокарцинома предстательной железы;
- Фокус, подозрительный в отношении аденокарциномы предстательной железы (атипическая мелко-ацинарная пролиферация);
- Простатическая интраэпители-альная неоплазия высокой степени;
- Нет данных за злокачественное образование.
В большинстве случаев злокачественные новообразования ПЖ представляют собой ацинарную аденокарциному. При формировании патологоанатомического заключения описывается длина каждого биоптата и процент протяженности опухоли в каждом из биоптатов; степень дифферен-цировки опухоли по системе градации Глисона; общее количество биоптатов с аденокарциномой; локализация опухоли, согласно схеме, предоставленной урологами; наличие опухоли в пери-простатической жировой ткани; наличие периневральной инвазии.
Протяженность опухолевой ткани в биоптатах подсчитывается в процентах. Расчет заключается в делении общей протяженности пораженной ткани биоптата на общую длину биоптата за исключением длины перипростатической ткани.
В биоптат ПЖ может попасть перипростатическая ткань и ткань семенных пузырьков, что позволяет патологу диагностировать экстрапрос-тическую инвазию и инвазию в семенные пузырьки.
Степень дифференцировки аденокарциномы ПЖ производится согласно шкале Глисона. Основным принципом данной шкалы является просмотр биоптатов под малым увеличением (объективы 4х-10х) с преимущественной оценкой тканевой атипии 11. За редким исключением РПЖ имеет неоднородную структуру [12,13,16,17]. Поэтому для того, чтобы подсчитать показатель Глисона при исследовании ткани ПЖ после биопсии суммируют две наиболее высоких градации, с указанием их процентного соотношения. Полученное число баллов служит важным прогностическим критерием, позволяющим предположить более быстрое прогрессирование заболевания, метастази-рование и снижение выживаемости.
Классификация Глисона остается стандартным подходом в гистологической градации аденокарциномы предстательной железы. Изменения, внесенные в классификацию Глисона в 2004 году, так же учтены и в классификации 2016 года. Существенным дополнением классификации 2016 года явилась рекомендация указывать процент 4 балла в случае суммы баллов 7, а так же введены так называемые прогностические группы.
В 2014 году, международное общество уропатологов (ISUP) модифицировало классификацию Глисона. Основные выводы следующие:
- решетчатые (крибриформные) структуры должны быть отнесены к баллу 4;
- железы с гломеруляциями должны быть отнесены к баллу 4;
- оценка муцинозной аденокарциномы ПЖ должна быть основана на ее основном характере роста.
В прошлом в некоторых случаях крибриформная аденокарцинома была оценена как балл 3, в соответствии с классификацией ВОЗ 2004 года редкие решетчатые железы могли быть оценены как балл 3. Однако последние данные показали, что крибриформная аденокарцинома является независимым фактором прогноза биохимического рецидива после радикальной простатэктомии (РПЭ), метастазирования после РПЭ и раковоспецифической выживаемости 18. Поэтому все крибриформные структуры принято относить к 4 баллу. Еще одним изменением в классификации ВОЗ 2004 года является то, что плохо сформированные железы относятся к баллу 4. В настоящее время балл 4 включает: решетчатые железы, сливающие железы, плохо сформированные железы, железы с гломеруляциями. В рекомендациях 2016 года требуется указывать процент балла 4 при сумме баллов 7 в патологических ответах биопсии ПЖ и в патологических заключениях после РПЭ, в рекомендациях ВОЗ 2004 года, патологические заключения, указывающие балл 4/5, не часто встречались в клинической практике. Указание процента 4 балла может иметь решающее значение в планировании дальнейшего лечения. Так, например, некоторым пациентам с суммой баллов 3+4=7, при низком проценте 4 балла, может быть предложено активное наблюдение. Множество данных, позволяет предположить, что указание процента аденокарциномы таких высоких грейдов как 4 и 5, является важным прогностическим показателем. Однако, метод, который необходимо использовать для определения процентного соотношения, не уточняется.
Недавно был разработан перечень прогностических групп. На конгрессе международного общества уропатологов в 2014 году состоялся консенсус с участием широкого круга патологов и клиницистов, на котором была предложен новый взгляд на использование шкалы Глисона, подразумевающий создание прогностических групп от 1 до 5 на основании суммы баллов градации Глисона и прогноза для пациента:
Группа 1: Сумма баллов, согласно градации Глисона 3+3=6;
Группа 2: Сумма баллов, согласно градации Глисона 3+4=7;
Группа 3: Сумма баллов, согласно градации Глисона 4+3=7;
Группа 4: Сумма баллов, согласно градации Глисона 4+4=8, 3+5=8, 5+3=8;
Группа 5: Сумма баллов, согласно градации Глисона 9-10.
Есть несколько оснований для создания групп: сумма баллов 2 и 5 не используется или используется крайне редко, баллы шкалы Глисона были сформированы достаточно давно с использованием других механизмов, определяющих факторы прогноза. Кроме того, группа 1 обозначает для клинициста и пациента, что сумма баллов 6 является минимально возможной из 6 групп, а не указывает на некую среднюю сумму баллов от 1 до 10. Данное положение является критическим и информирует все заинтересованные стороны, о том, что аденокарцинома ПЖ балл 1 имеет благоприятный прогноз. Таким образом, пациенты из группы 1 с учетом клинических данных (уровень ПСА сыворотки крови, клиническая стадия заболевания, количество опухоли в ткани всех биоптатов ткани ПЖ) могут быть кандидатами на активное наблюдение. Прогностическая значимость пяти групп была подтверждена в крупном исследовании с участием множества институтов. Было исследовано более 20 000 случаев РПЭ, более 16 000 случаев тонкоигольных биопсий ПЖ и более 5000 биопсий с последующей лучевой терапией [21]. Интересно так же, что существуют геномные корреляции в поддержку формирования данной групповой оценки прогноза заболевания [22]. В связи с чем, согласно рекомендациям ВОЗ 2016 г., прогностический балл в патологоанатомическом ответе необходимо указывать наряду с общепринятой градацией по шкале Глисона с учетом ее изменений в 2014 году.
ВЫВОДЫ
1. При выявлении атипической мелкоацинарной пролиферации рекомендовано выполнение повторной биопсии.
2. Сумма баллов по системе градации Глисона 2-4 всегда является заниженной и некорректной. Под этим диагнозом может скрываться аденокарцинома с суммой баллов 6 или аденоз (атипическая аденоматозная гиперплазия). Сумма баллов 5, практически всегда является заниженной и будет выше после радикальной простатэктомии.
3. При нескольких позитивных биоптатах, содержащих различные степени дифференцировки по системе градации Глисона, суммируются две наиболее высокие градации.
4. Средняя длина столбика ПЖ на микропрепарате должна составлять не менее 1 см.
5. Частота диагностики атипической мелкоацинарной пролиферации не должна превышать 5%.
6. Рекомендовано выполнять забор биопсийных столбиков согласно карте биопсии ПЖ, когда каждый биопсийный столбик погружается в отдельный маркированный контейнер.
7. Рекомендовано размещать на одном микропрепарате не более одного столбика ткани.
8. В патологоанатомическом ответе необходимо указывать прогностический балл наряду с общепринятой градацией по шкале Глисона с учетом ее изменений в 2014 году.
Работа выполнена при поддержке РНФ, соглашение № 14-15-01120.
ЛИТЕРАТУРА
1. Rogatsch H, Moser P, Volgger H. Diagnostic effect of an improved preembedding method of prostate needle biopsy specimens. Hum Pathol 2000; 31(9):1102-1107.
2. Delahunt B, Nacey JN. Broadsheet number 45: thin core biopsyof prostate. Pathol 1998; 30:247-256.
3. Ohori M, Kattan M, Scardinio PT. Radical Prostatectomy for carcinoma of the prostate. Mod Pathol 2004; 17(3):349-359.
4. Srigley JR, Jones B, Kapusta L. The effect of specimen submission protocols on the detection rate of histologic abnormalities in sextant prostate biopsies (abstract). Mod Pathol 2001; 14:123.
5. Lane RB, Lane CG, Mangold KA. Needle biopsy of prostate. What constitutes adequate histologic sampling? Arch Pathol Lab Med 1998; 122:833-835.
6. Murthy WM, Ramsey J, Soloway MS. A better nuclear fixative for diagnostic bladder and prostate biopsies. J Urol Pathol 1993; 1:79-87.
7. Boccon-Gibod L, van der Kwast TH, Montironi R, Boccon-Gibod L, Bono A. Handling and reporting of prostate biopsies. Eur Urol 2004; 46(2):177-181.
8. Reyes AJ, Humphrey PA. Diagnostic effect of complete histologic sampling of prostate needle biopsy specimens. Am J Clin Pathol 1998; 109:416-422.
9. Kao J, Upton M, Zhang P, Rosen S. Individual prostate biopsy core (Bc) embedding facilitates maximal tissue representation. J Urol 2002; 168(2):496-499.
10. Brat DJ, Wills ML, Lecksell KL, Epstein JI. How often are diagnostic feartures missed less extensive sampling of prostate needle biopsy specimens? Am J Surg Pathol 1999; 23:257-262.
11. Humphrey P. A. Prostate pathology. Chicago. 2007, 556 p.
12. Coard KS, Freeman VL. Gleason grading of prostate cancer: : level of concordance between pathologists at the University Hospital of the West Indies. Am J Clin Pathol 2004; 122:373-376.
13. Gleason DF. Histologic grading of prostate cancer: a perspective. Hum Pathol 1992; 23:273-279.
14. Cangiano TG, Litwin MS, Naitoh J, Dorey F, deKernion JB. Intraoperative frozen section monitoring of nerve sparing radical retropubic prostatectomy. J Urol 1999; 162(3 Pt 1):655-658.
15. Epstein JI. Pathologic assessment of the surgical specimen. Urol Clin North Am 2001; 28(3):567-594.
16. Humphrey PA. Gleason grading and prognostic factors in carcinoma of the prostate. Mod Pathol 2004; 17:292-306.
17. Gleason DF, Mellinger GT. Prediction of prognosis for prostatic adenocarcinoma by combined histological grading and clinical staging. J Urol 1974; 111 (1):59-64.
18. Kir G, Sarbay BC, Giimiij E, Topal CS. The association of the cribriform pattern with outcome for prostatic adenocarcinomas. Pathol Res Pract 2014;210(10):640-644. doi: 10.1016/j.prp.2014.06.002
19. Dong F, Yang P, Wang C, Wu S, Xiao Y, McDougal WS, et al. Architectural heterogeneity and cribriform pattern predict adverse clinical outcome for Gleason grade 4 prostatic adenocarcinoma. Am J Surg Pathol 2013; 37(12):1855-1861. doi: 10.1097/PAS.0b013e3182a02169.
20. Kweldam CF, Wildhagen MF, Steyerberg EW, Bangma CH, van der Kwast TH, van Leen-ders GJ. Cribriform growth is highly predictive for postoperative metastasis and disease-specific death in Gleason score 7 prostate cancer. Mod Pathol 2015; 28(3):457-464. doi: 10.1038/mod-pathol.2014.116.
21. Epstein JI, Zelefsky MJ, Sjoberg DD, Nelson JB, Egevad L, Magi-Galluzzi C, et al. A contemporary prostate cancer grading system: a validated alternative to the Gleason score. Eur Urol 2016; 69(3):428-435. doi: 10.1016/j.eururo.2015.06.046
22. Rubin MA, Girelli G, Demichelis F. Genomic correlates to the newly proposed grading prognostic groups for prostate cancer. Eur Urol 2016;69(4):557-560. doi: 10.1016/ j.eururo.2015.10.040.
Работа выполнена при поддержке РНФ, соглашение № 14-15-01120.
Диагностика рака предстательной железы является первоначальным и необходимым мероприятием для мужчин, у которых наблюдаются проблемы с простатой. Будучи на втором месте после рака легких, рак (карцинома) простаты ежегодно уносит десятки тысяч жизней. Высокий процент смертности от этой болезни медики напрямую связывают с поздним выявлением онкологии, когда болезнь уже находится на этапе метастазирования и у больного, к сожалению, невысокие шансы на выздоровление.
- Комплексное обследование
- Как отличить добро от зла
- Пальцевой осмотр
- Сканирование
- Лабораторные методы
- Анализ крови на ПСА
- Осмотр клеток под микроскопом
Комплексное обследование
Диагностика рака предстательной железы — это комплексное мероприятие, начинающееся в кабинете врача и заканчивающееся в диагностической лаборатории. Классическое обследование мужчин с подобными жалобами, особенно в возрасте от 45 лет, состоит из нескольких ступеней:
- Опрос больного и внимательный осмотр.
- Ректальное пальцевое обследование.
- Ультразвуковое исследование (УЗИ) железы.
- Биохимический анализ на ПСА.
- Гистологическая диагностика.
Поводом для посещения уролога должны быть любые появившиеся нарушения в работе организме, особенно это касается мужчин старшего возраста. Первыми характерными признаками возникновения увеличения простаты являются нарушение мочеиспускания, проблемы с половой функцией и возникающий при этом дискомфорт. При сдавливании растущей железой мочеиспускательного канала происходит нарушение нормального оттока мочи, следствие которого:
Такие жалобы типичны при доброкачественном процессе предстательной железы — аденоме, а также могут наблюдаться у мужчин при второй стадии рака простаты. Поэтому чем раньше будет дифференцирован доброкачественный и злокачественный процесс, тем быстрее больной получит необходимую помощь и тем больше у него будет шансов на полное выздоровление. Задача врача — быстро и правильно отличить аденому простаты от рака, это определяет дальнейшую тактику лечения и от этого зависит жизнь пациента.

Задайте вопрос врачу-урологу!

В диагностике рака простаты специалисты используют методы, позволяющие не только более детально рассмотреть проблемное место у мужчин. Качественное ультразвуковое обследование определяет место локализации опухоли, ее параметры, структуру и другие особенности. Биохимические и гистологические методы способны определить невидимые глазу изменения в организме и степень развития болезни, что облегчает врачу возможность сделать выводы об общем состоянии здоровья его пациента.
При первичном обращении мужчин к урологу проводится обязательная процедура — трансректальный пальцевой осмотр, который позволяет сделать предварительное заключение о характере течения заболевания.
Но одного пальпаторного обследования для окончательного выставления диагноза недостаточно, пациент должен пройти УЗИ и сдать кровь на простатический специфический антиген ПСА, своеобразный маркер онкологического процесса.
Третья стадия рака характеризуется распространением злокачественного процесса на близлежащие органы и появлением дополнительной симптоматики:
- Неравномерное увеличение органа, опухоль растет наружу.
- Присутствие крови в моче и семенной жидкости.
- Появление болей в области лобка, промежности и появление недержания мочи.
- Длительное отсутствие эрекции.
Эти симптомы, как правило, определяются при осмотре, на основании жалоб больного, предполагается степень распространения болезни. Назначается дополнительная расширенная диагностика.
Четвертая стадия рака простаты считается запущенной и имеет совсем неблагоприятный прогноз. При этом отмечаются значительные метастазы в дальних органах. Отображается это сильными болями в позвоночнике, костях, отечностью в ногах, анемией и кахексией. Больной отмечает заметную потерю в весе, снижение физической активности, отсутствие аппетита, слабость и утомляемость.
Одним из важнейших информативных методов диагностики является трансректальный пальцевой осмотр мужчин, отмечающих нарушения нормального мочеиспускания. Осмотр проводится урологом непосредственно на приеме и является обязательной процедурой. Предстательная железа анатомически близка к прямой кишке, поэтому прощупать ее указательным пальцем не представляет труда.

Здоровый орган имеет небольшой размер, эластичен и не болит при надавливании во время пальцевого осмотра. У здоровых мужчин борозда, делящая железу на две равные доли, хорошо пальпируется. Прощупать можно и семенные пузырьки, располагающиеся по бокам простаты.
При диагностике доброкачественной аденомы железа ощутимо увеличена в размерах, имеет некоторую сглаженность борозды, но сохраняется ее эластичность и отсутствует болезненность при надавливании. Это состояние дифференцируют с простатитом, при котором орган немного увеличен и уплотнен в результате воспалительного процесса, при этом также отмечаются некоторые болевые ощущения при пальцевом надавливании.
- Существенное неравномерное увеличение размеров органа.
- Врачом при пальпации определяется его высокая плотность.
- Наблюдается асимметричность борозды, доли неравные.
- Ощущение резкой боли от пальцевого прижатия.
Очередной осмотр пациента с раком предстательной должен проводиться с особым вниманием. Малейшее ухудшение внешнего вида, потеря в весе, изменение цвета кожи и увеличение лимфатических узлов могут указывать на прогрессирование болезни. Кроме основного урологического осмотра, проводится пальпация печени.
Ультразвуковое исследование УЗИ — наиболее популярный безопасный неинвазивный метод диагностики посредством ультразвуковых волн. УЗ сканером высокого класса можно получить достоверную информацию о внутренних органах человека, а именно — точно узнать их расположение, параметры, особенности структуры и кровоснабжение. Результат становится известным сразу после обследования.
Ультразвуковая диагностика предстательной железы в современной урологической практике может выполняться несколькими методами.
- Наружным — через стенку брюшины или промежность.
- Трансректальным — диагностика через прямую кишку.
- Трансуретральным — диагностика через уретру.
Наружная УЗИ-диагностика рака простаты — доступный и самый распространенный вариант, имеет небольшое неудобство: мочевой пузырь пациента на время осмотра должен быть полным, поэтому пациенту необходимо перед обследованием его наполнить, выпив около 1,5 л жидкости.
Сканирование проводится в поперечной, продольной и произвольной плоскости. Легко переносится и не имеет особых противопоказаний (исключение — наличие послеоперационной раны). Недостаток диагностики наружного ультразвукового сканирования — это слабая разрешающая способность, позволяющая определить только размеры железы и ее форму, и недостаточно точный результат. Цена этого метода диагностики находится в пределах 500 рублей.
Трансректальное УЗИ, или ТРУЗИ, является более информативным и удобным методом диагностики, так как позволяет обнаружить минимальные изменения структуры органа по периферии и не требует наполнения мочевого пузыря. Результаты ТРУЗИ расцениваются урологами как более полные. Цена методики находится в пределах 1500–3500 рублей и зависит от рейтинга клиники и класса диагностического оборудования.
Трансуретральное ультразвуковое исследование (ТУУЗИ) применяется редко, так как подразумевает введение датчика через уретру. Диагностическая процедура болезненна и проводится только под анестезией, существует риск при исследовании травмировать уретру. Главное достоинство метода — это возможность получить четкую и полную визуализацию предстательной железы.
Лабораторные методы
Диагностика карциномы простаты невозможна без биохимических анализов и гистологического исследования. Анализ на количество ПСА — простатического специфического антигена — несет ценную информацию о начале развития злокачественного процесса и позволяет определить рак простаты на ранних этапах, когда явно видимых отклонений от нормы визуально определить невозможно.
Обширный ряд исследований онкологической урологии и отзывы практикующих врачей доказали, что появление и рост карциномы в предстательной железе всегда сопровождается увеличением концентрации ПСА в сыворотке крови. Сам по себе простатический антиген — это вещество белковой природы, содержание в крови его достаточно лабильное и может периодически изменяться под действием разных причин. Но клинически доказано, что при раке предстательной железы концентрация ПСА всегда повышена.

Увеличение ПСА не всегда имеет злокачественное происхождение. Воспаление предстательной железы, вызванное инфекционным агентом, ДГПЖ или недавняя эякуляция могут также вызвать повышение его уровня в крови.
На сегодняшний день анализ на ПСА является обязательным для мужчин, состоящих в группе риска. Назначают его как с диагностической целью, так и с целью контроля эффективности химиотерапевтического лечения при раке у неоперабельных больных. Референтные показатели ПСА колеблются с возрастом. Нормальные показатели простатического антигена зависят от возраста:
- У мужчин до пятидесяти лет — не больше 2,4 нг/мл.
- 50-60 лет — не выше 3,4 нг/мл.
- После семидесяти — 6,4 нг/мл.
Средняя цена анализа ПСА — 340 рублей.
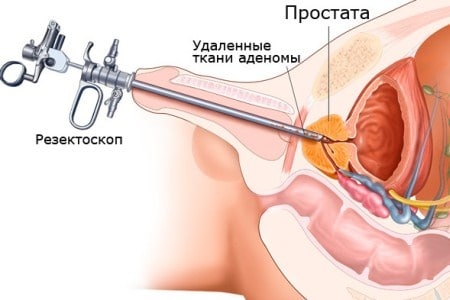
Последним этапом комплексной диагностики рака предстательной железы служит гистологический анализ, или биопсия, во время которой проводится выборочный забор биоматериала из опухоли предстательной железы для морфологического анализа клеток пораженных тканей под микроскопом с целью определения раковых клеток.
Трансректальную биопсию назначают в случае предположения рака предстательной железы. Процедура выполняется параллельно с УЗИ, позволяющим контролировать процесс забора материала с большого количества участков. Выглядит эта манипуляция так:
Биоматериал в дальнейшем исследуется в гистологической лаборатории с целью выявления/исключения раковых клеток. Диагностика при гистологическом исследовании напрямую зависит от количества заборов с различных участков. Чем больше заборов с разных участков органа, тем достовернее и точнее результат. Обычно таких участков больше десяти.
Диагностика карциномы предстательной железы порой занимает достаточно много времени. Иногда обследование нужно повторить, так как предыдущее не удовлетворяет врача. К примеру, недостаточно информативный гистологический анализ, в результате которого были рассмотрены не те участки ткани. Такое бывает, когда биопсию проводили вручную, без современного оборудования, позволяющего более точно определить пораженное место. Или изначально неверно была определена зона обследования и получен ложный результат. Проблему представляют также небольшие размеры онкологического образования, которые сложно обнаружить на УЗИ или определить, где лучше взять забор материала.
Даже если рак предстательной железы диагностирован, процесс обследования может продолжиться на протяжении всего лечения и реабилитации. Это необходимо для более детального представления о течении болезни и определении эффективности лечебного процесса, который состоит из хирургических и химиотерапевтических мероприятий.
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.
Читайте также:

