Веретеноклеточная саркома мягких тканей лечение прогноз
Злокачественную опухоль представляет недифференцированная ткань, к которой относится саркома. Виды:
- круглоклеточная;
- веретеноклеточная;
- полиморфноклеточная саркома;
- плеоморфная;
- гигантоклеточная.
Веретеноклеточная саркома – это зрелая саркома, которая по структуре представляет переплетение волокнистых нитей и густая по консистенции. Как и рак, упомянутая саркома представляет собой опухоль. Злокачественный процесс поражает слизистые оболочки и кожу. Если лечить на ранних стадиях – прогноз наилучший.
Веретеноклеточную саркому используют для характеристики редкого рака костной ткани. Развиваться может у людей старше 40-50 лет. В молодом возрасте как правило не встречается. Для лечения применяют методику борьбы с остеогенной саркомой. Часто для характеристики веретеноклеточной саркомы используют термин: злокачественная фиброзная гистиоцитоксантома.
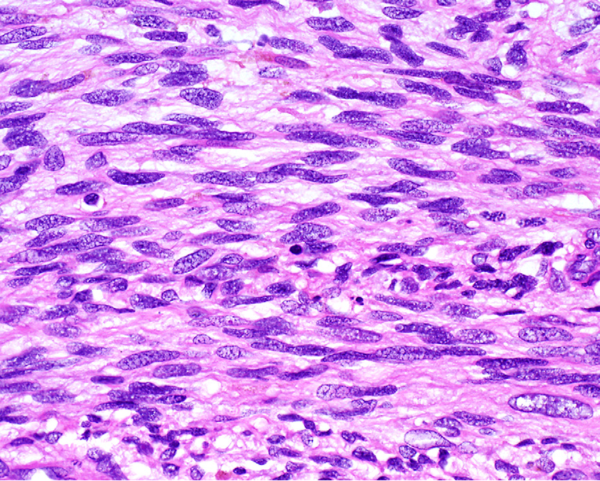
Микропрепарат – злокачественное веретенообразное образование, окрашенное гематоксилином и эозином. Клетки овальной формы, ядро с острыми концами. Клетки могут состоять из ядер неправильной формы. Соединительный процесс осуществляется за счёт веретенообразной ткани.
Симптомы
Общими характерными симптомами признаны:
- Быстрая утомляемость.
- Постоянная слабость.
- Резкое снижение веса.
- Опухоль визуально видима, выступает над поверхностью.
- Деформация и отечность поражённых тканей.
- Если веретеноклеточная опухоль заденет нервные окончания, появится боль.
В начале болезни симптоматика скудная, со временем приобретает характерные признаки. Всё зависит от локализации новообразования.
Разновидность веретеноклеточной саркомы
Среди разновидностей злокачественных новообразований мягких тканей неспецифированная фиброзная гистиоцитома встречается у большей части пациентов. Поражает такая саркома: соединительные ткани туловища, конечностей. Поражение веретенообразной саркомой забрюшинного пространства происходит редко. Развиваться такое новообразование может в глубине соединительной ткани, что ухудшает диагностику.
Новообразования, относящиеся к фиброзной гистиоцитоме, известны нескольких типов:
- гигантоклеточная;
- ииксоидная;
- воспалительная;
- типичная.
Явной чертой фиброзной злокачественной гистиоцитомы признаётся периодический рост, частые рецидивы. Типичная форма клеток включает в себя веретенообразный вид клеточной ткани, напоминающий фибробласты.
Симптоматика болезни зависит от места образования саркомы. Если опухоль локализуется наружно (на плечах, бёдрах), образуется уплотнение на теле диаметром 10 сантиметров. Внешний слой кожи над образованием краснеет. Если место локации в забрюшинном пространстве, вероятные признаки заболевания:
- сонливость, возможна потеря сознания;
- плохой аппетит;
- резкое снижение массы тела;
- повышение температуры;
- болезненные ощущения в области живота.

При появлении первых признаков фиброзной гистиоцитомы необходимо сделать диагностическое исследование, которое включает детальную диагностику новообразования. Томография установит характер патологии, определит метастазы, способные поразить головной мозг, печень или лёгкие.
Ультразвуковое обследование предоставит информацию обо всех особенностях фиброзной гистиоцитомы, а также оценит появление метастатического лимфогенного процесса.
Одним из самых важных методов обследования является микроскопическое изучение анализов. Изучение биопсии поставит точный диагноз и определит правильное лечение больного.
Современная медицина не способна сказать о факторах, провоцирующих появление заболевания, но выделяет несколько случаев, способствующих возникновению болезни:
- Наследственно-генетическая предрасположенность.
- Ослабленная иммунная защита организма.
- Взаимодействие с сильно токсичными веществами.
- Травмированные кожные покровы.
Морфологическое исследование
Морфологическая диагностика – очень сложный процесс вследствие больших различий опухолей, даже внутри одного подтипа. Выделяют больше 100 видов, которые требуют индивидуального лечения.
Характеристики сарком мягких тканей строятся на определении от доброкачественной опухоли без проявления метастазов с медленным ростом, до злокачественных с высоким ростом метастазов.
Склонность к осложнениям у каждого вида опухолей зависит от уровня злокачественности. Разработаны две методики определения характеристики злокачественности: NCI, FNCLCC.
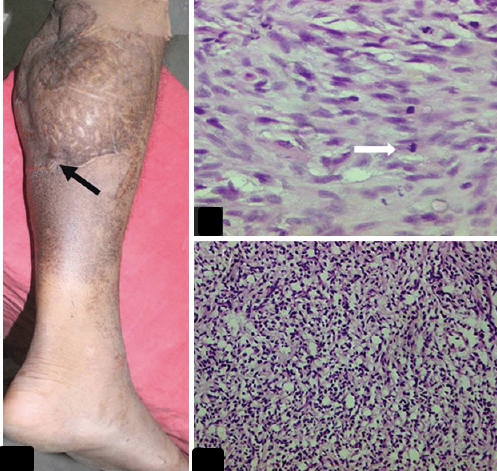
По методу NCI оцениваются гистологические группы, количество видимых клеток, плеоморфизм, количество поражённых органов и наличие явных мест воспаления.
- G1 – низкая степень злокачественности (высокодифференцированная опухоль): благоприятный прогноз, распространение на другие органы не происходит, реакции на химиотерапию нет.
- G2 – промежуточная степень злокачественности (умеренно дифференцированная опухоль).
- G3 – высокая степень злокачественности (низкодифференцированная опухоль): неблагоприятный прогноз, высокий потенциал метастазирования, в большинстве случаев чувствительна к препаратам химиотерапии.
По системе FNCLCC определяется трёхступенчатой методикой. Рассматривается сумма баллов, показывающая специфику клеток опухоли. Степени обеих систем совпадают.
Выявление уровня злокачественности – абсолютно субъективная процедура, поэтому предусмотрено классифицирование саркомы на 2 типа: высокой и низкой степени злокачественности.
Патогенез
Патогенез веретенообразной опухоли определяется генетическими факторами. Новообразование может быть единичным дефектом генома, так и следствием множественного нарушения в геноме.
В группу риска попадают люди с иммунодефицитными синдромами или принимающие средства, направленные на снижение защитных свойств организма.
Преимущественно в риске поражения оказываются:
- лёгкие;
- печень;
- кости;
- головной мозг.
Особенности распространения метастазов нужно знать для проведения терапевтических мероприятий и наблюдения за больным. Сроки проявления поражений разные для каждого вида образования. Рецидивы обычно появляются через пару месяцев, они либо схожи с удалённой саркомой, либо отличаются от неё по нескольким параметрам.
Этапы болезни
Выделяют 4 стадии протекания болезни. Для назначения правильного лечения полагается точно знать, на какой стадии развития находится веретеноклеточная саркома.
На первой стадии образование не распространяется за пределы поражённого органа. Размеры малы и роста не наблюдается. Болевой синдром отсутствует, метастазов нет. На этом этапе саркома хорошо лечится, даже если это высокодифференцированная клетка, образовавшаяся в лёгком или матке.
На соседние ткани не распространяется. Начинает проникать во все слои поражённого органа. Увеличивается размер. Возможно, появляются метастазы, образующиеся в лимфоузлах. Прогноз на полное выздоровление удовлетворительный, появление рецидива маловероятно.
Опухоль прогрессивно распространяется на соседние ткани. Проявляются симптомы (боль, дискомфорт в зоне поражения). Нарушается процесс кровоснабжения. Деформируется кость или кожные покровы в месте локации опухоли. При лечении на этой стадии возможны частые рецидивы.
Опухоль достигает огромных размеров, может распадаться и кровоточить. Метастазы поражают большую часть органов. Прогноз на выздоровление практически отсутствует.
Лечение
Веретеноклеточная саркома лечится комплексом терапевтических методик. Главное – хирургическое удаление. Лучевую терапию проводят после операции для удаления остатков новообразования. Химиотерапия проводится на всех стадиях лечения.
Комплекс мероприятий по лечению веретеноклеточной саркомы определяется исходя из полученной диагностической информации об опухоли: степень дифференциации, тип, на какой стадии находится опухоль и есть ли метастазы.
Перед операцией проводится микроскопическое изучение биоматериала саркомы. Удаляют опухоль скальпелем, и все соприкасающиеся с ней клетки. Если размер новообразования большой, то применяют дополнительный комплекс мер.
Для такого метода характерно применение облучающей терапии после удаления, ликвидирует оставшуюся ткань. Эффективно использовать, если нужно сохранить поражённые конечности. Однако лучевая терапия имеет сильные последствия в виде новых опухолей, поражения здоровых органов.
Инновационная методика удаления злокачественных опухолей. Наилучший исход прогнозируется на ранних стадиях лечения. Метод позволяет использовать сильное излучение, направленное только на злокачественные клетки.
Терапия чаще проходит до хирургического вмешательства и после. Бывают случаи, когда необходимо применить препараты во время операции.
Пересадка органов при обнаружении злокачественной опухоли запрещена.
По окончанию терапевтических процедур больному следует находиться под присмотром специалистов. Пациент продолжает получать симптоматическое лечение. Также проводят обследования: томография, УЗИ, рентген. Назначают поддерживающее лечение.
Следует после удаления веретеноклеточной саркомы ещё пару лет постоянно проходить обследование у онколога. Благодаря этому можно вовремя обнаружить осложнения после операции и вовремя назначить повторное лечение рецидива.
Диета после удаления
Диета после операции строится на ряде принципов.
- Приём пищи маленькими порциями, но часто, 5-6 раз в день. Перекусы и фаст-фуд исключить, могут плохо повлиять на состояние организма. Комплексно пропивать витаминные стимуляторы, минеральные вещества. Чаще включать в рацион овощи (термической обработки), фрукты (кроме цитрусовых). Больше пить свежих соков, кушать ягоды некислых видов и пить ягодные морсы.
- Печень животного происхождения содержит комплекс полезных веществ. Морковь, петрушка, тыква, перепелиное яйцо насыщены витамином А (антиоксидант), улучшают защитную работу организма..
- Постоянное применение крупы: гречиха, ячневая, геркулес. Полезны кедровый, грецкий и лесной орехи, обеспечивают нормальный клеточный обмен.
- Помидор, бобовые, свекла, брюссельская капуста и кисломолочная продукция играют главную роль в обновлении и росте клеток.
- Чтобы вывести вредные микроэлементы из организма, надо включить в рацион продукты с высоким содержанием витамина С, Е.
- Морская рыба, лук и чеснок предотвращают появление рецидивов.
- Чтобы поддержать гормональный баланс в организме, рекомендуется пища, насыщенная йодом. Можно рыбу или рыбий жир, а также йодированную соль применять для готовки.
- Воздержаться от употребления консервированных продуктов, полуфабрикатов, кондитерских изделий.
- Пиво и алкоголь запрещено употреблять.
- Воздержаться от потребления кислых продуктов, опухоль быстро размножается в кислой среде.
- Еда призвана содержать минимум быстрых углеводов, так как злокачественные клетки питаются глюкозой.
Саркомами называют опухоли, которые развиваются из клеток предшественниц соединительной ткани — мезодермы. Как и рак, они представляют собой злокачественные новообразования, но с той разницей, что источником раковой опухоли является эпителий, выстилающий внутренние органы и тело человека. Поэтому эти опухоли имеют привязку к конкретному органу, например, рак предстательной железы, рак молочной железы и др. Саркомы же развиваются из соединительной ткани и могут возникнуть в любом органе, где есть такие клетки, то есть фактически везде.
- Виды сарком мягких тканей
- Стадии развития
- Факторы риска
- Симптомы саркомы мягких тканей
- Диагностика саркомы мягких тканей
- Лечение саркомы мягких тканей
- Прогноз выживаемости при саркоме мягких тканей
Виды сарком мягких тканей
Саркома мягких тканей — это собирательный термин, который объединяет большое количество злокачественных опухолей, среди которых наиболее часто встречаются следующие:
- Лейомиосаркома — опухоль из гладкомышечных клеток.
- Рабдомиосаркома — опухоль из поперечно-полосатой мускулатуры.
- Липосаркома — злокачественная опухоль из жировой ткани.
- Ангиосаркома — злокачественное новообразование, произрастающее из ткани кровеносных сосудов.
- Фибросаркома — опухоль из фиброзной ткани.
Также саркомы мягких тканей принято разделять по степени злокачественности. Низкозлокачественные новообразования редко метастазируют, но склонны к упорному рецидивированию. Высокозлокачественные опухоли склонны давать метастазы гематогенным путем (с током крови), лимфатические узлы поражаются реже.
Стадии развития
Стадия саркомы мягких тканей определяется степенью злокачественности опухоли, ее размером и наличием метастазов.
- К 1 А стадии относят новообразования низкой степени злокачественности, размером менее 5 см, без метастазов в регионарных лимфатических узлы и отдаленных органах.
- 1 В стадия — опухоли низкой степени злокачественности, более 5 см без метастазов.
- 2А стадия — новообразования средней степени злокачественности, менее 5 см без метастазов.
- 2В стадия — новообразования средней степени злокачественности, более 5 см в наибольшем измерении, без метастазов.
- 3А стадия — саркомы высокой степени злокачественности, менее 5 см без поражения лимфатических узлов и внутренних органов.
- 3В стадия — саркомы высокой степени злокачественности, более 5 см без метастазов.
- 4 стадия — саркома любой степени злокачественности, любого размера при наличии поражения лимфатических узлов или метастазов во внутренних органах.

Факторы риска
В большинстве случаев, саркомы мягких тканей развиваются спонтанно, т. е. без видимых причин. Однако есть определенные обстоятельства, которые увеличивают вероятность развития данного заболевания:
- Воздействие химических канцерогенов, в частности гербицидов, хрорфенолов.
- Генетическая предрасположенность — нейрофиброматоз, синдром Ли-Фраумени, синдром Гарднера.
- Воздействие ионизирующего излучения, например, прохождение лучевой терапии.
- Иммунодефицитные состояния — иммуносупрессия после трансплантации органов, прохождение химиотерапии, СПИД.
- Некоторые виды сарком мягких тканей могут развиваться на фоне лимфостаза конечности.
Симптомы саркомы мягких тканей
На начальных этапах, саркома мягких тканей проявляется как безболезненная опухоль, которая медленно увеличивается в размерах. Может иметь капсулу, которая, впрочем, не мешает метастазированию. Также опухоль может иметь инфильтративный рост, в этом случае определить ее края проблематично.
При дальнейшем росте, симптоматика будет зависеть от локализации опухоли. Например, при саркомах матки будут кровотечения, при поверхностной локализации опухоль вызывает отечность и боли, при этом нарушается функция пораженного органа, например, руки или ноги.
Диагностика саркомы мягких тканей
В рамках диагностики саркомы мягких тканей проводится физикальное обследование, используются методы медицинской визуализации с последующим проведением биопсии и морфологического исследования полученного материала.
Обязательно проводится КТ или МРТ пораженной области. Во-первых, исследование помогает обнаружить опухоль, а во-вторых проконтролировать радикальность излечения.
Для постановки диагноза обязательно проводится морфологическое исследование фрагмента опухоли. Чтобы его получить, выполняют трепанбиопсию с помощью специальной толстой иглы под контролем УЗИ, или инцизионную биопсию, которая подразумевает хирургическое иссечение фрагмента новообразования. В ряде случаев, для уточнения типа саркомы необходимо более детальное исследование, тогда проводят иммуногистохимические и молекулярно-генетические анализы.
Для того чтобы установить степень распространения опухоли, проводят КТ грудной клетки, брюшной полости, а также ультразвуковое исследование лимфатических узлов.
Лечение саркомы мягких тканей
Выбор метода лечения саркомы определяется степенью ее злокачественности, местом расположения и наличием метастазов. Для лечения низкозлокачественных опухолей, лечение преимущественно хирургическое, в остальных случаях используются комбинированные методы, включающие облучение и химиотерапию.
При хирургическом лечении сарком используются следующие виды операций:
- Широкая местная резекция. Таким способом удаляются низкозлокачественные небольшие новообразования, располагающиеся в коже и подкожной клетчатке.
- Широкое иссечение. При таком вмешательстве саркома удаляется в пределах анатомической зоны, отступая от края новообразования не менее чем на 4-6 см.
- Радикальная органосохраняющая операция. При таком объеме вмешательства удаляется опухоль совместно с мышечными фасциями и неизмененными мышцами, которые отсекаются в месте их прикрепления. При вовлечении в процесс кровеносных сосудов, нервных стволов и костей, производят их резекцию с одномоментной пластикой кожным или кожно-мышечным лоскутом.
- Ампутации или экзартикуляции — удаление конечности или ее вычленение по линии суставной щели. Такие вмешательства проводятся при обширных местно-распространенных высокозлокачественных процессах с вовлечением магистральных кровеносных и нервных стволов на большом протяжении, а также костных структур и мышц.
Во время операции обязательно проводится интраоперационное срочное гистологическое исследование. При наличии злокачественных клеток в краях отсечения и при потенциальной возможности радикального удаления опухоли, выполняют реоперацию.
Лучевая терапия применяется в рамках комбинированного лечения в предоперационном и/или послеоперационном этапе. В первом случае преследуется цель — уменьшение размера саркомы и создание условий для проведения радикального вмешательства. Во втором — уничтожение оставшихся злокачественных клеток. Чтобы воздействие на опухоль было равномерным, используются многопольные методики облучения.
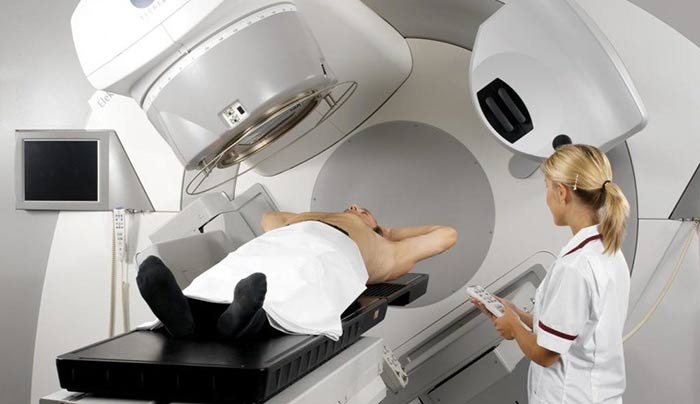
Предоперационная лучевая терапия
При предоперационной ЛТ, границы полей облучения (ПО) должны выходить за размеры ткани опухоли минимум на 3-4 см. Если опухоль имеет большие размеры, производят облучение в пределах 10 см от ее края до достижения суммарной очаговой дозы 45-50Гр. Затем ПО сокращают до размеров новообразования.
Если опухоль располагается на конечности, есть вероятность развития остеолучевого некроза, мышечных контрактур и отеков. Чтобы этого избежать, рекомендуется облучать не более 2/3 окружности конечности, если это возможно. Минимальная толщина необлучаемых тканей в зоне предплечья составляет 2 см, на бедре 4 см, и на голени — 3 см.
Послеоперационная лучевая терапия
Послеоперационная лучевая терапия показана в следующих случаях:
- Высокая степень злокачественности саркомы по данным гистологического исследования.
- Нерадикально проведенная операция — наличие злокачественных клеток в краях отсечения при невозможности проведения реоперации.
- Вскрытие капсулы саркомы во время хирургического вмешательства.
Послеоперационную ЛТ начинают выполнять не позднее, чем через 4 недели после окончания хирургического лечения.
Если предоперацинная ЛТ не выполнялась, поля облучения включают в себя следующие области:
- Ложе опухоли.
- Ткани, которые располагаются на расстоянии 2 см от удаленной опухоли.
- Послеоперационный рубец.
Облучение проводят в суммарной очаговой дозе 60 Гр. Если была проведена нерадикальная операция, дозу увеличивают до 70 Гр. В аналогичном режиме проводят лучевую терапию при невозможности оперативного лечения.
Химиотерапия широко используется для лечения высокозлокачественных сарком мягких тканей. Как и при лучевой терапии, ее могут назначать на дооперационном и/или послеоперационном этапе. Неоадъювантная (предоперационная) ХТ призвана воздействовать на очаг опухоли, уничтожать микрометастазы и создать условия для органосохраняющего хирургического лечения. С этой целью проводят 2-3 курса химиотерапии с перерывом в 3-4 недели.
Послеоперационная ХТ может проводиться для уничтожения микрометастазов или уже визуализируемых метастазов. С этой целью выполняют 3-4 курса лечения. При химиотерапевтическом лечении сарком применяют различные комбинации следующих препаратов:
- Доксорубицин.
- Этопозид.
- Винкристин.
- Ифосфамид.
- Дакарбазин.
- Цисплатин и др.
Схема химиотерапии будет определяться морфологическим вариантом опухоли и ее чувствительностью к ранее проводимому лечению.
Прогноз выживаемости при саркоме мягких тканей
Прогноз выживаемости зависит от многих факторов:
- Степень злокачественности саркомы. Наиболее благоприятное течение у низкозлокачественных сарком без метастазов во внутренних органах и лимфоузлах.
- Размеры опухоли.
- Возможность проведения радикального лечения.
- Возраст больного. Наиболее благоприятные прогнозы у детей. У них полного выздоровления удается достичь в 60% случаев. Наименее благоприятные прогнозы у людей старше 60 лет.
При своевременном лечении начальных стадий низкозлокачественных сарком мягких тканей, удается достичь 5-летней выживаемости у половины больных. При 4 стадии процесса, этот показатель не превышает 10%.
Эффективных методов профилактики саркомы мягких тканей нет. Общие рекомендации являются стандартными — отказ от вредных привычек, ведение здорового образа жизни.
К.Ю. Брюшковский, к.в.н., А.Г Клявин к.в.н.
Введение
Саркомы мягких тканей представляют собой одну из наименее изученных групп злокачественных опухолей у собак и кошек. Они весьма разнообразны по гистологическому строению, скорости роста, способности к метастазированию и реакции на лечение. Их частота встречаемости составляет примерно 15% от всех злокачественных новообразований у домашних животных. Однако они занимают 4-е место по причине смертности среди онкологических заболеваний собак и кошек. Это говорит о том, что эффективность лечения сарком мягких тканей в ветеринарии находится на весьма низком уровне.
Проблема эффективного лечения сарком мягких тканей связана с несколькими факторами. Во-первых, это разнообразие морфологических форм опухолей и трудность первичной цитологической диагностики вида опухоли. Во-вторых, необходимость неукоснительно соблюдать все принципы онкологической хирургии при удалении саркомы из организма животного. В-третьих, специфичность чувствительности разных морфологических форм опухолей к лучевой и химиотерапии. Исходя из этого, нам бы хотелось поделиться с коллегами нашим опытом лечения сарком мягких тканей у собак и кошек для того, чтобы совместно разработать наиболее оптимальный подход к лечению этих агрессивных злокачественных опухолей.
Что такое саркомы
С самого начала необходимо определить виды злокачественных новообразований, которые относят к большой группе сарком мягких тканей. Саркомами мягких тканей называют мезенхимальные опухоли, расположенные вне скелета и внутренних органов. В 2002 году вышла уточнённая классификация ВОЗ опухолей кожи и мягких тканей у домашних животных.
К саркомам мягких тканей относятся следующие новообразования.
а) поствакцинальная кошек;
б) высокодеффиринцированная верхней и нижней челюстей собак.
3. Злокачественная фиброзная гистиоцитома:
а) веретеновидно-плеоморфно клеточный тип;
а) ангиосаркома вентральной брюшной стенки кошек
Злокачественная опухоль оболочки периферических нервов кожи и подкожной клетчатки (нейрофибро-саркома, злокачественная шваннома)
Стадии
Основой успешного лечения в онкологии является его правильное и заблаговременное планирование. В случае с саркомами мягких тканей это особенно актуально. Чтобы определить оптимальное лечение необходимо знать стадию процесса:
TNM классификация
No - нет метастазов
N1 - есть метастазы
Мо - нет метастазов
М1 -наличие метастаз

При 4-й стадии процесса хирургическое удаление опухоли оправдано, только если это значительно улучшит качество жизни пациента, например, уберёт болевой синдром. Перед планированием операции мы всегда тщательно проводим диагностику наличия отдалённых метастазов в организме больного животного. Для этого необходимо провести рентген-диагностику грудной клетки и узи брюшной полости. Метастатическая способность сарком зависит от гистотипа опухоли:

В целом, следует отметить преобладание гематогенного пути метастазирования над лимфогенным. Перед началом планирования лечения необходимо оценить факторы, влияющие на агрессивность течения онкологического процесса.
Для сарком мягких тканей нужно обращать внимание на следующие факторы:
• опухоли у собак размером более 5 см имеют в 3 раза большую вероятность метастазирования;
• местоположение опухоли: средняя продолжительность жизни у собак при инвазии кожи была почти в 3 раза больше, чем у собак с инвазией мышечной ткани. Также саркомы на конечностях имеют более агрессивный рост, чем саркомы в области головы;
• подвижность относительно окружающих тканей является благоприятным фактором прогноза.
После проведения морфологического исследования у врача появляется ценная прогностическая информация:
• степень дифференцировки клеток опухоли - чем ниже дифференцировка, тем более вероятно отдалённое метастазирование и быстрый местный инвазивный рост опухоли;
• чем больше в опухоли очагов некроза, тем хуже её чувствительность к лучевой и химиотерапии;
• количество митозов в опухоли говорит о степени её злокачественности, наиболее злокачественные опухоли имеют более 20 митозов в поле зрения.
Методы лечения
Основной метод лечения сарком — хирургический. При этом очень важно удалить всю опухолевую ткань, то есть провести радикальную операцию. Для этого нужно соблюдать следующие принципы:
• Абластичность - полное удаление опухолевых клеток из организма и недопущение их попадания в операционную рану во время операции. Самое главное при абластичном удалении саркомы мягких тканей - правильно определить границы резекции опухоли в здоровых тканях. При росте саркома сдавливает окружающие ткани, при этом образуется так называемая псевдокапсула - участок уплотнённых тканей вокруг опухоли. Эта псевдокапсула не является барьером для прохождения опухолевых клеток, поэтому при удалении опухоли граница резекции должна проходить не ближе 3 см от границ псевдокапсулы. Для поствакцинальной саркомы кошек минимальное расстояние до края опухоли является 5 см. Недопустимо повреждать капсулу при удалении опухоли. Место взятия биопсии обязательно должно попасть в удаляемый участок тканей. Часто при планировании операции по удалению саркомы приходится планировать и реконструктивную часть для закрытия образовавшегося дефекта после удаления опухоли. Следует помнить, что после завершения онкологической части операции необходимо сменить перчатки и инструменты, чтобы избежать обсеменения опухолевыми клетками операционной раны. Если на опухоли имеются язвы или другие повреждения кожного покрова, необходимо их закрыть стерильными салфетками, чтобы перчатки и инструменты не касались опухолевой ткани. Во время операции опухоль не следует брать в руки, сжимать, надавливать на неё, так как всё это стимулирует выброс опухолевых клеток в кровоток организма.
• Принцип футлярности: саркомы мягких тканей распространяются по межфасциальным пространствам, поэтому при их удалении необходимо удалять все анатомические структуры и ткани, входящие с ней в общий фасциальный футляр, то есть все мышцы и покрывающие их фасции.
Алгоритм лечения мягкотканного образования

Если опухоль выходит за пределы мышечно-фасциальных границ, хирург должен руководствоваться принципами зональности и блочности. Особенно это актуально при удалении сарком, имеющих лимфагенный путь метастазирования, в первую очередь рабдомио-саркомы, гистиоцитарной саркомы и гемангиосаркомы. Такие опухоли должны удаляться единым блоком, с захватом всех тканей в зоне регионарного лимфооттока. Наличие опухолевых клеток в регионарных лимфатических узлах является плохим прогностическим фактором. Однако увеличение регионарных лимфатических узлов ещё не говорит о наличии в них опухолевых клеток. Мы встречали случай, когда после гистологического исследования удалённых увеличенных лимфоузлов у собак с саркомой мягких тканей опухолевых клеток не находили и ставили диагноз - реактивная гиперплазия. Таким пациентам мы не назначали системную химиотерапию.
При хирургическом удалении сарком мягких тканей можно использовать приёмы антибластики. В своей практике мы пробовали интраоперационное облучение операционной раны и интраоперационное использование фотодинамической терапии. Использование ионизирующего излучения интраоперационно связано с большими техническими сложностями, так как источник ионизирующего излучения находится за пределами нашей клиники. Также мы столкнулись с удлинением послеоперационного периода и осложнениями при заживлении операционного шва.
При использовании фотодинамической терапии интраоперационно мы за 1 час до операции вводили пациенту дозу фотодитазина 1 мг/кг веса. Удаляли новообразование и облучали ложе опухоли лазером с длиной волны 661 нм. Из послеоперационных осложнений замечали только отёчность операционного шва на 3-й-7-й день и наличие серомы.
Из технических сложностей следует отметить необходимость нахождения пациента после фотодинамической терапии 24 часа в тёмном помещении. После хирургической операции удалённый материал должен быть направлен на гистологическое исследование.
Основным фактором прогноза является наличие опухолевых клеток по краю резекции. Чтобы морфолог мог достоверно определить их присутствие, необходимо перед фиксацией специальной краской прокрасить все поверхности препарата, которые соприкасались с тканями организма. Когда для исследования невозможно представить весь удалённый материал, следует отметить краской наиболее подозрительные участки. В случае нахождения опухолевых клеток в прокрашенных участках операция считается нерадикальной и животному требуется дополнительное лечение. Наиболее эффективным считается повторная операция, с иссечением операционного рубца и захватом по 5 см ткани в каждую сторону, также можно использовать послеоперационное облучение границ резекции и окружающих тканей. Мы используем адъювантную лучевую терапию при положительных краях резекции, при рабдомиосаркоме, при саркомах высокой степени злокачественности - G3. Начинаем лучевую терапию не позднее 10-14 дня после операции в дозе СОД 50-60 Гр. Доза за одну фракцию - 5 Гр. Используются широкие поля облучения, отступая по 5-7 см от границ резекции. Сеансы лучевой терапии проводятся 3-5 раз в неделю, с применением седации. Время сеанса обычно 5-10 минут, для седации используются препараты короткого действия: пофол и домитор с антиседаном. Осложнений, связанных с анестезией у нас не было.
В гуманной медицине при лечении сарком мягких тканей широко используется предоперационное облучение. Его задачами являются:
• снижение злокачественного потенциала опухоли за счёт гибели наиболее агрессивных клеток;
• тотальное повреждение субклинических очагов опухоли;
• уменьшение объема опухоли.
Интервал между проведением курса лучевой терапии и операцией должен составлять не более 2-3 недель. Из-за этого после проведения неоадъювантной лучевой терапии регистрируется большое количество послеоперационных осложнений, до 40%. При сравнении предоперационной и послеоперационной лучевой терапии при саркомах мягких тканей не было обнаружено статически значимой разницы в эффективности. В своей практике мы используем только адъювантную лучевую терапию.
При лечении сарком мягких тканей высокой степени злокачественности (G3), особенно в случае гистологически подтвержденной гистиоцитарной саркоме, лимфангиосаркоме, синовиальной саркоме, гемангиосаркоме и рабдо-миосаркоме мы используем адъювантную химиотерапию. В качестве химиотерапевтического агента используется доксорубицин в монорежиме или его сочетание с циклофосфаном. По данным метанализа рандомизированных исследований в гуманной медицине, доксорубицин снижает риск местного и системного рецидива с тенденцией к увеличению выживаемости, которая лучше прослеживалась при локализации опухоли на конечности. Однако в ветеринарии такие исследования не проводились. Другие сочетания доксорубицина не показали большей эффективности по сравнению с доксорубицином в монорежиме.
Протокол адьювантной химиотерапии
• Доксорубицин - 30 мг/м 2 внутривенно 1 раз в 3 недели, 3-5 курсов.
• Доксорубицин - 30 мг/м 2
• Циклофосфан - 300 мг/м 2 - 1 раз в 3 недели -3-5 курсов.
Начинаем химиотерапию на 10-й-14-й день после операции. Следует помнить, что доксорубицин является достаточно токсичным химиопрепаратом. Он вызывает различные анафилактические реакции, миелосупрессию, кардиотоксичность у собак при коммулятивной дозе более 180 мг/м 2 и нефротоксичность у кошек. Всё это необходимо учитывать при проведении курса химиотерапии. В качестве дополнительного лекарственного лечения после хирургической операции возможно применение метрономной химиотерапии, которая направлена на замедление ангиогенеза в опухоли и на подавление регуляторных Т клеток, которые необходимы для роста опухоли. При этом протоколе химиотерапевтические препараты даются в сниженных дозах в ежедневном режиме длительное время. Мы используем сочетание пироксикама в дозе 0,3 мг/кг и циклофосфана в дозе 15 мг/м 2 ежедневно. Выводы об эффективности делать пока преждевременно, однако в специальной зарубежной литературе встречаются положительные отзывы.
При комплексном лечении сарком мягких тканей следует особенно выделить рабдомиосаркому. Эта опухоль является одной из самых агрессивных среди мягкотканных новообразований. Тем не менее, она лучше других сарком поддаётся лечению лучевой и химиотерапией. У животных она чаще всего локализуется на конечностях, но может появляться и в других частях тела (молочная железа, нижняя челюсть). Для лечения рабдомиосаркомы мы всегда применяем адьювантную лучевую терапию, независимо от степени злокачественности опухоли и состояния краев резекции. Рабдомиосаркома активно метастазирует, поэтому адьювантная химиотерапия, должна входить в состав комплексного лечения.
Протокол при рабдомиосаркоме
• Дактиномицин - 0,5 мг/м 2 1 раз в 3 недели.
• Винкристин - 0,5 мг/м 2 8 и 15 день.
• Циклофосфан - 250 мг/м 2 1 раз в 3 недели. Этот курс мы повторяем с интервалом в 21 день. Если дактиномитцин владельцы использовать не могут, мы проводим химиотерапию доксорубицином и циклофосфаном.
Для кошек одной из самых агрессивных сарком мягких тканей является поствакцинальная фибросаркома. Её название связано с гипотезой о том, что причиной возникновения данной опухоли является адъювант, входящий в состав многих вакцин. Вызывая хроническое воспаление с пролиферацией в зоне инъекции, он становится пусковым механизмом развития саркомы. Также есть данные о вирусной природе заболевания и о генетической предрасположенности определённых линий кошек к развитию данного новообразования. Эта опухоль обладает агрессивным инвазивным ростом и имеет минимальное время удвоения опухоли - 9 дней, для сравнения самая агрессивная опухоль молочной железы имеет скорость удвоения опухолевой массы - 30 дней. Поствакцинальная саркома метастазирует нечасто, менее чем в 20 % случаев и, как правило, в запущенных случаях или после нерадикальной операции при возникновении рецидива. Поэтому для излечения животного необходимо как можно раньше диагностировать болезнь и провести радикальную операцию. Любой ветеринарный врач должен развивать в себе онкологическую настороженность и проводить цитологическое исследование уплотнений у кошек в месте проведения вакцинации или введения инъекционных препаратов. Настораживающими признаками развития фибросаркомы являются:
• припухлость, которая сохраняется более 3 -х месяцев после вакцинации;
• уплотнение более 2 см в диаметре;
• уплотнение увеличивается в размерах спустя 4 недели после вакцинации.
Для абластического удаления данной опухоли необходимо провести широкое иссечение новообразования. Хирургические границы должны составлять не менее 2 см от края опухоли, однако и этого может оказаться недостаточным. Среди некоторых ветеринарных онкологов в настоящее время существует мнение, что безопасным следует считать расстояние в 5 см от видимой границы опухоли. Эффективность лучевой и химиотерапии в дополнение к хирургическому лечению поствакцинальной фибросаркомы кошек в настоящее время изучается. По нашему мнению, адьювантная химиотерапия оправдана при наличии положительного края резекции. Существуют исследования, которые показывают увеличение продолжительности жизни кошек при использовании адьювантной химиотерапии доксорубицином в монорежиме, однако эти данные требуют дополнительного изучения. В качестве профилактики и для улучшения возможной резектабильности опухоли можно предложить следующие меры:
• не вводить вакцину в область между лопатками;
• вакцину от бешенства вводить под кожу правой голени;
• вакцину от FeLV вводить под кожу левой голени;
• остальные вакцины вводить в правое плечо.
Выводы
Литература
1. Давыдов М.И. и др. Энциклопедия клинической онкологии. М. 2004 с 364-374
2. Алиев М.Д. Современные подходы к лечению сарком мягких тканей//Практическая онкология -2004 Т.5 №4 - с 250-253
З. Хандерсон Ральф А. Правила онкологии// Тезисы доклада. XX Московский международный Ветеринарный Конгресс М.2012
4. Ричард А.С.Уайт. Онкологические заболевания мелких домашних животных. М. 2003 - с 253 -258.
5. Шугабейнер П.Х., Малауэр М.М. Хирургия сарком мягких тканей. М. 1996.
6. Joanna Morris, Jane Pobson. Small Animal Oncology. Blackwell Science 2001.P 69-78
7. Stephea J. Withrow. David M. Vail. Small Animal Clinical Oncology 2007. P 425-455
8. McGlennon NJ, Houlton JEF, Gorman NT: Synovial cell sarcoma: a review, J Small Anim Pract 29:139-152, 1988.
9. Duda RB: biology of mesenchymal tumors, Cancer J 7:52-62, 1994.
10. Thrall DE, Gillette EL: Soft-tissue sarcomas, Semin Vet Med Surg Small Anim 10:173-179, 1995.
11. Kuntz CA, Dernell WS, Powers BE et al: Prognostic factors for surgical treatment of soft - tissue sarcomas in dogs: 75 cases (1986 - 1996), J Am Vet Med Assoc 21: 1147 -1151, 1997.
12. Baez JL, Hendrick MJ, Shofer FS et al: Liposarcomas in dogs: 56 cases ( 1989-2000), J Am Vet Med Assoc 224:887-891, 2004.
13. Ward H, Fox LE, Calderwood-Mays MB et al: Cutaneous hemangiosarcoma in 25 dogs: a retrospective study, J Vet Intern Med
14. McAbee KP, Ludwig LL, Bergman PJ et al: Feline cutaneous hemangiosarcoma: a retrospective study of 18 cases (1998-2003),
J Am Anim Hosp Assoc 41:110-116, 2005.
15. Baker-Gabb M, Hunt GB, France MP:Soft tissue sarcomas and mast cell tumours in dogsxlinical behaviour and response to surgery, Aust Vet J 81:732-738,2003.
16. Bregazzi VS, LaRue SM, McNiel E et al: Treatment with a combination of doxorubicin, surgery, and radiation versus surgery and radiation alone for cats with vaccine-associated sarcomas:25 cases (1995-2000), J Am Vet Med Assoc 218:547-550, 2001.
Читайте также:

