Протоколы лечения саркомы юинга
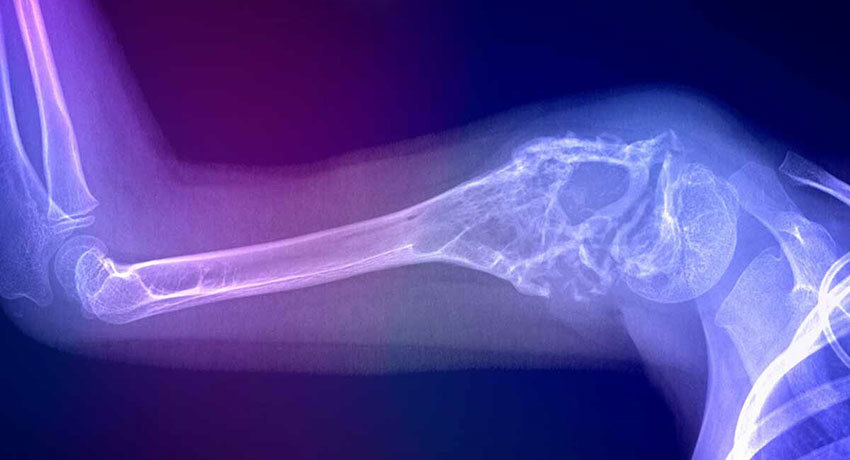
Саркома Юинга — агрессивная опухоль, которая быстро распространяется в окружающие ткани и метастазирует. До появления химиотерапии пятилетняя выживаемость пациентов при данном заболевании составляла меньше 10%. В годах прошлого столетия начала активно применяться лучевая терапия, и всё же большинство пациентов погибало в течение двух лет с момента установления диагноза.

Выбор тактики лечения при саркоме Юинга зависит от ряда факторов:
- Стадии заболевания: является ли саркома локализованной или распространенной. Подробнее об этом в нашей общей статье о саркоме Юинга.
- Размеров и локализации опухолевых очагов.
- Общего состояния больного, его возраста, сопутствующих заболеваний.
- В ряде случаев могут быть учтены личные пожелания пациента.
В настоящее время лечение локализованной саркомы Юинга состоит из трех обязательных этапов: начальной (индукционной) химиотерапии, локального лечения (хирургическое удаление опухоли или лучевая терапия) и последующей адъювантной химиотерапии.
В клинике Медицина 24/7 работают ведущие врачи-онкологи, хирурги-ортопеды. Применяются все современные методы лечения злокачественных опухолей костной ткани, лечение проводится в соответствии с современными международными протоколами и рекомендациями. Решения об оптимальной тактике лечения принимаются коллегиально, на врачебных консилиумах.
Химиотерапия при саркоме Юинга
Согласно современным представлениям, у всех пациентов с саркомой Юинга есть микроскопические метастазы, даже если они не выявляются во время обследования. Таким образом, даже если первичная опухоль полностью удалена, в дальнейшем может произойти рецидив в виде вторичных очагов. Поэтому системная химиотерапия является важной частью лечения: она помогает уничтожить опухолевые клетки в разных частях тела.
Индукционную химиотерапию, как правило, начинают минимум за 9 недель до операции или лучевой терапии. Применяют комбинацию из трех препаратов: Винкристина, Доксорубицина (Адриамицина) и Циклофосфамида. Сокращенно эта схема обозначается как VDC или VAC.
Адъювантная химиотерапия после операции или лучевой терапии включает два препарата: Этопозид и Ифосфамид. Она продолжается дольше индукционной химиотерапии, в общем курс лечения продолжается от 6 месяцев до года.
Во время курса химиотерапии периодически проводят контрольные общие и биохимические (показатели функции печени и почек) анализы крови, ЭКГ. Это нужно для того, чтобы вовремя выявить возможные побочные эффекты химиопрепаратов и скорректировать нарушения в организме.
Химиопрепараты также можно применять параллельно с курсом лучевой терапии.
Оставьте свой номер телефона
Хирургическое лечение
Локальное лечение саркомы Юинга должно быть проведено не позднее 2–3 недель после завершения курса индукционной химиотерапии. В последние 10–15 лет существенно расширились возможности органосохраняющих операций. Вопрос о возможности хирургического вмешательства, его оптимальном виде и объеме обсуждается на врачебном консилиуме с участием онколога, и других специалистов.
- При саркомах костей конечностей в ряде случаев может быть выполнено органосохраняющее вмешательство. Удаленную костную ткань замещают трансплантатом из других частей тела или искусственным протезом. Если опухоль расположена близко к суставу, выполняют его эндопротезирование. К ампутациям конечностей современные хирурги стараются прибегать только в крайних случаях, когда органосохраняющая операция объективно невозможна.
- При поражении ребер их удаляют вместе с соседними и заменяют искусственными имплантатами. Если имеются резектабельные опухолевые очаги в легких, их также удаляют.
- При саркоме Юинга в костях таза хирургическое вмешательство становится возможным, когда опухоль хорошо отвечает на индукционную химиотерапию. Обычно операцию дополняют лучевой терапией. В некоторых случаях удается удалить только пораженную кость и заменить ее имплантатом. Иногда, при обширных процессах, приходится удалять кости таза вместе с прикрепляющейся к ним нижней конечностью. В других случаях предпочтительным методом локального лечения является лучевая терапия.
- Поражения позвоночного столба очень сложно лечить хирургически. Большинству пациентов показана лучевая терапия. Если операцию удается выполнить, обычно ее дополняют облучением.
Во время операции важно удалить всю опухоль вместе с окружающими тканями. Удаленный материал отправляют на биопсию. Важно оценить край резекции — выяснить, есть ли опухолевые клетки рядом с линией разреза:
- Негативный край резекции (рядом с линией разреза нет опухолевых клеток) означает, что опухоль удалена полностью.
- Позитивный край резекции (рядом с линией разреза обнаружены опухолевые клетки) означает, что рядом с местом, где находилась саркома, могла остаться опухолевая ткань, которая приведет к рецидиву. В таких случаях показана лучевая терапия и химиотерапия в течение нескольких месяцев.
Оставьте свой номер телефона
Лучевая терапия
Чувствительность саркомы Юинга к облучению очень высока, поэтому лучевую терапию применяют у всех пациентов, у которых невозможно удалить опухоль, и которым противопоказано хирургическое вмешательство по состоянию здоровья. Также лучевая терапия может дополнять операцию.
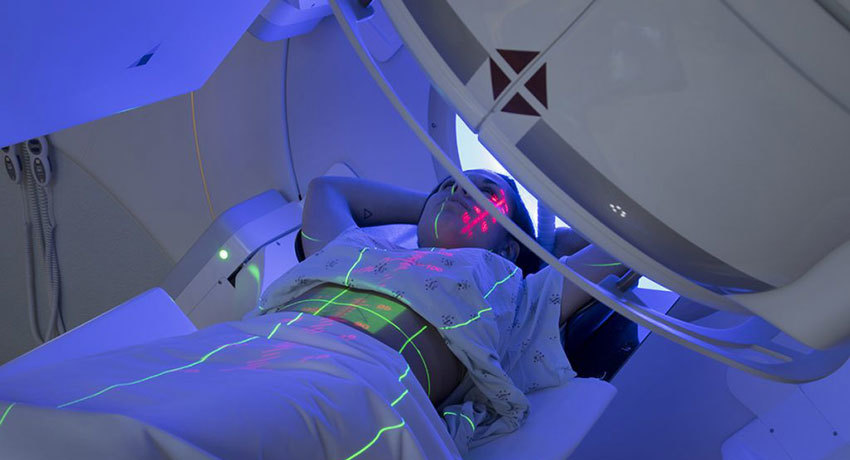
Обычно облучение проводят пять дней в неделю в течение нескольких недель. Процедура напоминает рентгенографию, но во время нее применяют более высокие дозы излучения.
Современные линейные ускорители способны генерировать излучение, форма которого в точности повторяет очертания злокачественной опухоли. Это позволяет эффективно уничтожать злокачественные клетки, не причиняя вреда окружающим тканям. В современных онкологических клиниках применяются такие методики, как лучевая терапия (), лучевая терапия с модуляцией интенсивности (IMRT).
Чтобы обеспечить высокую точность облучения, важно правильно провести подготовку к лучевой терапии. Этот процесс называется симуляцией, во время него применяют МРТ и другие методы визуализации — они помогают правильно рассчитать углы, под которыми будут направлены лучи.
Лечение распространенной саркомы Юинга
При метастатической саркоме Юинга прогноз наиболее благоприятен в случаях, когда имеются единичные очаги в легких, которые можно удалить, как и первичную опухоль. При поражении других органов и костей лечить заболевание намного сложнее.
Лечение начинают с химиотерапии, зачастую ее проводят в более интенсивном режиме, чем при локализованных опухолях. Затем проводят МРТ, КТ или , чтобы проверить, как опухолевые очаги отреагировали на химиопрепараты. Если это возможно, выполняют хирургическое вмешательство, зачастую дополняя его лучевой терапией, и назначают адъювантную химиотерапию. В остальных случаях применяют лучевую терапию и химиопрепараты.
В настоящее время ведутся клинические исследования, направленные на поиск новых эффективных способов лечения саркомы Юинга с метастазами. Пациенты могут принять в них участие, если являются подходящими кандидатами.
Реабилитация и наблюдение после лечения
После завершения лечения в организме пациента могут остаться опухолевые клетки, всегда сохраняется риск рецидива. В большинстве случаев саркомы Юинга рецидивируют в первые два года.
Каждый пациент после завершения лечения должен регулярно являться на контрольные осмотры врача и обследования. В течение первых лет они проводятся через каждые 2–3 месяца, затем реже. Обследование может включать рентгенографию, КТ, МРТ, , сцинтиграфию костей. После курса химиопрепаратов проводят контрольные анализы крови, ЭКГ.
В случае рецидива курс лечения начинают снова. Он также может включать хирургическое удаление новых очагов, химиотерапию, лучевую терапию.
После операций по поводу саркомы Юинга проводят реабилитационное лечение. Оно помогает восстановить утраченные функциональные возможности, вернуться к привычной жизни. Реабилитация включает физические упражнения, физиопроцедуры и другие методы. Для каждого пациента составляют индивидуальную программу.
К сожалению, в России направление реабилитации онкологических пациентов на данный момент развито довольно слабо. На базе клиники Медицина 24/7 функционирует современный реабилитационный центр, в нём работают ведущие врачи, инструкторы, применяются новейшие тренажеры. Это помогает пациентам максимально восстановить нарушенные функции и быстро вернуться к привычной, полноценной жизни.
Саркома Юинга — это злокачественная опухоль, которая чаще всего поражает детей и подростков. Заболевание является очень опасным из-за низкого процента выживаемости и проблем в диагностировании. Его нередко обнаруживают уже на поздней стадии, когда прогноз неутешителен.
Основные симптомы очень легко спутать с последствиями травм, остеопорозом и другими распространенными патологиями костей. Юный возраст большинства заболевших также создает трудности в обнаружении опухоли. Дети и молодые люди обычно не рассматриваются как группа риска в онкологии, а бытовые или спортивные повреждения суставов для них не являются редкостью.
Общие сведения о заболевании
Саркома Юинга может развиваться в любой части скелета и даже в мягких тканях, но чаще всего поражает конечности и длинные трубчатые кости. Еще Джеймс Юинг, открывший ее в 1921 году, писал об этом свойстве опухоли. Болезнь прогрессирует очень быстро с ранним развитием метастаз в костном мозге и легких.

Сама опухоль представляет собой маленькие круглые злокачественные клетки с небольшой цитоплазмой. Для них характерна правильная форма, низкая митотическая активность и перестройка определенной хромосомы (под номером 22). Характерной особенностью новообразования является раннее распространение на окружающие ткани, даже при локализованной форме обнаруживается мягкотканный компонент.
В одну группу заболеваний входят атипичная саркома Юинга и несколько других злокачественных периферических нейроэктодермальных опухолей. В момент постановки диагноза, метастазы обнаруживаются у 15-50% заболевших. Достаточно часто пациенты впервые обращаются за медицинской помощью уже при метастатическом поражении внутренних органов. Современный подход к лечению саркомы Юинга подразумевает наличие отдаленных микрометастазов практически у всех больных с локализованной формой опухоли.
Чаще всего опухоль развивается в следующих областях:
- Большеберцовой или малоберцовой кости (около 10% случаев);
- Костях таза (20-25%);
- Бедренных костях (до 27%);
- Верхних конечностях (15%).
Гораздо реже данный вид саркомы локализуется в ребрах, позвоночнике и ключице. Чем старше пациент, тем вероятнее обнаружить опухоль в нехарактерных для нее костях — черепе, лопатках, стопе, кистях или позвонках. В 2/3 случаев заболеваний отмечается поражение нижних конечностей и области таза. Нетипичными областями поражения являются: желудочно-кишечный тракт, почки, эндометрий, предстательная железа. В зарубежных источниках также упоминается опухоль Аскина, относящаяся к группе сарком Юинга, при которой новообразования распространяются в грудной полости, охватывая легкие и плевру.
Распространенность и группы риска
Пик заболевания приходится на возраст от 10 до 25 лет, период активного роста скелета наиболее опасен. Однако злокачественные образования данного типа могут поражать людей всех возрастов, известны случаи обнаружения опухоли у очень пожилых пациентов и младенцев. У больных старше 30 лет и детей младше 5-ти саркома Юинга встречается крайне редко. Начиная с 14-15 лет юноши болеют чаще девушек в 1,5 раза. Белые подростки подвержены опухоли в гораздо большей степени, чем чернокожие и азиаты.
Примерно у 40% пациентов 
саркома Юинга появляется после травмы. Ученые считают генетическую предрасположенность одним из определяющих факторов. Саркома Юинга является второй по частоте распространения среди опухолей костей у детей и подростков. Все же заболевание встречается достаточно редко — в среднем 0,6-3 случая на 1 млн населения.
Основные симптомы
Одним из первых симптомов заболевания отмечают локальную боль в области поражения. Сначала она носит периодический характер и может самопроизвольно ослабевать, но впоследствии становится интенсивной и постоянной. При поражении костей саркомой Юинга наблюдаются следующие симптомы:
- Небольшой отек в области очага развития опухоли;
- Повышенная температура (38-40С);
- Боль, локализующаяся в месте поражения;
- Расширение вен, расположенных близко к коже;
- Гиперемия участка поражения;
- Потеря в весе на фоне сниженного аппетита;
- Лихорадка;
- Общая слабость;
- Анемия и лейкопения.
Обычно с момента появления первых болевых симптомов до постановки окончательного диагноза проходит 6-12 месяцев. По мере развития заболевания опухоль быстро увеличивается в размерах, становится болезненна при пальпации.

Распространение опухоли в тазовой области провоцирует нарушение работы внутренних органов. Опухоль Аскина, относящаяся к группе сарком Юинга, вызывает дыхательную недостаточность и кровохарканье.
Боль усиливается по мере роста опухоли. Примерно в 1/3 случаев наблюдается локальное повышение температуры в области поражения. На более поздних стадиях (через 3-4 месяца) может происходить патологический перелом, он наблюдается у 5-10% больных.
Диагностика
Дифференциальная диагностика опухоли затруднена из-за ее схожести с другими мелкоклеточными злокачественными образованиями. По этой причине применяется несколько дополнительных исследований для постановки окончательного диагноза. При подозрении на саркому Юинга назначаются следующие виды обследований:
- Рентгенография области, пораженной опухолью;
- Магнитно-резонансная (МРТ) или компьютерная томография (КТ) ;
- Биопсия опухоли и костного мозга;
- Ультразвуковое исследование (УЗИ);
- Биохимический анализ крови;
- Позитронно-эмиссионная томография (ПЭТ);
- Цитогенетическое исследование;
- Иммуногистохимическое обследование;
- Молекулярно-генетический анализ;
- Флуоресцентная гибридизация;
- Миелограмма;
- Электрокардиограмма;
- Ангиография;
- Оостеосцинтиграфия.
Рентгенография места поражения проводится двух проекциях. Обследование должно определить наличие деструкции кости и распространение опухоли на мягкие ткани.

Для постановки диагноза одного гистологического исследования недостаточно. Морфологически саркома Юинга очень схожа с другими злокачественными опухолями, такими как синовиальная саркома, рабдомиосаркома, нейробластома и ряд других. Клетки расположены без видимой структуры и разделены фиброзными прослойками, для них характерен зеркальный вид за счет дисперсии хроматина в клеточных ядрах. Достаточно часто наблюдается некроз опухолевой ткани, при котором жизнеспособные клетки локализуются вокруг сосудов.
Диагностика заболевания требует выполнения расширенного иммуногистохимического исследования. Практически все клетки опухоли (95%) вырабатывают на своей поверхности определенный гликопротеин, который является продуктом онкогена. Для них также характерна экспрессия виментина, что отличает саркому Юинга от нейробластомы. Иммуногистохимический анализ подтверждает диагноз, поставленный на основе рентгенографического обследования.
Для цитологического исследования 
опухоли проводится биопсия. Процедура выполняется только опытным онкологом-ортопедом. Открытая инцизионная методика получения образцов ткани является более предпочтительной, чем тонкоигольная и трепан-биопсия. Многие специалисты также считают необходимым исследование костного мозга, поскольку его поражение является возможным даже при отсутствии метастазов в костях.
Магнитно-резонансная томография применяется для определения стадии заболевания. Метод позволяет оценить степень поражения мягких тканей, размеры опухоли и ее структуру.
Полимеразная цепная реакция используется при исследовании микроскопических метастазов в периферической крови и костном мозге. Биохимический анализ показывает повышение уровня С-реактивного белка, а также мочевины и креатинина, дисбаланс калия, натрия, кальция и другие характерные для опухоли изменения.
Лечение
Основными методами лечения Саркомы Юинга являются:
- Индукционная химиотерапия;
- Лучевая терапия;
- Хирургическая операция с эндопротезированием.
Комбинированное лечение саркомы Юинга является общепринятым, его длительность варьируется от 18 месяцев до 2-х лет. Химиотерапия обычно включает в себя несколько циклов с применением различных комбинаций следующих препаратов:
- Винкристин;
- Циклофосфан;
- Адриамицин;
- Цисплатин;
- Доксорубицин;
- Дактиномицин;
- Ифосфамид;
- Этопозид;
- Актиномицин.

После операции рекомендовано использование лучевой терапии. Объем и интенсивность определяют в зависимости от успеха предшествующего лечения, его показывает гистологическое исследование. При положительном исходе после завершения терапии пациентов обследуют сначала раз в 2-3 месяца в течение 2 лет, затем каждые 3 года.
Прогноз и успешность лечения
Выживаемость и успех лечения во многом зависят от локализации первичной опухоли. Прогноз благоприятнее при поражении длинных трубчатых костей, новообразования в тканях черепа гораздо труднее поддаются лечению. Локализованная форма саркомы Юинга при своевременной комплексной терапии характеризуется 70% выживаемостью. Прогноз значительно хуже для пациентов, лечение которых началось на стадии метастазирования в костный мозг. В этом случае даже химиотерапия в высоких дозах, тотальное облучение и операция по трансплантации не дают результатов выживаемости более 30%.
Однако методики и протоколы 
химиотерапии постоянно совершенствуются. Совсем недавно успешность лечения саркомы Юинга не превышала 10% от общего числа больных с метастатической формой заболевания. До начала применения цитостатических препаратов показатели 5-летней выживаемость оставались крайне низкими.
В борьбе со злокачественными периферическими опухолями костей и мягких тканей достигнут значительный прогресс. Сейчас можно с уверенностью сказать, Саркома Юинга излечима. Многие пациенты живут полноценной жизнью после завершения терапии, если к комплексному лечению приступают на ранней стадии заболевания.








Современные принципы лечения саркомы Юинга
I . Общие сведения
Саркома Юинга ( лат. myeloma endotheliale ) — злокачественная опухоль костного скелета . Саркома Юинга, как правило, поражает нижнюю часть длинных трубчатых костей, ребра , таз , лопатку , позвоночник и ключицу .
Была открыта Джеймсом Юингом в 1921 году . Учёный охарактеризовал её как опухоль, поражающую в основном длинные трубчатые кости .
Саркома Юинга является одной из самых агрессивных злокачественных опухолей. До применения системной терапии почти у 90 % больных развивались метастазы. Наиболее частая локализация метастазов на момент первичной диагностики — лёгкие, кости, костный мозг . 14—50 % пациентов к моменту установления диагноза уже имеют метастазы , выявляемые рутинными методами исследования, и гораздо больше больных имеют микрометастазы.
Саркома Юинга является второй по частоте среди злокачественных опухолей костей у детей — составляет 10-15 %. Эта опухоль редко встречается у детей моложе 5 лет и у взрослых старше 30 лет. Пик заболеваемости приходится на 10 −15 лет.
II .Причины возникновения, клиническая картина
К настоящему времени не удалось выявить потенциальные причины возникновения саркомы Юинга. Существует ряд научных данных, свидетельствующих о роли наследственного компонента в механизме развития заболевания. В частности, описано одновременное развитие саркомы у сиблингов, что позволяет судить о значении генетических дефектов. Также доказано, что в 40 % случаях возникновение костной саркомы провоцирует травма.
Саркома Юинга состоит из мелких круглых клеток со скудной цитоплазмой, круглым ядром, содержащим нежный хроматин и слабо просматривающиеся базофильные нуклеолы. В отличие от остеосаркомы, она не продуцирует остеоид.
Клиническая картина
Общие симптомы:
Боль (от момента появления первых болевых ощущений до установления диагноза проходит от 6 до 12 месяцев)
слабая и умеренной интенсивности
не стихает в покое
усиление по ночам
отсутствует облегчение при фиксации конечности.
По мере роста опухоли боль:
ограничивает движения в близлежащем суставе вплоть до контрактуры
нарушает повседневную активность
Быстроувеличивающаяся опухоль нередко с патологическим переломом (поздний признак — 3-4 мес)
Признаки местного воспаления:
болезненность при пальпации
пастозность (отечность) кожи
локальное повышение температуры
расширенные подкожные вены
Синдром общей опухолевой интоксикации
повышение температуры тела больного (субфебрильная и фебрильная лихорадка)
снижение веса и аппетита вплоть до кахексии
в лёгочную ткань (чаще всего)
в костную ткань
отдаленные метастазы (очень редко): в висцеральных органах, лимфатических узлах средостения и забрюшинного пространства, плевре, центральной нервной системе в виде поражения менингеальных оболочек и вещества головного и спинного мозга.
III .Диагностика
Рентгенография костей, пораженных опухолью и её метастазами
Рентгенография и КТ легких
КТ или МРТ участков скелета, мягких тканей и любых других анатомических областей, пораженных опухолевым процессом. Наиболее точно определяет размеры опухоли, её связь с окружающими тканями, сосудисто-нервным пучком, распространение опухоли по костно-мозговому каналу.
Позитронно-эмиссионная томография (ПЭТ)
Остеосцинтиграфия. Позволяет диагностировать отдаленные метастазы
IV. Современные методы лечения
IV .1 Локализованный опухолевый процесс:
При клинически локализованной форме заболевания к моменту установления диагноза 90% больных имеют микрометастазы, поэтому локальное лечение (операция или лучевая терапия) должно обязательно сопровождаться комбинированной химиотерапией. Комбинация химиотерапии, операции и/или лучевой терапии повысила уровень 5- летней выживаемости с 10% до 60%. После биопсии опухоли и тщательного обследования проводится от 4 до 6 циклов индукционной химиотерапии в течение 12- 24 недель, далее следует локальный метод лечения с последующим назначением от 6 до 10 циклов химиотерапии с 3-х недельным интервалом. Продолжительность лечения составляет 8-12 месяцев. Наиболее активными цитостатиками являются доксорубицин, циклофосфамид, ифосфамид, винкристин, дактиномицин и этопозид. Фактически все режимы лечения основаны на комбинациях из 4-6 перечисленных препаратов. Наиболее эффективные режимы лечения включали, как минимум, один алкилирующий химиопрепарат (ифосфамид или циклофосфамид) и доксорубицин. Добавление ифосфамида и этопозида в программу лечения значительно улучшило результаты терапии у пациентов с неметастатической Саркомой Юинга / ПНЭТ. Радикальная операция в тех случаях, когда она выполнима, расценивается как наилучшая возможность локального контроля. Лучевая терапия показана при невозможности выполнения радикального оперативного вмешательства и обсуждается в тех случаях, когда при гистологическом исследовании удаленного материала определяется недостаточный лечебный патоморфоз (то есть выявляется более 10% жизнеспособных опухолевых клеток). Нерадикальная операция с последующей лучевой терапией не более эффективна, чем только лучевая терапия. Лучевая терапия проводится в дозах 40-45 Гр при микроскопических остаточных опухолях и 50-60 Гр при наличии макроскопических изменений. Основным методом лечения пациентов этой морфологической группы остаётся химиотерапия. Радикальное хирургическое лечение, так же как и лучевая терапия обеспечивают локальный контроль над заболеванием. Выбор объёма хирургического лечения должен быть индивидуализированым и зависеть от расположения первичного очага, его размеров, ответа на проводимую химиотерапию, возраста пациента и предполагаемого прогноза жизни.
IV .2 Хирургическое лечение саркомы Юинга:
В современной практической онкоортопедии развитие химиотерапии, внедрение новых подходов в хирургической технике и проведении анестезиологического пособия, инновационное развитие технологии изготовления эндопротезов, позволило кардинально изменить качество жизни и улучшить выживаемость пациентов, максимально возможно продлить срок службы имплантатов. Вследствие чего в настоящий момент органосохранные операции являются золотым стандартом лечения пациентов с диагнозом саркома кости. В настоящий момент в онкоортопедии выделяют следующие виды оперативного лечения:
1.Калечащие операции (ампутации, экзартикуляции);
2.1 Не требующие последующий реконструкции дефекта;
2.2 Требующие последующей реконструкции дефекта.
Главным условием операбельности пациентов с диагнозом саркома кости является радикальность и абластичность удаления опухоли, что должно гарантировать отсутствие местного рецидива. Радикальными считается следующие виды оперативного лечения: 1. Ампутация или экзартикуляция конечности. 2. Костные резекции при наличии минимального необходимого отступа от предполагаемого края опухоли не менее 3—5 см (при условии отсутствия распространения опухоли в костномозговом канале оставшейся части кости). 3. Удаление опухоли без вскрытия псевдокапсулы (en Block). В настоящий момент основными показаниями к проведению калечащих операций в объёме ампутации или экзартикуляции являются: 1) Обширное первично-множественное распространение опухоли. 2) Вовлечение в опухолевый процесс на протяжении магистрального сосудистонервного пучка, значительный внекостный компонент опухоли, исключающий проведение реконструктивно-пластического этапа операции. 3) В паллиативных целях, при отрицательном эффекте проводимого консервативного лечения. 4) Отказ пациента от органосохранной операции. 5) Наличие распада опухоли и кровотечения. В остальных случаях в первую очередь следует рассматривать возможность выполнения органосохранных операций. Размер первичного очага опухоли, степень распространения внекостного компонента не могут использоваться, как самостоятельные независимые критерии в решении вопроса о проведении калечащей операции. В современной онкоортопедии среди различных способов восстановления дефекта и функции конечности после удаления опухолевого очага, лидирующие положения занимают высокотехнологические операции с использованием эндопротезов, что позволяет улучшить качество жизни пациентов в короткие сроки после операции на фоне хорошего функционального результата. Выделяют следующие виды реконструктивных операций в объёме эндопротезирования:
1. Стандартные первичные операции у взрослых;
2. Стандартные первичные операции у детей и подростков;
3. Эндопротезирование редких анатомических зон;
4. Ревизионное эндопротезиование.
Требования предъявляемые к конструкции эндопротеза при первичном эндопротезировании у взрослых:
1. Модульность конструкции эндопротеза.
2.Максимальная надёжность и ремонтопрегодность эндопротеза;
3. Универсальность компонентов эндопротеза;
4. Максимальный срок службы;
5. Стабильная фиксация эндопротеза;
6. Хороший функциональный результат;
7. Короткий срок изготовления эндопротеза.
Вышеперечисленные характеристики эндопротеза дают возможность при замещении различных сегментов костей и суставов отказаться от необходимости индивидуального заблаговременного изготовления имплантата, позволяя установить эндопротез наиболее соответствующий индивидуальным анатомическим размерам кости конкретного пациента из универсальных модулей. Требования предъявляемые к конструкции эндопротеза при первичном эндопротезировании у детей и подростков:
1. Модульность конструкции эндопротеза.
2. Максимальная надёжность и ремонтопрегодность эндопротеза
3. Универсальность компонентов эндопротеза
4. Максимальный срок службы;
5. Стабильная фиксация эндопротеза;
6. Хороший функциональный результат;
7. Короткий срок изготовления эндопротеза
IV .3 Лучевая терапия и современная химиотерапия
Лучевая терапия саркомы Юинга. Применяется дистанционная 3-D и интенсивно модулированная (IMRT) лучевая терапия в комбинации с химиотерапией при отказе или нерадикально выполненной операции в качестве локального лечения. РОД 2-2,5гр, СОД=60Гр. При метастазах в легкие – крупнопольная лучевая терапия РОД=2Гр, СОД=20Гр.
IV . 4 Режимы химиотерапии:
Чередование IE и VAC каждые 3-4 недели: IE этопозид 100 мг/м2 в/в в1-5 дни
ифосфамид 1,8 г/м2 в/в инфузия в1-5 дни с уромитексаном
VAC винкристин 1,5 мг/м2 в/в в 1 день
доксорубицин 75 мг/м2 в/в в1 день
циклофосфамид 1200 мг/м2 в/в в 1 день
VACА винкристин 1,5 мг/м2 в/в в 1 день 1, 4, 7, 10, 13, 16, 19, 22, 25, 28, 31, 34, 37, 40 недели
доксорубицин 20 мг/м2 4-часовая в/в инфузия в1-3 дни1, 7, 13, 19, 25, 31, 37 недели
циклофосфамид 1200 мг/м2 в/в в 1 день 1, 4, 7, 10, 13, 16, 19, 22, 25, 28, 31, 34, 37, 40 недели
дактиномицин 0,5 мг/м2 4-часовая в/в инфузия в 1-3 дни 4, 10, 16, 22, 28, 34, 40 недели
VAIА винкристин 1,5 мг/м 2 в/в в 1 день 1, 4, 7, 10, 13, 16, 19, 22, 25, 28, 31, 34, 37, 40 недели
доксорубицин 20 мг/м2 4-часовая в/в инфузия в1-3 дни 1, 7, 13, 19, 25, 31, 37 недели ифосфамид 2,0 г/м2 в/в инфузия в 1 день 1, 4, 7, 10, 13, 16, 19, 22, 25, 28, 31, 34, 37, 40 недели с уромитексаном дактиномицин 0,5 мг/м2 4-часовая в/в инфузия в 1-3 дни 4, 10, 16, 22, 28, 34, 40 недели 24 CyVADIC циклофосфамид 600 мг/м2 в/в в 1 день
винкристин 1,4 мг/м2 в/в еженедельно, всего 6, затем в 1 день каждого цикла доксорубицин 60 мг/м2 в/в 96-часовая инфузия.
Список литературы
1. “ Цикл лекций по онкологии" Июль, 2001 г.// Том 2, ст. 38 (стр. 196)
Читайте также:





