При недифференцированном раке щитовидной железы лучевое лечение
Лечение рака щитовидной железы радиоактивным иодом ( 131 I). В течение почти 50 лет радиоактивный изотоп иода ( 131 I) используется в качестве компонента терапевтических процедур. при лечении высокодифференцированной карциномы щитовидной железы.
Тактика послеоперационного лечения зависит от гистологических характеристик опухоли, степени ее распространения и объема хирургического удаления.
В большинстве наблюдений высокодифференцированного рака щитовидной железы (папиллярного и фолликулярного) для повышения абластичности операции больным назначают пероральный прием радиоактивного иода и проводят сканирование всего тела и области шеи.
Особенно это относится к случаям, когда у врача возникают сомнения в полноте хирургического удаления опухоли. Такая тактика лечения применяется почти в половине случаев фолликулярной карциномы и несколько реже для папиллярных опухолей. Для всех хорошо дифференцированных опухолей лечение 131 I не является необходимым, поскольку скрытые и интратиреоидные опухоли удаляются хирургическим путем и характеризуются очень благоприятным прогнозом. Поэтому при лечении этих опухолей, преимущественно встречающихся у больных молодого возраста, стараются избегать назначения им высоких доз излучения, особенно принимая во внимание возраст.
При необходимости терапии радиоактивным йодом больным следует назначать не очень большое количество радиоактивности, порядка 3 ГБк (в настоящее время вместо внесистемной единицы кюри используется беккерель, 1 Ки = 37 ГБк). При этом разрушается оставшаяся ткань щитовидной железы, которая в большей степени, чем опухоль, захватывает иод, что делает терапию 131 I неприменимой в случаях, когда после операции сохраняется значительная часть щитовидной железы. Если больному после операции назначали тироксин (Т4), то за месяц до начала йодной терапии его необходимо отменить, чтобы убедиться, что уровень TSH увеличился.
Важно увеличение уровня TSH, а не сама по себе отмена гормона. После проведения терапии йодом больному назначают короткий 6-недельный курс приема трииодтиронина (Т3). В отличие от Т4, последний обладает более продолжительным эффектом, который поэтому легче поддается контролю. Через 10 дней прием Т3 отменяют и больному снова проводят сканирование всего тела и шеи. Наличие области повышенного накопления изотопа в области шеи или в другом месте свидетельствует о наличии метастазов или неудаленной первичной опухоли. В таких случаях больным назначают терапевтическую дозу 131I (5,5-7,0 ГБк).
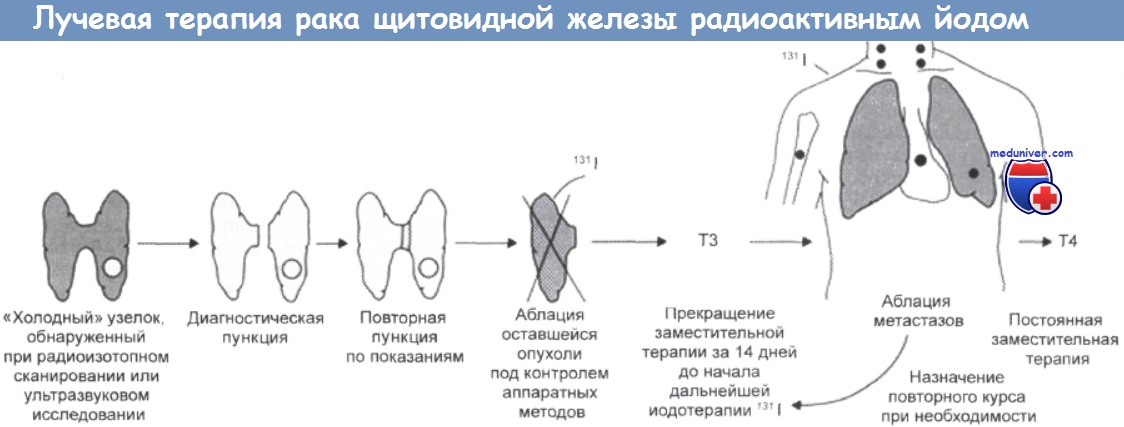
Лечение радиоактивным йодом относится к адресному типу лучевой терапии, который широко применяется для лечения рака у человека. Его можно повторять примерно через каждые три месяца (за 10 дней до начала йодной терапии нужно отменять назначение Т3) в течение всего времени, пока результаты повторного сканирования свидетельствуют о наличии очагов опухоли, т. е. фактически до полного исчезновения метастазов (если лечение вообще оказывается эффективным). Вместо отмены назначения тиреоидных гормонов можно использовать рекомбинатный препарат человеческого тиреотропина.
Несмотря на потенциальную опасность воздействия высоких доз радиации на шею, костный мозг, гонады и на другие критические органы, необходимо учитывать, что такой вид облучения оказывается эффективным даже для больных с множественными метастазами. Таким больным (фактически большинству с раком щитовидной железы) необходимо на протяжении всей жизни вводить Т4, поскольку вся функционально активная ткань щитовидной железы у них давно атрофирована. У больных, особенно молодого возраста, уже не реагирующих на йодную терапию, введение Т4 может привести к регрессии очагов остаточной опухоли, поскольку ее рост в определенной степени зависит от TSH, эффект которого снимается экзогенным Т4. В некоторых случаях, при прекращении больным приема ТЗ или Т4, ему следует назначить терапевтическую дозу 131 I. При этом за 2-3 дня до приема иода больному необходимо вводить TSH.
Хотя назначение 131 I после операции по поводу папиллярной карциномы сейчас рассматривается как перелечивание, в классических работах Маццаферри с сотрудниками (Италия) и Тюбиана с сотрудниками (Франция) продемонстрирована эффективность этой лечебной процедуры. К числу противопоказаний к йодной терапии относится возраст (более 40 лет), наличие большой первичной или плохо дифференцированной опухоли, а также ее распространение за пределы капсулы.
Локальные рецидивы возникают в два раза чаще после проведения субтотальной или тотальной тиреоэктомии, что приводит к увеличению смертности больных. Терапия радиоактивным иодом показана для больных с множественными, локально инвазивными и большими первичными опухолями, а также при отдаленных метастазах, для которых наблюдается хорошее поглощение изотопа. Разработка новых дозиметрических методов применительно к каждому больному обеспечивает более точное распределение изотопа и формирование более адекватной дозы облучения. Наконец, назначение Т4 полезно даже больным, которым не проводилась тотальная тиреоэктомия и которые не нуждаются в заместительной терапии.
Особенно важная роль уделяется постоянному наблюдению и периодическому обследованию больных, поскольку даже спустя много лет после полного излечения у них могут возникнуть рецидивы. Обследование должно включать тщательную пальпацию области щитовидной железы, регулярное рентгенографическое обследование грудной клетки (раз в три года, поскольку наиболее часто метастазы образуются в легких и в лимфатических узлах средостения), а также измерение уровня сывороточного тиреоглобулина. В настоящее время радиоизотопное сканирование используется редко, и прием больным Т4 должен сопровождаться ежегодным, в течение пяти лет после излечения, измерением уровня тиреоглобулина. В процессе дальнейшего наблюдения уровень тиреоглобулина измеряют через каждые два года.
Радиоизотопное сканирование проводят через 3-5 дней после назначения изотопа (в качестве безопасной амбулаторной дозы назначают 185 МБк радиоактивного иода). Этот метод все чаще используется при обследовании больных с аномальным уровнем тиреоглобулина, или прооперированных больных с неполностью удаленной опухолью.
Облучение рака щитовидной железы внешним пучком
Для больных, у которых не удается получить хорошую картину захвата радиоактивного иода, и особенно при наличии нерезектабельной локальной опухоли (включая большинство случаев анапластической карциномы и многие медуллярные карциномы), используют облучение внешним пучком.
Для предупреждения возникновения рецидива и обструкционного синдрома назначают достаточно радикальную дозу излучения, порядка 65 Гр за 7 недель. Такая доза обычно оказывает лечебное действие, которое, однако, лишь в редких случаях проявляется у больных с анапластической карциномой.
Для лечения больных с мелкоклеточными опухолями и лимфомами щитовидной железы почти всегда используется облучение внешним пучком. Эти опухоли облучают в меньшей дозе, порядка 40-50 Гр за 4-5 недель. Поскольку величина облучаемого объема ткани может достигать существенных размеров и захватывает часть спинного мозга, облучение щитовидной железы представляет собой трудную техническую задачу. В некоторых клиниках разработана специальная техника с использованием угловых или вращающихся полей.
В других предпочитают использовать более традиционную схему облучения с одного переднего поля, конфигурация которого задается с помощью свинцовых блоков, защищающих гортань и, при необходимости, легкие. Поля должны включать полностью щитовидную железу и, по возможности, надключичные и шейные лимфатические узлы, которые в первую очередь поражаются опухолью. При распространении опухоли на область верхнего средостения, поле облучения необходимо расширить вниз. Например, хорошо известно, что опухоли щитовидной железы могут распространяться внутритра-хеально, вызывая у больных стеноз.
Рак щитовидной железы – злокачественное узловое образование, способное образовываться из эпителия, естественно функционирующего в железе.
Рак щитовидной железы составляет более четверти всех злокачественных новообразований в области головы и шеи. За последние десятилетия, по данным ВОЗ, заболеваемость РЩЖ в мире выросла в 2 раза. Рак щитовидной железы ежегодно является причиной смерти 1% всех больных, умирающих от злокачественных опухолей. Среди всех злокачественных новообразований, это заболевание составляет 0.5 — 3.5 %. То есть на 100 000 населения РЩЖ заболевают в среднем 0.5-0.6 мужчин и 1.2-1.6 женщин.
В России самые высокие показатели заболеваемости отмечаются в Брянской области: 4.9 на 100 000 мужчин и 26.3 на 100 000 женщин. Также наиболее неблагополучные районы в отношении заболеваемости РЩЖ — Архангельская, Саратовская, Свердловская и Магаданская области.
Факторы риска развития рака щитовидной железы
Основные факторы риска:
- Йодная недостаточность
- Ионизирующее излучение (Радиация)
- Наследственность (Семейный анамнез)
К факторам риска также относится наличие у пациентов узловых образований в щитовидной железе, т.е. узловые зобы, рецидивирующие их формы, узловые формы хронических тироидитов.
Регионы мира с пониженным содержанием йода в воде и пищевых продуктах, являются эндемичными для узлового зоба, на фоне которого нередко развивается рак щитовидной железы. В Российской Федерации эндемичными районами считаются Алтайский край и республика Адыгея.
С момента обнаружения данного физического явления и до настоящего момента роль этого фактора, как причины развития РЩЖ, резко возросла. Действие данного фактора, прежде всего, связано с попаданием в организм радиоактивных изотопов йода ( 131 I, 125 I). Так, было установлено, что жители Хиросимы и Нагасаки, которые попали под облучение после взрыва атомных бомб, болели раком щитовидной железы в 10 раз чаще, чем остальные японцы.
В России был отмечен резкий рост заболеваемости РЩЖ, особенно у детей, в регионах, которые подверглись радиоактивному загрязнению после аварии на Чернобыльской АЭС, это Брянская, Тульская, Рязанская области.
Риск развития РЩЖ выше в семьях, где отмечались случаи этого заболевания. Наследственная форма рака связана с наследственными синдромами множественной эндокринной неоплазии (МЭН).
Типы рака щитовидной железы
По гистологическим формам классифицируются четыре типа рака щитовидной железы: папиллярный, фолликулярный, медуллярный и анапластический.
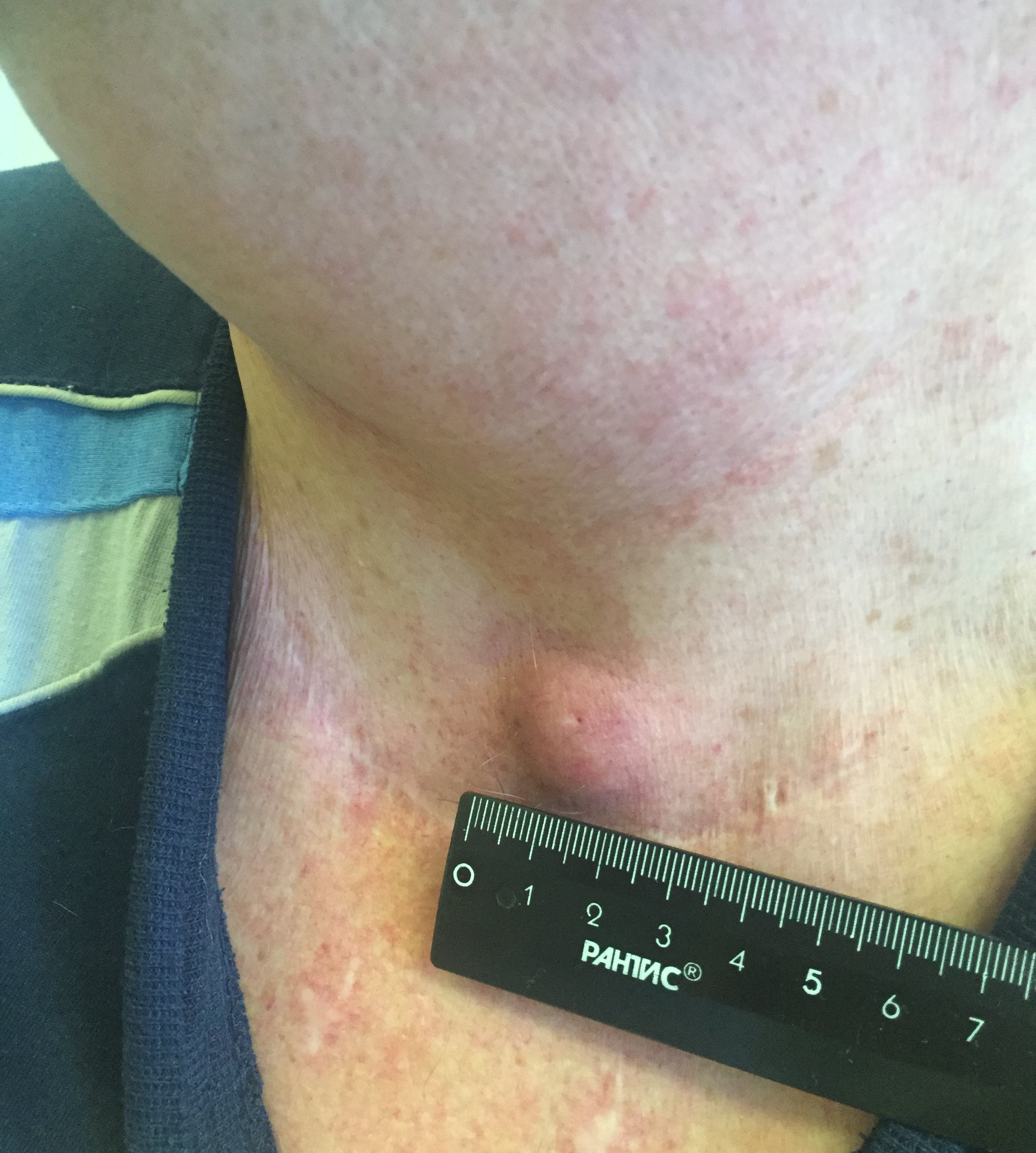
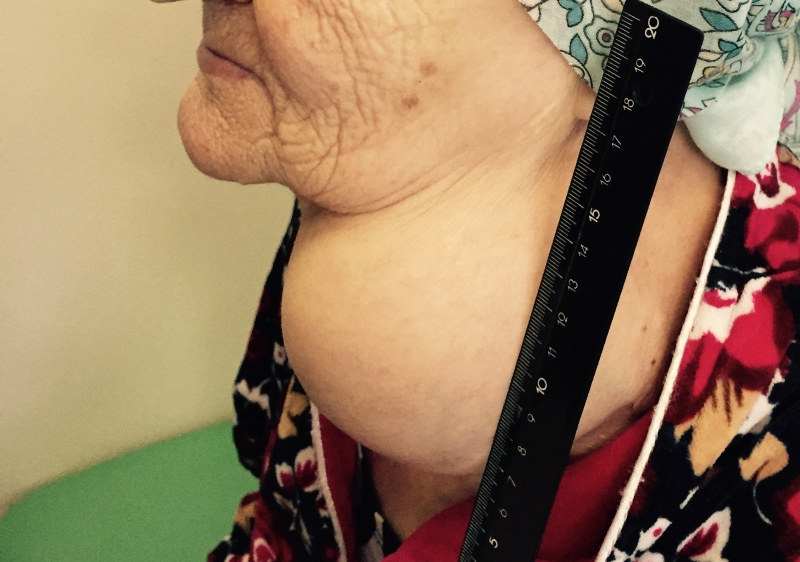
Папиллярный рак — наиболее благоприятный тип. Встречается у детей и взрослых, чаще заболевают в 30-40 лет. Является преобладающей формой РЩЖ у детей. Опухоль чаще возникает в одной из долей и лишь у 10-15% пациентов отмечается двустороннее поражение.
Папиллярная карцинома отличается достаточно медленным ростом. Метастазирует в лимфоузлы шеи, отдаленные метастазы в другие органы наблюдаются редко.
Фолликулярный рак встречается у взрослых с пиком заболеваемости в 50-55-м возрасте. Этот вид опухоли характеризуется медленным ростом. В поздних стадиях образует метастазы в лимфатических узлах шеи, а также в костях, печени и легких. Метастазы фолликулярного рака сохраняют способность захватывать йод и синтезировать тиреоглобулин.
Медуллярный рак может быть как самостоятельным заболеванием, так и компонентом МЭН синдрома. Чаще определяется в пожилой возрастной группе пациентов с узловым зобом. Характеризуется быстрым ростом с инвазией в близлежащие органы и ранним метастазированием.
Анапластический рак чаще возникает у пожилых пациентов с узловым зобом. Его отличает агрессивная форма и раннее метастазирование. Быстрый рост опухолевого узла может приводить к его некротическому распаду, изъязвлению и может служить источником кровотечений.
Гистогенетическая классификация рщж
| ИСТОЧНИК РАЗВИТИЯ | ГИСТОЛОГИЧЕСКАЯ СТРУКТУРА ОПУХОЛИ | |
| доброкачественные | злокачественные | |
| А-клетки | Папиллярная аденома | |
Симптомы
Заболевание может проявляться различными симптомами. Они зависят от стадии, распространенности опухолевого процесса и развившихся осложнений. Небольшие опухоли щитовидной железы обычно не сопровождаются клинической симптоматикой и выявляются случайно при ультразвуковом исследовании. Первой причиной обращения к врачу может послужить увеличение одного шейного лимфатического узла, который при дальнейшем обследовании оказывается метастазом РЩЖ.
Симптомы рака щитовидной железы часто схожи с симптомами простуды, ангины, инфекционных заболеваний:
- Припухлость на шее. Небольшие узлы на шее может выявить только врач, но иногда припухлость можно заметить во время глотания.
- Увеличение шейных лимфоузлов. Однако, этот симптом часто сопровождает простуду или ангину и не связан со злокачественным процессом.
- Изменение тембра голоса. Иногда большой узел щитовидной железы давит на гортань, это может вызвать охриплость.
- Одышка. Причиной может явиться то, что увеличившаяся щитовидная железа вызывает сужение просвета трахеи.
- Затруднение глотания. Также узел щитовидной железы может сдавливать пищевод.
- Боль в шее или горле. Развитие рака щитовидной железы редко вызывает боль, но в сочетании с другими симптомами это сигнал незамедлительно обратиться к врачу.
Большая часть подобных симптомов связана с появлением узла щитовидной железы, который в более чем 95% случаев оказывается доброкачественным. Узлы щитовидной железы довольно частое явление, и в пожилом возрасте риск их появления увеличивается. При обнаружении узелков в области щитовидной железы следует обратиться к врачу.
Диагностика
Ультразвуковая диагностика позволяет обнаружить опухолевые образования от 2-3 мм, определить точное топографическое расположение в железе, визуализировать инвазию капсулы, оценить размеры и состояние лимфатических узлов шеи.
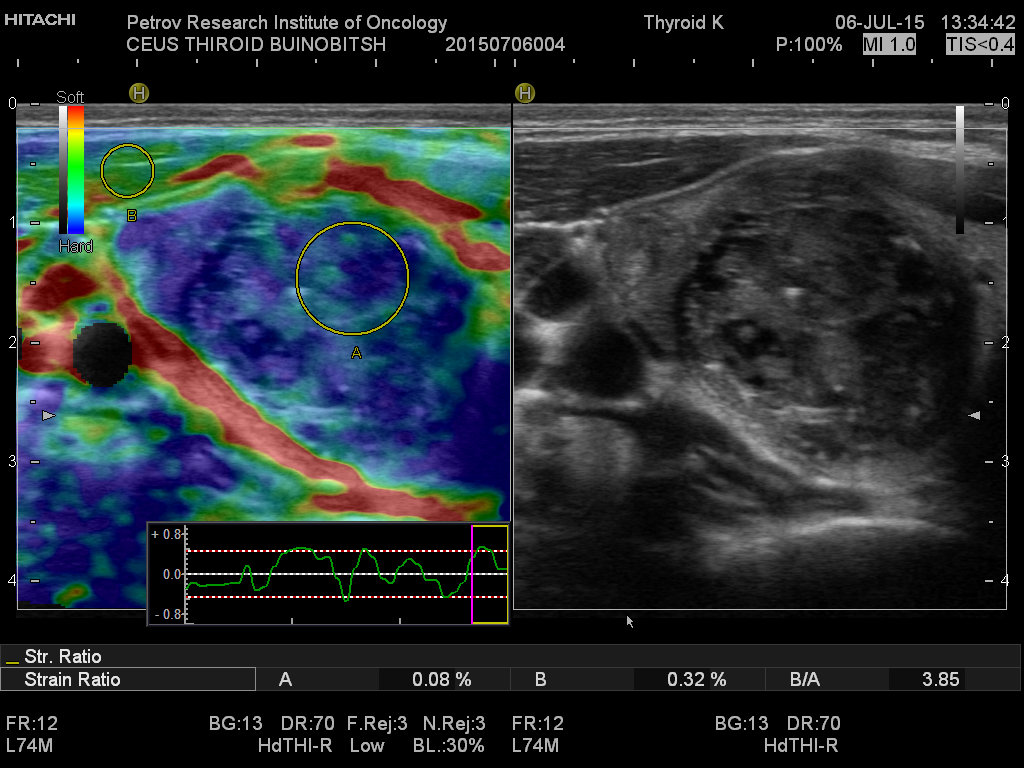
Магнитно-резонансная томография (МРТ) позволяет получить детальную топографо-анатомическую картину опухоли и ее соотношение с органами и структурами шеи. Это необходимо при планировании хирургического лечения в случае инвазии опухоли в соседние структуры.
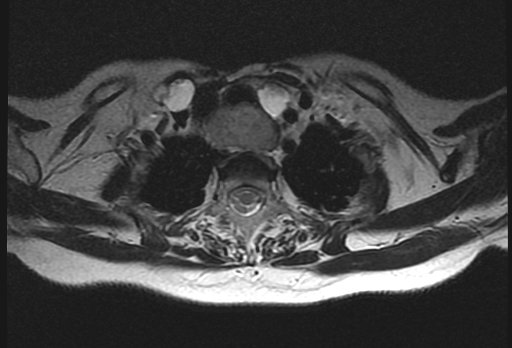
Компьютерная томография применяется для определения метастатического поражения легких и костей.
Сцинтиграфия щитовидной железы с 125 I, 131 I применяется в основном для выявления остаточной тиреоидной ткани после хирургического лечения, а также для диагностики рецидивов. Она позволяет оценить способность метастазов захватывать йод при планировании радиойодтерапии.
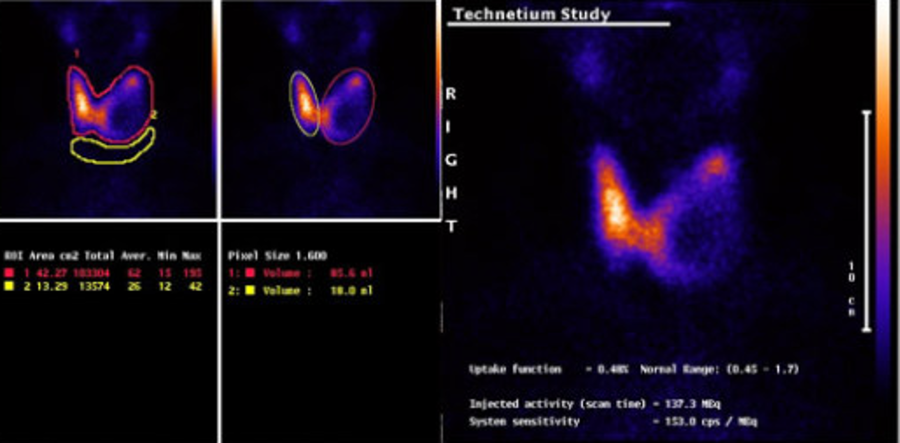
Остеосцинтиргафия позволяет оценить наличие/отсутствие метастатического поражения костей скелета.
Тонкоигольная аспирационная биопсия выполняется преимущественно под контролем УЗИ, позволяет прицельно получить материал для цитологического исследования, что позволяет в большинстве случаев верифицировать диагноз. ТАБ подозрительных лимфатических узлов дает возможность установить метастатический характер поражения.
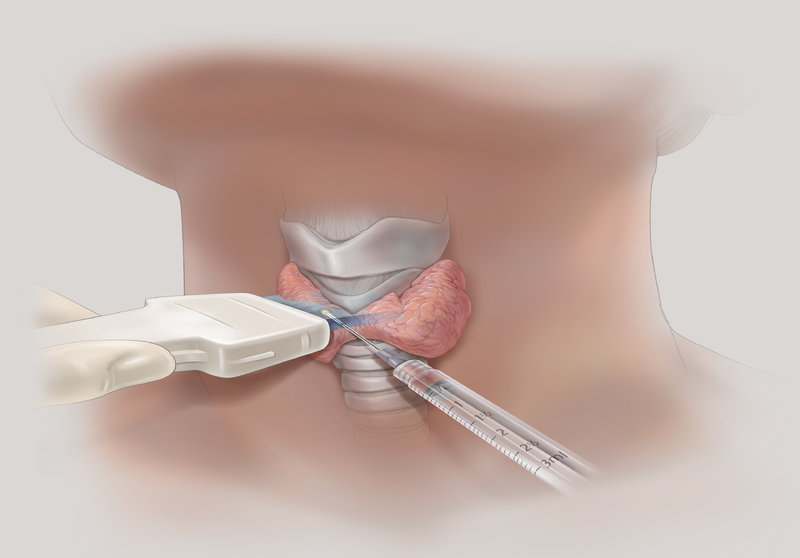
Позитронно-эмиссионная томография (ПЭТ) выявляет очаги повышенной метаболической активности, выполняется для диагностики метастазов РЩЖ, не накапливающих йод и не выявляемых при сцинтиграфии.
Кальцитонин: гормон щитовидной железы, вырабатывается С-клетками. (Норма-0-11,5 пг/мл). Значительное повышение уровня гормона наблюдается при медуллярном раке, уровень повышения связан со стадией заболевания и размерами опухоли.
Тиреоглобулин: определение уровня при дифференцированном раке щитовидной железы позволяет контролировать возникновение рецидива опухоли. После тиреоидэктомии уровень тиреоглобулина должен приближаться к нулю.
Стадирование рака щитовидной железы

Лечение
Основной метод лечения больных раком щитовидной железы – хирургическое лечение в сочетании с курсами радиойодтерапии, таргетной терапией и супрессивной гормонотерапией, а также дистанционной гамма-терапией по показаниям.
Объем оперативного вмешательства зависит в первую очередь от стадии заболевания, от того, насколько распространился злокачественный процесс. Кроме того, лечение определяется морфологическим вариантом опухоли и возрастом пациента.
У больных папиллярным и фолликулярным раком при небольших стадиях может выполняться гемитиреоидэктомия — удаление одной доли с оставлением или резекцией перешейка железы. При распространении опухоли (T1-3N0M0) производят тотальное удаление щитовидной железы. На поздних стадиях злокачественного процесса производят экстрафисциальную тотальную тиреоидэктомию с удалением лимфоузлов.
Если диагностирован медуллярный, недифференцированный и папиллярный рак, во всех случаях показано тотальное удаление железы — тиреоидэктомия.
Если лимфатические узлы шеи поражены метастазами, выполненяют шейную лимфаденэктомии, в некоторых случаях — расширенную шейную лимфаденэктомию с резекцией соседних органов и структур, в зависимости от распространенности процесса.
Радиойодтерапия После хирургического лечения пациентам с РПЖ назначают проведение радиойодтерапия для уничтожения возможных микрометастазов и остатков тиреоидной ткани (используется 131 I).
Дистанционная лучевая терапия: стандартом лечения является проведение неоадъювантной (предоперационной) терапии для больных с недифференцированным и плоскоклеточным РЩЖ.
Супрессивная гормональная терапия (СГТ) назначается пациентам с папиллярным и фолликулярным РЩЖ в качестве компонента комплексного лечения после операции, чтобы подавить секрецию тиреотропного гормона (ТТГ).
Химиотерапия показана при медуллярном и недифференцированном РЩЖ.
Таргетная терапия применяется для лечения медуллярного и радиойодрезистентных форм дифференцированного РЩЖ.
Наблюдение и прогноз
Сроки наблюдения
- 1й год после лечения – 1раз в 3 мес
- 2 – 3й год после лечения – 1 раз в 4 мес
- 4 – 5й год после лечения – 1 раз в 6 мес
- 6й и последующие годы после лечения – 1 раз в год
Прогноз
| 5-летняя выживаемость: | 10-летняя выживаемость: | |
| Папиллярный рак | 95,3% | 94,2% |
| Фолликулярный рак | 90,1% | 85,7% |
| Медуллярный рак | 87,8% | 80% |

РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Архив - Клинические протоколы МЗ РК - 2012 (Приказы №883, №165)
Общая информация


Классификация
Классификация применима только для рака, который должен быть подтвержден гистологически. Регионарными считаются лимфатические узлы шеи и верхнего средостения.
Факторы и группы риска
Диагностика
Диагностические критерии
На основании жалоб, анамнеза, клинико-инструментального и лабораторных видов обследования необходима консультация онколога.
Диагностические исследования при карциномах щитовидной железы
| Исследование | Цель |
| Ультразвуковое исследование | Оценка щитовидной железы, опухоли и лимфатических узлов шеи |
| Пункционная биопсия узла щитовидной железы | Верификация диагноза |
| Пункционная или эксцизионная биопсия лимфоузла шеи | Верификация диагноза |
| Рентгенография, томография шеи и средостения | Определение локализации и размеров опухоли |
| Рентгенография органов грудной полости | Диагностика метастазов в легких и лимфатических узлах средостения |
| Сканирование | Диагностика медиастинальных новообразований щитовидной железы или отдаленных метастазов рака (технеций-99м, йод-123, йод-131, таллий-201) |
| Компьютерная томография | Определение точных размеров, локализации и распространения опухоли |
| Ларингоскопия | Диагностика вовлечений в опухолевый процесс возвратного нерва |
| МРТ, томография | Уточнение данных о сосудистых структурах шеи и средостения. Выявление возможной инвазии пищевода, трахеи, магистральных сосудов |
| Эзофагоскопия, эзофагография | Диагностика инвазии пищевода |
| Бронхоскопия | Выявление инвазии опухоли в трахею |
| Гормональные исследования | Диагностика гипертиреоза, гипотиреоза и определение маркеров рака щитовидной железы |
Дифференциальный диагноз
| Нозологическая форма | Клинические проявления |
| Узловой зоб | Пальпаторно определяемое узловое образование в проекции щитовидной железы. Необходима пункционная биопсия. |
| Диффузно-токсический зоб | Влажность кожных покровов, тремор, тахикардия, видимое увеличение щитовидной железы. Необходим радиоиммунологический анализ. |
| Аутоиммунный тиреоидит | Диффузное увеличение щитовидной железы, равномерная деревянистая плотность. Поверхность однородная, зернистая. Необходимо проведение трепан-биопсии. |
Лечение
Цели лечения - ликвидация опухолевого очага и метастазов.
Лечение: основной метод лечения больных состоит в выполнении оперативных вмешательств в сочетании с супрессивной гормонотерапией L-тироксином, а также дистанционной гамма-терапии и курсами радиойодтерапии по индивидуальным показаниям. В большинстве наблюдений такой подход приводит к излечению больных.
Немедикаментозное лечение: режим - свободный. Диета стол - №1, №15.
Супрессивная терапия тироксином (стт)
Заместительная гормональная терапия (згт)
Дистанционная лучевая терапия
Хирургическое лечение
Радиойодтерапия
Госпитализация
Информация
- Периодические протоколы диагностики и лечения злокачественных новообразований у взрослых МЗ РК (Приказ №883 от 25.12.2012)
- 1. Bonner JA, Harari PM, Giralt J, et al. Cetuximab prolongs survival in patients with locoregionally advanced squamous cell carcinoma of head and neck: A phase III study of high dose radiation therapy with or without cetuximab (abstract). ASCO Annual Meeting Proceedings (post-meeting edition). J Clin Oncol 2004;22:5507. 2. Greene FL, Page DL, Fleming ID, et al (eds). AJCC Cancer Staging Manual, Sixth Edition Springer-Verlag: New York 2002. 3. Colasanto JM, Prasad P, Nash MA, et al. Nutritional support of patients undergoing radiation therapy for head and neck cancer. Oncology 2005;19:371-382 4. Медицинские клинические рекомендации Европейского общества медицинских онкологов (ЕSМО. Москва 2006г) 5. Piccirillo JF, Lacy PD, Basu A, et al. Development of a new head and neck cancer-specific comorbidity index. Arch Otolaryngol Head Neck Surg 2002;128:1172-1179. 6. Hall SF, Groome PA, Rothwell D. The impact of comorbidity on the survival of patients with squamous cell carcinoma of the head and neck. Head Neck 2000;22:317-322. 7. de Graeff A, de Leeuw JR, Ros WJ, et al. Pretreatment factors predicting quality of life after treatment for head and neck cancer. Head Neck 2000;22:398-407 8. Piccirillo JF, Costas I, Claybour P, et al. The measurement of comorbidity by cancer registries. J Reg Management 2003;30:8-14. 35. Johnson JT, Barnes EL, Myers EN, et al. The extracapsular spread of tumors in cervical node metastasis. Arch Otolaryngol Head Neck Surg 1981;107:725-729. 9. Horiot JC. [Controlled clinical trials of hyperfractionated and accelerated radiotherapy in otorhinolaryngologic cancers] [Article in French]. Bull Acad Natl Med 1998;182:1247-1260; discussion 1261.]. 10. Mittal BB, Kepka A, Mahadevan A, et al. Tissue/Dose Compensation to reduce toxicity from combined radiation and chemotherapy for advanced Head and Neck Cancers. Int J Cancer (Radiat Oncol Invest) 2001;96:61-70. 11. Teh BS, Mai WY, Grant WH 3rd, et al. Intensity modulated radiotherapy (IMRT) decreases treatment-related morbidity and potentially enhances tumor control. Cancer Invest 2002;20:437-451. 12. De Neve W, Duthoy W, Boterberg T, et al. Intensity Modulated Radiation Therapy: Results in Head and Neck cancer and Improvements ahead of us. Int J Radiat Oncol Biol Phys 2003;55:460. 13. Bernier J, Domenge C, Ozsahin M, et al. Postoperative irradiation with or without concomitant chemotherapy for locally advanced head and neck cancer. N Engl J Med 2004;350:1945-1952. 90 14. Cooper JS, Pajak TF, Forastiere AA, et al. Postoperative concurrent radiotherapy and chemotherapy for high-risk squamous-cell carcinoma of the head and neck. N Engl J Med 2004;350:1937-1944. 15. Bernier J, Cooper JS, Pajak TF, et al. Defining risk levels in locally advanced head and neck cancers: A comparative analysis of concurrent postoperative radiation plus chemotherapy trials of the EORTC (#22931) and RTOG (# 9501). Head Neck 2005;27:843-850. 16. Vokes EE, Stenson K, Rosen FR, et al. Weekly carboplatin and paclitaxel followed by concomitant paclitaxel, fluorouracil, and hydroxyurea chemoradiotherapy: curative and organ-preserving therapy for advanced head and neck cancer. J Clin Oncol 2003;21:320-326. 17. Hitt R, Grau J, Lopez-Pousa A, et al. Phase II/III trial of induction chemotherapy (ICT) with cisplatin/5-fluorouracil (PF) vs. docetaxel (T) plus PF (TPF) followed by chemoradiotherapy (CRT) vs. CRT for unresectable locally advanced head and neck cancer (LAHNC) (abstract). ASCO Annual Meeting Proceedings (post-meeting edition).J Clin Oncol 2005;23:5578. 18. Schrijvers D, Van Herpen C, Kerger J, et al. Docetaxel, cisplatin and 5-fluorouracil in patients with locally advanced unresectableor head and neck cancer: a phase I-II feasibility study. Ann Oncol 2004;15:638-645.
Организационные аспекты внедрения протокола
1. Процент вновь выявленных пациентов со злокачественным новообразованием щитовидной железы, получающих начальное лечение в течение двух месяцев после начала заболевания = (Количество пациентов, с установленным диагнозом рака щитовидной железы, получающих начальное лечение в течение двух месяцев после начала заболевания/Все пациенты с впервые установленным диагнозом рака щитовидной железы) х 100%;
2. Процент онкологических больных, получающих химиотерапию в течение двух месяцев после проведения оперативного лечения = (Количество онкологических больных, получающих химиотерапию в течение двух месяцев после проведения оперативного лечения/количество всех больных раком щитовидной железы после проведения оперативного лечения, которым требуется проведение химиотерапии) х 100%;
3. Процент рецидивов рака щитовидной железы у пациентов в течение двух лет = (Все пациенты с рецидивами рака щитовидной железы в течение двух лет/все прооперированные пациенты с диагнозом рака щитовидной железы) х 100%.
2. Абисатов Г.Х. - зав. каф. онкологии, маммологии Казахстанско-Российского медицинского университета, д.м.н., проф.
Результаты внешнего рецензирования: положительное решение.
Выбор метода лечения рака щитовидной железы во многом зависит от степени распространения опухоли, её морфологии, наличия региональных и/или отдалённых метастазов и других факторов.
Основной метод лечения - хирургический - применяют при дифференцированных формах рака, иногда дополняя другими методами.
При недифференцированных и неэпителиальных злокачественных опухолях щитовидной железы показано комбинированное и комплексное лечение.
Хирургическое лечение
Оптимальный объём операции остаётся предметом дискуссий. Некоторые авторы настаивают на тиреоидэктомии во всех случаях, аргументируя своё мнение, во-первых, высокой частотой первично множественного рака, во-вторых, тем, что оставляемая при резекции ткань щитовидной железы активно поглощает 131 I и затрудняет как диагностику рецидивов (тест с тиреоглобулином), так и лечение отдалённых метастазов радиоактивным йодом.
Сторонники щадящих операций считают, что удаление доли щитовидной железы с перешейком может быть выполнена при раке I и II стадии.
Они указывают, что представление о множественном поражении щитовидной железы преувеличено; согласно их данным, множественные очаги опухоли встречаются при высокодифференцированном раке у 12-15% больных. Исследования с контрастированием лимфатических сосудов щитовидной железы in vivo показали, что лимфоотток от каждой доли обособлен, а анастомозы между долями встречаются только в 8% случаев. Современные методы исследования (УЗИ и ТАБ) позволяют до операции определить морфологию подозрительных узлов и объём резекции.
Операция тиреоидэктомии, даже выполненная опытным хирургом, чревата серьёзными осложнениями. Так, повреждение возвратного нерва происходит в 5,2-15%, а гипопаратиреоз вследствие удаления или травматизации паращитовидных желёз развивается в 2,5-20,1% случаев.
Согласно рандомизированным исследованиям, проведённым МНИОИ им. П.А. Герцена совместно с несколькими онкологическими диспансерами, после тиреодектомии по поводу рака щитовидной железы I и II стадии выживают без рецидивов и метастазов 5 лет и более 94,1% больных, при выполнении лобэктомии с перешейком у аналогичной группы больных - 93,4% (т.е. разница статистически недостоверна).
Специалисты клиники Мэйо, США, предложили свою систему для выбора оптимального объёма операции (табл. 40-1, 40-2).
- Функционально-сохраняющая операция (лобэктомия с перешейком) допустима лишь при высокодифференцированном раке, поразившем одну долю щитовидной железы.
| Критерии | Значения |
| Возраст | Женщины старше 50 лет |
| Мужчины старше 40 лет | |
| Морфология | Высокодифференцированный рак |
| Инвазия | Опухоль ограничена долей или долей и перешейком |
| Размеры | Опухоль максимальным диаметром 4 см |
Оперативные вмешательства по поводу злокачественных опухолей щитовидной железы необходимо выполнять с соблюдением общих онкологических принципов. Поражённую долю целесообразно удалять экстрафасциально с перевязкой щитовидных артерий, выделением возвратного нерва и околощитовидных желёз, особенно если опухоль располагается вблизи капсулы железы (рис. 40-2).

Рис. 40-2. Фото момента операции: выделены паращитовидное тельце A) и возвратный нерв B).
Для окраски паращитовидных желёз с целью их обнаружения пользуются 1% раствором метиленового синего. При этом щитовидная железа приобретает бледно-голубой цвет, а паращитовидные железы - различные оттенки зелёного.
Для сохранения функции паращитовидных желёз перевязку нижней щитовидной артерии производят у собственной капсулы щитовидной железы. Необходим адекватный операционный доступ, позволяющий провести тщательную ревизию щитовидной железы и зон регионального лимфатического оттока, включая паратрахеальную клетчатку.
Увеличенные лимфатические узлы необходимо направить на срочное морфологическое исследование.
При обнаружении региональных метастазов показана фасциально-футлярная шейная диссекция по щитовидному варианту. При этой операции единым блоком удаляют клетчатку с лимфатическими узлами внутренней яремной цепи, бокового треугольника шеи, включая заакцессорную область.
Границами иссекаемой области служат: спереди - латеральный край трапециевидной мышцы, медиально - гортань и трахея, сверху - задняя часть двубрюшной мышцы, снизу - ключица, сзади - лестничные мышцы. При наличии паратрахеальных метастазов удаляют клетчатку этой области и области передневерхнего средостения.
При двустороннем региональном метастазировании возможно одномоментное удаление щитовидной железы и лимфатических узлов с одной стороны и поэтапное отсроченное удаление шейной клетчатки со второй стороны. Нежелательна одновременная перевязка обеих внутренних яремных вен, которая может стать причиной нарушения мозгового кровообращения.
Многие годы для удаления метастазов рака щитовидной железы, расположенных глубоко за грудиной, использовали Т-образную стернотомию. В настоящее время эту операцию выполняют без рассечения грудины с помощью эндоскопической техники. При этом онкологическая радикальность операции сохраняется.
Повторные операции
Основные причины нерадикальных операций при раке щитовидной железы - гиподиагностика и тактические ошибки при выборе объёма операции. Часто после гистологического исследования доли, удалённой по поводу аденомы, обнаруживают рак, и приходится решать вопрос о необходимости повторной операции. При обнаружении остаточной опухоли в щитовидной железе показана повторная операция.
Однако нередко после повторной операции опухоли обнаружить не удаётся, хотя объём операции (резекция доли, в которой локализовалась опухоль) не был адекватным. Если повторные операции выполнить всем больным после неадекватной по объёму первой операции, то у 38,8% больных в удалённом препарате не обнаруживают опухоли (табл. 40-3). Повторные операции в этих случаях показаны только при прорастании опухолью капсулы щитовидной железы, при медуллярном и низкодифференцированном раке, при размере удалённой опухоли более 3 см, если граница резекции прошла ближе 2,5 см от края опухоли.
Таблица 40-3. Операционные и гистологические находки после повторных операций (404 больных)
| Локализация поражения в щитовидной железе | Изменения в железе | Метастазы в лимфатические узлы шеи | |||
| Абс. | % | Абс. | % | ||
| Рак | в оперированной доле | 81 | 20,2 | 37 | 9,2 |
| в противоположной доле | 46 | 11,4 | 18 | 4,5 | |
| в обеих долях | 68 | 16,9 | 37 | 9,2 | |
| Аденомы | 51 | 12,7 | 7 | 1,7 | |
| Нет паталогий в железе | 158 | 38,8 | 73 | 18,2 | |
| Всего | 404 | 100 | 172 | 42,8 | |
Осложнения хирургического лечения
Заканчивая операцию, хирург должен тщательно ревизовать рану и убедиться в отсутствии кровотечения. В ближайшем послеоперационном периоде наиболее частым послеоперационном осложнением является кровотечение с образованием гематомы. Клинически это осложнение вызывает деформацию передней поверхности шеи, а также ухудшение дыхания больного, что требует срочного хирургического вмешательства.
Специфические осложнения операций на щитовидной железе - поражение возвратного нерва и паращитовидных желёз.
Частота повреждений возвратного нерва, по данным литературы, существенно колеблется (от 2,6 до 15%).
Нередко это связано с методикой оценки этого осложнения.
Известно, что голосовые связки могут быть парализованы в состоянии разведения в стороны (аддукционный паралич) или когда они располагаются по средней линии. При двустороннем аддукционном параличе происходит обтурация просвета гортани и необходима срочная трахеотомия по жизненным показаниям.
Односторонний аддукционный паралич суживает просвет гортани наполовину, клинически проявляясь одышкой при физической нагрузке. Голосовая функция при этом страдает незначительно, что иногда ошибочно трактуют как отсутствие поражения возвратного нерва. Таким образом, достоверно определить, повреждён ли возвратный нерв, можно только при визуальном осмотре гортани (непрямая или прямая ларингоскопия).
При оценке функции возвратного нерва необходимо различать временное нарушение его функций (парез) или постоянное (паралич). При парезе возвратного нерва после 2-3 нед адекватного лечения голосовая функция полностью восстанавливается. При двухстороннем параличе возвратного нерва, для того чтобы избавить больного от трахеотомической трубки, выполняют реконструктивную операцию (аритеноидэктомия с латерофиксацией).
Для купирования острого приступа судорог внутривенно медленно вводят 10-20 мл (в тяжёлых случаях - 40-50 мл и более) 10% раствора кальция хлорида. Введение препарата прекращают, как только исчезнут судорожные сокращения мышц кисти. Для предупреждения приступа внутримышечно вводят раствор кальция глюконата, тахистин, витамин D2.
Лучевая терапия
Лучевую терапию при злокачественных опухолях щитовидной железы можно проводить в виде наружного облучения и лечения радиоактивным йодом.
При дифференцированных формах рака щитовидной железы с прорастанием капсулы органа и обширным региональным метастазированием, особенно в паратрахеальные области и средостение, операцию дополняют дистанционным облучением.
При неоперабельном раке используют преимущественно лучевую терапию с классическим фракционированием дозы по 2 Гр 5 раз в нед до суммарной очаговой дозы 40 Гр. Облучают первичную опухоль, переднебоковые отделы шеи, медиальные 2/3 надключичных зон и область передневерхнего средостения.
Послеоперационное облучение показано при наличии сомнений в радикальности оперативного вмешательства и при гистологическом обнаружении недифференцированной опухоли. Используют лучевую терапию в суммарной очаговой дозе до 50 Гр с возможностью подведения на отдельные участки (остатки опухоли) до 70 Гр.
Лечение метастазов рака щитовидной железы радиоактивным йодом ( 131 I) эффективно только при отсутствии ткани щитовидной железы. Сохранённая ткань щитовидной железы поглощает весь введённый препарат, не позволяя ему достичь метастазов. При папиллярном и фолликулярном раке после тиреоидэктомии на 4 нед отменяют левотироксин.
Этого срока достаточно для выведения из организма тиреоидных гормонов.
Химиотерапия
Химиотерапия при злокачественных опухолях щитовидной железы имеет вспомогательное значение. Лишь при лимфосаркоме отмечена эффективность медикаментозного лечения в сочетании с лучевым воздействием. Опубликованы лишь единичные наблюдения эффективности современных схем противоопухолевого лекарственного воздействия при метастазах недифференцированного рака щитовидной железы.
Гормональная терапия
Уже в ближайшее время (на 7-8-е сут) после радикальной операции у больных развиваются гормональные нарушения и возникает необходимость в гормональной реабилитации. Таким больным рано назначают тиреоидные гормоны (левотироксин, лиотиронин, тиреокомб, тиреотом). Начальная доза зависит от веса и возраста больного, наличия сопутствующих сердечно-сосудистых заболеваний и составляет от 50-100 мкг при гемитиреоидэктомии до 200-250 мкг после тиреоидэктомии в сутки. В дальнейшем дозы корригируют с учётом содержания тиреоидных гормонов в сыворотке крови, определяемого радиоиммунным методом. Такая тактика позволяет нормализовать уровень Т3 и Т4 и подавить секрецию ТТГ.
Гормонотерапия с применением высоких доз тиреоидных препаратов может быть использована для замедления роста нерезектабельных злокачественных опухолей щитовидной железы.
Прогноз
Прогноз при злокачественных опухолях щитовидной железы зависит от степени дифференцировки опухоли, её первичной распространённости и адекватности лечения.
При высокодифференцированных формах опухоли - папиллярном и фолликулярном раке - более 80-90% больных живут без рецидивов 10-15 лет после операции. В то же время при недифференцированном и плоскоклеточном раке щитовидной железы описаны лишь единичные благоприятные исходы. Несмотря на использование современных методов комбинированного и комплексного лечения, большинство больных с этими высокозлокачественными опухолями живут менее 1 года с момента установления диагноза.
При распространении дифференцированного рака за пределы капсулы щитовидной железы прогноз ухудшается. Если у больных медуллярным раком щитовидной железы к моменту операции имеются метастазы в лимфатических узлах шеи и отдалённых органов, прогноз ухудшается, так как они не накапливают 131 I и не поддаются лучевой терапии.
Несомненное прогностическое значение имеют возраст и пол больного. Так, в молодом возрасте встречаются преимущественно высокодифференцированные опухоли с благоприятным прогнозом и медленным прогрессированием. У детей и подростков с дифференцированным раком щитовидной железы прогноз более благоприятный, чем у больных старше 40 лет. Результаты лечения дифференцированных форм рака приведены в табл. 40-4.
Таблица 40-4. Результаты лечения различных форм рака щитовидной железы
Читайте также:

