Фибро вейн для лечения гемангиом
Радикальное лечение гемангиом может быть осуществлено только хирургическими методами. Вместе с тем хирургическое вмешательство часто сопряжено с большими трудностями, такими как распространенность патологического процесса и трудно останавливаемое профузное кровотечение. Эти отягощающие моменты заставляют хирургов в ряде случаев, когда невозможно осуществить радикальное удаление гемангиомы, прибегать к вынужденным паллиативным операциям, направленным на уменьшение притока крови к опухоли, что способствует частичному сморщиванию, запустеванию и замещению сосудистых полостей соединительно-тканными элементами. К паллиативным методам относятся: перевязка крупных артерий, питающих гемангиоматозную опухоль, прошивание гемангиомы или обшивание ее по периферии и новый метод, нашедший признание у хирургов в последние годы и который также был подробно описан выше, - это эндоваскулярная окклюзия приводящих артерий. В большинстве же случаев такие паллиативные вмешательства, как перевязка и эндоваскулярная окклюзия приводящих артерий, при обширных поражениях являются первым этапом хирургического вмешательства, предшествующим более радикальной операции.
Радикальность хирургического лечения гемангиом заключается в полном удалении всех пораженных опухолью тканей с наложением первичного шва или аутодермопластикой, если дефект кожи значительный.
Характер оперативных вмешательств при обширных ангиоматозах конечностей, методика профилактики интра- и послеоперационной кровопотери были подробно описаны ранее. Следует еще раз напомнить о нарушении свертывающей системы крови, как одной из основных причин кровотечений при данной патологии, и необходимости тщательной предоперационной подготовки больных, включающей введение больших доз витаминов группы В и С, ингибиторов фибринолиза, препаратов, улучшающих функцию печени, а при резком снижении фибриназы - прямое, возможно, неоднократное переливание крови от донора с нормальным содержанием фибриназы. Дефицит фибриназы у этой категории больных может быть врожденным.
Диффузное поражение сосудистой опухолью всей конечности с одновременным поражением внутренних органов и нарушения свертывающей и фибринолитической систем крови являются противопоказанием для радикального удаления опухоли. Угроза кровотечений, прогрессирующее нарушение центральной гемодинамики в таких случаях служат показанием для ампутации конечности с целью спасения жизни больного.
Консервативное лечение
Из арсенала известных консервативных методов лечения в настоящее время сохраняют свое значение криотерапия и электрокоагуляция (Н.И. Кондрашин, 1963 г.; Н.И. Краковский, В.А. Таранович, 1974 г.; А.Ю. Соловко, И.М. Воронцов, 1980 г.; и др.). Наибольшее распространение в лечении поверхностных и небольших гемангиом у детей получила криотерапия, которая производится с помощью жидкого азота или жидкой углекислоты. Метод дает хороший косметический и лечебный эффект. Механизм терапии заключается в замораживании гемангиомы. Углекислота или азот находятся под высоким давлением в специальном металлическом баллоне. Выпускаемые через специальный металлический выпускник углекислота и азот превращаются в снежную массу с температурой до -80°. Комок снега накладывается на гемангиому, захватывая также участок здоровой кожи вокруг нее на 4-5 мм. Продолжительность первой аппликации на коже 20 с, на слизистой - 15 с. Реактивность тканей на криотерапию различна, поэтому нужно учитывать толщину кожных покровов и возраст детей. Если после первого сеанса на месте гемангиомы не появился пузырь, продолжительность следующей аппликации увеличивается на 3-5 с. После подсыхания пузыря и отторжения корочки через две недели на месте гемангиомы остается мало заметный рубец. При больших гемангиомах аппликацию следует начинать с одного края. При паукообразных простых кожных гемангиомах достаточно замораживать только центр опухоли, после чего исчезает неприятный рисунок гемангиомы.
Электрокоагуляция в виде точечных прижиганий электрокоагулятором показана при небольших кожных гемангиомах век, губ, наружного слухового прохода, подслизистого слоя ушной раковины и слизистой оболочки носа. Электрокоагуляция проводится под местным обезболиванием. Струп, образующийся от тотального электроожога, отторгается через 3-4 недели и остается гладкий белесоватый рубчик.
Лучевая терапия в настоящее время не проводится ввиду тяжелых специфических осложений и возникающих впоследствии соматических и генетических нарушений.
А.Ю. Соловко и И.М Воронцов (1980 г.) электрокоалуляцией пользовались более широко, применяя ее в лечении не только пятнистых и звездчатых гемангиом всех локализаций, но и для удаления кавернозных гемангиом, прорастающих кожу и подкожную клетчатку. В таких случаях они проводили только внутритканевую коагуляцию. Растянутый кожный мешок в дальнейшем при необходимости иссекался.
Лечение склерозирующими веществами определенного вида гемангиом не потеряло значения и сегодня, в настоящее время этот метод лечения многими авторами применяется достаточно широко. Для склерозирования гемангиом челюстно-лицевой области, небольших гемангиом на туловище, конечностях и волосистой части головы авторы (Л.В. Киселев, 1976 г.; В.Н. Дан, 1989 и 2003 гг.) чаще всего использовали спирт в разной концентрации (70-96%) в зависимости от возраста пациента, характера гемангиомы и ее локализации. После введения склерозирующего вещества целесообразно применять сдавливающую повязку. Склеротерапия в ряде случаев может сочетаться с перевязкой питающих гемангиому артерий. Для склерозирования небольших поверхностных гемангиом могут быть использованы современные склерозирующие препараты: тромбовар, этоксисклерол, фибро-вейн в разной концентрации. По данным вышеуказанных авторов, правильное применение склерозирующих веществ в лечении определенного вида гемангиом дает хороший лечебный и косметический эффект. Осложнения в виде некрозов кожи, изъязвлений и образования заметных рубцов бывают редко и при неправильном применении методики склерозирования.
Таким образом, лечение гемангиом представляет собой достаточно сложную задачу. Наиболее радикальным методом является хирургический или комбинированный, включающий оперативное вмешательство и эндоваскулярную окклюзию. Консервативные методы лечения показаны при поверхностных гемангиомах соответствующего строения и локализации и тогда, когда хирургическое лечение не показано или невыполнимо, например при гемангиоме языка. Лечение гемангиом необходимо начинать по возможности раньше, как только установлен точный диагноз.
Избранные лекции по ангиологии. Е.П. Кохан, И.К. Заварина
Возрастающий интерес к использованию лазеров в дерматокосметологии вполне оправдан. Они незаменимы при разрешении целого ряда проблем из области эстетической медицины и хирургической косметологии. В настоящее время существует великое множество лазеров дл
Возрастающий интерес к использованию лазеров в дерматокосметологии вполне оправдан. Они незаменимы при разрешении целого ряда проблем из области эстетической медицины и хирургической косметологии. В настоящее время существует великое множество лазеров для лечения различных по своему характеру заболеваний и дефектов кожи. Эти аппараты отличаются выходными характеристиками, механизмами взаимодействия их излучения с тканями и в большинстве своем предназначены для решения весьма узких и конкретных задач.
В настоящее время патология сосудов кожи является одной из основных причин обращения пациента к дерматокосметологу. Этой патологией страдает около 30 % населения, причем у 3 % из них эти сосудистые изменения имеются с рождения, поэтому очень важно выбрать оптимальный способ лечения подобных образований.
В 1981 г. Anderson и Parrish предложили концепцию селективного фототермолиза — о возможности избирательного воздействия лазерного света на хромофоры кожи. За прошедшие годы эта концепция многократно подтвердилась, и в настоящее время она служит теоретическим обоснованием лечения сосудистых и пигментных дефектов кожи.
Результат воздействия света на биологическую ткань определяют три фактора: длина волны света, длительность воздействия и плотность поглощенной энергии.
Длина волны. Главными хромофорами кожи являются меланин — пигмент эпидермиса — и гемоглобин — красный пигмент крови. Коллаген не влияет на выбор лазера для лечения сосудистых дефектов кожи, так как поглощает волны различной длины примерно одинаково. Меланин и оксигемоглобин представляют собой важнейшие компоненты при выборе волновой характеристики излучения. Каковы оптимальные длины волн для воздействия на эти хромофоры?
Из рисунка 1, на котором представлены адсорбционные спектры хромофоров кожи, видно, что хромофоры кожи — меланин и оксигемоглобин — поглощают волны различной длины видимого спектра с различной интенсивностью. Меланин поглощает целый диапазон длин волн, однако в сине-зеленом спектре поглощение более интенсивное (график построен в логарифмическом масштабе). Гемоглобин имеет кривую поглощения с локальным максимумом около 578 нм. Именно эта длина волны оказалась оптимальной для селективного воздействия на гемоглобин, так как поглощение меланина здесь меньше, а глубина проникновения света в ткань больше, чем в сине-зеленом спектре. Далее в красном спектре гемоглобин в меньшей степени поглощает свет, поэтому волны красной и инфракрасной длины менее эффективны для лечения сосудистых заболеваний кожи. Таким образом, для селективной коагуляции сосудистых дефектов кожи предпочтительно выбрать желтые длины волн вблизи максимума поглощения гемоглобина.
Длительность воздействия. Воздействие должно быть весьма непродолжительным, чтобы энергия, сообщенная световым импульсом кровеносному сосуду, пошла на его нагрев, не успев передаться окружающим тканям. А чтобы поднять температуру сосуда на несколько десятков градусов, источник света должен обеспечивать высокую плотность энергии.
Сосудистые патологии кожи вполне успешно устраняются лазерами уже более трех десятков лет. Наиболее эффективными, как с точки зрения теории селективного фототермолиза, так и на практике, оказались импульсные лазеры желтого света — лазер на красителях с ламповой накачкой (Flashlamp Pulsed Dye Laser — FPDL) и лазер на парах меди (Copper Vapor Laser — CVL). Иногда для лечения сосудистых патологий кожи применяется неодимовый лазер на гранате (Nd:YAG), с нелинейным кристаллом титанил фосфата калия (КТР) лазер, для удаления сосудов ног — Nd:YAG, александритовый и диодные лазеры с разными длинами волн. В последнее время нашли применение в этой области импульсные источники света. Все эти аппараты отличаются выходными характеристиками, а также особенностями воздействия на живую ткань.
Импульсные лазеры, излучающие желтый свет. Использование именно этих лазеров с точки зрения теории селективного фототермолиза является оптимальным для лечения сосудистых патологий кожи [3].
В лазере на красителях с ламповой накачкой (например, модели ScleroPlus и Vbeam фирмы Candela) с длиной волны 585 нм используется мощная импульсная дуговая лампа (лампа-вспышка), возбуждающая жидкий краситель, протекающий через стеклянную кювету, размещенную в резонаторе. Лазер на красителе нуждается в водяном охлаждении. Кроме того, краситель является органическим, токсичным веществом, а растворитель огнеопасен, что повышает требования безопасности при эксплуатации прибора. Требуется регулярная замена красителя, и, следовательно, эксплуатация лазера обходится довольно дорого.
Авторы большинства статей, опубликованных в международных журналах, признают, что этот тип лазера является одним из наиболее эффективных и безопасных для лечения самого широкого спектра сосудистой и другой патологии кожи.
Лазер на парах бромида меди (модели Yellow Star, Pro Yellow, Dual Yellow) также генерирует две длины волны — 511 и 578 нм, как и лазер на парах меди, так как активную среду составляют атомы меди. Но для получения атомов меди используется диссоциация паров бромида меди в электрическом разряде. Это позволяет снизить рабочую температуру разрядного канала до 500°. Однако сложные плазмохимические процессы в активной среде таких лазеров заметно снижают срок службы лазерной трубки по сравнению с лазерами на парах чистой меди.
Другие лазерные системы и источники света. В лазере KTP (модель VersaPulse V), с длиной волны 532 нм, используется удвоение частоты Nd:YAG лазера. Для удаления сосудистых дефектов кожи применяются только системы с импульсом 2–50 мс. KTP-лазер содержит сложную оптическую часть и требует серьезного технического обслуживания как лазера накачки, так и кристалла, служащего для удвоения частоты. Кроме того, как видно на рисунке 1, длина волны 532 нм не является оптимальной для селективной коагуляции сосудов. Желтый свет с длиной волны 577–578 нм более предпочтителен и безопасен для лечения сосудистых заболеваний, чем зеленое излучение 532 нм. Это происходит из-за того, что коэффициент поглощения гемоглобином и оксигемоглобином и глубина проникновения в ткань желтого излучения существенно выше, чем зеленого, несмотря на меньшую длину волны последнего. При переходе от зеленого спектра излучения к желтому коэффициент поглощения меланином излучения снижается. Таким образом, эффект от лечения менее выражен, а риск возникновения рубцов выше при длине волны 532 нм (зеленое излучение), что обусловлено низким уровнем коэффициента поглощения гемоглобином и оксигемоглобином и высоким уровнем коэффициента поглощения излучения меланином при данной длине волны (532 нм) по сравнению с аналогичными показателями при длине волны 578 нм.
Nd:YAG, александритовый и диодные лазеры излучают волны разной длины (1064, 755 и 810 нм соответственно) и находят применение при удалении более глубоко залегающих патологических сосудов — здесь используется свойство излучения этих лазеров более глубоко проникать в биологическую ткань. Но излучение этих лазеров не может селективно воздействовать на кровеносные сосуды, так как в диапазоне 700–1100 нм коэффициент поглощения гемоглобина в среднем в 100 раз меньше, чем на желтой длине волны (рис. 1), поэтому можно ожидать появления различных побочных эффектов, включая шрамы. Эти лазеры нежелательно применять для удаления сосудов на лице.
В импульсных источниках света IPL, или импульсных лампах (например, Photoderm, Quantum SR), используется импульсная лампа большой мощности, из спектра которой узкополосным фильтром выделяется нужная спектральная область, обычно 515–1200 нм.
На сегодняшний день это наиболее широко рекламируемые аппараты на рынке дерматологического и косметологического оборудования. Однако их использование вызывает споры среди специалистов. Недостатки этих аппаратов, причем в большинстве случаев непреодолимые, часто преподносятся как достоинства. Реклама утверждает, что прибор — импульсная лампа излучает и воздействует на организм волнами различной длины. Это действительно так, однако при этом умалчивается о том, что, в отличие от лазеров, все эти волны излучаются одновременно, и сделать с этим ничего нельзя. Поставляемые в комплекте фильтры способны убрать только часть излучаемого спектра, все остальные длины волн в диапазоне, например, 550–1100 нм (в зависимости от используемого фильтра) излучаются одновременно (рис. 1). Воздействие на ткани оказывается неселективным, волны в зависимости от длины поглощаются различными хромофорами. Кроме того, глубина проникновения этих длин волн варьирует от долей миллиметра до сантиметров, что представляет серьезную опасность при лечении кожи лица, особенно в периорбитальной области. Даже при наличии защитных очков существует опасность повреждения глаз пациента глубоко проникающими волнами при работе в периорбитальной области.
Если при сосудистой патологии для достижения лечебного эффекта лазера на красителе (FPDL) или лазера на парах меди плотность энергии устанавливается в диапазоне 6–8 Дж/см 2 , то рекомендуемая плотность энергии импульсной лампы составляет около 50 Дж/см 2 , т. е. почти в 10 раз выше(!), большая часть этой энергии идет на неконтролируемое нагревание тканей пациента.
Если бы мы смогли вырезать фильтрами узкую полосу спектра излучения вблизи максимума поглощения гемоглобина, что было бы наилучшим решением проблемы с точки зрения теории селективного фототермолиза, то на диапазон от 575 до 585 нм пришелся бы 1 Дж/см 2 (из 50 Дж/см 2 ), т. е. только эта энергия приходится на желтый диапазон спектра, который является наилучшим для селективной коагуляции сосудов. Остальные длины волн, присутствующие в излучении импульсной лампы, производят неконтролируемый и непредсказуемый нагрев тканей пациента. Этим объясняются высокий риск рубцевания и развития гипопигментаций после воздействия импульсной лампы, высокий уровень резистентности при лечении сосудистых патологий, необходимость большого количества сеансов (до 20) лечения.
Второй серьезный недостаток IPL состоит в невозможности сфокусировать излучение определенной мощности в достаточно маленькое пятно — типичный размер светового пятна IPL — 8 мм х 35 мм. Это ограничение IPL следует из некогерентной природы излучения импульсной лампы, фокусировка излучения в маленькое пятно возможна только для лазеров; для сравнения: размер светового пятна импульсного лазера на красителе может быть 2–3 мм, а лазера на парах меди — 0,6–1 мм в диаметре. Поэтому импульсная лампа не подходит для лечения мелких сосудистых дефектов кожи в области носа, носогубного треугольника, в уголках глаз и т. д. Кроме того, болевой эффект при воздействии импульсной лампы сильнее, чем после лазера, а побочные эффекты в виде отека и эритемы более выражены и держатся дольше, несмотря на принимаемые меры.
Таким образом, область применения импульсных ламп в лечении сосудистых патологий кожи ограничена неселективностью их воздействия и высоким риском развития побочных эффектов, включая образование шрамов.
Основные характеристики аппаратов и названия фирм производителей перечисленных лазерных и широкополосных источников света представлены в таблице.
В Лазерном центре кафедры дерматовенерологии ГМА им. И. И. Мечникова (Санкт-Петербург) за последние 10 лет накоплен опыт терапии самых разнообразных заболеваний и дефектов кожи посредством различных лазерных аппаратов, позволяющий проводить сравнительную оценку эффективности применения каждого из них для конкретной нозологии. За последние 5 лет лечение проводилось у 3000 пациентов с различной патологией кожи сосудистого генеза.
Сосудистая дисплазия — это нарушение организации кровеносного сосуда, чаще всего выражающееся в виде недоразвития, дегенерации или даже отсутствия одного или нескольких морфологических составляющих сосудистой стенки, вследствие прямого или опосредованного воздействия на нее факторов внешней или внутренней среды; данное нарушение проявляется расстройствами функции и макроскопическими изменениями строения сосудистой стенки, чаще всего в виде дилатации последней.
Среди опухолевых сосудистых образований наиболее часто встречались капиллярные (22,0%) и смешанные капиллярно-кавернозные гемангиомы (20,0%). Характерной особенностью всех вышеперечисленных новообразований является их практически абсолютная доброкачественность. То же самое можно сказать и в отношении пиогенной гранулемы, являвшейся причиной 12,5% обращений к врачу больных с новообразованиями кожи сосудистого происхождения. Из опухолей, расцениваемых как условно доброкачественные, наиболее часто встречались кавернозные гемангиомы (10,0%) и ангиокератомы (3,0%). Все перечисленные образования кожи требуют своевременного лечения с косметической целью. Случаи же диагностики настоящих злокачественных сосудистых опухолей, таких, как ангиоэндотелиома и ангиосаркома, были лишь единичными.
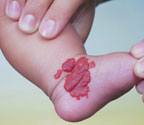
Особая тактика лечения существует при звездчатых гемангиомах. Мощность на выходе световолокна — 0,5–0,7 Вт, время экспозиции — 0,2 с.
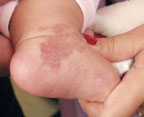 |
| Рисунок 2. Капиллярная гемангиома ноги младенца в возрасте 1 года до лечения (а) и через 1 мес после лечения (б) |
При лечении кавернозных гемангиом режим работы выбирается следующим образом: мощность — 0,7–0,8 Вт, время экспозиции — 0,3 с. Вся поверхность обрабатывается однократными или двойными импульсами.
Результаты фотокоагуляции сосудов проявляются непосредственно во время сеанса. Поверхность кавернозной гемангиомы белеет.
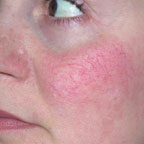
Для лечения телеангиэктазии в области лица мощность выбирается 0,5–0,6 Вт, время экспозиции — 0,1–0,2 с (рис. 3, а, б).
Для лечения телеангиэктазии на ногах устанавливается мощность 0,6–0,8 Вт, время экспозиции — 0,2–0,3 с. Коагуляция выполняется путем точечного воздействия на сосуды, расстояние между точками воздействия — 0,5–
1 мм. Во время обработки лазерный луч должен быть сфокусирован точно в сосуд, а не параллельно ему. Для удобства работы можно использовать увеличение.
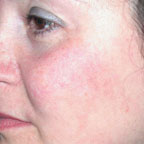 |
| Рисунок 3. Телеангиэктазии в области щек у пациентки в возрасте 21 г. до лечения (а) и через 2 нед после лечения (б) |
Процедура умеренно болезненная, большинство пациентов переносят ее без анестезии. Особенно впечатляющий медицинский и косметологический эффект дает комбинация лазерного лечения и склеротерапии: для сосудов малого (0,1–0,4 мм) и среднего (0,4–1 мм) диаметров проводится селективная лазерная коагуляция, непосредственно после этого для вен более 1 мм в диаметре выполняется склеротерапия. Склеротерапия осуществляется по Fegan или Sigg с последующей компрессией эластичными бинтами. Препараты: фибро-вейн 0,2% и этоксислерол 0,5 %. После склеротерапии выполняется бинтование.
Преимуществами лазерного метода лечения является то, что риск образования рубцов и травмирования окружающих тканей минимальный, период заживления значительно сокращается. Метод можно использовать во всех возрастных группах, а также у пациентов, имеющих сопутствующую соматическую патологию. Процедура занимает мало времени, бескровна, не требует анестезии.
С. В. Ключарева, кандидат медицинских наук
И. В. Пономарев, кандидат физико-математических наук
ГМА им. И. И. Мечникова, Физический институт им. П. Н. Лебедева, Санкт-Петербург, Москва
Действующее вещество:
Содержание
- 3D-изображения
- Состав и форма выпуска
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания препарата Фибро-Вейн
- Противопоказания
- Применение при беременности и кормлении грудью
- Побочные действия
- Способ применения и дозы
- Меры предосторожности
- Особые указания
- Условия хранения препарата Фибро-Вейн
- Срок годности препарата Фибро-Вейн
- Цены в аптеках
Фармакологическая группа
- Склерозирующие средства
Нозологическая классификация (МКБ-10)
- I83 Варикозное расширение вен нижних конечностей
3D-изображения
Состав и форма выпуска
1 мл водного раствора для инъекций содержит натрия тетрадецилсульфата:
2 мг во флаконах по 5 мл, в коробке 10 флаконов;
5 или 10 мг в ампулах по 2 мл; в коробке 5 ампул;
30 мг в ампулах по 2 мл или во флаконах по 5 мл; в коробке 5 ампул или 10 флаконов, соответственно.
Фармакологическое действие
При контакте с эндотелием вызывает быструю коагуляцию его белков.
Фармакодинамика
Коагулируя белки и раздражая гладкомышечные элементы стенки вены, значительно сокращает диаметр сосуда. Затем его просвет полностью закрывается и начинается соединительнотканная трансформация (фиброз). Обладает противосвертывающей активностью, предотвращает образование тромбов в месте инъекции.
Фармакокинетика
Как гипербарический раствор (имеет более высокую плотность, чем кровь) оказывает строго местное действие и не абсорбируется в системный кровоток. Входящие в состав фосфатный и гидрокарбонатный буфер обеспечивают нормальный уровень pH крови (даже при введении максимальных доз).
Показания препарата Фибро-Вейн ®
Различные формы варикозной болезни нижних конечностей, включая внутрикожный варикоз и телеангиэктазии.
Противопоказания
Повышенная чувствительность к компонентам препарата, острый тромбофлебит, острый тромбоз, артериальная недостаточность нижних конечностей, геморрагические диатезы, местная и общая инфекция.
Применение при беременности и кормлении грудью
Побочные действия
Местные реакции: возможна гиперемия кожи, незначительная болезненность или чувство жжения в месте введения.
Аллергические реакции: возникают редко.
Способ применения и дозы
В/в, в просвет изолированного сегмента пустой поверхностной вены с немедленным продолжительным ее сжатием (наложением компрессионного бандажа). Дозировку определяют в зависимости от размера вены, подвергаемой склерозированию; обычная доза — 1 мл (не более) в одно место. Для Фибро-Вейна 3% — максимальная однократная доза 4 мл, для 0,2; 0,5 и 1% растворов — до 10 мл. При необходимости дополнительные инъекции выполняют после 2-х недельного перерыва.
Меры предосторожности
Нельзя вводить п/к (вероятность развития воспалительных инфильтратов и некрозов), вблизи артерий и нервов.
Особые указания
Фибро-Вейн не взаимодействует с препаратами, используемыми для анестезии, не угнетает дыхания и сердечной деятельности, поэтому допускается его использование непосредственно во время хирургического вмешательства. Поскольку в составе нет этанола (как растворитель используется бутиловый спирт), может применяться у пациентов, получающих тетурам (антабус).
Условия хранения препарата Фибро-Вейн ®
Хранить в недоступном для детей месте.
Срок годности препарата Фибро-Вейн ®
Не применять по истечении срока годности, указанного на упаковке.
Синонимы нозологических групп
| Рубрика МКБ-10 | Синонимы заболеваний по МКБ-10 |
|---|---|
| I83 Варикозное расширение вен нижних конечностей | Варикоз диссеминированного типа |
| Варикозная болезнь | |
| Варикозная болезнь нижних конечностей | |
| Варикозное заболевание вен нижних конечностей | |
| Варикозное расширение поверхностных вен | |
| Варикозные вены | |
| Варикозные заболевания вен | |
| Варикозный симптомокомплекс | |
| Варикозный синдром | |
| Венозная хромота | |
| Венозный варикоз | |
| Заболевание вен | |
| Заболевание вен нижних конечностей | |
| Ощущение тяжести и усталости в нижних конечностях | |
| Преварикозный синдром | |
| Предварикозный синдром | |
| Склерозирование варикозно расширенных вен | |
| Хроническая варикозная болезнь |
Цены в аптеках Москвы
Оставьте свой комментарий
- раствор для внутривенного введения от 860 до 2616 p.
Текущий индекс информационного спроса, ‰
Регистрационные удостоверения Фибро-Вейн ®
П N014787/01 ![]()
П N014787/01-2003 ![]()
Еще много интересного
Все права защищены.
Не разрешается коммерческое использование материалов.
Информация предназначена для медицинских специалистов.
Когда рекомендуют медикаментозное лечение?
Гемангиома — доброкачественная опухоль над кожей, состоящая из сетки сосудов. При обнаружении красных пятнышек, которые увеличиваются в размере или приносит боль и дискомфорт, рекомендуется обратиться к педиатру или терапевту. Врач проведет осмотр, дополнительно назначит УЗИ, томографию, биопсию, общий анализ крови. Может потребоваться консультация хирурга, дерматолога. После подтверждения диагноза выбирается метод удаления — один из таблицы.
Раньше медикаменты от гемангиомы не применялись или были показаны при болях. Но последние научные исследования доказали, что препаратами можно бороться с проблемой без операции. В особо тяжелых случаях лекарства нужно пить перед операциями, в качестве подготовки. Такой подход позволяет уменьшить сосудистую опухоль, снять боль, и удалить опухоль с минимальной травматизацией здоровых тканей.

Для лечения гемангиом назначают бета-блокаторы, гормональные и улучшающие метаболизм препараты. Вернуться к оглавлению
Для лечения гемангиомы используют 3 схемы:
- употребление бета-блокаторов;
- препараты, улучшающие метаболизм и регенерацию тканей;
- гормональная терапия.
- сужению просвета сосудов, после чего гемангиома бледнеет;
- замедлению развития сосудистой сетки в новообразовании;
- уменьшению размеров гемангиомы.
Но даже одна таблетка средства способна вызвать побочные действия:
- нарушение сердечного ритма;
- падение артериального давления и количественного состава сахара в крови;
- появление аллергии, сыпи;
- интоксикация организма;
- нарушение функций печени.

При лучевой терапии гемангиом дополнительно потребуется приём глюкокортикоидов. Вернуться к оглавлению
Аппликации
Если наблюдается каверзная и капиллярная гемангиома на лице назначается лучевая терапия. Суть аппликации ― только на саму опухоль наносятся радиовещества. Используют радиоактивное излучение кобальтом и цезием, а при капиллярной гемангиоме показаны аппликации с радиоактивными фосфором и стронцием. Такая терапия проводится в 1 сеанс. Обрабатывать опухоль нельзя тем, у кого анемия.
Для аппликаций используют глюкокортикоиды:

Противозачаточные при гемангиоме усиливают рост имеющегося новообразования или могут его спровоцировать. Вернуться к оглавлению
Можно ли принимать противозачаточные?
Эстрогены влияют на рост опухоли. При беременности, а особенно в третьем триместре, опухоль в связи с изменением гормонального фона начинает активно развиваться. Так как противозачаточные препараты вызывают гормональную перестройку в организме, считается, что они способны отрицательно влиять на процесс роста гемангиомы. Прием любых лекарств при наличии сосудистой опухоли должен быть согласован с лечащим врачом.
Читайте также:


