Комбинированное лечение рака яичников
Онкология при ранней диагностике опухоли излечима. Комбинированное лечение рака яичников позволяет надеяться на избавление от опасного заболевания: важно максимально рано выявить новообразование и выбрать оптимальную тактику терапии.
Удаление опухоли является основой успешного излечения рака яичника
Лечение рака яичников – особенности выбора терапии
Поставив предварительный диагноз, врач направит на дополнительное обследование, целью которого является определение основных факторов, влияющих на выбор лечебной тактики. Необходимо обратить внимание на следующие критерии:
- возраст пациентки;
- стадия онкологического процесса;
- предположительный вид опухоли;
- наличие сопутствующей патологии в сердце, сосудах, легких, печени или эндокринной системе.
Важно точно выяснить первичность онкопроцесса – лечение рака яичников метастатического происхождения (вторичная опухоль) проводится с обязательным учетом очага, из которого в женские половые органы попали раковые клетки. До операции крайне сложно гарантировать доброкачественность процесса, поэтому врач всегда будет исходить из принципа онкологической настороженности (любая опухоль в придатках является злокачественной).
Основные виды лечения
Как и в случае с любыми другими разновидностями онкологии, главная задача – удалить новообразование. Лечение рака яичников обычно комбинированное – врач будет использовать следующие методы:
- Хирургическая операция;
- Лекарственная терапия;
- Курсовое лучевое воздействие.
Обязательное условие успешности лечебной тактики – строгое и последовательное выполнение рекомендаций врача-онколога. Бессмысленно использовать народные методики и растительные препараты (не надо терять время на нетрадиционную терапию – гарантированно вылечить травками и настойками рак не получится).
Чем раньше удалена опухоль, тем больше шансов для полного выздоровления. Лечение рака яичников основывается на радикальном хирургическом вмешательстве. Онколог предложит следующие виды операций:
- резекция яичника, пораженного опухолью;
- экстирпация матки с придатками;
- пангистерэктомия с удалением всех женских внутренних половых органов и большого сальника;
- удаление опухоли в 3 этапа (циторедукция при больших размерах новообразования) – уменьшение новообразования при первой операции, проведение курса радиотерапии, второе радикальное хирургическое вмешательство;
- паллиативные виды операции (при 4 стадии).
Органосохраняющие методы терапии используются только при начальных формах рака или при обнаружении пограничной кистомы. Любой радикальный вариант всегда повышает шансы для выздоровления, особенно если нет гистологического подтверждения на основе биопсии тканей. Паллиативные операции помогут продлить жизнь, но не решают главную задачу по выздоровлению.
Выбор метода хирургической операции – прерогатива доктора
В послеоперационном периоде врач-онколог назначит лекарственные препараты, которые помогут предотвратить метастазирование и прогрессирование опухоли. Обычно используется комбинация из следующих видов:
- химиотерапия;
- таргетная терапия.
Курсовая медикаментозная терапия преследует следующие цели:
- подавление оставшихся раковых клеток, которые могут стать причиной рецидива;
- стимуляция собственных защитных сил;
- продление жизни пациентки при запущенных формах онкопроцесса.
Необходимо аккуратно и точно выполнить назначения специалиста, не заменяя препараты и не снижая дозу лекарства.
Радиотерапия применяется на дооперационном этапе и в послеоперационном периоде. Лучевое лечение рака яичников преследует следующие цели:
- уменьшение размеров кистомы;
- предотвращение метастазирования;
- устранение болевого синдрома при 3-4 стадии.
Врач предложит индивидуально подобранную и эффективную комбинацию из хирургических, медикаментозных и лучевых методов – вовремя начатое лечение рака яичников позволяет надеяться на выздоровление.
Прогноз для жизни
Предположить положительный эффект при злокачественном новообразовании в области придатков сложно – лечение рака яичников по статистике зависит от стадии онкологии. 5-летняя выживаемость при 1 стадии составляет около 85-90%, при 2 – до 65%, при 3 – 39%, при 4 – 10-15%.
Ученые выяснили, что более интенсивная химиотерапия, усиленная известным препаратом, имеет множество преимуществ для пациенток с раком яичников. Результаты соответствующего исследования они представили на ежегодном конгрессе Европейского общества медицинской онкологии, который состоялся в Барселоне в минувшие выходные.
Исследователи продемонстрировали, что лечение опухолей яичника препаратом бевацизумаб может быть усилено олапарибом, являющимся ингибитором PARP, фермента, который участвует в репарации ДНК. Комбинированная терапия эффективна у всех пациентов, вне зависимости от статуса мутации BRCA. Ключевые выводы работы были представлены профессором Изабель Рэй-Кокард из онкологического центра лионского Университета Клода Бернара.
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную цену на лечение.
- Стандартное лечение рака яичников
- Структура клинического испытания
- Результаты
- Что дальше?
Стандартное лечение рака яичников
Рак яичников входит в пятерку наиболее распространенных видов онкологии среди женщин во всем мире и является одним из самых смертельно опасных: ежегодно этот тип гинекологических опухолей забирает тысячи жизней. Большинство пациенток погибают в течение года после обнаружения болезни во многом из-за того, что выявляют ее на поздней, более продвинутой стадии.
По словам исследователей, многие женщины хорошо отвечают на химиотерапию и лечение первой линии, но недуг часто возвращается в течение двух лет после установления ремиссии. В настоящее время традиционным лечением считается химиотерапия препаратами платины, которую проводят после хирургического удаления опухоли параллельно с курсом бевацизумаба. Кроме того, стандартной практикой является поддерживающая терапия одним только бевацизумабом.
Структура клинического испытания
В текущем исследовании команда ученых оценивала эффективность и безопасность совместного применения ингибитора PARP и бевацизумаба в качестве поддерживающей терапии у женщин с раком яичников в ремиссии с или без мутации в гене BRCA. Оно было международным, и участие в нем принимали 806 пациенток с опухолями яичника III и IV стадии, у которых наблюдался частичный или полный ответ на стандартное лечение с химиотерапией препаратом платины вместе с бевацизумабом.
Участниц разделили на две группы в формате 2:1. Большая группа принимала олапариб с бевацизумабом, меньшая – плацебо и бевацизумаб. Лечение олапарибом продолжалось до двух лет (в среднем 22,7 месяца для группы плацебо), тогда как бевацизумабом – в течение 15 месяцев. Исследователи изучали показатели выживаемости среди пациенток без прогрессирования болезни. Профессор Рэй-Кокард пояснила, что все участницы были включены в исследование в среднем через шесть недель после окончания первичной химиотерапии. По ее словам, это важно учитывать при сравнении полученных результатов с другими данными.
В России, Израиле, Германии рак яичников начинают лечить с операции. Удаляется матка с придатками, большой сальник, а также видимые проявления опухоли. Если выполнение операции маловероятно, т о начинают с химиотерапии. Это связано с тем, что рак яичников плохо отвечает на химию. Особенно низкую эффективность химиотерапии наблюдают при муцинозном и светлоклеточном раке яичников.

Операция при раке яичников
Хирургическое вмешательство – всегда всплеск опухолевого роста и метастазирования. Опухолевые клетки механически (скальпелем) разносятся по брюшине, попадают в кровоток. От избытка кислорода раковые клетки активизируются. Это чревато рецидивом и метастазами.
Если злокачественную опухоль до операции задавить химиотерапией, то это снизит активность клеток к росту и метастазированию, увеличит радикальность операции.
Простое введение химиопрепаратов малоэффективно. Поэтому в клинике “К-тест” химиотерапию усиливают, вводя препараты под нагревом методом общей электромагнитной гипертермии. В конечном счете предоперационная терапия по данной схеме улучшает результаты и выживаемость.
Общая гипертермия – перспективный метод лечения онкологии, который исследуется более полувека. Ученые разных стран пробуют возможные способы нагрева (в воде, в специальных камерах и т.д.). Разработками советских ученых в 80-х годах был предложен нагрев в электромагнитных полях. Нижегородские медики и физики объединились и была разработана и апробирована общая электромагнитная гипертермия. Ведущим онкологом этих исследований был профессор Карев. Сейчас он возглавляет клинику “К-тест”. Установки общей электромагнитной гипертермии в постперестроечный период не получили распространения в стране. Причина – высокая стоимость и сложность процедуры. В Нижнем Новгороде как начали лечить, так и лечат более 25 лет. Более простая и дешевая локальная гипертермия используется в ведущих онкоцентрах страны.
Если после 2-3 курсов проводимой химиотерапии в рамках стандартного лечения по ОМС нет заметной положительной динамики, улучшения самочувствия, уменьшения размеров опухоли и метастазов, то следует задуматься о необходимости усиления химиотерапии нагревом. Дальнейшее продолжение стандартной химиотерапии при отсутствии динамики, даже со сменой химиопрепаратов, приведет только к устойчивости рака яичников к лекарствам.
Лечение рака яичников после операции
После операции рекомендована курсовая общая электромагнитная гипертермия с химиотерапией. Для окончательного подавления опухоли и клеток, которые разнеслись по организму в ходе операции.
Введение химиопрепаратов на фоне разогрева тела до температуры гибели опухолевых клеток (42,5 °С и выше) решает проблему устойчивости опухоли к препаратам платины. Также до минимума снижает риск рецидивов.
Число курсов и выбор химиопрепаратов зависит от гистологической классификации опухоли и степени рака. С целью улучшения результата лечения может назначаться таргетная терапия (бевацизумаб).
Рецидив рака яичников можно остановить
Когда к нам обращались пациентки с прогрессированием опухоли яичников после химиотерапии первой линии (платинорефрактерный рак), введение этих же препаратов в условиях общей гипертермии давало ощутимый эффект: опухоль и метастазы уменьшалась уже после первого курса.
Такая картина наблюдалась даже у больных, которые до поступления к нам уже получали множество курсов химиотерапии второй и третьей линий (до 30 курсов) и их переводили на симптоматическую терапию.
Клинический пример:
Больная П., 44 года. Диагноз: Рак яичников T3cNoMo
В 2014 году больная в Екатеринбурге получала комбинированное лечение (экстирпация матки с придатками + адъювантная химиотерапия). Гистология и иммуногистохимия – аденокарцинома, метастазы в большой сальник. В январе 2019 года выявлен асцит. На ПЭТ КТ от 17.01.19 – рецидив опухоли в малом тазу. Проведена химиотерапия – 4 курса. На ПЭТ/КТ от 5.07.2019 выявлена отрицательная динамика – появились уплотнения и инфильтрация (канцероматоз) брюшины (SUV max 7.26), жидкость в малом тазу и брюшной полости. В надключичной области лимфоузлы 9х6 мм (SUV max 1,83). Субплеврально – очаг (SUV max 1,90).
Рак яичников 4 стадии
Применяемая схема позволяет добиться пятилетней выживаемости у 15-20 % пациенток с запущенным и рецидивирующим раком.
При платинорефрактерном раке яичников или рецидиве заболевания переход на химиотерапию в условиях нагрева предпочтительнее, чем химиотерапия второй или третьей линии, которая зачастую не увеличивает продолжительность жизни и ухудшает ее качество в связи с возникновением побочных эффектов.
Хорошие результаты при лечении внутрибрюшинных и отдаленных метастазов рака яичника в легкие и печень.
Под действием критической температуры происходит их резорбция. Становится возможно выполнение метастазэктомии (удаление крупных метастазов).
Лечебное действие электромагнитной гипертермии наряду с противоопухолевым эффектом снимает боли, стимулирует иммунитет, улучшает качество жизни больных.
Клинические примеры:
Сравнение схем лечения по стандарту ОМС и в клинике “К-тест”:
Значительно больше проблем возникает при лечении больных с распространёнными стадиями заболевания. В настоящее время нет сомнений в необходимости при первичном лечении этих больных проведения комбинированных или комплексных мероприятий.
неэффективность фармакологических препаратов снимается удалением основной массы опухоли со слабым кровотоком;
эффективность химиопрепаратов связана с высокой митотической активностью малых опухолей;
наименьшие остаточные опухоли требуют меньшего количества курсов химиотерапии, в то время как при больших массивах повышается вероятность появления резистентных форм;
удаление основных опухолевых масс приводит к относительной нормализации иммунной системы больной;
по возможности, удаляются фенотипически резистентные опухолевые клетки.
Для солидных новообразований характерен сравнительно бедный кровоток, что снижает концентрацию фармакологического препарата в опухолевых тканях и, соответственно, эффективность проводимого лечения. Особенно это выражается в центральных областях опухоли, где часто возникают обширные некрозы, связанные с нарушением трофики тканей. К некротическим участкам примыкают кровоснабжаемые из мелких сосудов многочисленные, особенно жизнеспособные, участки злокачественных тканей. Такое представление подтверждается, правда, косвенно, низким содержанием свободной глюкозы и высоким уровнем молочной кислоты во внутритканевой жидкости солидных опухолей.
Всё это приводит к временному снижению митотической активности злокачественных клеток и в результате к снижению эффективности проводимой химиотерапии, тропной к ДНК клетки только в определённую фазу. Для максимального эффекта большинства фармакологических агентов необходима фракция клеток с быстрым ростом, поэтому при удалении основной массы малочувствительных к химиотерапии клеток остаются более чувствительные небольшие очаги (диссеминаты), обладающие высокой митотической активностью. Кроме того, удаление большой массы опухоли приводит к восстановлению относительной иммунокомпетентности организмаопухоленосителя, в первую очередь вследствие снижения иммуносупрессии, индуцированной опухолью. Как известно, целью хирургического лечения считают удаление максимально возможного объёма первичной опухоли и её метастазов. Если полное удаление опухоли невозможно, удаляют большую её часть. Показано, что выживаемость больных в значительной степени коррелирует с размером оставшихся после операции метастазов. Так, при размерах остаточной опухоли, не превышающих 5 мм, средняя продолжительность жизни соответствует 40 мес, при размерах до 1,5 см -- 18 мес, а в группе больных с метастазами более 1,5 см -- 6 мес.
В связи с этим в настоящее время рекомендуют следующие стандартные положения для оперативных вмешательств.
Первичная циторедуктивная операция предусматривает удаление максимально возможного объёма опухоли и метастазов перед началом лекарственной терапии. Первичную циторедуктивную операцию считают стандартом при распространённом раке яичников, особенно при III стадии заболевания. Целью циторедуктивной операции должно быть полное или максимальное удаление опухоли. Роль циторедуктивной операции при IV стадии по FIGO противоречива, однако больным с наличием только плеврального выпота, метастазами в надключичные лимфатические узлы или единичными кожными метастазами можно назначать лечение, как при III стадии заболевания. Не показан данный объём операции больным с метастазами в печень и лёгкие. С другой стороны, неоадъювантную химиотерапию считают приемлемой альтернативой циторедуктивной операции при IV стадии заболевания или при технических трудностях хирургического лечения.
Промежуточную циторедуктивную операцию выполняют после короткого курса индукционной химиотерапии (обычно 2- 3 курса). Выполнение операции на данном этапе выступает приемлемым подходом в терапии больных, у которых первая операция была либо пробной, либо малоуспешной.
Вторичная циторедуктивная операция. Большинство вторичных циторедуктивных операций выполняют при локализованных рецидивах, возникших после комбинированного лечения. Предварительный анализ показал, что кандидаты для выполнения подобных операций могут быть определены с учётом факторов прогноза. Чаще всего это опухоли, которые рецидивируют спустя год и более после завершения первичного лечения и адекватно отвечают на проводимую ранее химиотерапию.
Паллиативные операции в основном производят для облегчения состояния больной, например при кишечной непроходимости на фоне спаечного процесса или прогрессировании заболевания.
К настоящему времени методы оперативного лечения при раке яичников практически не изменились, за небольшим исключением, в то время как лекарственное лечение стало более эффективным и продолжает совершенствоваться.
Широко разрабатываются новые перспективные методы консервативной терапии на стыке генетики, иммунологии, химиотерапии и лучевого лечения. Следует признать, что, вероятно, в ближайшем будущем лечение злокачественных опухолей яичников будет прерогативой консервативной медицины.


Несмотря на технические сложности и большой объём хирургии, операция при раке яичника необходима, но не всегда возможна на первом этапе.
Какие варианты рака яичников возникают
Рак яичников неоднороден — это восемь клеточных вариантов злокачественного процесса, развивающиеся из разных элементов слизистой оболочки яичников. К раку не относятся тоже злокачественные, но возникающие из другой по структуре ткани герминогенные и гранулезоклеточные опухоли.
Каждый морфологический вариант имеет собственные перспективы на дальнейшее развитие и индивидуальную чувствительность к лечебным мероприятиям:
Когда химиотерапия заменяет операцию
При всех клеточных вариантах рака яичников без операции излечение не гарантируется. Операция выполняется даже при обширном поражении брюшной полости и при асците. Всегда желательно полное удаление всех видимых раковых очагов, но, когда это технически невыполнимо, ограничиваются частью опухолевых узлов, а оставшиеся уничтожают химиотерапией.
Лапароскопические операции при раке яичников не признаются стандартом лечения, поскольку не позволяют обнаружить и удалить все рассыпанные по брюшной полости новообразования, лапароскопия используется исключительно для диагностики.
При невозможности хирургического вмешательства на первом этапе проводится химиотерапия. Стандарт лекарственного лечения — сочетание паклитаксела или доцетаксела с платиновым производным (цисплатин, карбоплатин).
После 2–3 курсов врачебный кворум повторно обсуждает вопрос возможности оперативного удаления остаточной опухоли. Курсы химиотерапии продолжаются и после операции — суммарным числом не больше 6. При полном отказе от хирургии не рекомендуется больше 8 циклов ХТ, так как опухоль уже выработала механизм устойчивости к применяемым цитостатикам и не реагирует на лечение.

Какие новые методы используются при раке яичников
Новые, помимо обновлённого стандарта химиотерапии, методы и способы лечения рака яичников отозвались существенным увеличением продолжительности жизни и процента излечившихся женщин.
- Первый из новых методов — цитостатическое лечение на 3 стадии рака яичников можно из внутривенного переформатировать на внутрибрюшинное введение, если во время операции установить лапаропорт. Введение препарата в брюшную полость легче переносится и можно вводить лекарство в большей дозе.
- Второе обновление касается лечения пациенток с 3 и 4 стадиями рака яичников — это добавление к стандартной химиотерапии моноклонального антитела бевацизумаба, повышающего результативность терапии. В качестве поддержки достигнутого результата введения могут продолжаться и после завершения всех циклов химиотерапии, в общей сложности чуть больше года. Препарат не рекомендуется использовать до операции.
- Третье обновление — использование блокатора фермента олапариба для сохранения позитивных результатов, достигнутых при лечении рецидивной опухоли цитостатиками.
- Четвёртая новация — признание эффективности гормональной терапии при раке яичников и назначение антигормонов профилактически и при генерализации. Так при наличии рецепторов половых гормонов в клетках серозной карциномы низкой злокачественности могут назначаться гормональные препараты.
- Пятая — существенно улучшает результат операции совмещение внутриполостной химиотерапии с локальной гипертермией (HIPEC). Это действительно инновационная методика пока доступна единичным клиникам и нашей тоже.
- Шестое — применение при рецидиве нечувствительного к платине рака принципа метрономной терапии, когда стабилизация ракового процесса достигается регулярным приёмом небольших доз цитостатиков в таблетках.
Химиотерапия в лечении рецидива рака яичников
Варианты химиотерапии при возврате болезни:
- Если после завершения первичной химиотерапии прошло меньше полугода, то схему лекарств полностью меняют, предлагая для лечения только один цитостатик из восьми возможных, а некоторые препараты можно комбинировать с бевацизумабом;
- Если рецидив случился более чем через полгода после завершения первичного лечения, то говорят о чувствительности к платиновым производным, что позволяет и дальше включать их в комбинацию вместе с ранее не применяемыми препаратами и бевацизумабом;
- Два свободных от болезни года позволяют вернуться к первичной схеме ХТ.
Проводят от 4 до 6 курсов, при резистентности, которая проявляется продолжающимся увеличением опухоли, предлагается метрономная терапия или антигормоны, но только при наличии рецепторов. Если достигается позитивный результат, для его закрепления возможен приём олапариба, блокирующего восстанавливающий ДНК фермент.
Значительно больше проблем возникает при лечении больных с распространёнными стадиями заболевания. В настоящее время нет сомнений в необходимости при первичном лечении этих больных проведения комбинированных или комплексных мероприятий.
неэффективность фармакологических препаратов снимается удалением основной массы опухоли со слабым кровотоком;
эффективность химиопрепаратов связана с высокой митотической активностью малых опухолей;
наименьшие остаточные опухоли требуют меньшего количества курсов химиотерапии, в то время как при больших массивах повышается вероятность появления резистентных форм;
удаление основных опухолевых масс приводит к относительной нормализации иммунной системы больной;
по возможности, удаляются фенотипически резистентные опухолевые клетки.
Для солидных новообразований характерен сравнительно бедный кровоток, что снижает концентрацию фармакологического препарата в опухолевых тканях и, соответственно, эффективность проводимого лечения. Особенно это выражается в центральных областях опухоли, где часто возникают обширные некрозы, связанные с нарушением трофики тканей. К некротическим участкам примыкают кровоснабжаемые из мелких сосудов многочисленные, особенно жизнеспособные, участки злокачественных тканей. Такое представление подтверждается, правда, косвенно, низким содержанием свободной глюкозы и высоким уровнем молочной кислоты во внутритканевой жидкости солидных опухолей.
Всё это приводит к временному снижению митотической активности злокачественных клеток и в результате к снижению эффективности проводимой химиотерапии, тропной к ДНК клетки только в определённую фазу. Для максимального эффекта большинства фармакологических агентов необходима фракция клеток с быстрым ростом, поэтому при удалении основной массы малочувствительных к химиотерапии клеток остаются более чувствительные небольшие очаги (диссеминаты), обладающие высокой митотической активностью. Кроме того, удаление большой массы опухоли приводит к восстановлению относительной иммунокомпетентности организмаопухоленосителя, в первую очередь вследствие снижения иммуносупрессии, индуцированной опухолью. Как известно, целью хирургического лечения считают удаление максимально возможного объёма первичной опухоли и её метастазов. Если полное удаление опухоли невозможно, удаляют большую её часть. Показано, что выживаемость больных в значительной степени коррелирует с размером оставшихся после операции метастазов. Так, при размерах остаточной опухоли, не превышающих 5 мм, средняя продолжительность жизни соответствует 40 мес, при размерах до 1,5 см — 18 мес, а в группе больных с метастазами более 1,5 см — 6 мес.
В связи с этим в настоящее время рекомендуют следующие стандартные положения для оперативных вмешательств.
Первичная циторедуктивная операция предусматривает удаление максимально возможного объёма опухоли и метастазов перед началом лекарственной терапии. Первичную циторедуктивную операцию считают стандартом при распространённом раке яичников, особенно при III стадии заболевания. Целью циторедуктивной операции должно быть полное или максимальное удаление опухоли. Роль циторедуктивной операции при IV стадии по FIGO противоречива, однако больным с наличием только плеврального выпота, метастазами в надключичные лимфатические узлы или единичными кожными метастазами можно назначать лечение, как при III стадии заболевания. Не показан данный объём операции больным с метастазами в печень и лёгкие. С другой стороны, неоадъювантную химиотерапию считают приемлемой альтернативой циторедуктивной операции при IV стадии заболевания или при технических трудностях хирургического лечения.
Промежуточную циторедуктивную операцию выполняют после короткого курса индукционной химиотерапии (обычно 2– 3 курса). Выполнение операции на данном этапе выступает приемлемым подходом в терапии больных, у которых первая операция была либо пробной, либо малоуспешной.
Вторичная циторедуктивная операция. Большинство вторичных циторедуктивных операций выполняют при локализованных рецидивах, возникших после комбинированного лечения. Предварительный анализ показал, что кандидаты для выполнения подобных операций могут быть определены с учётом факторов прогноза. Чаще всего это опухоли, которые рецидивируют спустя год и более после завершения первичного лечения и адекватно отвечают на проводимую ранее химиотерапию.
Паллиативные операции в основном производят для облегчения состояния больной, например при кишечной непроходимости на фоне спаечного процесса или прогрессировании заболевания.
К настоящему времени методы оперативного лечения при раке яичников практически не изменились, за небольшим исключением, в то время как лекарственное лечение стало более эффективным и продолжает совершенствоваться.
Широко разрабатываются новые перспективные методы консервативной терапии на стыке генетики, иммунологии, химиотерапии и лучевого лечения. Следует признать, что, вероятно, в ближайшем будущем лечение злокачественных опухолей яичников будет прерогативой консервативной медицины.
Моя миссия врача
Мой опыт лапароскопических оперативных вмешательств по поводу кист, опухолей и рака яичников составляет более 800 операций, который обобщен в многочисленных научных работах и монографиях. Регулярно по этой теме мной проводится мастер-классы для гинекологов и онкологов.
Выбор тактики лечения пациенток с раком яичников 3-4 стадии осуществляется тремя специалистами: врачом- хирургом, онкологом и химиотерапевтом, с обязательным участием морфолога высокого уровня.
Существует два основных подхода в лечении рака яичника 3-4 стадии.
Неоадъювантная химиотерапия с последующей интервальной циторедукцией (выполнение радикальной операции с удалением всех пораженных тканей и лимфоузлов) лапароскопическим способом. Этот метод я активно использую в своей практике в Швейцарской университетской клинике.
Этот метод подразумевает выполнение на первом этапе диагностической лапароскопии. Во время лапароскопии проводится ликвидация асцита (забор жидкости на цитологическое исследование), оценка состояния брюшной полости и малого таза, по возможности, если нет прорастания в окружающие органы и ткани, то удаление первичного очага (аднексэктомия). Затем обязательно выполняется биопсия яичника или образования с другой стороны, большого сальника, лимфоузлов, тазовой брюшины, биопсия метастазов из печени и диафрагмы. Далее вторым этапом по данным гистологического исследования выполняется 3 сеанса неоадъювантной химиотерапии.
После контрольного обследования брюшной полости и малого таза (ЯМРТ и МСК), через 1,5- 2 месяца после диагностической лапароскопии и 3-х курсов химиотерапии, выполняется лечебная лапароскопия, направленная на радикальное удалением первичного очага опухоли яичника ( если он не был удален при первичной лапароскопии). Обязательно проводится пангистерэктомия с экстирпацией большого сальника, аортокавальная и тазовая лимфаденэктомия, тазовая перитонеумэктомия и удаление обнаруживаемых метастазов. После окончательного гистологического исследования проводится последующая химиотерапия.
При использовании авторского подхода неоадъювантной химиотерапии, с последующей интервальной циторедукцией лапароскопическим способом, вся циторедукция выполняется малоинвазивным методом, через 3-4 прокола брюшной стенки.
Это позволяет:
- не иметь огромного количества хирургических осложнений связанных с лапаротомной операцией;
- начать химиотерапию через 10-14 дней после диагностической лапароскопии;
- получить немедленный эффект от терапии, в виде уменьшения первичной опухоли в несколько раз, отсутствия асцита, снижение отека параканкрозных тканей;
- в самых благоприятных условиях выполнить радикальную циторедукцию малоинвазивным лапароскопическим способом;
- начать последующую химиотерапию через 10-14 дней после повторной радикальной лапароскопии;
- сократить сроки госпитализации до 2 дней при диагностической лапароскопии и 2-3 дней при радикальной лапароскопии.
Использование неоадъювантной химиотерапии на первом этапе позволяет хирургу при повторной лапароскопии выполнить весь необходимый объем циторедукции в совершенно других условиях – при отсутствии отека тканей, воспалительных инфильтратов и больших размеров опухоли. Это дает возможность выполнить операцию уже не открытым, а лапаросокпическим способом, прецензионно выделять ткани, использовать современные лигирующие системы для гемостаза и лимфостаза. Операционное поле на протяжении всей операции остается сухим, кровопотеря минимальна, дренажи в брюшной полости оставляются крайне редко, лимфорея и лимфоцеле отсутствуют.
Первичная циторедукция ( радикальная операция открытым лапаротомным способом) с последующей химиотерапией. Это вид комбинированного лечения рака яичников, который используется большинством хирургов.
Этот метод подразумевает выполнение на первом этапе радикального оперативного вмешательства с удалением первичного очага (пангистерэктомия) и всех пораженных органов и тканей (большого сальника, лимфоузлов, перитонеумэктомия, удаление метастазов в брыжейке тонкой и толстой кишки, печени, диафрагме и т.д.). Далее вторым этапом по данным гистологического исследования назначается химиотерапия.
Недостатком этого подхода является очень высокая травматичность оперативного вмешательства. Операция в данной ситуации в 95% случаев может быть выполнена только открытым способом (разрез через весь живот от мечевидного отростка до лобка), сопровождается высокой кровопотерей (до 1-2 литров), длительностью (до 9-10 часов). Этот вид оперативного вмешательства сопровождается удалением большого количества органов и тканей. так как на этом этапе не возможно оценить их состояние - поражение вызвано онкологическим процессом или вторичным воспалительным отеком.
В послеоперационном периоде отмечается большое количество хирургических осложнений: несостоятельность кишечных швов, перитонит, эвентрация кишки в послеоперационную рану, нагноение раны, длительная лимфорея (вытекание лимфы по дренажам, с потерей белка и образованием лимфоцеле – больших скоплений лимфы в брюшной полости), образование вентральных грыж. Развитием анемии и гипопротеинемии. Все это приводит к длительному нахождению пациенток в реанимационном отделении и стационаре и сопровождается высокой послеоперационной летальностью.
Стоит обязательно отметить, что выполнение первого этапа подобным способом приводит к длительной задержке выполнения химиотерапии (до 2-3 месяцев), не менее важного, а скорее главного этапа в лечении рака яичника.
Сторонники первого подхода и предоперационной химиотерапии резонно отмечают, что для многих больных III-IV стадий рака яичника выполнение первичной оптимальной циторедукции даже открыто, невозможно технически и опасно операционными осложнениями. К сожалению, до сих пор не существует общепринятых критериев, предсказывающих возможность выполнения или невыполнения оптимальной циторедукции на первом этапе, поэтому проведение диагностической лапароскопии и предоперационной химиотерапии, которая повышает шанс ее выполнения на втором этапе, представляется логичным.
Одинаковые цифры безрецидивной и общей выживаемости, полученные при проведении рандомизированных исследований, сделали метод проведения предоперационной химиотерапии при раке яичников популярным в США и Европе, о чем свидетельствует увеличение частоты его использования.
По результатам двух рандомизированных исследований, сравнивающих выполнение первичной циторедуктивной операции с последующей химиотерапией и проведение 3 курсов предоперационной химиотерапии с последующим выполнением циторедукции и продолжением химиотерапии, были сделаны выводы о равнозначной эффективности этих двух лечебных тактик. При этом количество хирургических осложнений при лапароскопии уменьшается в 15 раз, а качество жизни во время лечения и после него вырастает в разы.
Учитывая вышесказанное, я придерживаюсь следующей тактики в лечении рака яичника 3-4 стадии – это неоадъювантная химиотерапия, с последующей интервальной циторедукцией лапароскопическим способом.
По желанию пациента, все курсы химиотерапии могут быть проведены в Швейцарской университетской клиники под контролем опытных онкологов и химиотерапевтов.
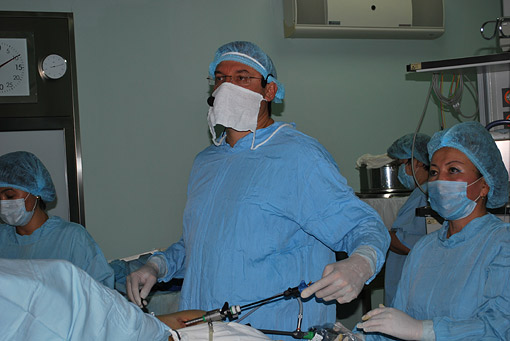
Лапароскопическое удаление кисты яичника (профессор К.В. Пучков, сентябрь 2011 года в г. Астана (Республика Казахстан).
- Пучков К.В., Фумич Л.М., Политова А.К., Козлачкова О.П., Рязанцев М.Е., Осипов В.В. Оперативное лечение опухолей и опухолевидных образований яичников с использованием лапароскопического доступа // 50 лет Рязанскому государственному медицинскому университету: научные итоги и перспективы.- Рязань, 2000.– Ч. 2.- С. 171-172.
- Пучков К.В., Фумич Л.М., Козлачкова О.П., Политова А.К., Осипов В.В. Оперативное лечение опухолей и опухолевидных образований яичников с использованием малоинвазивных технологий // Эндоскопия в диагностике, лечении и мониторинге женских болезней / под ред. В.И. Кулакова, Л.В. Адамян. – М., 2000. – С.132-134.
- Пучков К.В., Куликов Е.П., Фумич Л.М., Козлачкова О.П., Политова А.К., Осипов В.В. Современные подходы к хирургическому лечению овариальных образований // Эндоскопическая хирургия.– 2001. – Т.7, №3. – С. 69.
- . Пучков К.В., Фумич Л.М. Лапароскопический доступ в хирургическом лечении овариальных новообразований: адекватность и перспективы // Тихоокеанский мед. журн.– 2002. - №2 (спец. вып.). – С.39-41.

Пучков К.В., Политова А.К. Лапароскопические операции в гинекологии: монография.- М.: МЕДПРАКТИКА, 2005. - 212 с.

Пучков К.В., Баков В.С., Иванов В.В. Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии: Монография.- М.: ИД МЕДПРАКТИКА – М.- 2005.- 168 с.

Пучков К.В., Иванов В.В.. Технология дозированного лигирующего электротермического воздействия на этапах лапароскопических операций: монография.- М.: ИД МЕДПРАКТИКА, 2005.- 176 с.

«Когда вы пишете письмо, знайте: оно попадает мне на мою личную электронную почту. На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное - свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие.
Каждый день я по нескольку часов отвечаю на ваши письма.
Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы.
Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии. Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи.
Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами. В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.
Читайте также:



