Как лечат рецидив рака простаты после удаления простаты
Рак предстательной железы (РПЖ) диагностируют у 32 – 40% мужчин старше 50 лет. В половине случаев это локализованный рак, то есть опухоль не выходит за пределы простаты. Стандартом лечения в такой ситуации считается радикальная простатэктомия – одномоментное удаление новообразования. Не уступает по радикальности и лучевая терапия, которую часто рассматривают как альтернативу операции. Тем не менее, лечение не всегда эффективно. Иногда болезнь возвращается спустя несколько месяцев или лет после радикального лечения. Такое состояние называется рецидивом рака предстательной железы, который может быть локальным или местным, системным и биохимическим.
Вероятность рецидива после радикальной простатэктомии составляет от 10 до 28% в первые 5 лет после вмешательства. Это зависит от строения опухоли, соматического состояния пациента, размера новообразования. Например, если радикальную простатэктомию выполняли на стадии T3а (рак распространяется на клетчатку вокруг простаты), вероятность возрастает до 45%.

Развитие рецидива в течение 5 лет после лучевой терапии составляет 12 – 38%. При этом будут иметь значение не только особенности новообразования, но и доза облучения – чем она меньше, тем выше риски. Вид воздействия (брахитерапия или дистанционное) большой роли не играет.
Если же говорить о сроках в целом, 45% случаев регистрируются в течение 2 лет после радикального лечения, 77% – в пределах 5 лет, 96% – на протяжении 9 лет.
Биохимический рецидив
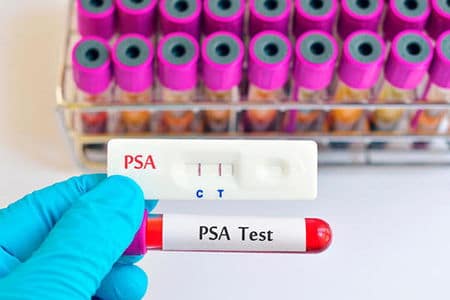
Протекает бессимптомно и определяется исключительно по результатам анализа на уровень простатспецифического антигена (ПСА или PSA). Это особый белок, который есть только в тканях предстательной железы. Соответственно, после ее удаления, уровень простатспецифического антигена должен резко снизиться до значений, не определяемых стандартными методами исследований. Если же, спустя некоторое время, уровень ПСА начинает вновь возрастать, это может означать лишь то, что в организме остались клетки опухоли, которые начали размножаться. Биохимический рецидив после радикальной простатэктомии диагностируют, когда уровень ПСА систематически увеличивается через три измерения подряд на 0,2 нг/мл и более, интервал между исследованиями больше или равен 2 неделям.
Подобная ситуация возможна и после радиотерапии. Конечно, при облучении часть тканей железы остается жизнеспособной и уровень ПСА не опускается до неопределяемых значений. Поэтому за исходную точку берут самый низкий уровень антигена.
Критерием биохимического рецидива считается повышение показателя PSA более чем на 2 нг/мл по сравнению с минимальным значением, отмечавшимся у больного.
Биохимический рецидив рака предстательной железы лечат облучением ложа простаты, иногда вместе с захватом области регионарных лимфоузлов.
Локальный рецидив
Локальный рецидив рака простаты после радикальной простатэктомии регистрируется в 15 – 35% случаев. Местным — считается появление очага опухоли в области расположения удаленной предстательной железы при отсутствии поражения лимфоузлов и отдаленных метастазов. Этот очаг должен быть визуализирован, то есть виден на УЗИ, компьютерной томограмме, при МРТ-обследовании или ПЭТ — КТ. Его злокачественность должна подтверждаться гистологически – то есть после взятия биопсии и исследования под микроскопом.
Клинических симптомов на ранней стадии обычно не бывает. Чаще всего во время очередного профилактического обследования у пациента обнаруживают вновь повысившийся уровень ПСА, после чего проводят углубленную диагностику и выявляют местный рост опухоли. Если пациент, вопреки рекомендациям, не обследуется профилактически после радикального лечения и рецидив на ранних стадиях не выявлен, на поздних этапах развития возвращаются некоторые симптомы запущенных стадий рака простаты: боли в промежности и над лобком, задержка мочи, запоры.

Лечение локального рецидива РПЖ зависит от того, какой метод был использован ранее.
Если первично возникший рак лечили с помощью лучевой терапии, при рецидиве выполняют радикальную простатэктомию (РПЭ). При этом вероятность послеоперационных осложнений выше, чем если бы хирургическое вмешательство было сделано при первичном раке: после облучения возрастает опасность повреждения прямой кишки, увеличивается кровопотеря во время вмешательства, высок риск возникновения недержания мочи, или, наоборот, контрактуры (патологического сокращения) шейки мочевого пузыря. 5-летняя безрецидивная выживаемость после операции 55 – 69%.
Если же первично была выполнена РПЭ, при лечении рецидива рака используют лучевую терапию. 5-летняя безрецидивная выживаемость при этом зависит от исходного уровня ПСА. Если он меньше 0,2 нг/мл, показатель 5-летней безрецидивной выживаемости достигает 77%, при 0,2 нг/мл опускается до 34%, а если уровень ПСА доходит до 1 нг/мл, прогноз расценивается как неблагоприятный.
Из экспериментальных методов, достоверной статистики эффективности которых пока нет, применяется криоабляция (замораживание) и воздействие сфокусированным ультразвуком высокой интенсивности (HIFU-терапия). Несмотря на то, что предварительные результаты исследований эффективности методик довольно обнадеживающие, в официальные гайдлайны эти манипуляции пока не включены.
Системный рецидив
Случается и так, что на момент радикального лечения остались недиагностированные микрометастазы, которые продолжили свое развитие после вмешательства. В этом случае трудно отличить системный рецидив (возобновление роста новообразования) от системной прогрессии опухоли (продолжения развития не удаленных очагов).
Отчасти, их можно различить по следующим критериям:
- повышение концентрации ПСА менее чем через год после операции;
- уровень ПСА удваивается за 4 – 6 месяцев;
- 8 – 10 баллов по шкале Глисона.
Системный рецидив клинически проявляется такими же симптомами, как и метастатический рак. Поскольку злокачественные новообразования предстательной железы метастазируют в кости, легкие, печень, возникают признаки поражения этих органов:
- боли в костях;
- патологические переломы;
- повышенный уровень кальция и щелочной фосфатазы крови;
- боли в позвоночнике;
- парезы, параличи (при сдавлении спинного мозга);
- боли в подреберье;
- увеличение печени;
- анемия.
Эти проявления сопровождаются общим недомоганием, повышением температуры до 37-38, потерей аппетита, резким снижением массы тела.
При системном рецидиве, равно как и при прогрессии рака предстательной железы применяют гормонотерапию, чаще всего – кастрацию.
Метастазы в кости подвергаются радиотерапии – облучение помогает уменьшить интенсивность болевого синдрома.
Оперативное удаление опухоли, облучение и химиотерапия не являются 100% гарантией исцеления рака предстательной железы. Благополучный исход определяют ранее выявление онкологии и выраженность злокачественного процесса. Через 5 лет после лечения больше чем у 1/3 пациентов обнаруживается рецидив рака простаты, через 10 лет РПЖ повторно диагностируют у > 50% мужчин. Под рецидивом понимают пальпаторно определяемую опухоль, метастазы и повышение показателей ПСА.
- Этиология и патогенез
- Симптомы и проявления
- Диагностика
- Как проводится лечение
- Прогноз
Этиология и патогенез
Возвращение болезни после операции происходит в результате неполного удаления раковых клеток. Последующие радио- и химиотерапевтические мероприятия по разным причинам оказываются неэффективными. Формируется новая опухоль либо обнаруживаются метастазы. Рецидив рака простаты чаще развивается у пациентов, начавших борьбу с онкологией поздно, на 3–4-й стадиях болезни. В этой ситуации онкологический процесс возобновляет метастатический узел.
Различают два вида рецидива:
- Местный (локальный) – поражает только предстательную железу. Обычно наступает через 2 года после операции. Характеризуется повышением уровня ПСА в 2 раза.
- Системный – в онкологический процесс вовлекаются другие органы. Биохимический рецидив развивается быстро – ПСА за год после РПЭ увеличивается более чем в 2 раза.
Новая волна злокачественного процесса возникает в результате некорректного либо запоздалого лечения. Возобновить рак может дессеминация организма мутировавшими клетками. Основные причины рецидива.
- неполное удаление опухоли в ходе операции;
- неэффективность лучевой и химиотерапии;
- позднее начало терапии (при 3–4 степени).
Полное излечение от рака простаты возможно при первых двух стадиях при условии своевременного лечения. Риск возвращения онкологии повышает прорастание опухоли в близлежащие органы.
Симптомы и проявления
Начало заболевания проходит незаметно. Первые симптомы местного рецидива возникают по мере роста раковой опухоли и сдавливания ею мочеиспускательного канала. Возникают проблемы с мочеиспусканием, потенцией и эякуляцией. Характерные симптомы:
- ощущение наполненности мочевого пузыря;
- частые позывы, вялая струя урины;
- беспрерывные боли в паху;
- нарушение потенции, ее отсутствие;
- боли при семяизвержении;
- наличие крови в эякуляте;
- эпизодические боли внизу живота.

Задайте вопрос врачу-урологу!

Запущенные стадии характеризуются разрастанием опухоли за границы капсулы железы, поражением окружающих тканей, прогрессивным метастазированием в соседние и отдаленные органы. Далее процесс распространяется на поясничный сегмент позвоночника, кости таза и конечностей. Эта стадия проявляется:
- сильными болями в позвоночнике, тазу;
- появлением неврологических расстройств;
- повышением частоты патологических переломов;
- хронической усталостью и слабостью;
- утратой аппетита, сильным похуданием.

Для инфильтрации опухоли в прямую кишку характерны проблемы с дефекацией (запоры, опорожнения с кровью). Достаточно быстро в злокачественный процесс вовлекаются легкие, печень, почки и головной мозг. Развивается последняя стадия рака, обычно с печальным финалом. Клиника системного рецидива РПЖ зависит от топографии метастазирования:
- в легких – боль в грудине, кашель, кровохаркание;
- печени – боль, увеличение печени, желтизна, отеки;
- почках – боли в пояснице, гематурия, дизурия;
- в мозге – сильные головные боли, тошнота.
Для поздних стадий рецидива рака простаты после РПЭ характерны общее истощение, кахексия с признаками интоксикации (повышение температуры тела, лихорадочное состояние).
Диагностика
После оперативного удаления опухоли и специфического лечения пациенты наблюдаются у уролога-онколога. Контролируется уровень ПСА – маркера карциномы простаты. Предположением на возвращение рака простаты будет повышение результатов выше 0,2 нг/мл. Это является поводом к обследованию. Диагностические мероприятия:
- Ректальный осмотр. Выявляет местный рецидив рака на этапе, когда опухоль разрослась и пальпируется через стенку прямой кишки.
- Опрос и осмотр пациента, выявление жалоб. Выясняется состояние больного: наличие и выраженность болей, потеря в весе.
- Биохимическое тестирование. Анализы крови (общий развернутый, на сахар, ПСА) и мочи.
- Аппаратные методы (ТРУЗИ, МРТ, КТ) – дают возможность определить рецидив на раннем этапе. Томография позволяет обнаружить метастазы.
Проводятся ПЭТ (двухфотонно-эмиссионная томография), сканирование с фтордезоксиглюкозой. Перед исследованием вводится радиофармпрепарат, маркирующий атипичные клетки.
Как проводится лечение
Тактика и длительность лечебных мероприятий рецидива рака простаты после лучевой терапии и операции отличаются и зависят от первичной методики. При недостаточной эффективности облучения назначается химиотерапевтический курс либо альтернативный метод. При местной форме эффективна дистанционная радиотерапия. Системный рак простаты лечат специфическими гормональными препаратами. Новыми эффективными методами лечения рецидива РПЖ являются следующие.
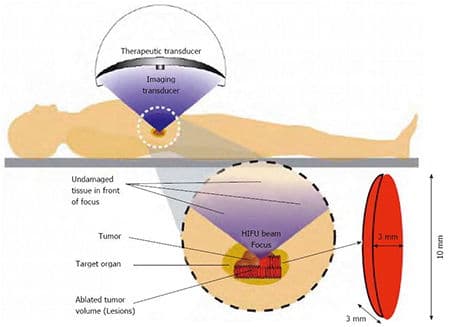
Спасительная (сальважная) HIFU терапия – при местном расположении опухоли у пациентов, перенесших полную простатэктомию. Используется высокоинтенсивный фокусированный ультразвук (High Intensity Focused Ultrasound).
Фотодинамическая терапия (ФДТ) — в/венное, локальное введение фотосенсибилизаторов, безопасных веществ, действующих на пораженный орган световым лучом заданной волны. Включает этапы:
- введение фотосенсибилизирующего препарата (минуты);
- накопление его в тканях-мишенях (дни);
- облучение опухоли лазером через световод (минуты);
- высвобождение токсинов, избирательно уничтожающих атипичные клетки.
Брахитерапия (контактное облучение) — источник излучения находится внутри ткани органа. При возобновлении рака простаты после облучения возможны локальная HIFU- и брахитерапия.
Пациент с диагнозом РПЖ после радикальной простатэктомии периодически обследуется у онколога. Проводится динамичное наблюдение показателей простатического антигена. При рецидиве рака терапевтическая тактика зависит от типа опухоли и характера ее прорастания. Учитываются возраст, иммунный статус, сопуствующие патологии. При биохимическом сигналом возвращения будет повышение уровня ПСА в крови. В этом случае назначается гормонотерапия с целью снижения уровня тестостерона.

Системный рецидив предполагает метастазирование раковых клеток в соседние органы и далее. Поздние стадии имеют выраженную онкологическую клинику. Метод борьбы со злокачественным процессом зависит от клинической ситуации. Мероприятия: химиотерапия, облучение, операция, гормональная терапия, фокусированная УЗ-абляция. Лекарства, назначаемые врачом при раке простаты:
- Золадекс (Гозарлин)— аналог гонадотропин-рилизинг гормона, назначается при гормон-резистентной форме патологии. Снижает уровень ПСА.
- Андрокур (ципротерона ацетат) — антиандроген, кастрационный препарат, осуществляет полную гормональную блокаду. Показания — метастазирующий и неоперабельный рак.
- Флутамид — нестероидный антиандроген. Препятствует усвоению клетками мужских гормонов. Снижает уровень тестостерона и, как следствие, ПСА.
Суть терапии биохимического рецидива РПЖ — нормализация показателей ПСА. Клинические рекомендации при малоэффективности гормональной терапии склоняются к проведению орхиэктомии (удалению тестикул).
Прогноз
Выживаемость пациентов с раком простаты довольно высокая. В среднем 80—90% своевременно оперированных остаются живы через 5 лет. Рецидивы также достаточно часты, 15—30% больным не удается одолеть онкологию. Смертность в течение 10 лет составляет 15—20 %. На статистику выживаемости влияет исходный уровень ПСА: чем меньше его показатели после радикальной простатоэктомии, тем лучше прогноз.
Выраженность распространения злокачественного процесса дает возможность оценить исход заболевания. Важным прогностическим фактором после РПЭ является положительный хирургический край. Рост новообразования по краю резекции и его выход за пределы капсулы значительно сокращают выздоровление.
В течение 5 лет у оперированных пациентов с негативным хирургическим краем вероятность рецидива — всего 20%, с позитивным — 40—60%. При прорастании опухоли в семенные пузырьки после удаления простаты местный рецидив рака возникает в 70% случаев. Хорошая 10-летняя выживаемость отмечается после брахитерапии (86%).
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.
Вопрос рецидива рака простаты беспокоит, конечно, каждого, кто прошел лечение рака простаты. Как бы нам не хотелось успокоить пациентов, на 100 процентов исключить его развитие нельзя. Но компетентные доктора предпринимают все возможное, чтобы предупредить развитие рака предстательной железы после пройденного лечения. Например, при определенных показаниях в профилактических целях назначают адьювантную лучевую терапию сразу после операции по удалению опухоли простаты.
ПРИ КАКИХ ПОКАЗАТЕЛЯХ ПСА ГОВОРЯТ О РЕЦИДИВЕ?
В зависимости от исходных данных заболевания и типа первичного лечения в терапии рецидива рака простаты может применяться радикальная лучевая терапия, гормональная терапия, лечение высокосфокуссированным ультразвуком (абляция).
КАК ЧАСТО ВСТРЕЧАЕТСЯ РЕЦИДИВ?
По данным исследований рецидив реже всего встречается у мужчин, которые прошли лечение на ранних стадиях рака простаты, когда рак ограничен капсулой органа. В таких случаях рецидив встречается лишь в 5-10 % случаев.
В этой категории пациентов принято различать три группы риска в отношении развития рецидива рака простаты:
- Низкий риск:
- ПСА ≤ 10 нг/мл и сумма Глисона ≤ 6 и
- клиническая стадия T1/T2a
- Средний риск:
- PSA 10-20 нг/мл или сумма Глисона 7, или
- клиническая стадия T2b
- Высокий риск: Сумма Глисона ≥ 8 или PSA > 20 нг/мл или
- клиническая стадия T2c-T3a
Если опухоль проросла капсулу и распространяется на соседние органы, то риск развития рецидива после операции повышается и встречается уже в 30-40 % случаев.
Но даже и в случае развития рецидива при своевременном вмешательстве и качественной медицинской помощи возможно если не излечить его, то противодействовать быстрому прогрессированию заболевания.
Список источников, на которых основана статья:
На нашем сайте мы расскажем о диагностике и лечении рака простаты в самых передовых по версии немецких экспертов клиниках Германии. Внимательно знакомьтесь с информацией, задавайте вопросы, записывайтесь на лечение и приезжайте в Германию. Все не так сложно, не так долго и главное — не так дорого как вам кажется.
Все клиники
Для нормального функционирования сайта мы используем технологию Cookies, собираем информацию об IP адресе и местоположении посетителей. Если Вы не согласны с этим, Вам следует прекратить пользование сайтом
-
6 минут на чтение
Рак простаты – нередкое заболевание среди мужчин в возрасте от 45 лет. Патология несет опасность не только до проведения лечения, но и после курса терапии. С течением времени, практически у половины пациентов рак развивается повторно.
Как часто диагностируется
Рецидив рака простаты у мужчин относится к злокачественным заболеваниям, которое развивается через 4-8 месяцев или спустя несколько лет после удаления первичной опухоли.
Основной причиной его возникновения считается не до конца удаленные или уничтоженные клетки рака. По данным статистики, рецидив рака предстательной железы на протяжении первых 10 лет после проведения медикаментозного лечения или хирургического вмешательства наблюдается у 26-54% мужчин.
Повторное заболевание имеет более агрессивное течение, сопровождается метастатическими поражениями, которые проникают в органы малого таза, легкие и головной мозг. Таким образом, мужчинам после лечения первичной патологии необходимо ежегодно посещать врача, проходить обследования, контролировать показатели ПСА и соблюдать ряд правил профилактики. Это поможет снизить риск рецидива.
Специалисты выделяют несколько типов повторного заболевания в зависимости от того, что стало провокатором повторного распространения патологически измененных клеток.
Также носит название локальный. Устанавливается спустя 2 года после осуществления лечения основного заболевания.
Местный рецидив выявляется по повышению ПСА более чем в два раза. Патологический процесс локализуется только в пораженном органе.
Онкологический процесс распространяется на соседние структуры. После удаления первичного злокачественного новообразования уже через год наблюдается повышение ПСА в крови пациента.
Патология развивается стремительно, имеет выраженные симптомы.
Особенностью является отсутствие симптомов. Определить наличие заболевания можно только по уровню ПСА, который за первый год увеличивается в два и более раз.
Иные клинические проявления длительное время способны отсутствовать. Они возникают только при поражении большого объема тканей.
Установить тип рецидива возможно только на ранних стадиях. Когда повторное заболевание сопровождается метастатическим поражениями и выраженными признаками определения характера невозможно.
Клиническая картина
На ранних стадиях при повторном раке симптомы могут полностью отсутствовать. Это обусловлено тем, что раковые клетки не поражают значительную область органа. Сразу определить заболевание не представляется возможным.
При распространении атипичных клеток наблюдается расстройство системы мочеиспускания. Мужчины жалуются на боли в нижней части живота. Они со временем начинают отдавать в область позвоночника и малого таза.
Нарушается процесс мочеиспускания. Струя становится слабой, выделение ее сопровождается интенсивными болевыми ощущениями и резью.
При вторичном раке предстательной железы возникает затруднение опорожнения кишечника. На 3 или 4 стадии в каловых массах появляются примеси слизи и крови.
У пациентов отмечается нарушение работы нервной системы. Они выражаются в постоянной слабости, головокружениях и головных болях. Мужчины жалуются на озноб.
В результате распространения патологически измененных клеток наступает интоксикация. Она характеризуется легкой тошнотой, отвращением к пище, головными болями, слабостью, чрезмерной усталостью. Пациент начинает отказываться от еды, что приводит к снижению веса и развитию анорексии.
По мере прогрессирования заболевания в предстательной железе начинает возникать туберкулез, который усугубляет течение основной патологии.
Клиническая картина имеет яркую выраженность только при тяжелом поражении организма, когда отмечается распространение метастатических поражений. Именно поэтому рекомендуется регулярно проходить диагностику и при появлении различных симптомов обращаться к специалисту.
Причины
Повторное развитие злокачественного образования, поражающего простату, имеет несколько причин. Чаще всего провокаторами повторного развития патологии становятся метастазы, которые поражают ткани и органы мочеполовой системы и проникают в лимфу. Также специалисты отмечают, что причинами становятся высокодифференцированный рак и не полностью удаленные атипичные клетки при осуществлении хирургического вмешательства.
В некоторых случаях патология возникает при несоблюдении пациентом предписаний врача после проведенного лечения при первичной опухоли.
Повторное развитие онокопатологии может наблюдаться при увеличении уровня ПСА. Именно поэтому мужчинам рекомендуется регулярное исследование крови на определение количества антигена. Диагноз устанавливается, когда его содержание увеличено более чем на 2 нг/мл.
Причиной рецидива рака после простатэктомии является наличие метастатических поражений, которые не были установлены при проведении диагностики и лечения.
При этом они постепенно развиваются, увеличиваются и распространяются на соседние, отдаленные ткани, органы, системы. Чаще всего они поражают печень, почки, лимфатические узлы, спинной и головной мозг.
Нередко лечение злокачественной опухоли простаты требует комплексного подхода. Перед операцией пациенту назначают лучевую или радиотерапию. Процедуры направлены на уничтожение атипичных клеток.
Но недостатком данных способов лечения является то, что они оказывают и негативное воздействие на здоровые ткани. Кроме этого, все клетки с помощью химиотерапии уничтожить невозможно.
Определить наличие рака можно только спустя месяц после проведения процедуры. В течение данного срока показатели ПСА не являются определяющим фактором наличия болезни.
Но даже хирургическое вмешательство в комплексе с иными методами воздействия, особенно на поздних стадиях заболевания, не могут гарантировать полное выздоровление.
Лечение
При своевременном диагностировании специалист определяет тип злокачественного новообразования, что влияет на метод лечения. Также при выборе тактики терапии врач учитывает возраст, наличие иных заболеваний, состояние иммунитета и особенности организма.
Лечение осуществляется как с помощью лекарственных препаратов, так и иных методов воздействия на патологически измененные клетки.
При обнаружении биохимического рецидива рака железы используются гормональные лекарственные препараты.
Они позволяют снизить количество антигена в крови и тестостерона. Но при выявлении системного или местного рецидива лекарства не применяются, так как они не способны оказать положительного воздействия. При этом назначается комплексное лечение.
Лечение рецидива рака предстательной железы проводится последовательно, за счет чего ПСА понижается до нужного уровня. При неэффективности гормональных средств пациентам назначается орхиэктомия.
Благодаря современным препаратам удается избежать серьезных побочных действий. Лекарства оказывают мягкое воздействие, отличаются высокой эффективностью.
При рецидиве рака после удаления простаты курс терапии подбирается в индивидуальном порядке. Повторное хирургическое вмешательство осуществляется в редких случаях.
Зачастую назначается химиотерапия или лучевая терапия. Также используются другие методы воздействия на злокачественное образование.
Проводится при помощи облучения области локализации опухоли. Применяется при наличии метастатических поражений.
Показаниями к назначению является локальное расположение новообразования и ранее проведенное хирургическое вмешательство.
Относится к новым способам терапии злокачественных образований. Осуществляется путем введения в ткани простаты растительного палладия.
Затем выполняют облучение специальным лазером или фотоэлементами. В результате воздействия вещество освобождает токсины, уничтожающие патологически измененные клетки. При этом практически полностью исключено негативное влияние на здоровые ткани.
Методика подразумевает воздействие на новообразование лазером, излучающего сфокусированные волны. Ткани опухоли нагреваются, что приводит к развитию некротического процесса.
Кроме современных способов лечения рецидива рака железы, используются и классические методы. Самыми популярными являются лучевая терапия и применение химиотерапевтических препаратов. Они назначаются в соответствии с наличием показаний. Но недостатком данных способов является большой риск повреждения здоровых тканей.
Повторная операция назначается в исключительных случаях, когда патологический процесс распространяется на соседние ткани, формируются метастатические поражения в отдаленных органах.
Осложнения
Повторное развитие рака простаты представляет большую опасность для организма мужчины. Отсутствие терапии или неправильное, несвоевременное лечение приводит к развитию осложнений.
В первую очередь наблюдается нарушение работы мочевыделительной и половой системы. Пациенты испытывают сильные боли. В результате распространения атипичных клеток возникает раковая интоксикация. Она характеризуется слабостью, постоянной усталостью, повышением температуры.
Метастатические поражения начинают распространяться на соседние и отдаленные ткани, нарушая их работоспособность. В результате наступает смертельный исход. Именно поэтому не следует затягивать с походом к специалисту и после проведения терапии первичной опухоли важно ежегодно посещать онколога, проходить диагностику.
Выживаемость
При повторном развитии рака предстательной железы выживаемость высокая. Но ухудшают статистику различные осложнения.
Прогноз может быть неблагоприятным, когда заболевание не было выявлено своевременно, а лечение не проведено на ранних стадиях развития патологии.
Более 70% мужчин при рецидиве рака простаты выживает, если терапия проведена на начальных стадиях, когда отсутствуют метастазы или их количество незначительно.
Но если вторичное образование злокачественного типа обнаружено на поздней стадии, болезнь запущена, выживаемость составляет не более 20% пациентов. Это обусловлено наличием большого числа метастазов.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Риск рецидива рака простаты (местного или системного) в течение 10 лет после простатэктомии или лучевой терапии составляет 27-53%. В течение 5 лет после первоначального лечения от 16 до 35% больных получают противорецидивное лечение.
Ранее под рецидивом понимали опухоль, пальпируемую через прямую кишку, а также отдалённые метастазы. Сейчас рецидивом считают рост уровня ПСА. Критерием рецидива после простатэктомии обычно считают уровень ПСА 0,2 нг/мл и более при двух последовательных измерениях. О рецидиве после лучевой терапии, согласно критериям ASTRO, можно говорить при трёх последовательных повышениях уровня ПСА.

[1], [2], [3], [4], [5], [6]
Код по МКБ-10
Где болит?
Местный и системный рецидив рака простаты
Если обнаружено повышение уровня ПСА, важно установить характер рецидива - местный или системный. После простатэктомии может идти речь о местном рецидиве, в остальных случаях - только о системном рецидиве или их сочетании.
Отличить местный рецидив от системного помогает время до повышения уровня ПСА, скорость прироста и время удвоения содержания ПСА, исходный уровень его и индекс Глисона.
Увеличение уровня ПСА в первые пол года после операции обычно указывает на системный рецидив. Медиана времени удвоения уровня ПСА при системных рецидивах может составлять 4,3, при местных - 11,7 мес. Скорость прироста уровня ПСА менее 0,75 нг/мл в год наблюдают у больных с местными рецидивами, более 0,7 нг/мл в год - у больных с отдалёнными метастазами.
На местный рецидив после лучевой терапии указывает медленный отсроченный рост уровня ПСА. Подтверждением местного рецидива служит положительный результат биопсии, выполненной через 18 мес. после облучения и позже (при отсутствии отдалённых метастазов по данным КТ, МРТ и сцинтиграфии).
Вероятность местного рецидива после простатэктомии составляет 80% при позднем подъёме уровня ПСА (более 3 лет), времени удвоения уровня ПСА более 11 мес, индексе Глисона менее 6 и стадии процесса ниже рТ3аN0 и pTxR1 Вероятность системного рецидива после простатэктомии превышает 80% при раннем подъёме уровня ПСА (менее одного года), времени удвоения уровня ПСА 4-6 мес, индексе Глисона 8-10, стадии рТ3b и pTxN1. Местный рецидив после лучевой терапии и HIFU диагностируют при положительном результате биопсии при отсутствии отдалённых метастазов. Биопсия предстательной железы показана лишь отдельным больным при планировании повторного местного лечения (например, простатэктомии или повторного сеанса HIFU).
Обследование при подозрении на рецидив рака простаты
Для подтверждения рецидива при повышении уровня ПСА обычно проводят физикальное обследование, УЗИ, КТ или МРТ малого таза, биопсию ложа опухоли и области анастомоза. При отсутствии симптомов эти исследования редко обнаруживают опухоль, так как рост уровня ПСА обычно происходит за 6-48 мес до явного рецидива.
Пальцевое ректальное исследование при нулевом или очень низком уровне ПСА обычно не приносит результатов. При повышении уровня ПСА назначают МРТ малого таза, КТ брюшной полости и сцинтиграфию костей, но из-за низкой чувствительности и специфичности при раннем рецидиве эти исследования малоинформативны. При подъёме уровня ПСА после простатэктомии результат сцинтиграфии положителен лишь у 4,1% больных. Вероятность положительного результата сцинтиграфии не превышает 5%, пока уровень ПСА не достигнет 40 нг/мл. Средний уровень ПСА, при котором сцинтиграфии обнаруживает метастазы должен превышать 60 нг/мл, а скорость прироста уровня ПСА - 22 нг/мл в год. Уровень и скорость прироста содержания ПСА позволяют предсказать результат сцинтиграфии, а скорость прироста уровня ПСА - результат КТ. Таким образом, при уровне ПСА менее 20 нг/мл или скорости прироста содержания ПСА менее 20 нг/мл в год сцинтиграфия и КТ не приносят дополнительной информации. Эндоректальная МРТ обнаруживает местный рецидив у 81% больных со средним уровнем ПСА 2 нг/мл.
ПЭТ рекомендуют для ранней диагностики рецидивов различных опухолей.
Сцинтиграфия с антителами к простатическому мембранному антигену (простасцинт) - один из новых методов обнаружения рецидивов. Его диагностическая точность достигает 81%. Независимо от уровня ПСА метод обнаруживает возникновение рецидива у 60-80% больных, что может помочь при выборе тактики лечения. Сцинтиграфия с этими антителами положительна у 72 из 255 больных с уровнем ПСА 0,1-4 нг/мл после простатэктомии, причём накопление изотопа наблюдают при любом уровне ПСА.
Биопсия зоны анастомоза позволяет обнаружить рецидив только у 54% больных. Лишь при наличии пальпируемого или гипоэхогенного образования вероятность положительного результата приближена к 80%. Существует четкая зависимость между этим показателем и уровнем ПСА: при содержании ПСА менее 0,5 нг/мл результат положителен у 28% больных, при уровне ПСА более 2 нг/мл - у 70% больных Учитывая эти данные, биопсию из зоны анастомоза обычно не берут и ориентируются на уровень ПСА и скорость его удвоения. Кроме того, выживаемость при доказанных рецидивах примерно такая же, как при регистрации изолированного повышении ПСА.
Согласно рекомендациям ASTRO, при повышении уровня ПСА после лучевой терапии биопсия предстательной железы не показана. Впрочем биопсия имеет ключевое значение для решения вопроса о простатэктомии или HIFU у таких больных. После лучевой терапии (дистанционной или брахитерапии) биопсию обычно проводят не ранее чем через 18 мес после криодеструкции или через 6 мес после ультразвуковой деструкции.

[7], [8], [9], [10], [11], [12]
Что нужно обследовать?
Как обследовать?
Какие анализы необходимы?
К кому обратиться?
Лечение рецидива рака простаты
Сроки и тактика лечения при подъёме уровня ПСА после простатэктомии или лучевой терапии вызывают дискуссии. В случае рецидива после операции возможны наблюдение, облучение ложа опухоли, HIFU-терапия рецидива, гормонотерапия рака простаты (в том числе комбинированная, периодическая или сочетанное применение финастерида и антиандрогенов), а также сочетание гормоно- и химиотерапии. Эти методы применимы и при рецидиве после лучевой терапии.
При высоком дооперационном уровне ПСА (более 20 нг/м, индексе Глисона более 7, нерадикальной операции и местнораспространённых опухолях рТ3b, рТxN1) целесообразна ранняя гормонотерапия. Однако ее влияние на выживаемость до сих пор не установлено. При ранней гормонотерапии метастазы возникают реже, чем при отсроченной, выживаемость в обоих случаях примерно одинаковая. Необходимость гормонотерапии подтверждает испытание МRС, в котором рецидив был отмечен у всех больных, получивших лучевую терапию по поводу роста уровня ПСА после простатэктомии при опухолях рТ3b, рТхN1, и индексе Глисона 8.
Монотерапию антиандрогенными препаратами больные переносят лучше, чем комбинированную (реже возникают приливы, снижение потенции, утрата полового влечения), однако антиандрогены вызывают гинекомастию и боль в сосках. У больных без отдалённых метастазов бикалутамид (по 150 мг/сут) достоверно снижает риск прогрессирования заболевания. Таким образом, антиандрогены могут быть альтернативой кастрации при повышении уровня ПСА после радикального лечения (особенно у относительно молодых больных без сопутствующих заболеваний).
Динамическое наблюдение обычно проводят при индексе Глисона менее 7, позднем (через 2 года после операции) повышении уровня ПСА и времени его удвоения более 10 месяцев. В таких случаях медиана времени до возникновения метастазов составляет 8 лет, а медиана времени от возникновения метастазов до наступления летального исхода - ещё 5 лет.
В последнее время появляется всё больше данных о результатах HIFU-терапии местного рецидива после РПЭ. Чаще всего рецидив обнаруживают при ТРУЗИ и подтверждают гистологически (биопсия). Тем не менее HIFU-терапия лить отодвигает сроки назначения гормонотерапии. Точные данные о выживаемости отсутствуют.
Клинические рекомендации по лечению рецидива после простатэктомии
При местном рецидиве и уровне ПСА менее 1,5 нг/мл показана лучевая терапия до СОД 64-66 Гр,
Если больной ослаблен или возражает против облучения, при местном рецидиве возможно динамическое наблюдение
При росте уровня ПСА, указывающем на системный рецидив, показана гормонотерапия, так как она снижает риск метастазирования.
В качестве гормонотерапии можно использовать аналоги гонадолиберина, кастрацию или бикалутамид (по 150 мг/сут).
Наиболее часто больные с рецидивом после лучевой терапии получают гормонотерапию (до 92%). Без лечения время от повышения уровня ПСА до манифестации рецидива составляет около 3 лет. Кроме гормонотерапии при рецидиве после облучения возможно и местное лечение - простатэктомия, HIFU-терапия, криотерапия, брахитерапия. Простатэктомия не нашла широкого применения из-за частых осложнений (недержание мочи, повреждение прямой кишки), а также из-за высокого риска местного рецидива. Однако при тщательном отборе больных эта операция может обеспечить длительный безрецидивный период,
По последним данным. 5-летняя безрецидивная выживаемость после лучевой терапии соответствует таковой после первичной простатэктомии, проведённой на тех же стадиях заболевания, 10-летняя выживаемость составляет 60-66%. В течение 10 лет от прогрессирования опухоли умирают 25-30% больных. При локализованных опухолях, отсутствии опухолевых клеток в крае резекции, инвазии семенных пузырьков и метастазирования в лимфатические узлы безрецидивная выживаемость достигает 70-80% по сравнению с 40-60% при местнораспространённых опухолях.
Простатэктомия при местном рецидиве оправдана при отсутствии тяжелых сопутствующих заболеваний, ожидаемой продолжительности ЖИЗНИ не менее 10 лет, опухолях индексе Глисона менее 7 и уровне ПСА менее 10 нг/мл. В остальных случаях до операции сложно определить распространённость опухоли, что повышает риск передней или тотальной экзентерации, осложнений, а также повторною рецидива.
Рекомендовано динамическое наблюдение за больными с вероятным местным рецидивом (из группы низкого риска, с поздним рецидивом и медленным ростом уровня ПСА), настроенными против повторного радикального лечения. Ретроспективный анализ не обнаружил преимуществ гормонотерапии по сравнению с динамическим наблюдением при времени удвоения уровня ПСА более 12 мес; 5-летняя выживаемость без метастазирования составила 88% при гормонотерапии и 92% - на фоне наблюдения.
После простатэктомии, если уровень ПСА менее 20 нг/мл и скорость его прироста менее 20 нг/мл в год, КТ брюшной полости и малого таза малоинформативна.
Эндоректальная МРТ помогает обнаружить местный рецидив при низком уровне ПСА (1-2 нг/мл). ПЭТ пока не получила широкого распространения.
Сцинтиграфия с мечеными антителами к простатическому мембранному антигену позволяет обнаружить рецилив у 60-80% больных независимо от уровня ПСА.
Биопсию для подтверждения местного рецидива проводят через 18 мес и более после облучения.

[13], [14], [15], [16], [17], [18], [19], [20]
У отдельных больных с местным рецидивом возможно выполнение простатэктомии.
При противопоказаниях к операции возможно проведение брахитерапии, HIFU-терапии или криодеструкции.
При вероятном системном рецидиве возможна гормонотерапия рака простаты.
Клинические рекомендации по лечению рецидивов после радикального лечения
Вероятный местный рецидив после простатэктомии
Возможна лучевая терапия в дозе не менее 64 Гр желательно начать её при уровне ПСА менее 1.5 нг/мл.
В остальных случаях предпочтительно наблюдение с последующей гормонотерапией
Вероятный местный рецидив после лучевой терапии
В отдельных случаях возможна простатэктомия, но больному нужно сообщить о сравнительно высоком риске осложнений.
В остальных случаях предпочтительно наблюдение с последующей гормонотерапией.
Вероятный системный рецидив
Ранняя гормонотерапия замедляет прогрессирование и может увеличить выживаемость по сравнению с отсроченной. Местное лечение проводят только в паллиативных целях.

[21], [22], [23], [24]
Читайте также:

