Ишемическая болезнь лечение рака
Ишемическая болезнь сердца
Ишемия миокарда, реже - инфаркт миокарда или аритмии, индуцированные ишемией, являются побочными эффектами ряда методов лечения онкозаболеваний. В основе этих осложнений лежит целый спектр механизмов: от прямого индуцирования вазоспазма, эндотелиального повреждения и развития артериального тромбоза до долгосрочных изменений метаболизма липидов и, соответственно, преждевременного развития атеросклероза (таблица 1). Лучевая терапия на область средостения может усугублять поражение коронарных артерий, вызванное химиопрепаратами.
Таблица 1. Патофизиологические механизмы развития ИБС на фоне лечения онкозаболеваний.
Фторпиримидины
Фторпиримидины (такие как 5-фторурацил и его пероральная форма капецитабин) используются для лечения онкозаболеваний ЖКТ и некоторых других локализаций. Риск развития ишемии миокарда зависит от дозы, пути введения и схемы химиотерапии. Боль в груди и изменения ЭКГ чаще возникают в покое в дни введения химиопрепарата. Иногда проявления ишемии сохраняются после отмены препаратов. Проблема ишемии миокарда, индуцированной фторпиримидинами, может быть недооценена клинически. Последние исследования показали, что у 5-6% пациентов, получавших 5-ФУ, при стресс-тестах выявлялась безболевая ишемия миокарда. Также применение 5-ФУ может приводить к развитию острого ИМ. Пациентам, получающим эти препараты, следует регулярно выполнять ЭКГ. При выявлении признаков ишемии миокарда следует прерывать терапию.
Иммунная и таргетная химиотерапия
Препараты этих групп, воздействующие на сигнальные пути фактора роста эндотелия сосудов (VEGF), увеличивают риск коронарного тромбоза. Эти сигнальные пути важны для поддержания жизнеспособности клеток эндотелия, а ингибирование этих путей приводит к повреждению клеток эндотелия и их гибели. Риск тромбоза зависит от исходного заболевания и конкретного препарата. Так, для моноклонального антитела к рецептору VEGF бевацизумаба, риск составляет менее 1% при адьювантной терапии рака молочной железы, а при лечении метастатических форм онкозаболеваний – 3,8%.
Лучевая терапия
Наддиафрагмальная (а при некоторых заболеваниях и поддиафрагмальная) лучевая терапия ассоциируется с высоким риском развития ИБС как за счет агрессивного течения атеросклероза, так и за счет других процессов, приводящих к разрывам бляшек и тромбозу коронарных артерий, а также, возможно, и за счет коронарного спазма. Для атеросклероза, вызванного лучевой терапией, характерно устьевое поражение коронарных артерий. Чаще всего затрагиваются передняя нисходящая артерия (при облучении левой молочной железы) и ствол левой коронарной артерии (при лечении лимфомы Ходжкина). Есть данные, что у женщин, которым проводилась лучевая терапия по поводу рака левой молочной железы, частота положительных стресс -тестов достоверно выше, чем у получавших лечение по поводу рака правой молочной железы.
Манифестация ИБС может быть быстрой (первое проявление болезни – ОКС или внезапная смерть), но чаще эффект бывает отсроченным. Например, изменения после лечения лимфомы чаще манифестируют через 15-20 лет (причем, молодые пациенты более восприимчивы к такому воздействию). Пациенты, выжившие после лечения лимфомы Ходжкина, характеризуются риском ИБС в 4-7 раз большим, чем вся популяция. Через 40 лет после лечения у 50% пациентов диагностируется ИБС.
Исходя из этих данных, оправдано проводить регулярное скрининговое обследование всех пациентов, которым проводилась лучевая терапия соответствующей локализации, начиная с момента 10-15 лет после лечения и далее пожизненно.
Дополнительными факторами риска возникновения или осложнений ИБС в результате лучевой терапии являются сопутствующий прием антрациклинов, молодой возраст, высокие дозы облучения (>30 Грей), отсутствие экранирования грудной клетки, классические факторы риска сердечно-сосудистых заболеваний и предсуществующая ИБС.
Внезапная сердечная смерть - явление, описанное у пациентов, подвергавшихся облучению. Связано оно было с диффузной гиперплазией интимы всех коронарных артерий или с гемодинамически значимым поражением ствола ЛКА.
Для предотвращения поражения сердца должны быть использованы такие методы, как максимально возможное снижение дозы облучения, тангенциальные поля облучения, экранирование структур сердца. В настоящее время существуют технологии, основанные на 3D планировании полей облучения с построением гистограмм доза-объем, а также различные симмуляционные программы. С помощью результатов КТ или МРТ можно достаточно точно идентифицировать контуры опухоли, а специальные программы рассчитывают распределение облучения.
Особенности диагностики и лечения
Перед началом химиотерапии или лучевой терапии важно выявить ИБС или другие сердечно-сосудистые заболевания, поскольку их исходное наличие значительно повышает риск дальнейших осложнений лечения онкозаболеваний.
Часто на фоне химио- и лучевой терапии развивается тромбоцитопения, поэтому лечение симптомной ИБС и ОКС крайне затруднено. Вообще, применение антитромботической терапии у получающих химио- или лучевую терапию часто противопоказано или очень ограничено. Пациентам, которым выполняется ЧКВ, необходимо использовать двойную антитромбоцитарную терапию как можно меньше по времени для минимизации риска кровотечений.
Клиника ИБС часто носит атипичный характер, зачастую развивается безболевая ишемия миокарда (за счет нейротоксических эффектов лучевой и химиотерапии).
В случае развития вазоспазма на фоне химиотерапии следует сменить используемый препарат. Если иных вариантов нет, продолжать терапию следует на фоне профилактического введения нитратов и/или антагонистов кальция под тщательным контролем.
В случае развития любых осложнений химио- и лучевой терапии со стороны сердечно-сосудистой системы пациенты подлежат длительному наблюдению кардиологом.
Тромбоэмболические осложнения фибрилляции предсердий
Для оптимизации антитромботической профилактики у пациентов с ФП обычно используют шкалы CHA2DS2-VASc и HAS-BLED. Однако обе эти шкалы не валидизировались у пациентов с онкозаболеваниями. У пациентов с онкозаболеваниями повышен риск как тромбоэмболических осложнений, так и кровотечений. Поэтому принятие решения о назначении антитромботической терапии может быть достаточно сложным и отличаться от общей популяции. Пациентам со значением CHA2DS2-VASc≥2 антикоагулянты могут быть назначены при числе тромбоцитов более 50 тыс/мкл (как правило, речь идет об АВК при условии хорошего контроля МНО – время пребывания в терапевтическом диапазоне МНО > 70%). В случае формально низкого риска ТЭО в соответствии со значениями CHA2DS2-VASc антикоагулянты все равно могут быть назначены, принимая во внимание риск венозной тромбоэмболии.
НМГ назначают в качестве краткосрочного лечения, либо как альтернатива варфарину у пациентов с высоким риском кровотечений или метастатическим поражением.
Данные по НОАК пока относительно ограничены. Кроме того, в исследования этих препаратов не включались пациенты с уровнем тромбоцитов менее 100 тыс/мкл. Однако мета-анализ исследований НОАК показал, что эти препараты безопасны для пациентов с онкозаболеваниями.
Артериальные тромбозы
Артериальные тромбозы достаточно редки у пациентов с онкозаболеваниями (около 1%). Чаще они развиваются у пациентов с метастазирующим раком поджелудочной железы, молочной железы, колоректальным раком или раком легких, а также у пациентов, получающих антрациклины, таксаны, химиопрепараты на основе платины, а также ингибиторы VEGF. Чаще всего речь идет о пациентах с неблагоприятным прогнозом. Протромботический статус может увеличивать риск ТЭО у пациентов с ФП.
У пациентов с раком молочных желез, получающих гормональную терапию, риск артериальных тромбозов выше у использующих ингибиторы ароматаз по сравнению с тамоксифеном (по- видимому, за счет несколько более благоприятного влияния тамоксифена на липидный профиль).
Особенности лечения артериальных тромбозов у онкологических пациентов плохо изучены.
В случае повторных эпизодов артериальных тромбозов следует исключить наличие антител к фосфолипидам.
Венозный тромбоз и тромбоэмболия развиваются у 20% госпитализированных больных с раком (причем часто эти осложнения остаются не диагностированными). Помимо собственного влияния онкозаболевания, риск ВТЭО может повышаться на фоне химиотерапии (в том числе, с учетом использования неудаляемых венозных катетеров). Антитромботическая профилактика должна проводиться минимум в течение 4 недель после оперативного лечения.
У амбулаторных пациентов с раком мочевого пузыря, толстой кишки, яичников, легких, желудка и поджелудочной железы, получающих химиотерапию, риск ВТЭО также повышен, но целесообразность медикаментозной профилактики у таких пациентов неясна.
Таблица 2. Факторы риска венозной тромбоэмболии у онкологических пациентов.

Химиотерапия в комбинации с ингибиторами VEGF повышает риск ВТЭО в 6 раз, повторных ВТЭО – в 2 раза.
Выявление тромботических эпизодов в первую очередь основывается на наличии соответствующих симптомов. Ни одна из стратегий скрининга тромботических осложнений себя не оправдала. Часто при визуализации очага поражения находками являются бессимптомные тромбозы и даже ТЭЛА. Оптимальная стратегия лечения в этом случае не ясна, однако с целью профилактики повторных эпизодов такие тромбозы лечат как обычные.
Для лечения подтвержденного острого эпизода ВТЭО у гемодинамически стабильных пациентов следует назначать НМГ на 3-6 месяцев (такая терапия эффективнее варфарина при сходной частоте кровотечений и смертности). Риск геморрагических осложнений на фоне антикоагулянтной терапии ВТЭО у онкологических пациентов в 6 раз выше в сравнении с обычными пациентами с ВТЭО.
Данные по НОАК у этой категории больных ограничены анализом в подгруппах в исследованиях, сравнивающих НОАК и варфарин (не было получено данных о различиях по частоте повторных ВТЭО и кровотечений). С НМГ НОАК не сравнивались. Разные НОАК могут отличаться между собой в связи с лекарственными взаимодействиями и разной чувствительностью к почечной и печеночной дисфункции.
Если повторное ВТЭО произошло на фоне антикоагулянтов, следует изменить терапию (перейти с АВК на НМГ, если пациент уже получает НМГ – увеличить дозу).
На настоящий момент нет четких доказательств целесообразности проведения тромболизиса в случае развития ТЭЛА с гемодинамической нестабильностью у этой категории пациентов, что связано со значительно повышенным риском кровотечений. Однако в ряде случаев (ориентируясь на ожидаемую продолжительность жизни) тромболизис может быть выполнен, принимая во внимание высокую смертность от такого типа ТЭЛА. Важно помнить о противопоказаниях к тромболизису у пациентов с опухолями ГМ и метастазами в ГМ. Также может быть выполнена хирургическая эмболэктомия, однако смертность во время этого вмешательства достаточно высока, и кардиопульмональное шунтирование требует агрессивной антикоагуляции.
Что касается профилактики ВТЭО у пациентов на химиотерапии, в настоящее время рекомендовано проводить медикаментозную профилактику (преимущественно, НМГ) амбулаторным пациентам с высоким риском ВТЭО (например, получающим анти-ангиогенные препараты по поводу множественной миеломы, либо химиотерапию по поводу местнораспространенного или метастатического рака поджелудочной железы или легких), но без высокого риска кровотечений.
У пациентов с центральным венозным катетером показано использование гепарина или АВК (причем применение гепарина ассоциировано с большей частотой тромбоцитопении и бессимптомных тромбозов глубоких вен).
Атеросклероз периферических артерий и инсульт
Тяжелое атеросклеротическое и неатеросклеротическое поражение артерий нижних конечностей может развиться у пациентов (до 30%), получающих нилотиниб, понатиниб или ингибиторы тирозин-киназы BCR-ABL (например, для лечения миелоидного лейкоза). Поражение может развиться даже в отсутствие факторов риска АПАНК, а в присутствии таких факторов риск поражения артерий нижних конечностей еще увеличивается. Поражение может развиться как в первый месяц терапии, так и отсрочено, в том числе – годы спустя после лечения. Ряд химиопрепаратов (например, L-аспарагиназа, цисплатин, метотрексат, 5-фторурацил и паклитаксел) может вызывать феномен Рейно.
Риск инсульта повышается (по меньшей мере, вдвое) после лучевой терапии на область средостения, шеи или головы. Происходит повреждение и тромбоз малых сосудов головного мозга. В сосудах среднего и крупного калибра описаны три патофизиологических механизма, повышающих риск инсульта – окклюзия vasa vasorum с последующим медианекрозом и фиброзом, фиброз адвентиции, а также прогрессирование атеросклероза (чаще развивается более чес через 10 лет после лучевой терапии). Похожие механизмы повреждения описаны для аорты и других периферических сосудов (включая подключичные и подвздошно-бедренные артерии, что приводит к ишемии конечностей).
Пациентам, которым проводилась лучевая терапия на область шеи или головы, а также лечение лимфомы, должно выполняться ультразвуковое исследование церебральных сосудов (особенно начиная с периода 5 лет после лучевой терапии). Исследование должно повторяться каждые 5 лет (или чаще, если при первом исследовании были обнаружены отклонения). Признаки постлучевых поражений других артерий выявляют при физикальном осмотре или по наличию соответствующих симптомов.
По материалам:
Материал подготовлен сотрудником лаборатории клинических проблем атеротромбоза отдела ангиологии РКНПК им. А.Л. Мясникова к.м.н. Шахматовой О.О.
Уважаемый посетитель NOAT.RU!
Настоящий раздел предназначен исключительно для лиц, имеющих среднее и высшее медицинское образование, а также студентов медицинских ВУЗов.
Никакие из опубликованных материалов не могут служить заменой медицинскому осмотру и не должны быть использованы как руководство к лечению. Только врач, который имеет личный контакт с пациентом, знаком с его историей болезни и наблюдает за состоянием его здоровья, может рекомендовать тот или иной метод лечения. Информация на данном сайте или другие предоставляемые им услуги не могут служить основанием для диагностики или лечения без соответствующего участия врача.
Ни при каких обстоятельствах администрация, составители, консультанты и правообладатели сайта не могут быть ответственны за любой непрямой, случайный или косвенный вред, причиненный здоровью и жизни, а также материальный ущерб или утерю прибыли, наступившую в результате любого использования или доступа или невозможности использования или получения доступа к ресурсу NOAT.RU или его содержимому.
Администрация NOAT.RU не несет ответственности за содержание баннеров и информационных материалов третьих лиц.
Сколько в России больных ишемической болезнью сердца (ИБС) точно никто не знает, под наблюдением находится чуть меньше 8 миллионов, ежегодно этот диагноз ставят 600–700 тысячам россиян и столько же умирает. Стенокардия — одна из форм ИБС уносит в мир иной на 8 лет раньше положенного. Известно, что четверть всех посетителей российских поликлиник обращаются именно по поводу ИБС. Почти половина перенёсших инфаркт в больнице впервые узнают, что, оказывается, страдают ишемической болезнью. Поэтому есть мнение, что больных ИБС гораздо больше, чем учтено официальной статистикой, возможно, что и вполовину больше.
Что сегодня понимают под ИБС?
- стенокардию и безболевую ишемию,
- инфаркт и очаговую дистрофию миокарда,
- постинфарктный кардиосклероз,
- нарушения ритма и сердечную недостаточность.
Стенокардии бывают разными: впервые возникшая, стабильная, прогрессирующая, спонтанная или вазоспастическая. Инфаркт миокарда может быть мелкоочаговым и крупноочаговым или трансмуральным. А вот дистрофия и кардиосклероз после инфаркта при ИБС только очаговые, обширные имеют иную природу и называются по-другому.

Почему возникает ишемическая болезнь?
Ишемическая болезнь сердца означает повреждение миокарда вследствие нарушения кровотока по коронарным артериям. Когда потребность сердечной мышцы в кислороде выше, чем возможность его доставки, тогда и возникает ишемия. Причины разные, частые: необратимое сужение атеросклеротической бляшкой, спазм сосуда, тромбоз его. Реже приступы ИБС вызывают врождённые аномалии с неправильным отхождением коронарного сосуда от основного питающего ствола, аутоиммунное поражение, передозировка сосудосуживающих препаратов и некоторых наркотиков.
Факторы риска
Какой бывает стенокардия
Классическая стенокардия имеет три особенных клинических признака, отличающих её от всего остального, эти признаки возникают в связке, но присутствие всех обязательно.
- Боль появляется во время напряжения физического или эмоционального.
- 2-5-минутная боль локализуется за грудиной, отдаёт в левую руку, спину или, реже, нижнюю челюсть. Не всегда боль может восприниматься как боль, иногда возникает ощущение тяжести, жжения за грудиной или одышка. В классический вариант стенокардии не вписываются боли под ложечкой или лопаткой, справа в грудной клетке, но когда есть третий признак, то сомнения что это стенокардия отпадают.
- Боль проходит от таблетки нитроглицерина или при прекращении движений.
Когда отмечаются только два признака из трёх классических, то говорят об атипичной или возможной стенокардии. Никакого отношения к стенокардии не имею другие болевые ощущения, локализующиеся не в типичных местах, локальные, продолжительностью более получаса, не связанные с движением, не реагирующие на нитроглицерин, усиливающиеся при ощупывании больного места. Это всё что угодно, но не стенокардия.
Стенокардические боли могут возникать при поражении не только самих коронарных артерий, но отходящих от них мелких сосудов. Этот вариант непросто выявить, потому что коронароангиография хорошо визуализирует артерии, диаметр которых не менее 0,4 мм, а мелкие сосудики в два-четыре раза уже. При физической нагрузке нарушение функционирования микрососудов приводит к избыточному их спазму и неадекватному расслаблению. Этот вариант стенокардии называют микрососудистым или Х-коронарный синдром.
Для микрососудистой тоже обязательны три собственных признака. Во-первых, по клинической картине это совершено типичная или атипичная стенокардия, с присущей ей локализацией болей и реакцией на нагрузку. Во-вторых, её диагностируют по ЭКГ с нагрузочными пробами, сцинтиграфии миокарда или ЭХО КГ. В-третьих, функция левого желудочка должна быть нормальной, а коронарные артерии крупного и среднего диаметра не должны быть изменёнными, то есть не могут быть причиной стенокардии. Но почти в 70% случаев классическая и микрососудистая стенокардии сосуществуют.
Вазоспастическая или вариантная стенокардия
Ишемия миокарда без болевого синдрома
Это не стенокардия, но тоже может довести до инфаркта миокарда. Не обязательно, что все приступы абсолютно безболезненны, возможно и чередование бессимптомной ишемии со стенокардией. Как правило, такая ишемия выявляется на ЭКГ с нагрузочными пробами или суточном мониторировании. Что интересно, при атеросклерозе у пятой части пациентов встречается такой вариант ишемии, характерна она и для больных диабетом. Она возникает днём, но при обширном атеросклерозе коронарных сосудов может развиться и ночью на фоне полного покоя. Понятно, что пациент ишемию без болевого синдрома не замечает.

Кого из нас хотя бы раз в жизни не беспокоила боль в сердце? Таких людей, к сожалению, очень мало. У некоторых боли в сердце возникают единовременно, у других – довольно часто. Причин таких ощущений достаточно много, одной из них является ишемическая болезнь сердца. ИБС – что это такое, как проявляется и как с этим справится расскажет эта статья.
Ишемическая болезнь сердца – это заболевание, в результате которого происходит несоответствие между потребностью сердечной мышцы в кислороде и его доставкой к ней. Может быть как остро протекающим процессом, так и хроническим.
Причины возникновения

ИБС – это болезнь, которая возникает при недостаточном поступлении крови к сердцу. К этому приводит поражение коронарных артерий. Такое может произойти в следующих случаях:
- атеросклеротическое поражение – является основной причиной возникновения заболевания. Атеросклеротическая бляшка, растущая в сосуде, закрывает его просвет, вследствие чего через коронарную артерию проходит меньший объем крови;
- врожденные генетические аномалии венечных артерий – порок развития, который сформировался внутриутробно;
- воспалительные заболевания венечных артерий (коронарииты), возникающие вследствие системных заболеваний соединительной ткани или узелкового периартериита;
- аневризма аорты, которая находится в процессе расслоения;
- сифилитическое поражение стенок коронарных сосудов;
- тромбоэмболия и эмболия венечных артерий;
- врожденные и приобретенные пороки сердца.
Группа риска

К этиологическим факторам можно отнести факторы риска, которые делятся на 2 группы – которые изменяются и не изменяются (то есть те, которые зависят от человека, и те, которые человек изменить не может).
Механизмы развития
ИБС – это то, что определяется как несоответствие между потребностью миокарда в кислороде и доставкой кислорода. Следовательно и механизмы развития связаны именно с этими двумя показателями.
Потребность сердца в необходимом ему количестве кислорода определяют следующие показатели:
- размеры сердечной мышцы;
- сократимость левого и правого желудочка;
- величина АД;
- частота сердечных сокращений (ЧСС).

Сбой в доставке кислорода происходит в основном из-за сужения просвета венечных сосудов атеросклеротическими бляшками. В пораженных сосудах происходит повреждение их внутренней оболочки, вследствие чего эндотелий прекращает выделять сосудорасширяющие вещества и начинает продуцировать сосудосуживающие, что еще больше уменьшает просвет сосудов.
Еще одним механизмом развития является разрыв атеросклеротической бляшки, вследствие чего тромбоциты прилипают к месту повреждения сосудистой стенки, образуя тромбоцитарные массы, которые закрывают просвет сосудов, уменьшая ток проходимой крови.
Виды ИБС
Ишемическая болезнь сердца классифицируется следующим образом:
- ВСС – внезапная сердечная смерть.
- Стенокардия:
- в покое;
- в напряжении (нестабильная, стабильная и впервые возникшая);
- спонтанная.
- Безболевая ишемия.
- Инфаркт миокарда (мелко и крупноочаговый).
- Кардиосклероз после инфаркта.
Иногда в данную классификацию включают еще два пункта, такие как сердечная недостаточность и нарушение сердечного ритма. Данная классификация ИБС была предложена ВОЗ и практически не изменилась до настоящего времени. Вышеперечисленные заболевания являются клиническими формами ИБС.
Клиническая картина
Симптомы ИБС зависят от ее клинической формы. Они могут различаться по силе, длительности и характеру боли, по наличию или отсутствию тех или иных симптомов.

Это смерть, которая наступила в течении одного часа после появления сердечных симптомов, связанная с сердечными причинами, естественная, которой предшествует потеря сознания.
Причинами внезапной смерти является непосредственно ИБС, инфаркт миокарда, врожденные пороки сердца, кардиомиопатии, аномалии венечных артерий и синдром Вольфа-Паркинсона-Уайта (предвозбуждение желудочков).
Симптомы данной ИБС (клинической формы) могут начинаться с неопределенных болей за грудиной, затем через несколько недель возникают одышка, усиленное сердцебиение и слабость. После возникновения этих симптомов возникает внезапная потеря сознания (в результате остановки сердца прекращается мозговое кровообращение). При осмотре выявляется расширение зрачков, отсутствие всех рефлексов и пульса, остановка дыхания.

Данная форма характеризуется возникновением болей за грудиной, которые появляются во время физических упражнений и/или сильных эмоций, при нахождении на холоде, а так же могут появляться в спокойном состоянии, при употреблении большого количества пищи.
В этой клинической форме можно немного подробнее разобраться с тем, что это такое, называемое ишемической болезнью. В результате разнообразных причин, которые были описаны выше, происходит ишемия миокарда, причем вначале страдают слои, которые располагаются под эндокардом. Вследствие этого нарушается сократительная функция и биохимические процессы в клетках: так как нет кислорода, то клетки переходят на анаэробный тип окисления, в результате которого глюкоза распадается до лактата, что уменьшает внутриклеточный pH. Уменьшение внутриклеточного показателя кислотности приводит к тому, что энергия в кардиомиоцитах постепенно истощается.
Кроме того, стенокардия приводит к тому, что концентрация калия внутри клетки снижается, при этом концентрация натрия возрастает. Из-за этого происходит сбой в процессе расслабления сердечной мышцы, и уже вторично страдает сократительная функция.
В зависимости от переносимости сердечной нагрузки канадское общество кардиологов выделило следующие функциональные классы стенокардии напряжения:
- Функциональный класс (ФК) I – приступ стенокардии не вызывается при обычной физической нагрузке, а возникает только при очень сильном или продолжительном напряжении.
- ФК II приравнивается к легкому ограничению физической активности. При этом приступ провоцируется ходьбой более 200 м по ровной местности или подъемом более чем на один пролет по лестнице.
- ФК III – значительное ограничение физической активности, при которой боли за грудиной возникают уже при ходьбе по ровной местности или подъеме на один лестничный пролет.
- При IV ФК стенокардии напряжения любая физическая нагрузка без возникновения дискомфорта и боли за грудиной невозможна, а также приступы могут возникать и в покое.
Симптомы ишемической болезни включают в себя боль и ее эквиваленты (одышка и резкая утомляемость). Боль локализуется за грудиной, длится от 1 до 15 минут, имеет нарастающий характер. Если длительность дискомфорта более 14 минут, есть опасность того, что это уже не стенокардия, а инфаркт миокарда. Существует два условия прекращения неприятных ощущений: отмена физ. нагрузки или прием нитроглицерина под язык.
Боль может быть сжимающего, давящего или распирающего характера, при этом возникает страх смерти. Иррадиация происходит как в левые, так и в правые отделы грудной клетки, в шею. Классической считается иррадиация в левую руку, плечо и лопатку.
Признаки ишемической болезни сердца включают в себя и возникающие сопутствующие симптомы: тошноту, рвоту, повышенную потливость, тахикардию и повышение АД. Больной бледный, замирает в одном позе, так как малейшее движение усиливает боль.
НС – это остро возникающая ишемия миокарда, тяжесть и продолжительность воздействия которой недостаточна для возникновения инфаркта миокарда.
Данный вид ИБС возникает из-за следующих причин:
- резкий спазм, тромбоз или эмболизация венечных артерий;
- воспаление коронарных сосудов;
- разрыв или эрозия атеросклеротической бляшки с дальнейшим формированием тромба на поврежденной поверхности сосуда.
К симптомам ишемической болезни сердца относят типичные и атипичные жалобы. К типичным жалобам относится длительный болевой синдром (более 15 мин.), наличие болей в покое, а также ночные приступы. При атипичных жалобах происходят боли в эпигастральной области, расстройство пищеварения, которое развивается остро, и усиление одышки.
В отличии от инфаркта миокарда, маркеров некроза в крови нет. Это является главным отличием при проведении дифференциальной диагностики.

Этот вид относится к вариантной, при которой неприятные ощущения за грудиной появляются в покое, при этом на электрокардиограмме определяется преходящий подъем сегмента ST. Возникает из-за временного, преходящего спазма венечных артерий, с физической нагрузкой вариантная стенокардия никак не связана. Болевой приступ может купироваться как самостоятельно, так и после приема нитроглицерина.
Ишемическая болезнь сердца данного вида характеризуется возникновением типичной сенокардиотической боли за грудиной, чаще в ночью или рано утром, продолжительностью более 15 мин. Сопутствующим признаком является появление мигрени и синдрома Рейно, а также при наличии данного вида стенокардии очень часто выявляется наличие аспириновой астмы.
Диагностическим признаком являются внезапно возникающие обмороки, вследствие желудочковых аритмий, появляющихся на пике боли.
Причиной ишемии миокарда в данном случае является не повышенная его потребность в кислороде, а просто снижение доставки кислорода к сердечной мышце.
Диагностика ишемической болезни сердца
Диагностирование ИБС включает в себя анамнез, данные физикального обследования (описанные выше), а также дополнительные методы исследования:
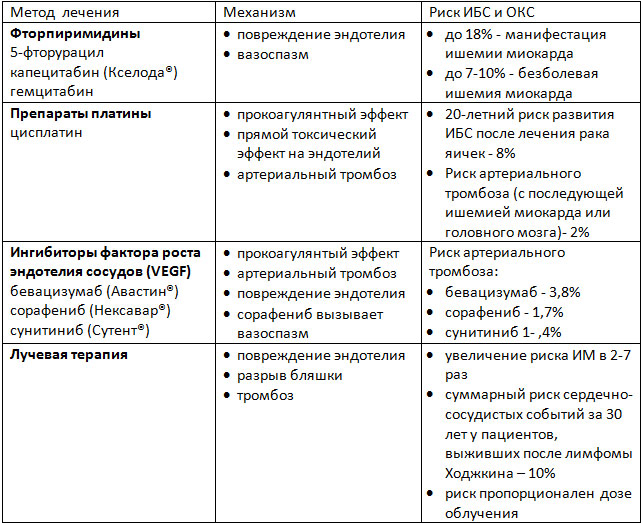
- ЭКГ – является одним из главных диагностических методов, одним из первых отражает происходящие во время приступа изменения в миокарде: возможно нарушение ритма и проводимости. В неясных диагностических случаях проводится суточное мониторирование ЭКГ (холтеровское).
- Лабораторные исследования – общий анализ крови (нет специфических изменений), биохимический анализ крови (повышение биохимических маркеров некроза миокарда: тропонинов, КФК, миоглобина).
- Нагрузочные пробы – применяются для дифференциальной диагностики клинических форм ИБС между собой, а также ИБС с другими заболеваниями, для определения индивидуальной переносимости физической нагрузки, экспертизы трудоспособности или для оценки эффективности лечения.
Случаи, когда нельзя делать нагрузочные пробы: свежий инфаркт миокарда (менее 7 суток), наличие нестабильной стенокардии, острое нарушение мозгового кровообращения, тромбофлебит, лихорадка или наличие выраженной легочной недостаточности.
Суть данной методики заключается в ступенчатом дозированном увеличении физ. нагрузки, при котором проводится одновременная запись электрокардиограммы и регистрация АД.
Положительной считается проба, при которой появляется типичная боль за грудиной, без изменения на ЭКГ. При возникновении признаков ишемии пробу следует немедленно прекратить.
- Эхокардиографическое исследование – проведение узи сердца, с целью оценки его сократительной способности. Возможно проведение стресс-узи, при котором оценивается подвижность структур и сегментов левого желудочка при увеличении частоты сердечных сокращений: после введения добутамина или физической нагрузке. Применяется для диагностики атипичных форм стенокардий или при невозможности проведения нагрузочных проб.
- Коронарная ангиография – является золотым стандартом диагностики ишемической болезни сердца. Проводится при тяжелых видах стенокардии или выраженной ишемии миокарда.
- Сцинтиграфия – визуализация сердечной мышцы, при которой возможно выявление участков ишемии (при их наличии).
Лечение ИБС

Лечение ишемической болезни сердца является комплексным и может быть как медикаментозным (консервативные и хирургические), так и немедикаментозным.
Немедикаментозное лечение ИБС включают в себя воздействие на факторы риска: устранение неправильного питания, снижение повышенной массы тела, нормализацию физических нагрузок и АД, а также коррекцию нарушений обмена углеводов (сахарный диабет).
Медикаментозное лечение основывается на назначении различных групп препаратов для наиболее полного и комплексного лечения. Выделяют следующие основные группы лекарств:
- Нитраты
- Короткого действия – используются для купирования приступа и не подходят для лечения. К ним относится нитроглицерин, эффект которого наступает уже через несколько минут (от одной до пяти).
- Длительного действия – к ним относятся изосорбид моно- и динитрат, используются для предупреждения возникновения приступов.
- Бета-адреноблокаторы – для уменьшения сократимости миокарда:
- Селективные (блокируют только один вид рецепторов) – метопролол и атенолол.
- Неселективные (блокируют все симпатические рецепторы, которые находятся как в сердце, так и в других органах и тканях) – пропранолол.
- Антиагреганты (аспирин, клопидогрель) – снижают свертываемость крови путем влияния на агрегацию тромбоцитов.
- Статины – симвастатин, нистатин (уменьшают концентрацию холестерина в липопротеидах низкой плотности, то есть воздействуют на факторы риска).
- Метаболические средства – предуктал, повышает доставку кислорода к сердечной мышце.
- Ингибиторы ангиотензинпревращающего фермента (лизиноприл, рамиприл) или блокаторы рецепторов ангиотензина (лозартан, валсартан).
Возможно использование комбинаций данных препаратов.
Оперативное вмешательство
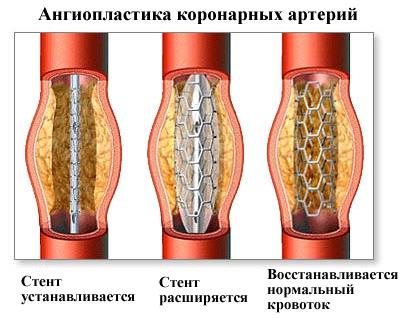
Хирургическое лечение ишемической болезни сердца состоит их двух основных методов: чрескожной транслюминальной коронарной ангиопластики (баллонная дилатация) и коронарного шунтирования.
- Баллонная дилатация является методом выбора при одно- двухсосудистом поражении при нормальной фракции выброса левого желудочка. Под высоким давлением в суженный участок коронарной артерии вводится баллон, который раздувается и фиксируется. Возможна имплантация стента, который предотвращает повторное стенозирование.
- Коронарное шунтирование – операция, при которой создается анастомоз между внутренней грудной артерией или аортой и коронарной артерией ниже места сужений. В результате этого восстанавливается кровоснабжение миокарда. Является методом выбора при двух- или трехсосудистом поражении, снижении фракции выброса левого желудочка менее 45% и при наличии сопутствующей патологии (например, сахарного диабета).
Коронарное шунтирование необходимо применять в следующих случаях:
- сужение левой венечной артерии более чем на 50%;
- ИБС III и IV функциональных классов, которая не поддается активной терапии;
- выраженная ишемия в сочетании с сужением двух и более коронарных артерий.

Осложнения после проведения процедуры делятся на ранние и поздние. К ранним относятся смерть и возникновение инфаркта миокарда. К поздним – повторное возникновение стеноза в коронарных артериях.
Ишемическая болезнь – заболевание грозное, но многие люди не понимают этого и пытаются лечиться самостоятельно, народными средствами. Это может привести к тяжелейшим последствиям, вплоть до смертельного исхода.
Врачи рекомендуют применение народных средств не вместо, а вместе с медицинским лечением или в качестве профилактики при наличии факторов риска. К одним из таких средств относятся боярышник, шиповник, пустырник и гречиха. Вообще, в медицине нельзя заниматься самолечением, особенно при наличии данной патологии, и даже применение народных средств должно быть обсуждено с врачом.
При наличии ишемии сердца, лечение и симптомы заболевания несколько отличаются в зависимости от того, какая клиническая форма у данного больного.
Таким образом, ИБС – опасное заболевание как само по себе, так и по развитию осложнений. При своевременной диагностике и лечении заболевание имеет благоприятный исход. Главное не затягивать с походом к врачу, особенно при наличии симптомов или хотя бы одного из факторов риска.
Читайте также:





