Инновационные методы лечения лимфомы
2020. Gilead заплатила $4.9 млрд за перспективный иммуно-онкологический препарат
Компания Gilead Sciences купила за $4.9 млрд стартап Forty Seven, чьим основным активом является препарат Magrolimab - антитело против раковых клеток. Оно нацелено на рецептор CD47, который позволяет раковым клеткам избежать нападения иммунной системы. В данный момент Magrolimab проходит клинические испытания сразу по нескольким типам рака: неходжкинская лимфома, В-клеточная лимфома, колоректальный рак, рак яичек и мочевого пузыря. Говорят, препарат действительно показывает многообещающие результаты и такая огромная сумма, заплаченная за него - это серьезное подтверждение.
2019. Новая иммунотерапия дает надежду на излечение лимфомы

Исследователи из Центра Маунт-Синай (в Нью-Йорке) под руководством доктора Джошуа Броди (на фото) разработали новый метод иммунотерапии, помогающий остановить развитие особо агрессивного и трудноизлечимого рака крови - неходжкинской лимфомы. Они создали вакцину, которая заставляет иммунные клетки организма (а именно, дендритные клетки) мигрировать к опухолям и помечать их маркерами для других иммунных клеток-убийц (Т-лимфоцитов). Броди говорит, что они вводят вакцину в одну опухоль, а остальные исчезают сами собой. Разработчики испытали вакцину на 11 пациентов с тяжелой формой лимфомы, и у 3 из них произошла значительная ремиссия.
2017. CAR-T иммунотерапия показала высокую эффективность для лечения неходжкинской лимфомы
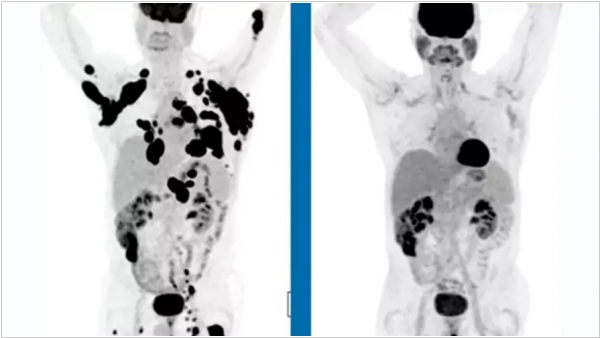
Фармацевтическая компания Kite Pharma обнародовала первые результаты клинических испытаний новой CAR-T иммунотерапии YESCARTA для лечения неходжкинской лимфомы. Новая технология позволяет перепрограммировать собственные иммунные клетки больного лимфомой человека за пределами его организма. Ученые модифицировают клетки, так, чтобы на своей поверхности они несли так называемые химерные антигенные рецепторы. Получившиеся модифицированные клетки начинают сами охотиться на раковые клетки и эффективно разрушать опухоли. В исследовании принимал участие 101 пациент с тремя различными формами лимфомы, причем в тяжелой, терминальной стадии заболевания, когда никакие способы лечения уже не действовали. В отчете говорится, что у трети таких пациентов спустя шесть месяцев наблюдалась полная ремиссия. На фоне успеха клинических испытаний акции компании выросли сразу на 25%. Конкуренты Kite Pharma - Juno Therapeutics и Novartis тоже проводят клинические испытания подобных препаратов.
2015. Ученые разработали гель для лечения лимфомы кожи

Первая фаза клинических исследований продемонстрировала безопасность и эффективность применения геля с резиквимодом (resiquimod) в терапии ранней стадии Т-клеточной лимфомы кожи. Результаты КИ были опубликованы в журнале Blood. В испытаниях экспериментального геля приняли участие 12 пациентов с Т-клеточной лимфомой кожи стадии IA-IIA. В течение 16 недель пациенты использовали гель с резиквимодом (0,03% и 0,06%) для обработки пораженных участков кожи. Согласно полученным результатам, состояние кожного покрова улучшилось у 75% пациентов, а у 30% полностью прошли поражения кожи. Ученые констатировали, что новый гель обладает позитивным профилем безопасности. Резиквимод (R-848) относится к группе имидозолинов и является модулятором иммунного ответа. Препарат обладает противоопухолевой и противовирусной активностью.
2015. В Китае разработали лекарство от лимфомы

Спустя 14 лет с начала разработок в китайская компания ChipScreen Biosciences начала продажи препарата Epidaza, предназначенного для лечения лимфомы – злокачественного новообразования лимфатических узлов. Epidaza стала первым в Китае и четвертым во всем мире препаратом класса селективных ингибиторов для пациентов с Т-клеточной лимфомой. На его исследование и разработку было потрачено $70 млн. ChipScreen Biosciences объявила, что месячный курс лечения Epidaza в Китае будет стоить 26 500 юаней ($4 275), что гораздо меньше стоимости ряда новых онкопрепаратов в США.
2012. Adcetris - первый в мире сертифицированный препарат для лечения лимфомы
Компания Seattle Genetics получила сертификацию FDA на свой препарат Adcetris, предназначенный для лечения злокачественных опухолей – лимфомы Ходжкина и анапластической крупноклеточной лимфомы. Препарат показан к применению взрослым пациентам с рецидивирующей формой этих заболеваний, а также пациентам, которым не помогают традиционные виды лечения. Adcetris направлен на уничтожение раковых клеток, однако, в отличие от стандартной химиотерапии, лекарство не уничтожает здоровые клетки и ткани организма. Adcetris – первый фармакологический препарат для лечения лимфогранулематоза, одобренный FDA с 1977, и вообще первый препарат, непосредственно рекомендованный для лечения анапластической крупноклеточной лимфомы.

Основные варианты лимфом - лимфома Ходжкина и неходжкинские лимфомы. Раньше считалось, что лимфомы и лейкозы являются полностью отдельными заболеваниями. Однако, последние достижения в понимании клеточных маркеров показали, что границы между этими заболеваниями часто размыты.
Представление о том, что опухолевое поражение при лимфоме ограничено лимфатической системой, а при лейкозах - костным мозгом, также не всегда правильно. Соответственно, диагностика и лечение лимфом у лучших Израильских врачей с самого первого этапа является важным, жизне-сохраняющим моментом. Современные методы лечения лимфомы в Израиле методами химиотерапии спасают множество жизней.
Симптомы лимфомы схожи со многими заболеваниями и пациенту сложно заподозрить опасность для его жизни на первых этапах болезни. Больные, как правило, обращаются с жалобами на безболезненное увеличение лимфоузлов или со случайно выявленной при рентгенографии медиастинальной лимфаденопатией. При биопсии лимфоузла выявляются патогномоничные двухъядерные клетки Рид–Штернберга - характерные только для лимофмы Ходжкина.
При применении поли-химиотерапии, иногда в комбинации с лучевой и иммуно-терапией, удается добиться излечения у 70–80% больных.
Симптомами заболевания могут быть лимфаденопатия, лихорадка, ночные поты, потеря веса, кожный зуд, спленомегалия и гепатомегалия. Диагноз ставится на основании данных биопсии лимфатических узлов.
Соотношение пациентов /мужчины:женщины/ составляет 1,4:1. Заболевание редко встречается у детей до 10 лет, чаще всего выявляется в возрасте от 15 до 40 лет; второй пик заболеваемости отмечается у людей старше 50–60 лет.
Причина развития этого заболевания неизвестна, однако определенное значение имеют генетическая предрасположенность и влияние окружающей среды (профессия, в т. ч. работа в деревообрабатывающей промышленности; история воздействия фенитоина, лучевой терапии или химиотерапии; инфицирование вирусом Эпштейна–Барр, Mycobacterium tuberculosis, герпесвирусом 6 типа, ВИЧ).
Риск также повышен у больных с иммуносупрессией (например, пациенты после трансплантации, получающие иммунодепрессанты), у больных с врожденной недостаточностью иммунитета (атаксия-телеангиэктазия, синдром Клайнфельтера, синдром Чедиака–Хигаси, болезнь Вискотта–Олдрича) и с аутоиммунными заболеваниями (ревматоидный артрит, целиакия, синдром Шенгрена, СКВ).
У большинства больных выявляется безболезненное увеличение шейных лимфоузлов. В ряде случаев может возникать болезненность пораженных лимфатических узлов сразу после приема алкогольных напитков, что позволяет установить диагноз на ранних этапах; механизм этого феномена остается неизвестным.
- Рентгеноскопическое исследование органов грудной клетки
- КТ органов грудной клетки, брюшной полости и малого таза
- Общий анализ крови, биохимический анализ крови: щелочная фосфатаза, ЛДГ, показатели функции печени, альбумин, кальций, креатинин
- Биопсия лимфоузла
- ПЭТ для стадирования, МРТ при наличии неврологических симптомов
- Биопсия костного мозга – в отдельных случаях
При классической лимфоме Ходжкина отсутствие признаков заболевания в течение 5 лет после завершения лечения считается излечением от болезни. Рецидив после 5 лет происходит очень редко. При применении химиотерапии с или без лучевой терапии излечение достигается у 70–80% больных.
К факторам высокого риска рецидива относятся мужской пол, возраст > 45 лет, множественные экстранодальные поражения, наличие симптомов интоксикации при диагностике. Больные, не достигшие полной ремиссии или рецидивировавшие в течение первых 12 месяцев после завершения лечения, имеют неблагоприятный прогноз.
Лечение
- Химиотерапия
- Лучевая терапия
- Хирургическое вмешательство
- В отдельных случаях – трансплантация гемопоэтических стволовых клеток
Выбор варианта лечения сложен и в первую очередь зависит от точного определения стадии заболевания. До начала лечения лимфомы в Израиле мужчинам детородного возраста предлагают консервацию спермы, а женщинам – гормональную защиту яичников.
Больные IА, IIА, IВ или IIВ стадиями болезни, как правило, получают режим полихимиотерапии AБВД, включающий доксорубицин (адриамицин), блеомицин, винбластин и дакарбазин в сочетании с лучевой терапией или режимом длительного курса химиотерапии без лучевой терапии. Применение этого варианта лечения приводит к излечиванию до 80% больных. У больных с массивным опухолевым поражением средостения необходимо применение большего числа циклов лечения или более агрессивного режима полихимиотерапии, при этом, как правило, применяется лучевая терапия.
Аутологичная трансплантация гемопоэтических стволовых клеток должна рассматриваться как вариант лечения у всех соматически сохранных больных рецидивами или рефрактерными формами лимфомы Ходжкина, ответившими на терапию 2 линии.

По статистическим данным, лимфома составляет до 5% всех случаев онкологии. Благоприятными условиями для образования лимфомы считаются условия, в которых иммунные клетки человека, а именно лимфоциты, делятся и развиваются бесконтрольно, вследствие чего обретают злокачественный характер. Важно определить лимфомную опухоль как можно раньше, для того, чтобы провести качественное лечение онкологии.
Почему появляется лимфома
Лимфома – это группа онкологических опухолей, которые возникают в следствие бесконтрольного деления клеток лимфоцитарного ряда, которые в результате воздействуют на лимфатические узлы, в некоторых случаях они поражают системы органов, такие как костный мозг, нервную систему и печень. К сожалению, на сегодняшний день в медицине неизвестны точные причины развития лимфомы. Современная медицина, в тандеме с лучшими медиками активно изучают причину развитие и причины возникновения данного заболевания.
Так как причины развития лимфомы до сих пор не изучены, лечение лимфомы является довольно сложным процессом, но тем не менее, мировые онкологи вывели ряд факторов риска, который помогает изучить данный вопрос:
- наследственность является одним из самых первых факторов риска;
- гормональный дисбаланс или нарушения в работе генного аппарата считается также причиной появления лимфомы и увеличивает шанс заболевания в несколько раз;
- инфекционные заболевания, такие как гепатит или герпетические инфекции;
- СПИД и ВИЧ, а также препараты, которые снижают иммунитет, такие как гормоны и противовоспалительные препараты.
На данный момент существует два вида лимфом: Т-лимфоцитарная и В-лимфоцитарная. Если говорить про второй вариант лимфомы, можно с уверенностью сказать, что она поддается активному лечению, в то время как Т-лимфоцитарная онкология почти неизлечима. Сегодня тестируется несколько методов для лечения Т-лимфомы, но пока это новое в лечении онкологии и судить о успешности методов нельзя. Данные заболевания также называют лимфомой Ходжкина и неходжкинская лимфома.
Данное заболевание характерно появлением лимфогранулём - это опухоли, которые локализуются в лимфоузлах и различных систем органов. Заболевание не имеет каких-либо возрастных признаков и встречается у людей любого возраста, однако чаще всего встречается у людей до тридцати и после пятидесяти лет.
Существуют некоторые гистологические варианты заболевания:
- тип, при котором полностью сформированы лимфоциты в области лимфоузлов называется лимфоидным преобладанием;
- случай, при котором в клетках опухоли находят узелки называют нодулярным склерозом;
- если при диагностике в лимфоузлах обнаруживают фибропластические структуры или плазмоциты называют смешанноклеточным;
Для того, чтобы отличить неходжкинскую лимфому от лимфомы Ходжкина стоит обратить внимание на наличие атипических клеток - именно их отсутствие и обозначает данное заболевание. Для того, чтобы проверить наличие клеток следует провести биопсию лимфатического узла. В данном виде онкологии также существует несколько видов:
- виды онкологических образований, которые развиваются медленно и не требуют срочного удаления называют индолентными;
- те, что быстро развиваются и дают метастазы на различные органы называют агрессивными;
- сверх агрессивной опухоли - это те, которые развиваются очень стремительно и распространяют злокачественные клетки по всему организму.
Данное заболевание является очень сложным и пока недостаточно изучено, именно поэтому следует как можно скорее провести диагностику и выявить тип и характер опухоли.
Важно: в связи с пандемией COVID-19
Для предотвращения распространения вируса COVID-19 нам всем необходимо соблюдать определенные меры: поддерживать иммунитет, соблюдать гигиену, а самое главное - оставаться дома и избегать общественных мест.
Лучшие клиники мира доступны для онлайн-консультаций и дистанционного лечения.
Запишитесь на заочный прием к ведущему доктору в любой стране.
Лимфома Ходжкина имени, или, болезнь Ходжкина, является одним из распространенных раковых заболеваний лимфатической системы. Несмотря на то, что болезнь имеет достаточно высокие показатели выздоровления пациентов, она характеризуется частыми рецидивами. Согласно данным нового исследования, новая методика лечения препаратом Brentuximab Vedotin позволяет значительно снизить риск рецидива после проведения пересадки костного мозга.
Автор Елена Левина

Новая методика лечения лимфомы Ходжкина может значительно снизить риск повторного возвращения заболевания после пересадки костного мозга.
Лимфома, или, болезнь Ходжкина, является одним из распространенных раковых заболеваний лимфатической системы. Несмотря на то, что болезнь имеет достаточно высокие показатели выздоровления пациентов, она характеризуется частыми рецидивами. Согласно данным нового исследования, новая методика лечения позволяет значительно снизить риск рецидива после проведения пересадки костного мозга.
Лимфатическая система является частью иммунной системы и состоит из белых кровяных клеток, называемых лимфоцитами, которые помогают защитить организм от инфекций и заболеваний. Патологические процессы начинают развиваться, когда происходит мутационный сбой внутри клеток, и они начинают размножаються бесконтрольно. Все большее число патологических лимфоцитов аккумулируются в скопления раковых клеток, образуя опухоль в лимфатических узлах и других органах тела.
Лимфома Ходжкина может возникнуть в любом возрасте, но чаще всего она встречается у подростков и молодых людей: более трети всех больных - это пациенты в возрасте 15-30. Только в Израиле ежегодно диагностируется около 250 молодых людей с подобным заболеванием. На сегодняшний день большая часть пациентов возвращается к нормальной жизни после проведения лечения, включающего в себя, обычно, пересадку костного мозга.
В зависимости от стадии заболевания, возраста пациента и других сопутствующих факторов, стандартным лечением лимфомы на первом этапе остается комплексное лечение химиотерапией и лучевой терапии. Примерно 85% пациентов удается добиться стойкой ремиссии на долгое время. Тем не менее, несмотря на высокие показатели эффективности лечения, 5-10% пациентов уже на первом этапе не реагируют на лечение, и у примерно 10-30% пациентов болезнь возвращается в той, или иной форме.
Препарат Brentuximab Vedotin, содержащий моноклональное антитело SGN-30 и цитостатик монометила ауристина Е, направлен на уничтожение клеток Ходжкина . Третья фаза клинических испытаний препарата показала, что пациенты, которые получали Brentuximab Vedotin сразу после пересадки костного мозга, имели большую продолжительность жизни без дальнейшего прогрессирования болезни.
Результаты доказывают, что у пациентов с различными факторами риска до трансплантации, которые сразу после пересадки костного мозга получили лечение препаратом Brentuximab Vedotin, отмечено снижение прогрессирования болезни в 43% случаев. Новая терапия является оптимальным вариантом для лечения сложных случаев лимфомы Ходжкина, она снижает риск возвращения заболевания и задерживает ее дальнейшее развитие

Неходжкинская лимфома – большая группа злокачественных заболеваний системы кроветворения, возникающих в результате мутаций ее лимфоидного ростка. Если патологической трансформации подвергаются B-лимфоциты, развивается B-клеточная лимфома, если трансформируются T-лимфоциты, возникает T-клеточная лимфома, а если натуральные киллер-клетки – NK-лимфома. Неходжкинские лимфомы составляют четыре пятых всех лимфом. В девяти случаях из десяти заболевают взрослые люди пожилого возраста.
В каждой из этих групп существует множество подвидов. Например, в группе B-лимфом – наиболее распространенных, составляющих 85% неходжкинских лимфом, различают более 10 различных вариантов. То же относится и к другим видам неходжкинских лимфом.
Столь же разнообразна и клиническая картина заболевания. Лимфома может протекать бурно и агрессивно (при этом она часто хорошо поддается лечению), а может – вяло (индолентно), долго не прогрессируя и даже не требуя лечения, но в то же время эти формы в большинстве своем неизлечимы.
Увеличение лимфоузлов, в первую очередь, подмышечных, паховых, шейных, безболезненное, не исчезающее на фоне антибиотикотерапии и нередко бессимптомное – постоянный признак лимфомы. По расположению и количеству лимфоузлов, вовлеченных в патологический процесс, определяют стадию заболевания.
Симптомы
Среди частых, но необязательных симптомов:
- выраженная общая слабость;
- обильная ночная потливость;
- быстрое и значительное похудение;
- стойкое повышение температуры, иногда более 38 градусов;
- локальные симптомы со стороны органов грудной клетки, брюшной полости, костей как отражение развившихся в них локальных опухолевых очагов.
Таким образом, симптомы неходжкинских лимфом неспецифичны, а формы многочисленны. Поэтому диагностика направлена не только на подтверждение лимфомы как таковой, но и на уточнение ее клинического варианта и стадии, так как от этого зависит тактика ведения пациента. Проводятся:
- клинические анализы крови с микроскопией мазков;
- биохимические анализы крови;
- трепанобиопсия грудины и подвздошных костей для получения образцов костного мозга. Иммунологические, гистохимические и цитогенетические исследования позволяют детально определить все особенности лимфомы у конкретного пациента. Например, мутация B-лимфоцитарного антигена CD-20, ответственного за пролиферацию лимфоцитов, приводит к их неконтролируемому размножению. Если такая мутация выявляется, могут быть назначены таргетные препараты, блокирующие этот ген;
- биопсия лимфоузлов с последующим лабораторным исследованием биоптата;
- компьютерная и магнитно-резонансная томография для первичной диагностики и динамического наблюдения очагов лимфомы в лимфатических узлах и внутренних органах;
- позитронно-эмиссионая компьютерная томография – для раннего выявления метастазов по вновь возникшим очагам аномального метаболизма.
К лечению агрессивных лимфом приступают немедленно по их выявлении, индолентные иногда наблюдают до первых признаков прогрессирования. Современная терапия неходжкинских лимфом включает в разных комбинациях:
- химиотерапию;
- лучевую терапию;
- иммунную терапию;
- трансплантацию костного мозга;
- хирургические методы.
Основу лечения составляет химиотерапия. Как правило, применяются протоколы из нескольких препаратов – полихимиотерапия. Лишь в отдельных случаях у пациентов преклонного возраста с тяжелыми сопутствующими заболеваниями и высокодифференцированными, относительно доброкачественно протекающими лимфомами, может быть проведено лечение единственным средством. Чаще всего применяются схемы из препаратов:
- циклофосфамид, доксорубицин, онковин, преднизолон;
- циклофосфамид, онковин, прокарбазин, преднизолон;
- блеомицин, адриабластин, циклофосфамид, онковин, преднизолон.
Закрепляющая, противорецидивная химиотерапия продолжается после полной нормализации анализов крови и ликвидации клинических проявлений на протяжении двух лет с интервалом в 3 месяца.
Лучевая терапия неходжкинских лимфом назначается ограниченно, в основном для воздействия на крупные локализованные очаги, а также в качестве паллиативной помощи при метастазах в костях.
Хирургические методы применяются индивидуально, в зависимости от локализации очагов лимфомы во внутренних органах и вызванных ими осложнений. Спленэктомия (удаление селезенки) выполняется очень часто, а при первичном ее поражении – практически всегда.
Трансплантация стволовых клеток (пересадка костного мозга) – сложная, но систематически выполняющаяся в иностранных гематологических клиниках процедура. Именно с помощью донорской (а при непораженном костном мозге пациента – и аутогенной) трансплантации там справляются с устойчивыми к химиотерапии, рецидивирующими и особо злокачественными вариантами неходжкинских лимфом. Перед трансплантацией проводится агрессивный курс высокодозной химиотерапии, позволяющий уничтожить практически все злокачественные лимфоидные клетки. Функция крови в дальнейшем восстанавливается благодаря трансплантированному и прижившемуся здоровому костному мозгу.
Трансплантация костного мозга – вмешательство с потенциально высоким риском. В ведущих гематологических центрах мира эти риски удается минимизировать за счет большого опыта и высокой квалификации персонала, регулярно проводящего подобные манипуляции, совершенной методики ее выполнения, а также обеспечения идеальной внешней среды для пациента в критические периоды терапии.
Квалификация специалистов, оснащение гематологических центров и доступность наиболее прогрессивных методов лечения в развитых зарубежных странах позволяют успешно решать наиболее сложные проблемы в лечении неходжкинских лимфом. Это лечение рецидивирующих, распространенных и прогностически неблагоприятных клинических вариантов. Для их преодоления в зарубежных клиниках широко используются иммунотерапия и трансплантация костного мозга, традиционная химиотерапия проводится только оригинальными препаратами. Поэтому полной длительной ремиссии достигают 70-80% пациентов, а 5-летняя выживаемость превышает 90%.
-->| Радиоперехваты круглых столов [8] |
| Радиомагазин-73 [505] |
Войти через uID
Эпидемиология. В связи с выраженной гетерогенностью рассматриваемой группы заболеваний сложно получить достоверные эпидемиологические данные по каждой из нозологических форм.
В целом на долю НЛ приходится около 10—15% от всех онкогематологических заболеваний, заболеваемость — 10,5 случаев на миллион жителей.
НЛ составляют 1/3 среди всех злокачественных заболеваний у детей.
У взрослых НЛ встречаются в любом возрасте.
Этиология
Среди этиологических факторов выделяют:
1) ионизирующее облучение;
2) воздействие различных канцерогенов;
3) вирусные инфекции (вирус Эпштейна—Барра, человеческие Т-лимфотропные вирусы, герпесвирусы 6, 8 и т.д.);
4) физиологическая нестабильность генома;
5) наличие хронической иммунной стимуляции, что может быть связано с развитием иммунодефицита (у больных с инфекцией H.pylory часто развиваются MALT-лимфомы, также имеется повышенный риск развития лимфом у больных хроническим гепатитом С, саркоидозом, аутоиммунными заболеваниями; у ВИЧ-инфицированных наиболее часто развитие лимфом связано с действием вируса Эпшейна-Барра).
Патогенез.
Под действием этиологических факторов клетки иммунной системы могут подвергаться злокачественной трансформации. Лнмфоидные клетки способны озлокачествляться на любом этапе дифференцировки.
При этом они пролиферируют и создают клон клеток с блоком дифференцировки на определенной стадии созревания.
Хромосомные транслокации характерны для гистологических подтипов, вовлекают в патологический процесс различные протоонкогены.
Сущностью транслокаций является реципрокная рекомбинация между двумя специфическими участками хромосом. При этом протоонкоген располагается рядом с гете- рологичными регуляторными последовательностями (чаще всего это регуляторные гены-энхансеры иммуноглобулиновых локусов — V,D,J и С-участков или локусов ТКР). Чаще всего протоонкогены, заинтересованные в транслокациях (C-MYC,PAX-5,PIM-1,BCL2), регулируют клеточный цикл, рост и дифференцировку клеток, апоптоз. Инактивация генов-супрессоров опухолевой прогрессии также имеет место в патогенезе лимфом, при этом чаще всего обнаруживается биаллельная инактивация таких генов, как р53, р16, ATM. Транслокации при лимфомах вовлекают в патогенез множество различных генов.
Хромосомные транслокации, выявляющиеся в случаях лимфом, могут приводить к возникновению опухоли, по меньшей мере, реализовываясь в одном из 4 механизмов:
1) регуляция апоптоза;
2) участие в регуляции клеточного цикла;
3) активация NF-kB;
4) сигнальная трансдукция от В-клеточных рецепторов.
Утрата контроля над пролиферацией, вызванная нарушением регуляции экспрессии с—muc или другими аналогичными последствиями транслокаций хромосомного материала, открывает путь к неоплазии, но сама по себе недостаточна для злокачественной трансформации.
Поражение костного мозга при лимфоме (лейкемизация) приводит к развитию недостаточности костномозгового кроветворения с развитием цитопении периферической крови.
Рост опухолевых узлов может нарушать функцию близлежащих органов и вызывать их дисфункцию. Накопление опухолевой массы приводит к общему истощению организма — кахексии.
Классификация НЛ.
Существует множество различных классификаций НЛ.
Рабочая классификация выделяет лимфомы в соответствии со степенью дифференцировки клеток:
1) низкой степени злокачественности, характеризующиеся высоко дифференцированными лимфоцитами;
2) промежуточной степени злокачественности;
3) высокой степени злокачественности, характеризующиеся недифференцированными лимфоидными клетками.
Классификация ВОЗ подразделяет НЛ на В- и Т- клеточные.
В-клеточные лимфомы:
1) В-клеточные лимфомы/лейкемии из клеток-предшественников;
2) зрелоклеточные (периферические) В-НЛ (лимфомы маргинальной зоны) — MALT-лимфома, возникающая из лимфоидных клеток слизистой ЖКТ; нодаль- ные лимфомы маргинальной зоны; селезеночные маргинальные лимфомы;
3) фолликулярные лимфомы;
4) лимфомы мантийной зоны;
5) диффузные крупноклеточные В-лимфомы;
6) лимфома Беркита.
Т-клеточные лимфомы:
1) Т-клеточные лимфомы из клеток-предшествеников;
2) зрелоклеточные (периферические) Т-клеточные НЛ — Т-пролимфоцитарная лимфома; Т-лимфоцитарная лимфома; агрессивная лимфома из NK-клеток (натуральных киллеров);
3) лимфомы кожи (грибовидный микоз, болезнь Сезари) и другие.
Клиническая картина лимфом полиморфна.
В отличие от острых лейкозов злокачественная пролиферация начинается не в костном мозге, а в экстрамедуллярной лимфоидной ткани.
Наиболее часто — в лимфоузлах, однако необходимо помнить о возможности первичного поражения любого органа, где имеет место лимфоидная ткань (кожа, слизистая желудка и кишечника, головной мозг, молочная железа и т.д.).
Лимфому следует заподозрить, когда где-либо появляется плотная опухоль, не приносящая больному беспокойства.
Иногда лимфоме сопутствуют признаки интоксикации, аутоиммунной гемолитической анемии, аутоиммунной тромбоцитопении, васкулита с поражением кожи.
Клинические проявления зависят от локализации опухолевой массы: при НЛ с поражением медиастинальных лимфоузлов может развиваться синдром сдавления верхней полой вены, при поражении желудка — тошнота, рвота, боли в эпигастрии и т. д.
Достаточно патогномонична, но не обязательна для лимфопролиферативной опухоли триада признаков: проливные поты, особенно в ночные часы, потеря веса, кожный зуд.
Довольно часто имеет место повышение температуры тела без признаков инфекции.
Иммунологическая недостаточность у больных с лимфомами провоцирует присоединение бактериальных и вирусных инфекций.
Бактериальные агенты чаще всего вызывают развитие острой пневмонии или инфекции мочевыводящих путей.
Среди вирусных инфекций на первом месте стоят герпетические инфекции.
В зависимости от распространения опухолевой массы выделяют 4 стадии в соответствии со шкалой Энн-Арбор:
1 стадия — увеличение одной группы лимфатических узлов;
2 стадия — увеличение двух и более групп лимфатических узлов по одну сторону от диафрагмы;
3 стадия — увеличение двух и более групп лимфатических узлов по обе стороны от диафрагмы;
4 стадия — поражение паренхиматозных органов, в том числе костного мозга.
Диагностика НЛ основывается на гистологическом исследовании субстрата опухоли (лимфоузла, слизистой и т. д.) с использованием иммуногисто-фенотипирования.
Для диагностики необходимо использовать именно гистологический материал, данные цитологической (аспирационной) биопсии непригодны для диагностики.
Для определения стадии НЛ используют пальпаторное исследование периферических лимфоузлов, КТ органов грудной, брюшной полости, малого таза, биопсию костного мозга.
Для выявления факторов риска — b2-микроглобулин.
Таким образом, современная диагностика лимфом представляет собой комплексный процесс, сочетающий сразу несколько методов исследования. Только такой подход может обеспечить точную верификацию диагноза, являющегося основой выбора максимально эффективного лечения для больного.
Периферическая кровь не изменена, если нет поражения костного мозга.
Лейкемизация характеризуется лейкоцитозом за счет опухолевых лимфоидных клеток, в случае лимфоцитарных лимфом — за счет зрелых лимфоцитов, при лимфобластных лимфомах — за счет лимфобластов.
Дифференциальная диагностика:
1.С реактивными лимфоаденопатиями на фоне регионального банального лимфаденита, инфекционного мононуклеоза, краснухи, аденовирусных инфекций, болезни кошачьих царапин, туберкулеза, бруцеллеза, туляремии и т. д. (в неясных случаях назначают антибиотикотерапию с контрольным посешением через 2—4 нед.
В случае исчезновения увеличенных лимфоузлов ставят диагноз реактивной лимфоаденопатии.
При сохранении увеличения лимфоузла — показана биопсия).
2. С болезнью Ходжкина (лимфогранулематозом) — на основании гистологии.
3. С метастазами соллидной опухоли — на основании гистологии.
Для лимфом низкой степени злокачественности используются: выжидательная тактика при отсутствии признаков прогрессии; локальная лучевая терапия при 1 стадии; хлорбутин с преднизолоном; монотерапия флюдарабином; флюдарабин с циклофосфаном; флюдарабин с циклофосфаном и мабтерой; зевалин (ибритумомаб); полихимиотерапия по схемам CHOP (циклофосфан, рубомицин, винкристин, преднизолон), CVP (циклофосфан, винкристин, преднизолон) и др.
Получены первые обнадеживающие результаты терапии рефрактерных или рецидивирующих лимфом низкой степени злокачественности велькейдом с мабтерой, новыми пуриновыми аналогами (FLAMP, 2 CDA).
Для лимфом промежуточной и высокой степени злокачественности — полихимиотерапия по схемам CHOP с/без мабтеры, в зависимости от экспрессии CD20 на злокачественных клетках, и другие схемы ПХТ.
Аутотрансплантация ГСК и аллогенная ТГСК показаны в качестве консолидации ремиссии при лимфомах высокой степени злокачественности 3—4 стадии, особенно при рецидивирующих лимфомах, а также при лимфоме мантийной зоны.
Исходы лечения.
Полная ремиссия: отсутствие признаков лимфомы (100% регресс опухолевой массы), подтвержденное КТ спустя 6 недель после окончания XT.
Частичная ремиссия: уменьшение размеров опухоли более чем на 50% по контрольным очагам (при измерении двух диаметров) при отсутствии появления новых очагов.
Стабилизация заболевания: изменение размеров опухолевых образований (+ или - 25%).
Прогрессирование заболевания: увеличение размеров опухолевых образований более чем на 25%, или появление новых опухолевых очагов несмотря на проводимую терапию.
Рецидив: появление опухолевых образований более 1,5 см после достижения полной ремиссии.
Современное лечение лимфом, базирующееся на точном морфологическом диагнозе, позволяющее продлевать и сохранять жизнь больным, требует слаженной работы многих специалистов, привлечения наукоемких и ресурсоемких технологий и, безусловно, зависит от экономической политики государства в области здравоохранения.
Прогноз.
Индивидуальный прогноз зависит or подварианта лимфомы и возможности проведения адекватного лечения.
10-летняя выживаемость пациентов с лимфомой маргинальной зоны составляет 70%; фолликулярной зоны 60%; анапластической крупноклеточной лимфомой — 60%; диффузной крупноклеточной В-лимфомой, Т-лимфомой кожи, лимфомой Беркита и лимфоцитарной лимфомой — 40-50%; лимфомой мантийной зоны — 10-15%.
Читайте также:

