Индивидуальная терапия в онкологии

Успехи современной клинической онкологии неоспоримы. Все более сложные операции, новые препараты, эффективные методы обезболивания и устранения мучительных симптомов. Мы в нашем блоге достаточно рассказывали о том, как сегодня можно продлить и облегчить жизнь пациентам даже на последних стадиях болезни.
Но, тем не менее, тысячи онкологических больных во всем мире ежедневно узнают, что опухоль, которая вчера поддавалась определенному лечению – сегодня снова растет или дает метастазы. Врачи регулярно оказываются в тупике: все положенные лекарства и методы лечения перепробованы, и эффективных для данного пациента – не осталось.
Однако даже из этого тупика можно найти выход. С развитием генетики и молекулярной биологии в руках онкологов оказался новый способ изучить опухоль, чтобы найти в ней уязвимые места.
Для этого используют молекулярно-генетическое тестирование – определение особенностей ДНК раковых клеток. Метод сложный технически, дорогой, требует специфических знаний от врача.
Исследование занимает 3 недели, стоит от 250 до 670 т.р. В результате врач получает отчет в 30 страниц сложной информации, которой он еще должен уметь воспользоваться. Но пациентам, которые уже было перестали надеяться, это дает дополнительное время жизни.
Сегодня мы хотим рассказать о том, как делается молекулярно-генетическое тестирование, в каких случаях оно может помочь пациенту и какие знания дает врачу.
Мы все – мутанты, это норма. Но некоторые мутации приводят к раку
Для этого все соматические клетки (те, из которых состоит организм), кроме эритроцитов, беспрестанно делятся.
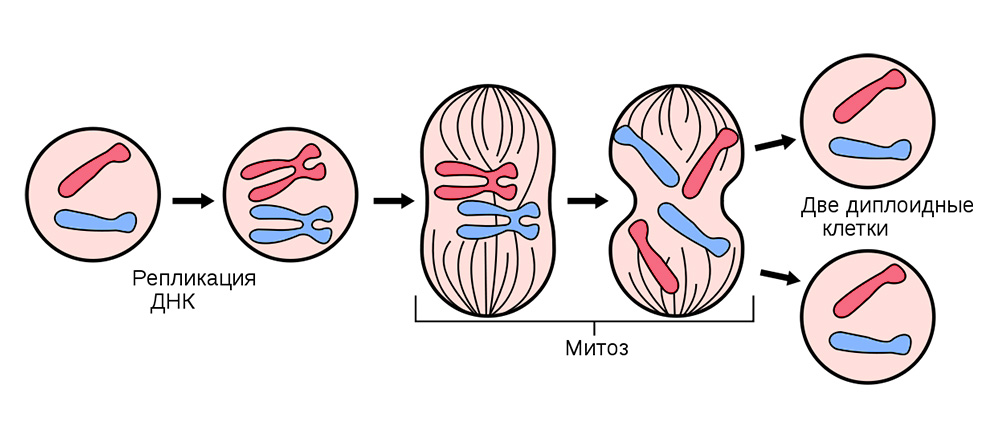
Деление соматических клеток происходит во всех органах и тканях
Иногда в процессе деления получаются сбои – мутации. То нить ДНК порвется, то скопируется с ошибкой, то участки хромосом перемешаются. Влиять на это может сотня факторов: от стресса и табачного дыма до воздействия радиации.
Мутации можно разделить на 4 вида.
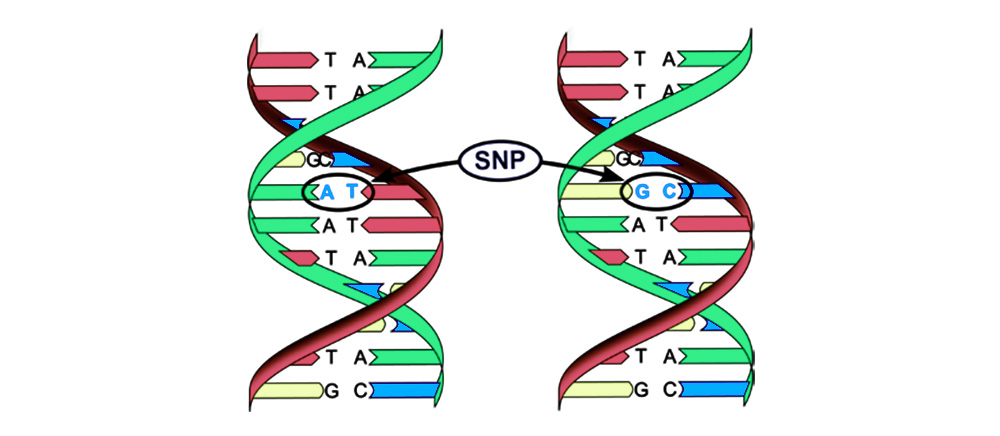
2. Хромосомные аберрации.
Делеция – утрата участка хромосомы. Происходят из-за обрыва концевого участка или разрыва ДНК сразу в двух местах. Всё – этот ген в хромосоме больше не экспрессируется.
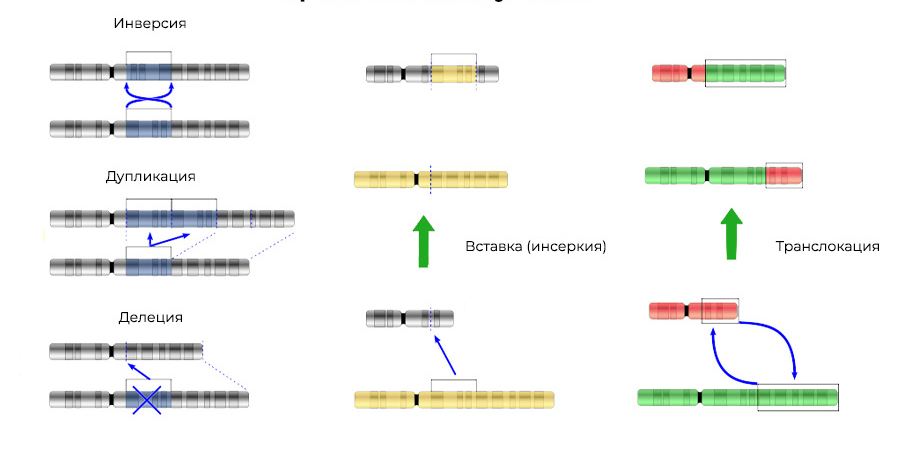
Мутации изменяют не только структуру участка ДНК, но и порядок этих участков
Злокачественную клетку от нормальной отличает нарушение клеточного цикла.
Клеточный цикл (жизнь клетки от деления до деления/гибели) строго регулируется работой специальных белков: киназы, циклины, факторы роста и транскрипционные факторы – в каждой живой клетке их десятки, и у каждого своя узкоспециальная, но важная функция.
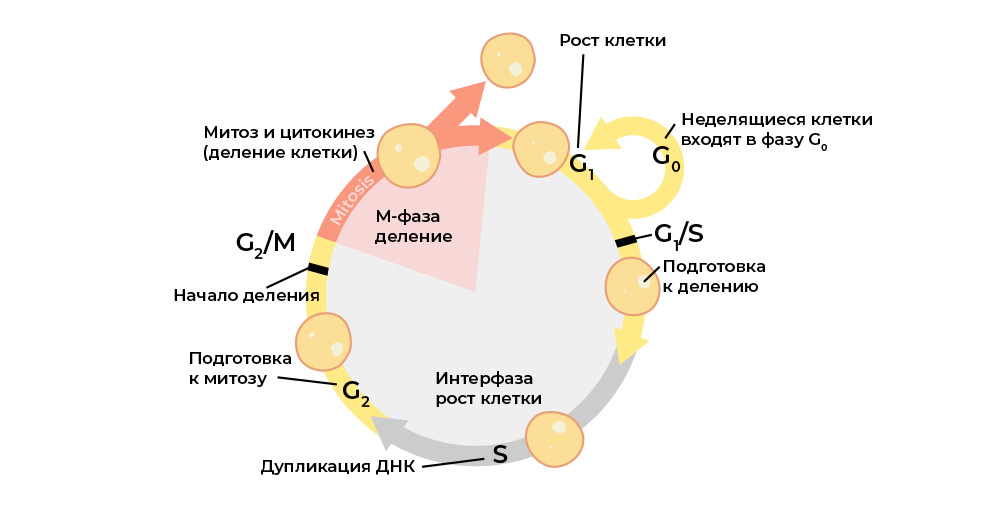
Каждый этап клеточного цикла контролируется белками-регуляторами
Таких значимых генов, изменения в которых могут привести к канцерогенезу (возникновению рака) – две больших группы.
Из тех, что наиболее хорошо изучены и у всех на слуху:
- EGFR, ALK, BRAF – немелкоклеточный рак легкого;
- BRAF – меланома;
- HER2 – рак молочной железы (РМЖ);
- KRAS – колоректальный рак.
Причем, мутации этих генов бывают обнаружены при нескольких видах опухолей. Например, повышенная экспрессия HER2 обнаруживается не только при РМЖ, но и при раке легкого и желудка.
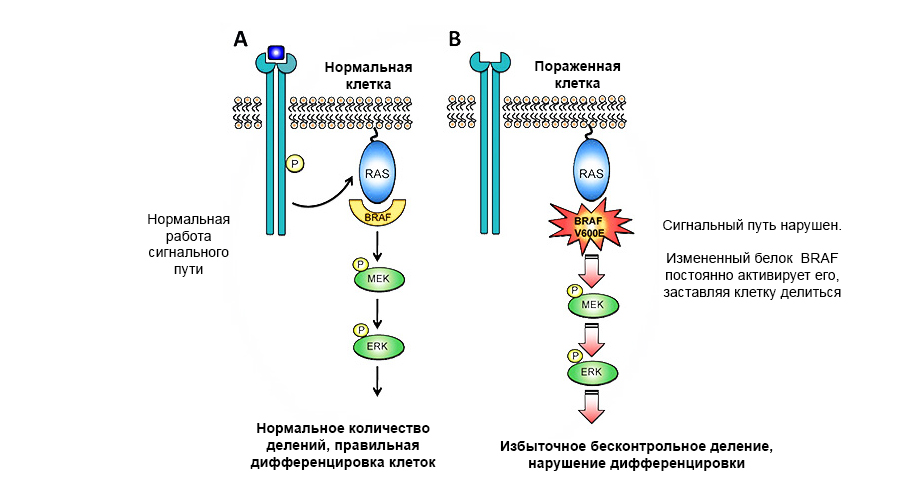
Мутация в протоонкогене белка BRAF приводит к неконтролируемому росту опухоли.
Гены-супрессоры опухоли (антионкогены) – напротив, могут подавить рост опухолевых клеток или участвуют в репарации (починке) поврежденной ДНК. А вот инактивация генов-супрессоров в результате мутации – резко увеличивает вероятность появления злокачественной опухоли.
Всего изучено влияние нескольких десятков протоонкогенов и опухолевых супрессоров на канцерогенез.
Зачем столько сложностей и как они продлевают жизнь пациентам
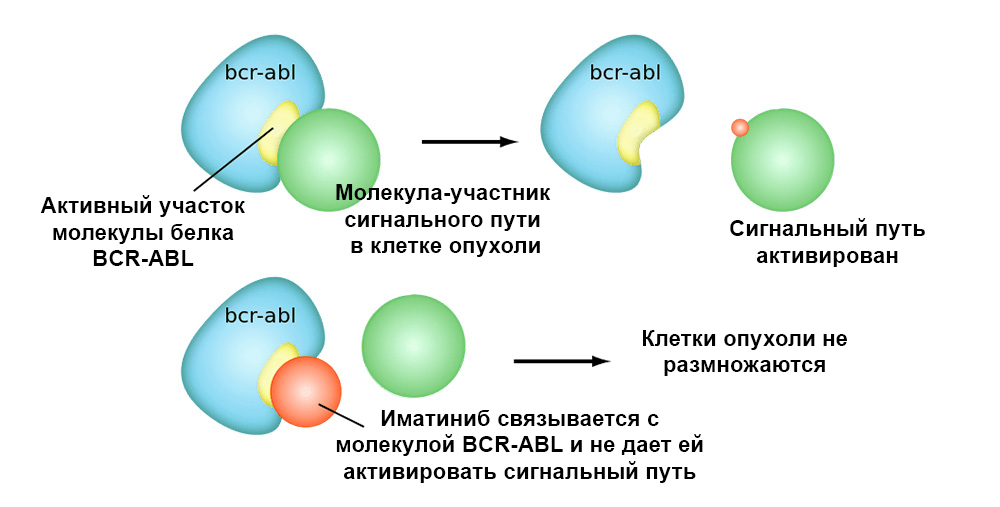
Иматиниб связывается с активным участком молекулы белка BCR-ABL, и блокирует его способность взаимодействовать с остальными молекулами в цепочках сигнальных путей.
Так что таргетные препараты имеют 2 важных преимущества перед классической химиотерапией.
Но и лечение для него должно быть соответствующее – индивидуально подобранное для конкретного пациента – на основе того, что мы определяем мутации в его опухолевых клетках.
В совсем недалеком прошлом злокачественные опухоли можно было классифицировать только по гистологии, то есть в зависимости от того, в каком органе они возникли, и как выглядели раковые клетки под микроскопом.
- узнаем чувствительность опухоли к препаратам;
- выясним, есть ли у опухоли устойчивость к определенным лекарствам;
- обнаружим генетические особенности, которые дают гиперчувствительность к препаратам;
- подберем новое лечение, если опухоль перестала отвечать на стандартную терапию;
обнаружим опухоль/метастаз на очень ранней стадии – по обрывкам ее ДНК в крови; - можем прогнозировать благоприятное или агрессивное течение заболевания.
Образцом выступает чаще всего ткань опухоли, либо взятая во время операции по удалению первичного очага, либо биопсия – микроскопический кусочек опухоли берут специальной тонкой длинной иглой.
Можно поискать ДНК опухолевых клеток в крови – тогда нужна так называемая жидкостная биопсия, две пробирки с кровью по 8,5 мл.
При биопсии мы часто сталкиваемся с тем, что многие пациенты боятся вообще трогать опухоль – опасаются, что ее это спровоцирует на рост. На сегодня не доступны какие-либо исследования, которые бы показали такую взаимосвязь. Конечно, биопсию надо выполнять правильно. У нас чаще всего врачи при заборе биоптата помечают место входа иглы: либо делают маленькую татуировочку (есть и такой инструмент ), либо скобку (хирургическую) ставят. Если потом понадобится операция, они иссекают весь этот ход, где была игла – от кожи до опухоли – так мы делаем шанс распространения раковых клеток за пределы опухоли еще меньше.
Далее образцы отправляются в лабораторию молекулярно-генетически исследований.
Причем применяют сразу несколько методов: секвенирования нового поколения (NGS), секвенирование по Сэнгеру и метод флуоресцентной гибридизации (FISH). Вместе они позволяют прочесть всю последовательность ДНК опухоли, выяснить драйверные мутации – то есть те, которые запустили злокачественный процесс и теперь могут быть мишенью для таргетной терапии – и даже визуализировать весь кариотип (хромосомный набор).
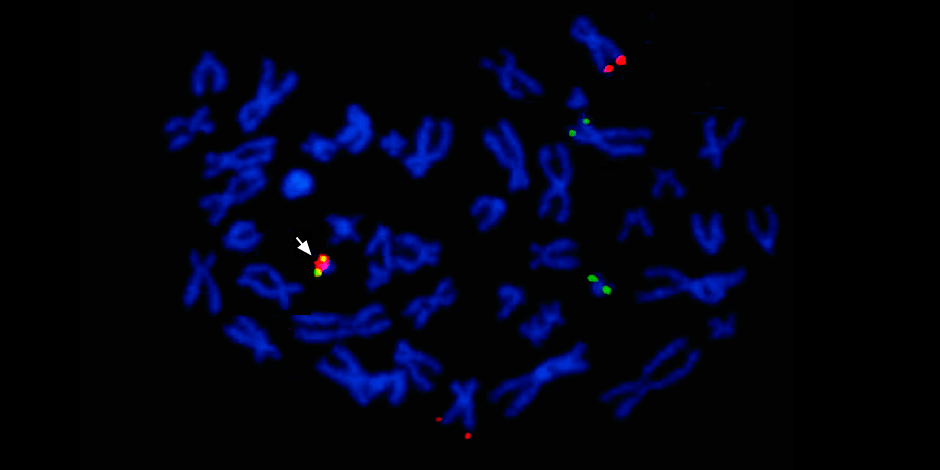
Под стрелкой слева – слияние красного и зеленого сигнала – свидетельство о слияния генетического материала хромосом 9 и 22 с образованием химерной филадельфийской хромосомы.
Кроме того, в полном молекулярно-генетическом исследовании обязательно определяют микросателлитную нестабильность (MSI, microsatellite instability) – нарушение в работе механизма репарации ДНК, которые приводят к быстрому накоплению мутаций в клетках. Этот фактор позволяет делать прогноз по поводу дальнейшего течения заболевания.
После получения молекулярно-генетического профиля опухоли – начинается его анализ
Специальные программы обрабатывают полученные результаты и составляют рекомендации автоматически. Но затем эти рекомендации обязательно вручную курируются командой экспертов. В анализе участвуют генетики, биоинформатики, врачи-онкологи, иммунологи и химиотерапевты. На этом этапе обязательно происходят уточнения и дополнения.
В итоге, в первой части отчета прописаны все найденные мутации в опухоли пациента, и таргетные препараты, которые будут наиболее эффективны в данном случае. Указана таргетная терапия, одобренная для данного типа опухолей с обнаруженными мутациями, и таргетная терапия, которая одобрена для лечения других типов рака с теми же мутациями. У нас в практике были случаи, когда назначались препараты именно второго порядка, off-label – и хорошо действовали.
Далее сотрудники лаборатории проводят огромную работу по мониторингу научных исследований, которые могут быть значимы в случае с данным пациентом.
Во второй части отчета находится обзор существующих на тот момент исследований с подробными данными о частоте встречаемости данной мутации, о действии разных препаратов и о возможности использовать тот или иной вид таргетной терапии при выявленных мутациях. Это помогает составить хотя бы приблизительный прогноз для пациента.
В третьей части отчета собраны актуальные клинические исследования, в которых пациент может принять участие, чтобы получить экспериментальное лечение. Это самый последний запасной способ, но знать о нем все подробности – полезно для спокойствия пациента.

Отчет получается довольно увесистым – 30 страниц захватывающего чтения
В этом случае молекулярно-генетическое исследование и дает нам понимание, какой препарат будет эффективен против данной опухоли, именно с этим набором мутаций. Назначение такого препарата позволяет выиграть главный для онкопациента ресурс – время.
Проблемы методики
Опухоли неоднородны. Они состоят из разных клеток, которые могут отличаться весьма значительно. И, например, в 80% клеток опухоли мутация определенного гена присутствует, а 20% клеток поделились с другим распределением хромосом – и остались немутировавшими. Да, мы назначаем препарат по результатам молекулярно-генетического теста, и против 80% опухолевых клеток он сработает эффективно, но для оставшихся 20% нужно будет придумывать другое лечение.
Некоторые виды рака более-менее гетерогенны, например, РМЖ. А некоторые опухоли, такие как саркомы, напоминают по структуре винегрет. Это затрудняет и диагностику, и лечение: нельзя заранее узнать, в какой части опухоли какие клетки, сколько их видов, как сильно они отличаются. И нельзя, грубо говоря, взять 10 образцов из разных мест опухоли – по ним придется сделать 10 отдельных генетических исследований.
До 30% таргетных и иммунопрепаратов в России назначается без соответствующего обоснования – без исследований генетики опухоли. И часть этих лекарств оказывается пустой тратой средств бюджета и денег пациента, потому что назначать таргетное лечение без понимания генетики опухоли – это рулетка: зарегистрировано более 600 препаратов. Например, для рака молочной железы есть пять протоколов лечения, в зависимости от мутации гена HER2/Neu.
В западной медицине определение генетического профиля опухоли уже становится стандартом лечения. Для российских онкопациентов молекулярно-генетические тестирования – все еще редкий случай, к сожалению – для бюджетной медицины это пока дорого. Но есть надежда, что все изменится к лучшему. Если сейчас оно стоит 600 тыс. руб., то 5 лет назад стоило больше миллиона – технология становится все проще и совершеннее, а, значит, популярнее и доступнее. Здесь время работает на нас.
Поэтому мало просо сделать генетический тест, нужно уметь понять результаты и сделать верные выводы. Мы с коллегами чаще всего сначала изучаем отчет сами (бывает, приходится посидеть над ним дома, в тишине после работы) – а потом еще и собираем консилиум, принимаем коллегиальное решение.
Но хорошие истории пациентов, честно говоря, всегда мотивируют лучше всего.
Сейчас у нас есть пациентка, 48 лет, с рецидивирующей глиобластомой (агрессивная опухоль мозга). К нам она попала после того, как прошла две линии терапии в государственном онкоцентре. Там все делали правильно, проводили лучевую терапию и назначали таргетный препарат, но опухоль все равно вернулась. Женщине отвели полгода жизни.
Мы предложили ей полное молекулярно-генетическое тестирование. Да, оно стоит 600 тыс. рублей, сокращенный вариант, за 250, в ее случае не подошел – нужно было расширенное тестирование, с максимально полным набором мутаций.
Но по результатам обследования назначили ей препарат, который предназначен обычно для лечения немелкоклеточного рака легкого. Он эффективен против опухолей с мутацией EGRF – у нашей пациентки глиобластома была именно с этой мутацией.
Женщина ходит к нам лечиться и наблюдаться уже 4 года. Это в 5 раз дольше, чем при стандартной терапии. Причем, она самостоятельна, живет эти 4 года обычной жизнью, ходит на работу и собирается дождаться внуков.

Врач-онколог разрабатывает программу лечения, исходя из типа, локализации, стадии опухоли, состояния здоровья больного. С пациентом работает команда специалистов, которая может включать онкологов, терапевтов, химиотерапевтов, радиологов, анестезиологов, психоонкологов, реабилитологов, хирургов-онкологов.
В данной статье будут рассмотрены основные методы лечения онкологических заболеваний, мы коротко остановимся на каждом из них и расскажем о важных моментах.
Хирургическое лечение
Во время операции хирург удаляет опухолевую ткань, пораженные близлежащие лимфатические узлы. Цели хирургического лечения могут быть разными:
- Удаление опухоли целиком.
- Удаление части опухоли (циторедуктивные операции). От рака это не излечит, но поможет повысить эффективность химиотерапии и других методов лечения.
Паллиативные операции обычно выполняют на поздних стадиях рака. Они помогают уменьшить боли, частично восстановить функции пораженного органа.
Иногда можно прибегнуть к миниинвазивному лапароскопическому вмешательству, в других случаях приходится делать большой разрез. Это зависит от размеров и локализации опухоли. При больших новообразованиях приходится удалять много тканей или даже целые части тела, например, молочную железу. В дальнейшем восстановить внешность помогают реконструктивно-пластические операции, протезы.
В случаях, когда это возможно, современные хирурги обходятся без скальпеля и прибегают к криохирургии (разрушение новообразования при помощи низкой температуры), лазерной хирургии, фотодинамической терапии (введение в опухоль специального препарата, который делает её чувствительной к свету, с последующим облучением).
Химиотерапия
Химиопрепараты уничтожают быстро делящиеся клетки. Химиотерапия может применяться как самостоятельно, так и в сочетании с другими методами, например, хирургическими вмешательствами, лучевой терапией. Химиотерапия может преследовать разные цели:
- Уменьшить опухоль перед хирургическим вмешательством или курсом лучевой терапии. В данном случае химиотерапия будет называться неоадъювантной.
- Уничтожить раковые клетки, которые остались в организме пациента после операции. Такую химиотерапию называют адъювантной.
- Повысить эффективность других методов лечения рака.
- Предотвратить рецидив после операции, лучевой терапии.
- Облегчить боль и другие симптомы, вызванные опухолью.
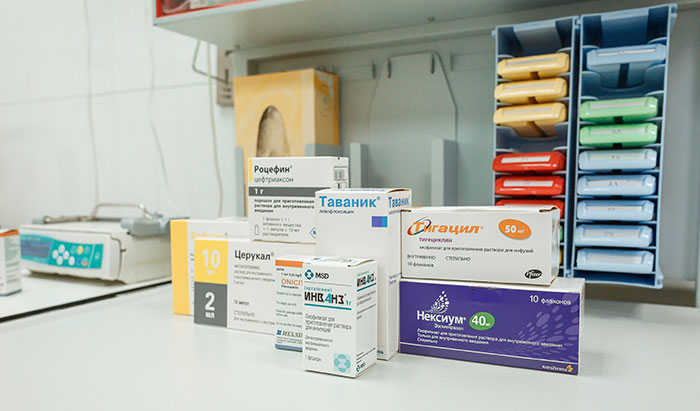
Химиопрепараты применяют в виде таблеток и капсул, внутривенных инъекций, также их могут вводить в организм другими способами.

Лучевая терапия
Лучевая терапия применяет ионизирующее излучение, которое, как и химиопрепараты, уничтожает быстро делящиеся клетки. Её можно использовать как для уничтожения опухоли, так и для облегчения боли и других симптомов.
Существуют две разновидности лучевой терапии:
- При внешнем облучении аппарат находится на расстоянии от пациента и посылает пучок лучей в область тела, где находится опухоль.
- При внутреннем облучении источник излучения вводят в тело пациента. Если источник излучения представляет собой твердый предмет (капсулу или ленту), такой вид лечения называется брахитерапией. В качестве источника излучения может выступать и жидкость, которую вводят внутривенно. Она распространяется по всему организму и уничтожает раковые клетки в разных органах. Такую методику используют, в частности, при раке щитовидной железы.
Лучевую терапию нередко сочетают с хирургическим лечением:
- Перед операцией она помогает уменьшить размеры опухоли.
- Во время операции хирург имеет возможность облучать опухоль непосредственно, так, чтобы лучи не проходили через кожу.
- После операции лучевая терапия помогает уничтожить оставшиеся раковые клетки.

Гормональная терапия
Рост злокачественных опухолей простаты и молочной железы сильно зависит от гормональных эффектов. Если раковые клетки имеют рецепторы к мужским или женским половым гормонам, врач назначит гормональную терапию. Препараты, которые при этом применяются, могут бороться с опухолью двумя путями:
Гормональную терапию очень редко назначают отдельно, чаще всего она дополняет другие виды лечения. Иногда прибегают к хирургическим вмешательствам, во время которых удаляют яичники или яички, чтобы половые гормоны в организме больше не вырабатывались.
Иммунотерапия
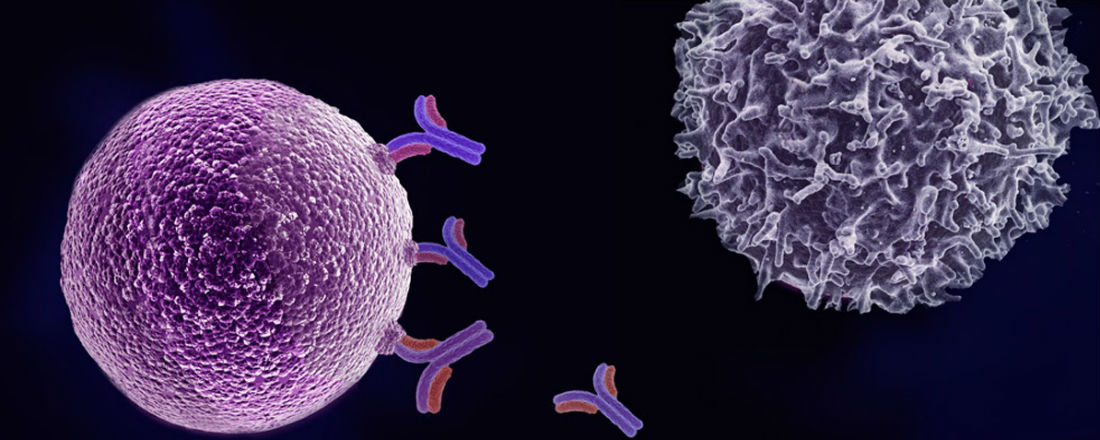
Современные ученые научились редактировать гены в иммунных клетках. У пациента берут Т-лимфоциты, изменяют их гены таким образом, чтобы они могли атаковать опухоль, искусственно размножают новые клетки в пробирке и возвращают в организм.
Таргетная терапия
В последние годы ученые многое узнали о молекулярных механизмах, которые помогают раковым клеткам расти, размножаться, выживать. Новые знания помогли создать новое направление в лечении рака — таргетную терапию. У таргетного препарата всегда есть конкретная цель — специфическая молекула, которая образуется в раковых клетках и нужна для роста, выживания опухоли.
Разные таргетные препараты действуют по-разному:
- работают как препараты для иммунотерапии;
- блокируют молекулярные сигналы, которые заставляют раковые клетки бесконтрольно делиться;
- блокируют молекулярные сигналы, которые нужны для роста новых сосудов и питания опухоли;
- делают клетки опухоли чувствительными к химиопрепаратам, излучению;
- вызывают естественную гибель раковых клеток — апоптоз;
- работают как препараты для гормональной терапии.
Таргетную терапию можно применять как отдельно, так и в сочетании с другими методами лечения.
Генная инженерия в лечении онкологических заболеваний
Несмотря на то, что за последние годы онкология шагнула далеко вперед, перед ней стоит еще много проблем. Даже современные методы лечения не всегда оказываются эффективными. Ученые постоянно ищут новые пути.
Ученые обнаружили, что в лаборатории с помощью CRISPR-Cas можно разрезать любые гены в нужном месте. Был открыт относительно простой, быстрый и недорогой метод редактирования генов. Он нашел применение во многих сферах, в том числе в онкологии. С помощью CRISPR-Cas изучают гены, ответственные за развитие злокачественных опухолей, создают новые лекарственные препараты, модифицируют иммунные клетки таким образом, чтобы они могли распознавать и атаковать раковые клетки. Несколько клинических исследований проводится прямо сейчас.
В 2016 году онкологам из США впервые удалось вылечить женщину от рака молочной железы IV стадии с помощью адаптивной T-клеточной иммунотерапии. 46-летняя Джуди Перкинс перенесла несколько курсов химиотерапии, но лечение оказалось безуспешным, опухоль продолжала прогрессировать, появились метастазы в печени.
В результате у женщины наступила ремиссия. В 2018 году ученые сообщили, что в ее организме вот уже два года не обнаруживаются признаки присутствия злокачественной опухоли. До этого врачи говорили, что Джуди осталось жить не более трех лет.
Лечащему врачу можно и нужно задавать вопросы. Когда пациент хорошо информирован, это идет на пользу лечению. Спросите онколога о том, какие виды лечения вам будут назначены, как будут проходить процедуры, на какой результат можно рассчитывать, какие возможны побочные эффекты, как их предотвратить и как с ними справиться. Врачи Европейской клиники применяют весь арсенал методик, которые на данный момент доступны в России. Мы постоянно следим за инновациями.
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
Что такое иммунотерапия?
Объясните, как это работает?
Откуда вообще взялся этот метод лечения?
Первые попытки вылечить пациентов, больных раком, с помощью иммунотерапии были предприняты более ста лет назад. Одним из родоначальников метода считается хирург Уильям Коли. Он заметил, что у некоторых пациентов с рожистым воспалением (бактериальной кожной инфекцией) онкологическое заболевание полностью регрессировало. Коли предположил, что инфекция стимулирует иммунитет на уничтожение опухолевых клеток, и решил подтвердить свои догадки экспериментально. В 1891 году он ввел стрептококковые бактерии пациенту с саркомой кости и смог добиться сокращения злокачественной опухоли.
Тогда его исследования подверглись активной критике, так как не имели внятного теоретического обоснования. Постепенно накапливались знания о физиологии иммунитета, вместе с этим предпринимались новые попытки активировать собственные защитные силы организма для борьбы со злокачественными опухолями — иммунотерапия получила развитие.
Если иммунотерапия существует так давно, почему о ней активно заговорили только сейчас?
Потому что настоящие прорывы произошли лишь в последние годы. Так, в 2018-м Нобелевскую премию по медицине вручили ученым Джеймсу Эллисону из США и Тасуку Хондзё из Японии за открытие контрольных точек — благодаря этому было создано несколько иммунотерапевтических препаратов. Короткий промежуток между теоретическим открытием и внедрением его результатов в медицинскую практику — еще одна причина того, что о новой методике активно говорят. Иммунотерапия открыла новые возможности для борьбы с онкологическими заболеваниями, которые лечатся с большим трудом, например с меланомой и раком легких. Теперь некоторые такие пациенты могут жить на несколько лет дольше без прогрессирования болезни.
Любой ли рак можно вылечить с помощью иммунотерапии?
Это зависит от препарата и особенностей опухоли. Так, препарат пембролизумаб стал первым, который можно назначать вне зависимости от места возникновения рака, если опухоль имеет специфический биомаркер — микросателлитную нестабильность, или PDL-экспрессию. Иммунотерапию применяют для лечения меланомы, рака легких, почки, желудка, мочевого пузыря, простаты, поджелудочной железы, глиобластомы, лимфомы Ходжкина и еще нескольких видов опухолей. Но пока лучшие результаты терапия показала в лечении меланомы и рака легких. Определить, какое лечение подойдет в конкретном случае, может только лечащий врач.
А побочные эффекты есть?
Есть. Так же как и у других эффективных методов лечения онкологических заболеваний — но они отличаются от нежелательных явлений при химиотерапии: причина их возникновения не токсическое действие самих препаратов, а сильный иммунный ответ. Нередко пациенты на иммунотерапии могут сталкиваться с усталостью, кашлем и тошнотой, теряют аппетит, а на коже может появиться сыпь. Реже эти лекарства могут вызывать более серьезные проблемы в легких, кишечнике, печени, почках и других органах. Обычно так бывает, если иммунитет начинает атаковать не только опухолевые клетки, но и здоровые. Пациенты, которые проходят лучевую терапию, также нередко испытывают усталость, у них могут быть проблемы с кожей, а люди, которые получают химиотерапию, сталкиваются с потерей волос, анемией, тошнотой и рядом других проблем.
Объясните, как проходит лечение. Обязательно ложиться в больницу?
В России этот метод лечения популярен?
Нет. Некоторые препараты, например пембролизумаб, ниволумаб, ипилимумаб и атезолизумаб, зарегистрированы в России. Но о широком доступе к терапии говорить не приходится. Препараты зарегистрированы не по всем показаниям, и во многих ситуациях назначить их можно только офлейбл (не по инструкции), но тогда лечение нельзя будет получить бесплатно по полису ОМС.
16 марта 2020 11:30

Мануэль Руис-Эчарри, онколог:
Еще один новый метод в онкологии — иммунная терапия. Разработке этого вида лекарственного лечения способствовало недавнее раскрытие механизма иммунного ответа при онкологических заболеваниях, за что в 2018 году американец Джеймс Эллисон и японец Тасуку Хондзе получили Нобелевскую премию. Иммунная терапия активизирует собственные защитные силы организма для борьбы со злокачественными клетками. Ее эффективность высока, переносится она удовлетворительно, а побочные эффекты легче, чем у химиотерапии. Иммунотерапевтические препараты стали важной частью противоопухолевого лечения меланомы, рака почки, рака печени, разных подтипов рака легкого, опухолей ЖКТ и других онкозаболеваний. При лимфоме Ходжкина иммунотерапия показывает высокую эффективность даже после трансплантации костного мозга. К сожалению, эффективно применять эту терапию ко всем видам рака невозможно, поскольку иммунная система человека может справиться не со всеми типами опухолей. Поэтому она изначально показана не всем пациентам.

Нидаль Салим, радиационный онколог:
Еще одна область радиационной онкологии — стереотаксическая радиохирургия. Роль скальпеля здесь выполняет пучок радиационных лучей, которые называют гамма- или киберножами. Существует и еще более новое оборудование — аппарат Varian EDGE, отличающийся максимально высокой точностью. Его можно сравнить с острейшим лезвием. Таких установок пока очень мало — единицы во всем мире. Одна из них установлена в EMC.
Дозы облучения при применении стереотаксиса в несколько десятков раз превышают дозы при лучевой терапии, но это позволяет практически избавиться от опухоли или единичных метастазов всего за один-три сеанса. При этом часть клеток может оказаться устойчивой даже к очень высоким дозам облучения, поэтому такая терапия тоже подходит не для всех случаев.

Фото: Saph Photography/Pexels

Алексей Кривошапкин, нейрохирург:
Почему с глиобластомой так трудно бороться? Потому что она развивается чрезвычайно быстро. Если выполняется лишь частичное удаление такой опухоли, операция может подстегнуть ее рост и даже сократить продолжительность жизни пациента. В настоящее время разработанные алгоритмы компьютерного зрения помогают врачам рассчитать риски математически. Благодаря этой возможности выяснилось, что если оставить опухоль после ее хирургического удаления объемом менее 2,5 кубических сантиметров, то больной достоверно проживет дольше. Остаток опухоли большего размера очень быстро перестраивается и превращается в еще более агрессивную опухоль.
Радикальное удаление опухоли — наилучший шанс для больного стать долгожителем среди людей с аналогичным диагнозом. Для максимально полного удаления новообразования нужны современные технологии. Это операционные микроскопы, оснащенные флуоресцентными блоками для определения границ злокачественной опухоли, методы нейронавигации и интраоперационной визуализации (магнитный резонанс, позитронно-эмиссионная томография).
Около двух лет назад специалисты нашей клиники запатентовали новый метод лечения пациентов с рецидивом глиобластомы. Сейчас его начинают применять нейрохирурги Европы и Америки. Суть заключается в том, что после хирургической резекции опухоли в образовавшейся полости размещают мягкий пластиковый баллон, который раздувают в соответствии с границами опухоли. Затем после контроля его позиции с помощью ультразвукового сканирования в баллон вводится источник электронного облучения. Медицинские физики могут быстро и точно рассчитать необходимую лечебную дозу. Этот метод называется баллонная электронная брахитерапия. Он не требует значительного операционного времени, безопасен для больного и медицинского персонала. Метод используется в общей онкологии. Усовершенствование технологии для нейроонкологии и внедрение методики в процесс лечения рецидива глиобластомы в рамках клинического исследования показали впечатляющие результаты, которые дают надежду пациентам на значительную прибавку в продолжительности и качестве жизни после операции.

Владимир Носов, хирург-онкогинеколог:
Среди последних достижений онкогинекологии стоит отметить прогресс онкогенетического тестирования. Большие надежды возлагаются на персонализированную медицину, а также на выявление конкретных молекулярных поломок и таргетную терапию.

Фото: Saph Photography/Pexels
Искра Даскалова, хирург-маммолог:
В последние десятилетия проблема рака молочной железы все реже решается объемным хирургическим вмешательством. Многие пациентки имеют возможность сохранить и грудь, и качество жизни без ухудшения прогноза заболевания. Уже давно доказано, что для пациенток с ранней стадией болезни щадящие (органосохраняющие) операции и последующая лучевая терапия ничем не уступают радикальной мастэктомии. Данные последних лет показывают, что онкологический прогноз у таких пациенток даже лучше.
В радикальном удалении молочной железы нуждаются около 30 процентов заболевших женщин, часто это связано с неблагоприятным соотношением размера груди к размеру опухоли, поскольку удалить новообразование нужно в пределах здоровых тканей. Даже когда речь идет об удалении груди, остаются возможности для последующей реконструкции с хорошими косметическими результатами.
Институт онкологии Европейского медицинского центра EMC — экспертная клиника международного уровня. Здесь пациенты могут получить весь комплекс услуг в одном здании: диагностику, таргетную терапию, иммуно- и химиотерапию, хирургию любой сложности, лучевую терапию, реабилитацию, психологическую поддержку пациента и его семьи. Лечение проводится по современным международным протоколам. Клиника оборудована по последнему слову техники: диагностическое оборудование экспертного уровня, 12 операционных блоков, хирургический робот последнего поколения da Vinci Si HD, отделение ПЭТ/ ОФЭКТ-диагностики с собственной лабораторией по производству радиофармпрепаратов, единственная в России сверхточная система для радиохирургии и лучевой терапии Varian EDGE, система для проведения интраоперационной лучевой терапии. Для каждого пациента разрабатывается индивидуальный план лечения, согласованный несколькими специалистами в области онкологии, радиологии, лучевой терапии, онкохирургии из США, Европы, Израиля и России.
Читайте также:





