Есть ли новые разработки по лечению рака
Однако в последние 10-15 лет невероятными темпами развиваются новые виды антираковой терапии. В мировую медицину пришли современные биотехнологии, благодаря которым на патологический процесс можно воздействовать на уровне генов и молекул. Это открывает перед врачами и пациентами невиданные возможности: вместо массовой терапии больные получили шанс на персонализированное лечение.
Немногие фармацевтические компании в мире вплотную занимаются разработкой и внедрением новых технологий в борьбе с раковыми заболеваниями. В этом списке в основном присутствуют глобальные биофармацевтические концерны, такие как Roche Holding (Швейцария), Bristol-Myers Squibb (США), транснациональная фармкомпания Merck Sharp & Dohme (MSD) (США), англо-шведская фармацевтическая компания AstraZeneca. Единственной отечественной компанией, относящейся к этому списку, стала российская биотехнологическая компания BIOCAD.
Итак, какие новые разработки готова предложить наука для борьбы с раком? Наибольшее внимание ученых и врачей сегодня привлекают препараты на основе моноклональных антител, препараты на основе малых молекул, генная и CAR-T терапия, а также комбинированный подход, использующий все перечисленные методы.
Познакомимся поближе с новыми путями терапии раковых заболеваний, созданными с помощью биотехнологии.

Ученые подумали: а что если пометить раковые клетки произведенными на заводе антителами, чтобы они начали восприниматься как чужеродные и включали защитную реакцию организма, которая их уничтожит так же, как ежедневно уничтожает сотни инфекционных агентов?
Моноклональные антитела избирательно соединяются с чужеродными или сверхпредставленными белками на поверхности клетки опухоли и приводят к ее распознаванию и нацеливанию на нее иммунной системы, тормозят рост опухоли, дополнительно активируют иммунные клетки, маркируют, тормозят рост или маркируют для последующей лучевой терапии. Таргетная (направленная) терапия приводит к значительному повышению эффективности и снижению количества и тяжести побочных реакций.
Механизмов воздействия с помощью моноклональных антител на опухоль множество:
Еще одно направление научных разработок – создание антител, которые способны связываться сразу с двумя мишенями-антигенами. То есть если в одном участке белка раковой клетки была мутация, то антитело все равно свяжется со вторым участком, другими словами – не упустит врага. Это поможет пациентам, нечувствительным к определенным препаратам.
Колоссальный потенциал у биспецифических антител, которые распознают разные антигены (то есть их чувствительность к специфическим клеткам повышается). Они способны использовать эффект синергии нескольких механизмов действия.
Исход болезни зависит во многом и оттого, насколько рано она будет выявлена, поэтому необходима регулярная диагностика в соответствии с полом и возрастом. Например, при прохождении диспансеризации шанс на раннее выявление онкологического заболевания будет выше, чем без нее. А при первых признаках неблагополучия, не откладывая, обращайтесь к врачу!
– Есть ли новые методы терапии и какой из них наиболее эффективный?
– Онкология бурно развивается, но она опирается на три основные методики: хирургия, лучевая терапия, системная лекарственная терапия. Первые два метода остаются базой в лечении большинства новообразований на ранних стадиях, так как обладают мощным воздействием на опухоль. Но как только она дает метастазы, за ними уже не может угнаться ни нож хирурга, ни ионизирующий луч. Здесь в дело вступает лекарственное лечение. Потенциально, где бы ни находилась опухолевая клетка, ее должно настигнуть лекарство, попавшее в организм. Вопрос в том, как сделать эту терапию более эффективной и безопасной?
Современная онкология дает шанс на излечение того, что считалось смертельным еще 15-20 лет назад. Если излечения добиться не удается, мы получаем возможность контролировать болезнь в течение многих лет. Появились новые эффективные медицинские технологии: таргетная терапия (использование препаратов, блокирующих определенные пути стимуляции опухолевой клетки) – как в виде малых молекул, проникающих внутрь клетки, так и антител к конкретной мишени на поверхности опухолевой клетки, иммунотерапия (препараты, активирующие собственный иммунитет для борьбы с опухолью). Но пока нет ответа на вопрос: какая из имеющихся методик лучше? Главное – это грамотный врач-онколог, эффективно эти методики применяющий.
Также идут клинические испытания иммунотерапии следующего уровня, разработанной в стенах той же компании, – искусственно модифицированных клеток иммунной системы (CAR-Т клеток), обладающих потрясающей результативностью при лечении некоторых злокачественных опухолей крови.
– Российские врачи и пациенты сталкиваются с проблемой замены зарубежных препаратов на отечественные – более дешевые, но менее эффективные.
– Страна происхождения – не определяющий фактор. Препарат должен быть в первую очередь эффективным! А цена рассматривается как аргумент только при доказанном качестве. Если отечественный препарат произведен с пониманием того, что ему надо будет выдержать конкуренцию по правилам, принятым в развитых странах мира, то этот препарат, скорее всего, будет столь же эффективен и безопасен, как и препараты, произведенные за рубежом. И этому в отечественной науке уже сейчас есть доказательства.
Возможно ли обмануть рак? Ученые уверены, в арсенале организма есть антитела, способные расправиться со смертоносными клетками. Но, если бы все было так просто… Болезнь и сама может обмануть организм, замаскировавшись под здоровые клетки. В результате, частичное или полное отсутствие болевых синдромов позволяет онкозараженным клеткам развиться до неоперабельной стадии. Только в минувшем году онкология забрала юмориста Михаила Задорнова, всемирно известного оперного баритона Дмитрия Хворостовского, американского певца Чарльза Бредли, композитора Владимира Шаинского и еще тысячи людей по всему миру.

Данные о ежегодном росте числа онкобольных шокируют. Согласно статистике, через 15 лет каждый житель планеты будет болен раком. Об этом в интервью Пятому каналу рассказал Юрий Покровский, кандидат медицинских наук.

Самый распространенный вид борьбы с раком — хирургическое вмешательство. Удаление пораженного органа может излечить пациента, если только опухоль не пустила метастазы, тогда грядет череда курсов химиотерапии и постоянное беспокойство — поможет ли…
Открытие, способное уничтожить одну из самых опасных форм онкологии — рак головного мозга, сделали ученые из лондонского Университета Лидса и Института изучения рака. Именно рак мозга убил певицу Жанну Фриске и баритона Дмитрия Хворостовского. Ученые выяснили, что с опухолью могут бороться некоторые типы вирусов. Об этом сообщил журнал Science Translational Medicine. В ходе исследования реовирусов, оказалось, что они способны преодолевать гемато-энцефалический барьер, защищающий мозг позвоночных от микроорганизмов.

Девять онкопациентов получали капельницы с реовирусом, после курса им удалили опухоли хирургическим путем. Ученые исследовали удаленные клетки рака и установили, что вирус смог размножиться и атаковать пораженные клетки, тем самым активировав иммунную систему на борьбу с опухолью. Принцип действия нового метода раскрыл соавтор исследования профессор Алан Мельчер:

Вирус быстро распознал рак, и иммунитет начал свою борьбу с ним. Исследователи полагают, что вирусные капельницы станут хорошим подспорьем в сочетании с другими методами лечения. Идею высоко оценил Евгений Черемушкин, старший научный сотрудник Института клинической онкологии ОНЦ РАМН.


Видео: youtube / New Scientist
Победа над болезнью не всегда позволяет вернуться к прежней жизни. В петербургском онкоцентре постоянно ведется работа по реабилитации пациентов, победивших недуг. Специалисты этого медучреждения изобрели инновационный метод голосового протезирования, который уже называют главным достижением 2017 года. Врачи вернули голос 80 пациентам, пережившим рак гортани, при котором полностью удаляется трахея и человек теряет способность говорить.

Действительно, ученые доказали, что не только банальное курение может вызвать рак, но и, например, увеличение груди, а именно, воздействие силиконового импланта на организм. Злую шутку могут сыграть и лекарства. Так Минздрав предписал указывать на некоторых препаратах для лечения аденомы простаты и облысения, что они могут привести к раку груди у мужчин, так как содержат опасное вещество финастерид. Таких примеров много. Спровоцировать меланому — рак кожи — может агрессивное солнце. Опасность повсюду и надо быть на чеку.

Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
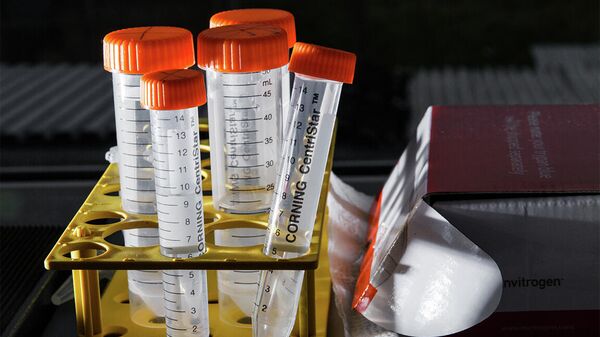
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела

С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела
Из бактерий выделяют генетический материал и расшифровывают
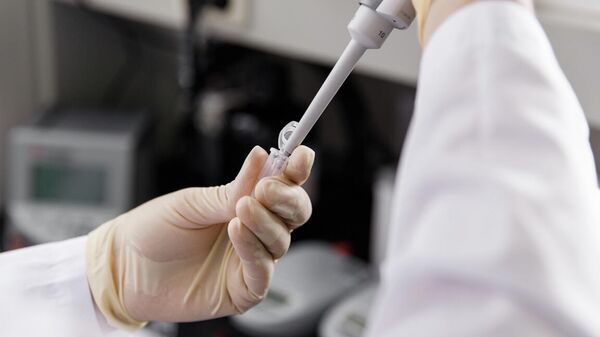
Из бактерий выделяют генетический материал и расшифровывают
Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека

Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела
Из бактерий выделяют генетический материал и расшифровывают
Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека
По данным Минздрава РФ, только в 2018 году в мире было зарегистрировано около 18 миллионов новых случаев рака и других злокачественных новообразований. Всемирная организация здравоохранения (ВОЗ) утверждает, что с онкологическими заболеваниями сталкивается каждый пятый мужчина и каждая шестая женщина.
Новые методы лечения рака позволяют помочь пациентам, которые ранее могли рассчитывать только на паллиативную помощь.
Люди, далекие от медицины и сами врачи связывают терапию онкологических заболеваний с массивными, калечащими операциями, изнуряющей химиотерапией, которая переносится тяжелее, чем сами симптомы болезни, долгим восстановлением и постоянным страхом, что болезнь вернется.
Как развивается рак
Клетки организма размножаются делением и начинают умирать после 50-52 циклов. Процесс естественной гибели называется апоптоз. Зараженные вирусом, мутирующие клетки выставляют на своих оболочках специальные маркеры. Их распознает и немедленно уничтожает иммунная система. Соседние клетки утилизируют продукты распада.
Бесконтрольное размножение приводит к тому, что клетки не успевают созревать, утрачивают свои свойства. Они распространяются в окружающие ткани или мигрируют с кровью, лимфой, образуя метастазы. Канцерогенез - процесс перерождения обычных клеток в атипичные.
Как работает традиционное лечение
Стандартные современные методы лечения рака направлены на уничтожение опухоли различными способами:
- оперативное вмешательство;
- введение химиопрепаратов;
- лучевая или радиотерапия
- иммунотерапия
При хирургическом лечении врач удаляет массив атипичных клеток. К недостаткам метода относят невозможность убедиться на месте, что рак удален в полном объеме, и сложность проведения операции в труднодоступных местах.
Во время химиотерапии пациент получает лекарства, которые нарушают жизнедеятельность, тормозят размножение клеток опухоли или стимулируют их апоптоз. Препараты воздействуют и на здоровые ткани организма, что ухудшает переносимость лечения. У ряда пациентов рак может и не реагировать на стандартные средства.
Радиотерапия борьба с опухолью различными видами излучения. Она повреждает ДНК быстро делящихся клеток, приводя к их гибели. Недостаток метода заключается в невозможности прицельного воздействия только на патологический очаг.
Чтобы стандартное лечение помогло пациенту, необходимо стечение обстоятельств:
- небольшой размер и хорошая доступность первичной опухоли,
- низкая злокачественность и хороший ответ на препараты,
- хорошая переносимость курса терапии.
А как же быть тем, чья история борьбы с раком осложнена отягчающими обстоятельствами? В области онкологии новости лечения связаны с преодолением стандартных проблем терапии:
- нечувствительность рака к препаратам или облучению;
- невозможность воздействия только на клетки опухоли;
- большой объем образования и риск непереносимости терапии;
- риск оставить рак на месте после операции.
Если иммунная система пропускает начало опухолевого процесса, болезнь прогрессирует. Раковые клетки действуют хитростью, маскируя свои рецепторы специальными белками.
Микробиологи изобрели так называемые моноклональные антитела. Это белковые молекулы, имеющие сродство только к определенным рецепторам. Антитела связываются с раковыми клетками, не только делая их видимыми для иммунной системы, но активируя их уничтожение.
Моноклональные антитела созданы для молекул, отвечающих за развитие разных заболеваний. Этот принцип лег в основу таргетной (прицельной) терапии. Например, препарат Ритуксимаб эффективен при лечении B-клеточных лимфом, Цетуксимаб для борьбы с раком толстой и прямой кишки, опухолями головы и шеи. Бевацизумаб применяют при опухоли молочной железы, толстого кишечника, головного мозга и немелкоклеточном раке легких.
Эти медикаменты доступны и в России. Первое время их производством занимались только иностранные компании. Пациенты с нечувствительностью к стандартной химиотерапии могли опасаться, что препарат не придет вовремя или будет стоить дороже. С 2012 года российская компания Biocad производит биоаналоги: Гертикад, Авегра, Ацеллбия.
CAR-T – найти и уничтожить
Универсальный рецептор на поверхности позволяет настраивать иммунитет против разных опухолевых антигенов. T-клетки легко проникают внутрь раковой опухоли. Так CAR-T позволяет уничтожать самые мелкие метастазы в головном и спинном мозге, снижая риск рецидива. Генную терапию считают более эффективной по сравнению с моноклональными антителами.
Достижения иммунной терапии
Среди последних новостей в онкологии – официальное разрешение американской федерации FDA на применение CAR-T в борьбе с B-клеточными лимфомами. Препарат Yescarta - лишь второе такое средство за всю историю генной терапии.
Ученые доказали, что применение моноклональных антител в комплексе с CAR-T – один из самых эффективных методов лечения рака у пациентов с плохой переносимостью и резистентностью к традиционной химиотерапии. Так у пациентки с 4 стадией карциномы молочной железы уменьшился в объеме первичный очаг и его метастазы.
В 2018 году Нобелевская премия за метод лечения рака была присуждена двум ученым Джеймсу Эллисону (США). Их исследования продолжались более 20 лет и привели к открытию белка PD-1 и рецепторов CD152 на лимфоцитах, мешающих иммунитету находить и уничтожать раковые клетки. Затем ученые синтезировали препараты, которые решают эту проблему. В перспективе средства позволят увеличить выживаемость при опухолях различной локализации, в том числе при наличии метастазов.
Эти новые методы лечения рака доступны и в России. Среди зарегистрированных зарубежных препаратов: Китруда, Ервой, Тецентрик.
Диагностика и лечение с помощью света
Фотодинамическая терапия основана на использовании светочувствительных веществ (фотосенсибилизаторов) и лазерной установки. Их молекулы поглощают кванты света, уничтожая раковые клетки и разрушая сосуды, питающие опухоль. Невозможность прицельного воздействия лазера позволяла применять его только для видимых кожных опухолей.
Нижегородские ученые синтезировали флуоресцентный белок, который позволяет обнаруживать клетки опухолей. В 2012 году они получили патент на воспроизведение пептида, уничтожающего рак шейки матки в поле лазера.
Прицельное воздействие на опухоль
Радиотерапия сопряжена с риском получения массивного облучения. Во время лечения повреждаются не только раковые, но и здоровые клетки. К самым сложным локализациям опухоли относят голову и шею ввиду опасности повреждения головного мозга и крупных сосудов. Поражение зрения, слуха неизбежно снижает качество жизни пациента. Кроме того, до ряда опухолей нельзя добраться хирургическим путем.
Уничтожить такой рак помогает стереотаксическая гамма-терапии (или гамма-нож). Лучевые диагносты определяют точную локализацию и размеры образования, после чего в патологический очаг направляют до 200 лучей из разных точек. Единственная процедура занимает несколько часов и дает результат, сопоставимый с 30 сеансами облучения.
Гамма-нож – неинвазивная хирургическая процедура, которая позволяет пациентам возвращаться домой в день ее проведения. В 2019 году в России действует 6 установок, позволяющих помочь 3 тысячам пациентов в год. Новости онкологии в этой области обнадеживают онкобольных перспективами открытия 20 таких центров в стране.
Снизить повреждение окружающих тканей возможно благодаря замене рентгеновского излучения на протонное. Оно лучше концентрируется в очаге. В 2018 году немецкие ученые из Центра им. Гельмгольца Дрезден-Россендорф успешно соединили протонную терапию с МРТ-сканером. Ранее визуализацию опухолей выполняли с помощью компьютерной томографии, на которой хорошо отображаются только неподвижные костные образования. Среди новостей в лучевом лечении рака в 2019 году – создание прибора, позволяющего ввести протонное облучение в клиническую практику.
Экспериментальное лечение рака
Внедрение новых методик терапии возможно благодаря клиническим исследованиям. В ходе экспериментального лечения используются методы, эффективность и безопасность которых полностью не изучена. Онкологи проводят набор пациентов с определенным заболеванием. Они полностью обследуют кандидатов и отсеивают тех, кто не подходит по состоянию здоровья.
Лица, прошедшие скрининг, получают бесплатную экспериментальную терапию. К ней относят:
- генное лечение;
- локальное замораживание тканей;
- точечный нагрев тканей;
- применение бактерий-анаэробов;
- вакцины против рака;
- лечение лазером;
- нанотехнологии.
Участие в клинических исследованиях дает шанс выйти в ремиссию пациентам, которым не помогают стандартные схемы лечения.
Можно ли считать, что экспериментальная терапия позволяет победить рак? Исследователи рассказывают о протоколах с ошеломляющими результатами. Так при испытании препарата Китруда в 2013 году около 76% участников почувствовали облегчение, а полностью излечилось от рака около 20%. Так препарат был включен в схемы лечения различных агрессивных опухолей.
При обнаружении немедленных или отсроченных негативных последствий протоколы закрывают, а средства или методы не допускают до рутинной практики.
С 2018 года работает сервис, позволяющий онкологам России искать больницы, в которых проводят экспериментальную терапию, и направлять туда пациентов. Он создан непосредственно Агентством клинических исследований и Российским онкологическим обществом RUSSCO.
Последние новости в онкологии: что ожидать в 2019 году?
Специалисты в области клинической иммунологии, радиологии, регенеративных технологий из России принимали японских коллег. Трансляция семинара позволила коллегам из 38 регионов получить актуальную информацию о применении новых дендритно-клеточных вакцин от рака, культивировании стволовых клеток с помощью роботов, инженерных методиках.
Кроме того, среди новостей онкологии 2019 года в России - успешное внедрение органосохраняющих операций при раке легких и эндоскопическое удаление новообразования желудка и толстого кишечника.

В 2018 году медики в России выявляли в среднем по 47 000 новых случаев онкологических заболеваний ежемесячно — таковы данные Минздрава, с января по август обнаружено 379 351 новых случаев злокачественных опухолей.
В последние годы данный показатель стабильно рос: если в 2012 году в РФ было зафиксировано около 526 тысяч заболевших раком, то по итогам 2017 года эта цифра составила уже свыше 617 тысяч человек.
Федеральное агентство новостей обратилось в Министерство здравоохранения РФ и в ведущий профильный исследовательский центр, НМИЦ радиологии, с вопросом: когда рак в России перестанет быть непобедимой болезнью? В ответ Минздрав и ученые рассказали о передовых технологиях лечения рака в нашей стране, однако точных дат эксперты не назвали.
Дело в том, что медицина за последнее время изучила десятки тысяч разновидностей злокачественных опухолей. У каждой — своя локализация, сценарии лечения и прогнозы выживаемости — и найти рецепт или изобрести вакцину от всего сразу невозможно. Но ответы все равно получились обнадеживающими. По некоторым из видов рака доля прошедших успешное лечение и вернувшихся к обычной жизни пациентов уже сейчас составляет 99,6%.
Еще пару десятилетий назад в лечении онкологических заболеваний все было относительно просто. Врачи различали виды рака только по органам, в которых он образовался, — например, лечили рак поджелудочной железы, не вдаваясь в подробности, какой вид мутации клеток в какой части органа вызвал опухолевый процесс. Весь спектр способов терапии чаще всего сводился к двум основным: химиотерапии и операции по удалению органа или его части.
Сегодня стало намного легче запутаться: тысячи видов рака, десятки методов воздействия на неправильные клетки, вплоть до редактирования генетического кода, — плюс еще большее количество комбинаций различных технологий, персонифицированных под каждого отдельный случай.
Впрочем, показатель общего числа смертей от рака при этом пока заметно не изменился. Если в 2012 году на 100 тысяч населения России приходился 201 случай смерти от онкологических заболеваний, то в прошлом году он составил в среднем 197,7 летальных исходов на то же число россиян. Получается, что медикам все чаще удается продлевать жизнь больным на несколько лет, но доля полностью выздоровевших пациентов пока ощутимо не выросла.

Протонный ускоритель, гамма-нож и лечение светом
Специалисты не исключают, что в ближайшее время удастся изменить показатели выживаемости и смертности при онкологических заболеваниях. Ведь с учетом современных темпов развития технологий, российская медицина образца января 2018 года уже серьезно отличается даже от нынешнего положения дел.
Важнейшим событием этого года в Минздраве РФ считают открытие в Обнинске Центра высокоточной радиологии Gamma Clinic.
Кроме того, Андрей Каприн отмечает еще одно достижение специалистов на базе Медицинского радиологического центра им. А.Ф. Цыба в Обнинске: там начали применять протонный ускоритель для воздействия на раковые клетки.

Еще одним значимым событием профессор называет начало производства отечественных радиоизотопов на базе одной из разновидностей йода. За эту работу коллектив ученых из НМИЦ радиологии и Физико-энергетического института им. Лейпуновского был удостоен премии правительства РФ в области науки и техники.
Сегодня метод брахитерапии, в котором используются радиоактивные фармпрепараты, применяют на целом ряде злокачественных новообразований: предстательной железы, матки, молочной железы, печени. Впервые в России он начал использоваться и при раке поджелудочной железы.

Кроме того, по словам медика, с помощью протонного ускорителя в России все чаще лечат опухоли головного мозга, легких и молочных желез. Активно развиваются комбинированные и комплексные методы лечения с использованием методик ядерной медицины: это адронная, протонная, нейтронная, радионуклидная терапии.
Российская система здравоохранения берет на вооружение и все последние достижения мировой науки. Одним из по-настоящему прорывных направлений в этой области является таргетная терапия, в том числе с использованием иммунных препаратов.
По мнению Андрея Каприна, проблемы онкозаболеваний нужно решать, объединяя усилия нескольких разнопрофильных специалистов и структур.

Совместно с учеными ИМЕТ РАН и МГУ в НМИЦ радиологии учатся восстанавливать вырезанные вместе с опухолью части органов и тканей, заново отпечатывая на 3D-принтере трехмерные импланты нужных параметров из биоматериалов и насыщая их необходимыми препаратами для лечения и восстановления утраченных функций.
На вопрос о том, когда будет найдено универсальное оружие для победы над раком, все специалисты единогласно отвечают: это невозможно.
Впрочем, по словам представителей ведомства и самих медиков, отсутствие универсального оружия еще не означает, что враг непобедим.
К слову, упомянутая медиком программа предполагает переоснащение около ста региональных учреждений в России для помощи онкобольным, формирование сети протонных центров для развития ядерной медицины, кластеров по подготовке радиохимиков, медицинских физиков, радиофизиков, амбулаторных онкологических служб на межрайонном и межмуниципальном уровнях.
Наиболее перспективной стратегией, по мнению специалистов Минздрава РФ, станет соединение различных подходов к лечению: от таргетной терапии до радиолучевого воздействия, а также персонализация лечения — выявление наиболее эффективных методов воздействия для каждого отдельного пациента.
Если с вектором движения и даже первыми успехами на этом пути в целом уже понятно, то с ответом на вопрос, когда рак больше не будет приговором, все сложнее. Впрочем, и здесь есть ориентиры, которые Министерство здравоохранения обозначило в своем ответе ФАН.
Есть шанс, что статистика следующих пяти лет будет заметно отличаться от нынешней в лучшую сторону. С точки зрения современного развития технологий, 2019 год может ознаменоваться переходом к новой эре оказания медицинской помощи онкобольным: каждый месяц практикующие врачи, ученые, фармацевты, инновационные предприниматели всего мира делают пусть незначительный, но шаг вперед к одной общей цели — победе человечества над раком.
Читайте также:

