Экспериментальные методы лечения рака печени
Новые технологии приходят в Россию.
Приглашаем пациентов принять участие в новых методах лечения онкологических заболеваний, а также в клинических испытаниях препаратов на основе Т-клеток (LAK-терапия). Терапия проводится в различных научно-исследовательских онкологических центрах, в зависимости от вида опухоли.
Отзыв о методе профессора Скворцовой В.И.
Комментарий о клеточных технологиях главного онколога России, академика Давыдова М.И.
Вне зависимости от места локализации злокачественные опухоли метастазируют чаще именно в печень. По статистическим данным метастазы печени встречаются в 20 раз чаще, чем гепатоцеллюларная карцинома (ГПК), холлангиокарцинома. Это обуславливается особенностью кровоснабжения органа — воротной веной и центральными артериями.
В большинстве случаев метастазы печени приходят из первичного очага который находится в желудке или кишечнике. Рак легких, яичников и молочной железы образуют метастазы в печени реже.
Метастазы в печени часто являются свидетельством вторичных поражений лимфатических узлов, костных структур, легких и других органов. В ситуациях распространенного опухолевого процесса рекомендуем пациентам принять участие в экспериментальной терапии заболевания метастазы печени.
Симптомы распространения
При существенной потере веса онкобольные имеют истощённый вид, при этом наблюдается увеличение объема живота. Размеры печени могут оставаться прежними, однако в некоторых случаях увеличивается до такой степени, что в верхних отделах живота возможно увидеть ее контуры.
Появление асцита свидетельствует о том, что брюшная полость также поражена. Необходимо диагностировать пациента на тромбоз воротной вены, который приводит к закрытию просвета вены, что приводит к летальному исходу. Гибель пациента наступает из-за отмирания поджелудочной железы, печени. В срочном порядке необходимо провести восстановление тока крови в обход воротной вены.
В чем заключается опасность метастазов в печени?
Как показывает практика, опасность заключается в том, что метастазы, развиваясь, приносят патологию:
• образование печеночной недостаточности;
• синдром Бадда Киари;
• развитие механической желтухи;
• тромбоз печеночных вен;
• появление портальной гипертензии;
• развитие кровотечений из расширенных вен.
Диагностические процедуры
Диагноз ставится обычно с помощью ПЭТ-, КТ- или МРТ-сканирования, вторичные поражения печени часто выявляют при поиске опухолей в других органах. Портография - один из лучших методов диагностирования опухолей печени, детальное исследование портальных сосудов проводится с помощью добавления контрастного вещества.
Микрометастазы на портограммах возможно увидеть по обеднению сосудистого рисунка в области метастатических образований. С помощью ангиографии можно заметить повреждения сосудистого русла, процедура контролируется на мониторе КТ. При гепатовенографии метастазы печени образуют патологию оттенения контрастного вещества в сегментах печени.
Введение химиопрепаратов в печёночную артерию
Любые опухоли в печени снабжаются кровью, как правило, из печёночной артерии. Лекарственные препараты рекомендуется целенаправленно вводить в опухоль с помощью катетера который устанавливается в печёночную артерию, его вводят сквозь гастродуоденальную артерию. В качестве химиопрепарата чаще применяется флоксуридин, 80-95 % которого всасывается при первичном прохождении сквозь пораженный орган.
Процедуру проводят с применением имплантируемого инфузора на протяжении двух недель. Такая терапия способствует к регрессии новообразования в 18 - 22% пациентов. Проведение исследований позволило установить, что химиоэмболизация приносит значительно больше результатов по сравнению с обычной химиотерапией.
Биоиммунотерапия
Распространение нескольких метастаз в печени является 4 стадией рака. В данном случае уже химиотерапия не приносит результатов, и онкобольного направляют в группу биоиммунотерапии, где возможно усилить действенность воздействия на опухолевые клетки.
• Моноклональные антитела обладают способностью точечно воздействовать на опухоль.
• Дендритная вакцина - необходим материал опухоли онкобольного, в лабораторных условиях дендритные клетки пациента обучают распознавать опухоль, далее обученные вводятся пациенту.
• TIL-технология - выделяют из крови пациента Т-лимфоциты, которые при генетической модификации становятся лекарственным препаратом.
Применение биоиммунотерапии рекомендовано практически при всех формах и стадиях онкологии. Основным достоинством данной методики является минимум побочных действий, что нельзя сказать о побочных действиях химиотерапии или радиотерапии. Специалисты работают над разработкой более новых и эффективных средств иммунотерапии. Получить более подробную информацию о всех группах и препаратах Вы можете, обратившись к нам.
Интраартериальная химиотерапия
Вход в ведущую к печени артерию осуществляют через паховую артерию методом ангиографии. Лекарственный препарат вводится непосредственно в орган раз в 2–3 недели. Возможность постановки в паховую артерию стационарного порт-катетера позволяет избежать необходимости постоянного проведения ангиографии. Это упрощает сеанс интраартериальной химиотерапии.

Радиоэмболизация
Применяется для лечения определенной доли печени. Осуществляется вход в сосуды, отвечающие за кровоснабжение опухоли. Радиоактивное вещество вводится микроинъекциями. Затем проводится КТ- и/или ПЭТ-сканирование. При положительном ответе опухоли на лечение назначается следующий сеанс. Перерыв между сеансами — 1–2 месяца. Основное направление применения метода — лечение метастазов печени.
Хирургический метод
Применяется для лечения молодых пациентов с удовлетворительным состоянием здоровья. При этом 1–4 очага расположены в одной доле органа, что должно подтверждаться результатами КТ-, ПЭТ- и МРТ-сканирования. Удаление пораженной доли печени проводится оперативным вмешательством. Для увеличения здоровой доли печени перед хирургической операцией используется эмболизация портальной вены.
Химиоэмболизация
Сначала выполняется вход в сосуды, снабжающие злокачественное новообразование кровью. С помощью микроинъекций в них вводится химиотерапевтический препарат. Перекрывается кровоснабжение опухоли и обеспечивается пролонгированный эффект инраартериальной химиотерапии. Для лучшего связывания химиотерапевтического лекарства с опухолевыми клетками к нему добавляется lipiodol. Методика высокоэффективна при лечении метастазов в печени.

Тотальное облучение
Тотальную лучевую терапию задействуют при множественном метастазировании. При такой процедуре облучается весь объем данного органа. Как правило, общая дозировка равняется 24 Греям за 10-12 фракций либо же 30 Греям за 12-15 фракций.
Далеко не каждый радиолог возьмется за такую процедуру, превышение указанных норм может привести к лучевому гепатиту. При сдавливании печеночных ворот увеличенными лимфоузлами может быть применено локальное облучение. Благодаря подобному облучению можно получить более хороший результат, с меньшим риском побочных эффектов, чем при химиотерапии.
Химиосатурация
Специальными фильтрами перекрываются кровеносные сосуды, исходящие из печени. Затем в орган вводится большая доза Melfalan — высокоэффективного химиотерапевтического препарата.
Блокировка сосудов предупреждает распространение лекарственного средства по всему организму, не допуская его интоксикации. Это дает возможность вводить дозы, превышающие обычные нормы в 50–100 раз. По организму распространяется кровь уже прошедшая очистку естественными фильтрами.
При незначительном количестве вторичных опухолей, при отсутствии нанесения ими существенного вреда жизнедеятельности организма их активность может контролироваться радиотерапией, химиотерапией, чрезкожной абляцией.
Для лечения пациентов с таким диагнозом может применяться химиоэмболяция, радиоэмболяция, интраартериальная химиотерапия. Решение о выборе плана лечения применяется врачом-онкологом совместно со специалистом интервенционной радиологии.
Прогноз по сроку жизни пациента
После того, как были найдены метастазы в печени, продолжительность жизни с применением химиотерапии составляет 12 -18 месяцев. Без лечения продолжительность жизни онкобольного может составить 4 - 8 месяцев.
Часто при низкодифференцированных опухолях и распространенном процессе химиотерапия лишь сокращает жизнь пациента. Некоторые больные добиваются значительного продления жизни, обратившись к экспериментальной терапии, которая проводится в ведущих НИИ РФ.
Для подбора эффективного метода лечения вы можете обратиться за
- методы инновационной терапии;
- возможности участия в экспериментальной терапии;
- как получить квоту на бесплатное лечение в онкоцентр;
- организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Рак печени — злокачественное новообразование с летальным исходом, занимающее 5 место по распространенности среди мужчин и 8 среди женщин. В большинстве случаев заболевание диагностируют на запущенных стадиях, сопровождающихся циррозом. В развитых странах у приблизительно 30% населения выявляют относительно благоприятную гепатоцеллюлярную карциному.
У таких больных результативно следующее лечение:
- Хирургическая резекция;
- Миниинвазивные методики:
- Химиоэмболизация;
- Радиочастотная (термическая) абляция;
- Микроволновая абляция;
- Радиоэмболизация.
- В ряде случаев показана трансплантация печени. [1]

Гепатоцеллюлярный рак зачастую возникает на фоне цирроза печени
Хирургическая резекция печени
Резекцией печени называется операция по удалению части органа. Она показана в случае необходимости удаления периферического участка печени, его сегментов, долей. Оперативное вмешательство проводится с применением общего наркоза. Выделяют анатомические (типичные) и атипичные (неанатомические) резекции.
Анатомическая резекция подразумевает удаление части печени согласно строению органа. При ней производят перевязку крупных сосудов и протоков в портальных и кавальных вратах органа. Ткань разделяют в пределах малососудистых участков – портальных фиссур. Атипичная резекция — удаление части печени, основанное не на ее анатомии, а на объеме охвата патологическим процессом тканей органа. Во время операции не учитывают особенности строения и направления сосудов, печеночных протоков, не производят предварительную перевязку печеночной ножки. Основным условием оперативного вмешательства является наложение гемостатического (кровоостанавливающего) шва или внутритканевая перевязка печеночных протоков и кровеносных сосудов.
Среди типичных резекций выделяют:
- Правостороннюю или левостороннюю гемигепатэктомию — удаление левой (удаляют 35% ткани органа) или правой (резекция 65% тканей) половины печени;
- Расширенная гемигепатэктомия – гепатэктомия с удалением дополнительных тканей (70% и более);
- Правостороннюю или левостороннюю латеральную лобэктомию – удаление 6,7 сегментов печени справа или 2,3 слева;
- Сегментэктомии (удаление сегмента органа) и би – трисегментэктомии (удаление 2-х и 3-х сегментов соответственно).
Среди атипичных резекций выделяют:
- Краевую;
- Клиновидную;
- Поперечную;
- Сегментарную;
- Долевую.
Трансплантация печени
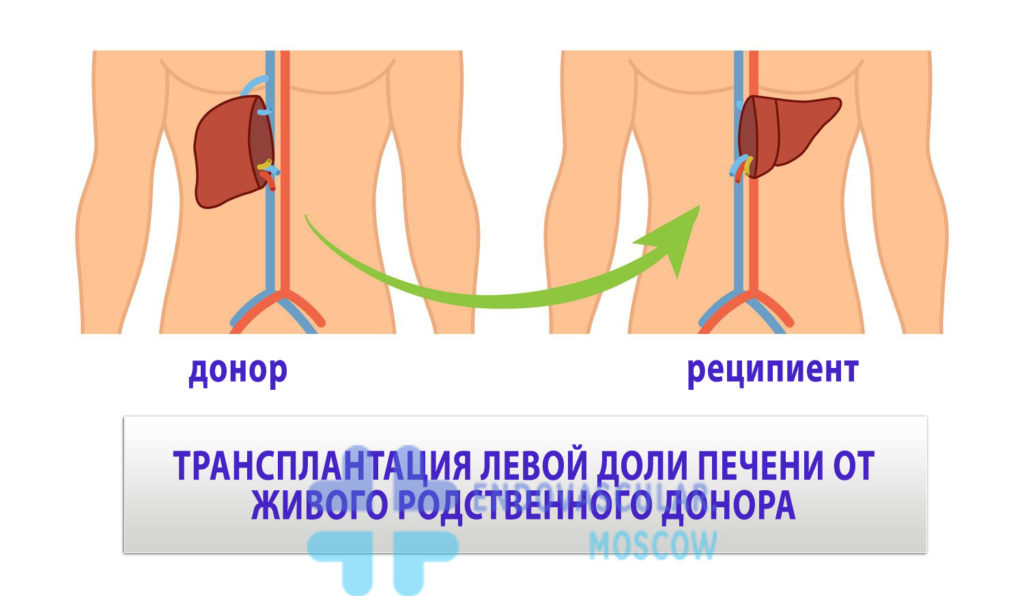
Можно пересадить как печень живого донора, так и мертвого. Связано это с регенераторной способностью печени – с 1 доли может вырасти целый орган. Оптимальной является пересадка органа от родственника (родителя, ребенка, сестры или брата) – т.о. снижается вероятность развития аутоиммунных реакций отторжения организмом трансплантата.
Требования к донорскому органу:
- Совместимость по группе крови и резус-фактору;
- Отсутствие заболеваний и/или повреждений органа;
- Отсутствие заболеваний, передающихся через кровь;
- Удовлетворительное общее состояние донора.
Операция заключается в удалении больного органа с участком полой вены, прекращении кровотока по сосудам, питающим орган, установке шунтов, по которым перекачивается кровь к сердцу из нижней полой вены. После чего пациенту пересаживают целый донорский орган, его долю или ее половину. Далее заново соединяют сосуды и желчные протоки. Средняя длительность операции 7-13 ч. По окончанию процедуры больного переводят минимум на 7 дней в реанимацию. В это время следят за состоянием больного и пересаженного органа, т. к. могут развиться осложнения трансплантации печени:
- отторжение трансплантата
- кровотечение;
- перитонит (воспаление брюшины);
- присоединение инфекции;
- недостаточность пересаженной печени (не функционирует).
Согласно показаниям к трансплантации печени, выдвинутым Калифорнийским университетом Сан-Франциско (критерии Сан-Франциско) 5-летняя послеоперационная выживаемость больных находится в пределах 50%. Критерии:
- наличие одиночного опухолевого узла чем 8 см суммарно.
Миниинвазивные методики лечения
Является комбинированной методикой терапии гепатоцеллюлярного рака. Представляет собой эмболизацию (закупорку питающей опухоль артерии) специальным средством и локальное введение противоопухолевых препаратов в сам сосуд. После чего в артерию вводят эмболизирующее средство, позволяющее лекарству длительно находиться в области введения, непрерывно воздействовать на опухоль. Эмболизирующим материалом могут быть специальный лекарственно насыщаемые микросферы (гепасферы) HepaSphere, DCBead и др.
Эффект химиоэмболизации основан на:
- одномоментном локальном введении значительного количества противоопухолевого препарата в зону опухоли, отсутствие негативного эффекта на организм в целом;
- резком прекращении притока крови к раковым клеткам, из-за чего они лишаются необходимых питательных веществ и кислорода;
- длительном воздействии препарата на опухоль.
Из-за особенностей кровоснабжения химиопрепарат вводят в саму печеночную артерию – он моментально доставляется к опухолевым клеткам и, что важно, практически не достигает и не повреждает здоровых. После прекращения кровотока по печеночной артерии приток крови к новообразованию прекращается, а кровоток в здоровых тканях обеспечивается через воротную (портальную) вену. Химиоэмболизация может быть выполнена бесплатно даже в ведущих государственных центрах Москвы.
Операция проводится в операционной, оснащенной рентгенологическим оборудованием, позволяющим визуализировать новообразование и питающие его сосуды. Перед вмешательством для защиты почек, больному назначают Аллопуринол, антибиотики (предупреждение инфекций), противорвотные средства и анальгетики. В большинстве ситуаций операцию проводят под местным обезболиванием. Спинальная или общая анестезия применяется по исключительным показаниям.
Перед операцией микросферы для химиоэмболизации наыщаются химиопрепаратом, в основном доксорубицином. Обычно используется насыщение 37,5 мг доксорубицина на 1мл микросфер.
Хирург делает кожный разрез 0,6*0,5 см или прокалывает кожные покровы. Под контролем рентген аппарата в бедренную артерию устанавливают катетер, продвигают его к сосудам печени. Затем вводят контрастное вещество и делают первичный контроль – ангиографию. Оценивается кровоснабжение опухоли печени, возможность селективной катетеризации питающей опухоль артерии.
Печень может иметь различные варианты артериального кровоснабжения (10 вариантов по Michels). Самое частое — отхождение какой-либо печеночной артерии от верхней брыжеечной. Поэтому помимо ангиографии чревного ствола (целиакографии) необходимо выполнение ангиографии верхней брыжеечной артерии.
Когда катетер размещен в сосудистом русле печени, по нему к опухоли подается противоопухолевый препарат и эмболизирующее вещество. Затем делается повторный рентген-контроль. После того, как хирург убедился, что новообразование достаточно обработано препаратами катетер извлекают и останавливают кровотечение. На область раны накладывают давящую повязку. Ушивание тканей не проводится.
Процедура длится не более 1,5-2 ч. По окончанию вмешательства больной наблюдается 8-10 ч, затем он может покинуть лечебное учреждение.
Под абляцией подразумевается методика локального разрушения новообразования без необходимости его удаления. К процедуре прибегают в случае наличия нескольких новообразований незначительных размеров, удалить которые невозможно традиционным хирургическим путем. Метод оптимален при наличии образований до 3 см. При больших опухолях (3-5 см) его сочетают с эмболизацией.
Не во всех случаях абляция позволяет излечить опухоль, но для больных с небольшими образованиями коэффициент 5-летней выживаемости приближается к таковому после традиционного хирургического вмешательства. Также абляция применима у пациентов, которым необходима пересадка печени.
Через кожный разрез или прокол под рентгенологическим или УЗИ контролем в новообразование вводят датчик диаметром в 0,5-0,7 мм. Затем делается контроль местонахождения датчика. При правильной установке на него подают электрический ток высокой частоты, под воздействием которого разрушаются белковые структуры опухолевых клеток. После коагуляции необходимого объема тканей делают повторный контроль и извлекают датчик, выполняют гемостаз (остановку кровотечения). На рану накладывают повязку.
После вмешательства пациент находится под наблюдением в течение 8-12 часов. При удовлетворительном состоянии больного его выписывают домой.
Микроволновая абляция — альтернатива оперативному вмешательству. Особенно в тех случаях, когда провести операцию или трансплантацию невозможно. Методика позволяет эффективно бороться с гепатоцеллюлярной карциномой путем точечного воздействия на новообразование, без нанесения вреда здоровым тканям. С ее помощью можно удалять не только одиночные, но и множественные новообразования за короткое время. Время вмешательства в пределах 30-40 мин.
Метод основан на эмболизации специальными микросферами с высоким содержанием радиоактивного материала Итрия-90, который доставляется к опухоли чрезсосудистым путем. Радиоактивное излучение локально влияет на клетки новообразования, которые из-за аномально активного обмена веществ высокочувствительны к излучению.
Радиоэмболизация показана как для лечения первичных форм рака, так и метастатических – из других органов. При гепатоцеллюлярном раке процедура проводится при безрезультативности химиотерапии или при неоперабельной опухоли. По индивидуальным показаниям метод можно использовать как терапию 1-й линии. Также она применима при неприемлемости химиоэмболизации (напр. при тромбозе портальной вены, крупной опухоли и др.).
Доступ к сосудам печени аналогичен таковому при химиоэмболизации. После достижения питающей опухоль артерии вводят радиоактивные микросферы с Итрием-90, выделяющие β-излучение, проникающее в глубину тканей на 1-1,5 см. Т.о. достигается избирательность воздействия на опухолевые клетки.
Радиоэмболизацию проводят двухэтапно, каждый этап занимает 1-1,5 нед. На 1 этапе проводят детальную ангиографию (рентгенологическое исследование сосудов) чтоб узнать их локализацию. Затем по катетеру вводят специальный датчик для определения оптимальной дозы излучения. 1 этап считается подготовительным, моделирующим. На 2 этапе проводят ангиографию, после чего переходят к введению радиоактивного вещества.
Подготовительный этап занимает до 1,5 ч, сама процедура до 2. В течение 5-7 ч радиоактивное вещество покидает организм. Радиоэмболизация не обладает системными побочными эффектами. Пациентов выписывают из стационара через 10-15 ч, после чего им показано амбулаторное лечение.
Печень – это орган с благоприятной анатомией для развития метастаз, ведь в нем проходит огромная портальная вена. Вторичные очаги возникают на фоне злокачественных новообразований в других органах, клетки которых проникают в печень с током крови. К сожалению, своевременно распознать процесс метастазирования практически невозможно, тем более сложно диагностировать рак на ранних этапах развития.
Что такое метастазы в печени?
Метастазы в печени – очаг опухолевой природы, который возникает на фоне переноса патологических клеток с другого пораженного участка. Одна из характерных особенностей злокачественного образования – способность к метастазированию. Именно от количества метастаз зависит продолжительность жизни пациента.
На сегодняшний день рак печени классифицируют по двум группам, в зависимости от первичности образования:
- первичный (опухоль образуется в полости печени);
- вторичный (в печень проникают метастазы от опухоли, прогрессирующей на других органах).

Разновидности метастаз
Основная классификация метастатического процесса основана на пути их распространения. Основными из них являются:
- Гематогенная – распространение метастаз происходит по крови.
- Лимфогенная – пораженные клетки распространяются через лимфу.
- Имплантационная — поражение осуществляется через другие виды жидкостей.
Кроме того, раковые клетки могут передвигваться по организму ортроградно (в направлении естественного кровяного потока) или ретроградно (в обратную сторону тока крови). Метастазы из больного органа перебираются на здоровый, формируя собой новые злокачественные очаги. Так, например, при раке шейки матки, желудка или кишечника необратимый процесс может поразить печень, почки, кости и прочие органы и системы.
Причины возникновения
Метастазы в печени и сопутствующие симптомы развиваются на фоне распространения патологических клеток по кровотоку. Если образование метастаз отдаленное, можно говорить о запущенности заболевания. В этом случае, скорее всего, речь идет о 4 стадии рака, которая не поддается лечению. Независимо от места поражения злокачественным новообразованием, рак ведет себя крайне агрессивно по отношению к организму.
Ежедневно печень пропускает сквозь себя большое количество крови – около 1,5 л за 60 секунд. Порядка 30-35% поступает по артериям, остальное количество – по воротной вене от кишечника.
В полости печени расположены специфические синусоидные капилляры, в которых кровоток замедляется, венозное содержимое соединяется с артериальным, после чего вновь поступает к сердцу по нижней полой вене. Именно такой принцип снабжения печени кровью является наиболее благоприятным для распространения и развития раковых клеток.
Раковые клетки способны путешествовать по всему организму от пораженного участка к здоровым тканям, поражая новые места. Так, метастазирование в печени может возникать на фоне рака следующих органов:
- желудка;
- предстательной железы;
- щитовидки;
- груди;
- поджелудочной железы;
- желчного;
- легких.
Если локализация онкозаболевания отмечается в вышеприведенных органах, с вероятностью в 50% диагностика больного укажет на разрастание метастаз именно в печени. Реже зафиксированы случаи, когда патологические клетки распространяются вследствие рака пищевода или меланом.
Опасность метастазов
Процесс метастазирования негативно отражается на работоспособности органа. Активное распространение метастазов чревато следующими последствиями:
- происходит задержка переработки витаминов и микроэлементов;
- органы не обеспечиваются глюкозой;
![]()
не продуцируются гормоны;- не вырабатываются печеночные ферменты, белки и жиры.
Кроме того метастазы могут поражать позвоночник, приводя к инвалидности. В случае экстренной ситуации может потребоваться срочное вмешательство хирурга.
Симптомы наличия метастаз в печени
На первых порах заболевание может себя никак не проявлять. Сразу могут быть замечены только общая слабость, снижение массы тела, лихорадка. Для постановки диагноза потребуется помощь специалистов. Наиболее характерным проявлением патологического процесса являются:
- болезненность в правом богу под ребрами;
- тошнота, рвотные позывы;
- чувство тяжести в животе;
- желтуха;
- потемнение мочи;
- посветление каловых масс;
- зуд;
- бледность;
- асцит;
- кровотечения.
Но, к сожалению, такие симптомы могут сопровождать и другие печеночные патологии. Поэтому при малейшем подозрении стоит посоветоваться с врачом.
Внимание! Сильная боль в печени – первый сигнал о слишком быстром увеличении опухоли в размерах. В этом случае стоит незамедлительно обратиться к врачу.
Диагностические методы
До того, как лечить метастазы в печени, очень важно точно определить степень рака. Чтобы назначить наиболее результативный способ лечения, медицина предлагает инновационные методы диагностики, а также инструментальные и лабораторные обследования.
Чтобы получить дополнительную информацию, врачи назначают лабораторные методы диагностики, а именно: 
- биохимический и общий анализы крови;
- анализ крови на наличие онкомаркеров.
Общий анализ крови является информативным на ранних этапах болезни. Судить о наличии рака и метастаз можно, если в результатах есть некоторые отклонения:
- количество лейкоцитов выше нормы;
- СОЭ превышает допустимые границы;
- гемоглобин понижен;
- тромбоциты в недостаточном количестве.
Но, поскольку подобные изменения могут быть выявлены в крови и по другим причинам, не стоит делать выводы только по результатам общего анализа крови, необходимы и дополнительные обследования.
Если больному назначен биохимический анализ, указать на рак может повышение мочевины, гамма-глобулина, билирубина, фибриногена. Анализ на онкомаркеры позволяет провести более результативное и правильное обследование, так как раковые клетки продуцируют специфические антигены – белки. Наиболее информативным считается анализ на АФП.
В целях диагностики метастаз и рака больным назначают и инструментальные методы обследований, которые включают в себя:
- УЗИ (ультразвуковое исследование используется для визуализации опухолей в печеночной ткани);
- КТ (рекомендуется для диагностики всех разновидностей рака);
- МРТ (помогает отличить злокачественное образование от доброкачественного, для большей точности может использоваться контрастирование);
- ангиографию (назначается для определения состояния сосудистой системы и кровотока, длительности
![]()
патологических трансформаций).
Также обязательно используется гистология, при которой производится забор измененных тканей для последующего изучения. Процедура может проводиться в виде взятия пункции, малоинвазивным путем, или во время операции.
Лечение метастаз
Метастазирование в печени – проблема, имеющая неблагоприятный прогноз. Многие пациенты уходят из жизни уже спустя год после обнаружения вторичных опухолей. Еще совсем недавно таким больным клиники отказывали в помощи, так как лечение не давало ожидаемого эффекта. Сегодня наиболее часто лечение метастаз в печени производится такими методами:
- химиотерапией;
- лучевой терапией;
- с помощью оперативного вмешательства.
Оперативное лечение метастазирования в печени используется очень широко, выживаемость на протяжении 5 лет составляет от 20 до 45%. Показанием к хирургическому лечению могут быть:
- одиночные метастазы;
- метастазы, которые не поразили сосудистую систему.
Лечение метастаз в печени оперативным путем не проводится в том случае, если есть отдаленные очаги вне органа.
Эта процедура – сочетание эмболизации сосудов с радиотерапией. Целью радиоэмболизации является остановка роста патогенных клеток и их деструкция. Для этого препарат вводится в артерии, которые снабжают злокачественное образование кровью. Именно это не позволяет опухоли питаться, увеличиваться и поражать здоровые органы.
Часто такая методика используется при раке печени, спинного и головного мозга. Несмотря на то, что радиоэмболизация позволяет достичь хорошего эффекта, метод чреват неприятными побочными реакциями – в том числе болевым синдромом, который можно купировать анестезирующим средством.

Для проведения терапии используются особенные свойства рентгеновских лучей, которым под силу проникать через ткани и ликвидировать патогенные клетки. Лучевая терапия может проводиться разными методами, а именно:
- наружным (на новообразование воздействуют аппаратом снаружи тела больного);
- трехмерно-конформным (опухоль обозначается с помощью компьютера, излучение воздействует только на раковые клетки, позволяя избежать облучения здоровых органов и тканей);
- стереотаксическим (на опухоль воздействуют прицельно сфокусированным пучком излучений большой мощности).
Химиотерапия – метод лечения онкологических заболеваний, в ходе которого используются химические вещества и препараты, направленные на удаление атипичных клеток.
Как правило, медикаменты вводятся внутривенно или через катетер, установленный непосредственно в пораженный орган. Также практикуется введение капсулы с препаратом в злокачественное новообразование в ходе операции.
Плюсом такого лечения считается минимальное количество побочных эффектов, направленное действие. В качестве химиопрепарата широко используются:
Таргетное лечение рака позволяет достичь эффекта, схожего с химиотерапевтической методикой, но при этом достаточно принимать препараты в таблетированной форме. Подобная терапия проводится только с цитостатиками, которые повышают результативность процедуры. Достоинством таргетной терапии считается:
- эффективность по отношению к раковым клеткам, которые устойчиво реагируют на химиотерапию;
- препараты не оказывают пагубного воздействия на здоровые клетки, действуют целенаправленно на опухоль, вызывая минимум побочных реакций;
- в сочетании с химиотерапией таргетные препараты повышают эффективность лечения;
Прогнозы на выздоровление
Когда метастазы поразили большую часть органа, не приходится говорить о благоприятном прогнозе, но на ранних этапах скорректировать патологию возможно. Вторичные злокачественные образования опасны, ведь они могут повлечь за собой внутреннее кровотечение, из-за чего положительность прогноза ухудшается.
Продолжительность жизни при метастазах
Как показывает врачебная практика, послеоперационные осложнения составляют от 19 до 43%. Летальный исход случается у 4-7% прооперированных. Если же онкология усугублена другими заболеваниями печени, количество смертей достигает 37%, при условии, что у пациентов без осложнений – всего 2%.
При множественных метастазах без необходимого лечения длительность жизни не превышает полгода. При этом проведение химиотерапии продлевает ее до 9 месяцев.

Продолжительность жизни пациента зависит от стадии, на которой диагностирована проблема. После вмешательства хирурга трехлетняя выживаемость на І этапе метастазирования составляет 73%, на ІІ – 60%, на ІІІ – всего 29%.
Обострение метастазов после проведенной резекции чаще возникает спустя 6-9 месяцев. Прожить без рецидива около 2 лет способны 46% пациентов, 3 года – только 28%.
Паллиативная терапия
Паллиативная терапия при онкологических патологиях используется в том случае, когда противоопухолевое лечение не позволяет достичь ожидаемого эффекта. Лечебные мероприятия помогают улучшить качество жизни пациента и функциональность пораженного органа.
Цель паллиативной терапии – максимально приблизить условия пребывания неизлечимого пациента в больнице к домашней обстановке до момента смерти. При этом специалисты проводят консультации, оказывают психологическую помощь, как умирающему, так и членам его семьи.
Симптомы перед смертью при метастазах в печени
- из-за накопления слизи в верхних дыхательных путях могут беспокоить хрипы, изменяется частота и интенсивность дыхания;
- появляется слабость, сонливость;
- бред, спутанное сознание, галлюцинации;
- судороги;
- пропажа аппетита, проблемы при глотании;
- неконтролируемое мочеиспускание и опорожнение кишечника;
- кожа становится бледной, иногда даже синюшной;
Больные с онкологическими заболеваниями чувствуют приближение неизбежного, надежда на выздоровление угасает. Человек чаще всего ведет лежачий образ жизни, находится без сознания, все время в полудреме, психологически настроен к уходу. Такие люди могут отстраняться от окружающей среды, теряют контроль над своей психикой.

Чтобы облегчить мучения, не стоит отказываться от помощи психолога. Родным нужно максимум своего времени посвятить умирающему члену семьи, пытаться отвлечь его, помочь вспомнить лучшие и положительные моменты из жизни, обеспечить комфортные условия.
Так как в таком состоянии боли очень сильные, врачи назначают обезболивающие препараты, в основном наркотические вещества, которые можно получить строго по рецепту.
От рака сегодня, к сожалению, не застрахован никто. И, несмотря на прогрессивность медицины и фармакологии, вылечиться от этого недуга полностью невозможно. Чтобы избежать необратимых последствий, не стоит забывать о регулярных осмотрах у врача. Только своевременная диагностика и правильная тактика лечения позволят продлить жизнь больного.
Читайте также:



