Эффективность лучевой терапии при рецидиве рака простаты
Повторное развитие онкологической опухоли в предстательной железе у мужчин носит название рецидив рака простаты. Он имеет несколько видов, которые удается распознать по характерной симптоматике. Даже грамотно составленное лечение не всегда помогает предупредить появление рецидива. Вот почему даже после наступления ремиссии пациент должен регулярно посещать онколога и проходить диагностику, чтобы иметь возможность своевременно определить повторное развитие злокачественного новообразования в железистом органе.
Причины рецидива рака простаты

Возвращение к пагубным пристрастиям повышает риск вторичного возникновения недуга
По завершению лечения рака после облучения или радикальной простатэктомии может случиться рецидив заболевания. Об этом должен помнить каждый пациент, которому был поставлен данный диагноз.
Больше всего рискуют столкнуться с повторным развитием раковой опухоли мужчины, которые начали ее лечение на поздних стадиях. К этому моменту по организму расходятся метастазы, которые могут стать предпосылками для рецидива.
Затруднительно избегать такого развития событий пациентам, которые игнорируют рекомендации своего лечащего врача. Нередко мужчины после лечения не пытаются вести здоровый образ жизни, не желают отказываться от вредных привычек. По итогу результат терапии не закрепляется, а организм слабеет.
Специалисты выделяют следующие причины рецидива рака предстательной железы:
- Инфильтрация злокачественных клеток в семенные пузырьки.
- Классификация новообразования, равная 8-10 баллам по Глисону.
- Неполное удаление опухоли.
Повлиять на появление рецидива может выбранный метод лечения рака.
Появления опухоли можно ожидать в послеоперационный период. Это значит, что рак возвращается спустя некоторое время после проведения операции по удалению злокачественного новообразования.
Вероятность возвращения рака после хирургического вмешательства составляет около 53% в первые 10 лет после удаления опухоли.
Несколько лет назад специалисты могли диагностировать опухоль с помощью ректального обследования прямой кишки. Сейчас же для выявления данного процесса применяются современные методики, предусматривающие использование инновационных технологий. Чаще всего послеоперационный рецидив обнаруживается благодаря результатам биопсии. К помощи данной диагностики принято прибегать в случае появления у больного следующих симптомов:
- Учащенные позывы в туалет в ночное время суток.
- Болезненные ощущения в заднем проходе и нижней части живота.
- Боли в области позвоночника.
- Расстройство мочеиспускания.
- Слабая струя во время опорожнения мочевого пузыря.
Наряду с этими симптомами у мужчины уменьшается вес тела без весомых на то причин, появляется хроническая усталость. Это могут быть клинические проявления рецидива рака простаты, с которыми обязательно нужно показаться специалисту.
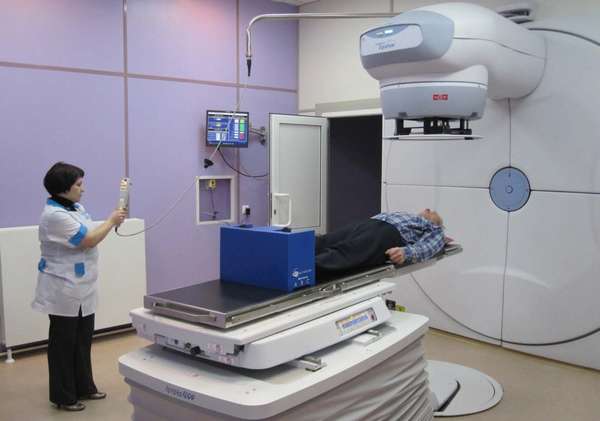
Даже современные методы порой не эффективны
После лучевой терапии вероятность рецидива рака простаты более высока, чем после хирургического вмешательства. Всего существует три основных класса повторного развития новообразования, которые отличаются друг от друга своей локализацией:
- Местный рецидив. Опухоль растет в том месте, в котором происходило облучение пораженных раком тканей. Также она может развиваться в ложе железистого органа.
- Биохимический рецидив. Патология выявляется в ходе повышения уровня ПСА.
- Системный рецидив. Злокачественное новообразование перестает быть локализованным.
Исходя из вышеуказанной информации, можно сделать вывод, что даже правильное лечение не всегда позволяет мужчине справиться с опасным заболеванием и достичь выздоровления.
Основные традиционные методы лечения рака простаты
Рецидив онкологии предстательной железы является опасным состоянием, которое нуждается в своевременной диагностике и правильном лечении. В противном случае повторное развитие злокачественной опухоли может привести к серьезным осложнениям и летальному исходу.
Существует несколько вариантов лечения онкологического новообразования в тканях предстательной железы:
- Оперативное удаление пораженного раковыми клетками органа, в данном случае, простаты.
- Лучевая терапия.
- Химиотерапия для купирования не только новообразования, но и метастазов.
После облучения или другого способа лечения рака должен вестись тщательный контроль над состоянием пациента с онкологией. Это обязательное условие независимо от того, был пройден курс радиотерапии, химиотерапии или совершено оперативное вмешательство. Соблюдение данного требования позволяет своевременно выявить рецидив рака после лучевой или другой терапии.
После лечения рака простаты пациент должен дважды в год проходить обследование в клинике.
Тактика действий после повторного развития злокачественного новообразования зависит от того, как мужчина лечился до этого. Например, если в первый раз онколог назначил больному оперативное вмешательство, то при рецидиве ему предложат пройти курс облучения.
Как лечить рецидив
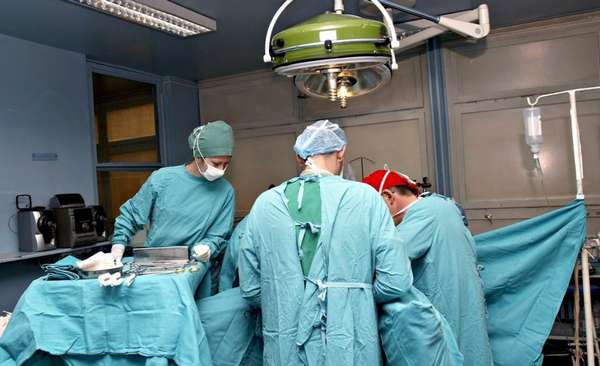
Радикальный метод не всегда нужен и подходит
Современная медицина предлагает несколько методов лечения злокачественной опухоли в предстательной железе. При таком заболевании нередко врачами предлагается оперативное вмешательство, которое позволяет удалить раковое новообразование. Но операция не во всех случаях эффективна, так как после нее в организме больного могут оставаться патогенные клетки.
После проведения лечения злокачественные клетки, оставшиеся в организме, начинают активизироваться и распространяться. Чтобы своевременно выявить данный процесс, требуется регулярно обследоваться у онколога. Лечащий врач изучит картину болезни пациента и предложит ему оптимальный вариант лечения, который, по его мнению, будет иметь благоприятный исход.
Одним из востребованных способов лечения рецидивирующего рака простаты является лучевая терапия. Перед ее проведением пациент должен пройти тщательное обследование всего организма. Имеет смысл предлагать данный вариант терапии лишь в случае, если рак имеет локализованный характер и отсутствуют метастазы. В противном случае он не будет особо полезен больному.
При рецидиве шансы на выздоровление при помощи лучевой терапии ниже, чем при лечении таким методом онкологии при первом проявлении.
Не все раковые клетки поддаются облучению. Часть из них может оставаться в первоначальном состоянии и продолжать распространяться за пределы пораженной предстательной железы. Именно поэтому лучевая терапия не особо эффективна при лечении рецидива онкологического заболевания.

Гормонотерапия является сопутствующим способом борьбы с недугом, а не основным
Гормональная терапия практикуется в клиниках, в которых занимаются лечением онкологических заболеваний. К такому методу прибегают после проведения биохимического курса.
В процессе проведения лечебных мероприятий в организме больного значительно снижается количество тестостерона. Именно этот гормон способствует активному разрастанию злокачественной опухоли.
Онкологи не раз говорили о том, что гормональное лечение не помогает полностью избавиться от рака и его рецидива. Это лишь вспомогательная мера, которая усиливает действие других терапевтических методик, направленных на борьбу со злокачественным новообразованием в предстательной железе.
Химиотерапия обычно назначается больным, у которых биохимический или другой тип рецидива рака простаты после выявления низкой эффективности гормонального лечения. Такие меры требуются в случае, если уровень тестостерона так и не удалось понизить.
Благодаря химиотерапии состояние пациента значительно улучшается за счет облегчения болезненной симптоматики.
Рецидив у мужчины может случиться после полного удаления предстательной железы, которая была поражена раком. В такой ситуации выходом из положения становится HIFU-терапия. Основное действие лечебного метода направлено на разрушение злокачественных клеток путем влияния на них высокосфокусированного ультразвука.
Терапия имеет ряд существенных преимуществ, которые делают данный метод лечения востребованным и эффективным. Она позволяет безболезненно справиться с рецидивирующим раком и при этом не приводит к опасным осложнениям.
Любой из существующих методов борьбы с таким заболеванием, как биохимический или другой рецидив рака предстательной железы, не дает стопроцентную гарантию купирования развития злокачественных процессов в организме мужчины. Результат терапии будет напрямую зависеть от ряда факторов, которые в момент борьбы с опухолью влияют на общее состояние пациента.
Профилактика

При наличии в анамнезе онкологического заболевания посещение пляжа категорически не рекомендовано
Каждый пациент, у которого выявлена склонность к развитию злокачественных новообразований, должен позаботиться о профилактике рака простаты и его рецидива.
Онколог во время ведения пациента должен разъяснить ему необходимость изменения образа жизни. От этого зависит успешность терапии и вероятность последующего развития онкологических опухолей.
Предупредить повторное развитие ракового заболевания у мужчин помогает регулярное соблюдение следующих профилактических мероприятий:
- Нужно отказаться от вредных привычек. В составе никотинового дыма находятся канцерогенные вещества, которые в больших количествах накапливаются в человеческом организме и способствуют развитию раковых опухолей. Не меньший вред мужчинам приносит злоупотребление спиртными напитками. Поэтому пациенты, которые не хотят в будущем столкнуться с раком, должны избавиться от пагубных привычек.
- Составление рациона на основе полезных продуктов питания. Пациентам, которые лечили рак и имеют предпосылки к его повторному развитию, настоятельно рекомендуется выбирать лечебный стол №5. Также для них подходит японская и средиземноморская диета.
- Избегать длительного нахождения под прямыми солнечными лучами. Лучше всего не загорать и по возможности прятать тело под одеждой даже в летний сезон.
- Необходимо избегать сильных нагрузок на область малого таза. Даже малейшая травма может привести к серьезным проблемам со здоровьем.
Мужчинам, которые прошли лечение рака простаты, необходимо продолжать регулярно посещать онколога в целях профилактики. Пренебрежение плановыми осмотрами у специалиста могут иметь неприятные последствия, так как из-за этого можно упустить оптимальный момент для начала борьбы с рецидивом, если он появится.
После того, как мужчина проходит курс лечения ультразвуком или облучением, ему дополнительно назначаются лекарственные препараты, с помощью которых проводится профилактика рецидива злокачественных заболеваний. Соблюдение такой схемы терапии позволяет уменьшить вероятность повторного развития рака на 20-25%.
Прогноз
Продолжительность жизни человека с раком простаты достаточно большая, если проводится адекватная терапия. Процент выживаемости может достигать 95% в случае удаления пораженного онкологией железистого органа.
Отрицательно сказывается на статистике выживаемости после заболевания раком простаты появление его рецидива. Около 15-30% пациентов с таким диагнозом ожидает летальный исход. Вторичная опухоль в 15-20% случаев сокращает жизнь мужчины. С таким заболеванием он может прожить не более 10 лет.
Оперативное удаление опухоли, облучение и химиотерапия не являются 100% гарантией исцеления рака предстательной железы. Благополучный исход определяют ранее выявление онкологии и выраженность злокачественного процесса. Через 5 лет после лечения больше чем у 1/3 пациентов обнаруживается рецидив рака простаты, через 10 лет РПЖ повторно диагностируют у > 50% мужчин. Под рецидивом понимают пальпаторно определяемую опухоль, метастазы и повышение показателей ПСА.
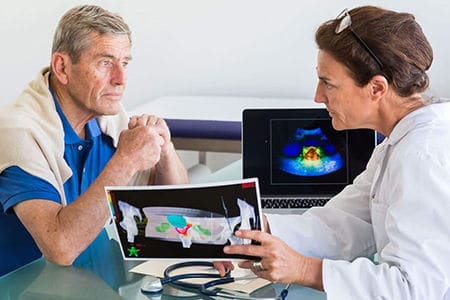
- Этиология и патогенез
- Симптомы и проявления
- Диагностика
- Как проводится лечение
- Прогноз
Этиология и патогенез
Возвращение болезни после операции происходит в результате неполного удаления раковых клеток. Последующие радио- и химиотерапевтические мероприятия по разным причинам оказываются неэффективными. Формируется новая опухоль либо обнаруживаются метастазы. Рецидив рака простаты чаще развивается у пациентов, начавших борьбу с онкологией поздно, на 3–4-й стадиях болезни. В этой ситуации онкологический процесс возобновляет метастатический узел.
Различают два вида рецидива:
- Местный (локальный) – поражает только предстательную железу. Обычно наступает через 2 года после операции. Характеризуется повышением уровня ПСА в 2 раза.
- Системный – в онкологический процесс вовлекаются другие органы. Биохимический рецидив развивается быстро – ПСА за год после РПЭ увеличивается более чем в 2 раза.
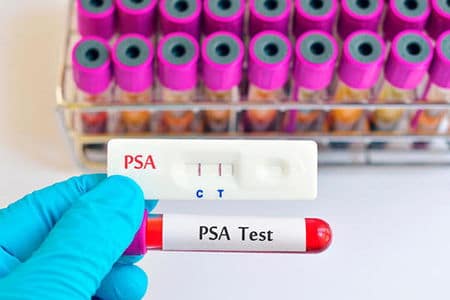
Новая волна злокачественного процесса возникает в результате некорректного либо запоздалого лечения. Возобновить рак может дессеминация организма мутировавшими клетками. Основные причины рецидива.
- неполное удаление опухоли в ходе операции;
- неэффективность лучевой и химиотерапии;
- позднее начало терапии (при 3–4 степени).
Полное излечение от рака простаты возможно при первых двух стадиях при условии своевременного лечения. Риск возвращения онкологии повышает прорастание опухоли в близлежащие органы.
Симптомы и проявления
Начало заболевания проходит незаметно. Первые симптомы местного рецидива возникают по мере роста раковой опухоли и сдавливания ею мочеиспускательного канала. Возникают проблемы с мочеиспусканием, потенцией и эякуляцией. Характерные симптомы:
- ощущение наполненности мочевого пузыря;
- частые позывы, вялая струя урины;
- беспрерывные боли в паху;
- нарушение потенции, ее отсутствие;
- боли при семяизвержении;
- наличие крови в эякуляте;
- эпизодические боли внизу живота.

Задайте вопрос врачу-урологу!

Запущенные стадии характеризуются разрастанием опухоли за границы капсулы железы, поражением окружающих тканей, прогрессивным метастазированием в соседние и отдаленные органы. Далее процесс распространяется на поясничный сегмент позвоночника, кости таза и конечностей. Эта стадия проявляется:
- сильными болями в позвоночнике, тазу;
- появлением неврологических расстройств;
- повышением частоты патологических переломов;
- хронической усталостью и слабостью;
- утратой аппетита, сильным похуданием.

Для инфильтрации опухоли в прямую кишку характерны проблемы с дефекацией (запоры, опорожнения с кровью). Достаточно быстро в злокачественный процесс вовлекаются легкие, печень, почки и головной мозг. Развивается последняя стадия рака, обычно с печальным финалом. Клиника системного рецидива РПЖ зависит от топографии метастазирования:
- в легких – боль в грудине, кашель, кровохаркание;
- печени – боль, увеличение печени, желтизна, отеки;
- почках – боли в пояснице, гематурия, дизурия;
- в мозге – сильные головные боли, тошнота.
Для поздних стадий рецидива рака простаты после РПЭ характерны общее истощение, кахексия с признаками интоксикации (повышение температуры тела, лихорадочное состояние).
Диагностика
После оперативного удаления опухоли и специфического лечения пациенты наблюдаются у уролога-онколога. Контролируется уровень ПСА – маркера карциномы простаты. Предположением на возвращение рака простаты будет повышение результатов выше 0,2 нг/мл. Это является поводом к обследованию. Диагностические мероприятия:
- Ректальный осмотр. Выявляет местный рецидив рака на этапе, когда опухоль разрослась и пальпируется через стенку прямой кишки.
- Опрос и осмотр пациента, выявление жалоб. Выясняется состояние больного: наличие и выраженность болей, потеря в весе.
- Биохимическое тестирование. Анализы крови (общий развернутый, на сахар, ПСА) и мочи.
- Аппаратные методы (ТРУЗИ, МРТ, КТ) – дают возможность определить рецидив на раннем этапе. Томография позволяет обнаружить метастазы.
Проводятся ПЭТ (двухфотонно-эмиссионная томография), сканирование с фтордезоксиглюкозой. Перед исследованием вводится радиофармпрепарат, маркирующий атипичные клетки.
Как проводится лечение
Тактика и длительность лечебных мероприятий рецидива рака простаты после лучевой терапии и операции отличаются и зависят от первичной методики. При недостаточной эффективности облучения назначается химиотерапевтический курс либо альтернативный метод. При местной форме эффективна дистанционная радиотерапия. Системный рак простаты лечат специфическими гормональными препаратами. Новыми эффективными методами лечения рецидива РПЖ являются следующие.
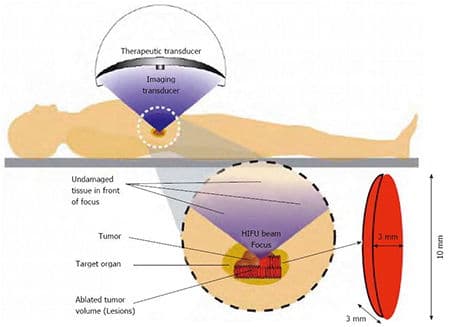
Спасительная (сальважная) HIFU терапия – при местном расположении опухоли у пациентов, перенесших полную простатэктомию. Используется высокоинтенсивный фокусированный ультразвук (High Intensity Focused Ultrasound).
Фотодинамическая терапия (ФДТ) — в/венное, локальное введение фотосенсибилизаторов, безопасных веществ, действующих на пораженный орган световым лучом заданной волны. Включает этапы:
- введение фотосенсибилизирующего препарата (минуты);
- накопление его в тканях-мишенях (дни);
- облучение опухоли лазером через световод (минуты);
- высвобождение токсинов, избирательно уничтожающих атипичные клетки.
Брахитерапия (контактное облучение) — источник излучения находится внутри ткани органа. При возобновлении рака простаты после облучения возможны локальная HIFU- и брахитерапия.
Пациент с диагнозом РПЖ после радикальной простатэктомии периодически обследуется у онколога. Проводится динамичное наблюдение показателей простатического антигена. При рецидиве рака терапевтическая тактика зависит от типа опухоли и характера ее прорастания. Учитываются возраст, иммунный статус, сопуствующие патологии. При биохимическом сигналом возвращения будет повышение уровня ПСА в крови. В этом случае назначается гормонотерапия с целью снижения уровня тестостерона.

Системный рецидив предполагает метастазирование раковых клеток в соседние органы и далее. Поздние стадии имеют выраженную онкологическую клинику. Метод борьбы со злокачественным процессом зависит от клинической ситуации. Мероприятия: химиотерапия, облучение, операция, гормональная терапия, фокусированная УЗ-абляция. Лекарства, назначаемые врачом при раке простаты:
- Золадекс (Гозарлин)— аналог гонадотропин-рилизинг гормона, назначается при гормон-резистентной форме патологии. Снижает уровень ПСА.
- Андрокур (ципротерона ацетат) — антиандроген, кастрационный препарат, осуществляет полную гормональную блокаду. Показания — метастазирующий и неоперабельный рак.
- Флутамид — нестероидный антиандроген. Препятствует усвоению клетками мужских гормонов. Снижает уровень тестостерона и, как следствие, ПСА.
Суть терапии биохимического рецидива РПЖ — нормализация показателей ПСА. Клинические рекомендации при малоэффективности гормональной терапии склоняются к проведению орхиэктомии (удалению тестикул).
Прогноз
Выживаемость пациентов с раком простаты довольно высокая. В среднем 80—90% своевременно оперированных остаются живы через 5 лет. Рецидивы также достаточно часты, 15—30% больным не удается одолеть онкологию. Смертность в течение 10 лет составляет 15—20 %. На статистику выживаемости влияет исходный уровень ПСА: чем меньше его показатели после радикальной простатоэктомии, тем лучше прогноз.
Выраженность распространения злокачественного процесса дает возможность оценить исход заболевания. Важным прогностическим фактором после РПЭ является положительный хирургический край. Рост новообразования по краю резекции и его выход за пределы капсулы значительно сокращают выздоровление.
В течение 5 лет у оперированных пациентов с негативным хирургическим краем вероятность рецидива — всего 20%, с позитивным — 40—60%. При прорастании опухоли в семенные пузырьки после удаления простаты местный рецидив рака возникает в 70% случаев. Хорошая 10-летняя выживаемость отмечается после брахитерапии (86%).
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.

Лучевая терапия при раке предстательной железы является одним из наиболее эффективных консервативных методов лечения. На ионизирующее излучение активнее всего реагируют быстро делящиеся клетки, к которым и относятся раковые. При облучении поражаются их ядра, в частности, ДНК, нарушаются обменные процессы, что приводит к гибели. На этом принципе и основана лучевая терапия. Радиационное дозированное облучение применяют для лечения локализованной (очаговый рак) и местнораспространенной (проросший сквозь капсулу, но без метастазов) форм заболевания. Технология, объем лучевого воздействия и суммарная доза подбираются индивидуально для каждого пациента, поэтому облучение здоровых тканей минимально.
Показания и противопоказания
Лучевая терапия является альтернативой радикальной простатэктомии, если речь идет о раке простаты на ранней стадии. Облучение опухоли позволяет контролировать ее разрастание, когда операция невозможна. При метастазирующем раке метод применяют для улучшения качества жизни, часто сочетают с гормональной терапией.
Если опухоль очень крупная, то ее распад после гибели клеток приведет к сильной интоксикации организма, поэтому облучение в таких случаях сочетают с хирургическими методами (простатэктомией).
Лучше всего реагируют на лучевую терапию неблагополучные с гистологической точки зрения опухоли – низкодифференцированные, клетки которых сильно отличаются от нормальных и быстро делятся. Высокодифференцированный медленно растущий рак поддается такому лечению гораздо хуже. Повысить чувствительность таких клеток можно при помощи медикаментов, насыщения опухоли кислородом, повышением ее температуры (локальная гипертермия), снижением уровня pH. Все эти меры продумываются на этапе планирования.
Противопоказания к лучевой терапии:
- Пиелонефрит, хроническая почечная недостаточность.
- Цистит.
- Истощение.
- Большой объем остаточной мочи.
- Возраст после 70 лет. В старческом возрасте отдают предпочтение медикаментозным паллиативным методам лечения.
В настоящее время благодаря новым методам предварительного планирования лучевая терапия становится безопаснее простатэктомии.
Виды лучевой терапии
Тип лучевой терапии подбирают в зависимости от вида рака. Каждая методика имеет свои показания, без учета которых воздействие может быть не только неэффективным, но и опасным. Существует два принципиально разных типа лучевой терапии: дистанционная и внутритканевая (контактная, или брахитерапия). Для повышения эффективности лечения их сочетают с ультразвуком, лазером, электрическими и магнитными полями, химио- и иммунотерапией.

Дистанционная (внешняя) лучевая терапия является наиболее распространенным видом облучения. Показана при раке, локализованном в капсуле простаты, на стадии Т1а-Т2с N0M0, а также при местнораспространенном на стадии Т3-Т4 N0M0 совместно с гормональной терапией.
- Ранее произведенное облучение малого таза;
- Острое воспаление прямой кишки;
- Установленный уретральный катетер;
- Ожирение 4 степени.
Относительными противопоказаниями к дистанционной лучевой терапии являются хроническая диарея, малый объем мочевого пузыря, нарушение проходимости уретры, язвенный колит.
Преимущества: возможность полного излечения без хирургического вмешательства, нет необходимости ложиться в стационар. Из минусов: долгое лечение (1,5-2 месяца), сопутствующая доброкачественная гиперплазия останется.
По технике облучения выделяют конвекционное и 3D-конформное. Первый метод подразумевает использование простых прямоугольных полей воздействия. Во втором случае создается трехмерная модель опухоли, он более точный, снижает нагрузку на жизненно важные органы.

Установка для облучения 
Оборудование для проведения лучевой терапии
Целью радиотерапевта при проведении дистанционной лучевой терапии является точечное направление потока излучения с захватом небольшого объема здоровой ткани во избежание рецидива. Эту задачу упрощают более современные методики.
Протонная терапия подразумевает воздействие протонами, разогнанными до больших энергий при помощи циклотрона. Пучки протонов распределяются в мишени таким образом, что полностью исключается их рассеивание за нее. Энергия протонного луча больше, чем радиационного. Длительность воздействия составляет 10-15 минут. В среднем на курс требуется 18 процедур.

Установка для протонной терапии ProBeam
IMRT – дистанционная лучевая терапия с модуляцией интенсивности, возможна только на специальных линейных ускорителях. Аппарат производит пространственное сканирование опухоли (3D) для направления радиационного луча под различным углом. В каждом положении система подбирает оптимальную интенсивность излучения и форму пучка облучающих частиц. Луч можно разбить на несколько сегментов. Таким образом основная лучевая нагрузка приходится на центр опухоли, а здоровые ткани подвергаются минимальному повреждению. 3D-модель простаты предварительно составляется при помощи МРТ или КТ.

Схема облучения
Если сразу дать высокую дозу радиации в режиме повышенной точности, то есть шанс убить рак без операции за 1-5 сеансов и существенно продлить жизнь больному, ранее считавшемуся неизлечимым. Такой инновационный метод лучевой терапии называется стереотаксической гипофракционной радиотерапией.
Облучение продолжается от 15 секунд до 2 минут. Опухолевые клетки погибают, некротизируются, на месте рака остается стабильный рубец. Данный процесс занимает некоторое время, поэтому результат будет не сразу. Лечение длится всего 2 недели: одна на подготовку, вторая на облучение.
Данный метод лучевой терапии больше всего подходит для лечения рака на начальной стадии, а также при наличии небольшого количества некрупных метастазов. Если опухоль крупная, а количество метастаз более 10, то SBRT не применяют.
Из осложнений чаще всего развивается лучевое воспаление кожи. Через 1-3 недели симптом пройдет, но в течение этого времени необходима защита от ультрафиолета (ткань, крем).
IGRT – лучевая 3D-терапия под визуальным контролем. Опухоли после каждого облучения меняют свои очертания, простата смещается при различной наполненности мочевого пузыря, аппарат фиксирует эти изменения, что дает возможность оказывать более точное воздействие. Программное обеспечение позволяет сопоставить снимки КТ и реальное изображение опухоли. Благодаря этому можно скорректировать положение пациента и направление потока излучения. Все параметры опухоли вводятся в систему. Если луч выйдет за обозначенные границы, установка отключится, после корректировки сеанс продолжается.
Это инновационная технология дистанционной лучевой терапии, позволяющая сократить сеанс лечения и повысить его эффективность за счет высокой вариабельности положений пациента и параметров установки. Аппарат поддерживает 360 позиций, в каждой из которых доступны дополнительные опции регулирования дозировки и мощности излучения. Методика Gated RapidArc обеспечивает корректировку потока, синхронизируя его направление с дыханием пациента. Само облучение длится пару минут, но точная укладка больного потребует не менее получаса.

Технология облучения VMAT RapidArc
В ходе облучения охватывается весь объем опухоли, обеспечивая идеальную схему лечения. На сегодняшний день это самый эффективный и безопасный метод лучевой терапии.
SDRT – это однофракционная экстракраниальная радиотерапия. Во время сеанса железу фиксируют ректальными баллонами и подвергают облучению в 8 Гр. Курс длится 5 дней. Как и во время IGRT, врач видит простату на экране. Подготовка и укладка пациента занимают полчаса, а само облучение длится несколько минут.
Фиксация помогает избежать осложнения со стороны мочеполовой системы. В основном негативные последствия ограничиваются учащенным дискомфортным мочеиспусканием, которое нормализуется в течение 3 недель.
Госпитализация не требуется. Данный метод лучевой терапии подходит для пожилых людей, а также страдающих сахарным диабетом, патологиями кровеносной системы. Если опухоль распространилась за пределы капсулы, то SDRT не применяют. Невозможность введения уретрального катетера и ректальных баллонов также является противопоказанием.
Брахитерапия
Брахитерапия подразумевает введение радиоактивного вещества на специальном носителе непосредственно в ткань опухоли. Основные типы контактной лучевой терапии: низкодозная и высокодозная. В первом случае при помощи специальных игл в опухоль вживляют радиационные зерна, которые остаются в ней навсегда. Излучение будет продолжаться некоторое время, потом прекратится. Во втором случае в иглы подводят источник радиации, выжидают несколько минут для воздействия и извлекают их из железы.

Примеры распределения лучевой нагрузки на простату методом фокальной брахитерапии: а – таргетная (ультрафокальная) схема; б – гемиаблативная (облучается одна доля простаты); в – фокусированная на видимый очаг; г – фокусированная на периферическую зону
Системная терапия
Одним из видов контактной радиотерапии является системная, при которой радиоактивные вещества вводят в кровоток (таблетки или инъекции в вену), после чего они распределяются по организму. Применяют в случае распространения метастаз по костной системе.

Сравнение эффективности различных видов лучевой терапии
Как проводится лучевая терапия при раке простаты
Сначала пациента консультирует онколог-радиолог (радиотерапевт). Специалист в соответствии с показаниями выбирает методику и обсуждает с больным дополнительные виды лечения.
Расстояние смещения опухоли при дыхании фиксируется рентгеном. Это важно для расчета облучающего объема. На симуляторе проверяют фокусировку луча. Он должен попасть четко в центр опухоли. Во время облучения пациент не испытывает никаких ощущений.
Последствия, осложнения, прогноз продолжительности жизни
Вероятность осложнений лучевой терапии напрямую зависит от дозы облучения и радиочувствительности окружающих тканей. Острые реакции возникают непосредственно во время курса лечения. В течение 2-6 недель эти симптомы проходят. Более поздние осложнения развиваются в срок от месяца до года после завершения облучения. Это лимфостаз нижних конечностей, эректильная дисфункция.

Ближайшие и отдаленные осложнения лучевой терапии (в %) 
Зависимость трехлетней безрецидивной выживаемости от уровня ПСА и дозы облучения
Минимизировать последствия лучевой терапии помогут профилактические меры:
- Исключить из рациона острую и соленую пищу, алкоголь.
- Тщательная гигиена половых органов и области промежности.
- При наличии цистита или пиелонефрита предварительно сделать бакпосев мочи с определением чувствительности к антибиотикам, пройти курс соответствующего лечения.
- Если наблюдается выраженное затруднение мочеиспускания, то лучевой терапии должна предшествовать гормональная либо ежедневная доза облучения должна начинаться с 0,5 Гр.
- Не проводить лучевую терапию после инструментальных вмешательств на уретре, не ранее, чем через 4-5 недель после трансуретральной резекции.
- У ослабленных больных следует делить курс облучения паузами в 2-3 недели, общая доза – не более 40-45 Гр.
Если есть предпосылки к развитию лучевого ректита (воспаление слизистой прямой кишки с отторжением выстилающей клетчатки), необходимо использовать свечи с белладонной, метилурацилом, анестезином, масляные.
ПСА после лучевой терапии рака простаты
После лучевой терапии уровень ПСА падает медленнее, чем после простатэктомии. Для достижения минимального уровня (0,5 нг/мл) может потребоваться 3 года и более. Были случаи, когда для снижения уровня ПСА после лучевой терапии потребовалось 5 лет. После брахитерапии первый анализ на ПСА сдают не раньше, чем через 3 месяца, затем контроль проводят раз в квартал.
У 30% пациентов после лучевой терапии наблюдается несущественный скачок ПСА, связанный с тем, что железа продолжает продуцировать антиген.

Рецидив рака простаты после лучевой терапии
Рецидив рака после лучевой терапии можно предсказать по времени увеличения уровня ПСА вдвое. Если срок составляет 13 месяцев, то диагностируется рост единичной опухоли (местный рецидив). Для системного рецидива (рост метастатических очагов) характерно быстрое время удвоения – 3 месяца.
Увеличение уровня ПСА является показанием для назначения других методов диагностики: МРТ, ПЭТ-КТ, остеосцинтиграфия (для определения метастазов в костях).
Реабилитация после лучевой терапии
После дистанционной лучевой терапии на коже может появиться ожог, как от солнца. Это место нельзя тереть мочалкой и подвергать другим механическим воздействиям.
После лучевой терапии важно полноценно питаться. Особенной диеты нет, но следует исключить копчености, соленья, маринады, алкоголь, острые блюда. В рацион обязательно должны входить фрукты (кроме кислых), овощи, крупы, жирная рыба, постное мясо, кисломолочные продукты. Если нет аппетита, то рекомендуется по утрам натощак рассасывать под языком чайную ложку перги (пчелиная пыльца). Полезен настой на пчелином подморе.

Желательно пить больше жидкости и двигаться. Лучевая терапия влечет за собой серьезную интоксикацию организма продуктами распада опухоли, которые необходимо выводить.
Секс не противопоказан. Чем быстрее начнется половая жизнь, тем больше шансов на восстановление эрекции. На начальном этапе можно стимулировать либидо при помощи БАДов, а эрекцию – приемом ингибиторов ФДЭ-5 (силденафил, тадалафил). Следует учесть, что после полного облучения и рубцевания простаты эякуляции не будет. Если мужчина планирует иметь детей, то ему следует заранее сдать сперму в криобанк.

Цены на лучевую терапию сильно колеблются в зависимости от типа учреждения, установки, программы подготовки. Высокоточные системы в РФ пока в единичных количествах. Лечение рака простаты лучевой терапией на скоростной установке TrueBeam можно пройти в Центре лучевой терапии в Москве. Протонная терапия доступна на установке ProBeam в центре протонной терапии (МИБС) в Санкт-Петербурге. Цена в МИБС:
- Подготовка и планирование – 200 тыс. руб.;
- Стереотаксическая лучевая терапия в режиме гипофракционирования – 180 тыс. руб.;
- Консультация радиотерапевта – 2500 руб.
В НИИ онкологии им. Петрова сеанс дистанционной лучевой терапии обойдется в 3460 руб., в Российском центре радиологии им. Гранова (СПб) сеанс стереотаксической терапии стоит 30000 руб., конформное облучение IMRT – 18000 руб.
Отзывы
Заключение
Лучевая терапия, по сути, является таким же радикальным методом лечения рака простаты, как и простатэктомия, но считается более щадящим, с точки зрения побочных эффектов. Последнее особенно актуально для инновационных высокоточных методик. На ранних стадиях большинство врачей рекомендуют простатэктомию, поскольку после нее остается широкий выбор других способов лечения. После лучевой терапии могут произойти изменения в структуре тканей, которые не дадут возможности для оперативного вмешательства.
Читайте также:

