Что такое симптоматическая терапия рака поджелудочной железы
Как известно, рак поджелудочной железы характеризуется высокими биологической агрессивностью и метастатическим потенциалом. К этому предрасполагают ее анатомо-физиологические особенности: орган не имеет хорошо выраженной капсулы, расположен в забрюшинном пространстве, имеет хорошо развитую сосудистую сеть, богато снабжен нервными окончаниями, расположен в непосредственной близости с жировой клетчаткой и многочисленными лимфоузлами забрюшинного пространства. В то же время появление опухоли в железе на первых этапах практически не вызывает специфических симптомов. Кроме того, выявление образований в ткани железы представляет определенные трудности в диагностическим плане: чаще всего при обычном ультразвуковом исследовании в условиях неудовлетворительной визуализации (газ и жидкость в желудке, кишечнике) поджелудочная железа видна плохо, фрагментарно, а ее опухоли достаточно часто имеют изоэхогенную структуру, т.е. аналогичную здоровой ткани. Эти обстоятельства предрасполагают к крайне низкой выявляемости этого вида опухоли на ранних стадиях и к тяжелому, не поддающемуся лечению дальнейшему прогрессированию рака.
Устранение симптомов
При установленном диагнозе рака поджелудочной железы неоперабельной стадии первой задачей является устранение жизнеугрожающих осложнений (механическая желтуха, препятствие для прохождения пищи по желудку или двенадцатиперстной кишки, кровотечение, болевой синдром), а также снятие болевого синдрома.
Дальнейшие варианты возможного лечения обсуждаются на консилиуме с участием специалистов онкохирургов, химиотерапевтов и лучевых терапевтов.
Что такое паллиативное лечение
Паллиативное лечение подразумевает под собой применение специальных методов противоопухолевого лечения: циторедуктивная операция (операция, уменьшающая объем опухоли и способствующая устранению осложнений), паллиативное химиотерапевтическое и радиотерапевтическое лечение. Поскольку полностью излечить этих больных невозможно, целью паллиативного лечения является уменьшение проявлений заболевания, улучшения качества и продление жизни пациентов.

При невозможности специального противоопухолевого лечения пациенты нуждаются в паллиативной помощи – симптоматическом лечении, направленном на снятие тягостных и жизнеугрожающих симптомов болезни, включающем хирургические способы, кровоостанавливающие средства, различные методы питательной (нутритивной) поддержки, обезболивание. Целью паллиативной помощи является борьба с симптомами, ухудшающими качество жизни больных.
Паллиативное и симптоматическое лечение необходимо и при прогрессировании рака поджелудочной железы после радикального лечения. Прогрессирование проявляется рецидивом в ложе удаленной опухоли, распространением опухоли по брюшной полости и развитием отдаленных метастазов.
Хирургическое паллиативное лечение

Хирургический компонент в паллиативном лечении применяется при наличии осложненного опухолевого процесса. Так, сужение желчных путей с развитием механической желтухи –показание к хирургическим манипуляциям для отвода желчи. При неоперабельном процессе возможно чрезкожное чрезпеченочное дренирование желчного пузыря или желчных протоков, однако при неоперабельном процессе отдают предпочтение различным видам стентирования протоков. Стентирование проводится с помощью эндоскопической техники, с заведением направляющей струны через канал эндоскопа в просвет холедоха. Процедура выполняется под рентгенологическим контролем в режиме реального времени с рентгеноконтрастным веществом, вводимым в желчные протоки. По проводнику, согласно данным выявленного уровня сужения протока, выполняется установление саморасправляющегося стента – трубочки в виде пружинки, которая будет удерживать просвет протока раскрытым. При отсутствии возможности стентирования выполняют симптоматическую шунтирующую операцию (соединение желчного пузыря или протока выше сужения с кишкой, т.н. билиодигестивное шунтирование).
Появление признаков желудочно-кишечного кровотечения – показание к гемостатической и гемозамещающая терапии (см.часть I).
Восстановление питания
При нарушении проходимости желудка и/или двенадцатиперстной кишки необходимо стремиться к восстановлению питания. Возможно эндоскопическое заведение зонда за зону сужения или эндоскопическое стентирование – установка саморасправляющейся конструкции в виде сетчатой трубки, раскрывающей просвет желудочно-кишечного тракта. При невозможности или неэффективности стентирования выполняется симптоматическая операция – формирование соустья нижележащих отделов кишечника с желудком – т.н. обходной гастроеюноанастомоз, позволяющий пище из желудка поступать в отделы кишечника, свободные от опухоли. В ряде ситуаций формируют противоестественное отверстие для питания – тонкокишечную стому (еюностомия). Существуют малоинвазивные (эндоскопические) методы еюностомии, их применение ограничено наличием выраженного опухолевого сужения, не позволяющего провести эндоскоп.

Пациенты с распространенным раком поджелудочной железы чаще всего находятся в состоянии пониженного питания, плоть до выраженного истощения (раковая кахексия). Для поддержания качества жизни применяются различные способы улучшения питания и восстановления водно-электролитного баланса:
- Частое дробное питание, исключения продуктов, раздражающих слизистую оболочку желудка (грубая пища, копчености, маринады, жирное и жареное, газированные и алкогольные напитки)
- Медикаментозные средства: ферменты поджелудочной железы (паркеатин, креон, панзинорм, эрмиталь и дт.), препараты, снижающие секрецию желудочного сока (омепразол, рабепразол и др.), спазмолитики (но-шпа, дюспаталин).
- Применение специальных сбалансированных питательных смесей – сухих или в разведении (Нутризон, Нутридринк, Суппортан и др.)
- Парэнтеральное (букв. помимо желудочно-кишечного тракта) питание – внутривенное введение питательных веществ – сбалансированных смесей углеводов, жиров и аминокислот, например, Кабивен, Оликлиномель.
- Введение витаминных комплексов и смесей (например, мильгамма, витамин С, цернивит и др.)
Консервативные методы лечения

При нерезектабельном местном опухолевом процессе без отдаленных метастазов, отсутствии жизнеугрожающих осложнений и сохранном общем состоянии пациента применяются консервативные паллиативные методы лечения. Проводят лучевую терапию в сочетании с противоопухолевыми лекарственными средствами (химиолучевое лечение) (см.часть I). Паллиативная лучевая терапия проводится по специальной щадящей схеме: подводится меньшая разовая доза облучения, более длительное лечение, меньше поле облучения. В качестве радиомодификаторов добавляются химиопрепараты.

Для самостоятельного паллиативного лечения неоперабельных больных с генерализованным, т.е. с отдаленными метастазами, раком проводят самостоятельную химиотерапию – лечение специальными противоопухолевыми препаратами (см.часть I). Химиотерапия проводится длительно, с большим числом курсов, сменой линий химиопрепаратов, регулярным контролем эффективности, активной сопроводительной симптоматической терапией. Эффективными химиопрепаратами считаются гемцитабин, препараты платины, капецитабин, иринотекан, прапараты таксанов и т.д. (см.часть I).
Применяют также таргетные препараты, блокирующие рост и размножение опухолевых клеток, воздействуя на индивидуально выявленные молекулы (цели), участвующие в росте и развитии опухолевых клеток. Это Тарцева (эрлотиниб), бевацизумаб, целекоксиб, Алимта. Препарат назначается в комбинации с обычными химиопрепаратами при выявленной чувствительности опухоли к тому или иному лекарственному агенту. Чувствительность определяется при молекулярно-биологическом исследовании опухоли.
При опухолях с эндокринной активностью, таких как нейроэндокринные опухоли (карциноиды), возможно применение аналога соматостатина – октреотида, в том числе с пролонгированным действием (Сандостатин Лар).
Обезболивание как способ лечения
При распространенной опухоли, определяемой как IV стадия, и при прогрессировании заболевания развиваются различные осложнения и состояния, описанные выше, а также изнуряющий болевой синдром. При наличии болей назначают обезболивающую терапию, в том числе с применением наркотических анальгетиков.
Врач-онколог не имеет права отказать онкологическому больному в обезболивании!
Обезболивающая терапия подбирается по мере нарастания боли, с применением специальных шкал. Для короткого курса обезболивания могут применяться нестероидные противовоспалительные средства (парацетамол, кетопрофен, кеторолак и др.), однако при необходимости длительного обезболивания подключают препараты с меньшими побочными эффектами – аналоги опиатов (трамадол), опиоидные анальгетики, глюкокортикоиды, транквилизаторы, антиконвульсанты, антидепрессанты.

Если традиционные методы обезболивания малоэффективны, обезболивающего эффекта добиваются введением в эпидуральное простраство (в позвоночный канал в пространство, омывающее нервные корешки) анестетика. Существуют программируемые помпы для дозированного введения обезболивающих, в т.ч. наркотических средств, например, программируемая морфиновая помпа.
Также производят разрушение нервных узлов симпатических нервов с одной или двух сторон (симпатспланхникэктомия) мини-инвазивным способом – при видеоторакоскопии.
Прогноз
При далеко зашедшем процессе все лечебные мероприятия позволяют прожить не более 6-8мес.
Видео о том, как происходит метастазирование раковых опухолей
При наступлении определенных неблагоприятных обстоятельств клетки, из которых состоят все органы и ткани человеческого организма, начинают перерождаться. Меняется структура и скорость деления этих клеток, нарушается их нормальная функциональность. Из таких патологических клеток впоследствии формируется раковая опухоль. Новообразование может поражать различные органы, в том числе и ткани поджелудочной железы (железистая ткань или протоки органа). В этом случае нарушается нормальная работа органа, страдает вся пищеварительная система. Кроме того, новообразование, склонное к агрессивному течению и быстрому развитию, дает метастазы в другие области организма, вызывая нарушения их работоспособности.

Рак поджелудочной железы, симптомы и проявления которого могут быть различными, является распространенной патологией, чаще всего патология наблюдается у людей преклонного возраста, преимущественно, у мужчин. Заболевание на начальной стадии никак себя не проявляет, и по мере его развития какие – либо симптомы, характерные именно для этого вида патологии, отсутствуют. Тем не менее, недуг весьма опасен, рак поджелудочной отличается тяжелым течением и может привести к летальному исходу.
Начальные признаки и проявления
Чаще всего признаки раннего развития раковой опухоли в поджелудочной железе отсутствуют. Если же и имеются какие – либо начальные симптомы, они не являются специфическими. То есть, те же самые признаки могут свидетельствовать как об онкологическом заболевании, так и о развитии других патологий пищеварительной системы.
К числу ранних признаков, говорящих о возможном развитии раковой опухоли, принято относить:
- Болезненные ощущения в области живота, дискомфорт, распирание;
- Чувство жжения в эпигастральной области;
- Понос, изменение консистенции кала (в его составе присутствует большое количество жировых элементов);
- Редкие позывы к рвоте;
- Сильная жажда;
- Потемнение мочи, потеря ее прозрачности;
- Нарушение аппетита, снижение массы тела без видимых на то причин;
- Слабость;
- Периодическая незначительная гипертермия, которая возникает внезапно.
Клинические симптомы рака поджелудочной
| Симптом | Характеристика и описание |
| Болевой синдром | Болезненные ощущения развиваются постепенно, по мере роста раковой опухоли. Боль имеет четкую локализацию, которая зависит от области поражения. С течением времени болевые ощущения могут иррадиировать в другие участки тела, чаще всего, в области спины. Боль становится более интенсивной в моменты физической активности, например, если человек совершает резкие наклоны вперед, либо в ночное время. |
| Изменения кожных покровов | Раковая опухоль, выросшая в размерах, может перекрывать желчевыводящий проток. Это особым образом сказывается на состоянии эпидермиса. Кожа приобретает характерный желтый окрас, становится более сухой и чувствительной. Нередко на тех или иных участках тела возникают высыпания, сопровождающиеся зудом. |
| Изменение выделений | Моча больного приобретает более темный оттенок, становится мутной. Также меняется цвет и консистенция каловых масс. Кал обесцвечивается, становится более жидким (мягкий или водянистый стул), в нем присутствуют выраженные жировые вкрапления. |
| Потеря веса | Поджелудочная железа, пораженная раковой опухолью, теряет свою функциональность, вырабатывает меньше ферментов, необходимых для нормального расщепления пищи. В результате этого питательные вещества не усваиваются организмом, а выводятся из него вместе с калом (этим обусловлена и повышенная жирность каловых масс). При недостаточном содержании питательных элементов происходит снижение веса, при том что режим питания и объемы потребляемой пищи остаются неизменными. |
| Снижение аппетита (вплоть до анорексии) | Данный симптом развивается не всегда. Нарушения работы пищеварительной системы, приводящие к чувству тяжести в животе, вызывают неприязнь к еде, либо чувство быстрого насыщения. |
| Рвотные позывы | Указанный признак возникает тогда, когда новообразование достигает значительных размеров. Опухоль сдавливает желудок и верхний отдел кишечника, мешая нормальному продвижению пищи по системе ЖКТ. Это приводит к тому, что плохо переваренные кусочки двигаются в ретроградном направлении, в результате чего возникает тошнота. |
| Сахарный диабет вторичной формы | Поджелудочная железа – гормонопродуцирующий орган. Если ее функции нарушены в результате развития онкологической патологии, она не может вырабатывать достаточное количество гормонов, способствующих расщеплению и усваиванию углеводистых соединений. Эти элементы накапливаются в организме, в результате чего развивается вторичный диабет. |
| Увеличение размеров селезенки | Если опухоль располагается в теле или хвосте органа, это негативно влияет на работу не только самой поджелудочной железы, но и других органов, расположенных поблизости. Прежде всего, это селезенка. Работа селезенки нарушается, и, чтобы как-то компенсировать утраченную функциональность, расширяется площадь органа, селезенка увеличивается в размерах. |
| Острый панкреатит | Длительное нарушение работы поджелудочной железы приводит к повреждению тканей органа, развитию характерных симптомов, таких как острая боль вверху живота, обильная рвота, резкое ухудшение состояния здоровья пациента. |

Стадии и степени тяжести
Онкологические опухоли развиваются и растут постепенно, это касается и рака поджелудочной железы. Выделяют несколько стадий развития патологического процесса, в зависимости от размеров новообразования и очага поражения.
| Этап развития | Проявления |
| Начальный этап | На первой стадии опухоль имеет незначительные размеры, очаг поражения располагается только в тканях пораженного органа, не затрагивая другие участки. Метастазирование отсутствует, клиническая картина не выражена, либо имеет стертые проявления. |
| Этап 2. | Вторую стадию рака поджелудочной принято делить на 2 этапа. Стадия 2А характеризуется незначительным разрастанием новообразования, которое поражает теперь не только поджелудочную железу, но и небольшие участки желчевыводящих протоков и двенадцатиперстной кишки. Лимфатическая система человека остается неизмененной. |

Классификация и формы
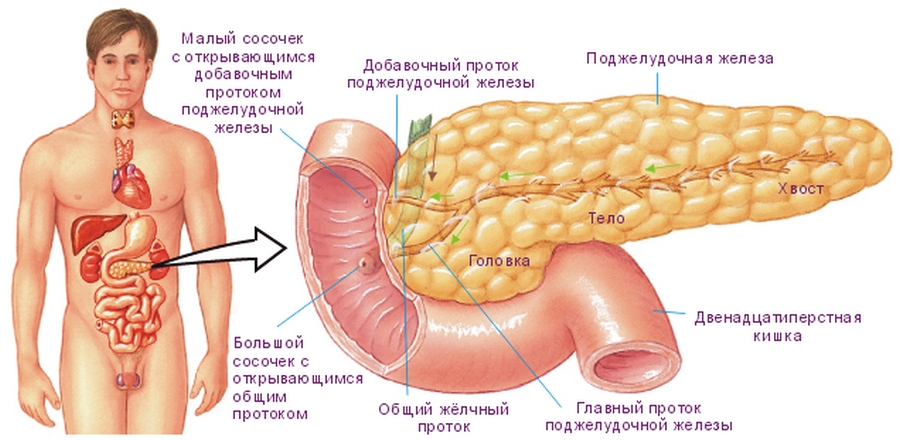
Поджелудочная железа имеет особое строение. Она включает в себя такие структурные элементы как головка, тело и хвост органа. Раковые опухоли с одинаковой долей вероятности могут поражать любой из этих участков. Локализация раковой опухоли имеет существенное влияние на течение и клиническую картину патологии.
Выделяют следующие разновидности заболевания в зависимости от локализации патологического процесса:
- Рак головки поджелудочной железы. Для данной формы характерны такие признаки как боль в верхней части брюшины, изменение окраса кожи, сухость верхнего слоя эпидермиса, появление кожной сыпи, снижение массы тела и стойкое отсутствие аппетита, развитие холецистита и панкреатита в острой форме;
- Поражение тела органа. При этом у пациента возникают такие проявления как стремительная потеря массы тела, возникновение вторичного диабета, увеличение селезенки;
- Для рака хвоста поджелудочной железы характерны следующие симптомы: выраженный болевой синдром, потеря веса, увеличение объемов выделяемой урины, сильная жажда, увеличение размеров селезенки, развитие обильных внутренних кровотечений в эпигастральной области.


Методы постановки диагноза
На основании одних лишь клинических проявлений патологии невозможно сделать какие – либо выводы, поэтому, для точного диагностирования раковой опухоли, врачу потребуются данные многочисленных лабораторных и инструментальных исследований.
Диагностика осуществляется поэтапно. Изначально пациенту потребуется сдать ряд анализов, данные которых позволят заподозрить наличие онкологического заболевания. После этого для получения более детальной картины, назначают инструментальную диагностику.
Лабораторное исследование включает в себя следующие виды анализов:
- Исследование крови для выявления онкомаркеров (веществ, выделяемых при наличии опухолевых новообразований);
- Исследование урины на содержание и уровень панкреатической амилазы;
- Анализ каловых масс для выявления панкреатической эластазы;
- Исследование крови на содержание и уровень альфа-амилазы (при раке поджелудочной железы она содержится не только в крови, но и в моче), щелочной фосфатазы, глюкагона, гастрина, пептидных элементов и инсулина.
При положительных результатах, полученных в ходе лабораторных анализов, пациенту назначают дальнейшую диагностику, включающую в себя различные инструментальные исследования, такие как:
- Скрининг органов области брюшины. Данный метод позволяет определить область, которая нуждается в дальнейшем обследовании. Каких – либо данных о форме или размерах опухоли скрининг не предоставляет;
- КТ поджелудочной железы – информативный метод, позволяющий определить очаг поражения и локализацию опухоли;
- МРТ для определения состояния тканей пораженного органа;
![]()
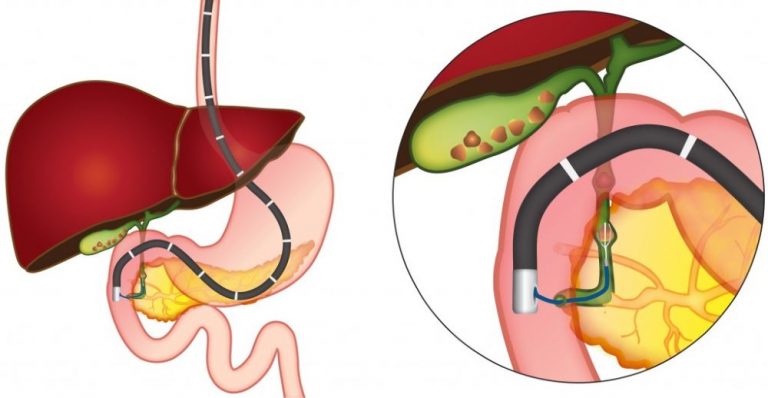
- ЭРХПГ – диагностический метод, позволяющий определить наличие опухоли в области головки органа. В ходе процедуры в двенадцатиперстную кишку вводят специальное контрастное вещество при помощи эндоскопа. Дальнейшее обследование осуществляется с использованием рентгеновского аппарата;
![]()
- ПЭТ. Через крупную вену в организм пациента вводят специальное вещество на основе изотопов сахара. Сахар накапливается в организме, но в различных количествах, в зависимости от состояния тканей тех или иных органов;
- Эндоскопическая холангиография. Данный диагностический способ применяется в том случае, если вещество с изотопами сахара не удается ввести через вену (препарат доставляют в пораженный участок через небольшой прокол в печени);
- Лапароскопия. Процедура считается инвазивной, поэтому проводят ее под анестезией. Через небольшой надрез в брюшной полости в живот пациента вставляется специальная трубка, через которую в брюшину закачивают газ (это необходимо чтобы защитить органы от травм при последующем их осмотре при помощи эндоскопа и обеспечить лучшую видимость). После этого в надрез вставляют эндоскоп, оснащенный камерой. Изображение внутренних органов пациента поступает на монитор врача, давая ему возможность визуально определить наличие раковой опухоли;
- Биопсия – обязательный метод исследования, необходимый для постановки точного диагноза. В ходе процедуры (во время эндоскопического исследования, описанного выше), из пораженных участков берут небольшое количество тканей, которые в дальнейшем изучаются под микроскопом. Данный способ позволяет определить структуру перерожденных клеток и сделать вывод относительно злокачественности опухоли.

Методы лечения рака поджелудочной железы
Основным и наиболее эффективным способом лечения считается хирургическая операция. Однако, далеко не всегда можно назначать оперативное вмешательство. Противопоказанием к операции является множественность опухоли, развитие метастазов в другие органы, слабое состояние здоровья пациента (когда существует вероятность того, что человек не перенесет сложную операцию).
При небольших единичных раковых образованиях пациента направляют на операцию панкреатодуоденальной резекции. Процедура считается весьма сложной, выполняется под общей анестезией. Врач делает надрез в области поврежденного органа, через него удаляет поджелудочную железу (или ее часть, в зависимости от локализации и размеров опухоли), кроме того, возможно потребуется удаление и других элементов пищеварительного тракта (часть желудка и двенадцатиперстной кишки). После удаления проводится пластика органов ЖКТ для восстановления пищеварительной функции и нормальной работоспособности.

При тяжелом поражении при запущенной стадии развития раковой опухоли в поджелудочной железе используют паллиативную технику лечения. Задача данного вида терапии заключается в продлении жизни пациента. Паллиативная терапия направлена на:
- Устранение внутренних кровотечений;
- Обеспечение оттока желчи;
- Устранение препятствий для продвижения пищи (при кишечной непроходимости);
- Поддержание работоспособности других жизненно-важных систем (при наличии метастазов в их тканях);
- Устранение выраженного болевого синдрома (на поздних стадиях развития патологии боль становится нестерпимой и практически никогда не отступает, поэтому, для облегчения состояния пациента ему назначают сильнодействующие обезболивающие препараты);
- Детоксикацию организма.
Данный метод лечения применяется при множественных метастазах (их можно удалить хирургическим путем, однако, в большинстве случаев метастатические опухоли появляются вновь, поэтому наиболее эффективным способом лечения является использование химических препаратов). В организм пациента вводят сильнодействующие химические средства, которые губительно действуют на клетки опухоли, разрушая их (часто данный метод применяется перед хирургической операцией).


Медикаментозные химические средства вводятся при помощи инъекций или пероральным способом. В состав препаратов входят агрессивные вещества, которые негативно влияют не только на клетки опухоли, но и на здоровые ткани человека. Поэтому у пациента часто возникают побочные эффекты, такие как:
- Ухудшение качества волос (вплоть до их полного выпадения);
- Проявления токсического поражения (приступы тошноты, сопровождающиеся обильной рвотой, понос);
- Патологии неврологического характера.

Препараты для лечения
Для борьбы с раковой опухолью и устранения симптомов патологического процесса пациенту назначат многочисленные лекарственные препараты различных групп. Это средства химиотерапии, разрушающие ткани опухоли, обезболивающие, противорвотные, антигистаминные, ферментные препараты.
Каждая группа имеет свое предназначение. Так, химиотерапевтические препараты направлены на устранение опухоли (или приостановление ее роста), борьбу с метастазами. Обезболивающие средства необходимы для облегчения состояния пациента, купирование выраженного болевого синдрома. Противорвотные препараты позволяют избежать обезвоживания организма и улучшить самочувствие больного, антигистаминные препараты борются с кожными проявлениями патологии, ферментные средства способствуют нормализации пищеварения.
| Название | Описание | Дозировка | Цена |
| Эрлотиниб |
Рекомендуемый рацион
При раковой опухоли, поражающей поджелудочную железу, страдает вся пищеварительная система. Поэтому, для нормализации работы ее органов, пациенту необходимо соблюдать особый рацион, предполагающий значительные ограничения.

Прогноз
Рак поджелудочной железы – опасное заболевание, склонное к быстрому развитию, поэтому прогнозы, в большинстве случаев, неблагоприятные. Однако, все зависит от того, насколько своевременным и правильным было проведенное лечение. Согласно статистике, выживаемость пациентов составляет:
- 5 и более лет при успешно проведенном хирургическом лечении (если опухоль проросла в соседние органы, добиться 5-летней выживаемости удается только в 20% случаев);
- При отсутствии лечения пациент не проживет более полугода;
- При одном химиотерапевтическом или радиационном лечении выживаемость составляет не более 12 мес.;
- Паллиативная терапия позволяет продлить жизнь человека на 1 год, а если ее сочетают с химиотерапией, средняя выживаемость увеличивается до полутора лет.

- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
В последние десятилетия отмечается рост пациентов со злокачественными опухолями органов гепатопанкреатодуоденальной зоны. При этом частота диагностики рака этих органов на ранних стадиях практически не повысилась. В основном пациенты продолжают поступать в стационары только при развитии осложнений, наиболее частым из которых является механическая желтуха. Рак головки поджелудочной железы находится на втором месте среди причин подпеченочной желтухи (30–35%), уступая лишь холедохолитиазу (35–40%), третье место занимает рак внепеченочных желчных протоков (10–12%), затем — рак большого сосочка двенадцатиперстной кишки (1–2%).

При этом, по данным литературы, только в 10–20% случаев при выявлении рака поджелудочной железы пациентам выполняется радикальная операция, несмотря на которую большинство умирает в первый год после вмешательства. К сожалению, большая часть больных по разным причинам не может рассчитывать на радикальное лечение. Лечение больных этой категории осложняется наличием обтурации желчных путей, холангита, а в большинстве случаев и печеночной недостаточности. Общепризнано, что оперативное вмешательство, выполненное при нарастающей механической желтухе, является чрезвычайно рискованным и сопровождается высокой летальностью, достигающей 20-60%, что наряду с возрастающей частотой опухолевого поражения поджелудочной железы, несомненно, обусловливает актуальность данной проблемы.
Антеградные методы декомпрессии желчевыводящей системы, реализуемые в виде чрескожно-чреспеченочной холангиостомии, продленного наружно-внутреннего дренирования, антеградного эндобилиарного стентирования, могут служить альтернативой эндоскопическим методам при их неэффективности или невозможности выполнения. При этом чрескожные миниинвазивные вмешательства позволяют либо успешно подготовить пациентов к основному этапу операции, в случае возможного выполнения радикального хирургического лечения, либо могут стать окончательным вмешательством, являясь примером паллиативного лечения. Целью нашего исследования явилась оценка эффективности паллиативного лечения с применением антеградных миниинвазивных технологий при раке поджелудочной железы.
Материалы и методы
За период с января 2010 по декабрь 2016 года в хирургическом отделении Орловской областной клинической больницы под наблюдением находилось 160 больных со злокачественным поражением поджелудочной железы, осложненным синдромом механической желтухи. В связи с чем все пациенты были госпитализированы в экстренном порядке. Больные доставлялись в стационар скорой медицинской помощью, направлялись другими лечебно-профилактическими учреждениями города и области, а также обращались самостоятельно. Женщин в исследуемой группе было 76 (47,5%), мужчин — 84 (52,5%). Возраст больных колебался от 48 до 76 лет. Проводилось комплексное обследование больных, включающее исследование клинико-лабораторных данных (общий и биохимический анализ крови, общий анализ мочи, коагулограмма и др.), выполнялось ультразвуковое исследование брюшной полости, гастродуоденоскопия, по показаниям эндоскопическая ретроградная холангиопанкреатография и мультиспиральная компьютерная томография, а также ряд других инструментальных исследований в зависимости от сопутствующей патологии.
У всех пациентов, находящихся под нашим наблюдением, при ультразвуковом исследовании были выявлены признаки актуальной желчной гипертензии, что наряду с невозможностью выполнения по различным причинам ретроградного эндоскопического дренирования явилось основанием для антеградного дренирования желчных путей под сонофлюороскопическим контролем по срочным показаниям (1-2 сутки от момента поступления в стационар). При этом во всех случаях антеградные миниинвазивные вмешательства несли не только лечебную, но и диагностическую нагрузку. Так как выполняемая интраоперационная антеградная холангиография позволяла уточнить уровень и степень блока. Адекватность выполненного чрескожного чреспеченочного дренирования оценивалась по изменению интенсивности желтухи, по суточному дебиту желчи, степени снижения гипербилирубинемии в биохимическом анализе крови, а также по устранению признаков билиарной гипертензии при динамическом ультразвуковом исследовании. После снижения уровня билирубина крови, дообследования и стабилизации состояния пациентов решался вопрос о переводе наружной холангиостомы в наружно-внутреннюю или об антеградном эндобилиарном стентировании.
Результаты исследования
Чувствительность, специфичность и диагностическая точность холангиографии во время постановки холангиостомы при раке поджелудочной железы составила соответственно 91,2%, 80,1% и 85,3%. Всего в группе пациентов со злокачественным поражением поджелудочной железы выполнено 204 минимально инвазивных вмешательств. Распределение характера вмешательств было следующим: наружная холангиостомия — 62,7% (128); антеградное эндобилиарное стентирование — 25% (51); наружно-внутреннее дренирование протоков — 10,3% (21); чрескожно-чреспеченочная микрохолецистостомия — 2% (4).
Учитывая, что у 51 пациента (32%) в исследуемой группе при проведении клинико-инструментальных и морфологических исследований был подтвержден неоперабельный характер поражения поджелудочной железы, выполнение радикального оперативного лечения не представлялось возможным. В связи с этим окончательным видом хирургического лечения, направленным на улучшение качества жизни, у данных больных, явилось антеградное стентирование внепеченочных желчных протоков.
В каждом исследуемом случае стентирование выполнялось вторым этапом после предварительной чрескожно-чреспеченочной холангиостомии или наружно-внутреннего дренирования. Техника стентирования заключалась в проведении металлического проводника через опухолевую структуру за зону большого сосочка двенадцатиперстной кишки под сонофлюороскопическим контролем, по которому в последующем производилась транспапиллярная установка стента. После выполненного стентирования в обязательном порядке производили постановку страховочной наружной холангиостомы, которая позволяла выполнять динамическую антеградную холангиографию для контроля процесса раскрытия стента и адекватности его функционирования в раннем послеоперационном периоде.
Выбор стента по диаметру раскрытия, длине и типу покрытия осуществлялся индивидуально в каждом конкретном случае в зависимости от протяженности зоны поражения. Использование покрытого стента при неоперабельном раке поджелудочной железы имеет ряд преимуществ, так как позволяет предотвратить возможное прорастание опухолевой или грануляционной тканью ячеистой стенки стента, тем самым вызывая обтурацию его просвета. Однако учитывая транспапиллярное положение устанавливаемого стента, применение покрытых форм было ограничено у пациентов с сохраненной проходимостью и функцией панкреатического протока.
Использование в подобных случаях покрытых форм стента значительно повышало риск перекрытия устья панкреатического протока. Как правило, в большинстве случаев сразу же после установки нитинолового саморасправляющегося стента под рентгенологическим контролем отмечали поступление контрастного препарата в просвет двенадцатиперстной кишки. Однако при этом рентгенологически сохранялась зона сужения в пораженном участке билиарного тракта. Полное раскрытие стента, сопровождавшееся свободным поступлением контрастного вещества в просвет двенадцатиперстной кишки, определялось в течение 24-48 часов с момента его установки. Восстановление пассажа подтверждалось контрольной антеградной холангиографией.
Обсуждение результатов
Осложнения после проведенных миниинвазивных вмешательств возникли в 26 случаях, и были связаны у 12 пациентов (7,5%) с дислокацией холангиостомического дренажа; в 4 случаях (2,5%) с развившимся острым холециститом; в 2 случаях (1,2%)с развившимся острым панкреатитом; у 5 пациентов с гидротораксом (3,1%). В отдаленные сроки после стентирования у 3 (1,9%) больных развился рецидив механической желтухи, обусловленный нарушением функции эндобилиарного стента.
В 2 наблюдениях через 4-5 мес. с момента постановки непокрытого стента произошла обтурация его внутреннего просвета за счет прорастания опухолевыми тканями ячеистой стенки.
Среди осложнений, развившихся после проведения антеградного эндобилиарного стентирования в ранний послеоперационный период, были зафиксированы острый холецистит (4 пациента) и острый панкреатит (2 пациента). В 3 случаях после установки непокрытого стента и в 1 после установки покрытого у пациентов отмечены клинико-эхографические признаки острого холецистита. У одного больного выполнена лапароскопическая холецистэктомия, у трех других произведена постановка чрескожно-чреспеченочной микрохолецистостомии под контролем УЗИ, на фоне которой клинические проявления острого холецистита удалось полностью купировать. Клиническая картина острого панкреатита, развившаяся в течение 24-48 часов после выполненного стентирования у двух пациентов, полностью купировалась на фоне проведенной консервативной терапии.
Выводы
У пациентов с неоперабельным раком поджелудочной железы выполнение антеградного эндобилиарного стентирования представляет собой окончательный вариант хирургического лечения, позволяющий при минимальном объеме вмешательства обеспечить адекватный дренирующий эффект желчевыводящих путей. Кроме того, отсутствие наружных дренажей улучшает качество жизни пациента, его психологическое состояние, позволяет активизировать его в более ранние сроки, избавляет от необходимости приема желчи внутрь.
Литература:
- Альянов А.Л., Мамошин А.В., Борсуков А.В., Мурадян В.Ф. Эффективность применения минимально инвазивных технологий в лечении больных с синдромом механической желтухи // Ученые записки Орловского государственного университета. Серия: Естественные, технические и медицинские науки. 2015. № 4. С. 280-284.
- Гальперин Э.И., Ветшев П.С. Руководство по хирургии желчных путей. М.: Издательский дом Видар-М, 2006.
- Данилов М.В., Фёдоров В.Д. Повторные и реконструктивные операции при заболеваниях поджелудочной железы.М.: Медицина, 2003.
- Долгушин Б.И., Авалиани М.В., Буйденок Ю.В. и др.Эндобилиарная интервенционная онкорадиология.М.: ООО "Медицинское информационное агентство«.2004. — 224 с.
- Затевахин И.И., Цициашвили М.Ш., Дзарасова Г.Ж. и др.Возможности доплеровской сонографии в оценке функционального состояния печени при механической желтухе // Анн. хирург. гепатолог. 2001. Т. № 1. С. 113-124.
- Ившин В.Г., Якунин А.Ю., Лукичев О.Д. Чрескожные диагностические и желчеотводящие вмешательства у больных механической желтухой. Тула, 2000. — 312 с.
- Израилов Р.Е. Миниинвазивные технологии в лечении больных с опухолями органов билиопанкреатодуоденальной зоны: автореф. дис. докт. мед. наук / Р.Е. Израилов.Москва, 2011. — 47 с.
- Кубышкин В.А., Вишневский В.А. Рак поджелудочной железы. М., 2003.
- Охотников О.И., Яковлева М.В., Григорьев С.Н., Пахомов В.И. Антеградные эндобилиарные вмешательства в лечении осложненной желчнокаменной болезни // Анн.хирург. гепатолог. 2013. Т. 18. № 1. С. 29-37.
- Патютко Ю.И., Котельников А.Г. Хирургия рака органов билиопанкреатодуоденальной зоны. М.: Медицина, 2007.
- Costamagna G., Pandolfi M. Endoscopic stenting for biliary and Pancreatic malignancies. J ClinGastroenterol 2004; 38: 59–67.
- Hans-Joachim Wagner. With or Against the Bile Flow?Radiology. 2002; 225: 7-9.
- Katsinelos P., Paikos D., Kountouras J. et al. Tannenbaum and metal stents in the palliative treatment of malignant distal bileduct obstruction: a comparative study of patency and cost effectiveness. SurgEndosc 2006; 20: 1587–1593.
- May A., Ell C. A New Self-Expanding Nitinol Stent for Palliation of Malignant Biliary obstruction. Endoscopy 2004; 36: 329–333.
- Mehmet M.D., Aksungur E., Seydaolu G. Percutaneousplacement of biliary metallic stents in patients with malignanthilar obstruction, unilobar versus bilobar drainage. Journal ofVascular and Interventional Radiology. 2003; 14: 1409-1416.
- Yushidome H., Miyazaki M., Shimizu H. et al. Obstructivejaundice impairs hepatic sinusoidal endothelial cell functionand renders liver susceptible to hepatic ischemia/ reperfusion //J. Hepatology. 2000. V.33 (1). P.59-67.
Читайте также:









