Взаимодействие оксида кальция с хлором
Оксид кальция, характеристика, свойства и получение, химические реакции.










Оксид кальция – неорганическое вещество, имеет химическую формулу CaO.
Краткая характеристика оксида кальция:
Оксид кальция – неорганическое вещество белого или бесцветного цвета.
Так как валентность кальция равна двум, то оксид кальция содержит один атом кислорода и один атом кальция.
Химическая формула оксида кальция CaO.
В воде не растворяется, а вступает в реакцию с ней.
Оксид кальция относится к высокотоксическим веществам. Класс опасности 2. Это едкое вещество, особенно опасен при смешивании с водой .
Физические свойства оксида кальция:
| Наименование параметра: | Значение: |
| Химическая формула | CaO |
| Синонимы и названия иностранном языке | calcium oxide (англ.) известь негашеная (рус.) кальция окись (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | Бесцветные, белые кубические кристаллы |
| Цвет | бесцветный, белый |
| Вкус | —* |
| Запах | — |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м 3 | 3370 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см 3 | 3,37 |
| Температура кипения, °C | 2850 |
| Температура плавления, °C | 2570 |
| Молярная масса, г/моль | 56,077 |
Получение оксида кальция:
Оксид кальция получается в результате следующих химических реакций:
- 1. путем термического разложения известняка:
Это промышленный способ получения оксида кальция. Технологически данный процесс в промышленности реализуют в специальных шахтных печах .
- 2. путем сжигания кальция на воздухе:
2Сa + О2 → 2CaО (t = 300 o C).
- 3. путем термического разложения гидроксида кальция:
Сa(OH)2 → СaO + H2О (t = 520-580 o C).
- 4. путем термического разложения нитрата кальция:
Химические свойства оксида кальция. Химические реакции оксида кальция:
Оксид кальция относится к основным оксидам.
Химические свойства оксида кальция аналогичны свойствам основных оксидов других металлов . Поэтому для него характерны следующие химические реакции:
1. реакция оксида кальция с хлором:
В результате реакции образуется хлорид кальция и кислород.
2. реакция оксида кальция с кремнием:
2CaO + 5Si → 2CaSi2 + SiO2 (t = 1300 o C).
В результате реакции образуется силицид кальция и оксид кремния .
3. реакция оксида кальция с углеродом:
CaО + 3С → CaС2 + СО (t = 1900-1950 o C);
2CaO + 5C → 2CaC2 + CO2 (t = 700 o C).
В результате реакции образуется карбид кальция и оксид углерода .
4. реакция оксида кальция с алюминием :
4CaО + 2Al → 2Ca + Ca(AlO2)2 (t = 1200 o C);
В результате реакции образуется кальций и соответственно алюминат кальция, оксид алюминия-кальция и алюмината трикальция.
5. реакция оксида кальция с водой:
6. реакция оксида кальция с оксидом углерода (углекислым газом):
Оксид кальция реагирует с углекислым газом (являющийся кислотным оксидом), образуя соль – карбонат кальция.
7. реакция оксида кальция с оксидом серы :
Оксид серы также является кислотным оксидом. В результате реакции образуется соответственно соль – в первом случае – сульфит кальция, во втором случае – сульфат кальция.
8. реакция оксида кальция с оксидом кремния:
CaО + SiО2 → CaSiО3 (t = 1100-1200 o C).
Оксид кремния также является кислотным оксидом. В результате реакции образуется соль – силикат кальция.
9. реакция оксида кальция с оксидом фосфора :
Оксид фосфора также является кислотным оксидом. В результате реакции образуется соль соответственно: метафосфат кальция, фосфат кальция и дифосфата кальция.
Аналогично проходят реакции оксида кальция и с другими кислотными оксидами.
10. реакция оксида кальция с оксидом алюминия :
Оксид алюминия является амфотерным оксидом. Это значит, что как амфотерный оксид оксид алюминия проявляет свойства как кислотных, так и основных соединений. В результате реакции образуется соль – алюминат кальция.
11. реакция оксида кальция с оксидом марганца :
Оксид алюминия является амфотерным оксидом. Это значит, что как амфотерный оксид оксид алюминия проявляет свойства как кислотных, так и основных соединений. В результате реакции образуется соответственно: соль – манганит кальция либо оксид марганца-кальция.
Аналогично проходят реакции оксида кальция и с другими амфотерными оксидами.
12. реакция оксида кальция с оксидом свинца :
В результате реакции образуется соль – плюмбит кальция. Реакция протекает при сплавлении реакционной смеси.
Аналогично проходят реакции оксида кальция и с другими оксидами.
13. реакция оксида кальция с тетраоксидом диазота:
Реакция идет в жидком тетраоксиде диазота. В результате реакции образуются оксид азота (III) и соль – нитрат кальция.
14. реакция оксида кальция с плавиковой кислотой:
В результате химической реакции получается соль – фторид кальция и вода.
15. реакция оксида кальция с азотной кислотой:
В результате химической реакции получается соль – нитрат кальция и вода .
Аналогично проходят реакции оксида кальция и с другими кислотами.
16. реакция оксида кальция с бромистым водородом (бромоводородом):
В результате химической реакции получается соль – бромид кальция и вода .
17. реакция оксида кальция с йодоводородом:
В результате химической реакции получается соль – йодид кальция и вода .
Применение и использование оксида кальция:
Оксид кальция используется в производстве строительных материалов, в качестве пищевой добавки E-529.










оксид кальция реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие оксида кальция
реакции с оксидом кальция

Определения и формулы основных, амфотерных и кислотных оксидов были приведены ранее в уроке 6.
Характерные химические свойства основных оксидов: реакции с кислотными оксидами с образованием солей и с кислотами с образованием солей и воды, например:
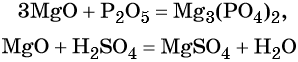
Некоторые основные оксиды реагируют с водой с образованием оснований. Эта реакция проходит в том случае, если продукт реакции растворим в воде:
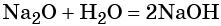
В аналогичных условиях, например, оксид железа (II) с водой реагировать не будет, так как гидроксид железа (II) в воде нерастворим.
Амфотерные оксиды взаимодействуют как с кислотами, так и с основаниями с образованием солей и воды или комплексных соединений:
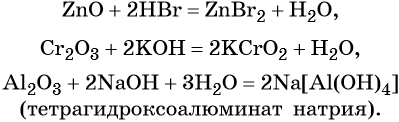
Кроме того, амфотерные оксиды могут взаимодействовать как с кислотными, так и с основными оксидами, например:
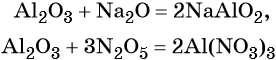
С водой амфотерные оксиды не взаимодействуют.
Кислотные оксиды реагируют с основными оксидами с образованием солей; с основаниями, с образованием солей и воды или кислых солей, а также с водой, в том случае если образующаяся в ходе такой реакции кислота растворима в воде:
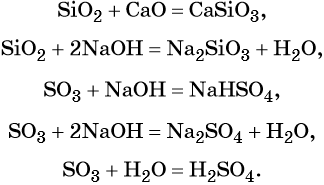
Кроме того, кислотные оксиды вступают в окислительно-восстановительные и обменные реакции:
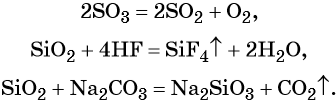
Тренировочные задания
1. Оксид натрия взаимодействует с каждым из двух веществ:
1) серная кислота и вода
2) уксусная кислота и азот
3) оксид лития и фосфор
4) оксид бария и серная кислота
2. Оксид калия взаимодействует с
1) азотом и фосфором
2) водой и сульфатом натрия
3) серной кислотой и оксидом фосфора (V)
4) литием и хлоридом натрия
3. Оксид кальция взаимодействует с
1) оксидом кремния
2) оксидом углерода (II)
3) оксидом азота (II)
4) оксидом азота (I)
4. Оксид бария взаимодействует с каждым из двух веществ:
1) азотной кислотой и водой
2) уксусной кислотой и хлором
3) оксидом натрия и азотом
4) оксидом серы (IV) и кремнием
5. Оксид магния не взаимодействует с
1) соляной кислотой
2) серной кислотой
3) оксидом лития
4) оксидом кремния
6. Оксид кальция взаимодействует с каждым из двух веществ:
1) оксидом фосфора (V), водой
2) оксидом углерода (IV) и сульфидом натрия
3) оксидом магния и азот
4) кислородом и сульфатом натрия
7. Оксид кальция реагирует с
1) медью
2) фосфором
3) оксидом углерода (IV)
4) оксидом магния
8. Оксид натрия реагирует с
1) водой
2) сульфатом калия
3) нитратом железа (II)
4) оксидом азота (II)
9. Оксид бария реагирует с каждым из двух веществ:
1) оксидом азота (II) и хлором
2) азотной кислотой и водой
3) оксидом углерода (II) и железом
4) серой и хлоридом кальция
10. Оксид магния реагирует с каждым из двух веществ:
1) оксидом кальция и оксидом железа (II)
2) оксидом алюминия и оксидом хрома (II)
3) соляной кислотой и оксидом кремния (VI)
4) оксидом фосфора (V) и цинком
11. Оксид цинка
1) растворяется в кислотах, но не реагирует с основаниями
2) растворяется в щелочах, но не реагирует с кислотами
3) реагирует с оксидом натрия, но не реагирует с водой
4) реагирует с оксидом калия и водой
12. Оксид хрома (III) реагирует с
1) оксидом калия
2) водой
3) оксидом серы (VI)
4) оксидом азота (I)
13. Оксид алюминия амфотерен, поскольку он способен взаимодействовать
1) как с азотной, так и серной кислотой
2) с водой и кислотами
3) с водой и щелочами
4) как с кислотами, так и со щелочами
14. Оксид алюминия реагирует с
1) сульфатом калия
2) оксидом калия
3) оксидом азота (II)
4) оксидом углерода (IV)
15. Оксид серы (VI) взаимодействует с каждым из двух веществ:
1) оксидом лития и углекислым газом
2) водой и углекислым газом
3) водой и гидроксидом калия
4) кислородом и натрием
16. Оксид фосфора (V) взаимодействует с каждым из двух веществ:
1) кислородом и водородом
2) водой и углекислым газом
3) водой и гидроксидом натрия
4) водой и оксидом углерода (II)
17. Оксид серы (VI) не взаимодействует с
1) водой
2) хлоридом калия
3) гидроксидом натрия
4) оксидом бария
18. Оксид серы (IV) взаимодействует с
1) оксидом углерода (IV) и водой
2) оксидом фосфора (V) и водой
3) сульфатом калия и водой
4) оксидом кальция и гидроксидом натрия
19. Оксид серы (IV) не взаимодействует с
1) водой
2) фосфатом кальция
3) раствором гидроксида натрия
4) гидроксидом кальция
20. Оксид хлора (VII) взаимодействует с каждым из двух веществ:
1) кальцием и углекислым газом
2) водой и углеродом
3) водой и оксидом калия
4) кислородом и азотом
21. Установите соответствие между реагирующими веществами и продуктами реакций.
22. Установите соответствие между реагирующими веществами и продуктами реакций.
23. Установите соответствие между реагирующими веществами и продуктами реакций.
24. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) CaO + SiO2 →
Б) CaO + H3PO4 (разб.) →
В) CaO + HCl →
25. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) ZnO + HCl →
Б) ZnO + NaOH ⎯⎯ H2O →
В) ZnO + Na2O ⎯⎯ сплавление →
26. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) ZnO + H3PO4 →
Б) ZnO + NaOH + H2O →
В) ZnO + C →
27. Установите соответствие между реагирующими веществами и продуктами реакций.
28. Установите соответствие между реагирующими веществами и продуктами реакций.
29. Установите соответствие между реагирующими веществами и продуктами реакций.
30. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) SO2 + H2S →
Б) SO2 (изб.) + NaOH →
В) SO2 + NaOH (изб.) →
31. Дана схема превращений:
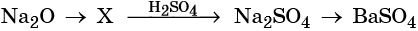
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
32. Дана схема превращений:
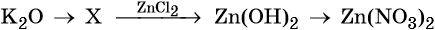
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
33. Дана схема превращений:
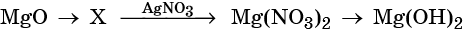
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
34. Дана схема превращений:
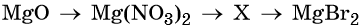
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции.
35. Дана схема превращений:
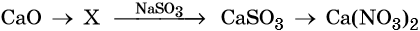
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
36. Дана схема превращений:
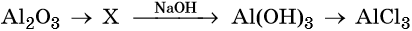
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
37. Дана схема превращений:
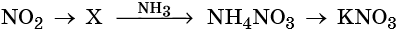
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
38. Дана схема превращений:
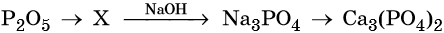
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
39. Дана схема превращений:
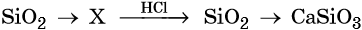
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
40. Дана схема превращений:
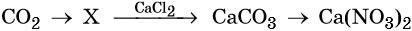
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
41. Дана схема превращений:
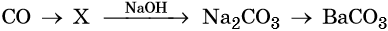
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
42. Дана схема превращений:
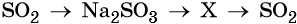
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции.
43. Дана схема превращений:
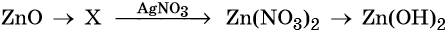
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
44. Дана схема превращений:
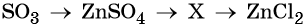
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
45. Дана схема превращений:
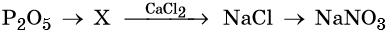
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
46. Дана схема превращений:
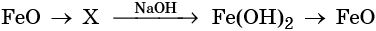
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
47. Дана схема превращений:
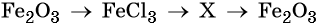
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции.
48. Дана схема превращений:
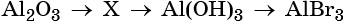
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
49. Дана схема превращений:
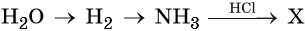
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
50. Дана схема превращений:
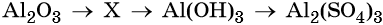
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
Задача 827.
Рассчитать, какое количество бертолетовой соли можно получить из 168 г гидроксида калия.
Решение:
М(КОН) = 56 г/моль, m(KOH) = 6 . 56 = 336 г;
М(KClO 3 ) = 122,45 г/моль, m(KClO 3 ) = 122,45 г.
Уравнение реакции имеет вид:
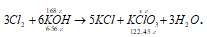
Находим массу бертолетовой соли из пропорции:
168 : 336 = х : 122,45; х = (168 . 122,45)/336 = 61,225 г.
Количество бертолетовой соли рассчитаем из уравнения:
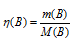
где 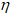
(B) - количество вещества, моль;
m(B) - масса вещества, г;
M(B) - молярная масса вещества (В), г/моль.
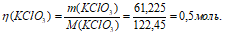
Ответ: m(KClO3) = 61,225 г; М(KClO3) = 0,5 моль.
Задача 828.
Как получить хлорную известь, исходя из карбоната кальция, хлорида натрия и воды? Написать уравнения процессов, которые необходимо для этого осуществить. Какие при этом получаются побочные продукты?
Решение:
Получение хлорной извести, исходя из карбоната кальция, хлорида натрия и воды.
а) При нагревании в 1000 0 С карбонат кальция разлагается на оксид кальция и углекислый газ:
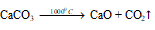
б) Оксид кальция, растворяясь в воде, образует гидроксид кальция:
в) Электролизом водного раствора хлорида натрия можно получить хлор, который выделяется у анода:
г) При действии хлора на гашеную известь получается так называемая белильная (или хлорная) известь и вода:
CaOCl2 соответствует структурная формула:
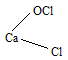
Хлорная известь применяется для отбелки растительных волокон (тканей, бумаги) и для дезинфекции.
Задача 829.
Обосновать невозможность получения оксидов хлора непосредственным взаимодействием хлора с кислородом.
Решение:
Хлор непосредственно не взаимодействует с кислородом. Это обусловлено небольшой энергией связи Cl—O и невозможностью использования высоких температур для осуществления реакций:
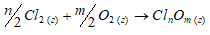
Задача 830.
Указать лабораторный и промышленный способы получения хлората калия.
Решение:
а) В лаборатории хлорат калия получают электролизом горячего раствора КCl:
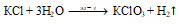
При охлаждении раствора хлорат калия выпадает в осадок, так как мало растворим в холодной воде.
б) В промышленности хлорат калия получают пропусканием хлора в горячий раствор гидроксида калия:
3Cl2 + 6KOH 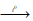
5KCl + KClO3 + 3H2O.
Поскольку хлорат калия (или бертолетовая соль) мало растворим в холодной воде, то при охлаждении раствора он выпадает в осадок.
В промышленности оксид кальция получают
термическим разложением известняка (карбоната
CaCO3 = CaO + CO2
Также оксид кальция можно получить при взаимодействии простых веществ:
или при термическом разложении гидроксида кальция и кальциевых солей некоторых кислородсодержащих кислот:
2Ca(NO3)2 = 2CaO + 4NO2 + O2
Получают взаимодействием хлора с гашеной известью (гидроксидом кальция):
Реально продукт, получаемый хлорированием гидроксида кальция, является смесью соединений, образованных молекулами Ca(OCl)2, CaCl2, Ca(OH)2 и кристаллизационной воды. Формально его состав выражают формулой Ca(Cl)OCl.
Общая характеристика бора,хим.св-ва,его получение. элемент главной подгруппы третьей группы, второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 5. Обозначается символом B (лат. Borum). В свободном состоянии бор — бесцветное, серое или красное кристаллическое либо тёмное аморфное вещество. Известно более 10 аллотропных модификаций бора, образование и взаимные переходы которых определяютсятемпературой, при которой бор был получен.Впервые был получен в 1808г:B2O3+6K=2B+3K2O
Из природного сырья:2Ca2B6O11+4Na2CO3+H2O=3Na2B4O7+4CaCO3+2NaOH;Na2B4O7+H2SO4+5H2O=4H3BO3+Na2SO4;2H3BO3=B2O3+3H2O(обезвоживание)
Технический амфотерный B2O3+3Mg=2B+3MgO
Но можно Na2B4O7+3Mg=2B+3MgO+2NaBO2
Особо чистый: B2H6=2B+3H2;
В химическом отношении бор довольно энертен,при обычных условиях взаимодействует только со фтором:
2B+3F=2BF3;С повышение t активность бора возрастает.t= 400 реагирует с Cl2,при 600 с Br2,при 700 с I2
t>600 с халькогенами B2Г3,выше 900 с фосфором ВР,при 1200 с азотом BN и около 2000 с углеродом-карбиды B12C3,B13C2.С водородом непосредственно не реагирует,кислоты не явл.окислителями не с бором не реагируют,концентрированная азотная,серная и царская водка окисляют до борной кислоты:
При сплавлении на воздухе(либо в присутствии другого окислителя) со щелочами образ.бораты:
Получение Al,его оксида и гироксида в промышленности.
А)Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием расходуемых коксовых или графитовых электродов.
1)диссоциация Al2O3 в расплаве Al2O3↔Al(+3)+AlO3(3-)
Общая характеристика и хим.св-ва Al,In,Ga,Tl
р-элемены.Основной степенью окисления остальных хим.эл-тов (+3).Исключение составляет таллий(+1).Соединения Tl(+1) могут быть переведены в состояние Tl(+3) только сильными окислителями.Таким образом в группе по вертекали от бора к таллию увелич.стабильность низших степеней окисления.Соединения элементов это подгруппы имею структуру:1)треугольная плоская,за счет sp2-гибритизации(ЭГ3)
2)тетраэдрическая структура sp3-гибритизации
3)октаэдрическая за счет sp3d2-гибридных АО.В ряду напряжений эти металлы стоят левее водорода и вытесняют его из кислоты.
На воздухе In,Ga покрыты оксидной пленкой,Tl на воздухе быстро окисляется.
Оксид,гироксид,соли Al: их получение с св-ва
Al2O3-существует в основном в виде трех кристаллических модификаций.Аморфный Al2O3,алюмогель,образуетя при дегидратации(иногда частичной) гелеобразного гидроксида Al(OH)3 или при термич.разложении ацетата алюминия:
Прокаленный оксид инертен и лишь при нагревании растворяется в щелочах:
При сплавл. С щлочами образ.мета-алюминаты
Типичное афотерное соединение
При высокотемпературном сплавлении с кремнеземом SiO2 оксид алюминия образует многочисленные алюмосиликаты.
(пример (Na,K)Al2Si2O8).Алюминиевые квасцы
M2SO4∙Al2(SO4)3∙24H2O(M-Na,K)Алюминий при высоких температурах прямым синтезом образует бориды,карбиды,нитриды,сульфиды.
Общая характеристика и хим.св-ва азота.
Азот -без цвета и запаха,малорастворим в воде.Проявляет очень слабые в-ные и ок-ные св-ва.При комнатной t он реагирует только с литием.
при нагревании он реагирует с некоторыми другими металлами и неметаллами, также образуя нитриды:
N2(г) + 3H2(г) ↔ 2NH3(г) + 91,84 кДж
Используется для получения аммиака,а так же в качестве инертного газа в с-ме.
Характеристика и химические св-ва углерода.
Среднее содержание С в земной коре составляет 0,48% по массе.Значительная часть углерода литосферы сосредоточена в известняках(СаСО3),
доломитах и др.Огромное кол-во выделяется при сжигании топлева.В атоме углеровада число валентных электронов равно числу вал.орбителей..
Углерод образует ковалентные связи со многими эл-ми,как с эл.полож. так и с эл.отриц,может проявлять валентность II,IV,и степени окисления (-4),(0),(+2),(+4).Важная особенность:р-орбитали его атома перекрываясь с р-орбиталями атомов,имеющих близкие размеры,способны образовывать прочные п-связи.Имеет алотропные модификации:алмаз,графит,карбин,фуллерен,нанотрубки,а так же аморфные формы.Углерод реагирует со многими элементами. Соединения с неметаллами имеют свои собственные названия — метан, тетрафторметан.Продукты горения углерода в кислороде являются CO и CO2(монооксид углерода и диоксид углерода соответственно). Известен также неустойчивый недооксид углерода С3О2 (температура плавления −111 °C, температура кипения 7 °C) и некоторые другие оксиды (например C12O9, C5O2, C12O12). Графит и аморфный углерод начинают реагировать с водородом при температуре 1200 °C, с фтором при 900 °C.Углекислый газ реагирует с водой, образуя слабую угольную кислоту — H2CO3, которая образует соли — карбонаты. На Земле наиболее широко распространеныкарбонаты кальция.Графит с галогенами, щелочными металлами и др. веществами образует соединения включения. При пропускании электрического разряда между угольнымиэлектродами в атмосфере азота образуется циан. При высоких температурах взаимодействием углерода со смесью Н2 и N2 получают синильную кислоту:
При реакции углерода с серой получается сероуглерод CS2, известны также CS и C3S2. С большинством металлов, алюминием и кальцием углерод образует карбиды, например:
Ca+2C=CaC2(t)Важна в промышленности реакция углерода с водяным паром:С+Н2О=СО+H2 (газификация твердых топлив)
Общая характеристика и хим.св-ва германия,свинда,олова.Германий явл.рассеяным эл-том.Есть более 12-ти минералов,но нет самостоятельных руд.Олово и свинец-рдкие металлы.В природе редко встречаются в свободном сосояние.Геомания,имея кристаллическую решетку,как у алмаза,обладает высокой твердостью и проявл.полупроводниковые св-ва.Олово сущ.в виде трех аллотропных модификаций .Свинец самый мягкий среди тяжёлых металлов.
В присутствии ок-лей:
Ge+4HCl(k)+2H2O2=GeCl4+4H2O(с примесью H2[GeCl6])
Лучше всего р-ется в царской водке:
Растворяются в концентрированной азотной и серной к-тах.
В отличии от германия,олово и свинец взаимодействуют с водным р-ром щелочи и в остсутствии ок-лей
(в присутствии О2 свинец и олово р-ют с орг.к-ми)
Последнее изменение этой страницы: 2016-08-16; Нарушение авторского права страницы
Читайте также:

