Ученый который нашел решение рака
Ученые нашли причину появления рака. Можно ли от него защититься?
Фото: Phanie / NCI-ARNOLD / Diomedia
Опасные сожители
Известно, что основными причинами рака являются курение, нездоровое питание, а также воздействие инфекционных агентов, включая вирусы, бактерии и паразитов. Инфекции стоят на третьем месте среди лидирующих факторов развития опухолей и отвечают за 10 процентов смертей от этой болезни. В то же время на поверхности и внутри человеческого тела обитают миллионы микроорганизмов, чей состав уникален для каждого человека и составляет его микробиом. Микробиом влияет на здоровье человека, защищает его, но при нарушениях может спровоцировать развитие целого ряда заболеваний, включая онкологические. Микробы отвечают за уязвимость к раку, его прогрессирование и восприимчивость к лечению.
Важную роль в защите от бактерий играет слизистая оболочка, выстилающая внутреннюю поверхность пищеварительных, дыхательных и других органов. Она содержит гликопротеины — соединения, пронизывающие мембраны клеток эпителия. Эти молекулы формируют защитный слой. Степень гликозилирования (то есть уровень гликопротеинов) слизистой оболочки определяет уровень невосприимчивости к инфекциям. Однако во время заражения происходят изменения в гликопротеинах, затрагивающие как ту часть (домен), что находится внутри клетки, так и наружную. Это может либо способствовать ликвидации микроба, либо привести к инфекции и воспалению.
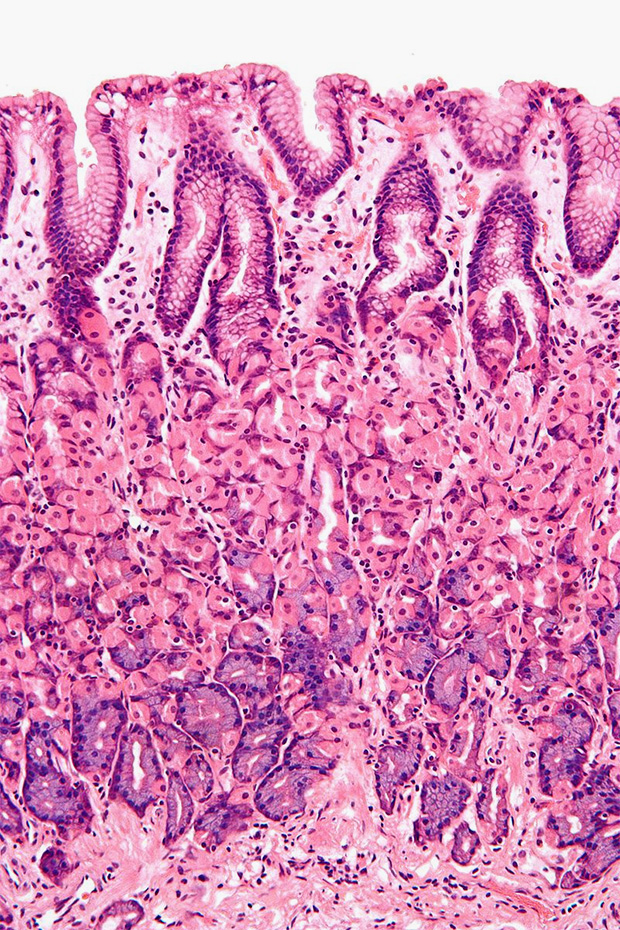
Слизистая оболочка и эпителиальная ткань
Защитник и враг
Когда наружная часть MUC1 связывается с бактерией, происходит отделение внутреннего домена. К нему присоединяются фосфорные остатки, что запускает целый ряд разных процессов: синтез провоспалительных факторов, адгезию (сцепление) эпителиальных клеток, их дифференциацию и программируемую клеточную смерть, называемую апоптозом.
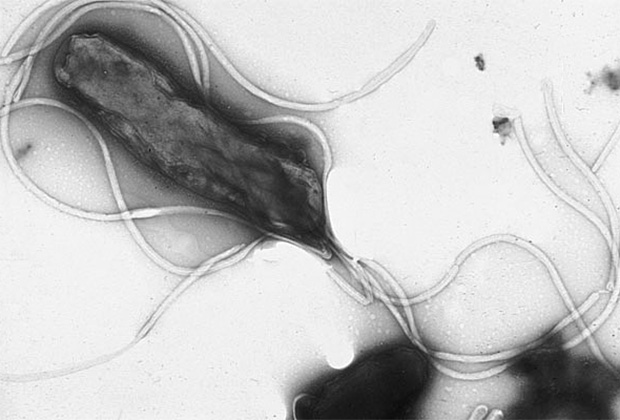
Пока бактерии не рассматриваются как основная причина раковых заболеваний в отличие от тех же вирусов. Лишь для нескольких бактерий показано, что они могут спровоцировать развитие злокачественных опухолей через провоцирование воспалительных процессов, выделение токсинов и других повреждающих ДНК метаболитов или нарушение сигнальных путей клеток. Известны две широко распространенные бактериальные инфекции, которые могут вызывать рак. Это Helicobacter pylori, связанная с раком желудка и лимфомой, и Salmonella typhi, связанная с карциномой желчного пузыря у тех, кто страдает от хронического тифа. Но могут быть и другие инфекции, повышающие риск.
Главные угрозы
Campylobacter jejuni — одна из самых частых причин инфекционных отравлений, возбудитель кампилобактериоза. Бактерия проникает через слизистый слой в эпителиальную ткань пищеварительного тракта, провоцируя гастроэнтерит. Когда микроорганизм связывается с MUC1, гликопротеин высвобождается вместе с микробом в слой слизи. Пока неизвестно, предотвращает ли это развитие рака. Сама бактерия попадает в организм человека через загрязненную пищу и воду. В группу риска входят дети, пожилые люди, пациенты с ослабленным иммунитетом. Методом профилактики является правильное приготовление пищи.
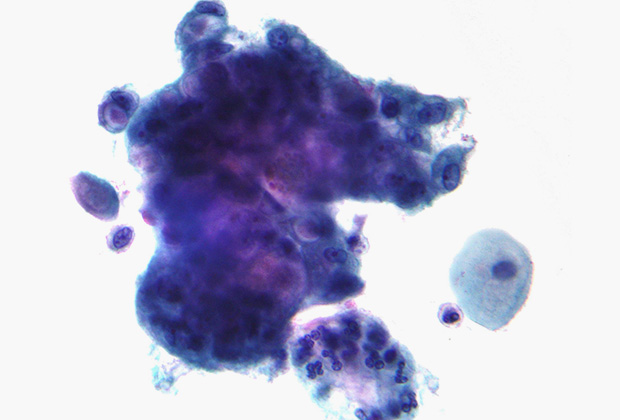
Клетка с вакуолями, содержащими муцины
Хроническая инфекция Helicobacter pylori приводит к язвам и раку. Показано, что муцины являются важным препятствием для бактерии. Однако внутриклеточный домен MUC1 при связывании с бактерией способен взаимодействовать с NF-kB — транскрипционным фактором, который отвечает за регулирование апоптоза и клеточного цикла. Нарушение регуляции данного сигнального пути приводит к воспалениям, аутоиммунным заболеваниям и развитию опухолей. Для профилактики инфекции специалисты рекомендуют соблюдать гигиену рук. Заражение происходит через контакт с загрязненными предметами и людьми — носителями инфекции.
Haemophilus influenzae вызывает инфекции дыхательных путей, в том числе пневмонию. При хронической обструктивной болезни легких (ХОБЛ) дыхательные пути часто колонизируются этой бактерией. Кроме того, ХОБЛ является одним из факторов риска рака легких. Показано, что взаимодействие микроба с MUC1 вызывает изменения в регуляции специфических рецепторов, которые, в свою очередь, участвуют в прогрессировании легочных аденокарцином.
Еще одним потенциальным виновником опухолей является кишечная палочка Escherichia coli, возбудитель заболеваний кишечника. При взаимодействии микроба с MUC1 возникает воспалительный процесс. Показано, что инфекции связаны с колоректальным раком и раком мочевого пузыря, но пока не совсем понятно, могут ли они быть онкогенным фактором.
Другие вредители
Среди онкогенных вирусов достаточно известны вирус Эпштейна-Барр (вирус герпеса) и вирус папилломы человека. Первый ассоциирован с крайне агрессивной назофарингеальной карциномой (рак носоглотки), лимфомой Ходжкина (рак лимфатической системы), лимфомой Беркитта, Т-клеточной лимфомой и раком желудка. Второй может вызвать рак шейки матки, а также опухоли на гениталиях, в заднем проходе, горле и голове. При отсутствии вируса рак шейки матки не развивается, то есть это заболевание четко связано с хронической инфекцией.
Опасность представляют и другие вирусы, в том числе возбудитель гриппа, однако при подобных инфекциях MUC1 эффективно защищает слизистую от патогена. Вирус гепатита часто становится причиной рака печени.
Что касается паразитов, то к онкологическим заболеваниям могут привести заражение кровяной шистосомой, которая проникает в организм человека через мочевыводящие пути. Червь провоцирует развитие плоскоклеточного рака мочевого пузыря, являясь второй ведущей причиной этого заболевания. Заражение обычно происходит в тропических регионах планеты при купании в естественных водоемах. Часто жертвами паразита становятся туристы и жители развивающихся стран с неблагополучной санитарной обстановкой. По подсчетам, во всем мире инфицировано более 207 миллионов человек.
Еще одним онкогенным паразитом является червь Opisthorchis viverrini, заражающий желчный пузырь и способствующий развитию холангиокарциномы. Этот тип опухолей редко встречается в западных странах, но распространен в Юго-Восточной Азии.
Как спастись
Некоторое время назад исследователи из Американского онкологического общества (ACS) пришли к выводу, что причиной половины случаев заболевания раком является нездоровый образ жизни. В целом внешние факторы среды отвечают за львиную долю онкологических заболеваний, неподконтрольными остаются лишь генетические факторы и просто случайные мутации в ДНК, на которые мы никак не можем повлиять.
Многие из воздействий можно исключить, другие — снизить до минимума. Среди этих мер обычно называют поддержание здорового веса, физические упражнения, отказ от курения и алкоголя, избегание длительного воздействия солнечных лучей и контакта с различными химическими загрязнителями. Однако теперь к этому можно добавить прививки (особенно, от ВИЧ и гепатита) и другие типы профилактики инфекционных и паразитарных заболеваний.








К сожалению, у меня не осталось фотографий, где я в самом начале болезни, когда еще не выпали волосы после химиотерапии. У меня украли ноутбук с жестким диском, где был фотоархив: прямо возле онкологического центра, где я проходила лечение, разбили стекло в машине и все вытащили. Кроме первой серии проекта, пропали все съемки за последние три года. Для меня это был удар. Тогда я постоянно думала, как бы не сломаться, как бы не опустить руки. Какое-то время я даже не фотографировала. . Фото: Алена Кочеткова
- Опухоли - это расплата за эволюцию, - говорит известный онколог, руководитель отдела лекарственного лечения опухолей Московского научно-исследовательского онкологического института им. П.А. Герцена Николай Жуков. - Геном человека меняется, неизбежно возникают мутации, накопление самых опасных из них ведет к раку.
Поэтому практически нереально добиться, чтобы онкоболезни полностью исчезли с лица Земли. Однако прорывы в медицине позволят превратить рак в несмертельную хроническую болезнь, с которой люди смогут жить долгие годы, считают ученые. Эксперты обсудили самые передовые и многообещающие методы диагностики и лечения на Международной конференции OncoTech, которая прошла в Федеральном научно-клиническом центре детской гематологии, онкологии и иммунологии им. Димы Рогачева в Москве .
1. Иммунотерапия
- Два самых мощных метода воздействия на опухоли - хирургия и лучевая терапия - достигли потолка своей эффективности, - поясняет Николай Жуков . - После того, как научились проводить тотальное облучение всего тела и удалять целые органы, выше уже не прыгнуть. Поэтому самые большие горизонты сейчас открываются в лекарственном лечении рака.
Одно из прорывных направлений - иммунотерапия.
Врачи отмечают, что во многих случаях больным даже удается избежать алопеции (облысения) и нейтропении (опасный побочный эффект, когда гибнут клетки-нейтрофилы, отвечающие за распознавание и уничтожение опасных микробов. - Авт.). Однако такой метод, к сожалению, мало подходит для людей, чей организм серьезно ослаблен облучением и лекарствами более старых поколений, которые сильно били по иммунитету.
ВАЖНО
В России некоторые средства иммунотерапии (препараты на основе так называемых моноклональных антител) входят в программы бесплатного лечения онкозаболеваний. В частности, они используются при лечении рака молочной железы, желудка, кишечника, лимфом.
2. Вирусы против опухоли
Недавно в США и Европе был одобрен для лечения рака первый в мире препарат с онколитическим вирусом.
Сейчас запатентован такой способ лечения для меланомы - одной из самых агрессивных и смертоносных форм рака кожи, очень быстро дающей метастазы. Пациентам вкалывают препарат прямо в опухоль, и, как показали клинические испытания, очаги рака начинают уменьшаться.
3. Всемирное досье на рак
- В каждой человеческой клетке постоянно происходит огромное количество реакций, представьте себе: число пар нуклеотидов, то есть соединений, которые образуют нашу с вами ДНК, свыше 3 миллиардов! - увлеченно рассказывает руководитель Московского Центра исследований и разработок EMC по облачным технологиям и большим данным Камиль Исаев. - Чтобы сделать диагностику болезней максимально ранней и точной - а для рака это важно в первую очередь, нужно расшифровать геном человека и понять, за что отвечает тот или иной ген. Затем выяснить, какие мутации и в каких генах запускают рост разных видов опухолей. И как люди с определенными генотипами реагируют на разные лекарства против рака.
- Когда исследователи начали анализировать опухоли на генетическом уровне, выяснилось: даже у одного человека в одном органе нередко возникают разные типы раковых клеток. Они по-разному реагируют на лекарства, - говорит онколог Николай Жуков.
Сейчас уникальный алгоритм используется в рамках экспериментального лечения в нескольких московских медицинских центрах, в том числе в Институте имени Герцена .
5. Ранний диагноз по крови
Новое открытие поможет бороться с раком лёгких, который плохо подаётся терапии.
Иллюстрация Global Look Press.
Специалисты из России обнаружили вещества, препятствующие росту самых опасных злокачественных опухолей. Важное открытие может стать основой для новых стратегий лечения этой смертоносной болезни.
Достижение описано в научной статье, опубликованной в журнале Bioscience Reports учёными из Центра высокоточного редактирования и генетических технологий для биомедицины, в который входят Институт молекулярной биологии им. В.А. Энгельгардта РАН, Институт биологии гена РАН, РНИМУ им. Пирогова Минздрава России и Федеральный научно-клинический центр физико-химической медицины ФМБА России.
Известно великое множество видов рака. Однако большинство смертей от онкологических заболеваний приходится на рак лёгких, если же говорить точнее, то на немелкоклеточный рак лёгкого. Злокачественные опухоли этого типа очень агрессивны и с трудом поддаются терапии.
Теперь исследователи обнаружили группу белков, участвующих в естественной защите организма от этого зла. Подробнее изучив функционирование этих белков, учёные смогут создать новые стратегии лечения рака.
Речь идёт о фосфатазах CТDSP1, CTDSP2 и CTDSPL. Они участвуют во многих жизненно важных для клетки процессах. Но лишь недавно российские специалисты обнаружили у этих белков новую функцию: противодействие раку.
Отметим, что это не первые известные белки, препятствующие развитию онкологических заболеваний. Но каждое такое открытие бесценно для человечества, потому что дарит надежду на спасение многочисленным пациентам, которым угрожает смерть от опасного недуга.
Исследователи из нескольких российских НИИ обнаружили, что фосфатазы замедляют рост аденокарциномы лёгкого (это один из типов злокачественной опухоли при немелкоклеточном раке лёгкого) и вызывает старение раковых клеток. Подчеркнём, что эксперименты проводились на культурах тканей, то есть "в пробирке".
В чём может быть секрет "целебного" действия этих фосфатаз? Специалисты полагают, что они помогают другому нашему естественному защитнику – белку Rb. Фосфатазы способствуют выработке активных форм этого белка, способных противостоять опухоли.
Более того, учёные обнаружили, что нехватка упомянутых фосфатаз может способствовать развитию онкологического заболевания. Эксперимент показал, что активация хорошо известной группы онкогенов miR-96/182/183 ведёт к уменьшению количества спасительных ферментов. Естественно предположить, что с этим и связано зловредное действие опасных генов.
Пока ещё рано говорить о том, какие лекарства можно создать благодаря этим новым знаниям. Это дело будущих исследований, но вряд ли они заставят себя долго ждать.
К слову, ранее Вести.Ru рассказывали о том, что в России успешно опробовали новый метод диагностики рака. Также учёные нашей страны нашли белок, делающий клетки рака более чувствительными к химиотерапии.













Учёные под руководством профессора химического факультета МГУ и Университета Северной Каролины Александра Кабанова исследовала действие наномицелл противовирусного препарата резикимод против злокачественной опухоли легких.
Ученые провели испытания на лабораторных мышах и показали эффективность резикимода по сравнению с альтернативными видами терапии. Результаты исследования опубликованы в журнале Science Advances.
Мелкоклеточный рак легкого (НМРЛ) – самое распространенное злокачественное новообразование легких (от 80 до 85% случаев рака легких) и причина большинства смертей от рака во всем мире. Послеоперационный рецидив и метастазирование вызывают гибель в значительном проценте случаев НМРЛ.
Развитие опухолей обеспечено несколькими механизмами защиты от иммунной системы организма.
Programmed cell death-1 (PD-1) – рецептор, играющий ключевую роль в толерантности Т-клеток иммунной системы к нормальным клеткам организма. Для обмана иммунитета онкоклетки активно экспрессируют лиганд PD-L1, который связывается с PD-1 и выключает атаку T-клеток на раковую опухоль. Управление за качеством пищевых продуктов и медикаментов CША (Food and Drug Administration, FDA) одобрило лечение НРМЛ с помощью ингибиторов PD-1/PD-L1, однако большинству пациентов с НРМЛ такая терапия не помогает.
Пока в онкотерапии применяют только один препарат-антагонист TLR7 имиквимод – крем для лечения поверхностного базальноклеточного рака и бородавок. Плохая растворимость низкомолекулярных антагонистов TLR в воде снижает их эффективность в качестве противоопухолевых препаратов. В виде наночастиц, не превышающих 100 нм, антагонисты TLR можно адресно доставить до опухолей.
Сотрудники Университета Северной Каролины в Чапел-Хилле (США) под руководством профессора кафедры химической энзимологии химического факультета МГУ и Университета Северной Каролины, члена-корреспондента РАН Александра Кабанова синтезировали наномицеллы препарата резикимод и проверили его противопухолевую активность на лабораторных мышах.
Резикимод, антагонист TLR7 и TLR8, был разработан ранее как стимулятор противовирусного иммунного ответа. Однако он оказался слишком активным и вызывал гриппоподобный симптом, сродни цитокиновому шторму, о котором сейчас широко известно благодаря COVID-19. Из-за побочных эффектов для лечения вирусных заболеваний резикимод не подошёл. Однако, подобные побочные эффекты от вещества хорошо изучены в иммунотерапии рака, поэтому российские и американские ученые решили попробовать резикимод против НМРЛ.
Ученые показали, что резикимод снижает рост опухоли и многократно увеличивает продолжительность жизни больных животных, чего не наблюдается в случае ингибитора PD-1. Медиана выживаемости у больных животных, которых лечили резикимодом, более чем в два раза превышала выживаемость у группы, которой давали терапию ингибитором PD-1. Обычные химиотерапевтические препараты против таких опухолей бессильны.
Невероятно, но современная история исследования рака начинается с морских ежей. В первом десятилетии 20 в. немецкий биолог Теодор Бовери обнаружил, что если оплодотворить яйца морских ежей не одним, а двумя спермиями, то некоторые из клеток в конечном итоге будут иметь нарушения в наборе хромосом и не смогут правильно развиваться. Ещё до возникновения современной генетики, Бовери знал, что раковые клетки, как и измененные клетки морских ежей, содержат неправильные хромосомы; он предположил, что, чем бы ни был вызван рак, это каким-то образом влияет на хромосомы.
В наши дни именно Бовери знаменит как первооткрыватель природы рака, но другой немецкий ученый, Отто Варбург, изучал клетки морских ежей примерно в тоже время, что и Бовери. Его исследование тогда было расценено как крупный прорыв в нашем понимании рака. Однако в последующие десятилетия открытие Варбурга почти полностью пропало из раковых хроник, его вклад считался столь незначительным, что упоминания о нем исчезли и из учебников.
В отличие от Бовери, Варбурга не интересовали хромосомы морских ежей. Вместо этого Варбург сосредоточил внимание на энергии, получаемой клетками — на том, что способствовало их росту. Со временем Варбург переключился с морских ежей на опухолевые клетки крыс. В 1923 году он уже знал, что клетки морских ежей с ростом существенно увеличивают потребление кислорода, поэтому ожидал увидеть тот же эффект у крыс. Вместо этого раковые клетки, подпитывая собственный рост, поглощали глюкозу (сахар в крови) в громадных количествах и усваивали ее, обходясь без кислорода. Это не имело никакого смысла. Реакции, вызванные поглощением кислорода, гораздо более эффективны в планепреобразования питательных веществ в энергию, а раковым клеткам было доступно много кислорода. Однако когда Варбург проводил дополнительные эксперименты, в том числе и на человеческой опухоли, он каждый раз получал один и тот же результат. Раковые клетки жаждали глюкозы.
Это открытие впоследствии было названо эффектом Варбурга, который встречается примерно в 80% случаев рака. Это настолько распространенное явление для раковых опухолей, что при проведении позитронно-эмиссионной томографии (ПЭТ), которая является важнейшим инструментом для определения стадии развития и диагностики рака, томограф просто выявляет места, где клетки поглощают глюкозу в излишних количествах. В большинстве случаев, чем больше глюкозы потребляют клетки, тем хуже состояние пациента.

Как правило, в каждом отдельном случае наблюдается множество раковых мутаций. Однако существует определенный набор способов, с помощью которых организм может поддерживать рост клеток. Раковые клетки прибегают к тем из них, которые не используются здоровыми клетками. Ученые, стоящие в авангарде возрождения идей Варбурга, возлагают свои надежды на то, что можно замедлить — или даже остановить — рост опухоли, если прервать одну или большинство химических реакций, которые используют клетки для активного размножения и при этом заставить клетки голодать от недостатка питательных веществ, в которых те отчаянно нуждаются.
Родившись в 1883 году в знаменитой семье Варбургов, Отто Варбург воспитывался как будущий вундеркинд от науки. Еще задолго до смерти Варбург был признан одним из величайших биохимиков 20 века, человеком, чьи открытия стали ключевыми не только в области исследования рака, но также в сфере понимания природы фотосинтеза и дыхания клеток. В 1931 году он стал лауреатом Нобелевской премии за свою работу о дыхании и еще дважды на нее выдвигался — оба раза за разные открытия. Согласно отчетам, он должен был снова удостоиться ее в 1944 году, но нацисты запрещали немецким гражданам принимать Премию.
Даже если эта теория может объяснить причины эффекта Варбурга, она все еще оставляет нерешенным вопрос о том, что именно толкает клетку на путь к эффекту Варбурга и раку. Ученые из ряда лучших онкологических больниц страны возглавили кампанию по возобновлению изучения эффекта Варбурга, надеясь найти ответ. Эти исследователи, в большинстве своем молекулярные биологи по образованию, обратились к проблемам метаболизма и эффекту Варбурга, потому что их собственные исследования привели каждого из них к одному и тому же выводу: ряд генов, вызывающих рак, долгое время известные за их роль в клеточном делении, также регулируют процесс потребления клеткой питательных веществ.
Крэйг Томпсон, президент и исполнительный директор Ракового центра имени Слоуна Кеттеринга, является одним из самых ярых сторонников такого обновленного фокуса на метаболизме. Согласно приводимой Томпсоном аналогии, эффект Варбурга можно воспринимать как социальный провал: расторжение договора одноклеточных организмов об обмене питательными веществами, подписанного, когда они объединили силы и стали многоклеточными организмами. Его исследование показало, что для питания клеткам необходимо получать сигналы от других клеток, точно так же, как при делении. Томпсон выдвинул предположение, что если ему удастся определить, какие мутации влияют на чрезмерное употребление клеткой глюкозы, это позволит в значительной степени объяснить, как в клетке начинает развиваться эффект Варбурга и рак в целом. Но поиски таких мутаций не привели Томпсона к абсолютно новому открытию. Вместо этого, они привели его к АКТ (внутриклеточный фермент, один из трех членов семейства протеинкиназ В — прим. Newочём), гену, уже известному молекулярным биологам своей ролью в стимуляции деления клеток. Сейчас Томпсон считает, что АКТ играет еще более фундаментальную роль в метаболизме.
В то время как Томпсон придал новый смысл роли АКТ, Чи Ван Данг, директор Ракового центра им. Абрамсона в Университете Пенсильвании, помог миру онкологии по-настоящему оценить то, как один в значительной степени изученный ген может весьма существенно повлиять на метаболизм опухоли. В 1997 году Данг стал одним из первых ученых, объединивших научные сферы молекулярной биологии и клеточного метаболизма, когда продемонстрировал, что МУС (ген, который кодирует белок, связывающийся с ДНК и являющийся фактором транскрипции — прим. Newочём ) — так называемый регуляторный ген, известный своей ролью в пролиферации клеток — напрямую нацелен на фермент, который может запустить эффект Варбурга. Данг вспоминает, как другие исследователи скептически относились к его заинтересованности вспомогательными ферментами, но он не сдавался, потому что понял важность следующего факта: раковые клетки не могут перестать есть.

Семинар Варбурга: Институт клеточной физиологии им. Кайзера Вильгельма (на данный момент является частью Общества Макса Планка) в Берлине, 1931 г. Источник: архив Общества Макса Планка в Берлине
Терапевтические методы, основанные на изучении метаболизма, имели впечатляющие успехи. Компания Agios Pharmaceuticals, среди основателей которой и сам Томпсон, в настоящий момент тестирует препарат, применяемый в случаях острого миелоидного лейкоза, когда другие методы лечения были неэффективны. Препарат ингибирует мутировавшие элементы метаболического фермента IDH 2 (изоцитрат дегидрогеназы — прим. Newочём). Клинические испытания показали, что почти у 40% пациентов с данным видом мутации наблюдается по меньшей мере частичная ремиссия.
Принимая во внимание случай игнорирования Варбурга, вполне объяснимо, что возможно самый перспективный метаболический препарат для лечения рака на протяжении десятилетий находился у всех на виду. Этот препарат, метформин, уже широко применяется для понижения уровня глюкозы в крови у диабетиков (в 2014 году в США было выписано 76,9 млн рецептов). В последующие годы, скорее всего, метформин будут использовать для лечения рака или, по крайней мере, для профилактики развития некоторых его разновидностей. Ввиду того, что метформин способен влиять на ряд путей обмена веществ, точный механизм достижения им противораковых эффектов остается предметом споров. Однако результаты множества эпидемиологических исследований поразительны. У диабетиков, принимающих метформин, рак развивается со значительно меньшей вероятностью, чем у больных сахарным диабетом, не принимающих данный препарат; даже в случае развития онкологического заболевания вероятность летального исхода у первой группы по-прежнему значительно меньше.
К концу своей жизни Варбург становился все более и более одержим своей диетой. Он верил в то, что появление рака можно предотвратить, и считал, что добавление химикатов в пищу и сельскохозяйственные продукты может провоцировать рост опухолей, так как это вредит процессу дыхания. Он не ел хлебобулочные изделия, если они не были приготовлены у него дома. Он пил молоко, взятое у коров определенной породы, и использовал центрифугу в своей лаборатории для производства собственных сливок и масла.
Высокий уровень инсулина прочно связан с ожирением; ожидается, что оно в скором времени обгонит курение и станет лидирующим этиологическим фактором предотвратимых онкологических заболеваний. У разновидностей рака, связанных с ожирением и/или диабетом, присутствует большее количество рецепторов инсулина и ИФР-1, а у людей с дефектными рецепторами ИФР-1 фактически наблюдается иммунитет к раковым заболеваниям. Ретроспективные исследования, анализирующие истории болезни онкобольных, указывают на то, что многие больные с раком груди, поджелудочной железы или колоректальным раком имели повышенный уровень инсулина до постановки диагноза. Возможно, не так уж это и удивительно, что, когда исследователи хотят вырастить клетки рака груди в лаборатории, они добавляют инсулин в тканевую культуру. Когда они извлекают инсулин, раковые клетки погибают.
Исследователи из Университета Британской Колумбии выявили состояние, которое может стать предшественником рака. По мнению экспертов, уровень инсулина в крови напрямую связан с онкологическими заболеваниями.
Учёные нашли связь гиперинсулинемии - высокого уровня инсулина в крови - с раком. Специалисты отметили, что особенно страдает поджелудочная железа, которая быстрее изнашивается, вырабатывая в течение длительного периода слишком много инсулина, - сообщает "Medicalxpress".
"Связь между онкологией и гиперинсулинемией была обнаружена при различных раковых заболеваниях, включая, например, рак молочной железы", - пояснили эксперты.
Специалисты в ходе проведения экспериментов на мышах выяснили, что сниженный уровень инсулина позволяет защитить организм от рака поджелудочной железы. По словам учёных, данное исследование поможет улучшить диагностику онкологии. Эксперты добавили, что выявленное явление может распространить и на другие виды рака.
Названа причина смерти Марины Макаровой на 46 году жизни

Актриса из сериалов "Убойная сила", "Тайны следствия" Марина Макарова умерла в 45 лет

Ученые рассказали, могут ли комары быть разносчиками коронавируса
Доктор медицинских наук назвала первый симптом раковой опухоли щитовидной железы


В сети появилось фото, как Стас Пьеха коротко подстригся, но не побрился

Бывшая жена Владимира Машкова Елена Шевченко вышла замуж в США

В квартире Елены Батуриной обнаружили тело пенсионерки, сообщают СМИ

Врачи озвучили симптомы, которые могут указывать на раковую опухоль в кишечнике

Отец Фриске понадеялся, что Заворотнюк поможет то лекарство, которое не разрешили Жанне

Что мы знаем о биографии Наили Аскер-заде
-
Введите свой электронный адрес, после чего выберите любой удобный способ оплаты годовой подписки

Читайте также:


