Темпы роста доброкачественной опухоли
Хроническая системная болезнь с неумолимо прогрессирующим течением. История рака молочной железы начинается с одной мутантной клетки и заканчивается печальным исходом опухолевого роста: от начала до конца проходит от 2 до 20 лет.
От одной дефектной клетки до разросшейся опухоли в молочной железе
История рака молочной железы
Крайне редко бывает стремительный рост карциномы. История рака молочной железы – это временной промежуток от момента появления первой раковой клетки до гибели женского организма при достижении опухоли определенной критической массы. Длительность очень вариабельна: у большинства пациенток опухоль растет медленно, у редких женщин возникает взрывной рост в злокачественном узле. Скорость увеличения новообразования зависит от множества факторов, которые как ускоряют, так и замедляют прогрессирование рака. В любом случае, время всегда на стороне карциномы.
Скорость роста опухоли
Чаще всего медленно и неторопливо, но порой история рака молочной железы – это внезапный и резкий спурт опухолевого роста. Выделяют 2 варианта:
- Потенциальная скорость роста;
- Фактическая.
Первый показатель условен – мы можем предположительно оценить ситуацию, принять во внимание внутренние и внешние факторы, действующие на прогресс опухоли, и предположить, как будет увеличиваться карцинома. Второй показатель – суровая реальность у каждого конкретного человека. Статистически в жизни выделяют 3 варианта:
- Стремительный рак молочных желез (время удвоения размера первично возникшего новообразования составляет менее 30 дней), который бывает у 20% пациенток;
- Умеренный темп роста новообразования (время удвоения – до 100 дней, у 60% женщин);
- Медленные опухоли (более 110 дней, 20% пациенток).
Факторы замедляющие прогрессирование
Медленное увеличение объема опухолевой ткани объясняется следующими факторами:
- Замедление ангиогенеза (питающие рак сосуды не успевают обеспечивать быстрый рост опухолевой ткани);
- Некроз опухоли (частичное разрушение злокачественного новообразования);
- Влияние противоопухолевого иммунитета (организм продолжает бороться даже тогда, когда нет ни одного шанса на выживание);
- Метастазирование (уменьшение величины первичного очага за счет метастатического распространения опухоли).
В большинстве случаев история рака молочной железы – это путь от одной генетически дефектной клетки до смертельно опасного увеличения объема злокачественного новообразования. В среднем – это 10-12 лет (от 2 до 20 лет). Время всегда вассал раковой опухоли: неторопливая и размеренная инвазия с поглощением близлежащих тканей и захватом новых отдаленных территорий может длиться годами. Карцинома никуда не торопится – поселившись в молочной железе, опухоль ведет неутомимую битву с противоопухолевым иммунитетом, неумолимо разрушает здоровые ткани и рано метастазирует, жертвуя скоростью роста ради проникновения в отдаленные места хозяйского организма.
Основным предметом спора при обсуждении биологии опухолей являются факторы, влияющие на темпы роста, клинические проявления и ответ на терапию неоплазий. Один из вопросов — сколько времени нужно для развития диагностируемой опухоли.
Достоверно подсчитано, что исходная трансформированная клетка (диаметр 10 мкм) и ее производные должны пройти путь по крайней мере 30 удвоений клеточной популяции для достижения количества 10 9 клеток (масса 12 клеток (масса 1 кг) нужно всего 10 удвоений клеточной популяции, что соответствует максимальному размеру опухоли, совместимому с жизнью пациента. Приведенные расчеты основаны на предположении, что все потомки трансформированной клетки сохраняют способность делиться и не происходит потери пула делящихся клеток.
Темпы роста опухолей определяются тремя факторами:
(1) временем удвоения опухолевых клеток;
(2) фракцией опухолевых клеток, составляющих репликативный пул;
(3) скоростью выхода клеток из митотического цикла или их смерти.
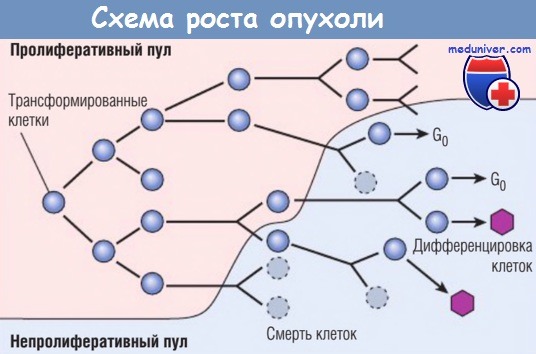
Схема роста опухоли.
По мере роста популяции опухолевых клеток все большее их количество покидает делящийся пул,
переходит в непролиферативную фазу клеточного цикла (G0) и дифференцируется, другие погибают.
Поскольку в большинстве опухолей механизмы контроля клеточного цикла нарушены, клетки могут не выйти из митотического цикла без участия обычных механизмов. Делящиеся опухолевые клетки проходят митотический цикл не быстрее нормальных клеток, а за то же время или даже большее. Следовательно, рост опухоли не связан с укорочением времени их митотического цикла.
Клинические и экспериментальные исследования позволили установить, что на ранних субмикроскопических стадиях пролиферативный пул составляют трансформированные клетки. Эту группу опухолевых клеток называют фракцией роста. По мере роста опухоли клетки покидают пролиферативный пул в результате недостаточного питания, некроза, апоптоза, дифференцировки, перехода в непролиферативную фазу клеточного цикла (G0). Таким образом, к моменту клинической диагностики большинство опухолевых клеток уже не относятся к пролиферативному пулу.
Даже в некоторых быстрорастущих опухолях фракция роста составляет около 20% клеток или менее.
Прогрессирование опухоли и скорость ее роста определяются преобладанием процессов продукции клеток над их потерей. В ряде опухолей, прежде всего тех, которые содержат относительно большую фракцию роста, дисбаланс значителен, что обусловливает более быстрый темп роста опухоли по сравнению с опухолями, в которых пролиферация клеток незначительно превышает их потери.
Некоторые лейкемии, лимфомы и определенные виды рака легкого (например, мелкоклеточная карцинома) имеют относительно большую фракцию роста, что и определяет быстрое прогрессирование процесса. В сравнении с ними такие опухоли, как рак толстой кишки и рак молочной железы, характеризуются наличием небольшой фракции роста (количество пролиферирующих клеток в них превышает потери клеток примерно на 10%), растут значительно медленнее.
Изучение клеточной кинетики позволило сделать важные концептуальные и практические выводы:
- в быстрорастущих опухолях происходит быстрое обновление клеток при наличии высокого уровня пролиферации и апоптоза клеток, т.е. если опухоль растет, то уровень пролиферации опухолевых клеток выше уровня их смерти;
- фракция роста чрезвычайно чувствительна к химиотерапии. Поскольку большинство противоопухолевых препаратов действуют на клетки, находящиеся в митотическом цикле, следовательно, опухоли с репликативным пулом, составляющим 5% клеток, будут расти медленно, но при этом проявлять рефрактерность к действию препаратов, убивающих делящиеся клетки.
В связи с этим первостепенной задачей в стратегии лечения опухолей с низкой фракцией делящихся клеток (например, рака толстой кишки и рака молочной железы) является перевод опухолевых клеток из фазы G0 в митотический цикл. Затем возможны паллиативное удаление новообразования или радиотерапия. Выжившие после этого опухолевые клетки имеют тенденцию входить в митотический цикл и становиться чувствительными к лекарственной терапии. Подобные подходы лежат в основе принципа комбинированной терапии. Некоторые агрессивные опухоли (определенные лимфомы и лейкемии), содержащие крупный пул пролиферирующих клеток, буквально плавятся под действием химиотерапии, т.е. излечение возможно.
Теперь вернемся к вопросу, поставленному ранее: сколько времени нужно трансформированной клетке, чтобы сформировать клинически выявляемую опухоль, содержащую 10 9 клеток? При условии, что каждая из дочерних клеток остается в клеточном цикле и ни одна не выходит из цикла и не погибает, ожидаемый ответ — 90 дней (30 удвоений при продолжительности клеточного цикла 3 дня). В действительности же латентный период развития диагностируемой опухоли предсказать невозможно. Он значительно больше, чем 90 дней, и измеряется годами для большинства солидных опухолей. Это еще раз подчеркивает, что злокачественные опухоли у человека удается диагностировать только после значительных перестроек клеточного цикла. После того как опухоль стала клинически выявляемой, среднее время удвоения ее объема, например при раке толстой кишки и раке легкого, составляет 2-3 месяца.
Как показал анализ факторов, определяющих скорость роста, вариабельность времени удвоения опухоли чрезвычайно широка: менее 1 месяца при злокачественных неоплазиях у детей и более 1 года при определенных опухолях слюнных желез. Злокачественные опухоли в действительности являются непредсказуемым заболеванием.
Темпы роста опухолей в целом коррелируют с их уровнем дифференцировки. Большинство злокачественных новообразований растут быстрее, чем доброкачественные опухоли, но существует множество исключений из данного правила. Некоторые доброкачественные опухоли растут значительно быстрее отдельных злокачественных. Более того, темпы роста злокачественных и доброкачественных опухолей не постоянны. На темпы роста опухолей могут влиять такие факторы, как гормональное воздействие, адекватность кровоснабжения, или неизвестные воздействия.
Например, темпы роста лейомиом (доброкачественных опухолей гладких мышц) матки зависят от уровня эстрогенов и могут меняться соответственно уровню гормонов. Нередко такие опухоли не увеличиваются в размерах в течение 10 лет, что подтверждают повторные клинические обследования женщин. Во время беременности лейомиомы часто быстро увеличиваются в размерах. После менопаузы опухоли могут прекращать расти, становясь в значительной степени фиброзированными и кальцинированными. Подобные изменения связаны с восприимчивостью опухоли к уровню циркулирующих стероидных гормонов, в частности эстрогенов. Злокачественные опухоли отличаются большим разнообразием темпов роста. Некоторые из них медленно растут на протяжении многих лет, затем входят в фазу быстрого роста, моментально диссеминируют, приводя к летальному исходу в течение нескольких месяцев после обнаружения.
- Рекомендуем ознакомиться со следующей статьей "Механизмы клонирования опухолевых клеток"
Естественное развитие большинства злокачественных новообразований проходит через четыре главные фазы: малигнизацию (трансформацию) клеток-мишеней, рост малигнизированных клеток, местную инвазию и развитие дистантных метастазов.
Относительная автономность роста опухолей
Одним из кардинальных свойств опухолей является автономность роста — относительная независимость опухоли от воздействия регуляторных систем организма опухоленосителя и приобретение ею способности к самоуправлению.
При аутокринном механизме клетки опухоли могут одновременно секретировать сигналы для пролиферации и рецепторы для них, что позволяет делящимся клеткам неоплазмы не реагировать на внешние регуляторные влияния организма и быть независимыми от них.
Паракринный механизм связан с секрецией факторов роста опухолевыми клетками и действием их на соседние клетки. Более того, в опухолевых клетках может осуществляться синтез цитокинов и факторов роста и воспринимающих их рецепторов, не характерных для нормальных гистогенетических предшественников.
В то же время автономность роста опухоли относительна. Опухолевые клетки для своей жизнедеятельности должны получать из кровотока питательные вещества и кислород, что делает невозможным их существование вне связи с организмом.
Кроме того, они испытывают постоянное влияние со стороны окружающих нормальных клеток, элементов экстрацеллюлярного матрикса стромы. иммунной, эндокринной и нервной систем. Известно также, что на прогрессирование заболевания влияет пол и возраст больного, У молодых рост и развитие опухопи происходит намного быстрее, чем у пожилых; по частоте заболеваемости рак желудка преобладает у мужчин, а меланома кожи — у женщин и т.д.
Кинетика опухолевых клеток
Скорость роста каждой конкретной опухоли индивидуальна и определяется тремя основными параметрами: продолжительностью клеточного цикла, величиной пролиферативного пула (т.е. числом способных делиться кпеток в опухоли) и уровнем преобладания воспроизведения клеток над их потерей.
Размножение клеток в норме осуществляется путем деления. Время, за которое происходит удвоение клетки и осуществляется полноценная передача генетической информации, называют клеточным циклом (циклом деления), или кинетикой клетки.
Клеточный цикл состоит из двух этапов. Более продолжительный из них — интерфаза. Она занимает до 99% всего времени цикла деления клетки и состоит из трех периодов: G1, G2 и S. Во время интерфазы клетка обладает высокой синтетической активностью и занята воспроизведением своих компонентов.
Затем следует короткий период — митоз (М), во время которого завершается процесс разделения на две дочерние клетки. Клетки, возникающие в результате митотических делений и образующие живой организм, называют соматическими. Основные периоды клеточного цикла показаны на рисунке 6.1.

Рис. 6.1. Схема фаз нормального клеточного цикла [по Вольпе П., 1979 с изменениями].
Первая фаза цикла деления — пресинтетический период или G1-период, наступает поспе митоза и составляет около половины всего жизненного цикла клетки. В этот период происходит интенсивное увеличение цитоплазмы клетки, синтезируются и накапливаются вещества, необходимые для репликации (самовоспроизведения) ДНК. В позднем G1-периоде часть клеток могут выходить из клеточного цикла, дифференцироваться и переходить к выполнению своих функций.
Эти клетки, выполнив свою функцию, в конечном счете погибают. Однако как исключение существуют ткани, в которых специализированные клетки могут возвращаться в клеточный цикл, например клетки печени. Такой клеточный цикл называется продленным.
Опухолевые клетки также способны выходить из клеточного цикла, находиться в фазе покоя и вновь возвращаться в клеточный цикл, сохраняя способность к дальнейшему делению.
Вторая фаза — S-период или синтетический, составляет до 30% продолжительности цикла и характеризуется удвоением числа хромосом, в результате чего плоидность клетки возрастает до четырех. При входе в эту фазу клетка всегда проходит и все последующие стадии цикла деления.
Третья фаза — постсинтетический период или G2-период, когда клетка готовится к митозу. В ней происходит интенсивный синтез цитоплазматических белков и белков, связанных с ДНК. G2-период занимает около 19-20% продолжительности всего цикла.
Митоз, или фаза М, — самый короткий по продолжительности период, занимающий примерно 1% времени всего цикла.
В этой фазе в тетраплоидной клетке (общее число хромосом 4n) каждая хромосома разделяется вдоль по длине, образуя две копии (сестринские хроматиды), ядро раздваивается, а цитоплазма делится пополам, и в результате образуются две дочерние клетки. Каждая дочерняя клетка после митоза содержит по две копии каждой хромосомы. Эти копии называются гомологичными хромосомами.
Общее число хромосом в клетке, известное как диплоидный набор, обозначают 2n. Митотическое деление гарантирует постоянство набора хромосом в соматических клетках. Что касается продолжитепьности клеточного цикла, то в норме она варьирует в разных клетках. По классическим представлениям фазы цикла относительно стабильны по продолжительности (в среднем, G1 — 8 ч; S — 6 ч: G2 — 4 ч; М — до 2 ч), а весь цикл занимает у клеток млекопитающих, в среднем, около 20 ч (рис 6.1).
Следует сказать, что одним из ведущих механизмов действия современных противоопухолевых химиопрепаратов является избирательное воздействие на определенные структуры клетки в разные фазы клеточного цикла. Фазовозависимость цитостатиков обязательно учитывается при проведении химиотерапии.
В опухолевых клетках имеются те же фазы, что и в нормальных. Иногда при злокачественном росте встречается прямое деление — амитоз, когда клетка делится без разрушения ядра и ядрышек.
Кишки большинства опухолей обладают такой же и даже большей продолжительностью клеточного цикла, чем клетки нормальных, быстро обновляющихся тканей. Об этом убедительно говорят авторадиографические исследования. Не существует ни одной опухоли, клетки которой достигали бы скорости размножения нормальных костно-мозговых клеток или клеток покровного эпителия кишечника.
Здесь следует отметить, что, к сожалению, более высокий уровень пролиферации клеток в нормальных тканях, чем в некоторых опухолях, является существенным препятствием для их успешного химиолучевого лечения.
Изучение опухолей показало, что их клональный характер не означает одинаковости всех их клеток, особенно — в отношении клеточного цикла. Клеточный состав опухоли обычно представлен необратимо постмитотическими клетками (составляют от 30 до 70% всех клеток опухоли), т.е. не способными делится, вплоть до момента гибели; покоящимися клетками (законсервированы в фазе G0), способными снова войти в митотический цикл (стволовые опухолевые клетки) и клетками с различной продолжительностью фазы G1, составляющие пролиферирующий пул опухолевых клеток и относящиеся к фракции роста (рис. 6.2).

Рис. 6.2. Клеточный состав типичной опухоли [Cajano А. и соавт., 1972].
I — необратимо посмитотические клетки;
II — покоящиеся клетки (способны снова войти в митотический цикл);
Ill — клетки в митотическом цикле с различной продолжительностью фазы G1
Темп роста новообразования и определяется в основном величиной фракции роста. На ранних, субмикроскопических стадиях опухолевого роста подавляющее большинство злокачественных клеток находится в цикле, составляя пролиферативный пул или фракцию роста.
По мере роста опухоли клетки во все более увеличивающемся количестве покидают этот пул вследствие потерь или возвращения в фазу G0. Поэтому ко времени клинического обнаружения опухоли большинство ее клеток не находится в репликационном пуле.
В тоже время многие опухоли, например рак толстой кишки или молочной железы, имеют небольшие фракции роста. Наилучшим, хоть и грубым морфологическим выражением темпа роста опухоли (пролиферативной активности) является частота митозов или митотический индекс (доля митозов в исследуемой популяции клеток).
Их можно оценить просто по количеству фигур митоза в единице площади гистологического среза опухолевой ткани, с помощью проточной цитометрии или методом авторадиографии с меченым предшественником ДНК — Н-тимидином.
Общеизвестно, что от величины фракции роста опухолевых клеток зависит чувствительность новообразования к химиотерапии. Поскольку большинство цитостатиков действуют на клетки, активно синтезирующие ДНК, нетрудно понять, почему опухоли, содержащие, скажем, 5% своих клеток в репликационном пуле, являются медленно растущими, но относительно устойчивыми к химиотерапии.
И напротив, агрессивные, быстро растущие опухоли (лимфомы и др.), имеющие большой пуп делящихся клеток, подчас буквально тают на глазах под влиянием химиотерапии, и лечение может оказаться эффективным.
Среди опухолевых клеток особого внимания заслуживают сравнительно небольшая часть клеток, которые можно охарактеризовать, как опухолевые стволовые клетки (tumor stem cells). Они способны длительное время существовать в организме вне митотического цикла, в периоде относительного покоя и называются еще покоящиеся (G0), клоногенные клетки.
Однако, под влиянием каких-либо стимулов, эти клетки могут выходить из стагнированного состояния, вступать в клеточный цикл и неограниченно делиться, пополняя пуп пролиферирующих клеток, потомство которых расселяется и колонизирует новые участки тканей.
Уровень воспроизведения опухолевых клеток и клеточные потери. Во взрослом организме количество клеток постоянно, так как количество новообразованных и утратившихся тонко и надежно сбалансировано. При развитии опухолей происходит нарушение этого баланса.
Однако по мере увеличения размеров опухоли темп роста снижается, клеточная пролиферация замедляется, клеточные потери увеличиваются вследствие иммунного воздействия и недостаточного кровоснабжения. При этом доминирующий фактор клеточных потерь — ишемический некроз.
Основными причинами возникновения очагов некроза являются уменьшение по мере роста функционирующей сосудистой сети на единицу объема опухоли и сосудистый стаз. Поэтому доля некротизированных клеток по мере увеличения размеров опухоли всегда увеличивается.
Таким образом, темп роста злокачественных новообразований определяется в основном величиной фракции роста (пулом пропиферирующих клеток) и показателем преобладания воспроизведения клеток над их потерей. В некоторых случаях, особенно с относительно большой фракцией роста, это преобладание велико и приводит к быстрому увеличению массы опухоли, а в других случаях оно весьма незначительно.
Так, в карциномах желудочно-кишечного тракта воспроизведение клеток превышает их потерю примерно лишь на 10% и они имеют тенденцию к гораздо более медленному росту.
Инфильтративный рост опухолей
Инфильтративный (инвазивный) рост (от лат. infiltratio — проникновение) заключается в прямом проникновении (прорастании) опухолевых клеток в окружающие ткани и является одним из основных свойств злокачественности.
В отличие от злокачественных, для доброкачественных опухолей характерен экспансивный рост, т.е. при росте они сдавливают и раздвигают (отодвигают) окружающие нормальные ткани.
При этом сдавленные опухолью элементы окружающей ткани атрофируются, но их количество нарастает и образует вокруг опухоли подобие капсулы (псевдокапсула), В тоже время и некоторые злокачественные опухоли (рак почки, околощитовидной железы, фибросаркома) также растут экспансивно.
Артерии обычно не подвергаются инфильтрирующему росту, так как имеющиеся в их стенке эластин и коллагеновые волокна оказывают значительное сопротивление опухолевым клеткам. Высказывается предположение, что резистентности артерий способствует и высокое внутрисосудистое давление.
Понятно, что вследствие инвазивного роста опухоли прорастают в окружающие анатомические структуры и органы и вызывают нарушения соответствующих функций. Именно эти патогенетические особенности злокачественного роста лежат в основе развития вторичных симптомов и клинических феноменов новообразований.
Кроме того, инвазивный рост является обязательным компонентом метастатического каскада: диссеминации опухолевых клеток по организму предшествует их инвазия из первичного очага в окружающие ткани.
Макроскопические формы рака зависят от того, в каком направлении происходит распространение опухолевой массы: в толщу органа (эндофитная) или за его пределы в виде выбухающего узла (экзофитная) (рис. 6.3).

Рис. 6.3. Основные клинико-морфологические формы роста опухолей.
Экзофитная форма — новообразование имеет вид узла, который выступает в просвет полого органа, или распространяется в толще паренхиматозного, или выступает над поверхностью тела и довольно четко отграничен от здоровых тканей. При этом граница опухоли от видимого ее края составляет около 1 см. Независимо от формы роста раковая опухоль характеризуется склонностью к распаду и изъязвлению, что объясняется особенностями ее кровоснабжения.
Экзофитные опухопи при распаде приобретают вид блюдца — язвы с выступающими, подрытыми в виде валика краями. Такие опухоли называют блюдцеобразными. Экзофитные опухоли в паренхиматозных органах представляют собой округлые узлы, при наружном осмотре они обычно не видны.
При длительном росте из-за особенностей кровоснабжения в центре опухолей происходит распад. Такие формы экзофитных опухолей паренхиматозных органов получили название полостных. По характеру происходящих процессов они аналогичны блюдцеобразным ракам полых органов, но по внешнему виду довольно далеки от них.
Эндофитная форма — раковые клетки распространяются преимущественно в пределах стенки органа. В этих случаях стенка или сам орган становятся толще и плотнее, границы опухоли четко не определяются, а микроскопически от видимого края опухоли распространяется приблизительно на 6 см.
Такой характер роста называют инфильтративным, а опухоль — эндофитным, или инфильтративным раком. Инфильтративный рост новообразования в паренхиматозных органах встречается редко и такая форма опухоли называется диффузной.
Обычно такие опухоли выделяют в качестве особых разновидностей, например в легком — перибронхиальная разветвленная и пневмониелодобная формы, в молочной железе — инфильтративно-отечная, маститоподобная и рожистоподобная формы, в печени — инфильтративная, рак-цирроз и т.д.
Инфильтративно рак протекает более злокачественно, отличается быстрым течением, ранним и бурным метастазированием и плохим прогнозом. При распаде эндофитного рака валикообразные края вокруг изъязвления не образуются, а такие опухоли называются язвенно-инфильтративными. Когда наблюдается сочетание экзо- и эндофитного компонентов опухоли, говорят смешанной форме опухолевого роста.
Делению на основные четыре формы рака (экзофитная, блюдцеобразная, инфильтративная и язвенно-инфильтративная) в наибольшей степени соответствуют новообразования желудочно-кишечного тракта. Рак наружных локализаций обычно имеет вид экзофитной или изъязвленной (соответствует блюдцеобразной) опухоли.
Кроме того, вышеназванным формам роста опухолей часто сопутствует так называемый оппозиционный или вовлекающий рост. Он характерен для воспаления, которое часто сопутствует опухолевому процессу, увеличивая объем и размеры опухоли.
Возможность наличия оппозиционного роста необходимо учитывать при планировании специального лечения, а подготовка к операции или лучевой терапии должна включать противовоспалительную и антибактериальную составляющую.
Формирование опухолевого узла из клональных потомков трансформированной клетки — это сложный процесс роста новообразования, на который влияет множество факторов. Среди них ведущими являются: кинетика (динамика) роста опухолевых клеток, опухолевая прогрессия и гетерогенность, а также ангиогенез в опухоли.
Угляница К.Н., Луд Н.Г., Угляница Н.К.
Доброкачественная опухоль является патологическим новообразованием с замедленным темпом развития. Своевременная терапия при этом дает положительный прогноз: в большинстве ситуаций пациенты полностью избавляются от заболевания, а рецидивов почти не бывает. Опасность для здоровья представляют опухоли, скрытно развивающиеся в организме. На фоне отсутствия симптоматики диагностировать болезнь сложно, что угрожает перерождением в злокачественное образование. О том, каковы причины появления доброкачественных опухолей, каковы стадии их развития и как проводится лечение, расскажем далее.
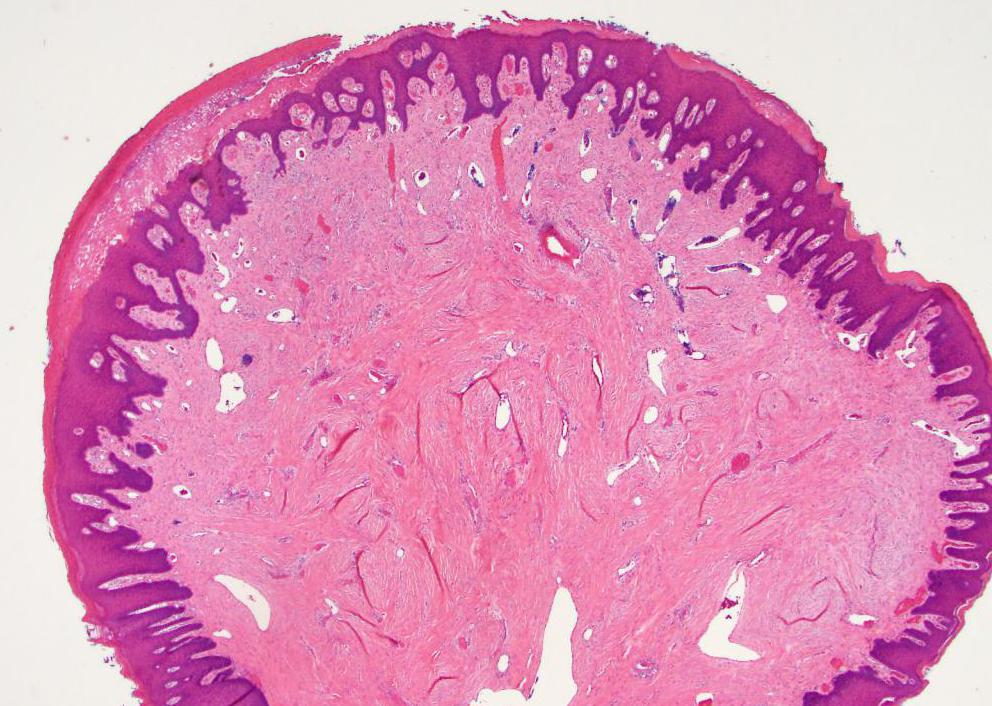
Причины возникновения
В человеческом организме каждая клетка проходит один и тот же путь: она растет, затем развивается, после чего отмирает спустя сорок два часа. На смену приходит новая, которая проживает аналогичный период. В том случае, если в результате какой-то причины клетка не погибнет, а продолжит расти, то возникнет опухоль. Доброкачественные и злокачественные опухоли сильно отличаются.
Наукой доказано, что доброкачественные образования являются следствием мутации человеческого ДНК, к чему приводят следующие факторы:
- Деятельность человека на вредном производстве, наряду с регулярным вдыханием опасных ядов или паров.
- Вредные привычки в форме курения, приема наркотиков и токсикомании.
- Прием алкоголя.
- Влияние ионизирующей радиации.
- Получение организмом частого воздействия ультрафиолетового излучения.
- Появление гормонального сбоя.
- Возникновение нарушений в работе иммунитета.
- Проникновение в организм различных вирусов.
- Получение травм и переломов.
- Нездоровое питание, употребление в пищу вредных продуктов.
- Отсутствие сбалансированного режима дня, к примеру, частые недосыпания, работа по ночам и тому подобное.
Предрасположенность
Согласно исследованиям установлено, что предрасположенность к появлению доброкачественных опухолей есть абсолютно у каждого. А предупредить развитие таковых можно лишь, ведя активный и здоровый образ жизни. Неблагоприятное действие на клетки оказывают частые нервные стрессы. Далее узнаем, через какие стадии проходит доброкачественное образование в процессе своего развития.
Стадии роста опухоли
Всего различают три следующие стадии развития доброкачественных опухолей:
- Стадия инициации. На этой стадии обнаружить мутировавший ген почти невозможно. Инициация связана с изменением ДНК-клетки под влиянием неблагоприятных факторов.
- Стадия промоции. На этом этапе мутированная клетка начинает свое активное размножение. Стадия промоции способна длиться в течение нескольких лет, почти не проявляя себя.
- Стадия прогрессии. На третьей стадии опухолевого роста происходит стремительное увеличение количества мутационных клеток, которые образуют опухоль. Доброкачественное образование на этой стадии оказывается причиной ухудшения самочувствия, возникают нарушения в функциональности организма, появляются пятна на коже. Это значительно облегчает процесс диагностики. Обнаружить опухоль на этом этапе нетрудно.

Временной период
Период, в течение которого происходит развитие доброкачественной опухоли, может продолжаться от пары месяцев до десятков лет. Нередко данную болезнь диагностируют лишь после смерти во время проведения вскрытия. При этом опухоль не всегда служит основной причиной гибели человека. Может ли доброкачественная опухоль перерасти в рак? Разберемся.
Перерождение
Стадия прогрессии опасна в первую очередь тем, что воздействие неблагоприятных факторов наряду с отсутствием лечения приводит к скорому перерождению опухоли. Продолжается процесс мутации генов, опасные клетки размножаются еще более активно. Они начинают распространяться по организму и оседать в органах. Такой процесс называют метастазированием. На этом этапе врачи диагностируют уже злокачественное новообразование, которое считается угрозой для жизни.
Доброкачественные опухоли делятся на определенные виды. Далее выясним, на какие именно типы в медицине подразделяют подобные новообразования.
Доброкачественная опухоль способна произрастать абсолютно в любой ткани человеческого организма. Существует несколько видов таких новообразований:
- Фиброма представляет собой опухоль, которая состоит из волокнистых соединительных тканей. Фибромы возникают чаще всего на половых органах у женщин. При этом у пациенток отмечаются нарушения менструального цикла, бесплодие и сильные боли при половых актах.
- Липому по-другому называют жировой опухолью. Липомы часто образуются у женщин во время менопаузы, такая опухоль может достигать очень больших размеров.
- Хондрома состоит преимущественно из хрящевых тканей. Причиной ее развития становятся травмы или повреждения тканей. Хондрома проявляется не только в единичном экземпляре, но и во множественном. Обычно поражает конечности.
- Нейрофиброматоз врачи иначе называют заболеванием Реклингхаузена. Патология характеризуется образованием фибром, а, кроме того, пигментных пятен. При этом может присоединиться воспаление нервов.
- Остеомой называется доброкачественное образование, которое состоит из костной ткани. Она обладает четкими границами и редко перерождается в злокачественную опухоль. Этот вид является врожденной патологией.
- Миома выступает одиночным или множественным образованием, имеющим плотную основу. Это заболевание формируется в мышечных тканях и поражает преимущественно половую систему у женщин. Причиной служат гормональные нарушения наряду с абортами и ожирением. Симптомы доброкачественной опухоли на начальных этапах могут отсутствовать полностью.
- Под ангиомой понимают опухоль, развивающуюся из кровеносных сосудов. Это заболевание является врожденным, располагается преимущественно на щеках, или слизистой рта.
- Лимфангиома состоит из лимфатических сосудов. Она формируется в период эмбрионального развития, продолжая расти в раннем детстве. Зачастую лимфангиома останавливается в своем развитии и не представляет угрозу для жизни.
- Невринома, как правило, развивается на периферических нервах, а, кроме того, в спинном мозге. Реже встречают невриному на черепных нервах. Выглядит эта опухоль в виде небольших узлов различных размеров.
- Неврома может образовываться на разных элементах нервной системы. Причиной этого заболевания зачастую становится ампутация наряду с повреждением нерва. Могут встречаться и врожденные невромы.
Что представляет собой доброкачественная опухоль мозга? Об этом далее.
Какие еще виды опухолей выделяются в медицине?
Помимо всего прочего, существуют следующие виды доброкачественных новообразований:
- Ганглионеврома развивается обычно в брюшной полости. Это чаще всего плотное образование с большими размерами. Такое заболевание начинает формироваться еще в утробе матери. Причинами его возникновения служат нарушения развития нервной системы наряду с воздействием неблагоприятных факторов при вынашивании плода.
- Параганглиома состоит из хромаффинных клеток. Это заболевание способно развиваться в любых органах. Опухоль является врожденной и начинает себя проявлять еще в раннем возрасте. Такая болезнь может представлять собой опасность из-за возможности развития метастаз.
- Папилломы представляют собой новообразования в форме небольших сосков, в центре которых находится кровеносный сосуд. Этот тип является наиболее распространенным видом доброкачественной опухоли, его легко удалять. Как правило, после проведения хирургического вмешательства рецидивы не возникают. Папиллома появляется в результате влияния на организм вируса. Очень часто это заболевание атакует половые органы. Помимо этого к папилломам относятся бородавки, которые в большинстве случаев безопасны и не требуют какого-либо лечения. Исключения обычно составляют те образования, которые начинают кровоточить или приносить боль. Также опасность для человека обычно представляют увеличивающиеся и меняющие цвет образования.
- Аденома обладает одной характерной особенностью: она может повторять форму органа, на котором формируется. Состоит такая опухоль обычно из желез и крайне редко перерождается в злокачественный тип. Зачастую такая опухоль поражает простату у мужчин старше сорока пяти лет. Это заболевание может проявляться болезненным мочеиспусканием, понижением сексуальной активности, бесплодием и ранними семяизвержениями. Аденома, как таковая, не опасна для жизни, но может значительно ухудшить ее качество и привести к психическим расстройствам.
- Что такое доброкачественная опухоль головного мозга? Киста является образованием, не имеющим четких границ. Она состоит из полости, наполненной жидкостью. Киста может стремительно развивается, что может представлять угрозу. В случаях разрыва этой опухоли возникает риск появления заражения крови. Появляются кисты обычно на половых органах, в костной ткани или в районе головного мозга.
Существуют доброкачественные опухоли головного мозга, у которых врожденная природа. К ним относят:
- краниофарингиомахордому;
- герминому;
- тератому;
- дермоидную кисту;
- ангиому.
Менингиома — это доброкачественное новообразование, которое характеризуется вторичным проявлением даже после удаления. От величины, размеров опухоли, быстроты роста и места локализации зависят симптомы, лечение, а также последствия возникновения такого вида опухоли. Слишком большие размеры доброкачественных образований мозга ухудшают его интеллектуальные функции.
Доброкачественные опухоли легких образуются из высокодифференцированных клеток, которые похожи на здоровые по строению и функциям. У них относительно медленный рост, они не инфильтрируют и не разрушают ткани, не образуют метастазы. Происходит атрофия ткани, расположенной вокруг опухоли, в результате чего образуется соединительнотканная капсула (псевдокапсула), окружающая новообразование. Опухоли легкого склонны к малигнизации.
Доброкачественные опухоли молочных желез
Образуются из-за патологического разрастания тканей. Доброкачественные уплотнения не срастаются с кожей, в отличие от злокачественных.
Чаще доброкачественные опухоли молочных желез возникают у женщин, которые сделали много абортов, не родили детей и не кормили грудью в положенное время. Возраст - тоже фактор, обуславливающий появление опухоли в той или иной форме.
Так, липомы и мастопатия диагностируются у женщин в возрасте 35-50 лет, после 35 лет – кисты, в 20-35 лет – фиброаденомы. Внутрипротоковая папиллома не зависит от возраста.
В большинстве случаев проводить удаление доброкачественных новообразований не требуется. Необходимо регулярно проходить осмотры и обследования, в ходе которых можно убедиться в отсутствии активности доброкачественной опухоли железы.

Лечение
Опухоли, которые были диагностированы на раннем этапе развития, очень легко поддаются лечению. В рамках выявления болезни используется несколько различных способов. Подобные образования можно увидеть с помощью ультразвукового исследования или проведения пальпации. Для того чтобы поставить верный диагноз, исследуется кровь и кусочки ткани, которые берутся при биопсии или во время лапароскопии.
От чего зависит терапия?
Лечение доброкачественной опухоли напрямую зависит от ее типа и состояния больного. Но важно отметить, что оставлять без внимания врачей это заболевание ни в коем случае нельзя. Даже небольшие новообразования могут приводить к печальным последствиям или продолжительному и дорогостоящему лечению.
Современной медициной предлагаются несколько эффективных методик лечения таких опухолей, среди которых на первом месте стоит удаление. Операция помогает предотвращать дальнейшее развитие болезни и устраняет скопление мутировавших клеток. После процедуры удаления рецидивы, как правило, не возникают, и наступает абсолютное выздоровление. В крайне редких ситуациях требуется повторная операция в случае разрастания мутированных клеток.
Доброкачественные и злокачественные опухоли имеют одно важное отличие – первая не опасна для жизни.
Удаление опухоли
Удаление доброкачественных новообразований осуществляется с использованием различных хирургических инструментов или посредством специального лазера. Перед операцией место удаления опухоли обрабатывают дезинфицирующими средствами, а пациента вводят в общий наркоз. Чаще всего удаление происходит посредством надреза ткани и вылущивания новообразования. Это дает возможность уменьшить размеры шва и предотвращает инфицирование.
Проведение криокоагуляции
К более современной методике лечения доброкачественной опухоли относят криокоагуляцию. Ее проводят в случае образования опухолей на мягких тканях. Этот метод впервые был испробован в Израиле, после чего получил весьма широкое распространение по всему миру. Криокоагуляция дарит шансы на выздоровление пациентам с раком костей. Лечение позволяет удалить новообразование без каких-либо последствий для ткани и скелета.
Проведение заместительной терапии
Многие образования доброкачественной природы возникают по причине сбоя работы гормональной системы. В том случае, если опухоль имеет небольшие размеры и не демонстрирует признаков дальнейшего развития, пациенту назначают заместительную терапию. При этом пациент находится под пристальным присмотром специалистов и проходит регулярные обследования.
Читайте также:

