Селективная ангиография при раке поджелудочной железы

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- К кому обратиться?

Больные с заболеваниями поджелудочной железы могут предъявлять жалобы на боли в животе, а также диспепсические явления, общую слабость.
Жалобы
Боли в животе, достаточно разнообразные по продолжительности и характеру, локализуются чаще всего в верхней половине живота, преимущественно в эпигастральной области или левом подреберье, иррадиируя в спину. Они могут быть острыми, интенсивными, опоясывающего характера, с иррадиацией в поясничную область, что при остром панкреатите связано с нарушением оттока секрета из поджелудочной железы и воздействием собственных протеолитических ферментов. Продолжительные и интенсивные боли характерны для опухолей; они нередко усиливаются в положении больного на спине, что вынуждает больных занять полусогнутое положение.
Диспепсические явления, тошнота, рвота часто возникают при различных заболеваниях поджелудочной железы в результате изменения ее ферментативной деятельности или рефлекторно.
Механическая желтуха с зудом кожи характерна для поражения головки поджелудочной железы с нарушением оттока желчи.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]
Физические методы исследования поджелудочной железы
При осмотре выявляют истощение, желтуху с ее характерными последствиями в виде расчесов, геморрагии. Пальпация поджелудочной железы остается малоэффективным методом. Лишь при выраженном увеличении железы вследствие опухолевого поражения при глубокой скользящей пальпации удается обнаружить новообразование.
Дополнительные методы исследования поджелудочной железы
Лабораторные и инструментальные методы позволяют более точно обнаружить активный деструктивный процесс в железе; оценить остаточную экзокринную панкреатическую функцию; оценить эндокринную функцию поджелудочной железы и оценить морфологические особенности железы.
Рентгенологическое исследование поджелудочной железы. Обзорный рентгеновский снимок брюшной полости позволяет обнаружить кальцификаты в железе. При введении бариевого контраста можно получить косвенные признаки воспалительного и неопластического процессов в проксимальной части поджелудочной железы, учитывая изменения слизистой оболочки двенадцатиперстной кишки.
Ультразвуковое исследование поджелудочной железы. Этот неинвазивный и безопасный метод позволяет обнаружить в поджелудочной железе кисты и новообразования, а также определить ее увеличение в результате отека или уплотнение (фиброз).
Компьютерная томография. У больных с ожирением и кишечной непроходимостью ультразвуковое исследование обычно затруднено, поэтому целесообразно провести компьютерную томографию, которая также позволяет оценить морфологические изменения железы, выявить опухоль, кисту, очаги воспаления, отек.
Ангиография артерий поджелудочной железы. Селективная ангиография артерий, снабжающих кровью поджелудочную железу, целесообразна при диагностике опухолей. Она позволяет обнаружить сужение просвета сосудов и нарушение их положения. Обычно это исследование проводят после ультразвукового исследования и компьютерной томографии.
Эндоскопическая ретроградная холангиопанкреатография. Это исследование считается одним из наиболее ценных методов визуализации панкреатического и желчного ходов. Через эндоскоп вводят в общий желчный проток контрастное йодированное вещество и затем проводят рентгенографию, что позволяет не только установить причину механической желтухи, но и выявить изменения поджелудочной железы, характерные для воспалительного и неопластического процессов. При хроническом панкреатите проток может быть деформирован, видны участки сужения и расширения. При наличии опухоли возможен изолированный стеноз протока или полная его обструкция.
Радиоизотопное исследование поджелудочной железы. Это исследование поджелудочной железы с применением метионина, меченного радиоактивным изотопом селена, в целом значительно менее точно, чем перечисленные методы исследования.
Исследование панкреатических ферментов в крови и моче. Некроз панкреатической ткани в результате обструкции протока железы может быть оценен по повышению концентрации ферментов поджелудочной железы в крови, моче и других средах организма. Наиболее распространено измерение активности амилазы и липазы. Во время острого панкреатита повышенный уровень сывороточной амилазы сохраняется до 10 дней и обычно сопровождается гиперамилазурией. Увеличение содержания амилазы в сыворотке крови и моче имеет место не только при панкреатите, но и при патологии желчных путей, перфорации язвы желудка, кишечной непроходимости, некоторых вирусных заболеваниях, что связано, по-видимому, с сопутствующим поражением поджелудочной железы.
В связи с тем что амилаза поступает в кровь не только из поджелудочной железы, но и из слюнных желез, в настоящее время делаются попытки определения ее изоферментов. С помощью радиоиммунного исследования оценивают активность в сыворотке крови других ферментов - трипсина, липазы, эластазы.
Исследование функции поджелудочной железы. Экзокринная функция поджелудочной железы оценивается с помощью прямой и непрямой стимуляции. Прямая стимуляция состоит в парентеральном введении ряда гормонов, в частности секретина и холецисто-кинина, а также их сочетания. Непрямая стимуляция состоит в приеме внутрь пищевых веществ. В обоих случаях используют измерение панкреатических ферментов - амилазы, трипсина, липазы (концентрация которых под влиянием секретина первоначально несколько снижается, а затем увеличивается) в дуоденальном содержимом, которое получают с помощью зонда. Дополнительным и важным методом оценки экзокринной функции поджелудочной железы является исследование кала с целью определения содержания в нем жиров и белковых продуктов.
Количественная оценка содержания жира в каловых массах, а также химотрипсина и трипсина достаточно точно позволяет обнаружить прогрессирующее снижение функции железы.
Тест на толерантность к глюкозе позволяет оценить эндокринную функцию поджелудочной железы, которая нарушается у 3/4 больных с панкреатитом или с опухолью поджелудочной железы.
Исследование функции поджелудочной железы, прежде всего экзокринной, имеет значение у больных с нарушением всасывания для уточнения причины этой патологии и, в частности, для определения роли снижения функции поджелудочной железы.

[13], [14], [15], [16], [17], [18], [19], [20]
Компьютерная томография постепенно приобретает наиболее важное значение в диагностике рака поджелудочной железы. Hа томограммах определяется увеличение всей железы или ее части и на фоне железы выделяется опухолевое образование. Внутривенное введение трийодированного контрастного вещества способствует лучшей видимости опухоли, особенно участков некроза или кистозного превращения в ней. Контуры тени опухоли неровные, бугристые.
Обычно удается заметить прорастание опухоли в лимфатические узлы, в забрюшинную клетчатку, в печень, а также нередко метастазы в печень. Для прогредиентных форм рака характерны потеря очертания брюшной аорты, невидимость тени верхней брыжеечной артерии. Сдавление общего желчного протока приводит к увеличению желчного пузыря и расширению вне- и внутрипеченочных желчных протоков, что также заметно на томограммах.
Но не следует переоценивать этот метод. Modder и соавт. (1979) обследовали 168 больных раком поджелудочной железы (диагноз был достоверен). По компьютерным томограммам точный диагноз был поставлен лишь у 74,5% больных. У 9% человек патологический процесс был истолкован неправильно. Необходимо учитывать, что компьютерная томография не обеспечивает раннего выявления опухоли. Поэтому серьезную роль в диагностике опухолей по-прежнему отводят ангиографии.
Богатое кровоснабжение поджелудочной железы содействует ангиографической диагностике. Но рентгенолог неизбежно встречается с большими диагностическими трудностями, поскольку поджелудочная железа получает артериальную кровь из разных участков. Это объясняет сравнительно слабую тень железы в паренхиматозной фазе. На изображение артерий железы проецируются тени других артерий, в частности желудочных, и ветвей артерий, идущих к поперечной ободочной кишке.
Сосудистые веточки имеют небольшие размеры и по ангиограммам нелегко уловить патологические изменения в них. Кроме того, аналогичные изменения могут вызвать как воспалительные, так и опухолевые поражения.
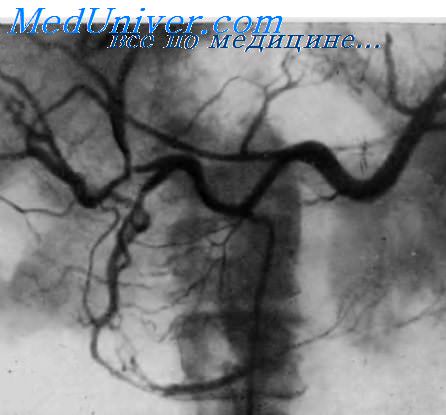
Просвет каждого сосуда неравномерен, некоторые мелкие ответвления слепо заканчиваются в аваскулярном участке. Узурация стенки артерии является следствием опухолевой инфильтрации сосуда. Пораженная артерия обычно сужена, а контур ее неровный. Эти изменения могут выявляться как в сравнительно небольших сосудах (дорсальная и задняя артерии поджелудочной железы, нижняя поджелудочнодвенадцатиперстная артерия и их ветви), так и в крупных внеорганных артериях.
К симптому узурации следует причислить и эксцентрические дефекты наполнения в тени сосуда, которые могут быть одиночными или множественными.
По данным литературы, при рентгенологическом исследовании длина поджелудочной железы достигает 27 см (в среднем 20,5 см), высота ее тела составляет 1,5—4,5 см, а вертикальный размер головки варьирует от 3,5 до 8 см. Согласно измерениям Т. В. Привезенцевой (1973), наибольший размер головки по паравертебральной линии равен 5,5—5,8 см. Однако не так важны в диагностическом плане абсолютные величины этих показателей, как другие ангиографические признаки увеличения железы.
Так, при увеличении головки поджелудочной железы нарастает расстояние между ее наружным краем и стволом желудочно-двенадцатиперстной артерии, между артериями, составляющими переднюю и заднюю артериальные аркады поджелудочной железы. Кроме того, крупные артерии удлиняются, выпрямляются. Аваскулярная зона является результатом нарушения кровотока из-за сдавления и тромбоза мелких артерий поджелудочной железы.
Для малых опухолей характерен такой признак, как узурация артерий. При больших опухолях отчетливо определяется также смещение сосудов, прилегающих к ней. Вторичный панкреатит может сопровождаться изменением артериального рисунка в свободной от опухоли части железы; для него типично увеличение числа артерий и их расширение, что приводит к гиперваскуляризации железы. В случае развития желтухи ангиография позволяет заметить увеличение желчного пузыря, при этом в артериальной фазе передняя и задняя ветви артерии желчного пузыря раздвинуты и удлинены, а в паренхиматозной фазе появляется прямое изображение увеличенного желчного пузыря.
Поражение крупных артерий обычно указывает на неоперабельность рака. При раке головки поджелудочной железы поражаются чревная, печеночная и брыжеечная артерии, при раке тела и хвоста — селезеночная артерия. Селезеночная артерия в таких случаях смещена кверху, имеет неровные очертания. Ее сужение или окклюзия ведут к образованию коллатеральной сети сосудов, которые могут напоминать опухолевые сосуды.
Контрастирование венозной системы брюшной полости и забрюшинного пространства может быть применено не столько для диагностики опухоли, сколько для определения ее операбельности. При раке головки Rosch (1975) считал целесообразным проведение чрескожной чреспеченочной портографии с контрастированием ее крупных ветвей и с определением разницы давления в селезеночной и верхней брыжеечных венах, с одной стороны, и в воротной вене — с другой. Dux и соавт. (1978) применяли контрастирование нижней полой вены и забрюшинных вен. Блокада последних рассматривалась как признак неоперабельности опухоли.
Необходимо лишь учитывать, что изменения в крупных венах — воротной, верхней брыжеечной, селезеночной, нижней полой, правой или левой восходящей поясничных — могут быть результатом непосредственного сдавления или прорастания их опухолью, а также метастазами в лимфатические узлы. Как указал Swart (1975), поражение воротной и селезеночной вен может вызвать типичную картину подпеченочного блока с варикозным расширением вен желудка и пищевода. Weigand, Georgi (1978) на трупах разработали методику окклюзионной флебографии поджелудочной железы путем введения трехпросветного зонда через пупочную вену. В клинике это исследование еще не апробировано.
Ангиографией называют исследование структуры и функционирования сосудов, проводимое при помощи специальной аппаратуры и рентгенконтрастного вещества, введенного в сосуд. Выделяют следующие разновидности ангиографии брюшной полости:
- Вено или флебография — исследование вен,
- Артериография -артерий,
- Лимфография -лимфатических сосудов.
В зависимости от того, что необходимо исследовать проводится избирательная (селективная) или общая ангиография брюшной полости. Введение контрастного вещества в сосуд производится посредством катетеризации или пункции.
Исследование делают в специализированном рентгенологическом кабинете, в котором установлено ангиографическое оборудование, снабженное устройством для быстрой крупноформатной серийной съемки, аппарат для рентгеновской видеозаписи, флюорографическая скоростная камера и компьютер для обработки полученных результатов и вывода их на монитор. Современный метод вычислительной ангиографии позволяет получить дополнительные сведения о гемодинамике и состоянии сосудов.
Методика проведения и цели исследования
Современная ангиография брюшной полости проводится при помощи двух методик: инвазивной и неинвазивной. Исследование проводится для того чтобы определить патологические состояния органов брюшной полости которые развиваются на фоне нарушения функциональных или структурных особенностей кровеносных сосудов.
Инвазивной методикой ангиографии считается рентгенологическое обследование сосудов, при котором в внутрь артерии вводится безвредный для здоровья человека рентгенконтрастный препарат. Исследование состоит из трех этапов:
- Введение катетера — специальная тонкая пластиковая трубка при исследовании сосудов органов брюшной полости вводится через небольшой надрез в бедренную или подмышечную артерии, локтевую или бедренную вены (в зависимости от того какие сосуды необходимо обследовать) и продвигается до аорты. Перед введением катетера кожу обрабатывают дезинфицирующим препаратом, зачастую проводят обезболивание. За перемещением катетера внутри кровеносного сосуда следят с помощью рентгенотелевидения.
- Введение контрастного вещества начинают сразу же после первого этапа, затем начинают быструю рентгеновскую съемку. Пациент в этот момент ощущает тепло, такое ощущение длится на протяжении нескольких секунд. Рентгенконтрастное вещество вводят 2−4 раза в течение процедуры.
- Удаление катетера производится немедленно после исследования, место ввода прижимается, чтобы остановить кровотечение. Через 10− 15 минут необходимо наложить давящую стерильную повязку.
- Магнитно-резонансная ангиография — при ее помощи можно узнать функциональные и анатомические особенности сосудов,
- Компьютерно-томографическая ангиография — дает детальный рисунок кровеносного сосуда,
- Ультразвуковая допплерография органов брюшной полости (преимущественно печени) проводится только в тех случаях, когда получить информацию другими методами невозможно.
Ангиографическое исследование брюшного отдела аорты
Брюшная аортография или ангиография брюшной аорты исследование брюшной части аорты и отходящих от нее сосудов при помощи рентгенологического метода.
Показаниями к проведению являются следующие патологии:
- Повреждения органов брюшной полости при травмах или хронических заболеваниях (цирроз печени, портальная гипертензия)
- Повреждение забрюшинного пространства
- Кровотечения в желудочно-кишечный тракт или брюшную полость
- Различные патологии сосудов
- Доброкачественные и злокачественные новообразования (и их метастазы)
При этом исследовании катетер, как, правило, вводится через бедренную или подмышечную артерию и под контролем рентгеноскопа устанавливается в брюшной аорте или брыжеечных артериях.
Подготовка к исследованию:
- При подготовке к исследованию назначается анализ крови (для того чтобы определить общие параметры и свертываемость)
- Нельзя принимать пищу за 8 часов до процедуры
- Если у вас есть аллергия на йод, необходимо сообщить об этом врачу перед назначением исследования
- Непосредственно перед процедурой надо подписать информированное согласие
- Перед исследованием пациент должен сходить в туалет, снять все металлические предметы (поскольку они отражаются на рентгеновских снимках и могут исказить картину) и переодеться в специальную одежду
- В течение проведения ангиографии пациент находится в положении лежа и фиксируется к столу, чтобы обеспечить неподвижность.
Это важно! Для того чтобы результаты ангиографического исследования были наиболее точными вам необходимо в течение всей процедуры лежать неподвижно, и обязательно опорожнить кишечник и мочевой пузырь перед процедурой.
Ангиографическое исследование поджелудочной железы
Ангиография поджелудочной железы чаще всего используется для:
- Диагностирования злокачественных новообразований данного органа
- При диагностике доброкачественных опухолей и кист поджелудочной железы,
- При хроническом воспалительном процессе (панкреатите)
- Для определения структуры органа
- При травматических повреждениях железы.
Сложность ангиографического исследования поджелудочной железы заключается в том, что в кровоснабжении органа принимают участие несколько артерий, а опухоли практически не содержат сосудов. Поэтому ангиография применяется в основном для определения размера новообразования, его распространения, связи с основными сосудами и патологии самих сосудов.
Проводится исследование методом селективной артериографии путем катетеризации брюшной части аорты через бедренную артерию и продвижения катетера в ее ветви (целиакография и мезентерикография).
В ходе исследования можно выделить три этапа:
- Артериографию — рентгенконтрастное вещество наполняет артерии,
- Паренхимографию - контрастное вещество проникает во все капилляры и видны контуры железы,
- Флебографию — наполнены вены, по которым кровь отходит от органа.
Подготовка и проведение исследования не отличаются от брюшной аортографии.
Осложнения ангиографического исследования брюшной полости
К основным осложнениям ангиографического исследования органов брюшной полости относятся:
- Кровотечение, гематома, боль или отечность в месте введения катетера
- Аллергическая реакция на йод, входящий в состав рентгенконтрастного вещества
- Повреждение стенки сосуда
- Развитие острой печеночной или почечной недостаточности
- Нарушения сердечного ритма.
Для того, чтобы избежать развития осложнений необходимо провести тщательную подготовку к исследованию и выбрать наименее опасную методику его проведения.
Среди сцинтиграфических методик выделяют:
• панкреатоспинтиграфию (внутривенное введение метионина, меченного 75Se);
• панкреатоангиосцинтиграфию (селективное введение макроагрегата альбумина, меченного 131I,99mТс или 113Тс в артерии ПЖ).
На практике обычно применяют первый метод, технически более простой и необременительный для больного.
При сцинтиграфии получают изображение распределения радионуклида в ПЖ после его внутривенного введения. Характер и качество изображения зависят от скорости перераспределения радиофармакологического препарата и частоты получения сцинтиграмм. Кроме того, можно получить данные о количественном распределении радиофармпрепарата.
До настоящего времени не найдено химических веществ, обладающих способностью к избирательному накоплению только в паренхиме ПЖ. Обычно применяемая меченая аминокислота 75Sе-метионин накапливается во всех органах, где происходит синтез белка, в том числе в ПЖ, печени, почках, что не позволяет получить изолированного изображения ПЖ, так как на качество изображения органа влияет его окружение. Так, при использовании сцинтилляционной камеры в её поле зрения попадает целый ряд органов, синтезирующих протеин, которые могут помешать получению сцинтиграмм ПЖ. Нормальная ПЖ имеет несколько больший процент синтеза протеинов на грамм ткани, чем соседние органы, однако при её заболеваниях накопление радионуклида в ней снижено.
В связи с тем, что сцинтиграфическое изображение массивной печени — основная помеха для визуализации ПЖ, после получения первичной сцинтиграммы необходимо вычитание изображения печени.
Наибольшую концентрацию 75Se-метионина в ПЖ наблюдают через 30 мин после введения радиофармпрепарата. В этот период удельная активность 75Sе-метионина на единицу поверхности ПЖ в 4—8 раз больше, чем на поверхности печени. Через 20 мин 75Se-метионин, связанный с ферментами ПЖ, начинает поступать в просвет ДПК.
75Se — чистый гамма-излучатель, имеющий два фотопика. Период полувыведения препарата из организма колеблется от 20 до 67 дней (в среднем — 47 дней). В норме выведение 75Sе-метионина из организма составляет 15—20% за сутки, а из печени — 25—30% введённого количества препарата. 75Se-метионин выводят почки; в течение первых 2—3 ч выделяется 5—10% введённой дозы. ПЖ усваивает лишь незначительную часть (примерно 7%) введённой дозы 75Sе-метио-нина. При сцинтиграфии в ней обнаруживают лишь 0,185—3,7 МБк 75Sе-метионина, тогда как общая доза препарата, введённого больному, составляет 9,25 МБк препарата.
Накопление 75Sе-метионина поджелудочной железой зависит от численности функционирующих паренхиматозных клеток. Дегенеративные изменения их приводят к снижению усвоения меченой аминокислоты.
Неизменённая ПЖ на сцинтиграмме имеет длину 14-18 см, ширину — 3—4 см и доходит до ворот селезёнки или входит в них на 1—2 см. Фиброз или липоматоз ПЖ приводит к укорочению изображения органа, который на сканограмме может отстоять от селезёнки на 3—5 см. Уменьшение ширины железы до 2 см отмечают при фиброзных изменениях. Увеличение органа наблюдают после перенесённого обострения ХП. Возможно расширение изображения всей ПЖ или части, достигающее 6-8 см.
Опухолевидные образования соседних органов, сращения после перенесённых операций могут привести к смещению изображения всей ПЖ или её отделов.
Сканографическая картина нормальной ПЖ разнообразна. Выделяют четыре варианта ПЖ: S-образная, крючковидная, подковообразная и вытянутая.
Сцинтиграфически охарактеризовать нормальную ПЖ не всегда легко. В норме её изображение на сцинтиграмме однородно, гомогенно, без дефектов накопления изотопа; край ровный и гладкий. Нормальная железа имеет обычные топографические отношения с окружающими тканями, без выраженного её смещения. Головка накапливает больше изотопа на единицу поверхности, чем тело и хвост. Перешеек, как правило, тоньше, чем головка и тело, и поэтому на сцинтиграмме составляет 2/3 толщины головки или тела.
Возрастные изменения чаще всего выражаются артериосктеротическими сосудистыми процессами в железе, приводящими к липомагазу. Размеры нормальной ПЖ пожилых людей несколько меньше на сцинтитраммах, чем у молодых людей. Она редко бывает совершенно гомогенной и однородной.
Различные хронические заболевания ПЖ заметны на сцинтиграфической картине органа, что обычно позволяет уловить ухудшение течения заболевания. Обострение рецидивирующего ХП приводит к снижению или почти полному прекращению фиксации железой радиометки. Хорошая визуализация ПЖ восстанавливается не ранее чем через 3 нед с момента купирования приступа.
У больных с ХП в периоде ремиссии на сцинтиграмме обнаруживают очаговые изменения, которые нередко сочетаются с увеличением головки органа. При обострении процесса отмечают признаки отёчности железы на фоне очаговых изменений фиброзного характера.
При латентном (безрецидивном) течении ХП, не сопровождающемся возникновением панкреонекроза и грубого фиброза, железа обычно сохраняет свою первоначальную форму, но становится уже, и, как правило, короче. В конечной стадии заболевания, характеризующейся выраженным фиброзом железы, на сцинтиграмме могут возникать как локальные, так и генерализованные его признаки. Фиброзная ткань не накапливает 75Sе-метионин, в связи с чем не всегда на сцинтиграмме удаётся получать изображение изменённой ПЖ, а при визуализации орган, как правило, выглядит узким.
Важнейшая задача сцинтиграфического исследования — отличить патологически изменённую ПЖ от нормальной. Патологические изменения на сцинтитраммах отмечают в 90% случаев ХП, ложноположительные результаты — в 14%. Таким образом, можно считать, что сцинтиграфия — достаточно чувствительный метод обнаружения патологических изменений в ПЖ.
Один из важнейших признаков очаговых поражений ПЖ — возникновение на сцинтитраммах дефекта накопления метионина, меченного 75Se.
Причины резкого изменения степени накопления радионуклида состоят либо в нарушении нормального метаболизма в той или иной области ПЖ (например, вследствие локального воспалительного процесса, вызванного обструкцией протока), либо в дегенеративных изменениях паренхимы органа при кисте, очаговом фиброзе или опухолевом поражении.
Сцинтиграфические признаки кисты ПЖ:
♦ различные по величине и локализации округлой формы дефекты накопления индикатора с неизменёнными участками железы по периферии;
♦ оттеснение этих участков железы кистозными образованиями;
♦ резкое снижение накопления индикатора в тканях железы;
♦ ускоренное поступление меченого панкреатического секрета в кишечник.
Сцинтиграфическая картина панкреатической кисты зависит от её размера. В связи с тем, что внутри кисты не происходит синтез белка, накопление 75Sе-метионина в кистозно перерождённом отделе железы всегда снижено или отсутствует. Небольшие кисты обычно создают небольшие дефекты накопления изотопа по периферии железы.
Лучевая нагрузка при проведении сцинтиграфии ПЖ сравнительно высока и обусловлена длительностью периода полураспада 75Sе-метионина (120 дней).
В связи с высокой лучевой нагрузкой обязательным считают строгое установление показаний к проведению исследования. Больных до 35 лет нежелательно подвергать панкреатосцинтиграфии (особенно повторной).
Необходимо отметить, что накопление 758е-метионина железой может быть нарушенным при целом ряде заболеваний, не связанных с поражением этого органа. Всё это в сочетании с высокой лучевой нагрузкой при проведении исследования не даёт основания причислять панкреатосцинтиграфию к числу ведущих методов исследования морфологического состояния ПЖ. Однако установлено, что получение нормальной сиинтиграммы органа с большой долей вероятности позволяет исключить заболевание ПЖ. Наконец, панкреатосцингиграфия может служить ориентировочным способом оценки тяжести поражения железы (независимо от этиологии) и, следовательно, тестом, позволяющим оценить динамику течения ХП и эффективность лечения.
Позитронно-эмисионная томография — новейший метод лучевой диагностики, только в последнее время нашедший реальное клиническое применение. Будучи частью радионуклидной диагностики, этот метод обладает уникальными возможностями определения регионального метаболизма естественных биологически активных веществ. Получение трёхмерных изображений позволяет провести оценку биохимических и обменных процессов во всём организме и в отдельном органе.
Использование этого метода для исследования ПЖ ещё практически не изучено. В зависимости от степени накопления радиофармпрепарта можно с уверенностью дифференцировать доброкачественные и злокачественные новообразования ПЖ, а при диффузном снижении накопления радиофармпрепарата — диагностировать ХП.
Ангиография
Ангиография — один из самых инвазивных методов диагностики заболеваний ПЖ. Прямые показания к применению метода у большинства больных с заболеваниями ПЖ отсутствуют. Ангиографию применяют только Д1Я дифференциальной диагностики опухолей, при подозрении на ХП сосудистого генеза и аномалию строения ПЖ. При предоперационном обследовании больных с раком ПЖ ангиография способна помочь в точном определении распространения опухоли (см. рис. 2-23) и диагностике тромбоза мезентсриальных сосудов, определяющего послеоперационный прогноз.
Читайте также:

