Саркоматоидный вариант рака почки
Таргетная терапия в лечении метастатического почечно-клеточного рака была недавно введена в урологическую практику. Препараты для этой терапии используются у очень ограниченного числа пациентов и только при светлоклеточной гистологии. Мы представляем случай применения сорафениба, мультикиназного ингибитора клеточной пролиферации и ангиогенеза опухоли, у пациента с метастатическим почечно-клеточным раком светлоклеточной гистологии. Мы обнаружили, что наши результаты отличаются от ранее опубликованных исследований, потому что саркоматоидная дифференциация в гистологическим ответе этого пациента была очевидна. В результате лечения был получен отличный ответ на сорафениб. Этот случай может быть доказательством того, что антиангиогенные агенты могут быть активны при любом гистологическом типе рака почки. Тем не менее, нет доступных данных, которые могли бы продемонстрировать длительность ответа и прирост выживаемости. [J Chin Med Assoc 2010;73(5):262–264]
Ключевые слова: метастазы, почечно-клеточный рак, саркоматоидная дифференциация, сорафениб
Введение
Сорафениб и сунитиниб, мультикиназные ингибиторы опухолевой пролиферации и ангиогенеза, как было показано, имеют некоторую активность в 2 двойных слепых, плацебоконтролируемых исследованиях у пациентов с метастатическим почечно-клеточным раком (ПКР). Гистологический ответ у всех пациентов - светлоклеточный рак почки. В настоящее время нет исследований, показывающих, что сорафениб и сунитиниб также эффективны при метастатическом раке почки несветлоклеточного происхождения. Мы сообщаем о случае использования сорафениба у пациента с метастатическим раком почки и саркоматоидной дифференциацией.
История болезни
38-летний мужчина с метастатическим раком почки продемонстрировал прогрессирование заболевания после стандартной терапии интерлейкином-2 (ИЛ) и интерферон-α (ИФН-α). Компьютерная томография (КТ) органов брюшной полости показала опухоль левой почки 73˟65 мм и метастаз 15 мм с перифокальным отеком в теменной доле головного мозга. Мы также наблюдали несколько метастатических узелков в паренхиме обеих легких (рис. 1,3).
Рисунок 1: а – на компьютерной томографии до операции видна опухоль левой почки, б – компьютерная томография брюшной полости после операции
Рисунок 2: а – множественные метастазы в легких, б – после лечения метастазы отсутствуют
Рисунок 3: удаленная левая почка
Радикальная нефрэктомия слева была проведена в октябре 2005 года. Патогистологическая экспертиза показала светлоклеточный рак с диффузной саркоматоидной дифференциацией. Ядерная атипия по Фурману III. Патогистологическое стадирование – T3, хирургический край положителен. Инвазии в ЛУ и надпочечники не отмечено (рис. 4 и 5).
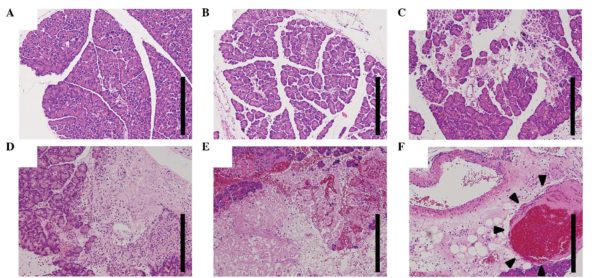
Рисунок 4: Светло-клеточный рак почки с саркоматоидной дифференциацией (окраска гематоксилин-эозин)
Рисунок 5: Метастаз в теменной доле головного мозга с перифокальным отеком
Послеоперационная лучевая терапия на область метастаза в головном мозге и перифокального отека была выполнена сразу после вмешательства. Поглощенная доза рентгентерапии этой зоны составила 30 Гр: 10 процедур по 3 Гр. В январе 2006 года наблюдался регресс размеров внутричерепной опухоли и отека. После этого пациент получал иммунотерапию ИЛ-2 и ИФН-α на протяжении 8 недель (20 МЕ/сутки, 3,5 дней в неделю ИФН-α и 72000 МЕ/кг ИЛ-2). К сожалению, во время осмотра после иммунотерапии ответа не наблюдалось, более того, в левой почечной ямке обнаружена новая опухоль.
Мы решили, что таргетная терапия сорафенибом - последний вариант лечения данного пациента. В апреле 2006 года, пациент начал лечение сорафенибом перорально в дозе 400 мг два раза в день в соответствии с рекомендациями Kroog и Motzer. Через 6 месяцев пациент был еще жив, КТ всего тела не показало клинической прогрессии. КТ брюшной полости и грудной клетки не выявлено метастатических очагов ни в левой почечной ямке, ни в паренхиме легких.
К сожалению, пациент умер из-за прогрессирования заболевания с множественными метастазами через 22 месяца после установки диагноза, не смотря на полный ответ с исчезновение всех опухолевых метастазов через 6 месяцев после начала терапии. Тем не менее, выживаемость в данном случае составила 22 месяца. У пациента был невыраженный подошвенно-ладонный синдром из-за токсичности препарата. Данное осложнение не нуждалось в дополнительной медикаментозной коррекции.
Обсуждение
ПКР является наиболее агрессивным и летальным раком мочеполовой системы, с более чем 40% онкоспецифической летальностью. К сожалению, для метастатического рака почки до сих пор не разработано надежного альтернативного лечения. В последнее время исследования в таргетной терапии, в том числе мультикиназное ингибирование и антиангиогенез, обнадежили врачей демонстрацией некоторой активности в лечении метастатического рака почки. В целом, преимущества выживания без прогрессирования на фоне таргетной терапии были продемонстрированы в 2 двойных слепых, плацебо-контролируемых исследованиях лечения метастатического заболевания. Тем не менее, многие вопросы остаются без ответа.
Уровень ответа при различных гистологических типах не определен. Мы применяли сорафениб у пациента с метастатическим раком почки и саркоматоидной дифференциацией и получили отличный результат.
Этот случай является доказательством того, что определенные антиангиогенные агенты могут быть активными при раке почки, отличном от светлоклеточного. Дополнительные данные об устойчивости ответа могут прояснить ситуацию касательно полного ответа и выживаемости.
Эпидемиология и этиология
Рак почки, или почечно-клеточный рак (ПКР), — наиболее распространенное солидное новообразование почек, на него приходится около 90% всех злокачественных опухолей этого органа.
Заболеваемость среди мужчин в 1,5 раза выше, чем среди женщин.
Пик заболеваемости приходится на возрастной промежуток 60-70 лет.
ПКР составляет 2-3% всех эпителиальных опухолей.
Отмечен ежегодный прирост частоты возникновения рака почки как во всем мире, так и в России. Ежегодно в Европейском союзе фиксируют приблизительно 65 000 новых случаев рака почки и 26 000 смертей, связанных с этим типом рака.
За последнее десятилетие успехи молекулярной биологии привели к разделению почечно-клеточного рака на различные подтипы с характерными специфическими патогистологичеекими и генетическими характеристиками.
Важные этиологические факторы риска — образ жизни, курение, ожирение и артериальная гипертензия. Наличие рака почки в анамнезе у родственников первой степени также ассоциируется с повышенным риском развития ПКР.
Наиболее доказанными эффективными мерами профилактики заболевания служат отказ от курения и борьба с ожирением.
Диагностика и стадирование
Клиническая картина
Во многих клинических наблюдениях опухоль почки не пальпируется, вплоть до поздних стадий заболевания. В настоящее время около 70% всех случаев почечно-клеточного рака обнаруживают случайно во время обследования по поводу других заболеваний.
Классическая триада клинических симптомов (боль в боку, макрогематурия и пальпируемое образование в брюшной полости) сегодня встречается редко (6-10% случаев).
Экстрарснальные или иаранеопластические синдромы рака почки отмечают приблизительно у 30% больных, имеющих клинические признаки ПКР,
Наиболее распространенными парансопластическими признаками являются следующие:
• артериальная гипертензия;
• лихорадка;
• эритроцитоз;
• анемия;
• гиперкалыдиемия;
• повышенная скорость оседания эритроцитов (СОЭ);
• кахексия; снижение массы тела;
• нейромиопатия;
• амилоидоз;
• нарушения функций печени;
• симптомы метастатического заболевания, такие как боль в костях или кашель.
Физикальное обследование
Роль физикального обследования в диагностировании почечно-клеточного рака невелика.
Однако обнаружение следующих симптомов должно стать поводом для проведения более детального лучевого обследования:
• наличие пальпируемой опухоли в брюшной полости; пальпируемые шейные лимфатические узлы;
• неспадающееся левостороннее варикоцеле или варикоцеле справа;
• двусторонний отек нижних конечностей (может свидетельствовать о вовлечении венозной или лимфатической дренажной системы).
Лабораторная диагностика
Среди лабораторных параметров наиболее информативно с точки зрения прогноза течения заболевания определение количества сывороточного креатинина, скорости клубочковой фильтрации, содержания гемоглобина, СОЭ, активности щелочной фосфатазы, лактатдегидрогеназы и концентрации сывороточного кальция.
Функциональное состояние почек особенно необходимо оценивать в следующих ситуациях:
• при наличии риска значительного снижения почечных функций в процессе лечения (опухоль единственной почки, опухолевое поражение обеих почек);
• при снижении функций почек, на что указывает повышение содержания креатинина сыворотки крови;
• у пациентов, имеющих риск снижения функций почек в будущем по причине наличия сопутствующих заболеваний, таких как сахарный диабет, хронический пиелонефрит, реноваскулит, почечнокаменная болезнь или поликистоз почек.
Лучевая диагностика
Большую часть новообразований почечной паренхимы выявляют при УЗИ или КТ, выполняемых по другому поводу. Визуализацию можно использовать для дифференциации образований почек на солидные и кистозные. Для солидных образований в почках важнейшим дифференциальным критерием злокачественных новообразований служит наличие контрастирования.
Традиционно для выявления и характеристики образований почек используют УЗИ, КТ или магнитно-резонансная томография (МРТ). Большинство образований в почках можно точно диагностировать при помощи только методов визуализации. УЗИ с контрастированием может быть полезным в особых случаях (например, при хронической почечной недостаточности с относительными противопоказаниями к использованию контрастных веществ на основе гадолиния или йодированных контрастных веществ).
КТ или МРТ используют для определения характера новообразований почки. Необходимо получать изображения как до, так и после внутривенного введения контрастного вещества. На снимках КТ контрастирование в новообразованиях почек определяют путем сравнения контрастности по шкале Хаунсфилда (в единицах шкалы HU) до и после введения контраста. Изменение контрастности на 20 HU или более служит убедительным доказательством контрастирования. Для более точной дифференциальной диагностики оценку следует проводить по изображениям, соответствующим нефрографической фазе:
КТ органов брюшной полости позволяет диагностировать ПКР и получить информацию о:
• строении и функциях контралатеральной почки;
• распространении первичной опухоли за пределы почки;
• вовлечение в поражение венозной системы;
• увеличении регионарных лимфатических узлов;
• состоянии надпочечников и печени.
КТ-ангиографию сосудов брюшной полости с применением контрастного вещества можно с успехом использовать для получения подробных сведений о состоянии кровоснабжения почек.
В случае если результаты КТ неопределенные, можно прибегнуть к МРТ и получить дополнительную информацию относительно:
• выявления контрастирования в новообразованиях почек; исследования местно-распространенного злокачественного образования;
• степени поражения венозной системы, если при КТ плохо определяется распространение опухолевого тромба в нижнюю полую вену. МРТ-визуализация также показана пациентам с аллергией на рентгеновский контраст и беременным без нарушения функций почек. Оценить распространение опухолевого тромба можно с помощью ультразвуковой допплерографии.
Почечная артериография и кавография имеют ограниченные показания, их используют в качестве дополнительных средств диагностики у отдельных пациентов. У больных с малейшими признаками снижения функций почек следует рассмотреть вопрос об обязательном проведении изотопной ренографии и полной оценке функций почек с целью оптимизации планируемого лечения, например при необходимости сохранения почечных функций. Подлинное значение позитронно-эмиссионной томографии (ПЭТ), применяемой для диагностики рака почки и последующего наблюдения за больными, еще предстоит определить. В настоящее время ПЭТ не является стандартным методом исследования.
Исследования при метастатической форме почечно-клеточного рака
КТ органов грудной клетки служит наиболее точным методом выявления метастазов в легких. При недоступности КТ для обнаружения легочных метастазов следует выполнять хотя бы рентгенографию органов грудной клетки. На сегодняшний день считается, что большая часть метастазов в кости и головной мозг имеют те или иные клинические проявления к моменту постановки диагноза, поэтому рутинное сканирование костей скелета и КТ головного мозга обычно не показаны. При наличии соответствующих показаний (клинические или лабораторные признаки) могут быть выполнены и другие диагностические процедуры, такие как сканирование костей скелета, КТ или МРТ головного мозга.
При выявлении кистозных новообразований почек их целесообразно классифицировать. Наиболее эффективной классификацией служит разделение по Босняку.
Классификация по Босняку, используемая для оценки кистозных новообразований в почках, подразумевает разделение кист почек на пять категорий на основании их вида на КТ-изображениях с целью прогнозирования риска возникновения злокачественного образования. Система Босняка также содержит рекомендации по лечению для каждой из этих категорий (табл. 2-1).
Таблица 2-1. Классификация кист почек по Босняку

Биопсия опухоли почки
Биопсия опухоли почки все чаще находит применение в диагностике, последующем клиническом наблюдении за больными и абляционных видах лечения. Толсто игольная биопсия в большинстве серий демонстрирует высокую специфичность и чувствительность в определении злокачественных образований, хотя следует отметить, что 10-20% биопсий не дают возможности составить заключение о результате.
Цель биопсии — определение потенциальной злокачественности, типа и степени дифференцировки оцениваемого новообразования почки. Чрескожная биопсия при наличии в почках крупных образований, подлежащих нефрэктомии, нужна редко. Прогностическая ценность положительною результата по данным визуализации настолько высока, что отрицательный результат биопсии не изменяет назначений.
Биопсия также показана пациентам с метастазирующим раком перед началом проведения им системной таргетной терапии, так как определение типа опухоли может иметь значение в выборе того или иного таргетного препарата.
Морфологическая диагностика
Морфологический диагноз почечно-клеточного рака устанавливают после хирургического удаления опухоли почки или исследования образца, взятого при биопсии. При раке почки общепринята классификация Фурмана по степени дифференцировки (I, II, III и IV), представляющая важный независимый прогностический фактор течения и прогрессирования заболевания.
Существует пять морфологических подтипов рака почки:
• светлоклеточный (80-90%);
• папиллярный (10-15%) I и II подтипов;
• хромофобный (4-5%);
• саркомоподобный.
Эти типы отличаются гистологическими и молекулярно-генетическими характеристиками, которые представлены в табл. 2-2. Папиллярный рак почки, в свою очередь, подразделяют на два различных подтипа: I и II, отличающийся неблагоприятным клиническим течением (см. табл. 2-2).
10 15% опухолей почек включают разнообразные редкие спорадические и семейные карциномы, некоторые из них были недавно описаны, и гpyппy неклассифицированных карцином.
Таблица 2-2. Основные гистологические подтипы почечно-клеточного рака

Согласно классификации по Босняку, основанной на критериях визуализации, мультилокулярный светаоклеточный ПКР представляет собой кистозные новообразования II или III типа. Однако такие же типы новообразований по Босняку характерны для смешанной эпителиально-стромальной опухоли почки, кистозной нефромы или мулыилокулярной кисты (все они относятся к доброкачественным опухолям).
Во многих случаях выполнение предоперационной биопсии и интраоперационное исследование замороженных срезов не дают возможности установить правильный диагноз. К счастью, для всех этих опухолей существует одна и та же стратегия оперативного лечения. По этой причине рекомендуют (если это технически осуществимо) в случае обнаружения в почках комплексных мультикистозных новообразований, имеющих повышенную плотность, выбирать органосохраняющее лечение.
Папиллярные аденомы — опухоли папиллярного или тубулярного строения с низкой степенью дифференцировки и диаметром 4 см в диаметре);
• если больная — женщина детородного возраста;
• если осуществление последующею контроля или возможность срочного реагирования для данного пациента затруднены.
В большинстве случаев больного с ангиомиолипомой можно вылечить с помощью консервативных органосохраняющих подходов, но в некоторых ситуациях необходимо полное, удаление почки. Кроме стандартных хирургических вмешательств, могут быть использованы селективная артериальная эмболизация и радиочастотная абляция. Несмотря на то что селективная эмболизация артерий эффективна для остановки кровотечения в остром случае, для долгосрочного решения проблемы ангиомиолипомы ее эффективность ограничена.
Другие опухоли почек
Обзор прочих опухолей почек с указанием возможности малигнизации и рекомендаций по проведению лечения представлен в табл. 2-3.
Таблица 2-3. Прочие опухоли почек и их лечение


Точное стадирование ПКР с помощью КТ или МРТ органов брюшной и грудной полостей является обязательным. КТ — наиболее чувствительный метод. Использование сканирования костей скелета и КТ головного мозга при отсутствии специфических клинических показаний не считают оправданным. В последнее время все больше уделяют внимание проведению тонкоигольной биопсии для оценки и абляционной терапии при небольших опухолях почки.
За последние 10 лет рак почки стал встречаться почти вдвое чаще, но все равно относится к редким видам злокачественных опухолей. Современная классификация выделяет 4 гистологических типа рака почки, и сейчас мы расскажем о каждом из них:
Светлоклеточный рак почки
Самым распространенным гистологическим типов рака почки является светлоклеточный рак почки. Он составляет, приблизительно, 80% от всех встречающихся видов рака почки. Светлоклеточный рак почки отличается умеренной злокачественностью и хорошо поддается лечению.
В настоящее время светлоклеточный рак почки лечится с помощью таргетной терапии. Существует множество линии таргетной терапии, что позволяет увеличить продолжительность жизни пациента.


Папиллярный рак почки
Папиллярный рак почки стоит на втором месте по распространенности и подразделяется на два подтипа:
-
Папиллярный хромофильный рак почки (15% от всех случаев рака почки) и
Папиллярный рак почки характеризуется спокойным течением и редким метастазированием. В современной онкологии он также лечится с помощью таргетной терапии.


Рак почки из собирательных трубочек и Медуллярный рак почки
Редкими видами рака почки являются рак почки из собирательных трубочек и медуллярный рак почки. Они встречаются в 2% случаев от всех диагностируемых типов рака почки. При этих гистологических типах применяется только оперативное и химиотерапевтическое лечение. Таргетная терапия при данных гистологических типах не показана.


Рак почки из собирательных трубочек на микрофотографии и на снимке КТ


Медуллярный рак почки на микрофотографии и на снимке КТ
Саркоматоидный подтип рака почки
Саркоматоидный подтип рака почки не является самостоятельным гистологическим типом рака почки и может встречаться при любых гистологических вариациях рака почки.
Наличие саркоматоидного подтипа указывает на крайне неблагоприятный прогноз и тяжелое течение заболевания.
1. 2016 Клинические рекомендации "Рак почки" (Российское общество урологов)
Классификация
Т Первичная опухоль
ТХ Первичная опухоль не может быть оценена
Т0 Нет подтверждений наличия первичной опухоли
Т1 Опухоль ≤7 см в самом большом измерении, ограниченная почкой
- Т1а Опухоль ≤4 см в самом большом измерении, ограниченная почкой
- Т1b Опухоль>4 см, но менее 7 см в самом большом измерении, ограниченная почкой
T2 Опухоль более 7 см в самом большом измерении, ограниченная почкой
- Т2а Опухоль более 7 см, но ≤10 см в самом большом измерении, ограниченная почкой
- Т2b Опухоль болеее 10 см в самом большом измерении, ограниченная почкой
T3 Опухоль распространяется в крупные вены, непосредственно прорастает в надпочечник, но не в ипсилатеральный надпочечник и не распространяется за пределы фасции Герота
- T3a Опухоль распространяется в почечную вену или ее сегментарные ветви, надпочечник или распространяется на паранефральную и/или парапельвикальную клетчатку, но в пределах фасции Герота
- T3b Опухоль распространяется в нижнюю полую вену ниже диафрагмы
- T3c Опухоль распространяется в нижнюю полую вену выше диафрагмы или врастает в стенку нижней полой вены
T4 Опухоль распространяется за пределы фасции Герота, включая прорастание в ипсилатеральный надпочечник
N Регионарные лимфатические узлы
NX Регионарные лимфатические узлы не могут быть оценены
N0 Отсутствие метастазов в регионарных лимфатических узлах
N1 Метастазы в регионарных лимфатических узлах
M Отдаленные метастазы
MX Отдаленные метастазы не могут быть оценены
M0 Отсутствие отдаленных метастазо
M1 Отдаленные метастазы
| Стадия | Категория T | Категория N | Категория M |
| I | T1 | N0 | M0 |
| II | T2 | N0 | M0 |
| III | T3 | N0 | M0 |
| IV | T1,T2,T3 T4 T любое | N1 N любое N любое | M0 M0 M1 |
Анатомические классификации, такие как шкалы PADUA, R.E.N.A.L. и C-индекс, необходимы для того, чтобы стандартизировать описание опухолей почек. Эти классификации включают оценку размеров опухоли экзофитного или эндофитного характера роста, близость к собирательной системе почки и переднее или заднее расположение. Использование таких шкал полезно, поскольку оно позволяет объективно прогнозировать потенциальную сложность выполнения резекции почки и аблативных методик.
ПКР включают широкий спектр гистологических вариантов, описанных в 2004 г. в классификации Всемирной организации здравоохранения (ВОЗ) и модифицированных в Ванкуверской классификации Международного общества урологических патоморфологов (ISUP).
Существуют три основных варианта ПКР: светлоклеточный, папиллярный I и II типа и хромофобный.
Варианты ПКР были подтверждены с помощью цитогенетических и генетических анализов. Рак собирательных трубочек и другие редкие опухоли почек обсуждаются в
Гистологический диагноз включает помимо варианта ПКР степень ядерной дифференцировки, наличие саркоматоидного компонента, сосудистой инвазии, некрозов в опухоли и распространение в паранефральную клетчатку и собирательную систему почки. Наиболее приемлемой считается классификация по Фурману. Общество ISUP предложило упрощенную классификацию как альтернативу классификации Фурмана, основанную только на размере и форме ядер.
Светлоклеточные варианты опухолей почки, как правило, хорошо ограничены, капсула отсутствует. На срезе опухоль золотисто-желтого цвета, часто с очагами кровоизлияния и некрозом. Наиболее часто используется классификация Фурмана. Наиболее часто диагностируют следующие генетические изменения: делецию 3р хромосомы и мутацию гена VHL (von Hippel – Lindau) в хромосоме 3p25. Светлоклеточный вариант ПКР имеет худший прогноз по сравнению с папиллярным и хромофобным вариантами, даже при стратификации по стадиям. Пятилетняя опухолево-
специфическая выживаемость составляет 91, 74, 67 и 32% для TNM стадий I, II, III и IV соответственно (у больных, пролеченных в 1987–1998 гг.). Вялотекущим вариантом светлоклеточного ПКР является многокамерная киста почки, которая встречается в 4% всех светлоклеточных вариантов ПКР.
Макроскопически папиллярный ПКР окружен псевдокапсулой чаще желтого или коричневого цвета и мягкой консистенции. Наиболее часто диагностируют следующие генетические изменения: трисомии хромосом 7 и 17 и делецию хромосомы Y. Папиллярный ПКР является гетерогенным, существуют три различных типа: два основных (1-й и 2-й) и третий онкоцитарный тип. По сравнению со светлоклеточным ПКР папиллярный ПКР чаще диагностируют на уровне локализованного опухолевого процесса (pT1-2N0M0). Для папиллярного ПКР характерны высокие показатели пятилетней опухолевоспецифической выживаемости [39]. Прогноз для папиллярного ПКР 2-го типа хуже, чем для 1-го типа.
Экзофитный характер роста, псевдонекротические изменения и наличие псевдокапсулы являются типичными признаками папиллярного ПКР 1-го типа. Формирование псевдокапсул и обширный некроз формируют сферическую экзофитную опухоль. Опухоли с массивными некрозами хрупки и склонны к спонтанным разрывам с последующим кровотечением в результате минимальной травмы забрюшинного пространства.
Хорошо развитая псевдокапсула папиллярного ПКР 1-го типа, вероятно, предотвращает разрыв этих опухолей, несмотря на наличие некрозов. Некроз окруженный живой опухолевой тканью при КТ визуализируется как серпигинозные края с усиленным контрастированием. Некоторые авторы считают, что онкоцитарный папиллярный ПКР не формирует псевдокапсулы или массивного некроза, редко распространяется экстраренально и обладает низким злокачественным потенциалом, хотя этот вид не является общепринятым.
Хромофобный ПКР представлен опухолью бледно-коричневого цвета, относительно гомогенной и плотной, как правило с хорошо ограниченными массами без капсулы. G.P. Paner и соавт. в 2010 г. вместо классификации Фурмана предложили новую классификацию.
Наиболее часто диагностируют следующие генетические изменения: потерю хромосом 2, 10, 13, 17 и 21. Прогноз относительно благоприятный с высокими показателями пятилетней безрецидивной и десятилетней опухолевоспецифической выживаемости.
Редкие варианты опухоли почек составляют 10–15% от всех опухолей почек.
Высокий, очень агрессивный рак.
Медиана общей выживаемости
30 мес.
Высокий, очень агрессивный рак.
Медиана общей выживаемости
5 мес.
*ОСЛ – органосберегающее лечение
Большинство ангиомиолипом требует активного наблюдения.
Лечить с помощью эмболизации или резекции почки необходимо в следующих случаях:
- большие опухоли ( более 4 см)
- женщины детородного возраста
- пациенты, которые не будут наблюдаться и у которых ограничен доступ к неотложной помощи
При кистозных поражениях почки, соответствующих III и IV категории по классификации Босниака, показано хирургическое лечение.
При кистозных образованиях III категории следует выполнить резекцию почки (органосберегающая операция).
Если диагноз онкоцитомы верифицирован с помощью биопсии, то лучше прибегнуть к активновыжидательной тактике
При ангиомиолипоме методы лечения, направленные на ее удаление (нефрэктомия или резекция почки) либо разрушение (термоабляция или селективная эмболизация питающей артерии), показаны лишь в отдельных случаях, при этом предпочтительно выполнение органосберегающей операции
При редких вариантах опухолей почки в распространенной стадии стандартизированного подхода к лечению не существует, необходим индивидуальный подход.
Почечно-клеточный рак – серьёзное поражение тела, которое часто заканчивается смертельным исходом. Это обусловлено бессимптомным течением начальных стадий патологического процесса. Данные статистики тревожат: согласно отчётам, частота встречаемости недуга ежегодно растёт.
Группу риска по болезни составляют мужчины 50-70 лет. У женщин и молодежи эта карцинома встречается, но реже. При отсутствии своевременного обращения за медицинской помощью этот вид онкологии представляет серьёзную опасность для жизни человека.
Понятие почечно-клеточной онкологии
Почечно-клеточный рак – онкология в мочеполовой системе. Клетки опухоли имеют округлый вид, по размеру образование способно занимать половину брюшной полости. Очаг поражения – эпителий почки и ткани почечных лоханок. Болезнь носит непредсказуемый стремительный характер развития. Наиболее часто при почечно-клеточной онкологии метастазы идут в ткани лёгких и печени, в костную ткань, в отделы головного мозга.
Признаки почечно-клеточной опухоли
Начало болезни почки бессимптомно. Первостепенные признаки патологического процесса в органе:
- в моче присутствуют нитевидные кровяные образования;
- дискомфорт внизу спины;
- уплотнение в почках, обнаруживается при пальпации.
Если из вышеперечисленных обнаружен хотя бы единственный симптом, стоит незамедлительно обратиться к врачу. Если отложить визит в медицинское учреждение, к указанным симптомам вскоре добавляется постоянная ноющая боль внизу спины, беспричинная лихорадка, недомогание, усталость, потеря массы тела.
Причины почечно-клеточного злокачественного процесса
Списка точных причин, гарантированно приводящих к онкологии, нет. Однако учёными определены факторы, помогающие развитию заболевания:
- табакокурение и алкоголизм;
- чрезмерное употребление красного мяса;
- избыточная масса тела;
- гормональные сбои в организме;
- сахарный диабет;
- заболевание мочеполовой системы воспалительного характера;
- артериальная гипертензия;
- бесконтрольное употребление в качестве обезболивающего средства фенацетина;
- воздействие радиоактивных лучей;
- поликистоз почек в результате гемодиализной терапии;
- генетическая предрасположенность;
- травмы почек;
- работа на вредном производстве, связанная с воздействием на организм асбеста, рентгеноконтрастных и кожедубильных веществ.
Этапы развития болезни и её разновидности
Почечно-клеточная карцинома проходит 4 стадии развития. Система TNM представляет описание онкологии: буква Т обозначает факт новообразования. N – отражает вовлеченность в метастазирование лимфоузлов. М – характеризует метастазирование. Течение почечно-клеточной онкологии распределяется по стадиям:
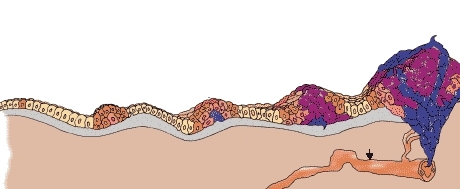
Стадия 0 – размер опухоли маленький, обнаружить её с помощью средств лабораторной диагностики невозможно. Иначе стадия называется g1 – клетки опухоли мало отличаются от здоровых.
Стадия 1 – онкологический процесс начинает прогрессировать. Опухолевое образование в диаметре до 7 см. Это стадия g2, степень патологического процесса средняя.
Стадия 2 – размер опухоли от 7 до 10 см. Новообразование размещается в тканях почки. Метастазов нет. Это стадия g3, онкоклетки специфически выглядят.
Стадия 3 – опухоль разрастается, но не выходит за пределы почечной капсулы. Это стадия g4, при которой онкоклетки резко отличаются от здоровых тканей.
Стадия 4 – рак распространяется метастазами в лимфоузлы, нарушая контуры капсулы почки. Это последний шаг развития недуга. Это стадия gх, онкоклеток уже больше, чем здоровых.
Почечно-клеточный рак классифицируют и по другому критерию:
- Онкология со светлыми клетками. Светлоклеточный вариант рака появляется в результате начала патологического процесса в клетках паренхимы.
- Папиллярный вариант рака. Образуется в тканях почечной лоханки. Онкоклетки этого заболевания называются сосочковыми. Патология встречается редко, но хорошо лечится.
- Хромофобная опухоль. Поражает каналец внутри почек и его корковый слой. Этот вид онкологии представляет интерес для исследователей: сейчас наука располагает ограниченной информацией об указанной разновидности опухоли.
- Онкоцитарная опухоль – заболевание редкое, отличается стремительным развитием, но незначительными метастазами.
- Протоковая онкология – рак трубочек. Этот вид карциномы появляется в центре почки и агрессивно метастазирует. Самый редкий злокачественный тип опухоли.

Диагностика рака опирается на результаты гистологических лабораторных исследований. Благодаря уровню развития современной медицины врачам всё чаще удаётся выявить наличие признаков злокачественного процесса на его начальных стадиях. Это определяет увеличение числа случаев успешного исцеления.
Диагностика почечно-клеточного рака
Как правило, заболевание обнаруживается на поздних стадиях. Для определения типа и этапа развития онкологии применяются специальные процедуры:
- Урография и общий анализ мочи. Процедуры помогают оценить дисфункцию почек в результате онкопоражения. Результат анализа свидетельствует о повышенном СОЭ.
- Ангиография почек – вариант рентген-диагностики. При этой процедуре диагностируются сосуды в почках с помощью рентген-аппарата.
- Рентген-исследование грудной клетки. Посредством исследования врачи делают выводы о метастазах в область лёгких через костную ткань.
- Результат анализа крови свидетельствует о повышенном уровне эритроцитов, креатинина, кальция, СОЭ. Показатели гемоглобина при раке низкие, что связано с анемией.
- УЗИ почек. Эта диагностика позволяет установить локализацию новообразования, оценить его размер и наличие метастазирования в соседние ткани и органы.
- УЗИ с использованием доплера. Данная процедура позволяет изучить состояние кровоснабжения почек и установить наличие поражения онкологией кровеносных сосудов.
- МРТ и КТ. Эти компьютерные исследования призваны подтвердить и уточнить данные, полученные с помощью УЗИ.
- Гистологический анализ. Для анализа берётся образец онкоткани, по которому определяется стадия болезни и разновидность.
Людям, занятым на вредном производстве, рекомендуется систематически проходить обследование на выявление онкологии, так как работа в таких условиях считается одним из факторов риска возникновения рака.
Лечение почечно-клеточного рака
Этот вид рака обнаруживает специфические особенности в лечении:
- Устойчивость поражённых клеток к воздействию консервативных способов терапии, в частности – к лучевой терапии и препаратам, применяемым в химиотерапии.
- Иногда размер опухоли сокращается, а течение болезни замедляется без медицинского вмешательства.
Основное лечение почечно-клеточного рака – операция.
Если размер новообразования не превышает 4 см в диаметре, врач может принять решение о проведении органосберегающего вида хирургического вмешательства: в ходе операции удаляется только сама опухоль с минимальным количеством здоровых тканей почки. В качестве сопутствующей медикаментозной терапии будет назначен микропрепарат.
Если опухоль к моменту назначения операции разрослась, врач принимает решение о проведении полного удаления органа мочеполовой системы. В этом случае помимо почки удаляются и близлежащие лимфоузлы и жировые ткани, чтобы избежать вторичного развития онкологии. После кардинального оперативного вмешательства назначают определённый макропрепарат, оказывающий противоонкологическое действие для купирования начального распространения метастазов.
Вспомогательным методом лечения рака после операции является иммунотерапия, цель которой – искусственное формирование иммунитета и защитных сил организма. Эффективны препараты с интерферонами.
Учёными-медиками ведутся разработки новых противораковых препаратов, способные гарантировать выздоровление. К инновационным средствам лечения относится радиочастотная абляция, микроволновая абляция, криодеструкция.
Прогноз при онкологии мочеполовой системы зависит от степени прогрессирования онкологии и её вида. Если рак находится на 4 стадии, лишь 10% больных проживают 5 лет после операции. Соблюдение медицинских рекомендаций и иммунотерапия чуть-чуть продлевают жизнь человека. Если же пациент обратился за медицинской помощью на начальных стадиях болезни, то с вероятностью в 80% прогноз будет благоприятный: соблюдение клинических рекомендаций будет препятствовать повторному развитию рака и способствовать долголетней жизни человека.
Многие патологии возможно предотвратить. Для снижения риска возникновения рака мочеполовых органов рекомендуется:
- Бросить курить и по возможности отказаться от употребления крепких алкогольных напитков. Характерная особенность этой болезни – небольшие дозы алкоголя служат профилактическим и лечебным средством в борьбе с раком.
- Если выявлена воспалительная патанатомия различной локализации, стоит обращаться в медицинское учреждение за назначением лечения. Людям, у которых диагностированы заболевания мочеполовой системы, рекомендуется 1-2 раза в год прописать курс Канефрона, заваривать чай с брусничным листом, пить морсы.
- При гормональных сбоях в организме, о которых свидетельствуют задержки менструации у женщин или изменение характера влагалищных выделений, а также ухудшение качества волос, ногтей, кожи, рекомендуется обратиться за консультацией к гинекологу-эндокринологу для назначения гормональных препаратов для стабилизации уровня гормонов в организме.
- При первых тревожных симптомах со стороны почек незамедлительно проходить обследование, чтобы скорее вскрылась патологическая анатомия органа.
Читайте также:

