Резекция печени колоректальный рак прогноз
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Прогноз нелеченых метастазов печени при колоректальном раке плохой. В настоящей публикации представлен опыт резекций метастазов, накопленный хирургами роттердамской клиники St. Claraziekenhuis. Всего за 7-летний период прооперировано 26 больных. Определены факторы и показатели, имеющие существенное значение для преоперационной оценки опухолей, описаны тактика вмешательства и меры, направленные на предотвращение осложнений. Не было случаев смерти, возникновения кровотечений или развития печеночной недостаточности. Подчеркивается необходимость тесного сотрудничества с региональным онкоцентром с целью улучшения результатов лечения. The prognosis of untreated hepatic metastases in colorectal cancer. The paper presents the experience gained by the surgeons from the St. Claraziekenhuis Clinic in Rotterdam in using metastatic resections. A total of 26 patients were operated on during 7 years. The factors and indices that are of great impоrtance for the preoperative assessment of tumors are definеd. An interventionаl policy and measures aimed at preventing complications are described. There were no deaths, hemorrhage, or hepatic failure. The need of close collaboration with a regional cancer center to improve treatment outcomes is emphasized.
J.F. Lange, хирург, Claraziekenhuis, Роттердам, Netherlands.
В St.Claraziekenhuis в Роттердаме уже 7 лет колоректальные метастазы печени оцениваются и оперируются в соответствии с протоколом. Контингент больных отбирается из собственных пациентов, находящихся под поликлиническим наблюдением. Число пациентов из-за этого ограничено (n=26), и пока что не было случаев смерти. Резекции печени выполняют три хирурга, один из которых на протяжении года стажировался в известной специализированной гепатобилиарной хирургической клинике за рубежом. Эта бригада хирургов также привлекается для резекций печени в других больницах.
Предоперационная оценка
Пациентов с гистологически доказанным метастазом в печени при колоректальной опухоли обследуют посредством компьютeрно-томографической (КТ) портографии для исключения двусторонних метастазов в печени. Число односторонних метастазов или их величина не имеют значения, хотя их множественность, вероятно, отрицательно влияет на прогноз. Колоноскопию выполняют для исключения локального рецидива на уровне анастомоза или же второй первичной опухоли в другом месте толстой кишки. Затем выполняют КТ-исследование грудной клетки и брюшной полости для выявления внепеченочных метастазов.
Календарный возраст пациентов менее важен, чем биологический. Самый старый из прооперированных пациентов был в возрасте 81 года. Момент резекции при синхронных метастазах печени зависит от размеров и локализации. Если речь идет о маленьком одиночном одностороннем метастазе печени диаметром менее 4 см, расположенном благоприятно, то тогда одновременно с резекцией толстой кишки может быть выполнена неанатомическая метастазэктомия.
Если метастазы расположены таким образом, что для получения свободного от опухоли края более чем 1 см, должна быть выполнена гемигепатэктомия, то тогда операция выполняется через 3 мес после первичной колонорезекции. Последующая онкологическая тактика обсуждается в онкологической рабочей группе.
Тактика во время операции
Вмешательство начинается с диагностической лапароскопии для исключения внепеченочных метастазов и нежелательного карциноматозного перитонита. Также выполняется лапароскопическое эхографическое исследование, при котором еще раз проверяют печень на наличие двусторонних метастазов. Под контролем эхографии во время операции может быть выполнено гистологическое исследование подозреваемых очагов с помощью замороженных препаратов. Если двусторонние метастазы печени и внепеченочные проявления исключены, то проводится лапаротомия, при которой следует избегать торакально-абдоминального разреза из-за риска легочных осложнений.
Периоперативно может быть выполнено эхографическое исследование печени для уточнения локализации метастазов и для оценки возможного вовлечения ветвей воротной и печеночных вен. Также может быть определен свободный от опухоли край.
Изолируются инфра- и супрапеченочные части полой вены (включая vena surenalis и ligamentum hepatoduodenale) для возможного тотального васкулярного исключения печени при случайных кровотечениях или васкулярном вовлечении метастазов. При тотальном васкулярном исключении печень полностью обескровлена на протяжении максимум 45 мин. Вследствие пережатия полой вены происходит значительное снижение кровяной нагрузки на сердце. В связи с этим всем пациентам перед операцией вводят термодилюционный катетер. Тотальное васкулярное исключение может применяться лишь в том случае, если удается удержать на необходимом уровне сердечный выброс и артериальное давление.
Резекция производится предпочтительно анатомически на основе разделения по Couinaud (см. рисунок; 8 функциональных сегментов, равномерно разделенных по обеим половинам печени) во избежание некроза краев резекции с развитием кровотечений и подтекания желчи. Лишь в случае маленьких единичных метастазов печени (меньше 4 см) может быть выполнена так называемая неанатомическая метастазэктомия. Во время гепатэктомии васкулярные структуры в ligamentum hepatoduodenale (a.hepatica propria и vena portae) пережимаются для предотвращения кровопотери. Этот так называемый Pringle-маневр может длиться лишь 25 мин во время паренхимной фазы операции. Необходимо придерживаться свободных от опухолей краев в 2 см как минимум. С целью ограничения кровопотери при больших паренхимных резекциях применяется ультразвуковой нож (CUSA).
Периоперативно проводят холангиографическое исследование для того, чтобы выявить и при необходимости устранить подтекание желчи в плоскости резекции. После тщательного гемостаза и контроля на подтекание желчи в оставшейся плоскости резекции печени брюшную полость закрывают.
Послеоперационное ведение
Помимо послеоперационного кровотечения, наиболее часто встречающегося осложнения (20%), после крупных резекций печени наблюдается билома. Если при эхографическом обследовании возникает подозрение на билому, то в большинстве случаев может быть выполнен чрескожный дренаж. Таким образом, колоректальные метастазы печени могут быть безопасно прооперированы; пока что еще не было случаев смерти, развития кровотечений или печеночной недостаточности. Недостаток средств для обеспечения специфическими ноу-хау и аппаратурой часто является препятствием для выполнения операций на печени, главным образом для периферийных больниц. Несмотря на это, во многих крупных периферийных больницах, так же как в St. Clarazielenhuis, проводятся операции на печени хорошего качества. Очень важно интенсивное сотрудничество с региональным онкологическим центром для обеспечения адъювантной терапии с целью улучшения в большинстве случаев недостаточных результатов хирургического лечения.
Взято из "IKR-bulletin", 1995;19(4);27-8 с разрешения редакции.
В рамках материалов о лечении онкологических заболеваний мы в своем блоге до сих пор не затронули такую ответственную область, как хирургия. Хотя именно хирургическое удаление опухоли – единственный радикальный метод лечения, существующий в онкологии.
Операции на печени – не самое главное и популярное направление работы клиники. Однако тот факт, что в нашем стационаре в принципе делают такие манипуляции, а не отправляют пациентов куда-то еще – это маркер и показатель высшей квалификации команды хирургов.
Операции на печени приравниваются к операциям на головном мозге и открытом сердце. Как правило, это седьмая категория сложности из 7 возможных.
При этом, успешное хирургическое лечение злокачественных новообразований в печени позволяет рассчитывать на продление жизни пациента: пятилетняя выживаемость в 40-50% при первичном раке печени или единичных метастазах – хороший результат.
К нам часто попадают пациенты, которых в других клиниках не стали оперировать по тем или иным официальным причинам. Но люди хотят воспользоваться вторым шансом, и мы им его даём.
В этой статье постараемся объяснить, из-за чего именно печень так часто требует внимания при лечении рака, почему не каждый хирург рискует ее оперировать и есть ли альтернативы скальпелю.
Печень — удивительно многозадачный орган. Работу ее можно поделить на 3 направления.
1. Депонирование. В печени организм хранит многие нужные вещи: энергетические резервы в виде гликогена; некоторые витамины (A, D, B12, К, РР); микроэлементы (главный из которых – железо).
Также здесь постоянно находится весьма значительный объем крови. Если в организме в результате травмы образуется не предусмотренное природой отверстие, то этот кровяной резерв будет экстренно выброшен в основное кровяное русло и на время скомпенсирует кровопотерю.
3. Детокс. Печень – уникальна тем, что умеет обезвреживать яды, токсины, аллергены и прочие опасные вещества, попавшие в организм извне, а также возникшие как продукт нашего обмена веществ.
Все эти важные функции печени обеспечиваются ее особенной системой кровоснабжения.
За минуту через печень проходит около 1,5 литров крови. Примерно четверть этого объема поступает по печеночной артерии, остальные 75% — по воротной вене от кишечника.
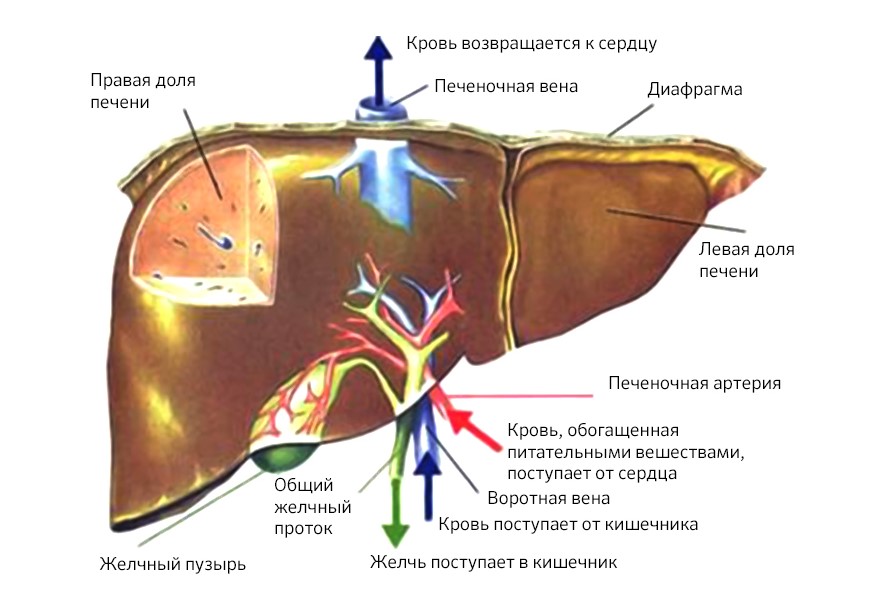
Схема кровообращения в печени
Но эта же замечательная система, которая позволяет печени фильтровать 2 000 л крови в сутки, способствует и распространению раковых клеток. Они с кровотоком разносятся по организму, а печень, пропускающая и задерживающая в себе все лишнее, таким образом становится мишенью для метастазов.
По статистике, первичная опухоль печени – гепатоцеллюлярный рак – встречается реже, чем метастазы в этом органе от других злокачественных новообразований. Общее количество больных с метастазами в печени в России составляет более 100 000 – в разы больше, чем пациентов с первичными опухолями печени и внутрипеченочных желчных протоков (их менее 15 000).
Но практически все злокачественные новообразования метастазируют именно в печень. Рак толстой кишки (колоректальный рак) делает это в 50% случаев. В 30% случаев здесь возникают метастатические поражения при меланоме и раке молочной железы.
Наш ведущий хирург-онколог в этой области, Антон Александрович Иванов, приводит один из самых интересных примеров в своей практике.
«Пациентка с метастазами рака молочной железы в печени. Обычно такие случаи не принято оперировать вообще. Но при обследовании мы выяснили, что печень – единственный орган, который поддался метастазированию. Это было редкой удачей, и хирурги приняли коллегиальное решение: оперировать.
К сожалению, и рак печени, и метастазы в ней часто бывают диагностированы в уже запущенном состоянии.
При этом УЗИ и даже КТ могут пропустить узел в печени, если он еще совсем маленький, и не в 100% случаев такие исследования дают понять точный размер, очертания и природу очага.
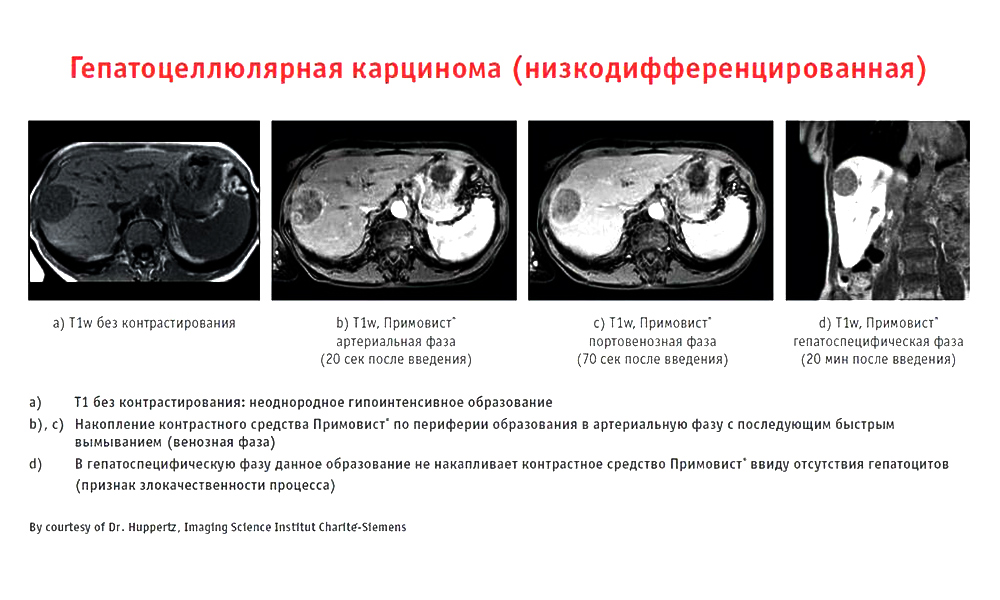
Пример работы контрастного препарата Примовист
Но, к сожалению, во многих регионах ситуация сложнее: найти там клиники, которые знают и используют Примовист, по-прежнему трудно, как 10 лет назад.
Эта зона включает печень (греч. hepar), поджелудочную железу (лат. pancreas), желчный пузырь (лат. vesica biliaris) и желчные протоки. Все эти органы тесно связаны анатомически и функционально.
Большинство вмешательств в других областях хирургии проходит на одной небольшой конкретной локализации, а если речь идет о резекции (удалении части) печени, то объем работы велик, даже при затрагивании одного-двух сегментов.
Сложно это, во-первых, чисто технически.
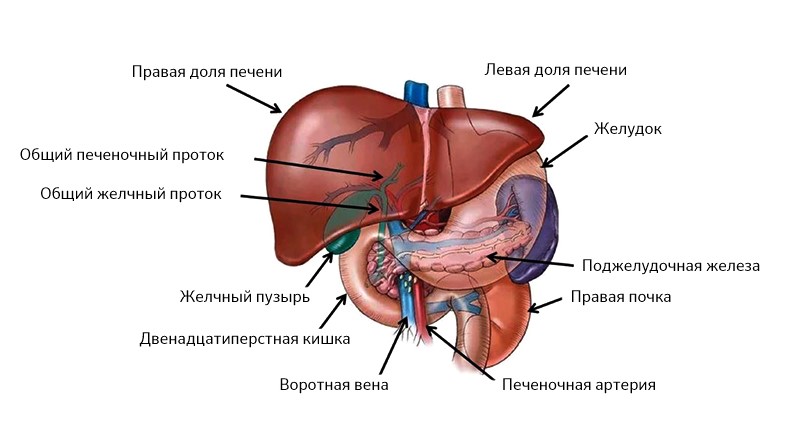
Печень находится по правую сторону, поджелудочная – по левую, все их протоки объединяются в один и выходят в двенадцатиперстную кишку
Печень весьма сложно устроена, она состоит из сегментов и долей, между которыми есть связки, все они буквально опутаны и пронизаны венами, артериями и желчными протоками.
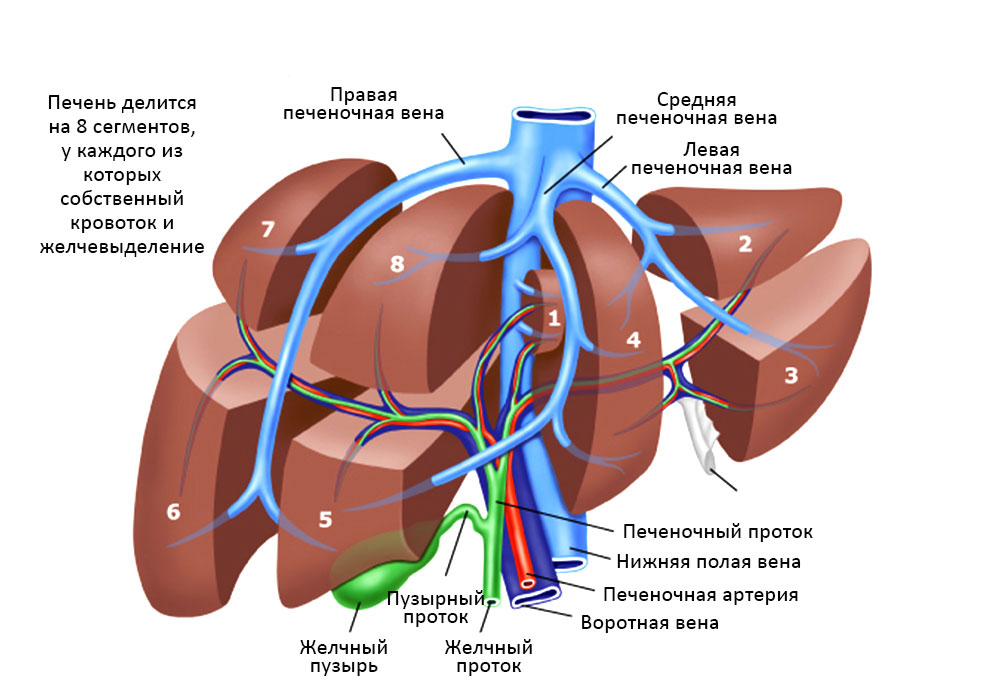
Взаимосвязи сегментов печени, желчных протоков и кровеносных сосудов
Есть риск в том, что в этой области расположен большой сосудистый пучок, все происходит очень близко к нижней полой вене, печеночной артерии: это большие магистральные сосуды. Сама по себе печень – сильно кровоточит. Соответственно, существует опасность серьезной кровопотери, операция должна быть одновременно максимально быстрой и исключительно аккуратной.
К операциям на печени и врач, и пациент тщательно готовятся, чтобы все прошло максимально предсказуемо. Антон Александрович Иванов подробно объяснил, как хирург-онколог и его бригада готовится к операции на печени, и что стараются предусмотреть всё.
«Для того, чтобы точно определить объем и способ вмешательства, проводят все необходимые исследования. Область операции визуализируется с максимальной точностью. Учитываются результаты множества анализов. Например, при определенных инфекционных заболеваниях или снижении количества тромбоцитов в крови врач сначала подберет терапию для восстановления нормальных показателей и только потом назначит операцию.
Непосредственно в момент проведения вмешательства в операционной кроме врача находится целая команда специалистов, контролирующих жизнедеятельность пациента: анестезиологи, реаниматологи, трансфузиологи, операционная сестра. Конечно, сегодня даже зуб врач не удаляет в одиночестве, но операции на печени собирают в операционной самую большую бригаду.
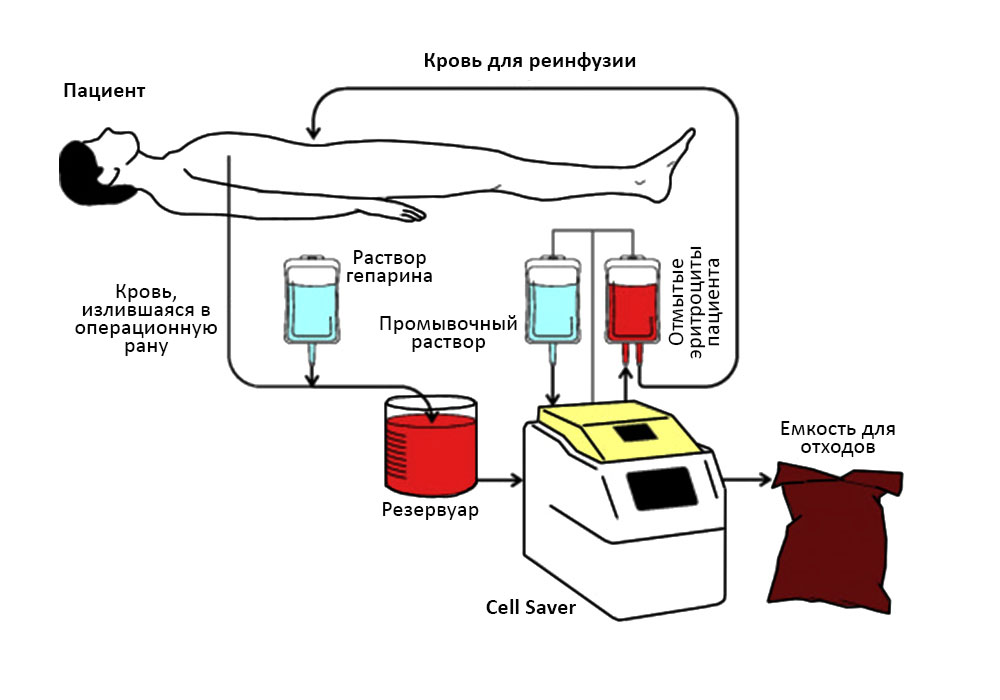
Кровь пациента поступает в аппарат Cell Saver, и он возвращает эритроциты пациенту
Довольно регулярно операции бывают симультанными (одномоментными): резекция печени проходит одновременно с другими вмешательствами. Удаляются и первичный очаг, например, в толстой кишке, и метастаз в печени.
Однако, даже при максимальной предсказуемости и полном контроле процесса, хирургам случается отходить от намеченного плана.
Например, в ходе операции по поводу первичной опухоли желудка может произойти случайная находка: небольшой одиночный метастаз в печени. В этом случае хирурги могут приглашать коллег, специалистов по операциям на печени, чтобы они провели свой этап: удаление часть печени.
Совместные операции хороши тем, что пациент подвергается наркозу и трудностям восстановительного периода только один раз.
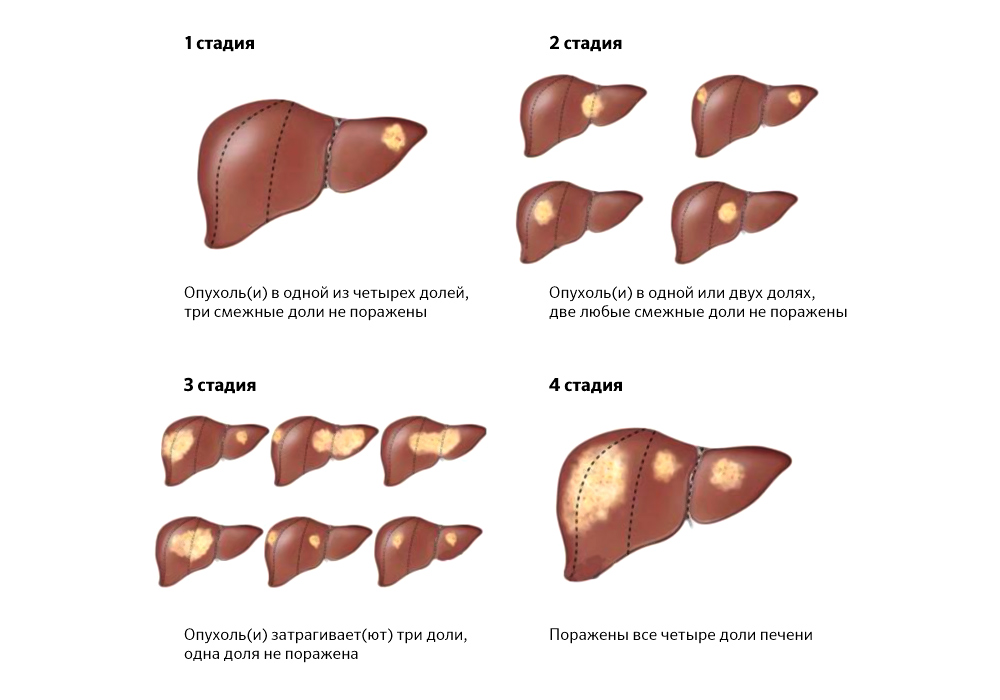
Распространенность опухолевых очагов иногда делает хирургическое лечение невозможным
Противопоказания. Это такие состояния здоровья пациента, которые делают успех предполагаемой операции статистически минимальным.
2. Некупируемый асцит – скопление большого количества жидкости в брюшной полости. Кроме того, что это создает сложности при операции, асцит действует как фактор, провоцирующий распространение метастазов. Если его не удается контролировать, то высока вероятность, что метастазы быстро рецидивируют.
3. Механическая желтуха. Опухолевый очаг, сдавливающий желчные протоки, нарушает отток желчи и провоцирует поступление билирубина (продукт распада гемоглобина) в кровь. Накапливаясь, он окрашивает склеры (белки глаз), кожу и слизистые пациента в желтый цвет. Это опасно: билирубин токсичен и утяжеляет состояние больного.
Однако, даже для таких пациентов, кому недоступны хирургические вмешательства, существуют методы лечения.
Химиоэмболизация сосудов, питающих опухоль – основной способ эндоваскулярного лечения рака печени. Тонкий катетер, вводимый через бедренную артерию, продвигается непосредственно в сосуд, кровоснабжающий ткань опухоли, и подает в него препарат, содержащий микрокапсулы из специального медицинского пластика. Они механически перекрывают кровоток, лишая опухолевые клетки питания, и выделяют лекарство против роста опухоли, причем прямо в очаг поражения и в высокой концентрации.
Этот метод способен сократить объем опухоли в печени, а, значит, в ряде случаев – сделать возможным один из вариантов хирургической резекции.
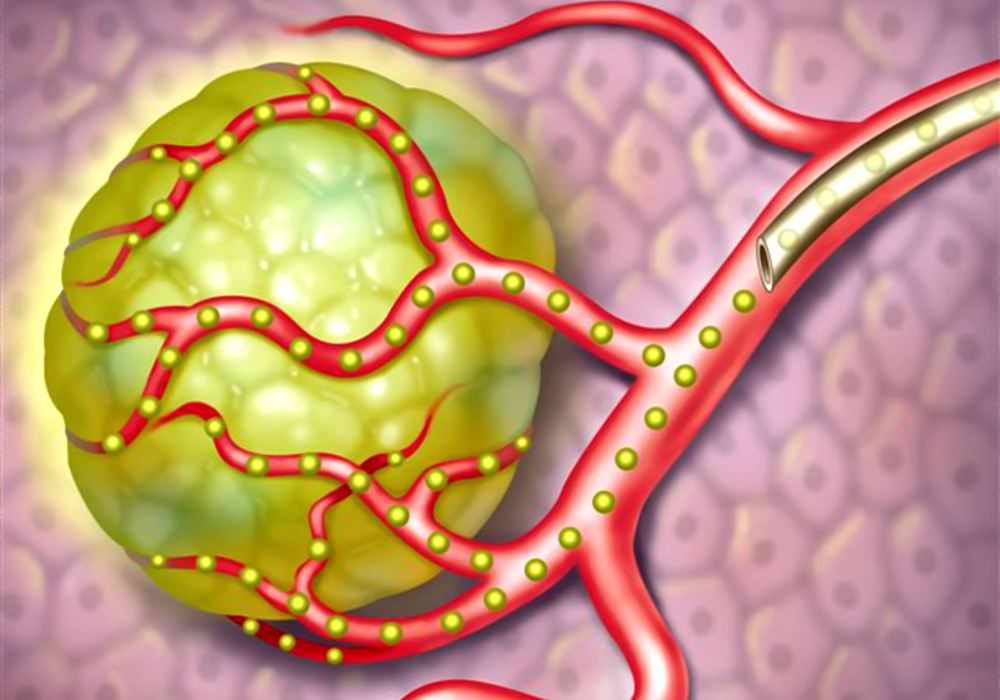
Схема введения эмбол (микрокапсул) через катетер прямо к опухоли
Стентирование. Установка стента (расширителя) в сдавленный опухолью желчный проток или сосуд помогает побороть, например, механическую желтуху, наладить кровоток и отток желчи – т.е. убрать одно из основных противопоказаний для хирургического вмешательства.
Это самые популярные у нас в клинике методы. В других случаях мы применяем и криодеструкцию (разрушение опухоли низкими температурами), и гипертермическую химиотерапию HIPEC (против канцероматоза брюшины), и иные подходящие методы.
Есть врачи, кто честно признает, что таких операций не делает, и направляет больного в крупные центры, в столицы. С одной стороны, это безопаснее, чем хирург-недоучка, с другой – попасть на бесплатное лечение такому пациенту крайне сложно. Даже в системе ОМС операция на печени не входит в стандарт оказания медпомощи. Это высокотехнологичное хирургическое вмешательство, выполняемое по квотам.
В любом случае, пациент должен помнить, каким бы пугающим не был вердикт, необходимо получить второе мнение: это справедливо не только в терапии, клинической онкологии, но и в хирургии.
Цена. Для тех, кому не повезло добиться квоты на бесплатную операцию, хирургическое лечение опухолей печени стоит серьезных денег. В рамках нашего частного стационара, например, сама резекция, плюс нахождение в клинике, пред- и постоперационные исследования, реанимация – стоят порядка 700 000 р.
За рубежом, при том, что используются те же технологии и присутствуют те же риски, операция на печени при метастатическом поражении стоит в 6 раз дороже: от 60 000 евро.
Трудности с трансплантацией. Для каждого из пациентов с нерезектабельными опухолями и наличием противопоказаний к иным вмешательствам, в идеале, всегда должен оставаться последний шанс: пересадка печени. Но в России трансплантология пока отстает от мирового опыта.
Во многом – из-за проблем административного характера. Не до конца отрегулировано законодательство и выдача лицензий на осуществление пересадок донорских органов; большой лист ожидания, причем списки нуждающихся в пересадке не объединяются по регионам. В ЕС, например, система контроля донорских органов централизована: подходящая печень, появившаяся в одной из стран, может быть оперативно привезена в другую страну, где она экстренно необходима.
К тому же проблема – в общественном сознании. В Западной Европе или США согласие, скажем, племянницы отдать часть печени для пересадки дяде – достаточно обыденный сюжет. У нас – родственники отказываются становиться донорами. Не все люди знают, насколько успешно восстанавливается печень, от которой отняли часть, но и не все хирурги готовы рискнуть двумя жизнями, а не одной.
А пока светлые умы исследователей придумывают, как решить проблему нехватки донорского материала, золотые руки наших хирургов обретают новый опыт.
Методика ALPPS (англ. Associated Liver Partition and Portal vein ligation for Staged hepatectomy), описанная и опробованная немецкими хирургами в 2012 году, расширяет возможности для хирургического лечения опухолей печени, ранее считавшихся нерезектабельными.
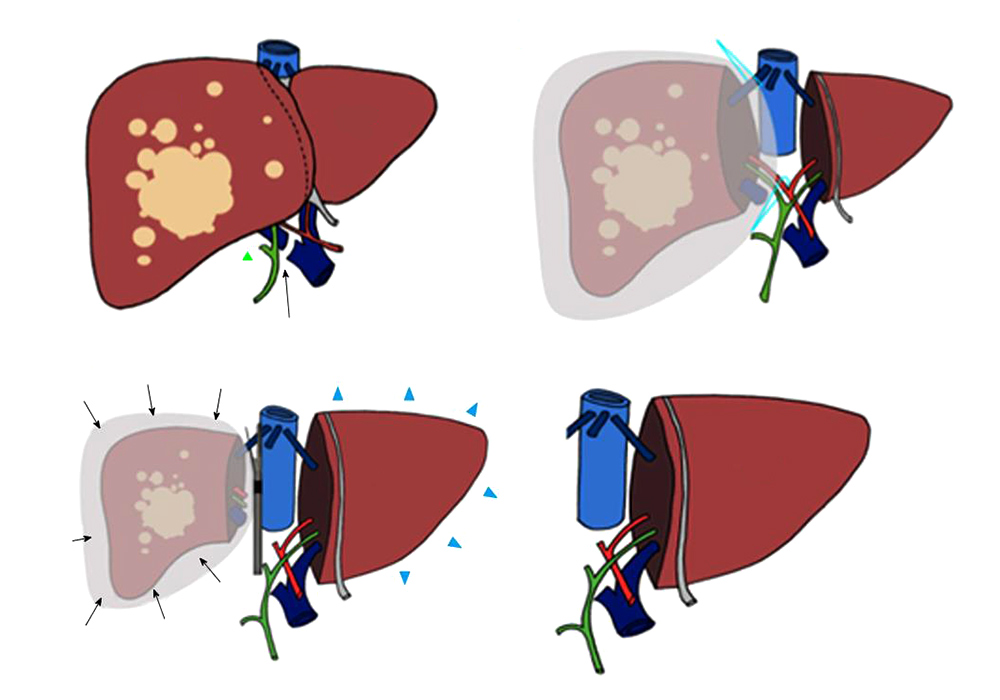
За неделю левая доля печени вырастает до размеров, позволяющих нормально работать
В России ALPPS пока применяется не повсеместно, но тот опыт, который уже есть у наших отечественных коллег, показывает столь же успешные результаты, как и у зарубежных хирургов.
Развитие эндоскопической хирургии. Техническое оснащение все же развивается быстро. Сейчас мы можем, используя тонкие гибкие микроинструменты, введенные в два прокола кожи, вылечить человека, удалить целый орган и т.д. Хирурги могут проводить очень сложные манипуляции, которые не были возможны 20-30 лет назад. Качество картинки с микроскопических камер при таких операциях улучшается каждый год.
Главное – нужно достаточно мотивации и желания у врачей, чтобы учиться, осваивать эти технологии. И конечно, необходимы серьезные деньги на покупку сложного оборудования и обучение врачей. Оба этих фактора редко могут объединиться в лечебном учреждении, даже если это передовой научный институт. А среди частных клиник, мы – единственные, кто производит центральную резекцию печени
Около 5% гепатоцеллюлярного рака связаны с афлатоксином – крайне ядовитым веществом, которое вырабатывают грибки, паразитирующие на арахисе, кунжуте, подсолнечных семечках, кукурузе, рисе и других культурах. Жители цивилизованных стран сталкиваются с ним нечасто, но он, тем не менее, весьма опасен, если съесть зараженные таким грибком продукты: яд необратимо повреждает клетки печени.
Однако, самым существенным фактором риска, по статистике, более опасным, чем алкоголь, сегодня является заражение вирусными гепатитами. Полвека назад это было проблемой в Азии и Африке, а сегодня заболеваемость гепатитами B и C в Европе и, в том числе, в России, приводит к росту появления первичного рака печени. Причем случается, что гепатит не проявляет симптомов, и люди могут долгое время не знать, что являются носителями вируса.
Поэтому не нужно пренебрегать прививками от гепатита B и ежегодно проверяться на наличие гепатита C – от него прививок пока не изобрели.
Регулярно проверяться – принципиальная основа основ успешной профилактики, или, как минимум, ранней диагностики (а значит, эффективного лечения).
И аккуратнее выбирайте орехи. На всякий случай.
Печень - наиболее типичное место для метастатической диссеминации опухолей ЖКТ. Активное выявление и лечение оправдано у сохранных больных, поскольку улучшает отдаленную выживаемость. Системная химиотерапия показана, если переносима. Преимуществ применения внутриартериальной инфузии химиопрепаратов не отмечено.
Резекция печени потенциально позволяет добиться длительной выживаемости у 30-50% отобранных больных, по сравнению с 1% 5-летней выживаемости без лечения.
Сроки резекции печени:
• Одноэтапный подход: симультанная резекция (с первичной опухолью), если обе операции относительно простые.
• Двухэтапный подход: резекция печени после химиотерапии длительностью 8-12 недель. Преимущества: оценка чувствительности опухоли к химиотерапии, уменьшение размеров опухоли и лучшая резектабельность, исключение пациентов с быстропрогрессирующим заболеванием.
• Двухэтапный подход в обратном порядке (сомнительная целесообразность и преимущества): вначале резекция печени, затем после химиотерапии - резекция первичной опухоли.
а) Эпидемиология. Возникают у 40-50% больных колоректальным раком (КРР): 20% больных КРР => синхронные метастазы на момент постановки диагноза; 20-30% => метахронные метастазы после резекции первичной опухоли.
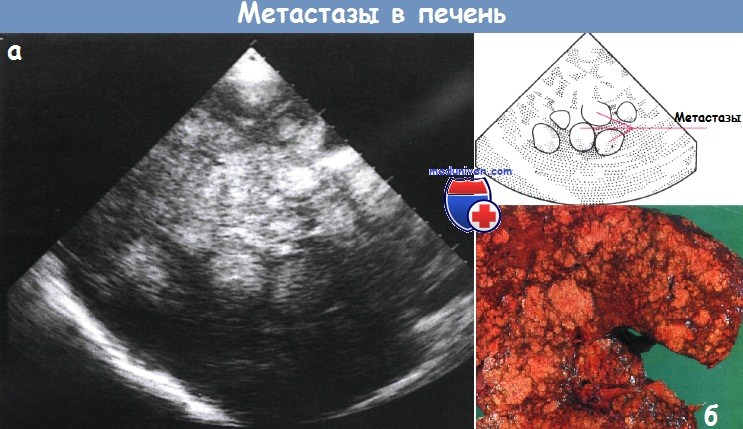
а - Множественные метастазы в печени. Ультрасонограмма.
б - Макроскопическая картина печени с множественными метастазами.
б) Симптомы метастаза рака кишки в печень:
• Обычно бессимптомное течение: выявление во время операции по поводу первичной опухоли или при обследовании на основании данных методов лучевой визуализации, РЭА/печеночных проб, взятых до операции или во время наблюдения после проведенного лечения.
• Осложнения: печеночная недостаточность (в частности, после операции), если > 50% объема печени замещено метастазами; редко - разрыв метастаза => внутрибрюшное кровотечение => геморрагический шок, перитонит, диссеминация рака.
в) Дифференциальный диагноз:
• Неопухолевые поражения печени: кисты, гемангиомы, эхинококк, аденома печени, очаговая узловая гиперплазия.
• Гепатоцеллюлярный рак.
• Метастазы другой первичной опухоли.
г) Патоморфология. Такая же, как и у первичной опухоли.
д) Обследование при метастазе рака кишки в печень
Необходимый минимальный стандарт:
• Анамнез заболевания, общее состояние больного, сопутствующие заболевания, операбельность.
• Клиническое обследование: пальпируемая опухоль, желтуха, вздутие живота, оценка функции сердца и легких.
• Анализы крови: анемия, функция печени (альбумин, АЧТВ, ПТИ).
• Онкомаркер: РЭА.
• Методы лучевой визуализации для оценки печени и выявления внепеченочных метастазов:
- КТ органов грудной клетки/брюшной полости/малого таза: гиподенсные очаговые образования, чувствительность - 70-80%.
- МРТ (с контрастированием): чувствительность - 65-90%.
- ПЭТ-КТ: наиболее точный метод для отбора пациентов, чувствительность > 90%, если исследование выполнено до проведения химиотерапии.
Дополнительные исследования (необязательные):
• Биопсия метастаза - подтверждение.
• Биопсия ткани печени - выявление цирроза.
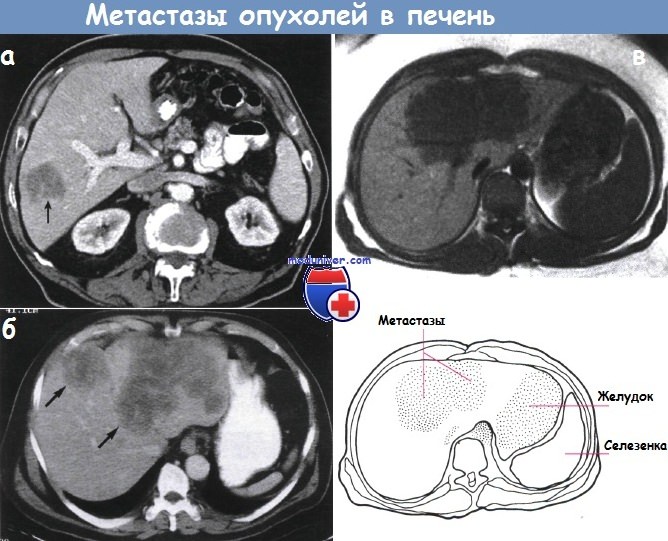
а - На компьютерной томограмме в правой доле печени виден единичныей четкоочерченный (стрелка) метастаз.
б - Компьютерная томограмма метастазы рака толстой кишки в печень.
Большую часть левой доли печени замещает большая дольчатая неоднородная масса низкой плотности (стрелки).
в - МРТ большого образования в печени. Это яркое изображение получено после отдельной двухсекундной экспозиции. 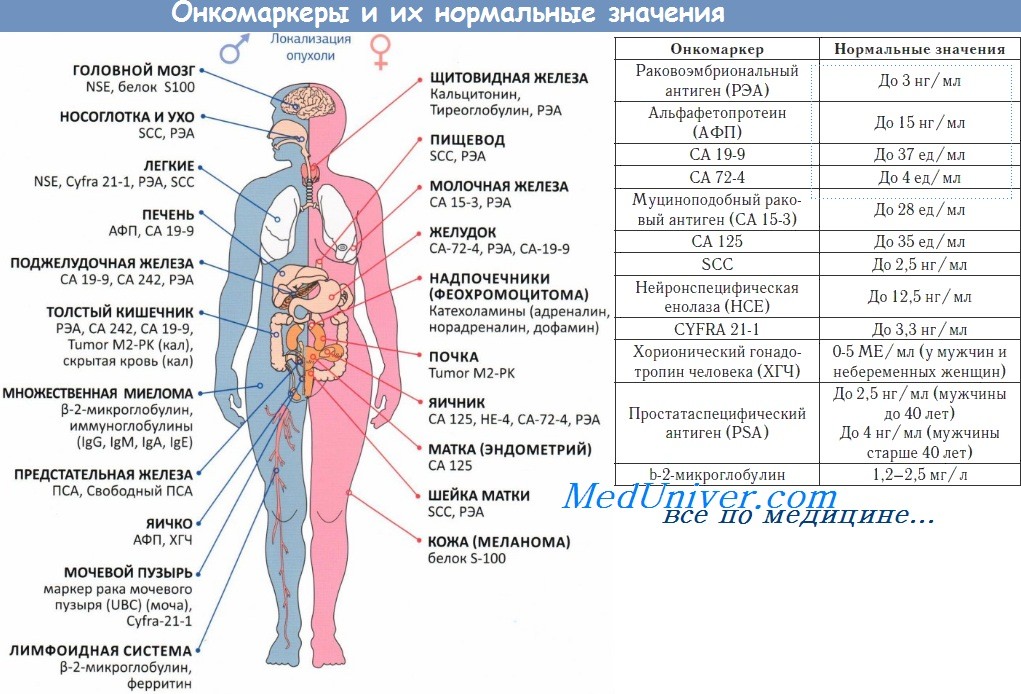
е) Классификация:
• Резектабельные метастазы в печени.
• Потенциально резектабельные метастазы.
• Нерезектабельные метастазы (в связи с количеством, распределением, близостью к жизненно важным структурам).
ж) Лечение без операции метастаза рака в печень:
- Неоперабельные больные с сопутствующими заболеваниями и плохим общим состоянием.
- Внепеченочные проявления опухоли (инкурабельная распространенность).
- Метастазы в печени:
• Нерезектабельные
• Потенциально резектабельные.
— паллиативная химиотерапия; оценка резектабельности при ответе на лечение.
— радиочастотная аблация или криодеструкция.
— преимущества внутриартериальной химиотерапии, инъекций этанола, облучения и пересадки отсутствуют.
з) Операция при метастазе рака в печень
Показания:
• Резектабельные метастазы (за исключением абсолютных противопоказаний, таких как сопутствующие заболевания, внепеченочная диссеминация).
• Резектабельность: возможность выполнить R0 резекцию, сохранить два соседних сегмента печени, сосудистый приток/отток и желчные пути, остающаяся часть печени с нормальной структурой > 20% от всего объема печени.
Хирургический подход:
1. Интраоперационный подход при метастазах, выявленных до операции:
• Следует рассмотреть вопрос о выполнении диагностической лапароскопии с лапароскопической интраоперационной ультрасонографией (в частности, в отсутствие высококачественных методов предоперационного обследования), поскольку ненужная лапаротомия может быть исключена у 25% больных.
• Интраоперационный УЗ => изменение или уточнение плана операции.
• R0 резекция с целью достижения безопасных краев резекции (1 см), минимальная граница > 1 мм небезупречна.
- Анатомическая резекция: гемигепатэктомия, трисегментэктомия.
- Неанатомическая резекция: метастазэктомия, сегментэктомия.
- Комбинация: например, гемигепатэктомия + радиочастотная аблация контралатерального очага.
2. Интраоперационный подход при метастазах, невыделенных до операции:
• Резекция, если возможна.
• По крайней мере, трепанобиопсия для подтверждения.
• Лигирование ветвей портальной вены (не является общей рекомендацией).
и) Результаты лечения метастаза рака в печень:
• Пятилетняя выживаемость после резекции метастазов в печени: 30-50% (строгий отбор пациентов). Летальность после плановых операций снизилась с 20% до 1%.
• Осложнения: кровотечение, раневая инфекция (5%), желчеистечение, билома, печеночная недостаточность.
к) Наблюдение и дальнейшее лечение при метастазе рака в печень
1. Продолжение адъювантной/паллиативной химиотерапии показано:
• Всем больным после метастаззктомии.
• Пациентам, неподходящим для резекции, до тех пор, пока польза превышает тяжесть побочных эффектов.
2. Онкологическое наблюдение:
• Колоноскопия в зависимости от общего прогноза и состояния толстой кишки.
• Клиническое обследование , по крайней мере, каждые 3 месяца.
• КТ органов грудной клетки/брюшной полости/малого таза, ПЭТ в зависимости от клинического течения и протокола лечения.
3. Повторные хирургические вмешательства:
• Ререзекция рецидивных метастазов у тщательно отобранных пациентов.
• Резекция метастазов в легких у отобранных пациентов.
Читайте также:
- Можно ли спутать эндометриоидную кисту с фолликулом
- Можно ли при онкологии есть тыкву
- Ретикулез что это такое
- Инфантильная гемангиома что это такое
- Как принимать кедровую настойку при онкологии

