Рак щитовидной железы слепцов
Дистанционная оценка медицинской документации
Дистанционный мониторинг состояния здоровья (для пациентов, получивших первичную очную консультацию)
Срочная дистанционная оценка медицинской документации
С 2015 года Слепцов Илья Валерьевич - единственный российский хирург-эндокринолог, успешно сдавший квалификационные экзамены и прошедший сертификацию в Департаменте эндокринной хирургии Европейского совета по хирургии.
Личный опыт проведения операций на щитовидной железе, паращитовидных (околощитовидных) железах: более 6000 операций, 600-700 операций ежегодно. Владеет полным спектром операций на шее, включая традиционные и видеоассистированные вмешательства, эндоскопические операции из подмышечного доступа, расширенные операции при распространенном раке. Проводит операции на щитовидной железе, околощитовидных железах детям любого возраста с использованием современных малотравматичных технологий.
Слепцов И.В. проводит обширную работу по консервативному лечению пациентов с эндокринными заболеваниями - аутоиммунным тиреоидитом, диффузным токсическим зобом (болезнью Грейвса), подострым тиреоидитом, послеродовым тиреоидитом, нарушениями фосфорно-кальциевого обмена (первичный, вторичный гиперпаратиреоз, постменопаузальный остеопороз) и др. В процессе консультаций определяется схема консервативной терапии, объем необходимого обследования, даются рекомендации по питанию и режиму жизни пациентов. Ежемесячно проводятся очные консультации более 400 пациентов.
Врачебная деятельность:
Образование:
Участие в конференциях и конгрессах:
Выездные лекции:
- 2018 г. - Архангельск
- 2018 г. - Вологда
- 2018 г. - Ижевск
- 2018 г. - Калининград
- 2018 г. - Кемерово
- 2018 г. - Мурманск
- 2018 г. - Орёл
- 2018 г. - Оренбург
- 2018 г. - Ростов-на-Дону
- 2018 г. - Рязань
- 2018 г. - Самара
- 2018 г. - Саранск
- 2018 г. - Ставрополь
- 2018 г. - Нальчик
- 2018 г. - Тюмень
- 2018 г. - Уфа
- 2018 г. - Челябинск
- 2018 г. - Ереван
- 2017 г. - Ереван
- 2017 г. - Архангельск
- 2017 г. - Нижний Новгород
- 2017 г. - Челябинск
- 2017 г. - Череповец
- 2017 г. - Казань
- 2017 г. - Тюмень
- 2016 г. - Вологда
- 2016 г. - Новосибирск
- 2016 г. - Кемерово
- 2016 г. - Красноярск
- 2016 г. - Архангельск
- 2016 г. - Чебоксары
- 2016 г. - Новгород
- 2016 г. - Псков
- 2015 г. - Тюмень
- 2015 г. - Самара
Область научных и практических интересов: хирургия органов эндокринной системы (щитовидная железа, околощитовидные железы, надпочечники, нейроэндокринные опухоли), от расширенных операций при злокачественных опухолях до малоинвазивных вмешательств при доброкачественных новообразованиях. Методы консервативного лечения патологии щитовидной железы. Радионуклидные методы диагностики и лечения.
Патенты и публикации: 12 патентов, 120 печатных работ
СОСТАВ СОГЛАСИТЕЛЬНОЙ КОМИССИИ
1. ГУ РОНЦ им. Н.Н. Блохина РАМН: В.Ж. Бржезовский, Т.И. Зайцева, Т.Т. Кондратьева, М.А. Кропотов, Е.Г. Матякин, А.И. Павловская, А.И. Пачес, В.Г. Поляков, С. Субраманиан, Р.В. Шишков, В.Н. Шолохов
2. ФГУ ЭНЦ Росмедтехнологий: А.Ю. Абросимов, Д.Г. Бельцевич, В.Э. Ванушко, И.И. Дедов, Н.С. Кузнецов, Н.В. Мазурина, Г.А. Мельниченко, Н.М. Платонова, В.Н. Сморщок, Е.А. Трошина, В.В. Фадеев
3. ФГУ МНИОИ им. П.А. Герцена Росмедтехнологий: В.О. Ольшанский, И.В. Решетов
4. ГУ МРНЦ РАМН: П.И. Гарбузов, Б.Я. Дрозодвский, А.А. Ильин, В.С. Паршин, А.А. Родичев, П.О. Румянцев, А.Ф. Цыб
5. НИИ онкологии СО: Е.Ц. Чойнозов
6. ФГУ НИИ онкологии им. Н.Н. Петрова Росмедтехнологий (СПб): А.С. Барчук, Л.М.Берштейн, Р.И. Вагнер, Е.В. Левченко, А.Е. Михнин
7. Ростовский НИИ онкологии Минздравсоцразвития РФ: П.В. Светицкий
8. ОКД N 1 г. Москвы: Л.Г. Кожанов, М.А. Сдвижков, М.Р. Финкельштерн
9. Алтайский филиал ГУ РОНЦ им. Н.Н. Блохина РАМН: И.В. Вихлянов
10. ФХК ММА им. И.М. Сеченова: Л.И. Ипполитов, С.С. Харнас, К.Е. Чилингариди
11. ФГУ НМЦХ им. Н.И. Пирогова Росмедтехнологий: П.С. Ветшев, В.А. Животов, А.А. Знаменский
12. СПб КОД: С.В. Рачинский
13. РМАПО: В.О. Бондаренко, Т.И. Дэпюи
14. СПб ГПМА: А.Ф. Романчишен
15. СПб ГМУ им. И.П. Павлова: Е.Н. Гринева
16. СПб Северо-западный медицинский центр МАПО: А.Н. Бубнов, И.В. Слепцов
17. Ленинградский ООД: А.В. Карпенко
18. ГОУ ВПО Челябинская ГМА Росздрава: В.А. Привалов, С.В. Яйцев
19. Самарский ООД: В.И. Письменный
20. Свердловский ООД: Г.А. Гинзбург
21. Ярославский онкологический центр: А.Л. Ключихин
22. Новокузнецкий ГОД: И.Ю. Пеганов
23. ГОУ ВПО Смоленская ГМА Росздрава: А.Н. Барсуков
1. Введение
1.1. Цель и статус рекомендаций
Представленные рекомендации являются документом, объединяющим мнение членов согласительной комиссии по ключевым и наиболее спорным проблемам диагностики и лечения дифференцированного рака щитовидной железы, которые сложились в отечественной клинической практике. Эти рекомендации не являются официальным документом, утвержденным теми или иными структурами системы здравоохранения, и носят рекомендательный характер. Согласительная комиссия является инициативной группой специалистов, работающих в разных лечебных и научно-исследовательских учреждениях, а сами рекомендации – документом, созданным в ходе многочисленных дискуссий, проходивших на заседаниях и в процессе подготовки итогового текста по электронной почте. Основными предпосылками к созданию этого согласительного документа явились:
- отсутствие единых подходов к диагностике и лечению больных дифференцированным РЩЖ,
- необходимость адаптации ряда международных клинических рекомендаций, вышедших в последние годы, положения которых существенно отличаются от реальной клинической практики, сложившейся в РФ,
- необходимость мультидисциплинарного подхода к диагностике и лечению пациентов с дифференцированным РЩЖ, что отражено составом согласительной комиссии (онкологи, хирурги, радиологи, эндокринологи, патоморфологи).
Мнение отдельных членов комиссии может несколько отличаться от приведенных положений, поскольку в случае значительных расхождений, текст рекомендаций будет отражать мнение доминирующего большинства. В случае разделения мнений, будет указана доля экспертов, поддерживающих то или иное положение рекомендаций.
1.2. Ограничения рекомендаций
Представленные рекомендации не претендуют на систематическое изложение всех аспектов диагностики и лечения дифференцированного РЩЖ, не призваны заменить руководства и учебные пособия по этому вопросу, и носят рекомендательный характер. Они отражают согласительное мнение лишь по наиболее спорным вопросам. В реальной клинической практике могут возникать ситуации, выходящие за рамки представленных рекомендаций, в связи, с чем окончательное решение в отношении конкретного пациента и ответственность за его лечение возлагается на лечащего врача.
2. Диагностика
2.1. Первичная диагностика
Диагностика РЩЖ подразумевает комплекс методов физикального и инструментального обследования. Подавляющее большинство наблюдений РЩЖ выявляется при обследовании пациентов по поводу узлового эутиреоидного зоба. Несмотря на высокую разрешающую способность, УЗИ не следует использовать в качестве скрининга для выявления РЩЖ, за исключением отдельных групп больных (см. ниже), в связи с низкой эффективностью как с клинических, так и с финансовых позиций, связанных с верификацией большого числа наблюдений узлового коллоидного зоба, который, как правило, не имеет патологического значения и не требует хирургического лечения.
2.2. УЗИ щитовидной железы
Показания к применению:
- Пациенты с пальпируемыми узлами и/или увеличением ЩЖ.
- Пациенты с семейным анамнезом РЩЖ.
- Пациенты с синдромами множественных эндокринных неоплазий 2-го типа (МЭН 2).
- Пациенты с облучением головы и шеи в анамнезе.
- Пациенты с увеличенными лимфоузлами шеи.
- Пациенты с неопределенными симптомами (дисфония, дисфагия, цервикальная боль, постоянный кашель) при отсутствии доказанных заболеваний верхних отделов дыхательного и пищеварительного тракта.
2.3. Тонкоигольная аспирационная биопсия
Тонкоигольная аспирационная биопсия (ТАБ) ЩЖ с последующим цитологическим изучением материала является основным методом морфологической диагностики при узловом зобе. Показаниями для ТАБ являются:
- Пальпируемые узловые образования ЩЖ размером 1 см и более.
- Узловые образования ЩЖ размером 1 см и более, случайно выявленные при УЗИ.
- Образования ЩЖ менее 1 см, пальпируемые или выявленные случайно при УЗИ, при наличии характерных для РЩЖ ультразвуковых признаков.
- Все образования ЩЖ при наличии анамнестических, клинических или лабораторных данных о высокой вероятности наличия РЩЖ.
2.4. Сцинтиграфия щитовидной железы с изотопами йода
Сцинтиграфия ЩЖ и всего тела с изотопами йода (131, 123) является методом топической и радиологической диагностики метастазов дифференцированного РЩЖ и остаточной ткани ЩЖ после проведенной тиреоидэктомии.
2.5. Другие методы
В рамках обследования пациента с узловым зобом и РЩЖ обязательным является оценка функции ЩЖ (определение уровня ТТГ). Другие методы (рентгенография, КТ, МРТ, ПЭТ) могут использоваться для уточнения степени местного распространения опухоли и топической диагностики метастазов по индивидуальным показаниям.
3. Лечение
Лечение и наблюдение пациентов с дифференцированным РЩЖ должно проводиться в специализированных медицинских учреждениях, обладающих полноценным арсеналом средств диагностики и высококвалифицированного лечения дифференцированного РЩЖ (онкологические стационары и отделения, отделения хирургии эндокринных органов).
3.1. Хирургическое лечение
3.1.1. Объем хирургического вмешательства
Стандартной операцией при дифференцированном РЩЖ является экстрафасциальная тиреоидэктомия. Экстрафасциальная тиреоидэктомия снижает риск летальности и персистенции заболевания и сопряжена с минимальным риском осложнений в руках опытного хирурга.
Ситуация, когда может быть выполнена экстрафасциальная гемитиреоидэктомия – солитарная опухоль до 2 см (Т1), при отсутствии достоверных до- и интраоперационных данных о поражении регионарных лимфатических узлов и отдаленных метастазов.
Помимо операционных рисков и возможных осложнениях, пациент, которому предлагается экстрафасциальная гемитиреоидэктомия, должен быть предупрежден о том, что оставшаяся доля ЩЖ будет служить препятствием для возможного проведения послеоперационной терапии радиоактивным йодом и последующего наблюдения с использованием самого высокочувствительного маркера персистенции заболевания – тиреоглобулина (ТГ).
3.1.2. Хирургическое вмешательство на лимфоузлах шеи
Удаление лимфатических узлов центральной зоны (VI уровень) должно быть выполнено во всех наблюдениях, где есть дооперационное подозрение о наличии метастазов этой зоны или метастазы подтверждены интраоперационно. Преимущества профилактического удаления этих лимфоузлов спорны; пока нет убедительных доказательств, что эта процедура достоверно снижает летальность и вероятность персистенции РЩЖ. Тем не менее, удаление лимфоузлов центральной зоны позволяет четко определить стадию распространения процесса, исключает необходимость хирургических манипуляций при повторных операциях в связи с метастатическим поражением этих лимфоузлов, что влечет за собой более высокую частоту операционных осложнений.
Учитывая высокую частоту метастатического поражения неизмененных по данным дооперационного обследования лимфоузлов центральной зоны (25 – 30%), подавляющее большинство экспертов согласительной комиссии рекомендуют их превентивное удаление, дополняющее вмешательство на ЩЖ.
Вмешательство на лимфатическом коллекторе II – V уровня шеи показано при доказанном их метастатическом поражении.
3.2. Послеоперационное определение стадии процесса
Послеоперационное определение стадии процесса необходимо для оценки индивидуального прогноза и выбора протокола дальнейшего ведения пациента.
- Группа низкого риска – солитарная опухоль Т1 (менее 2 см) N0M0 без признаков экстратиреоидного распространения.
- Группа среднего риска – Т2N0M0 или первично-множественный T1N0M0.
- Группа высокого риска – любой Т3 и Т4 или любой Т, N1 или М1, пациенты с персистенцией РЩЖ, пациенты после паллиативных операций.
3.3. Терапия радиоактивным йодом
Удаление остаточной тиреоидной ткани при помощи изотопа йода-131 в дальнейшем облегчает раннее выявление прогрессирования заболевания при помощи сывороточного ТГ и сцинтиграфии всего тела.
Терапия изотопом йода-131 позволяет уничтожить микроскопические остатки опухоли, оказывая положительное влияние на прогноз.
Применение высоких активностей изотопом йода-131 позволяет на 2 – 5 сутки после процедуры выполнять сцинтиграфию всего тела и выявлять ранее недиагностированные метастазы.
Показания для проведения терапии складываются из послеоперационного определения стадии процесса:
Группа низкого риска. послеоперационная терапия изотопом йода-131 не показана. Не установлено преимуществ в отношении частоты рецидива и летальности.
Группа среднего риска. Показания определяются индивидуально. Нет однозначного мнения, должна ли терапия изотопом йода-131 применяться у всех пациентов или только у тех, где есть сомнения в полном хирургическом удалении ЩЖ. Нет однозначного мнения об оптимальных лечебных активностях изотопом йода-131 и преимущественном методе стимуляции захвата (эндогенном или с помощью рекомбинантного ТТГ).
Группа высокого риска. Послеоперационная терапия изотопом йода-131 показана всем больным, так как достоверно уменьшает вероятность прогрессирования опухоли и увеличивает выживаемость.
3.4. Супрессивная терапия препаратами тиреоидных гормонов
Супрессивная терапия препаратами тиреоидных гормонов направлена на коррекцию послеоперационного гипотиреоза и подавление ТТГ-зависимого роста резидуальных опухолевых клеток. Препаратом выбора является левотироксин (L-T4); применение лиотиронина (L-T3) ограничено отдельными случаями и короткими курсами подготовки больного к сцинтиграфии с изотопом йода -131. Для большинства пациентов показано достижение супрессии уровня ТТГ (целевое значение ТТГ
- 2587
- 1,8
- 1
- 3
![]()
Аполлинария Боголюбова![]()
Андрей Панов



Спонсором приза зрительских симпатий выступила компания BioVitrum.
Несомненно, XXI век — время развития научно-технического прогресса. Вместе с совершенствованием технологий приходит и их доступность в повсеместном использовании. Медицина не является исключением. Благодаря развитию технологий диагностики и лечения самых разных заболеваний мы стали спасать тех пациентов, которые когда-то входили в число неизлечимых. Однако не на все сферы медицины прогресс повлиял так положительно. Поэтому сегодня мы бы хотели познакомить вас с такими животрепещущими вопросами медицины, как гипердиагностика и гиперлечение. Сейчас мы остановимся лишь на одной, но весьма значимой стороне данной проблемы — гипердиагностика узлов щитовидной железы, а также гиперлечение этих узлов и рака щитовидной железы.
Что мы знаем сегодня про узлы щитовидной железы?
Однако то, что эта проблема была озвучена совсем недавно, не значит, что о ней больше не надо писать. Мы не хотим загружать вас медицинской терминологией, вновь писать о TI-RADS и разбирать по кусочкам, что может написать функциональный диагност в заключении. Мы обращаемся к вам в качестве потенциальных пациентов и хотим донести мысль, что не всегда узел в щитовидной железе опасен, а рак априори смертелен.
База, с которой нам нужно познакомиться: щитовидная железа
Немножко о щитовидной железе (ЩЖ). Это орган эндокринной системы человека, который располагается на передней поверхности шеи в области гортани, прямо перед щитовидным хрящом. Состоит железа из левой и правой долей и перешейка. ЩЖ богато кровоснабжается разными артериями, а иннервируется гортанными нервами.
Главной функцией щитовидной железы (лат. glandula thyroidea) является синтез тиреоидных гормонов, необходимых нашему организму. Под тиреоидными гормонами мы подразумеваем два соединения: тироксин (Т4) и трийодтиронин (Т3). Основной функцией Т4 и Т3 является увеличение потребления клетками кислорода. Иначе говоря, эти гормоны стимулируют все энергетические процессы в клетке и обмен веществ, причем их влияние распространяется на все клетки организма.
Также клетки ЩЖ производят кальцитонин, ответственный за обмен кальция в организме.
Прямо за щитовидной железой располагаются четыре небольшие паращитовидные железы. Последние производят паратиреоидный гормон, который также отвечает за поддержание уровня кальция в организме, причем в большей степени, чем кальцитонин.
Откуда берется столько случаев рака щитовидки?
Рак щитовидной железы (РЩЖ) — наиболее распространенное злокачественное новообразование эндокринной системы [2]. Все чаще мы слышим, что заболеваемость РЩЖ неуклонно растет. И звучит это ужасающе, однако так ли всё просто на самом деле? Возможно, вы будете шокированы, какая правда скрывается за этими, на первый взгляд, однозначными научными фактами. И прежде, чем мы разберемся с истинной причиной роста заболеваемости РЩЖ, необходимо ознакомиться с тем, какие виды рака щитовидки существуют.
Итак, начнем. Сейчас нам понадобится привести немного численных данных, но не пугайтесь их, всё крайне просто. В научном сообществе выделяют пять типов РЩЖ:
- Папиллярный (80–85% случаев).
- Фолликулярный (10–15% случаев).
- Медуллярный (5% случаев).
- Низкодифференцированный (1% случаев).
- Недифференцированный (0,1–0,2% случаев).
Наиболее благоприятными принято считать два первых типа РЩЖ. И как мы можем заметить, они встречаются наиболее часто. Их также называют высокодифференцированными типами рака. Медуллярный, низкодифференцированный и недифференцированный типы считаются агрессивными формами РЩЖ. В нашей статье мы сделаем акцент лишь на первых двух типах РЩЖ, так как они являются наиболее распространенными.
Что касается рака — если клетки, из которых состоит опухоль, являются высокодифференцированными, в большинстве случаев врачи считают исход благоприятным. Однако если опухоль состоит из низкодифференцированных клеток, то с большой вероятностью она склонна к агрессивному течению. Как уже было сказано, наиболее часто выявляемые РЩЖ являются высокодифференцированными.
Папиллярный РЩЖ — наиболее распространенная форма: 80–85%. И с самым хорошим прогнозом. Пятилетняя выживаемость пациентов с РЩЖ — 98,1% [2]. Что это значит для пациента? Что наиболее часто выявляемые случаи РЩЖ имеют благоприятный исход!
Рак, ушедший в себя
Подбираемся к корню проблемы: статистика и диагностика
Вернемся к распространенности РЩЖ. Теперь мы готовы понять, что возросшее число случаев данной патологии не является поводом для беспокойства.
В 1975 году заболеваемость РЩЖ составляла 4,9 на 100 000 человек и оставалась относительно стабильной до начала 1990-х годов [6]. За последние 25 лет заболеваемость РЩЖ выросла более чем в 3 раза, то есть на 300% (рис. 1) [7], [8], причем в большинстве случаев за счет высокодифференцированного папиллярного РЩЖ. При этом очень важно понимать, что, несмотря на такой значительный рост, смертность от РЩЖ остается стабильной, примерно 0,5 случаев на 100 000 человек [6].
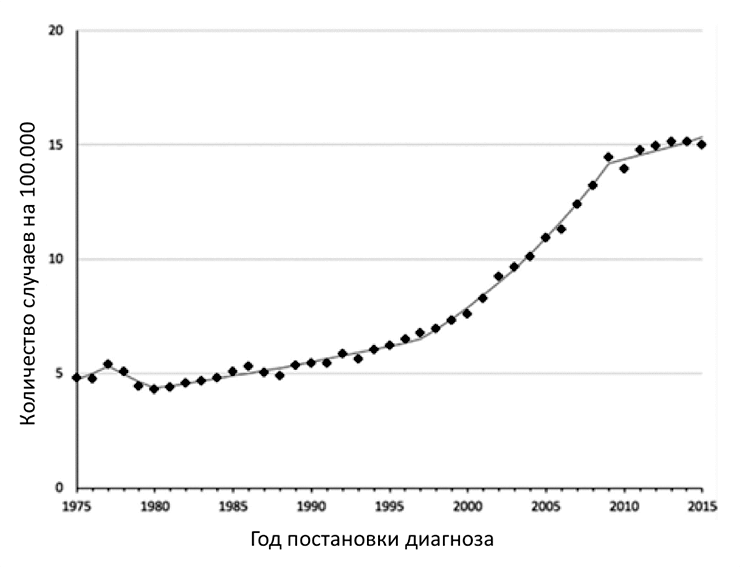
Рисунок 1. Данные заболеваемости раком щитовидной железы в период с 1975 по 2015 годы
Чувствуете, что тут что-то не так? Нет связи между возросшим числом случаев РЩЖ и смертностью от этой патологии! Среди врачей и ученых до сих пор продолжаются дебаты, почему так происходит. Сейчас выделяют несколько теорий. Наиболее вероятная — широкое распространение методов ультразвуковой диагностики (УЗИ). Пусть корни УЗИ уходят к Леонардо да Винчи и XV веку, широкое медицинское распространение данный метод получил с 50-х годов XX века [9], [10]. Сегодня УЗИ является наиболее простым, дешевым, неинвазивным и информативным методом выявления опухолевых образований щитовидной железы. Поэтому, как вы можете догадаться, УЗИ стали делать почти всем, причем независимо от показаний.
Сейчас научное сообщество активно дискутирует на тему, связаны ли такие показатели с истинным увеличением заболеваемости РЩЖ, или же проблема в гипердиагностике тех небольших образований ЩЖ, которые не требуют никакого вмешательства со стороны человека [11], [12].
Для более полного понимания проблемы вернемся на чуть более ранний этап диагностики РЩЖ.
Что такое узлы и как их найти?
Узлы ЩЖ — это радиологически различимые объемные образования в ЩЖ, которые могут быть доброкачественными и злокачественными. Узлы можно найти в 50% случаев всех проводимых УЗИ ЩЖ. При этом только 5% выявляемых образований будут злокачественными [13], [14].
Весомый вклад УЗИ в возросшее количество диагностированных узлов и РЩЖ можно показать на примере одного нашумевшего исследования в Южной Корее [3], [15], [16]. В 1999 году там была утверждена национальная программа, направленная на скрининг злокачественных заболеваний. Под программу попала и щитовидная железы. В результате повсеместного внедрения УЗИ щитовидки частота выявления рака выросла в 15 (!) раз с 1993 по 2011 год. И это мы еще не говорим просто об узлах, которые также могут быть психологической проблемой пациента. Большинство выявляемых случаев — папиллярный РЩЖ. Как вы помните, этот вид рака имеет весьма благоприятный исход. Однако простому населению идея жить с раком настолько чужда и неприятна, что было проведено огромное число полного удаления щитовидных желез, причем часто без видимой на то необходимости! А такая операция имеет серьезные последствия, о которых мы расскажем чуть ниже.
Врачи, осознав свою ошибку, убрали УЗИ щитовидки из списка обязательных скрининговых тестов. И результат не заставил себя ждать. В последней на эту тему публикации 2015 года сказано, что на 30% снизилась заболеваемость РЩЖ, а число операций на щитовидной железе снижалось на 35% ежегодно. Вывод напрашивается сам собой: в основе увеличения числа диагностированных случаев узлов щитовидки (в том числе и РЩЖ) является ставшее таким доступным УЗИ.
Думаем, следует также сказать, что образования ЩЖ выявляются не только при выполнении УЗИ, но и при использовании других методов лучевой диагностики (КТ, МРТ, ПЭТ), что стало возможным благодаря улучшению разрешающей способности оборудования. Следовательно, увеличилось чисто случайно выявляемых образований щитовидной железы (в том числе, рака) — инциденталóм (от англ. incidence — случайность) [17]. Инциденталомы клинически никак себя не проявляют и могут оставаться в организме бессимптомно всю жизнь. И многие из таких инциденталом обнаруживались лишь посмертно, случайно, и не являлись причиной кончины человека. Это позволяет говорить нам о существовании резервуара пациентов с узлами или раком щитовидной железы, который клинически является скрытым и никак себя не проявляет до его случайного обнаружения [18].
Приведенные данные обобщены на рисунке 2.

Рисунок 2. Что даст нам УЗИ щитовидки на самом деле?
рисунок авторов статьи
Напомним, что в нашей статье мы делаем акцент на наиболее распространенных типах РЩЖ (папиллярный, фолликулярный). Агрессивные формы РЩЖ (медуллярный, низкодифференцированный, недифференцированный и редко папиллярный) требуют дальнейшего более детального изучения
Самое главное: почему гипердиагностика и гиперлечение РЩЖ являются проблемой?
В связи с выявленным фактом, что в оперативном лечении таких РЩЖ, вполне возможно, нет необходимости (а ведь удаление ЩЖ сопровождается серьезными последствиями, о чем мы расскажем далее), с 2015 года в США уже принимаются меры по снижению частоты гипердиагностики и гиперлечения [24]. Например, уже настоятельно рекомендовано не проходить скрининг РЩЖ пациентам, у которых нет никаких симптомов, поскольку выявление агрессивных типов рака в этом случае крайне маловероятно.
Что врачи думают о данной проблеме?
Проблема гиперлечения РЩЖ существует не только среди пациентов, но и среди медицинского сообщества.
Конечно, выбор, удалять ли щитовидную железу или нет, стоит больше перед пациентом, нежели перед лечащим врачом. И пациент вполне может выбрать хирургическую тактику лечения. А врач должен определять, сколько ткани щитовидной железы в конкретном случае нужно убирать.
В качестве уменьшения гипердиагностики Американская тиреоидологическая ассоциация рекомендует воздержаться от скрининга и биопсии мелких образований щитовидной железы при отсутствии на то иных клинических симптомов [6].
Как вообще лечат рак щитовидной железы?
Давайте разберемся, какие существуют пути лечения РЩЖ [26].
- Полное удаление ЩЖ, тотальная тиреоидэктомия, вместе с окружающей клетчаткой, а иногда и рядом лежащими лимфатическими узлами.
- Терапия радиоактивным йодом I 131 после тотальной тиреиодэктомии. Не пугайтесь — это не опасно! Такой йод влияет только на клетки щитовидной железы и убивает их.
Почему мы, авторы, так не хотим, чтобы щитовидную железу удаляли без серьезных на то причин? Казалось бы, мы уберем орган, где сидит рак, и будем жить себе спокойно, только лишь принимая препараты гормонов щитовидной железы. Это ведь лучше, чем жить с раком. Или все-таки нет? Так вот, сама сложность вопроса заключается в операции.
Чем чревато полное удаление щитовидки (или, как говорят врачи, тотальная тиреоидэктомия)?
Существует два серьезных осложнения тотальной тиреоидэктомии [27].
- Стойкое снижение функции щитовидной железы (гипопаратиреоз). Наиболее серьезное и жизнеугрожающее осложнение. Итак, прямо за щитовидной железой располагаются четыре паращитовидные железы. Они производят паратиреоидный гормон, который отвечает за обмен кальция в нашем организме (а из него состоит бóльшая часть наших костей!). Паращитовидные железы совсем маленькие: диаметром 5 мм и весом 0,5 г. Их легко не заметить во время операции и удалить вместе с щитовидной железой. К тому же, даже если сохранить эти железы, высока вероятность повреждения питающих их кровеносных сосудов и нервов. А значит, железы просто перестанут работать, и в организм перестанет поступать паратиреиодный гормон. Это чревато возникновением тетанических приступов (подергиваний, которые могут переходит в судороги), нарушением питания волос и ногтей, кожи, эмали зубов, а также отложением кальция вне костей, например, между нервными клетками, что может проявляться в виде паркинсонизма или хореоатетоза — комбинации быстрых порывистых движений с медленными судорожными.
- Повреждение возвратного гортанного нерва и парез гортани. Щитовидная железа располагается прямо перед гортанью. Там же рядом находятся голосовые связки. Все эти структуры иннервируются гортанными нервами. И в случае повреждение некоторых из них — возвратных гортанных нервов — у пациента будет наблюдаться уменьшение активности гортанных мышц, что влечет за собой проблемы работы голосовых связок (в основном, осиплость голоса) и нарушения функций дыхания.
Какой существует выход?
Одним из наиболее перспективных выходов из ситуации является частичное удаление ткани ЩЖ, а именно поврежденной доли. В таком случае пациент, во-первых, избавляется от необходимости принимать пожизненную заместительную терапию гормонами щитовидной железы, а во-вторых, избегает тех серьезных последствий, которые несет за собой операция полного удаления ЩЖ. Однако стоит понимать, что такой вариант не касается опухолей большого размера, а также тех новообразований, которые потенциально могут быть агрессивными (это решает врач!).
Сейчас терапевты и хирурги, которые занимаются патологией щитовидной железы, разделились на два лагеря: те, кто считает, что лучше перестраховаться, и при выявлении даже самой маленькой опухоли удалить всю щитовидную железу, и те, кто считает, что лучшим выходом будет частичное удаление ткани железы, а именно поврежденной ее доли. К сожалению, этот вопрос до сих пор остается открытым. Врачи все еще не могут прийти к единому знаменателю в данном вопросе. Проблема в том, что достоверная объективная доказательная база, на которую врачи могли бы опираться в качестве актуального клинического руководства, вовсе отсутствует. Существуют лишь отдельные исследования, которые обозревают вопрос лишь с одной субъективной стороны [21]. Оптимальным решением данной проблемы, на наш взгляд, стало бы объединение всех существующих статей с объективным и всесторонним взглядом на этот вопрос. Однако подобное исследование лишь ожидает нас в будущем.
Финальный аккорд
С этими и другими мыслями вы можете ознакомится по оставленной нами ссылке [26].
Итак, дорогие наши читатели! Опираясь на всё, о чем мы рассказали выше, мы бы хотели, чтобы вы сделали три главных вывода:
Всем хорошего дня, и берегите свои щитовидки и нервы. :)
Читайте также:



