Рак принцип его действия

Сильное влияние Луны делает Раков чуткими, эмоциональными и загадочными. Эти люди стараются придерживаться принципов, связанных с человеколюбием, ответственностью и взаимопомощью. Вот несколько правил, которым они стараются следовать.
Принцип 1. Дом – это крепость, а не поле боя!
И верно, ведь Раки очень миролюбивы, не любят скандалов и всегда выступают в роле миротворца. Они очень добросердечны и привыкли сохранять мир в отношениях, для чего часто идут на уступки, и могут простить домочадцам даже серьёзные проступки.
Принцип 2. Чуткость к чужим проблемам спасёт мир!
Водная стихия в купе с Лунным влиянием делает представителей этого знака чрезвычайно восприимчивыми к страданиям и бедам окружающих. Но суть в том, что Раки не остаются глухи к чужим несчастьям, что является их основным принципом! Они искренне пытаются посодействовать и дать хороший совет или помочь другу облегчить душу.
Принцип 3. Я не запасливый, а предусмотрительный
В закромах Рака можно отыскать всё необходимое, хоть для поездки загород, хоть на случай ядерной войны! А дело в том, что Рак – знак перестраховщик, но это качество достаточно часто его выручает. К тому же на случай хандры, полный холодильник всегда оказывается кстати.
Принцип 4. Умение ждать – это дар
Ещё один важный постулат каждого Рака – это умение выжидать, присматриваться к людям и здраво оценивать собственные силы. Они не спешат с близкими отношениями, новой работой и предпочитают не ввязываться в авантюры. Именно эти качества обеспечивают им стабильность в жизни и уверенность в завтрашнем дне!
Принцип 5. Нет ничего душевнее чем болтовня на кухне!
Надо сказать, что Рак обожает общаться в камерной, уютной обстановке. А лучшее место для разговоров и маленьких секретов – это собственное обиталище, в котором известен каждый уголок. Потому то люди упомянутого знака не жалуют уличные кафе, благоразумно полагая их неоправданной тратой средств для дружеских посиделок.
Принцип 6. Мама всегда права!
Любовь к родителям – один из основополагающих принципов Рака, и он весьма оправдан, так как с позиции большего опыта они дают дельные советы и готовы поддержать в трудную минуту. Поэтому каждый представитель упомянутого знака, в первую очередь, советуется с родственниками, прежде чем принять важное решение.
Принцип 7. Качество стоит потраченных средств
Бережливость – одна из основных характеристик людей этого созвездия, но она не намекает на скупость, а только подчёркивает трезвый расчёт, с которым Раки подходят к покупкам. Ведь лучше приобрести что-то стоящее, но немного подкопить, чем довольствоваться несколькими подделками, которые выйдут из строя быстрее оригинала!
Принцип 8. Хорошая работа – это дружный коллектив!
Что касается труда и карьеры, то Раки поступают весьма необычно, привыкая к сослуживцам и со временем начиная воспринимать их как членов дружной семьи! Всё от того, что эти люди ставят во главу угла эмоции, которые испытывают в коллективе, а не зарплату или возможность карьерного роста. К тому же польза обществу доставляет Раку настоящую радость и дарит душевное равновесие!
Принцип 9. В прошлом наше будущее
Этот принцип обусловлен всё тем же Лунным влиянием, делающим Раков очень сентиментальными. Они не забывают добра, которое им делали знакомые, помнят о праздниках и очень любят преподносить подарки. К тому же Рак бережно относится к полученному им опыту, дабы не совершать одни и те же ошибки!
Принцип 10. Дети – наше счастье
Дело в том, что Рак – один из самых заботливых, чутких и нежных родителей! Он искренне любит своих детей, пытается передать им собственный опыт и уберечь от ошибок. К тому же эти люди обожают большие семьи и отлично справляются с ролью наставников.
Иммунотерапия: как всё начиналось
Иммунотерапию можно назвать старейшим видом лечения злокачественных новообразований. И в античных, и в средневековых источниках описывались случаи, когда злокачественные опухоли, как правило, локализующиеся на видимых участках тела, значительно уменьшались после явного воспаления с лихорадкой или каких-то других воспалительных заболеваний, перенесённых человеком.
Одним из примеров такого исцеления можно назвать чудо, произошедшее с итальянским святым Пеллегрино Лациози (1265-1345) у которого после сильной лихорадки регрессировала опухоль правой ноги. То есть произошёл сильный запуск местного иммунитета, который привёл к самоизлечению злокачественного процесса.
Научные изыскания в сфере влияния иммунитета на злокачественные новообразования ведутся с 70-80-х годов XX века. И сегодня, на наших глазах, произошло прорывное событие в онкологии и в лекарственной терапии злокачественных опухолей – разработана и внедрена в клиническую практику иммуноонкологическая терапия.
Создатели современного метода иммунотерапии: Джеймс Эллисон и Тасуку Хондзо в 2018 году были удостоены Нобелевской премии – открытый ими принцип положил начало иммуноонкологическим препаратам.

В настоящее время это направление активно развивается – расширяется список онкологических заболеваний, при которых показано и эффективно лечение иммунными препаратами, применяемыми в клинической практике. Используются различные комбинации иммуноонкологических препаратов, они сочетаются либо с другими иммуноонкологическими, либо с таргетными или химиотерапевтическими препаратами.
Действующие сегодня стандарты лечения предполагают применение иммуноонкологической терапии в лечении пациентов после хирургического вмешательства, в рамках так называемой адъювантной, то есть поддерживающей терапии. Сейчас изучается возможность лечения иммуноонкологическими препаратами пациентов с ранними стадиями онкологических заболеваний перед хирургическим вмешательством – в неоадъювантном режиме. То есть стандарты использования этой группы препаратов, скорее всего, будут пересмотрены, а применение расширено.
Как работает иммунная система, и каким образом на неё действует иммунотерапия
Иммунитет – особая биологическая система в пределах нашего организма, которая работает по своим сложным алгоритмам. Она обладает способностью активироваться при любом инфекционном, воспалительном процессе, в то же время у неё есть и собственные подавляющие механизмы.
Когда опухолевые клетки только зарождаются в организме человека в результате генетических мутаций, влияния канцерогенных факторов и др., иммунная система их уничтожает. Но на каком-то этапе вдруг наступает сбой, и происходит её торможение. На самом деле, это нормальная, непатологическая функция иммунитета, которая включается и у здорового человека.
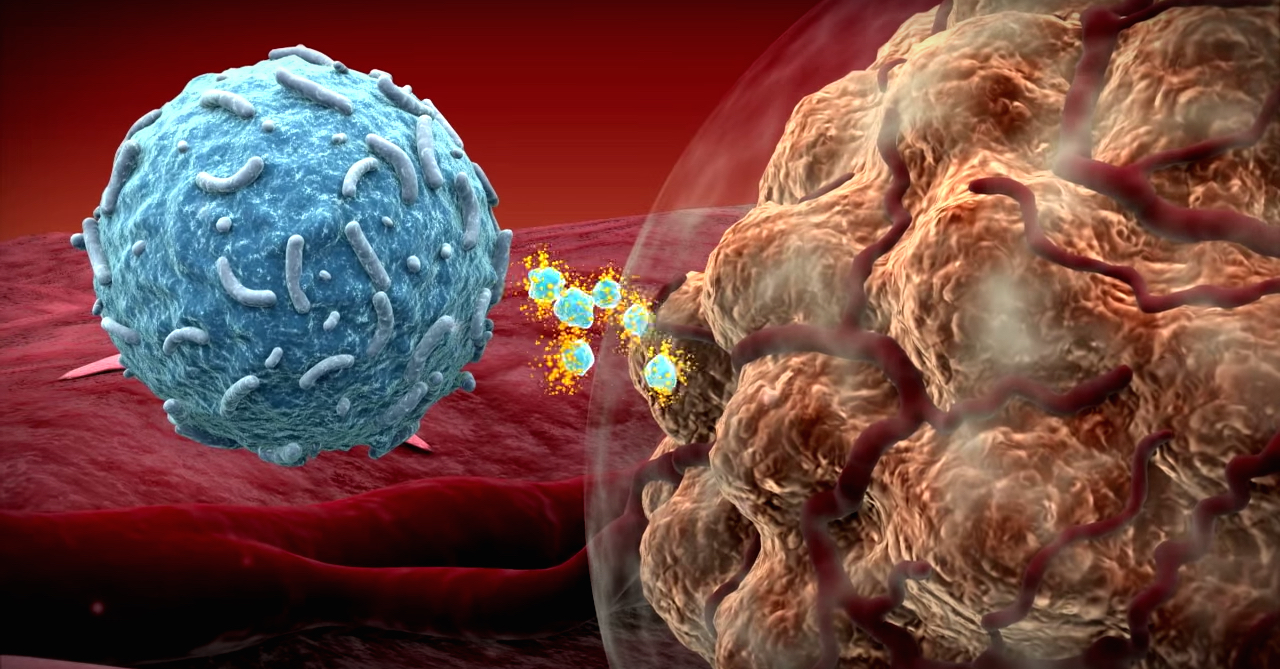
В чём её назначение? Известен целый ряд аутоиммунных (ревматических) заболеваний, при которых иммунная система начинает вырабатывать антитела и бороться с собственными клетками. Это происходит при системной волчанке, ревматоидных артритах и ряде других заболеваний. У пациентов с такими диагнозами здоровые суставы и мышцы поражаются собственной иммунной системой. В организме здоровых людей этому препятствуют специальные механизмы торможения/блокировки. Развиваясь, злокачественный процесс их запускает, и они блокируют иммунный ответ. Опухоль набирает силу. Наступает процесс равновесия, когда иммунная система ещё контролирует патологические клетки, но справляется с ними уже с трудом. Потом происходит ускользание, иммунная система перестаёт распознавать опухоль, которая начинает бесконтрольно расти и распространяться по всему организму.
Необходимо очень тонко воздействовать на противоопухолевый иммунитет с помощью современных имунноонкологических препаратов, чтобы снять все возникшие факторы торможения.

Цель иммунотерапии – помочь собственной иммунной системе бороться с опухолью. Это единственное направление современной лекарственной терапии, которое не предполагает введения ядовитых веществ – молекул, которые влияют на биологию опухоли. Иммунотерапия разблокирует собственную иммунную систему человека, заставляет её снова активно уничтожать патологические клетки. Ведь работают не чужеродные лекарственные препараты, а собственная иммунная система пациента.
Ингибиторы иммунных точек контроля: как работают, когда наступает эффект и как долго он длится
Воздействие на иммунную систему может производиться разными путями. Одно из направлений – это лекарственные препараты, которые активируют иммунную систему организма, противоопухолевый иммунитет, специалисты называют их ингибиторы иммунных точек контроля.
Постоянно расширяется перечень опухолей с доказанной эффективностью лечения блокаторами иммунных точек контроля. Сегодня это не только пигментная опухоль (меланома), это и опухоль лёгкого, лимфопролиферативные заболевания (лимфома Ходжкина), опухоль почки, мочевого пузыря, печени и т.д.
Принцип применения этого вида иммунотерапии – универсальность. Используется один препарат, который работает при многих опухолях, в отличие от химиопрепаратов, которые специализируются на тех или иных видах опухолей: при опухоли молочной железы работают одни агенты, при опухоли кишки – другие. В иммунотерапии используется один препарат – ингибитор PDL-1, который работает и при опухоли желудка, и опухоли кишки, и опухоли лёгкого и т.д. Он влияет не на опухоль, а на иммунную систему, с помощью этого антитела разблокируются её клетки.
Клиническое применение иммуноонкологических препаратов за рубежом началось в 2000-х, то есть за многими клиническими случаями, конкретными пациентами, врачи наблюдают на протяжении 10 лет с того момента окончания лечение. Многие из них живы, они считаются излеченными. То есть речь идёт даже уже не о пятилетней ремиссии, при наличии которой пациенты считаются излеченными, а о десятилетней выживаемости без признаков заболевания.

Несмотря на то что иммунотерапия, как и все другие виды лечения не панацея, отвечают на неё 20-30% пациентов, но она способна полностью излечить от заболевания, позволить контролировать его длительное время.
Специалистам НМИЦ онкологии им. Н.Н. Петрова также встречались клинические случаи, когда выраженный регресс опухоли происходил довольно быстро – на протяжении трёх месяцев.
В иммунотерапии важен опыт врача, поскольку опухолевая масса элиминируется (гибнет) в организме, необходимо провести процесс её выведения без интоксикации продуктами распада, без повышенной реакции со стороны иммунной системы.
Часто злокачественные опухоли дают метастазы в головной мозг, это всегда отягощает течение заболевания, требует проведения лучевой терапии или операции, поскольку это действительно очень серьёзное проявление заболевания. Иммунотерапия работает и при поражении головного мозга.
Пока механизм действия иммунной системы остаётся загадкой, которую в полной мере ещё не разгадали, но полученные сегодня результаты воодушевляют.
Даёт ли иммунотерапия осложнения?
Как и любой другой вид лечения, иммунотерапия даёт осложнения. Они непохожи на осложнения при химиотерапии или гормонотерапии ни по своим проявлениям, ни по схемам их лечения.

Важно, чтобы пациенты понимали механизмы всех осложнений, знали, на что обращать внимание, как быстро нужно обращаться к врачу при их возникновении, чтобы они не достигли степени, когда будет сложно с ними бороться.
Осложнения иммунотерапии связаны с тем, что иммунитет сильно активируется и начинает бороться не только с опухолевыми клетками, но и с любыми собственными тканями. Чем больше мы лечим иммуноонкологическими препаратами, тем более редкие осложнения встречаем. Это, например, изолированное поражение языка – воспаление, уплотнение, сложности с речью или реакция со стороны органов зрения – конъюнктивит или иридоциклит.
Почему важно, чтобы врач и пациент знали, что любой орган системы может быть поражён именно воздействием иммунной системы? Чтобы пациент, например, при конъюнктивите не пошёл сразу на приём к офтальмологу, который, скорее всего, пропишет ему капли от сезонного конъюнктивита, а на самом деле, это будет осложнение иммунотерапии, и лечить его нужно определённым способом. Перечисленные выше осложнения были успешно вылечены по протоколу стандартного лечения осложнений, связанных с гиператакой иммунной системы против собственного организма.
Примерные сроки проявления осложнений
Сроки появления осложнений могут быть разными: как в ближайшее время после введения иммунного препарата, так и через несколько лет. Описаны случаи, когда осложнения возникали через пять лет после завершения терапии, поэтому необходимо всегда быть начеку. Как правило, более ранние осложнения – со стороны кожных покровов, более поздние – со стороны печени, и эндокринной системы.
Если пациент отмечает какие-либо непонятные неприятные изменения в своём состоянии: высыпания, расстройство стула, то не надо заниматься самолечением, а необходимо срочно обратиться к своему лечащему врачу-химиотерапевту. Он уже определит, нужно ли подключать дополнительно узких специалистов или назначит лечение, которое, как правило, будет успешным в плане коррекции возникших осложнений.

Многие осложнения могут представлять угрозу для жизни, например, очень выраженное расстройство стула способно привести к обезвоживанию, нарушению электролитного обмена и работы сердца. К лечащему врачу-онкологу необходимо обращаться на самых ранних этапах возникновения осложнений.
Наиболее частые осложнения иммунотерапии
Чаще всего страдают кожа, желудочно-кишечный тракт, печень, эндокринная система, нервная система, дыхательная система. Список можно продолжить, потому что появляются данные, что могут поражаться и миокард (сердечная мышца), и почки, наверное, нет органа, который не может быть поражён гиперактивной иммунной системой.
Кишечные осложнения проявляются не очень специфично, то есть если у пациента многократный жидкий стул с примесью крови или слизи, боли в животе, повышение температуры, пациент может подумать или неопытный врач решить, что это пищевое отравление. Но, к сожалению, это проявление агрессии иммунной системы в отношении здорового кишечника. В этой ситуации обязательно используются высокие дозы кортикостероидов, при этом пациент должен быть госпитализирован. Всё, что связано с кишечником, это, безусловно, уже серьёзные осложнения, которые требуют наблюдения в условиях стационара.
Как правило, врач, который проводит лечение, снабжает пациента памяткой, где указаны все основные проявления, которые могут возникнуть при проведении данного лечения, моменты, на которые нужно обратить внимание, и особенности диеты, которая назначается при том или ином осложнении.
У многих пациентов возникает вопрос: зачем после получения иммуностимулирующего препарата использовать иммуносупрессрующий, т.е. подавляющий иммунную систему (в эту группу входят кортикостероиды). Не скажется ли это на эффективности лечения?
Доказано, что использование кортикостероидов для лечения осложнений не сказывается на эффекте иммунотерапевтического лечения. При этом очень важно их применение в назначенных врачами дозах. По имеющимся данным, наличие осложнений, то есть проявление гиперактивности иммунной системы, это косвенный признак эффективности лечения.
Со стороны кожи наблюдаются самые различные осложнения. Как правило, это высыпания, локализующиеся в первую очередь в подмышечных впадинах, подколенных ямках, локтевых сгибах. Они могут покрывать практически всю поверхность тела. Это уже серьёзно: если кожные покровы повреждены сильно, то происходит инфицирование. Воспаление кожных покровов – элемент выраженной интоксикации, поэтому при первых появлениях высыпаний нужно обязательно обратиться к врачу.
Изменения со стороны печени часто протекают бессимптомно, чтобы их выявить, перед очередным введением препарата необходимо сделать биохимический анализ крови. Аутоиммунную реакцию со стороны печени можно определить по повышению трансаминазы, печёночных ферментов, билирубина. Бывает, что при иммунотерапевтическом лечении значение трансмаминазы у пациента – 1500 единиц (при максимально допустимом – 35-50 единиц). При этом нет жалоб и других симптомов. Это основание для того, чтобы отменить очередное введение иммуноонкологического препарата, назначить большие дозы кортикостероидов и иное лечение.
Чаще всего страдает щитовидная железа, чуть реже – гипофиз, который находится в головном мозге, а также надпочечники. Симптомы при этом очень неспецифические, это может быть слабость, сухость кожи, потливость, сильное сердцебиение.
Осложнения со стороны дыхательной системы могут быть серьёзными: пульмониты, пневмониты, лёгочная ткань может стать отёчной и не фильтроваться, может произойти отёк висцеральной ткани лёгкого. Этот может стимулировать присоединение инфекции. Поэтому о любых изменениях со стороны дыхательной системы пациент должен рассказать своему доктору.
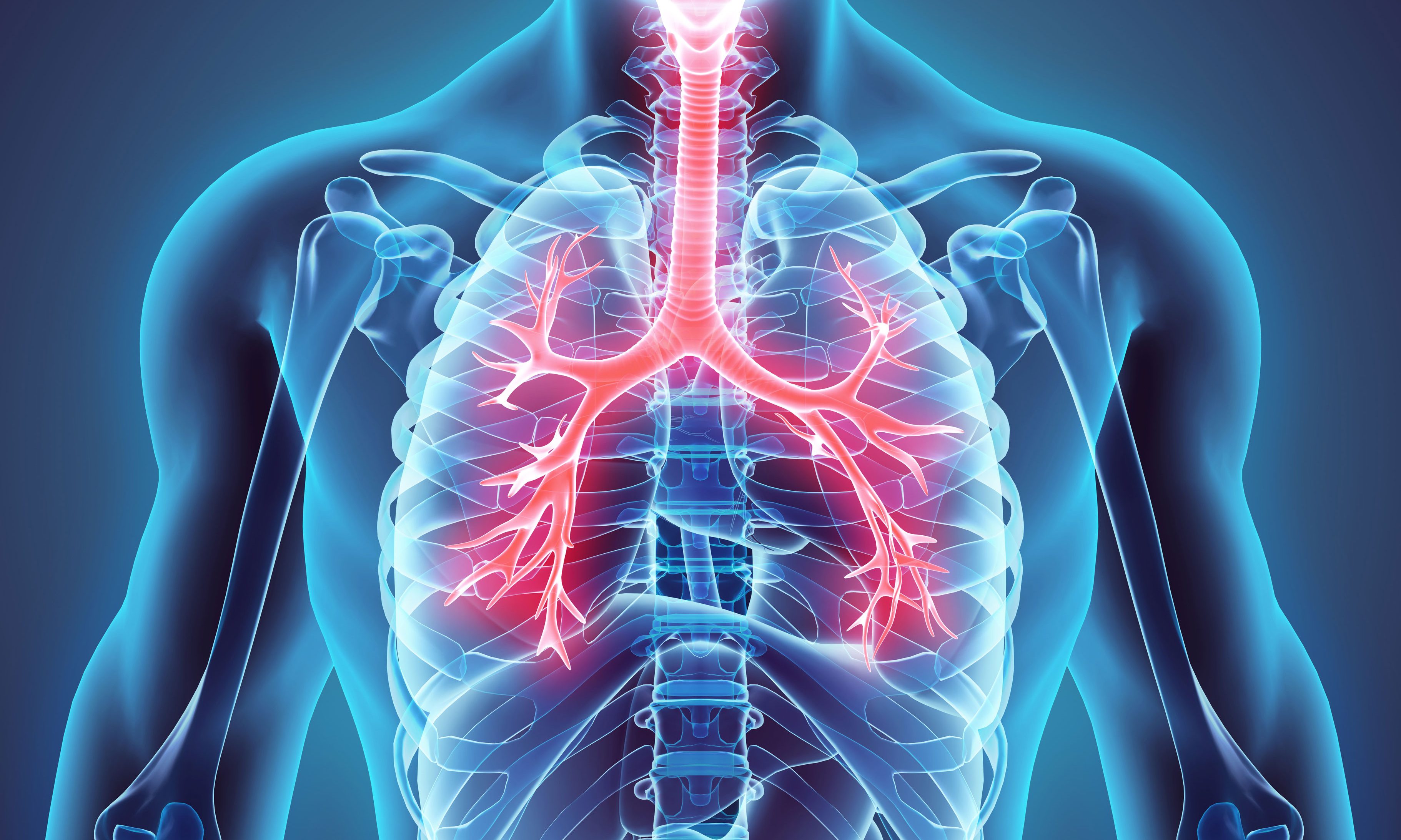
Токсическое действие иммунотерапии на лёгочную ткань может не иметь клинических проявлений и быть выявленным только на КТ.
Осложнения могут иметь рецидивирующее волнообразное течение. Это случается, как правило, если курс лечения кортикостероидами проведён не полностью, например, через одну или две недели после начала он прерван пациентом или доктором по неопытности. В этом случае иммунная система вновь становится активной и с большей степенью тяжести воздействует на тот же поражённый орган. Так что длительное лечение осложнений должно быть обязательным, при этом даже интервалы между введениями иммунных препаратов могут быть большими.
Пациенты должны помнить, что все осложнения иммунотерапии требуют специального лечения: самолечение здесь недопустимо! Необходимо поддерживать контакт со своим лечащим врачом и следовать его рекомендациям, а для лечения ряда осложнений может потребоваться и госпитализация в стационар.


Авторская публикация:
Семенова А. И.
Старший научный сотрудник
НМИЦ онкологии им Н.Н. Петрова,
врач-онколог, химиотерапевт, доцент

Доклад подготовлен:
Новик А. В.
Старший научный сотрудник
НМИЦ онкологии им. Н.Н. Петрова,
врач-онколог, трансфузиолог, аллерголог, иммунолог

В настоящее время лучевая терапия рака назначается почти половине онкобольных: рассмотрим виды радиотерапии, показания и биологические аспекты лечения.
В последние годы достигнут значительный прогресс в понимании механизмов развития, способов диагностики и лечения онкологических заболеваний.
С ростом заболеваемости онкология продолжает оставаться главной медицинской проблемой XXI века.
Современные методы лечения включают хирургическое удаление опухолей, лучевую терапию, химиотерапию, иммунотерапию, таргетную и гормональную терапию.
Лучевая терапия, которую получают 50% онкологических больных, остается важнейшим компонентом лечения рака в мире.
По оценкам британских экспертов, она обеспечивает в среднем 40% суммарной клинической эффективности.
Цель лучевой терапии — лишить раковые клетки их потенциала размножения.
Минуло более 100 лет с тех пор, как Мария Кюри получила вторую Нобелевскую премию за исследования радия. За этот век постоянный прогресс в радиотерапии и понимании биологии опухолей способствовал многократному увеличению выживаемости онкобольных и минимизации побочных эффектов лечения.
Стремительный прогресс обусловлен достижениями в области медицинской визуализации, компьютеризированных систем планирования и аппаратов для радиотерапии.
В этой статье мы обсудим принципы, разновидности и показания к лучевой терапии.
Принципы действия лучевой терапии
Радиация — это физический агент, который используется для уничтожения клеток рака.
Ионизирующее излучение получило такое название, потому что оно формирует ионы (электрически заряженные частицы) и выделяет энергию в клетках тканей, через которые проходит. Эта депонированная энергия может убить раковые клетки или вызвать генетические изменения, приводящие к их последующей гибели.
Высокоэнергетическое излучение повреждает генетический материал клеток (дезоксирибонуклеиновая кислота, ДНК) и блокирует их способность делиться.
Но радиация повреждает как нормальные, так и раковые клетки.
Поэтому цель лучевой терапии в том, чтобы максимизировать дозу облучения аномальных клеток, сводя к минимуму воздействие на здоровые клетки, которые примыкают непосредственно к опухоли или находятся на пути ионизирующих лучей.
Нормальные клетки могут восстанавливаться быстрее раковых и способны сохранять нормальный функциональный статус после перенесенного облучения.
Раковые клетки гораздо более чувствительны к ионизирующему излучению, а их внутренние механизмы хуже справляются с восстановлением повреждений генетического материала.
Радиотерапия может с успехом применяться как в куративной терапии (с целью излечения рака), так и в паллиативной терапии (для облегчения симптомов, вызванных заболеванием).
Для повышения эффективности лечения были разработаны комбинированные стратегии, объединяющие облучение с хирургическими методами, химиотерапией и иммунотерапией.
При использовании до операции (неоадъювантная терапия) облучение будет направлено на уменьшение опухоли.
При использовании после операции (адъювантная терапия) облучение разрушит микроскопические резидуальные опухолевые клетки, оставшиеся после хирургического вмешательства.

Основные показания к лучевой терапии
Хорошо известно, что опухоли отличаются по чувствительности к облучению.
Основные показания к лучевой терапии рака перечислены ниже.
Виды рака, которые на ранних стадиях излечиваются только лучевой терапией:
• Плоскоклеточный рак кожи
• Базальноклеточный рак кожи
• Рак предстательной железы
• Ходжкинские и неходжкинские лимфомы
• Немелкоклеточный рак легкого
• Рак головы и шеи
• Рак шейки матки.
Виды рака, которые излечиваются лучевой терапией в комбинации с другими методами:
• Саркомы мягких тканей
• Рак молочной железы
• Рак прямой кишки и анального канала
• Местно-распространенный рак шейки матки
• Местно-распространенный рак головы и шеи
• Лимфомы на поздних стадиях
• Рак мочевого пузыря
• Рак эндометрия
• Рак мозга.
Существует множество других заболеваний, при которых радиотерапия может принести клиническую пользу. В настоящее время этот список расширяется благодаря внедрению более эффективных комбинированных схем лечения.
Виды лучевой терапии рака
Существует два принципиально отличающихся способа доставки радиации в область локализации опухоли — внутренняя и внешняя лучевая терапия.
Внешняя лучевая терапия действует извне тела, направляя высокоэнергетические лучи (фотоны, протоны или частицы излучения) в опухолевую ткань. Это наиболее простой и часто используемый способ в реальной клинической практике.
Внутренняя лучевая терапия, или брахитерапия, основывается на доставке радиоактивных источников, которые запечатывают в катетеры или зерна, доставляемые непосредственно в опухоль. Брахитерапию широко применяют в лечении гинекологических опухолей и злокачественных новообразований предстательной железы.
Цель любой радиотерапии состоит в том, чтобы доставить как можно большую дозу в опухоли, сохраняя здоровые ткани. Технические достижения, включая новые способы получения изображений, более мощные компьютеры, программное обеспечение и усовершенствованные линейные ускорители, помогают достичь этого.
Лучевая терапия, выполняемая во фракционированном режиме, основана на различии радиобиологических свойств опухолевых и нормальных клеток.
Это режим, при котором выживаемость здоровых клеток обеспечивается путем более щадящего, сублетального воздействия нескольких малых доз радиации.
Нормальные клетки организма делятся относительно медленно по сравнению с быстро пролиферирующими опухолевыми клетками, а потому они имеют больше времени для восстановления повреждений ДНК перед репликацией.

Самые первые наблюдения эффектов фракционированной лучевой терапии относятся еще к 1920-м годам. После длительных исследований предложены схемы радиотерапии с разными дозами, количеством сеансов и общем временем лечения.
Современные режимы основаны на усовершенствованной линейно-квадратичной формуле, которая учитывает временные и дозовые факторы для разных типов опухолей и нормальных тканей человеческого организма.
Типичный режим лучевой терапии в настоящее время состоит из ежедневных фракций с дозами от 1,5 до 3 Гр, назначаемых в течение нескольких недель.
2D-лучевая терапия с использованием прямоугольных полей на основе рентгеновской визуализации была заменена 3D-лучевой терапией на основе данных КТ. 3D-CRT позволяет точно локализовать опухоль и жизненно важные структуры здоровых органов для оптимального размещения луча и экранирования.
Суть в том, чтобы доставить излучение в общий объем опухоли (GTV) с запасом для микроскопического расширения опухоли — это называется клиническим целевым объемом облучения (CTV). При этом следует учитывать неопределенности от движения тела и изменения настроек — это называется плановым целевым объемом (PTV).
IMRT позволяет врачу задавать области облучения неправильной формы, которые соответствуют геометрии опухоли, одновременно огибая расположенные рядом органы.
Лучевая терапия с модуляцией интенсивности требует двух компонентов:
• Программное обеспечение для обратного планирования
• Управляемая компьютером модуляция интенсивности нескольких пучков.
В настоящее время IMRT доступна в большинстве клинических центров мира, которые оборудованы линейными ускорителями со статическими или же динамическими многолистовыми коллиматорами или томотерапевтическими аппаратами.
Это позволило улучшить терапевтическое соотношение для нескольких типов опухолей, расположенных в разных частях тела. IMRT особенно эффективна при раке головы и шеи, гинекологическом раке, а также при раке предстательной железы.
По мере того, как границы облучения становятся тонкими и конформными, риск пропустить опухоль из-за движения органа и изменений в настройках аппарата становится все выше.
Когда критически важные структуры находятся близко к опухоли, незначительная ошибка в положении тела может привести к непреднамеренному облучению нормальных органов.
IGRT позволяет обнаруживать такие ошибки по информации, полученной с помощью визуализации непосредственно перед сеансом облучения. Один из источников данных — ежедневные КТ-исследования с коническим лучом перед каждым сеансом.
Повышенная точность сделала возможным существенное повышение дозы облучения и улучшение терапевтического соотношения для рака головы и шеи и рака предстательной железы и ряда других злокачественных новообразований.
Вышеуказанные технологические достижения привели к разработке метода SBRT, который с высокой точностью доставляет высокие индивидуальные дозы облучения всего за несколько фракций, позволяя удалять небольшие, четко очерченные первичные или олигометастатические опухоли в любом месте тела.
Из-за высокой дозы облучения любая ткань, непосредственно прилегающая к опухолям, потенциально может быть повреждена. Но, поскольку объем нормальной ткани в области высоких доз небольшой, клинически значимая токсичность минимальна.
Этот вид лучевой терапии показал отличные результаты в лечении немелкоклеточного рака легкого на ранней стадии у пациентов, не подходящих для хирургического вмешательства.
SBRT хорошо подходит для лечения рака предстательной железы, опухолей головы и шеи, печеночно-клеточного рака, рака почки, рака поджелудочной железы и опухолей ЦНС.
Типы излучения: рентгеновские и гамма-лучи
Рентгеновские лучи и гамма-лучи, широко используемые в клинической практике, являются разреженным ионизирующим излучением. Все это электромагнитные лучи с низкой линейной передачей энергии, состоящие из безмассовых частиц (фотоны).

Рентгеновские лучи генерируются устройством, которое возбуждает электроны (например, электронно-лучевые трубки и линейные ускорители), а гамма-лучи возникают в результате распада радиоактивных веществ (например, кобальта-60, радия и цезия).
Электронные лучи чаще всего используются в лучевой терапии.
Они особенно полезны для лечения опухолей вблизи поверхности тела, поскольку не проникают достаточно глубоко в биологические объекты.
Внешняя лучевая терапия также осуществляется с тяжелыми частицами:
• нейтроны, генерируемые нейтронными генераторами и циклотронами;
• протоны, создаваемые циклотронами и синхротронами;
• тяжелые ионы (гелий, углерод, азот, аргон, неон), вырабатываемые синхроциклотронами и синхротронами.
Протонные пучки — относительно новая форма излучения, используемая в онкологии. Протонная терапия рака предлагает лучшее распределение дозы благодаря уникальному профилю поглощения в тканях, известному как пик Брэгга.
Суть этого явления заключается в том, что протоны выбрасывают максимальную разрушительную энергию на строго определенной глубине внутри опухоли, сводя к минимуму повреждение здоровых тканей вдоль их пути.
Нейтронные пучки генерируются внутри нейтронных генераторов после отклонения протонных пучков к цели. Они имеют высокий показатель линейной передачи энергии (ЛПЭ), и могут вызвать большее повреждение ДНК, чем фотоны.
Ограничения терапии нейтронами связаны, главным образом, со сложностью генерации нейтронных частиц, а также со строительством ускорителей соответствующего типа.
Радиотерапия тяжелыми заряженными частицами отличается тем, что частицы имеют более высокие значения ЛПЭ и высокую биологическую эффективность. Следовательно, тяжелые частицы могут быть более эффективными при радиорезистентных онкологических заболеваниях, таких как саркома, меланома и глиобластома.
Оборудование для радиотерапии тяжелыми заряженными частицами значительно дороже, чем для облучения фотонами (рентгеновскими и гамма-лучами).
Однако потенциальная эффективность этого метода поддерживает повышенный интерес исследователей. Снижение стоимости циклотронов, вероятно, приведет к более широкому использованию протонов и тяжелых частиц в будущем.
Биологические аспекты лучевой терапии
Биологическая эффективность радиотерапии рака (уничтожение клеток) зависит от значения линейного переноса энергии, суммарной дозы, фракционирования, а также радиочувствительности клеток или тканей-мишеней.
Излучение с низкой ЛПЭ доставляет относительно небольшое количество энергии, в то время как излучение с высокой ЛПЭ доставляет в клетки рака более высокую энергию.
Хотя облучение направлено на уничтожение опухолевой клетки, незлокачественные нормальные ткани, окружающие опухоль, также повреждаются радиацией.
Целью лучевой терапии является максимизация дозы для опухолевых клеток при минимально возможном воздействии на нормальные здоровые клетки.
Биологическое действие радиотерапии может быть прямым или непрямым:
• Прямое действие: облучение — повреждение ДНК — клеточная смерть.
• Непрямое действие: облучение — высвобождение свободных радикалов — окислительное повреждение ДНК — клеточная смерть.
Таким образом, радиация может либо напрямую дестабилизировать генетический материал раковых клеток, либо инициировать повреждение ДНК свободными радикалами в результате ионизации и возбуждения водного компонента клеток.
Двухцепочечные разрывы ДНК являются непоправимыми и более опасными для клетки, чем одноцепочечные разрывы ДНК. Это фатальное повреждение, как для большей части раковых клеток, так и для окружающих опухоль нормальных клеток.
Основная цель лучевой терапии — лишить раковые клетки потенциала размножения с последующей неизбежной гибелью. Клетки, ДНК которых повреждена без возможности восстановления (репарации), перестают делиться и вскоре погибают.
Однако механизмы клеточной смерти при лучевой терапии являются сложными, разнообразными и не до конца изученными на молекулярном уровне.
Определение варианта радиационно-индуцированной гибели клеток и других задействованных механизмов важно для улучшения результатов радиотерапии.

Лучевая терапия, как и большинство типов противоопухолевого лечения, достигает терапевтического эффекта путем индукции гибели клеток.
При этом раковые клетки погибают не сразу. Требуются часы, дни и недели лечения, прежде чем они начинают умирать, после чего процесс разрушения опухоли продолжается в течение недель или даже месяцев после окончания курса.
Варианты гибели раковых клеток под воздействием радиации:
Запрограммированная гибель клеток, или апоптоз, является основным механизмом разрушения опухоли при радиотерапии.
Апоптоз характеризуется уменьшением клеток и образованием апоптотических тел. Митохондрии играют ведущую роль в этом процессе. Апоптоз клеток сопровождает блеббинг клеточной мембраны с фрагментацией ДНК.
Индукция апоптоза в раковых клетках играет ключевую роль в лучевой терапии.
Гибель клеток этого типа происходит во время или после аберрантного митоза (деления клеток), и вызывается неправильной сегрегацией хромосом, приводящей к образованию гигантских клеток с аберрантной ядерной морфологией и множественными ядрами.
Клетки имеют одно или несколько микроядер. После облучения гибель солидных опухолевых клеток происходит в результате аберрантных митотических событий.
Вышеуказанные два типа гибели клеток составляют основу биологического действия, вызванного ионизирующим излучением.
Клетки имеют атипичную форму ядер с вакуолизацией, неконденсированным хроматином и дезинтегрированными клеточными органеллами. Они характеризуются митохондриальным набуханием и разрывом плазматической мембраны с последующей потерей внутриклеточного содержимого.
После лучевой терапии некроз наблюдается реже, но встречается в некоторых экспериментальных раковых клеточных линиях или тканях.
Старением называют постоянную и необратимую потери способности клеток к делению. Стареющие клетки жизнеспособны, но не делятся, перестают синтезировать ДНК, увеличиваются в размерах и сплющиваются, в них повышается гранулярность.
Сообщалось, что старение наблюдается в раковых клетках после выраженного клеточного стресса. Это может происходить в результате повреждения ДНК, вызванного радиационным излучением. Позже клетки умирают, главным образом, в результате апоптоза.
Это явление описано относительно недавно. Аутофагия представляет собой вариант гибели клеток в ответ на облучение. Аутофагия — генетически регулируемая запрограммированная гибель клеток, при которой клетка переваривает сама себя.
Данный процесс задействует аутофагический / лизосомальный компартмент. Он характеризуется образованием двойных мембранных вакуолей в цитоплазме, которые изолируют органеллы, конденсированный ядерный хроматин и рибосомы.
Сообщалось, что разные гены и внутриклеточные пути (р53, каспазы, ФНО-альфа, mTOR) участвуют в различных вариантах радиационно-индуцированной гибели раковых клеток.
Тем не менее, исследователям многое еще предстоит понять в отношении путей гибели клеток, которые вызывают онкогенез и устойчивость к радиотерапии.
В последние годы быстро растет объем знаний о внутренних молекулярных путях, участвующих в гибели клеток после облучения.
Особый интерес представляют механизмы ответа и восстановления повреждений ДНК, внутриклеточной передачи сигналов в ответ на однократное или же фракционированное излучение, а также воздействия облучения на микроокружение опухоли.
Новые достижения в секвенировании генома открывают более широкие молекулярно-направленные стратегии лучевой терапии рака в следующем десятилетии.
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
Читайте также:

