Радиоизотопное сканирование при опухолях легких
При обследовании первых 250 пациентов выявлено, что для РМЖ типичным является узловое включение РФП при величине индекса накопления "опухоль/фон" > 1.30. Специфичность метода в нашем исследовании превышала 95 %.
Использование 67Ga хотя и позволяет визуализировать рак легкого, но при этом неспецифичен и аккумулируется в легких также при различных воепалительных повреждениях, что затрудняет дифференциальный диагноз. Кроме того, при использовании 67Ga значительна лучевая нагрузка для пациента. 201Tl намного более специфичен для диагностики первичных опухолевых поражений в легком, нежели 67Ga. Однако дороговизна производства 201Tl существенно ограничивает' его доступность. Таким образом, проблема сцинти-графического выявления первичного очага опухоли при раке легкого остается практически нерешенной.
В работе изучены показатели накопления отечественного препарата 99mTc- МИБИ-99m Тс -технетрила - при раке легкого и прочих опухолевидных образованьях в легком, используя технику однофотонной эмиссионной компьютерной томографии (ОЭКТ).
Обследовано 73 пациента со злокачественными опухолями легкого и 16 больных с неопухолсвой патологией легкого, из них 73 мужчин и 19-женщин, средний возраст обследованных 61+9 лет. Периферическая опухоль диагностирована у 26 больных, в 4 случаях имело место метастатическое поражение легкого, центральный рак легкого верифицирован у 43 пациентов. В группе пациентов с неопухолевыми заболеваниями легочной ткани вошли 3 пациента с туберкуломами легкого, 3 пациента с доброкачественными опухолями, у 7 диагностирован локальный фиброз как остаточные явления перенесенной пневмонии, 3 пациента с острой неспецифической пневмонией в 2 случаях осложненной деструкцией легочной ткани.
Во всех случаях диагноз верифицирован морфологически при хирургическом вмешательстве или при трансторакальной пункционной биопсии.
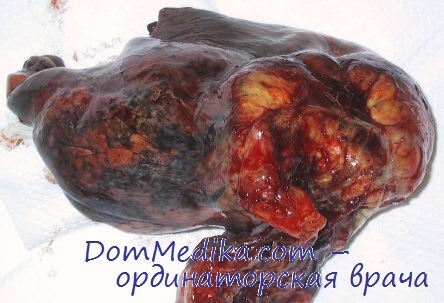
Для полуколичественной оценки 99mTc-МИБИ в опухолях легких рассчитывалось отношение величин поглощения в области патологического включения радиофармпрепарата в летком, пораженном опухолью, к поглощению в области миокарда, который использовался в качестве референспой зоны. Кроме того рассчитывалось аналогичное соотношение также относительно области фона, которое служили симметричные области коигралагерального здорового легкого. Локальное накопление препарата в легких оценивалось как патологическое при визуально определяемом очаговом характере накопления РФП в регионе легкого и соотношении поглощения РФП (опухоль/миокард) свыше 0.28.
По данным исследований в контрольной группе индекс легкое/миокард не превышал 0.23. Среднее соотношение составило у контрольных лиц 0.19+0,05 и не отличалось между правым и левым легким. При визуальном анализе сагиттальных ОЭКТ - срезов грудной клетки у пациентов с раком легкого включение РФП в опухолевый очаг было отмечено у 70 (81,1%) больных в ранние сроки после введения, в 3 (9.9%) наблюдениях включение РФП в месте локализации карциномы легкого отсутствовало.
При периферической и центральной форме рака легкого включение РФП было близкой интенсивности. Соотношение накопления РФП опухоль/миокард составило, соответственно 0.29 + и 0.28 + 0.05. Интенсивное накопление 99mТс-МИБИ наблюдалось при мезастатическом поражении легкого У всех 4 обследованных больных , индекс накопления 0,28 + 0.06. Минимальный размер визуализируемой опухоли составил 1,2-1,5 см, что подтверждено данными КТ - обследования грудной клетки и хирургическим вмешательством.
В контрольной группе из 16 пациентов в одном случае отмечено ложноположительная реакция в виде слабо интенсивного облаковидного накопления РФП, индекс накопления опухоль/миокард 0.27, у больной ранее оперированной по поводу папилляроного рака щитовидной железы. При послеоперационное морфологическое исследование диагностирована гамартома легкого.
Таким образом, представленные результаты показывают, что 99mTc-МИБИ высокоспецифичный онкотронный радиофармпрепарат и может быть использован для диагностики первичного и метастатического опухолевого поражения легких, определения топографии, размеров и распространенности рака легкого.
Ранняя диагностика рака легких способна предотвратить прогрессирование заболевания и обеспечить результативное лечение. Выявление опухоли на 1—2 стадии положительно отображается на дальнейшем прогнозе. При 3—4 стадии диагностические мероприятия выполняются для выявления новообразования и контроля лечения. Важно понимать, что профилактические осмотры и периодическое обследование легких нужно осуществлять минимум 1 раз в год, чтобы уберечь себя от негативных последствий.

Когда нужна диагностика?
К показаниям проведения обследования относятся:
- курение;
- хронический бронхит;
- бронхиальная астма;
- бронхоэктатическая болезнь;
- доброкачественное образование;
- ежегодное профилактическое исследование;
- рак легких в семейном анамнезе;
- затяжной кашель и боль в груди;
- выделение мокроты в больших количествах;
- кровь в легочном отделяемом;
- общая слабость и недомогание.
Методы диагностики
Это метод ранней диагностики рака легкого, который должен проходить каждый человек 1 раз в год, а люди, работающие в сфере медицины или учебных заведений — дважды. Флюорография относится к безопасным процедурам и способна проверить, есть ли в органах дыхательной системы патологические очаги. Снимок не покажет вид и стадию рака, но, обнаружив изменения, можно применять иные методы исследования для уточнения диагноза.
С помощью флюорографии рак диагностируется на начальных этапах развития, что имеет положительное влияние на дальнейшее лечение и прогноз.
Это высокотехнологические методики, позволяющие послойно изучить не только пораженный орган, но и целый организм. Диагностика легких этим способом дает возможность узнать все физические характеристики новообразования, особенности его кровоснабжения, степень инвазии в соседние ткани и распространение. КТ и МРТ выявляют метастазы в лимфатических узлах и других органах даже при их незначительных размерах, благодаря использованию контрастных средств.
Рак легкого включает этот метод, как дополнительный, поскольку при этом организм пациента поддается сильному влиянию позитронов, что может негативно отобразиться на состоянии у пожилых людей или детей. Механизм работы этого устройства основан на фиксировании с помощью излучений степени обмена веществ в органах и структурах. Далее изображение в разнообразной цветовой гамме переносится на экран. Каждый цвет обозначает степень интенсивности обмена. Клетки опухоли непрерывно и неконтролируемо делятся, и это отображается на снимках.
Существует метод позитронно-эмиссионной томографии в сочетании с КТ. Они диагностируют рак и предоставляют целый спектр необходимых сведений — локализацию, размеры опухоли, точные границы новообразования, распространение в лимфатические узлы и отдаленные метастазы. Результаты этих исследований определяют дальнейшую тактику лечения и способы терапии.
При обнаружении опухоли с помощью КТ или МРТ в обязательном порядке нужно исследовать патологическую ткань. Для этого нужно проникнуть в первичный очаг и отделить от него небольшую частицу. Далее материал отправляется на гистологическое и цитологическое исследование, с помощью которого определяется степень злокачественности клеток, скорость их деления и развития.
Существуют следующие разновидности проведения биопсии:
- При бронхоскопии. Методика, подразумевающая введение бронхоскопа в дыхательную систему до участка образования, и специальным приспособлением отщепление части патогенной ткани, что граничит со здоровыми структурами.
- При медиастиноскопии. Введение эндоскопа осуществляется через средостение. Эту методику используют при поражении левого легкого. Для введения аппарата делают специальный разрез на шее, проводят трубку к злокачественному очагу и щипцами забирают материал.
- Пункционная биопсия. Проводится длинной тонкой иглой, которую вводят непосредственно в месте проекции опухоли под контролем УЗИ до контакта с образованием. После получения материала, иглу извлекают.
Этот метод основан на введении радиоизотопного средства — технеция, который способен излучать гамма-волны. Специальное устройство фиксирует, как препарат распространяется в легких, и отображает это на снимках. Даже на ранних стадиях рака можно выявить патологическое скопление технеция в месте новообразования. Чем большая злокачественность клеток, тем значительнее концентрация вещества.
Сцинтиграфию костей успешно применяют для диагностики метастазов в опорно-двигательной системе в случае отсутствия результатов на рентгеновских снимках.
К дополнительным способам диагностики образований в дыхательной системе относится рентгенография. Ее проводят при подозрении на пневмонию, туберкулез или плеврит, но сделав снимок, можно обнаружить опухолевидное образование. Часто случается, что диагностические мероприятия по другом поводу обнаруживают рак на ранних стадиях. УЗИ органов брюшной полости, забрюшинного пространства и лимфатических узлов проводится для обнаружения участков метастазов.
Сканирование с использованием радиоактивных изотопов является простой и наиболее широко распространенной техникой обнаружения опухолевых метастазов. В ряде случаев эта методика бывает весьма неточна, т. е. выдает большой процент некорректных результатов. Это может быть связано, с одной стороны, с недостаточной чувствительностью детектирующих методов (влияет на процент позитивных результатов в опухолевой ткани), а с другой стороны — с низкой специфичностью (влияет на процент негативных результатов в здоровой ткани).
Однако доза получаемой пациентами радиации крайне низка, методика признана безопасной и обладает хорошей воспроизводимостью результатов. Кроме того, она относительно дешева в применении.
Изотопное сканирование наиболее ярко проявляет себя в диагностике скелетных метастазов. Сканирование костной ткани в настоящее время является процедурой, которую наиболее часто проводят в большинстве сервисных клинико-диагностических лабораторий. В сканировании обычно используют фосфоросодержащие соединения, помеченные технецием.
Изотопы быстро накапливаются в костной ткани, причем уровень поглощения зависит от регионального кровоснабжения и скорости образования новых костных тканей. Так как метастазы обычно характеризуются усиленным кровоснабжением и повышенной активностью остеобластов, эти области накапливают изотопные метки более интенсивно, чем здоровые ткани. У данного правила есть и исключения. Например, множественная миелома характеризуется крайне низкой активностью остеокластов.
Так как процесс поглощения изотопов является неспецифическим процессом, множество причин могут вызвать его увеличение. Трещины и переломы ребер, артриты и деформации позвоночника при остеопорозе — все это может вызвать повышенное поглощение изотопной метки и быть ошибочно принято за наличие метастазов у больных раком. Таким образом, наличие единичной области повышенного поглощения изотопа следует интерпретировать с большой осторожностью.
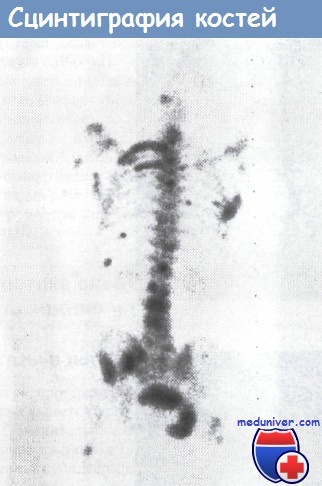
Изотопное сканирование костей скелета обнаруживает многочисленные костные метастазы.
Представлены исследования больного карциномой простаты.
При обнаружении данного факта следует обследовать подозрительную область организма радиографически, а если потребуется, то и с помощью компьютерно-томографических методов. Особенно это касается обнаружения единичных областей повышенного поглощения в позвоночном столбе, так как для него характерна высокая вероятность дегенеративных заболеваний. И все же обнаружение областей повышенного накопления радиоактивной метки у онкологических больных чаще всего бывает связано с возникновением вторичных опухолей, и каждый такой случай нуждается в тщательной проверке.
При обнаружении множества очагов повышенного накопления изотопа почти с уверенностью можно говорить о распространении опухоли. В настоящее время изотопное сканирование костей считается основной диагностической процедурой в определении стадии заболеваемости и проводится у всех больных с первичной карциномой молочной железы.
При диагностике опухолей печени в сканировании используют серный коллоид, меченный 99m Тс. Метастазы детектируются как области пониженного поглощения изотопа. Изотопное сканирование печени является менее точным методом, чем КТ-сканирование, и использование этой методики в последнее время постоянно сокращается.
Для обнаружения отдаленных метастазов при колоректаль-ном раке сейчас используют сцинтиграфию — новую методику с применением следовых количеств меченных монокло-нальных антител. При раке молочной железы и злокачественной меланоме сейчас часто практикуется удаление железы Вирхова как альтернатива стандартной региональной лимфаденоктомии.
При хирургическом удалении железы Вирхова часто отпадает необходимость в чистке подмышечных лимфоузлов — например, у больных раком молочной железы эта операция с вероятностью 95% предотвращает их поражение. Данная методика требует предварительного проведения лимфосцинтиграфии для точной локализации железы и минимализации хирургического вмешательства.
В диагностике опухолей нейроэндокринной системы для точной локализации метастазов можно пометить лекарственные препараты, такие как окситоцин (аналог соматостатина), которые будут специфически связываться с соматостатиновыми рецепторами.
В. Д. Стоногин, А. В. Богданов
Из 2-й кафедры хирургии (заведующий кафедрой профессор Тимофей Павлович Макаренко) Центрального ордена Ленина института усовершенствования врачей (ректор М. Д. Ковригина) на базе Центральной клинической больницы Министерства Путей Сообщения (начальник В. Н. Захарченко), Москва, Россия.
Публикация посвящена памяти Василия Дмитриевича Стоногина (1933-2005).
V. D. Stonogin, A. V. Bogdanov
From the 2-nd faculty of surgery (professor Timofej Pavlovich Makarenko managing faculty) Lenin's Central award of institute of improvement of doctors (rector M.D. Kovrigina) on the basis of the Central clinical hospital of The Ministries of Railways (chief V.N. Zaharchenko), Moscow, Russia.
The publication is devoted to memory of Vasily Dmitrievich Stonogin (1933-2005).
Based on the analysis of 154 scannograms, performed in patients with pulmonary cancer, and comparison of the scanning findings with the results of roentgenological study, angiopneumography, operation and histological findings, it is concluded that radioisotope scanning of the lung is a simple and safe method of investigation of the lung capillary blood flow providing valuable accessory information about disturbances in the pulmonary circulation, that enabled to judge the functional and anatomical operability of a patient.
В исследовании больных с заболеваниями лёгких большое значение имеет изучение малого круга кровообращения и именно периферического отдела его, непосредственно участвующего в газообмене.
До настоящего времени основными методами исследования лёгочного кровообращения являются зондирование сердца и лёгочных сосудов и ангиопульмонография.
Однако, техническая сложность, некоторая опасность для больного, а также наличие ряда противопоказаний ограничивает широкое использование этих методов в клинике. Всё это заставляет искать новые, более простые и безопасные методы исследования лёгочного кровотока. С 1963 года за рубежом, а затем и у нас в стране начала развиваться новая, явно прогрессивная методика изучения лёгочного кровотока -радиоизотопное скеннирование лёгких (1, 2, 5, 6, 7 и др.). Метод основан на временной задержке частиц меченого альбумина в лёгочных артериолах и капиллярах после внутривенного введения препарата. Распре¬деление макроагрегатов в этих сосудах, регистрируемое на скеннограммах, позволяет наглядно и объективно оценивать лёгочное кровообращение сразу во всех отделах обоих лёгких.
Во 2-й хирургической клинике ЦОЛИУв скеннирование лёгких начали применять с 1966г. Широкому клиническому использованию метода предшествовали экспериментальные исследования на собаках (3).
К настоящему времени проведено 532 скеннирования легких, 507 больным с различными заболеваниями лёгких (25 исследованы повторно, после операции).
Среди обследованных у 165 больных был хронический нагноительный процесс в лёгком, у 154 - рак лёгкого, у 122 - туберкулез лёгких, у 32 - тромбоэмболия лёгочной артерии и её ветвей, у 34 - прочие заболевания лёгких (солитарная киста лёгкого, актиномикоз, саркоидоз Бека, пневмосклероз и другие).
Из 154 больных раком лёгкого у 124 рак был центральный, у 28 - периферический, и у 2 - метастаз рака из других органов. Возраст обследованных больных был от 40 до 65 лет, мужчин было 142, женщин - 12.
Методика исследования. За 2-3 дня до исследования больному назначается раствор Люголя по 10-15 капель 2 раза в день. После такой подготовки йод, образующийся в результате распада макроальбумина, будет выделяться почками, почти не накапливаясь в щитовидной железе.
Доза вводимого для исследования макроальбумина составляет 3-4 мк кюри на 1 кг веса исследуемого. Альбумин вводится медленно в течение 3-5 минут. Положение больного в момент введения препарата строго горизонтальное на спине: в таком положении препарат более равномерно распределяется в лёгких (4). Исследование начинается сразу же после введения препарата. Скеннирование производили на скеннере МВ-7101 венгерского производства с коническим коллиматором с диаметром отверстия 12мм, углом диафрагмы 250°. Часть исследований была выполнена на скеннере американского производства (фирмы Nuclear Chicago Corporation).
Положение больного в момент скеннирования на спине. Однако в некоторых случаях, когда очаг поражения расположен в 10-15см от поверхности воспринимающего устройства, целесообразно проводить, исследование в положении больного на животе. Скеннирование лёгких производили при следующих режимах: скорость движения головки счетчика 30 или 10 см/мин, промежутки между строками 3 или 6мм, шкала пересчета А4 или А2, делитель кратности Д7 или Д9, отсечка фона 15-20%. Показатели режима работы скеннера при каждом исследовании несколько меняются, что зависит от физикотехнической характеристики макроальбумина, дозы препарата, вводимой исследуемому, конституциональных особенностей пациента и от предполагаемых изменений в лёгком.
Результаты скеннирования сопоставляли с рентгенологическими (рентгенография, томография, бронхография), с данными общей и селективной ангиопульмонографии, с результатами раздельной бронхоспирометрии.
Из 154 обследованных больных раком лёгких, 86 были оперированы и результаты скеннирования сопоставлены с операционными данными и с результатами гистологического исследования удаленных препаратов.
Нормальная скеннограмма лёгких человека (рис. 1), констатирующая полноценный лёгочный кровоток в лёгочных артериях и капиллярах, представляется в виде плотной и равномерной штриховки, напоминающей контуры лёгких.

Рисунок 1 - Скеннограмма легких в норме. Положение больного в момент скеннирования на спине.
Сердце и крупные сосуды дают зону резкого уменьшения радиоактивности, выявляя очертания средостения. Сцинти¬графическая картина напоминает изображения их на рентгенограммах. При патологическом процессе в лёгком на скеннограмме в области очага поражения наблюдается уменьшение по сравнение со здоровыми участками лёгкого накопления макроальбумина или полное отсутствие его. Причем сцинтиграфическая картина зависит как от характера про¬цесса, так и от его локализации и распространенности.
При обследовании больных раком лёгкого нами было выявлено 4 группы наблюдений.
В первую группу вошли 8 больных периферическим раком, у которых размер опухоли, определяемый рентгенологически, не превышал 2,5-3см в диаметре. На скеннограмму у этих больных зона аваскуляризации или совсем не выявлялась, или была недостаточно четкой. По-видимому, пока это предел метода. По мере совершенствования конструкций скеннеров будет расти и их разрешающая способность.
Во вторую группу вошли 63 больных центральным и периферическим раком легкого, у которых данные скеннографии полностью соответствовали рентгенологическим, т. е. резкое уменьшение радиактивности над сегментарным или долевым ателектазом. Результаты скеннографии у этих больных указывают на выраженное уменьшение артериоло-капиллярного кровотока в зоне гиповентиляции легочной ткани.
Первый пример. Больной Ш., 55 лет поступил в клинику с жалобами на боли в правой половине грудной клетки, сухой кашель, боли в суставах. Рентгенологически (рис. 2а) в верхней доле правого легкого определяется округлое образование с четкими контурами, размером 4*3 см, расположенное субплеврально.
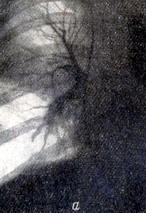


Рисунок 2 - а - ангиопульмонограмма больного Ш. Зона аваскуляризации в области опухоли; б - прямая рентгенограмма грудной клетки того же больного. Тень опухоли в области верхней доли; в - скеннограмма того же больного. Отсутствие радиоактивности над проекцией опухоли.
В анализах мокроты обнаружены раковые клетки. На ангиопульмонограмме (рис. 2б) - зона аваскуляризации соответственно расположению опухоли. Видны множественные культи мелких артериальных сосудов на уровне опухоли. На скеннограмме (рис. 2в) отсутствие накопления изотопа над проекцией расположения опухоли.
Второй пример. Больной К., 56 лет, поступил в клинику 4.V.1968 года с жалобами на боли в левой половине грудной клетки. Болен 2 месяца. Состояние удовлетворительное. Перкуторно - над правым лёгким ясный лёгочный звук, слева - в области проекции верхней доли звук притуплен. Аускультативно - слева над верхней долей дыхание ослаблено. Рентгенологически (рис. 3а) шаровидное образование в верхней доле левого лёгкого с ателектазом всей доли. На скеннограмме (рис. 3б) - отсутствие изотопа над проекцией верхней доли.
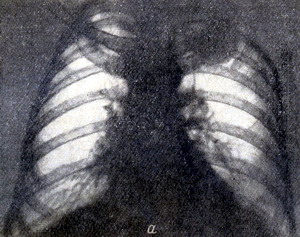

Рисунок 3 - а - прямая рентгенограмма грудной клетки больного К. В области верхней доли шаровидное образование; б - скеннограмма того же больного. Отсутствие радиоактивности над проекцией верхней доли.
22.V.1968 г. больной оперирован. В верхней доле левого лёгкого обнаружена опухоль, локализующаяся в области I и III сегментов, размером 7*7см, расположенная субплеврально. В корне лёгкого увеличенных лимфоузлов нет. Про¬изведено удаление верхней доли. Гистологически: плоскоклеточный рак.
В третью группу вошли 62 больных центральным и периферическим раком легких, у которых по данным сцинтиграфии объем поражения значительно превышал рентгенологически определяемое поражение лёгкого. Так, у больных центральным раком легкого без ателектаза всего лёгкого или частичным ателектазом, но с неполным сдавленней легочной артерии, увеличенными лимфоузлами, как правило, наблюдается резкое, но равномерное снижение накопления изотопа.
Пример. Больной К., 48 лет. В результате обследования в клинике установлен рак верхней доли левого лёгкого. На рентгенограмме тень опухоли в области II сегмента, ателектаз верхней доли слева. На скеннограмме (рис. 4) - значительное снижение, почти полное отсутствие накопления изотопа в левом лёгком.

Рисунок 4 – Скеннограмма больного К. Отсутствие радиоактивности над верхней долей и значительное снижение над нижней долей левого лёгкого.
Больной оперирован. Опухоль диаметром 5см в верхней доле, ателектаз последней, пакет увеличенных, плотных лимфоузлов вокруг лёгочной артерии, интимно с ней связанных и сдавливающих её. Произведена пневмонэктомия с большими техническими трудностями. Через 4 месяца после операции больной умер от метастазов в лимфоузлы средостения.
В четвертую группу (21 больной) вошли больные центральным и периферическим раком лёгкого, у которых данные скеннографии указывали на полное отсутствие артериоло-капиллярного лёгочного кровотока на стороне поражения.
Если при периферическом раке лёгкого отсутствует накопление изотопа над проекцией всего лёгкого, то это говорит о вовлечении в процесс сосудов корня лёгкого за счет метастазов в лимфоузлы корня и о неоперабельности больного.
При отсутствии накопления радиактивного вещества в лёгком и при наличии ателектаза лёгкого говорить о неоперабельности только по данным скеннирования нельзя, поскольку сцинтиграфическое исследование отражает состояние артериоло-капиллярного русла. Известно, что при нарушении вентиляции (при ателектазе) нарушается и капиллярный кровоток. Другими словами, вентиляция и кровоток являются взаимосвязанными процессами, снижение или прекращение вентиляции ведет к уменьшению или прекращению кровотока в артериоло-капиллярном русле лёгкого. Но при центральном раке, если на скеннограмме отсутствует накопление изотопа во всем лёгком, а полного ателектаза пет, можно с уверенностью говорить о вовлечении в процесс легочной артерии и о неоперабельности больного.
Пример. Больной К-ой, 57 лет, поступил в клинику с жалобами на одышку, сухой кашель. Болен 4,5 месяца. Установлен диагноз - рак левого лёгкого. Рентгенологически: в верхней доле левого лёгкого - опухолевое образование (рис. 5а). Гиповентиляция верхней зоны. На скеннограмме (рис. 5в) - отсутствие накопления изотопа в левом лёгком.
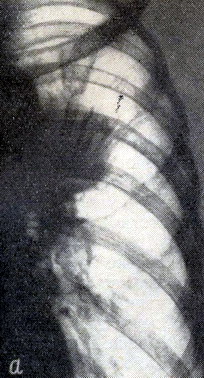
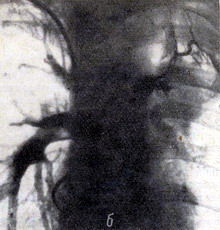

Рисунок 5 - а - прямая рентгенограмма грудной клетки больного К-ой. Тень опухоли в об¬ласти верхней доли; б - ангиопульмонограмма того же больного. Культя левой лёгочной артерии; в - скеннограмма того же больного. Отсутствие накопления изотопа в левом лёгком.
Выраженное несоответствие рентгенологических и сцинтиграфических данных позволило заподозрить вовлечение в опухолевый процесс крупных артериальных стволов. Последующая ангиопульмонография (рис. 5б) подтвердила это предположение: обнаружена культя левой лёгочной артерии.
Таким образом, анализ результатов скеннографии в сопоставлении с данными клинико-инструментальных методов исследования позволяет считать, что скеннирование при раке лёгких дает ценную дополнительную информацию о нарушениях лёгочного кровообращения. Осложнений, связанных с применением метода, мы не наблюдали.
Выводы
- В комплексном обследовании больных раком лёгких радиоизотопное скеннирование позволяет определить состояние лёгочного кровотока в обоих лёгких и таким образом судить о функциональном состоянии всего дыхательного аппарата.
- У больных периферическим раком лёгких без метастазов в лимфоузлы корня результаты скеннирования соответствуют рентгенологическим данным.
- У больных центральной формой рака, а также периферической с наличием метастазов в лимфоузлах корня лёгкого, зона расстройства кровообращения, определяемая с помощью скеннирования, превышает рентгенологически определяемое поражение. Отсутствие накопления изотопа на стороне поражения указывает на вовлечение в процесс крупных артериальных стволов и на неоперабельность больного.
1. В. Л. Маневич, В. К. Модестов, В. С. Афанасьева, В. И. Хроменков, В. В. Галкин. Хирургия, 1968, 4, 35-41.
2. В. И. Стручков, В. Г. Спесивцева, А. В. Григорян, М. П. Рубин, Л. М. Недвецкая, В. В. Прохоров. Сов. мед., 1968, 5, 10-15.
3. В. И. Хроменков. Радиоизотопное скеннирование лёгких в хирургической клинике. Автореф. канд. дисс., М., 1969.
4. Doern F., Wolf К. Brock R., Storek U. Fortschr. Rontgenstr., 1967, 106, 1, 34-42.
5. Tap1in G. W., Jоhnsоn D. E., Dаrе Е. К., Кap1an H. S. JASA Athom., 1964,20-24, 11,3-34.
6. Taplin G.W., Griswold W. G., Johnson D. E. Kaplan H. S., Akcay М. М. G. Nucl., Med., 1964, 382-384.
7. Wagner N. H,, Sobiston D. C, Mc. Abeс G. C, Meger J. K. J. A. M. A., 1964, 187, 8, 601-608.
Data on authors:
Восстановление текста, компьютерная графика - Сергей Васильевич Стоногин.
Любое копирование материала запрещено без письменного разрешения авторов и редактора.
Работа защищена Федеральным законом о защите авторских прав Российской Федерации.
Restoration of the text, computer schedule - Sergey Vasiljevich Stonogin.
Any copying of the material is forbidden without the written sanction of authors and the editor.
Work is protected by the Federal law on protection of copyrights of the Russian Federation.
Томографические исследования на сегодняшний день являются самыми эффективными среди неинвазивных методов исследования. Особенно широко они используются для диагностики онкологических заболеваний.
Термин «,томография», имеет греческое происхождение: «,tomos», означает «,слой»,, «,graphо», – писать. Томографией в медицине называется любой метод диагностики, который позволяет получить послойные изображения структуры человеческого тела.
- Компьютерная томография в диагностике рака легких
- Магнитно-резонансная томография
- Признаки рака легких на КТ и МРТ
Виды томографических исследований при раке легких
В современной онкологии томография является основным диагностическим методом исследования. Томографические исследования проводятся с помощью специальных аппаратов – томографов. В зависимости от принципа, положенного в работу томографа, различают:
- Компьютерную томографию (КТ): спиральную КТ, контрастную КТ (КТ-ангиографиию), мультиспиральную КТ (МСКТ), позитронно-эмиссионную томографию (ПЭТ-КТ).
- Магнитно-резонансную томографию (МРТ).
Все разновидности компьютерной томографии выполняются на специальных аппаратах – компьютерных томографах. Действие компьютерных томографов основано на использовании низкодозового рентгеновского излучения.
Проведение компьютерной томографии дает возможность выполнить серию послойных снимков грудной клетки с заданной толщиной срезов. Обрабатывая полученные снимки, выполненные в разных плоскостях, компьютер может создать трехмерное изображение легких и органов средостения.
Для улучшения визуализации новообразований в легких применяется метод контрастирования (КТ-ангиография). В вену пациента вводят контраст, который быстро с током крови достигает малого круга кровообращения и «,подсвечивает», сосуды легких.
Суть контрастирования при опухолях в том, что новообразования имеют более разветвленную кровеносную систему, чем окружающие ткани, поэтому именно в раковых сосудах контраст будет накапливаться больше всего.
Компьютерная томография легких может выполняться в нескольких режимах:
- пульмональном, когда основными четко определяемыми структурными элементами грудной клетки являются бронхи, междолевые щели, межсегментарные перегородки, сосуды легких,
- средостенном, когда детально визуализируются органы средостения (сердце, верхняя полая вена, аорта, трахея, лимфоузлы).
Для обнаружения новообразований в легких чаще используют пульмональный режим, а при наличии метастазирования этой опухоли – оба.
Мультиспиральная КТ отличается от спиральной тем, что движение источника излучения происходит по нескольким спиралям вокруг томографического стола. Это высокоскоростное сканирование при диагностике рака легких является более информативным, чем обычная КТ, но и более дорогостоящим.
С помощью него можно выявить мельчайшие новообразования в легких, в том числе опухолевые метастазы в лимфоузлах или органах средостения, обнаружить патологические параканкрозные (околоопухолевые) процессы.
Позитронно-эмиссионная компьютерная томография (ПЭТ-КТ) является высокочувствительным методом диагностики раковых опухолей, поскольку помогает изучить молекулярную структуру раковых клеток.
Этот метод КТ основан на визуализации опухолевых клеток и изучении их метаболизма с помощью радиоактивного фармпрепарата , 18-фтордезоксиглюкозы. Срезы, полученные после введения этого препарата, позволяют создать трехмерную модель опухолевого образования и установить его точную локализацию.
Суть работы магнитно-резонансного томографа заключается в улавливании радиоволновых сигналов, которые исходят от всех клеток организма человека. С помощью контейнера томографа происходит отграничение сигналов, идущих от клеток организма, от сигналов, исходящих от объектов окружающей среды.
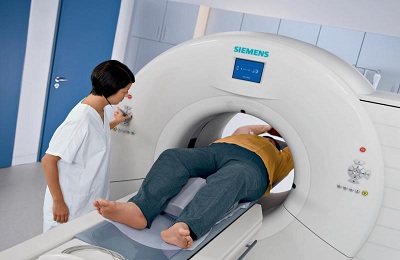
Мощный магнит, входящий в структуру магнитно-резонансного аппарата, создает сильное магнитное поле, которое возбуждает молекулы воды в клетках человеческого организма, принуждая их производить радиоволновые импульсы. Сверхчувствительные датчики воспринимают и особым образом обрабатывают полученные сигналы, преобразуя их в отпечаток среза.
Компьютер накладывает срезы друг на друга, моделируя трехмерное изображение исследуемой области. МРТ позволяет выполнять сканирование срезами от 1 мм в нескольких плоскостях одновременно, что обеспечивает получение снимков высокой четкости.
Преимущества и недостатки. Показания и противопоказания к проведению томографии
Компьютерная и магнитно-резонансная томографии имеют много преимуществ перед другими методами исследования. Эти преимущества позволили внести их в стандартные протоколы диагностики пациентов с подозрением на рак легких и с установленной онкопатологией.
Преимуществами КТ и МРТ при диагностике рака легких являются:
- высокая информативность методов (с их помощью можно обнаружить опухолевые новообразования при их минимальных размерах, что очень важно на ранних стадиях заболевания),
- четкость изображений (послойные изображения имеют высокую четкость, что позволяет рассмотреть мельчайшие детали на снимке, и свести к минимуму вероятность артефактов),
- низкая доза облучения при компьютерной и ее отсутствие при магнитно-резонансной томографии (позволяет проводить несколько процедур за короткий период времени),
![]()
безболезненность исследований (пациент не ощущает боли или другого дискомфорта при проведении процедур, поэтому не требует назначения обезболивающих или успокоительных препаратов),- отсутствие побочных эффектов после проведенного исследования (больные после процедуры не испытывают неприятных ощущений – тошноты, головокружения, болей, поэтому не требует медицинского наблюдения),
- отсутствие специальной подготовки к процедуре (это дает возможность проводить исследование амбулаторно, в любое удобное время, без клизмирования, бритья и других подготовительных манипуляций),
- удобство хранения результатов (на пленке, на бумаге, в электронном виде).
Показаниями к проведению томографического исследования в онкологической практике являются:
- дифференциальная диагностика между неонкологическими и онкологическими патологиями,
- выявление первичной раковой опухоли и ее характеристик,
- обнаружение метастазов,
- определение степени вовлечения окружающих тканей в процесс,
- оценка эффективности проведенного лечения,
- предупреждение рецидивирования патологии.
Томографические диагностические процедуры практически не имеют противопоказаний, поэтому могут назначаться практически всем пациентам. Но небольшой перечень противопоказаний к проведению этих процедур имеется.

Для всех томографических исследований:
- беременность (особенно в первом триместре),
- психические заболевания (в связи с опасностью проявлений клаустрофобии или неадекватного поведения),
- значительная степень ожирения (пациент может физически не поместиться в аппарат).
Для процедуры КТ с контрастированием:
- аллергия на рентгеноконтрастные препараты,
- отягощенный аллергологический анамнез пациента,
- тяжелое состояние больного,
- декомпенсированные хронические заболевания сердечно-сосудистой системы, почек, печени,
- миеломная болезнь,
- тяжелая форма сахарного диабета.
Для процедуры МРТ (заменяют на КТ):
![]()
установленные в теле пациента медицинские приборы, например, кардиостимуляторы,- наличие в организме металлосодержащих несъемных изделий (скоб, клипс, протезов, пуль, осколков).
Большинство из этих противопоказаний являются относительными (кроме наличия металлосодержащих приборов и аллергии), поэтому процедуры при них могут выполняться, но лишь тогда, когда их эффективность значительно превышает риск возникновения побочных эффектов или последствий.
Проведение томографических исследований при карциноме легких
Согласно стандартному протоколу, при подозрении на наличие у больного рака легких проводится спиральная компьютерная томография, которая проводится на вдохе.
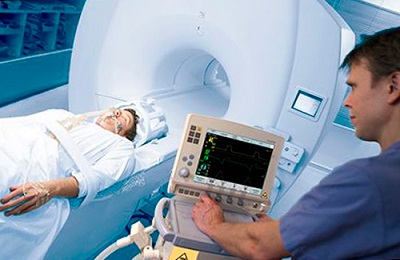
В зависимости от целей КТ:выполняется с разным шагом срезов (коллимацией):
- 5 мм – при подозрении на наличие опухоли в легких,
- 3-5 мм – при подозрении на вовлечение регионарных лимфоузлов и органов средостения,
- 0,5 мм – после установки диагноза для выбора тактики хирургического лечения.
При проведении спиральной КТ также используют разные дозы облучения для определения морфологической структуры опухоли. При этом низкой дозой облучения для мужчин и женщин считается 0,5 и 0,4 мЗв соответственно. При такой лучевой нагрузке и тонких срезах в ткани легкого можно определить узелки.
Тактика дальнейшей диагностики рака легкого после его обнаружения зависит от размера выявленных узлов и степени риска у пациента:
- При размере узелка до 4 мм включительно повторная КТ проводится не ранее, чем через 12 месяцев.
- При размере узлов от 4 до 6 мм: у пациентов с низкой степенью риска – повторная КТ через 12 месяцев, у пациентов с высокой степенью риска – повторная КТ проводится дважды (через 6-12 и 18-24 месяца).
- При размере узлов от 6 до 8 мм: у пациентов с низкой степенью риска , повторная КТ проводится дважды (через 6-12 и 18-24 месяца), у пациентов с высокой степенью риска , повторная КТ проводится дважды (через 3-6 и 6-12 месяцев).
- При размере узлов свыше 8 мм пациентам назначается контрастная КТ, ПЭТ-КТ (позитронно-эмиссионная компьютерная томография) и биопсия.
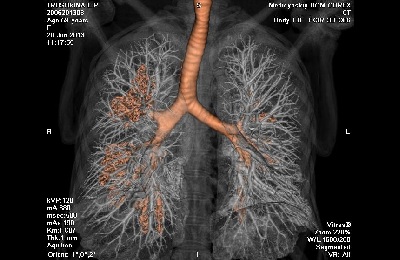
Контрастную КТ применяют для определения границы между опухолевой и неповрежденной тканью для определения тактики терапии и уточнения объема оперативного вмешательства. После введения контраста (Омнипак, Ультравист) происходит его избыточное накопление в опухолевой ткани. При этом на фотографиях срезов хорошо определяются сосуды, питающие опухоль.
Процедура томографического исследования проводится амбулаторно и не требует специальной подготовки пациента.
Обследуемого помещают на томографический стол аппарата, который во время процедуры движется вдоль источников излучения (рентгеновского или магнитного). Длительность исследования зависит от размера исследуемого участка тела и может составлять от 20-30 минут до 1,5 часов. При этом пациент никаких болезненных ощущений не испытывает.
Расшифровка снимков, полученных с помощью компьютерной томографии, осуществляется по разработанным стандартным алгоритмам.
Зная, как выглядит рак легких на КТ, опытные рентгенологи могут установить диагноз рака легкого по имеющимся снимкам.
Картина рака легких зависит от вида опухоли, поскольку для каждого ее вида имеются свои морфологические признаки, определяемые рентгенологически:
-
Аденокарцинома (встречается в 35% случаев рака легких) на снимках определяется в виде узлов округлой или неправильной формы с неоднородной структурой. Чаще всего локализируется в верхних долях легких и имеет дольчатое строение,
Плоскоклеточный рак (около 30% случаев) выглядит как плотный узел с неровными краями, вызывающий непроходимость воздухоносных путей легких, что приводит к обструктивному пневмониту или коллапсу легкого.
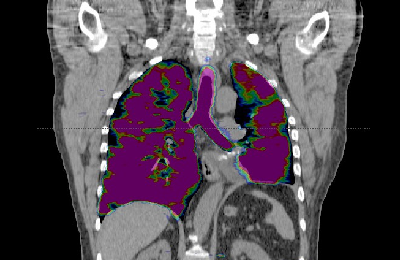
Чаще располагается вблизи корней легкого. Во многих случаях плоскоклеточной карциномы определяется симптом кавитации – образование полости внутри узла, что является признаком распада опухоли,
Признаки опухолевого процесса на снимках МРТ мало чем отличаются от признаков на КТ.
Компьютерная и магнитно-резонансная томографии – эффективные диагностические методы. Они помогают устанавливать диагноз онкологической патологии на самых ранних стадиях заболевания.
Еще пять-десять лет назад пройти процедуру КТ или МРТ было достаточно трудно и очень дорого. Сегодня эти виды диагностики стали намного доступнее. Именно благодаря этому, увеличилась частота выявляемости рака легких на ранних стадиях, а вследствие своевременного лечения – пятилетняя выживаемость пациентов. Чем раньше выявлена раковая патология, тем большей будет результативность проводимого лечения.
Читайте также:


