Радиочастотная термоабляция опухоли поджелудочной
Под радиочастотной абляцией поджелудочной железы подразумевается выпаривание патологического очага при помощи электрического воздействия. При соблюдении всех технологических деталей здоровые ткани не повреждаются. Именно абляция является достаточно популярной и эффективной альтернативой традиционной хирургической методике. Абляция поджелудочной железы применяется в следующих случаях:
• гормональнозависимых опухолях;
• метастатических очагов из раковых образований другой локализации;
• первичной опухоли, при ее небольших размерах;
• паллиативное вмешательство при большом патологическом злокачественном очаге для уменьшения болевого синдрома.
В зависимости от физического фактора, при помощи которого осуществляется абляция, выделяют следующие ее виды: радиочастотная, электропорация, микроволновая и ультразвуковая.
Радиочастотная абляция
В зависимости от физического фактора, при помощи которого осуществляется абляция, выделяют следующие ее виды: радиочастотная, электропорация, микроволновая и ультразвуковая.

В данном случае воздействие осуществляется с помощью радиочастотных волн. Существует транскутанный (чрезкожный) вариант такой абляции и лапароскопический. В первом случае иголкоподобный электрод вводится через небольшой разрез в коже, во втором – необходим оперативный доступ к органу, если подвести электрод не позволяет расположение прилегающих важных органов.
В результате радиочастотного воздействия патологические клетки испаряются и заменяются соединительнотканным рубцом. Данная методика рассматривается как малоинвазивная, применяется в различных случаях: от метастазов до удаления небольшой первичной опухоли поджелудочной железы. Возможно полное и частичное удаление опухолевого образования. Последний вариант применяется при больших размерах патологического очага как паллиативное вмешательство с целью уменьшения болевых ощущений.
Электропорация
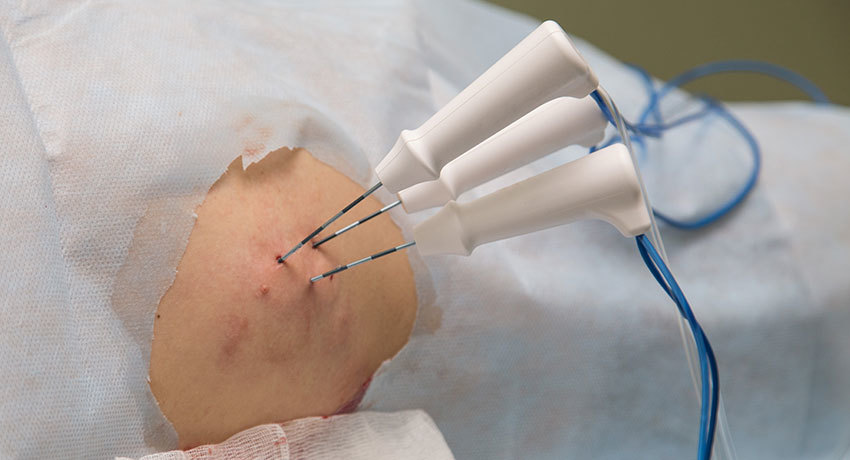
Применяется узконаправленное действие электрического поля большой интенсивности. В условиях общей анальгезии (комбинированный наркоз) 4 тонких иглоподобных электрода вводятся строго в область патологического роста (под контролем УЗИ или данных компьютерной томографии). По электродам подается высоковольтный строго дозированный электрический ток. Возможна повторная операция такой абляции при рецидиве онкологического процесса или метастазировании. Возможно сочетание с другими способами лечения неопластических процессов поджелудочной железы.

Микроволновая термотерапия (HIFU)
Микроволновая термометрия (HIFU) – это один из малоинвазивных видов оперативного вмешательства, который осуществляется с помощью ультразвукового воздействия.
Чем отличается HIFU от обычного ультразвука? Многие доктора хорошо знакомы с диагностическим вариантом ультразвука частотой от 1 до 20 MГц. При HIFU образуется волна с другими параметрами воздействия.
В медицине ультразвуковые волны со специальными характеристиками получают при необходимом изменении напряжения внутри пьезоэлектрического материала, например, такого как цирконат титана. В дальнейшем этот материал передает колебательные движения в необходимом ритме подведенному электроду.
В процессе проведения HIFU ультразвук высокой энергии (механическая волна с частотой выше 16 кГЦ) беспрепятственно проникает через кожные покровы непосредственно в очаг патологического роста. Возникают циклы пониженного и повышенного давления. Именно высокая частота волны позволяет сконцентрировать ее в одной точке, не повреждая здоровые ткани. То есть сфокусированный ультразвук удаляет и разрушает только атипичные раковые клетки, не оказывая никакого воздействия на здоровые клетки поджелудочной железы.
Преимущества микроволновой терапии
• отсутствие лучевой нагрузки позволяет повторять операцию сколько угодно много раз;
• сведен к минимуму риск метастазирования по ходу иглы (электрода), что весьма вероятно при классическом варианте оперативного вмешательства;
• уменьшается вероятность возникновения послеоперационного кровотечения;
• при небольших размерах опухоли удаляется только патологический очаг, а орган сохраняет свои анатомо-функциональные способности;
• послеоперационный период и реабилитация менее продолжительны, чем после классической операции;
• возможность применения как средства паллиативного лечения, например, как разновидность циторедуктивной терапии у пациентов с предполагаемым неблагоприятным исходом болезни.
На сегодняшний день известно лишь очень ограниченное количество онкологический центров, на баpе которых лечения неопластических процессов поджелудочной железы осуществляется с привлечением новейших современных методик. Среди них наиболее перспективны следующие варианты:
• введение в клиническую практику электропорации, криодеструкции, микроволновой термометрии, радиочастотной абляции;
• комбинированная терапия с назначением высокоэффективных химиопрепаратов;
• осуществление лучевой терапии только на современных вариантах линейных ускорителей последнего новейшего поколения с наиболее высоким уровнем безопасности;
• использование различных схем введения химиопрепаратов, в том числе эмболизации, трансартериальной и внутриартериальной методики;
• предпочтение малоинвазивных методик классическому оперативному вмешательству, но при необходимости – возможность использования и этого метода.
Для подбора эффективного метода лечения вы можете обратиться за
- методы инновационной терапии;
- возможности участия в экспериментальной терапии;
- как получить квоту на бесплатное лечение в онкоцентр;
- организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Рак поджелудочной железы можно взять под контроль только с помощью своевременного и радикального уничтожения опухоли. Как правило, это возможно только у 10-15% пациентов на определенной стадии заболевания. Во многих случаях, в качестве альтернативы хирургической операции, в Онкологическом центре MEMORIAL, проводятся различные виды абляций, в том числе Нано-нож абляция (NanoKnife).
Стадия болезни определяет тактику лечения рака поджелудочной железы
Выбор метода лечения рака поджелудочной железы жестко зависит от стадии болезни, на которой обнаружено заболевание. Стадия болезни определяется размерами опухоли и степенью распространения рака за пределы органа.
Опухоль поджелудочной железы, выявленная на ранних стадиях, имеет самые высокие шансы на излечение с помощью хирургических или аблятивных методов. Тем не менее, некоторые виды абляций подходят и пациентам с распространенным раком, поскольку помогают контролировать симптомы опухоли, уменьшают боль и увеличивают продолжительность жизни.
По мнению ведущих специалистов онкологического центра MEMORIAL экзокринный и эндокринный рак поджелудочной железы подлежит радикальному хирургическому лечению или абляции на первых трех стадиях болезни (Т1, Т2, Т3), при условии отсутствия критического распространения опухоли за пределы органа. К сожалению, даже на начальных стадиях болезни до сих пор нет абсолютно достоверного диагностического метода определения уровня метастазирования опухоли в лимфатические узлы.
На стадии выраженного распространения опухоли или отдаленного метастазирования только паллиативное химиотерапевтическое лечение может контролировать симптомы болезни и улучшать качество жизни пациента.
Метод абляции для лечения рака поджелудочной железы и метастазов рака
Наиболее часто аблятивные методы применяются для лечения:
- Нейроэндокринных опухолей поджелудочной железы с местнораспространенным характером роста
- Отдаленных метастазов рака поджелудочной железы в печени
- Первичных очагов или метастазов экзокринного рака поджелудочной железы, если они единичны и имеют небольшие размеры
- Крупных опухолевых очагов в поджелудочной железе, в этом случае абляция полностью не ликвидирует опухоль, но эффективно снижает боль
Виды абляций для лечения рака в Онкологическом центре МЕМОРИАЛ
Это малоинвазивный метод лечения патологических раковых очагов. Иголкообразный электрод вводится в ткань опухоли, по нему подаются радиочастотные волны, под влиянием которых ткань опухоли нагревается и разрушается. На месте разрушенных тканей через несколько месяцев образуется рубец.
Радиочастотная абляция обычно используется с целью полного или частичного разрушения опухоли. В некоторых случаях она является альтернативой оперативному вмешательству. Данный метод иногда применяют для паллиативной терапии рака при тяжелом неоперабельном состоянии пациента, а также при особых локализациях опухоли, например, рядом с жизненно-важными структурами или кровеносными сосудами. Радиочастотную абляцию можно сочетать с другими методами лечения рака. Радиочастотная абляция может проводиться и во время операции в качестве дополнительного метода уничтожения метастатических очагов или разрушения опухоли.
Радиочастотная абляция применяется в нескольких формах:
- Транскутанная радиочастотная абляция, когда зонд-электрод вводится в опухоль через кожу, этот способ абляции сегодня наиболее распространен.
- Лапароскопическая радиочастотная абляция, когда электрод подводится к опухоли лапароскопическим путем, через небольшой разрез. Этот вариант лечения применяется при труднодоступной локализации опухолей в брюшной полости.
Эта процедура отличается от радиочастотной абляции только тем, что для нагревания и разрушения опухолевых тканей используются микроволны. Метод микроволновой термотерапии не является методом излечения рака, а служит для временного облегчения симптомов ракового заболевания. Применение этого метода диктуется необходимостью улучшить качество жизни пациента, не прибегая при этом к обширным хирургическим вмешательствам.
Суть метода криотерапии заключается в заморозке опухоли с помощью очень низких температур. В ткань опухоли вводятся несколько тонких полых электродов в виде игл, которые затем заполняются жидким азотом или углекислотой. Под влиянием очень низких температур содержимое раковых клеток превращается в лед и разрушается, что называется криодеструкцией.
С помощью криотерапии можно лечить не только первичные опухолевые очаги в поджелудочной железе, но и костные метастазы рака. Метод криотерапии также используется для паллиативного лечения болевого синдрома. Криотерапия проводится с помощью лапароскопической техники или транскутанно (через кожу передней брюшной стенки) под контролем УЗИ.
Это метод необратимого и целенаправленного разрушения раковых клеток при помощи сильных локализованных электрических полей. Процедура проводится под общим наркозом в специальной операционной, оснащенной лечебной и диагностической аппаратурой.
В края раковой опухоли, под контролем УЗИ и компьютерной томографии, прицельно вводятся четыре тонкоигольных электрода. Затем с помощью аппарата NanoKnife® происходит строго дозированное воздействие высоковольтного электрического тока (3000 Вольт) и разрушение опухоли.
Процедура лечения рака поджелудочной железы Нано-Ножом на сегодняшний день считается одним из самых эффективных способов разрушения опухоли, если она проводится опытными и квалифицированными специалистами. Исключительно важно то, что процедуру лечения Нано-ножом можно проводить повторно и при рецидивах рака, и при отдаленных метастазах, а также в случае неоперабельного рака.
МЕМОРИАЛ – специализированный онкологический центр для лечения рака поджелудочной железы
Во всем в мире найдется не так уж много квалифицированных онкологических клиник, где для лечения рака поджелудочной железы успешно и безопасно используются все новейшие методы современной медицины, в том числе:
- Новейшие комбинированные прототоколы химиотерапии с применением высокоэффективных, оригинальных химиопрепаратов
- Лечение рака с помощью абляций: радиочастотная абляция, микроволновая термотерапия, криодеструкция
- Нано-нож электропорация
- Эмболизация и внутриартериальная химиотерапия, в том числе трансартериальная химиоэмболизация
- SIRT-терапия (селективная внутренняя радиационная терапия)
- Лучевая терапия, модифицированная по интенсивности, на современных и безопасных линейных ускорителях последнего поколения
- Хирургические операции любой категории сложности, в том числе с использованием малоинвазивной лапароскопической техники
В онкологической клинике МЕМОРИАЛ собрана команда опытных и компетентных специалистов по всем видам лечения, которые применяются при раке поджелудочной железы. Консультируют пациентов и определяют тактику лечения рака ведущие онкологи, специалисты мирового уровня.
- Онкология
- Онкологические центры
- Все для лечения рака
- Онкологический центр, Анталия
- Детская онкология
- Страничка главного онколога
- Что мы лечим, заболевания
- Центр онкогематологии
- Центр гематологии и онкогематологии
- Пересадка костного мозга
- Онкологический диагноз
- Как правильно понимать онкологический диагноз
- Проверьте Ваш диагноз
- Актуальные методы лечения
- Актуальные методы лечения рака
- Чрескожная абляция
- Химиоэмболизация
- Химиотерапия
- Химиотерапия в MEMORIAL
- Рекомендации для пациентов
- Метастазы
- Метастазы и рецидив рака
- Метастазы в кости
- Метастазы в печень
- Разное
- Нано-Нож
- Робот Да Винчи
- Паллиативное лечение
- ПЭТ / КТ сканирование
- Урология
- Робот Да Винчи
- Робот Да Винчи в клинике MEMORIAL
- Роботизированные операции
- Часто задаваемые вопросы
- Рак предстательной железы
- Лечение и диагностика рака предстательной железы
- Cкрининг предстательной железы
- Методы лечения
- Факторы риска
- Разное
- Роботизированная хирургия в лечении рака почки
- Лечение рака мочевого пузыря
- Аденома простаты
- Кардиология
- Радиочастотная абляция
- Аорто-коронарное шунтирование
- Трансплантология
- Пересадка печени
- Пересадка почек
- Пересадка волос
- Бесплатная индивидуальная консультация
- Наша клиника пересадки волос
- Как происходит пересадка волос
- Цены на пересадку волос
- Как выбрать клинику для пересадки
- Наш опыт пересадки волос
- Отзывы наших пациентов
- Жизнь после пересадки волос
- Правда и вымысел о пересадке волос
- Пересадка волос и PRP-терапия
- Другое
- Лечение бесплодия и ЭКО
- Офтальмология
- Гинекология
- Ортопедия и травматология
- Хирургия позвоночника
- Пластическая хирургия
- Лечение ожирения
- Лечение гепатитов
- Check-up
- Пересадка волос
- Наши Контакты
- Лейкозы
- Лечение лейкозов
- Рак предстательной железы
- Робот Да Винчи
- Рак мочевого пузыря
- Роботизированная хирургия
- Рак поджелудочной железы
- Ранняя диагностика рака поджелудочной железы
- Методы лечения рака поджелудочной железы
- Интервенционная радиология
- Лучевая терапия (радиотерапия)
- Питание при раке поджелудочной железы
- Рак яичников, шейки матки
- Рак желудка
- Рак желудка: подробнее о болезни
- Рак легких
- Рак легких: важная информация о болезни
- Опухоли головного и спинного мозга
- Рак молочной железы

В марте 2002 года клиника MEMORIAL Шишли стала первым в Турции и 21-м в мире медицинским учреждением, получившим аккредитационный сертификат качества JCI (Joint Commission International)
Радиочастотная аблация (РЧА) - метод местного воздействия на опухоль с помощью высокой температуры, создаваемой высокочастотными радиоволнами.
Для лечения рака с помощью радиочастотной аблации в центр опухолевой ткани вводят электрод, через который подают ток высокой частоты, вызывающий усиленные колебательные движения ионов и освобождение энергии в виде тепла. Вследствие сильного нагрева ткани опухолевые клетки гибнут, образуя вокруг стержня зону некроза, то есть мертвой ткани. Сначала воздействуют на центр опухолевого узла, затем выжигают его края. Клетки опухоли начинают погибать при температуре 50°С, но их нагревают обычно до 80-110°с, чтобы вызвать полную гибель раковых клеток. Затем мертвая ткань постепенно рассасывается - поглощается плазматическими клетками, и на месте опухоли образуется рубцовая ткань.
Современная аппаратура позволяет точно дозировать воздействие на опухоль и направлять ток так, чтобы не повредить здоровую ткань. Процедуру проводят под контролем УЗИ или компьютерного томографа.
Согласно статистике, число рецидивов рака после радиочастотной аблации не превышает 10%, это ниже, чем после хирургического удаления опухоли (20-30%).
Для проведения процедуры применяют следующие доступы к опухоли:
- чрескожный - тонкий зонд вводят путем пункции или через небольшой надрез кожи;
- эндоскопический – при раке гортани, эндобронхиальном раке легких, раке пищевода, раке желудка, колоректальном раке, раке мочевого пузыря, раке шейки матки;
- лапароскопический – при раке печени, поджелудочной железы, простаты, матки, яичников;
- хирургический – как дополнительное воздействие во время операции при любой локализации рака.
РЧА применяют при небольших единичных опухолях или метастазах в следующих органах:
- печени
- почках
- лёгких
- надпочечниках
- простаты
- костной системы.
Широко используют радиочастотную аблацию при неоперабельных опухолях, или когда больному по состоянию здоровья противопоказана хирургическая операция или химиотерапевтическое лечение.
РЧА эффективна при локализации рака на слизистых оболочках полых органов в начальной стадии.
- Крупные опухоли (более 7 см)
- Расположение опухоли вблизи крупных сосудов
- Опухоль, занимающая более половину органа
- Нарушения свертываемости крови, острые или генерализованные инфекции
РЧА более щадящий метод по общему воздействию на организм, чем операция или химиотерапия. Тем не менее, и аблация имеет недостатки, это:
- формирование абсцесса в месте некроза опухоли;
- образование гематомы;
- образование желчных свищей при воздействии на печень
- повреждение полостной системы в почках
- повреждение соседних органов и тканей.
Чтобы избежать осложнений, проводить радиочастотную аблацию нужно после точного определения расположения опухоли и под строгим контролем УЗИ, КТГ или МРТ в условиях специализированного онкоцентра.
Метод РЧА активно применяется для лечения рака последние несколько лет и уже успел завоевать свою достойную нишу, потому что:
- в большинстве случаев выполняется посредством пункции, не требует разрезов
- для ее проведения не нужен интубационный наркоз, обычно это кратковременная внутривенная или регионарная анестезия
- меньше времени вмешательства, чем при операции
- короче реабилитационный период и болевой синдром
- рецидивы опухоли после местного воздействия РЧА возникают в 2-3 раза реже, чем после хирургического удаления
- стоимость РЧА ниже, чем оперативного лечения.
Посредством небольших разрезов в брюшной стенке либо при операции на брюшной полости в центр опухоли вводят зонд с электродами в форме зубцов. Местное нагревание приводит к расплавлению ткани, расположенной вокруг зонда. Процедура занимает около 10–15 минут. Весь ход процедуры РЧА контролируют с помощью ультразвукового сканирования. В идеале радиочастотную аблацию следует применять при опухолях размером менее 3 см. При более крупных опухолях может потребоваться более одного сеанса.
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
Применение радиочастотной абляции для лечения нарушений ритма сердца началось только в годах. Первые же публикации относительно объема коагулируемой ткани в печени относятся к началу годов ХХ века.
В годах опубликованы и другие экспериментальные данные о применении радиочастотной абляции печени. В середине годов ХХ века появились первые сообщения о паллиативном лечении метастатического поражения печени с использованием радиочастотной абляции. А вскоре и лечения опухолей легких и почек.
В настоящее время в России не более 10 центров, занимающихся проблемой лечения метастатического рака печени. В основном они располагаются в крупных городах, областных центрах с сильной медицинской школой — Москве, , Новосибирске, Томске. Таким образом, потребность в данной высокотехнологичной медицинской помощи удовлетворяется не более чем на 15%. Другой проблемой, сдерживающей развитие данной методики, является дороговизна аппаратного обеспечения. Так, стоимость одноразового набора для радиочастотной абляции составляет до 1000 долларов США, стоимость одного сеанса криоабляции может составлять до 5000 долларов США.
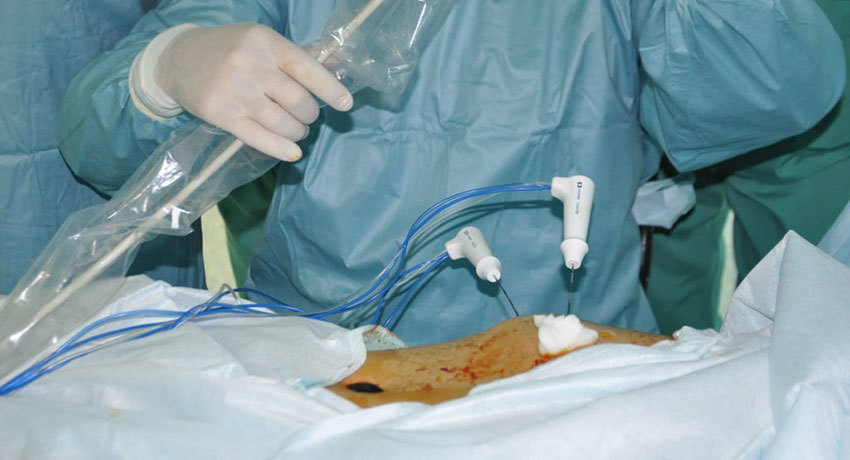
Методика термоабляции новообразований (физические основы абляции тканей)
Основным элементом электрохирургической системы является электрогенератор. Высокочастотный ток передается на электроды. Аппарат нагревает прилегающие к электроду мягкие ткани высокочастотным током специальной формы. В процессе разогрева с периодичностью 2 мс контролируется импеданс тканей. Высокочастотный ток может подаваться однократно или циклически в течение заданного времени. При однократной подаче высокочастотный ток разогревает прилегающие к электроду ткани до температуры (95–110 С) и в момент полного высушивания тканей подача тока автоматически прекращается. При циклической подаче аппарат в течение установленного времени повторяет следующие циклы: подача высокочастотного тока до разогрева (95–110 С) и полного высушивания тканей, выдержка паузы для увлажнения (уменьшения импеданса), возобновление подачи высокочастотного тока. Циклический процесс подачи тока, разогрева и высушивания, повторяющийся многократно, позволяет поддерживать высокую температуру в зоне абляции длительное время и достигать большого объёма коагулированной ткани.
Форма и объём зоны абляции зависят от выбранного электрода и режима работы. Зона абляции делится на три области по степени поражения ткани:
- ближе к электроду расположена область высушивания (дессикации) мягких тканей;
- далее располагается область коагуляции мягких тканей;
- область девитализации располагается вокруг зоны коагуляции.
При увеличении длительности (экспозиции) процедуры абляции общая зона абляции растёт незначительно, однако область дессикации увеличивается.
Показания и противопоказания
Абляцию опухолей применяют в тех случаях, когда невозможно выполнить радикальное оперативное лечение. Это может быть неоперабельность первичной опухоли или сопутствующая патология, которая делает невозможным выполнение радикальной операции в силу её объема и тяжести, но не препятствует выполнению абляции.
Согласно национальным рекомендациям, имеются следующие показания и противопоказания к радиочастотной абляции опухолей печени:
При чрескожном доступе:
- Предшествующее радикальное хирургическое лечение первичной опухоли;
- Отсутствие внепеченочных проявлений заболевания (при колоректальных метастазах);
- Наличие в печени 5 и менее опухолевых узлов (при метастазах нейроэндокринного рака допускается большее количество узлов);
- Диаметр узлов не более 5 см каждый (допустимо подвергать воздействию узлы исходно большего диаметра, но регрессировавшие в объеме под воздействием химиотерапии и других методов лечения);
- Остаточная опухоль после ранее проведенной РЧА либо другого метода лечения;
- Местный рецидив после ранее проведенной РЧА, резекции печени либо другого метода лечения;
- Метахронные метастазы после ранее проведенной РЧА, резекции печени либо другого метода лечения.
Показания к проведению РЧА лапароскопическим доступом:
- Отсутствие выраженных сращений;
- Отсутствие стандартных противопоказаний для всех лапароскопических вмешательств;
- Расположение очага в зонах, доступных лапароскопии;
- Подкапсульное расположение с возможным прилежанием к органам, которые в ходе вмешательства возможно отведением обезопасить от термического воздействия;
- При билобарном поражении печени наличие единичных небольших (до 5 см) узлов в правой доле, в то время как образование левой доли может быть удалено лапароскопически.
Показания к проведению РЧА в ходе открытого вмешательства:
- Билобарное поражение, при котором возможно удалить большую часть пораженной печени и подвергнуть РЧА остающиеся очаги;
- Прилежание к органам брюшной полости и забрюшинного пространства, магистральным сосудам и диафрагме, когда возможно отделение (резекция) этих участков;
- Заранее планируемое сочетанное вмешательство;
- Выраженные сращения, процесс в брюшной полости, особенно после ранее произведенных операциях на печени, когда патологический очаг расположен непосредственно по краю резекции;
- Наличие кроме внутрипеченочного еще и экстраорганного, но удалимого опухолевого узла; общее операбельное состояние пациента; согласие больного на выполнение данного вида лечения.
Противопоказания к проведению РЧА:
Показания к проведению радиочастотной абляции опухолей легких (по Herrera L.J. et al.):
- Больные НМКРЛст., не подлежащие хирургическому лечению по следующим причинам: сопутствующие заболевания, отказ пациента от хирургического лечения.
- Больные, имеющие несколько метастазов в разных долях легких.
- Рецидив опухоли менее чем через 6 месяцев после резекции легкого.
- Диаметр опухоли до 4 см.
- Согласие больного на проведение лечения.
Противопоказания к проведению гипертермической абляции опухолей печени (по et al.):
- Расположение опухоли ближе 3 см от прикорневых структур.
- Первичная опухоль не удалена.
- Более 3 метастазов в каждом легком.
- Общее количество метастазов более 5.
- Имеется метастатический плеврит.
Показания к абляции первичного рака почки:
- Пациентов с тяжелой сопутствующей патологией, либо отказавшихся от хирургического лечения.
- Наличие опухолевого узла до 5 см в диаметре (лучшие результаты при РЧА экзофитно расположенных опухолей до 3 см в диаметре).
- Опухоль единственной почки.
Выполнение РЧА чрескожным или лапароскопическим доступом требует соблюдения ряда условий:
При чрескожном доступе:
- Четкая визуализация патологических очагов при УЗИ и КТ/МРТ (в зависимости от способа навигации);
- Возможность достаточно безопасного доступа к опухолевому узлу (достаточная отдаленность от магистральных печеночных сосудов и желчных протоков);
- Отсутствие прорастания (тесного контакта) диафрагмы, почки, желудка, кишки, желчного пузыря;
- Невозможность выполнения оперативного вмешательства в силу соматического состояния;
- Полная обеспеченность возможности экстренной лапаротомии и адекватности традиционного вмешательства;
- Согласие больного на выполнение данного вида лечения;
При лапароскопическом доступе:
- возможность обеспечения достаточно полноценного со стороны брюшной полости;
- полная обеспеченность возможности экстренной лапаротомии и адекватности традиционного вмешательства;
- согласие больного на выполнение данного вида лечения.
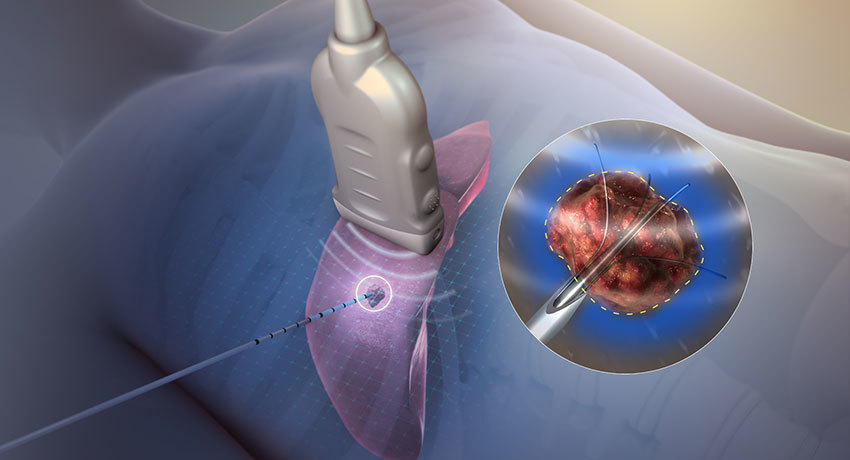
Используемое оборудование и инструментарий
В настоящее время на рынке имеется множество приспособлений для выполнения радиочастотной абляции тканей. Пожалуй, наиболее известным является аппарат Radionics ® Ablation System и набор водоохлаждаемых электродов RITA ® Medical Systems (Angiodynamics, США).
Эта система комплектуется тремя моделями многозубцовых электродов:
Доступы для проведения процедуры абляции
На сегодняшний день нет единого мнения о выборе доступа для проведения абляции. Для позиционирования электрода используется чреcкожный доступ под УЗИ, КТ- или . И интраоперационные доступы при лапаротомии под УЗИ наведением и чреcкожный доступ под контролем лапароскопии.
Методики РЧА
Наиболее часто прибегают к чреcкожным методам позиционирования электрода. В качестве метода контроля над движением электрода наиболее часто используется ультразвуковая навигация.
Преимущества ультразвуковых методов заключаются в простоте проведения процедуры, отсутствии вредных воздействий на пациента в виде лучевой нагрузки, контроль над происходящими процессами в реальном времени, возможность визуализации сосудистых структур органа, а также наличие направляющих адаптеров на рукоятке ультразвукового датчика.
При выборе направления движения электрода необходимо учитывать расстояние от кожи до места проведения абляции, наличие на пути электрода полых органов, таких как кишка, желудок, желчный пузырь, крупных сосудов, синусов плевры.
Также необходимо учесть угол, под которым будет осуществляться ультразвуковой контроль, дыхательную экскурсию, что особенно важно при поддиафрагмальном расположении опухолевых узлов. Немаловажным является и расположение опухолевых узлов относительно правой или левой долей печени. Так, при расположении опухоли в левой доли печени наиболее целесообразным будет выбор эпигастральной области в качестве места проведения электрода.
При локализации опухолевого узла в правых сегментах печени более целесообразным представляется установка электродов в межреберьях. В этих случаях необходима четкая визуализация расположения плеврального синуса.
В целом выбор области для проведения чрескожной абляции аналогичен таковому при проведении пункционных биопсий очаговых образований печени.
В ряде случаев выполнение абляции под ультразвуковым наведением может оказаться затруднительным или даже невозможным. Это может быть связано с изоэхогенной структурой опухоли, когда выполнить её четкую визуализацию не представляется возможным, наличием выраженной гиперэхогенной зоны при неоднократном проведении процедуры абляции, а также наличием костей или заполненных газами полых органов на предполагаемом пути установки электрода. В таких случаях для позиционирования электрода можно воспользоваться компьютерной томографией.
Выделяются 5 этапов абляции:
- Планирование;
- Прицеливание;
- Мониторинг;
- Контроль эффективности;
- Оценка эффективности.
Сначала определяют точку введения электрода путем размещения пациента на столе в наиболее удобном для доступа к опухоли положении, установки стола на уровне среза, выбранного для доступа, и маркировки точки введения электрода.
После установки электрода и его продвижения производят контроль его положения путем последовательного сканирования, при этом дистальная тень позволяет контролировать положение кончика электрода.
В тех случаях, когда опухоль не визуализируется ни при УЗИ, ни при КТ без контрастного усиления, можно выполнить предварительную жировую эмболизацию.
Преимуществом МРТ перед КТ является отсутствие ионизирующего излучения, хорошая контрастность мягких тканей, возможность мультипланарной реконструкции, возможность отображать функциональность и температуру ткани.
Лапаротомия или торакотомия, которые выполняют для проведения абляции, имеют ряд преимуществ по сравнению с чрескожными методами. К ним относятся возможность интраоперационной ревизии органов, выполнение ИОУЗИ печени, уточнение распространения опухоли, стадии онкологического процесса, выявления необнаруженных на дооперационном этапе отсевов опухоли.
Кроме того, возможно выполнить освобождение предполагаемой области вмешательства от прилегающих петель кишки, выполнить абляцию на участках, прилегающих к желчному пузырю, куполу диафрагмы, сосудам.
Читайте также:





