Противоопухолевые препараты при лейкозах

Противоопухолевые препараты пугают онкологических пациентов непредсказуемостью позитивного и частого негативного действия. Большинство пациентов предпочло бы остановиться на хирургическом лечении или облучении, но эти строго локальные методы не всегда технически возможны. На все опухолевые очаги системно удается воздействовать только лекарственными препаратами, поскольку они проникают всюду, где есть кровь вне зависимости от способа введения.
- Что такое противоопухолевые препараты и как они работают?
- Классификация и виды противоопухолевых средств
- Алкилирующие средства
- Противоопухолевые препараты растительного происхождения
- Противораковые препараты нового поколения
- Препараты на гормональной основе
- Побочные явления
Что такое противоопухолевые препараты и как они работают?
Все убивающие злокачественные клетки препараты можно называть противоопухолевыми, не смотря на существенную разнородность лекарственных молекул и механизм повреждающего действия. Большинство противоопухолевых препаратов влияет на деление клеток, нарушая структуру их ДНК или веретена, помогающего развести хромосомы в образующиеся дочерние клетки. Вероятно, цитостатики повреждают не только геном, лучше всего изучено их действие образование сшивок между частями одной нити ДНК и двумя параллельными нитями, заплетенными в спираль. У клетки есть способы для восстановления малого повреждения генетического аппарата, но при существенном нарушении она вынуждена уйти в сторону апоптоза — смерти.
Клеточные популяции в опухолевом узле очень разнородны: какие-то клетки только собираются делиться, другие уже вошли в процесс и активно синтезируют две копии структур для дочерней клеточки, некоторые находятся в покое, а часть после завершения жизненной программы устремилась к гибели. Считается, что находящиеся в состоянии покоя клеточные популяции устойчивы к агрессии противоопухолевых лекарств, зато делящиеся и планирующие войти в эту фазу — самые чувствительные к химиопрепаратам. Делящиеся клетки составляют фракцию опухолевого роста, чем она крупнее, тем агрессивнее рак и одновременно более чувствителен к противоопухолевому воздействию.
Классификация и виды противоопухолевых средств
Противоопухолевые лекарства представлены химиотерапевтическими препаратами, то есть цитостатиками, эндокринными или гормональными средствами, таргетными препаратами. Все они различаются механизмом инициации клеточной смерти.
Цитостатики используются с 1946 года и представлены несколькими группами лекарственных средств:
- алкилирущие получили свое название от химической реакции, реализующей ведущий механизм повреждения — алкилирование, то есть замену атома водорода нуклеиновых кислот нитей ДНК на алкильную группу лекарства с образованием связок и деформацией структуры;
- антиметаболиты прекращают жизнедеятельность клетки, вмешиваясь в её метаболизм и подменяя собой структурные компоненты нуклеиновых оснований ДНК и РНК или блокируя участвующие в синтезе этих оснований ферменты;
- противоопухолевые антибиотики тоже формируют ДНК-сшивки, а традиционное для антибактериальных препаратов противовоспалительное и противомикробное действие у них практически равно нулю;
- препараты растительного происхождения очень разнородны, преимущественный механизм действия — нарушение клеточного деления, общее у них одно — их выделили из растительного сырья, а позже стали синтезировать химическим способом, удешевляя и облегчая процесс производства;
- различные препараты невозможно было отнести к четырём основным группам ни по одному объединяющему критерию.
Алкилирующие средства
Это самые первые противораковые лекарства, начавшие историю химиотерапии. Ярчайшие представители группы — циклофосфамид, нитрозометилмочевина и производные платины.
Алкилирование противоопухолевыми агентами ДНК приводит к разрывам её цепи и сшиванию с закрученной в параллельную спираль второй нитью, образуемые сшивки не хаотичны — в определенном месте и с конкретным нуклеотидом. В конечном итоге предотвращается репликация, то есть сборка второго комплекта структур для разделения клетки. Принципиально алкилирование возможно в любую фазу клеточного цикла, но особенно активно осуществляется во время синтеза.
Препараты этой группы обладают широким противоопухолевым спектром, используются в терапии рака, в том числе сарком и онкогематологических процессов.
Циклофосфамид, более привычное торговое наименование циклофосфан, применяется более 60 лет в качестве компонента полихимиотерапии, в одиночку используется при злокачественных заболеваниях крови и лимфатической ткани. Вводится разными способами: в таблетках, внутривенно и внутримышечно. Для местного применения бесполезен, потому что активируется исключительно в ткани печени, куда попадает с кровью.
Редкая особенность препарата ифосфамида — наличие антидота уромитексана, защищающего слизистую мочевого пузыря от повреждений.
Первое производное платины — цисплатин было синтезировано в середине XIX века, а в клинику пришло в последней четверти прошлого века. Препарат легко проникает в клетки, потому что его молекула не заряжена ни положительно, ни отрицательно, чем и обусловлена его высокая агрессивность в отношении множества злокачественных процессов. Сегодня применяются уже три поколения платиновых производных, при неизменно высокой активности существенно различаются побочные эффекты.
Препараты нитрозометилмочевины преимущественно используются при злокачественных новообразованиях ЦНС и в онкогематологии.
Противоопухолевые препараты растительного происхождения
Вещества растительного происхождения представлены несколькими группами:
- винкаалкалоиды выделены из растения барвинок, у всех четырёх лекарственных средств идентичный механизм противоопухолевого действия — нарушение белка тубулина и вследствие этого остановка клеточного митоза;
- таксаны немногочисленны, первоначально был выделен из коры тихоокеанского тисового кустарника паклитаксел, а через 15 лет уже из игл европейского тиса добыли доцетаксел, сегодня таксаны наполовину синтетические, кроме высокой эффективности они стали первенцами среди слишком дорогих химиопрепаратов;
- камптотецины добывают из южно-китайского ниссового кустарника, препарат нарушает фермент топоизомеразу, не позволяя раскрутиться суперспирали ДНК, сегодняшние полусинтетические аналоги камптотецина топотекан используются при опухолях ЦНС, иринотекан незаменим в схемах химиотерапии карцином толстой кишки, легкого и яичников;
- эпиподофиллотоксины — полусинтетические аналоги смолы из корней американской мадрагоры и самый яркий представитель подгруппы — этопозид оказался эффективнее природного аналога.
Противораковые препараты нового поколения

Иммуноонкологические средства способствуют восстановлению естественной иммунной защиты организма, подавленной злокачественной опухолью. Средства отличаются от стандартных иммунных препаратов, аналогом которых были вырабатываемые организмом цитокины — интерферон и интерлейкин. Лекарства, как и таргетные, создаются целенаправленно на основе фундаментальных достижений науки. Иммунотерапия сдвинула с мертвой точки лечение меланомы, устойчивой к цитостатикам, мало чувствительный рак легкого и желудка, почечноклеточную карциному и рак печени.
Препараты на гормональной основе
Эндокринная терапия призвана снизить выработку половых гормонов или не допустить их внутрь опухолевой клетки, дабы исключить стимуляцию роста чувствительного к уровню гормонов злокачественного процесса.
Классификация эндокринных препаратов по механизму действия:
- центральные, подавляющие выработку гормонов гипофиза, регулирующих синтез эндокринных веществ половыми клетками, и главные представители группы — агонисты ЛГРГ;
- периферические — снижают функцию половых желез или нарушают в жировой ткани работу фермента ароматазы, отвечающего за трансформацию тестостерона в эстроген — группа ингибиторов ароматазы;
- клеточные — связывающиеся на мембране с рецептором и не пропускающие гормоны внутрь клетки и по своей сути антигормоны, как антиэстроген тамоксифен.
Применяются гормональные противоопухолевые лекарства при карциномах молочной и предстательной железы, а также некоторых вариантах рака тела матки, несущие на своей клеточной поверхности специальные рецепторы гормонов. Как правило, лечение рассчитано на несколько лет, поскольку реализация противоопухолевого эффекта очень медленная.
Побочные явления
Точка приложения противоопухолевых препаратов — клетка, причём не только опухолевая, но и нормальная, поэтому при противоопухолевой терапии закономерны осложнения. Спектр побочных эффектов каждого препарата изучен, но токсические проявления у отдельного пациента строго индивидуальны и непредсказуемы по интенсивности.
Даже препараты одной подгруппы при общем механизме действия имеют разные точки приложения, к примеру, очень небольшие отличия в строении алкалоидов барвинка винкристин и винбластин обернулись существенными различиями в спектре активности и токсичности, их применяют при разных болезнях. Скопированный с натурального растительного винбластина синтетический аналог виндезин, по биологическому действию и осложнениям больше походит на винкристин. Структурно схожий с природными винкаалкалоидами и полностью синтетический винорелбин по спектру действия и токсичности совсем не походит на натуральные аналоги.
Противоопухолевые лекарства не гарантируют 100% результата, раковые клетки уникальны в способности самовосстановления и скорости воспроизводства популяции.
Искусство химиотерапии — это не только умелый подбор оптимальной комбинации, обещающей максимально возможный результат, но и минимизация программных осложнений лекарственного лечения. В нашей Клинике не только помогают каждому пациенту легче перенести химиотерапию, но заблаговременно по индивидуальной программе, учитывающей все особенности организма, готовят к курсу лечения.
Противоопухолевые антибиотики — фармакологическая группа, объединяющая противоопухолевые препараты-антибиотики с противоопухолевым действием.

Противоопухолевые антибиотики - применяются почти при всех онкологических заболеваниях, в том числе и гематологического профиля (для лечения острых лейкозов и хронических в стадии бластного криза).
Дактиномицин (актиномицин D) – первый в мире противоопухолевый антибиотик, был синтезирован в 1963 году.
Впоследствии скрининг продуктов жизнедеятельности микроорганизмов привёл к открытию целого ряда высокоэффективных химиотерапевтических противоопухолевых препаратов, являющихся либо продуктами разнообразных почвенных грибов, либо их синтетическими производными.
На сегодняшний день из данной группы препаратов наибольшее практическое значение имеют антрациклины, или антрахиноновые соединения; относящийся к флеомицинам блеомицин; являющийся актиномицином дактиномицин, а также представляющий собой своеобразный антибиотик, обладающий алкилирующим механизмом действия, митомицин.
Антрациклины, средства рубицинового ряда (даунорубицин, идарубицин, доксорубицин, эпирубицин, карубицин и др.) относятся к числу наиболее эффективных противоопухолевых средств. В то же время это одни из наиболее труднопереносимых лекарств, отличающиеся очень высоким уровнем токсичности.
Они способны вызывать гранулоцитопению, анемию, тромбоцитопению, обладают потенциально необратимым кумулятивным дозозависимым кардиотоксическим эффектом, провоцируют тошноту, рвоту, развитие стоматитов, нарушение функции печени, почек, вызывают алопецию (облысение), аллергические реакции и, наконец, приводят к склерозированию вен после многократных внутривенных вливаний.
Особенно опасны они для сердечно-сосудистой системы, становясь причиной возникновения кардиомиопатий, сердечной недостаточности, болей в области сердца, нарушений ритма, снижения артериального давления. В случае тяжёлых нарушений сердечного ритма либо застойной недостаточности, лечение данными препаратами немедленно прекращают.
Действие антрациклинов не избирательное, а системное, то есть действующие высокотоксичные вещества угнетает все быстро делящиеся клетки (в первую очередь это, конечно, клетки опухоли, но так же страдают все нормальные клетки крови, волосы, слизистые оболочки полости рта, желудка и проч.).
Механизм цитотоксического действия антрациклиновых противоопухолевых антибиотиков обусловлен, главным образом, ингибированием выработки нуклеиновых кислот посредством интеркаляции между парами азотистых оснований, нарушением процесса вторичной спирализации дезоксирибонуклеиновой кислоты за счёт взаимодействия с ДНК-топоизомеразой II и связыванием с липидами, входящими в состав клеточных мембран. Всё это обусловливает высокую антимитотическую активность на фоне низкой избирательности действия.
Антрациклины оказывают иммунодепрессивное, а именно – миелосупрессивное влияние и антибактериальный эффект, однако в качестве антимикробных средств они не используются.
На сегодняшний день антрациклиновые антибиотики применяются в лечении многих злокачественных новообразований и, в том числе, при различных гематологических вариантах рака.
Спектр показаний к назначению какого-либо конкретного противоопухолевого антибиотика определяется несколькими параметрами: его химической структурой, фармакокинетическими и фармакодинамическими свойствами, степенью изученности лекарственного средства.

Противовоспалительное дерматотропное лекарственное средство.

Сегодня поговорим об Эритромициновой мази. Что за средство, как действует на организм? Какие имеет показания и противопоказания? Как и в каких дозах используется? Чем можно заменить? Что за мазь и от чего помогает Эритромициновая мазь относится к антибактериальным средствам и оказывает мощное бактериостатическое воздействие на организм. Подробно информирует о препарате эритромициновая мазь инструкция по применению. […]

Регенеративное лекарственное средство. Применение: раны, ожоги, пролежни, язвы. Цена от 111 руб.

Натуральное смягчающее гигиеническое лекарственное средство. Применение: сухая кожа, трещины в сосках, дерматит. Цена от 612 руб. Аналоги:

Негормональное антисептическое противомикробное лекарственное средство.

Негормональное ангиопротекторное противоотечное лекарственное средство.
Противоопухолевые средства – это препараты на основе химических веществ, выпускаемых в разных фармакологических группах для перорального приема, внутривенных и внутримышечных инъекций. В медицинской практике, есть несколько главных типов онкосредств для терапии раковых опухолей.

Лекарства от рака получившие признание в медицине, а частности в онкологии делятся на следующие группы:
- таблетки;
- растворы для внутривенного и внутримышечного введения;
- порошки;
- пероральные субстанции.
Многие противораковые вещества, дают эффект только при определенных новообразованиях, их места нахождения и гистологических особенностей. В некоторых ситуациях лекарства направляют свое действие только на вторичные опухоли (метастазы).
Классификация
Вещества делятся на несколько типов, в зависимости от классификации противоопухолевые препараты они могут быть:
- гормональными;
- алкилирующими агентами;
- антиметаболитами;
- медикаментами природного происхождения.
Алкилирующие препараты препятствуют копированию ДНК раковых клеток. Это происходит за счет подавления выработки элементов на клеточном уровне. Из-за этого новообразование перестает развиваться и погибает.

Химические лекарства от рака имеют хорошие метаболические свойства, но из-за высокой токсичности некоторые группы веществ принято вводить внутривенно. Большинство онкопрепаратов выводятся из организма уже через сутки после применения. Через гематоэнцефалический барьер проникают такие алкилирующие агенты, как производные нитрозомочевины.
Практически все препараты синтетического происхождения вызывают ряд побочных эффектов:
- расстройство желудочно-кишечного тракта (рвота, тошнота, в некоторых случаях диарея);
- влияют на систему кроветворения;
- развиваются парестезии и приступы головокружения.
Антиметаболиты вступают в конкуренцию с метаболитами и приводят к нарушению жизнедеятельности раковых клеток.
Большая часть пациентов предпочитают использовать медикаменты против онкоопухолей на растительной основе. Противораковыми свойствами обладают многие растения: куркума, дерево Гинкго, имбирь, женьшень, расторопша.
Подобная фитотерапия дает результаты только в той ситуации, когда используемые медикаменты достигают значимой для фармакологии активности.

1 Действие противораковых антибиотиков, объясняется активным воздействием растительный алкалоидов, они купируют митоз на стадии метафазы. В результате получается, что антибиотики имеют антимитотическое свойство. Популярными природными антибиотиками является Колхамин (из-за большой токсичности, используют для лечения поверхностного рака в форме мази), Винбластин (используется при гемобластозах и в случае острого лейкоза).
2 Ферменты. Группа данных лекарств используется в случае острого лимфобластном лейкозе. Некоторые виды патологии не способны синтезировать аспарагин, они используют аспарагин, который находится в лимфе и крови.
3 Гормональные противоопухолевые препараты, их синтетические аналоги, а также антигормональные вещества широко используются в онкологии при гормонально-зависимых опухолях. Для гормонотерапии злокачественных опухолей применяют эстрогены, гестагены андрогены и кортикостероиды.
Все противораковые гормональные медикаменты используются при карциномах, в случае некоторых видов раковой опухоли матки. Как правило, терапия длиться несколько лет, поскольку действие лекарственных средств довольно медленное.
Показания к применению
Показаниями для назначения онкопрепаратов являются следующие состояния:
- патологии поверхностного типа с характерной подлежащей хрящевой ткани;
- при рецидивах;
- комплексная терапия базалиомы и болезни Боуэна.

Кроме того, противораковые вещества используются для подавления воспалительного процесса, и замедлить развитие заболевания.
Принцип действия
Все противоопухолевые мази и гели оказывают пагубное влияние на раковые клетки, не затрагивая здоровую часть мягких тканей. Большая часть лекарств купируют дальнейшее развитие раковой опухоли за счет подавления выработки дезоксирибонуклеиновой кислоты.
Побочные эффекты и осложнения
Из-за высокого уровня токсичности противоопухолевых средства, способны вызывать ряд серьезных осложнений. В редких случаях они оказывают неблагоприятное воздействие на здоровую часть клеток пораженного органа.
В результате этого могут появиться следующие побочные эффекты:
- возникновение гиперурикемии;
- тромбоцитопения;
- расстройство желудочно-кишечного тракта;
- развитие дерматитов;
- депрессивные состояния;
- стоматиты.

Из-за осложнений и побочных явлений врачи рекомендуют проходить терапию под строгим контролем врачей-онкологов.
Методы введения
Противоопухолевые средства вводятся внутривенно, перорально, а также в брюшную и плевральную полости.
Лечение поверхностных злокачественных образований подразумевает локальное использование медикаментов.
Помимо этого, были разработаны способы введения противораковых веществ через сосуды, которые снабжают новообразование кровью. Этот метод повышается эффективность лечения, одновременно уменьшая негативное воздействие медикаментов.
Противопоказания
Среди общих противопоказаний к применению отмечают:
- тяжелую кахексию;
- терминальные стадии.
Основные противоопухолевые средства
В перечень главных лекарственных средств против рака входят.
Нужно сказать, что универсальных онкосредств не бывает. Но при этом результат лечения маленького новообразования будет гораздо лучше, чем при терапии крупной опухоли.
Врачи рекомендуют, ежегодно проходит обследование на выявление онкомаркеров в крови, что позволит своевременно выявить заболевания и начать терапию.

Современная стратегия химиотерапии острого лейкоза, разработанная 20—25 лет назад и претерпевшая за это время определенные изменения в плане интенсификации, к сожалению, уже не может принципиально изменить результаты лечения: ни частоты достижения ремиссий, ни долгосрочной выживаемости.
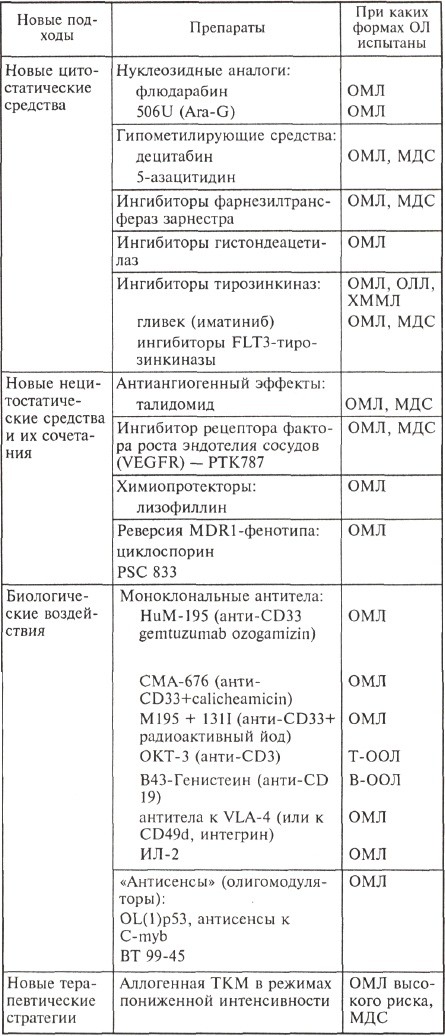
Эффективность стандартной химиотерапии, по-видимому, еще может быть повышена, но в основном благодаря усовершенствованию тактики выхаживания пациентов после цитостатического воздействия. Собственно антилейкемический потенциал самой стратегии химиотерапии уже исчерпан, поэтому все современные исследования в лейкозологии направлены на поиск и внедрение новых, порой не связанных с цитостатическими эффектами способов воздействия на лейкемические клетки. Основные направления этой работы отражены в таблице.
Данные, представленные в таблице, отражают лишь те новые подходы, которые были испытаны в клинических исследованиях I—II и даже III фаз. Безусловно, не перечислены еще многие исследовательские работы, в основном те, которые не вышли из рамок поисковых. К ним относится, например, так называемая вакцинация:
1) введение в организм больного собственных лейкемических клеток (аутологичная клеточная вакцина), в которые с помощью ретровирусов были введены гены определенных молекул (например, В7-1), являющихся мощными костимуляторами Т-клеточного ответа;
2) коммитирование и культивирование, а затем введение в организм больного собственных дендритных (антигенпрезентирующих) клеток, полученных из лейкемических, с целью усиления иммунного ответа на опухолевые антигены.
Традиционным направлением многих исследований является разработка новых противоопухолевых препаратов. Особого внимания заслуживают ингибиторы тирозинкиназ, в частности c-ABL-тирозинкиназа (Гливек). Этот препарат полностью изменил терапевтические подходы в лечении ХМЛ. В программах терапии острого лейкоза его используют в случае обнаружения химерного транскрипта BCR-ABL или t(9;22).
У 30 % больных острым миелоидным лейкозом выявляют мутации гена FLT3, продуктом которого является FLT3-тирозинкиназа. Проведены первые клинические испытания II фазы по применению ингибиторов FLT3 тирозинкиназы.
При использовании молекулы РКС412 были зафиксированы выраженные эффекты у больных с рефрактерным острым миелоидным лейкозом. Так, из 20 больных у одного достигнута полная ремиссия, у 6 отмечено значительное (более чем в 100 раз) уменьшение числа властных клеток в крови, у 7 больных оно составило на 50 % от исходного. Аналогичные эффекты наблюдались и при использовании другого ингибитора FLT3-тирозинкиназы - СЕР-701.
Ингибиторы гистондеацетилаз — это препараты, которые влияют на процесс транскрипции. Создано несколько молекул различных классов: производные бутировой кислоты — ВА (пивалоилоксиметил бутират, бутироилоксиалкиловые эфиры глутаровой и никотиновой кислот, бутироилоксиметиловые эфиры); диэтиловый эфир фосфорной кислоты; субероиланилидгидроксаминовая кислота (SAHA); циннамил гидроксамат LAQ824 и др.
Большинство из этих молекул демонстрирует высокую активность в лабораторных условиях на клеточных линиях острого лейкоза. Клинические исследования проводят лишь с единичными препаратами. Так, применение SAHA у больных с периферическими Т-клеточными лимфомами позволило у 5 из них получить частичную ремиссию, у 5 — стабилизацию. У 25 больных рефрактерным острым миелоидным лейкозом исследование I фазы по применению ингибитора гистондеацитилаз МС-275 было не столь эффективным — получены лишь незначительные гематологические эффекты.
Создается впечатление, что в скором времени из огромного числа синтезируемых ингибиторов гистондеацетилаз будут отобраны наиболее эффективные препараты.
В настоящее время проходят клинические испытания препараты из новой группы лекарственных средств — ингибиторы фарнезилтрансферазы. Основой для разработки использования этих препаратов стали исследования, свидетельствующие об увеличении частоты мутаций онкогена RAS у больных острым миелоидным лейкозом. RAS-протеины являются важным звеном в цепи передачи сигналов внутри клетки и становятся функционально активными после присоединения фарнезильтных остатков с помощью фарнезилтрансферазы.
Результаты первых клинических испытаний препарата типифарниба (R115 777, Зарнестра) свидетельствуют об его определенной активности: общий гематологический эффект отмечен у 37 % больных острым миелоидным лейкозом старше 60 лет.
Нуклеозидные аналоги завоевывают место в программах лечения не только острый миелоидный лейкоз и хронических лимфопролиферативных заболеваний, определенный оптимизм внушает эффективность некоторых из них при остром лимфобластном лейкозе. Так, арабинозилметоксигуанин (Ara-G или 506U), вводимый в дозе 40—50 мг/кг внутривенно 1 раз в день в течение 5 дней, позволил добиться полной ремиссии у 44 % и частичной ремиссии у 32 % больных с рецидивами Т-клеточного острого лимфобластного лейкоза.
Анализ работ по применению гипометилирующих агентов — 5-азацитидина и 5-аза-деоксицитидина (децитабина) — позволяет сделать заключение о более высокой эффективности децитабина. Его применение в дозе 50—75 мг/м2 в виде постоянной инфузии в 1—3-й день позволяет получить полную ремиссию у 30—37 % больных ОМЛ или МДС из группы высокого риска. При использовании децитабина в сочетании с антрациклинами или амсакрином полный ответ отмечен у 35 % больных ОМЛ из группы высокого риска. Следует подчеркнуть, что клинических исследований по изучению этих препаратов еще очень мало, и требуется время, чтобы реально оценить эффективность каждого из них.
Бесспорным является лишь тот факт, что эти средства обладают уникальным механизмом действия: помимо гипометилирующих эффектов (а гиперметилирование ДНК является признаком опухолевой устойчивости и прогрессии), они вызывают клеточную дифференцировку, активируют супрессорные гены и могут in vitro ингибировать пролиферацию клоногенных лейкемических клеток.
Очень интересным направлением в разработке новых противоопухолевых препаратов является создание средств, влияющих на ангиогенез. Талидомид как антиангиогенный препарат давно занял прочное место в лечении множественной миеломы, однако его эффективность при ОЛ и миелодисплазиях незначительна. К новым средствам относятся молекулы, ингибирующие рецепторы ростового фактора эндотелия сосудов (VEGFR). Показано, что ОЛ, при которых бластные клетки экспрессируют VEGFR в больших количествах, отличаются неблагоприятным прогнозом. В испытаниях I фазы исследователи отметили незначительную эффективность ингибитора VEGFR — PTK787 при минимальной токсичности.
Острый лимфобластный лейкоз – это злокачественное неопластическое заболевание крови (лейкемия, рак крови), которое поражает в большей степени детей младшего возраста, особенно мальчиков.
Органами мишенями при лимфобластном лейкозе становятся костный мозг, лимфатические узлы, селезенка и другие органы, так как кровь, которая циркулирует в организме, содержит патологические клетки.
К сожалению, точной причины развития острого лимфобластного лейкоза у детей до сих пор так и не выявлены. На сегодня установлены наиболее распространенные факторы, которые могут спровоцировать развитие заболевания:
- Воздействие радиактивного излучения.
- Инфекционные заболевания.
- Действие различных химических агентов.
- Наследственность.
- Патология хромосом.
Не редки случаи, когда причиной развития лимфобластного лейкоза становилось рентгенологическое обследование будущей мамы, проведенное за год до планирования беременности. То же касается продуктов, которые употребляет в пищу беременная женщина.
Особую группу риска составляют дети, рожденные с генетическими аномалиями, врожденной патологией сердечно – сосудистой системы.
Не исключено развитие лейкоза и у взрослых. У такой возрастной группы заболевание протекает гораздо тяжелее.
Основная опасность лимфобластного лейкоза – это то, что зачастую заболевание проявляет себя уже на поздних стадиях, когда процесс уже неконтролируем и тяжело поддается лечению.
Даже при малейших признаках, таких как, необоснованная слабость, усталость, бледность, кровоточивость стоит немедленно обращаться к врачу. Своевременно проведенная диагностика позволяет на ранних этапах выявить заболевание и начать с ним бороться.
Основным принципом лечения лимфобластного лейкоза является трехступенчатая терапия, которая включает в себя индукцию ремиссии, консолидацию и поддерживающее лечение.
Существует ряд лекарственных средств, без которых не обойтись в лечении лимфобластного лейкоза. Одним из таких средств является Пури – Нетол.
На Пури – Нетол инструкция указывает о том, что лекарственное средство является антиметаболитом на основе меркаптопурина. Именно Пури – Нетол купить рекомендуют врачи для лечения лимфобластного лейкоза. Почему? Ведь в обычных аптеках есть немало препаратов на основе меркаптопурина.
Отличие Пури – Нетола (Германия – страна производитель) прежде всего в том, что производится препарат в Европе по всем необходимым стандартам и под строгим контролем качества. Он отличается высоким качеством очистки молекулы, что дает возможность проходить лечение с применением наиболее качественного, эффективного и менее токсичного препарата, ведь при лейкозе для организма даже малейшее токсическое воздействие может быть губительно.
Организм человека, подверженный лейкемии, гораздо более чувствителен к низкопробным лекарствам, которые помимо относительной, временной пользы приносят массу вреда.
Для препарата Пури – Нетол применение показано для индукции ремиссии при остром лимфобластном и нелимфобластном лекйкозах, остром лейкозе и хроническом миелолейкозе. Согласно данным, которые представлены на Пури – Нетол в инструкции по применению, препарат может использоваться как в виде сочетанного лечения, так и в виде монотерапии.
Еще сравнительно недавно купить Пури – Нетол в Германии было единственной возможностью заполучить средство для лечения лимфобластного лейкоза высокого качества, так как Пури – Нетол купить в аптеках Москвы не представлялось возможным.
Но сейчас все стало гораздо доступнее, несмотря на то, что Пури – Нетол купить в аптеках также достаточно трудно.
Наша интернет аптека максимально старается обеспечить пациентов с различными заболеваниями, в том числе и с лимфобластным лейкозом, наиболее эффективными и качественными лекарствами. Поэтому Пури – Нетол купить в Москве просто – обращайтесь к нам и начинайте лечение самыми лучшими препаратами во всем мире. А на Пури – Нетол цена у нас доступна для каждого покупателя, что сделает не только лечение, а также профилактику заболевания выгодным и недорогим.
Читайте также:



