Классификация опухолей почки по tnm
Рак почки еще называют почечно-клеточным раком. Заболеваемость им в последнее время растет. По степени распространения болезнь находится после рака предстательной железы. По этой причине ее классификации уделяют много внимания. Какие другие виды новообразований, опухоли почек злокачественной природы классифицируются по TNM. Она позволяет наиболее полно отразить диагноз, влияет на дальнейшее лечение и прогноз.
Как осуществляется классификация рака почки по критериям TNM
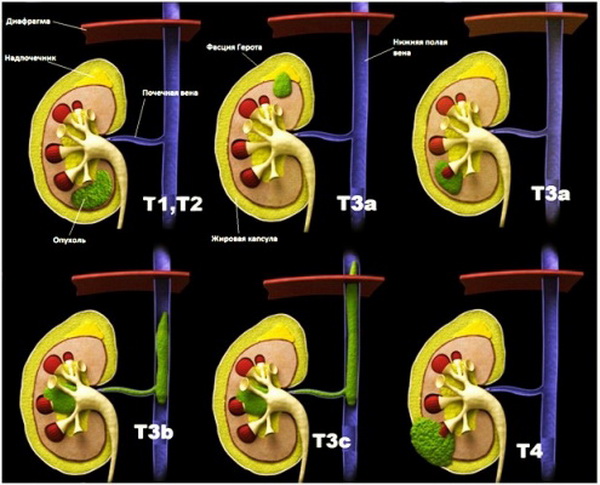
В основе классификации лежат 3 критерия:
Расшифровка первых двух обозначений по оценке первичной опухоли:
- Tx – не поддается оценке.
- T0 – данные о новообразовании отсутствуют.
Обозначение T1 – максимальный размер опухоли не более 7 см, она ограничена пределами почки. Эта категория делится еще на несколько подстадий:
- T1a – диаметр опухоли до 4 см.
- T1b – размеры опухоли достигают 4-7 см.
Подкатегории при необходимости позволяют дополнительно уточнить стадию рака почки по THM.
Обозначение T2 – максимальный размер опухоли превышает 7 см. Новообразование также ограничено пределами почки.
Следующая стадия – T3, при которой обнаруживают распространение первичной опухоли на соседние ткани, крупные вены или надпочечник. Но она все еще остается в пределах фасции Герота. Стадия T3 тоже подразделяется на несколько подстадий:
- T3a. Опухолевые клетки в тканях надпочечника или паранефральной клетчатке в пределах фасции Герота.
- T3b. Новообразование переходит на почечную или достигает нижней полой вены ниже диафрагмы.
- T3c. Опухолевое образование прорастает стенку или достигает нижней полой вены выше диафрагмы.
Обозначение T4 присваивается, если опухолевые клетки появляются уже за пределами фасции Герота. Так называется волокнистая соединительная ткань, в которую заключены почки и надпочечники.
К регионарным лимфоузлам относятся абдоминальные параквальные и параортальные узлы, а также лимфатические узлы ворот почки. Классификация по критерию N не зависит от стороны поражения. Расшифровка обозначений следующая:
- Nx – нельзя оценить состояние регионарных лимфоузлов.
- N0 – отсутствуют метастазы в регионарных лимфоузлах.
- N1 – метастазами поражен только один лимфоузел.
- N2 – метастазирование наблюдается в более чем одном лимфатическом узле.
У 25-40% пациентов с раком почки отмечается распространение опухоли далеко за пределы органа. Чаще всего они появляются в легких, мягких тканях, костных структурах и печени. Еще метастазы могут находиться в надпочечниках, коже и центральной нервной системе.
- M0 – отдаленные метастазы отсутствуют.
- M1 – метастазы в отдаленных органах присутствуют.
В Государственном центре урологии имеют большой практический опыт диагностики и лечения рака почки. Мы оказываем медицинскую помощь в рамках ОМС, поэтому вы можете наблюдаться у нас бесплатно. Для этого необходимо записаться на прием к урологу. Свяжитесь с нами, и мы сможем подобрать для вас удобное время для консультации.

Рак почки или по другому - почечно-клеточным раком. Заболевание представляет собой злокачественную опухоль почки, которая во многих случаях появляется из эпителия проксимальных канальцев нефрона или чашечно-лоханочной системы.
Основные факторы риска
Существует три фактора, которые повышают риск развития рака почки:
- Первый - это мужской пол. Согласно статистике, у мужчин рак почек развивается в три раза чаще, чем у женщин.
- Второй - курение, которое повышает риск развития рака почек в два раза.
- Третье - ожирение. У людей страдающих избыточным весом риск появления рака увеличивается на двадцать процентов.
Клиническая классификация рака почки
Рак почки , как и все другие злокачественные опухоли, классифицируется по системе TNM, согласно клиническим проявлениям. Клиническая классификация больше всего помогает правильно выбрать тактику лечения и определить какой будет прогноз.
Система TNM клинической классификации рака почек
Т - первичная опухоль;
Тх - невозможно оценить первичную опухоль;
Т0 - данных о первичной опухоли нет;
Т1 – первичная опухоль не более 7 см в диаметра, ограниченная почкой;
T1a - опухоль до 4 см в диаметре;
T1b - опухоль 4-7 см в диаметре;
Т2 - опухоль более 7 см в диаметре, ограниченная почкой;
Т3 – означает, что опухоль распространяется на крупные вены, или возможно в надпочечник либо окружающие ткани, но при этом не выходит за пределы фасции Герота;
Т3а – опухоль прорастает надпочечник или паранефральную клетчатку в пределклинической классификации рака почеках фасции Герота;
Т3b - опухоль распространяется на почечную вену или нижнюю полую вену ниже диафрагмы;
Т3с - опухоль распространяется на нижнюю полую вену выше диафрагмы или прорастает в ее стенку;
Т4 - опухоль распространяется за пределы фасции Герота;
N - регионарные лимфатические узлы;
Nх – невозможно определить регионарные лимфатические узлы;
N0 - метастазов в регионарных лимфатические узлах нет;
N1 - метастаз в одном регионарном лимфоузле;
N2 - метастазы более чем в одном регионарном лимфоузле;
М - отдаленные метастазы;
Мх – невозможно определить отдаленные метастазы;
М0 - отдаленных метастазов нет;
М1 - отдаленные метастазы есть.
Помимо классификации TNM есть также классификация Робсона:
- Стадия первая. Опухоль ограничена почкой и не проникает через ее капсулу.
- Стадия вторая. Опухоль проникает через капсулу почки.
- Стадия третья. Опухоль проникает в лимфоузлы или переходит на почечную вену или нижнюю полую вену.
- Стадия четвёртая. Опухоль переходит на соседние с почкой органы (например, поджелудочная железа или кишечник) либо имеют место отдаленные метастазы (например, в легкие).
Гистологическая классификация почечно-клеточного рака
Раньше почечно-клеточный рак классифицировали по типу его клеток, а также по характеру роста. Но было установлено, что рак почки в большинстве случаев смешанный. Современная и новая классификация берёт основу на морфологических, цитогенетических и молекулярных исследованиях. Помимо этого она основывается на иммуногистохимическом анализе и выделяет 5 видов рака:
- светлоклеточный рак почки,
- хромофильный рак почки,
- хромофобный рак почки,
- онкоцитарный рак почки,
- рак из собирательных трубочек.
Классификация
Общепринятой системой стадирования почечно-клеточного рака (ПКР) служит классификация TNM, рекомендованная для использования в клинической и научной работе.
Эта классификация периодически претерпевает изменения с учетом накапливаемых знаний.
Последние изменения были внесены в 2009 г. (табл. 2-4).
Таблица 2-4. Классификация почечно-клеточного рака по системе TNM

Выделение подстадии pT1 более не является предметом дискуссий. Деление опухолей стадии Т2 по размерам было недавно включено в классификацию TNM (2009).
Опухоли с инвазией в клетчатку почечного синуса ранее относили к стадии рТ1. Однако с учетом накопленных данных можно предположить, что при инвазии опухоли в почечный синус прогноз хуже, чем при инвазии в паранефральную жировую клетчатку, следовательно, такие опухоли не нужно включать в группу стадирования рТ1.
Известно, что инвазия опухоли в надпочечник — крайне плохой прогностический признак, такие формы рака почки следует классифицировать как опухоли стадии Т4. В предыдущих версиях классификации TNM в ipynny рТ3b включали опухоли с инвазией как в почечную, так и в нижнюю полую вену.
В результате проведения многочисленных исследований прогностическою значения инвазии в нижнюю полую вену по сравнению с инвазией в почечную вену эти две ipyniibi в последнюю версию классификации TNM включены по отдельности. Точность разделения на N1 и N2 обсуждается. Для определения категории М у больных раком почки необходимо выполнять тщательное дооперационное инструментальное обследование, на сегодня включающее компьютерной томографии (КТ) грудной и брюшной полостей.
Прогностические факторы
К гистологическим факторам относятся степень ядерной дифференцировки по Фурману, подтип ПКР, признаки саркоматоидного характера, инвазия в мелкие сосуды, некроз опухоли и инвазия в собирательную систему. Степень дифференцировки по Фурману является общепринятой системой гистологической классификации в случае рака почки, которая служит независимым прогностическим фактором.
Выделяют три основных гистологических подтипа почечно-клеточного рака: свелоклеточный — 80-90%, папиллярный — 10-15%, хромофобный — 4-5% случаев. Более благоприятный прогноз течения заболевания отмечают у пациентов с хромофобным раком по сравнению с таковым у больных папиллярным или светлоклеточным раком ночки. Однако прогностическое значение различий в гистологическом строении нивелируется при учете стадии опухолевого процесса.
Среди больных папиллярным раком было выделено две прогностически различные труппы: тип I — опухоль с низким злокачественным потенциалом, клетки с хромофильной цитоплазмой, благоприятный прогноз; тип II — опухоль высокого злокачественного потенциала, клетки с эозинофильной цитоплазмой, высокая предрасположенность к метастазированию.
В последние годы были разработаны послеоперационные прогностические системы и номограммы, включающие комбинации независимых прогностических факторов. Наиболее распространенные прогностические системы приведены в табл. 2-5.
Таблица 2-5. Наиболее распространенные прогностические модели для локализованного и метастатического рака почки

Динамическое наблюдение после нефрэктомии, резекции почки или аблятивной терапии почечно-клеточного рака
Динамическое наблюдение, проводимое после хирургического лечения, позволяет оценить функции почек, выявить наличие послеоперационных осложнений, местных рецидивов, развившихся после резекции почки или аблятивного лечения, рецидивов в контралатеральной почке, а также проанализировать возможность появления отдаленных метастазов.
Методам и срокам проведения контрольных обследований посвящено множество публикаций. В настоящее время нет единого мнения о необходимости динамического наблюдения за пациентами после лечения по поводу рака почки, и практически отсутствуют данные о том, что раннее выявление рецидива способствует улучшению выживаемости по сравнению с поздним его обнаружением. Однако послеоперационное наблюдение и контроль важны для того, чтобы увеличить объем знаний о ПКР. и урологи должны проводить его и указывать время, прошедшее с момента окончания лечения до наступления рецидива или развития метастазов.
Оценку послеоперационных осложнений и выделительной функции почек проводят на основании анамнеза, физикального обследования, определения концентрации сывороточного креатинина и EGFR. Осуществление регулярного контроля уровня EGFR в течение длительного времени позволяет увидеть, ухудшились функции почек после оперативного вмешательства или еще до операции.
Функционирование почек и выживаемость без признаков рака можно оптимизировать путем выполнения (по возможности) органосохраняющих операций в случае наличия опухолей стадий Т1 и Т2. Частота развития местных рецидивов невысока и составляет 2,9%, однако важно выявлять их на ранних стадиях, поскольку наиболее эффективным методом лечения в этом случае бывает выполнение циторедуктивных операций. Рецидив в контралатеральной почке также встречается редко (1,2%), риск его развития повышается при наличии опухолевой ткани по краю резекции, мультифокальном росте и высокой степе пи клеточной анаплазии.
Основная цель динамического наблюдения — раннее выявление метастазов. В частности, это важно при проведении абляционной терапии, такой как криотерапия или радиочастотная абляция. Даже несмотря на то что частота возникновения местных рецидивов в данном случае выше, чем при обычном хирургическом вмешательстве, больного все же можно вылечить путем повторной аблативной терапии или нефрэктомии.
Большее распространение опухоли при метастатическом течении заболевания может ограничить возможности хирургического лечения, которое служит стандартом при обнаружении резектабельных, особенно солитарных, метастазов. К тому же осуществление ранней диагностики рецидива, когда масса опухолевой ткани еще невелика, может способствовать повышению эффективности системной терапии, в том числе в рамках клинических исследований.
Интенсивное лучевое обследование не считают необходимым для всех пациентов, К примеру, при выполнении операций по поводу опухолей стадии Т1а и новообразований низких стадий почти всегда достигают хороших результатов. В связи с этим в зависимости от риска рецидивирования и метастазирования целесообразно осуществлять дифференцированный режим наблюдения. Данных рандомизированных исследований пока не существует, но результаты исследований прогностических факторов с большим сроком наблюдения больных уже позволяют сделать некоторые выводы.
При низкой вероятности развития рецидива может быть достаточно выполнения рентгенографии грудной клетки и ультразвукового исследования (УЗИ). Однако рентгенография малочувствительна к небольшим метастазам, а диагностическая ценность УЗИ имеет ограничения.
При наличии среднего или высокого риска возникновения рецидива методом выбора становится КТ органов грудной клетки и брюшной полости, хотя при этом следует учитывать побочное действие облучения, возникающее при проведении повторных КТ-исследований.
В зависимости от наличия новых эффективных методов лечения может потребоваться применение более жестких схем послеоперационного контроля и наблюдения, в частности при известном более высоком риске развития местного рецидива после проведения криотерапии или радиочастотной абляции. Проблемой является определение оптимального срока наблюдения за больным.
Существует мнение, что проведение наблюдения при помощи методов визуализации после 5 лег выживаемости уже нецелесообразно. Однако возникновение поздних метастазов возможно, хотя они с большей вероятностью будут одиночными и для их излечения понадобится более агрессивное лечение. Кроме того, пациенты, у которых опухоль дает рецидив в контралатеральную почку, могут быть излечены посредством выполнения органосохраняющей операции, если обнаруженная опухоль имеет небольшие размеры. Более того, для опухолей диаметром менее 4 см в ходе послеоперационного наблюдения не выявлено разницы в частоте возникновения рецидивов после осуществления нефрэктомии или резекции почки.
Некоторые авторы, в частности, M.W. Kattan, J.S. Lam, B.C. Liebovich и P.l. Karakiewicz, разработали системы баллов и номограммы для количественного определения вероятности возникновения рецидива, метастазов и последующей смерти пациента. Эти системы сравнивались и проходили валидацию. Было предложено несколько режимов осуществления динамического наблюдения в зависимости от стадии заболевания с использованием прогностических переменных, но ни один из них не включал применение абляционных методов лечения.
Разработаны послеоперационные номограммы, позволяющие оценить вероятность достижения безрецидивной 5-летней выживаемости. Совсем недавно была опубликована и прошла валидацию дооперационная прогностическая модель, основанная на возрасте, симптомах и стадировании по TNM. Соответственно для осуществления мониторинга больных почечно-клеточным раком необходимо использование алгоритма динамического наблюдения, в котором учитывался бы не только риск развития рецидива или появления метастазов, но также и эффективность проведенного лечения (табл. 2-7).
Таблица 2-7. Алгоритм динамического наблюдения с учетом профиля риска прогрессирования

Примечание: НЭ — нефрэктомия; РП — резекция почки; РГК — рентгенография грудной клетки; крио — криоабляция; РА — радиочастотная абляция.
Динамическое наблюдение, осуществляемое за пациентами после лечения по поводу рака почки, должно быть основано па факторах риска, выявленных для данного пациента, и типа полученного им лечения. Цель такого наблюдения — обнаружение местного рецидива или метастазирования на той стадии, когда больного еще можно излечить путем выполнения оперативного вмешательства.

Эпидемиология
В последние годы заболеваемость почечно-клеточным раком в большинстве развитых стран возрастает, причём по темпам прироста заболеваемости рак почки уступает только новообразованиям предстательной и щитовидной железы. Так в 2011 году в России рака почки был впервые установлен 19 657 (2,6 % от всех впервые выявленных опухолей различных локализаций), при этом злокачественное новообразование почки было выявлено у 10 872 мужчин и 8 785 женщин. В том же году от рака почки в России умерло 8 561 пациент[3]. Основные факторы риска
Основными факторами риска рака почки являются: Мужской пол (мужчины в 2 раза чаще болеют раком почки), Курение повышает риск в 2 раза и Ожирение, при котором вероятность заболевания увеличивается на 20 %.
Классификация рака почки
Клиническая классификация определяет тактику лечения и оказывает главное влияние прогноз заболевания.
Применительно к почечно-клеточному раку TNM-классификация выглядит следующим образом: Т — первичная опухоль Тх — невозможно оценить первичную опухоль. Т0 — данных о первичной опухоли нет. Т1 — первичная опухоль не более 7 см в наибольшем измерении, ограниченная почкой. 1. T1a — опухоль до 4 см в диаметре. 2. T1b — опухоль 4—7 см в диаметре. Т2 — опухоль более 7 см в наибольшем измерении, ограниченная почкой. Т3 — опухоль распространяется на крупные вены, или в надпочечник либо окружающие ткани, но при этом не выходит за пределы фасции Герота. 1. Т3а — опухоль прорастает надпочечник или паранефральную клетчатку в пределах фасции Герота. 2. Т3b — опухоль распространяется на почечную вену или нижнюю полую вену ниже диафрагмы. 3. Т3с — опухоль распространяется на нижнюю полую вену выше диафрагмы или прорастает в её стенку. Т4 — опухоль распространяется за пределы фасции Герота.
N — регионарные лимфатические узлы Nх — невозможно оценить регионарные лимфатические узлы. N0 — метастазов в регионарных лимфатических узлах нет. N1 — метастаз в одном регионарном лимфоузле. N2 — метастазы более чем в одном регионарном лимфоузле.
М — отдалённые метастазы Мх — невозможно оценить отдалённые метастазы. М0 — отдалённых метастазов нет. М1 — отдалённые метастазы есть.
Кроме классификации TNM, существует также классификация Робсона: Стадия I. Опухоль ограничена почкой и не проникает через её капсулу. Стадия II. Опухоль проникает через капсулу почки. Стадия III. Опухоль проникает в лимфоузлы или переходит на почечную вену или нижнюю полую вену. Стадия IV. Опухоль переходит на соседние с почкой органы (например, на поджелудочную железу или кишечник) либо имеют место отдалённые метастазы (например, в лёгкие).
Метастазирование
Основными путями метастазирования рака почки является гематогенный и лимфогенный. Отдаленные метастазы наблюдаются у 25 % пациентов уже на момент установлки диагноза. Еще у 30-50 % больных метастазы появляются в отдаленный период после лечения. При этом выживаемость составляет от 6 до 12 месяцев и только 10 % переживают 2 года, а 5-летняя выживаемость не превышает 9 %. Частыми локализациями множественных метастазов являются: лёгкие (76 %), лимфатические узлы (64 %), кости (43 %), печень (41 %), ипсилатеральный и контралатеральный надпочечники (19 % и 11,5 %), контралатеральная почка (25 %), головной мозг (11,2 %). Единичные метастазы или метастатическое поражение только одного органа встречается только в 8—11 % случаев.
Тактика лечения метастазов зависит от их распространенности. При солитарных метастазах возможно их удаление (независимо от времени возникновения), что позволяет достичь радикального лечения, а при множественных поражениях чаще возможны лишь малоинвазивные хирургические вмешательства, направленные на улучшении качества жизни пациента.
Гистологическая классификация рака почки
Современная классификация основывается на морфологических, цитогенетических и молекулярных исследованиях, а также иммуногистохимическом анализе. При этом следует учитывать, что разные типы рака по-разному отвечают на различные препараты для химиотерапии, лучевую терапию и т. д.
- светлоклеточный рак почки (около 75 %)
- хромофильный (папиллярный) рак почки
- хромофобный рак почки
- онкоцитарный рак почки
- рак собирательных трубочек
Симптомы рака почки
Следует отметить, что на ранних стадиях рак почки часто проходит безсимптомно (инцидентальные опухоли почек — опухоли, не проявившие себя клинически) и выявляется случайно во время УЗИ или КТ исследования по поводу сопутствующих заболеваний, что наблюдается почти в 60 % случаев выявления рака почки. Основными симптомами рака почки являются появление крови в моче (гематурия) и, как следствие, снижение гемоглобина. Иногда повышение давления крови (вторичная артериальная гипертензия). На более поздних стадиях процесса может появиться боль в поясничной области, пальпируемое образование в проекции почки, а также общие симптомы рака (длительная постоянная потеря веса, постоянная субфебрильная температура, хронически нарастающая слабость)
Диагностика рака почки
Основными методами диагностики рака почки являются:
- Ультразвуковое исследование почек (УЗИ)
- Рентгенологическое исследование с применением контрастирующих препаратов — внутривенная урография
- Компьютерная томография
- Магнитно-резонансная томография (МРТ)
- Главная
- О раке
- О лечении рака
- Личные истории
- Сообщество
- Курсы
- Глоссарий
- Основное
- Документы
- Блоги
- Персоны
- Новости
- Портал
- О нас
- Поддержка и консультации
- Для врачей
- О раке
- О лечении рака
- Личные истории
- Сообщество
- Курсы
- Глоссарий
Морфологическая классификация
В основе традиционных классификаций рака почки лежат особенности морфологии клетки и клеточного ядра. Современные классификации учитывают данные морфологических, цитогенетических и молекулярных исследований и выделяют 5 видов рака почки:
- Светлоклеточный – 60-85%
- Хромофильный (Папиллярный) - 7-14%
- Хромофобный – 4-10%
- Онкоцитарный – 2-5%
- Рак собирательных протоков – 1-2%
О прогностической значимости различных вариантов почечно-клеточного рака будет сказано ниже.
Метастазирование
Рак почки метастазирует гематогенным и лимфогенным путем. Метастазы обнаруживаются у 25% пациентов на момент установления диагноза . Выживаемость данных больных составляет от 6 до 12 месяцев и только 10% переживают 2 года. Приблизительно у 30-50% больных в различные сроки после нефрэктомии появляются метахронные метастазы. Прогноз последней группы несколько лучше, однако, 5-летняя выживаемость не превышает 9%. По данным Saitoh et al. (1982) наиболее частыми локализациями множественных метастазов являются легкие 76%, лимфатические узлы 64%, кости 43%, печень 41%, ипсилатеральный и контралатеральный надпочечник 19% и 11,5%, контралатеральная почка 25%, головной мозг 11.2%. Солитарные метастазы или метастатическое поражение только одного органа имеет место только в 8-11% случаев.
Говоря о течении метастатической болезни при раке почки, нельзя не упомянуть о случаях спонтанной регрессии и стабилизации. Спонтанная регрессия отмечается у 0,4%-0,8% больных раком почки. Это касается в подавляющем большинстве случаев регрессии легочных метастазов. Стабилизация болезни, определяемая, как отсутствие роста и появления новых метастазов, наблюдается у 20-30% больных. С такой же частотой отмечается стабилизация болезни (отсутствие роста первичной опухоли) у больных раком почки без метастазов. Этот феномен должен учитываться при решении вопроса о хирургическом или системном лечении больных с высоким риском, которые в действительности, могут прожить дольше без всякого лечения.
Классификация рака почки
Почечно-клеточный рак характеризуется весьма вариабельным клиническим течением, что обусловлено генетической гетерогенностью и морфологическим разнообразием данной группы опухолей.
В настоящее время в России, как и во многих странах, используется классификация, предложенная Международным противораковым союзом ((UICC) tumor, node, metastasis (TNM)), подробно освещающая степень распространенности опухолевого процесса с целью определения лечебной тактики.
TNM клиническая классификация почечно-клеточного рака (2002)
Т - первичная опухоль
ТХ - первичная опухоль не может быть оценена
Т0 - нет данных о первичной опухоли
Т1 - опухоль не более 7 см в наибольшем измерении, ограниченная почкой
- T1a - опухоль до 4 см
- T1b - опухоль 4-7 см
Т2 - опухоль более 7 см в наибольшем измерении, ограниченная почкой
Т3 - опухоль распространяется в крупные вены, или инвазирует надпочечник, или окружающие ткани, но не выходит за пределы фасции Герота
- Т3а - опухолевая инвазия надпочечника или паранефральной клетчатки впределах фасции Герота
- Т3b - опухоль распространяется в почечную вену или нижнюю полую вену ниже диафрагмы
- Т3с - опухоль распространяется в нижнюю полую вену выше диафрагмы или инвазирует ее стенку.
Т4 - Опухоль распространяется за пределы фасции Герота
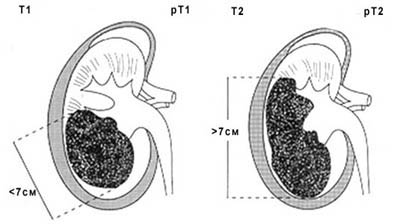
Рисунок 1. Схематическое изображение стадий Т1 и Т2
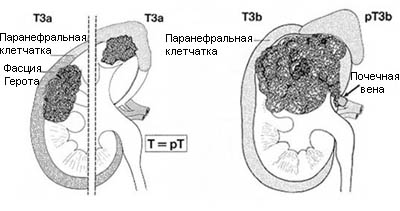
Рисунок 2. Схематическое изображение стадий Т3а и Т3b
N - регионарные лимфатические узлы
NX - регионарные лимфатические узлы не могут быть оценены
N0 - нет метастазов в регионарных лимфатические узлах
N1 - метастаз в одном регионарном лимфатическом узле
N2 - метастазы более чем в одном регионарном лимфатическом узле
М - отдаленные метастазы
МХ - отдаленные метастазы не могут быть оценены
М0 - нет отдаленных метастазов
М1 - отдаленные метастазы
pTNM - патологоанатомическая классификация
pT, pN и pM категории соответствуют T, N и М категориям
G - гистопаталогическая градация
GX - степень дифференцировки не может быть оценена
G1 - высоко дифференцированная опухоль
G2 - умеренно дифференцированная опухоль
G3-4 - низко дифференцированная/недифференцированная опухоль
Группировка по стадиям
Стадия I
Cтадия II
Стадия III
Стадия IV
Факторы прогноза
Клинические факторы
Одним из важнейших направлений современной онкоурологии является выделение факторов, позволяющих составить индивидуальный прогноз и определить оптимальную тактику лечения больных раком почки.
По данным ряда авторов прогностически неблагоприятным являются: тяжелое общее состояние больного, наличие клинических симптомов заболевания на момент установления диагноза, снижение массы тела более чем на 10%. Напротив, возраст, пол и национальность не влияют на прогноз. В ряде исследований продемонстрировано достоверное неблагоприятное влияние на выживаемость увеличения скорости оседания эритроцитов (СОЭ), гаптоглобулина, ферритина, С-реактивного белка, орозомукоида, ?-1-антитрипсина, интерлейкина-6.
У больных диссеминированным почечно-клеточным раком прогностическое значение имеют анемия, гиперкалиемия, гипоальбуминемия и повышение уровня щелочной фосфатазы сыворотки крови.
Показано влияние на исход заболевания таких факторов, как хромогранин А, нейронспецифическая энолаза (NSE), раковый антиген 125 (СА-125), опухоль-ассоциированный ингибитор трипсина (TATI) и эритропоэтин. В настоящее время проводятся исследования, посвященные изучению генетических маркеров в крови и моче, которые могут позволить составить индивидуальный прогноз больных раком почки.
Патоморфологические факторы
Стадия опухолевого процесса (Т), отражающая анатомическую распространенность новообразования, является наиболее значимым фактором прогноза при раке почки. Пациенты с опухолью, ограниченной почкой, имеют лучший прогноз. Инвазия за пределы капсулы Герота (T3a) уменьшает выживаемость на 27%, наличие опухолевого тромбоза почечной и нижней полой вен (T3b-c) – на 40% (таблица 1, рисунок 3).
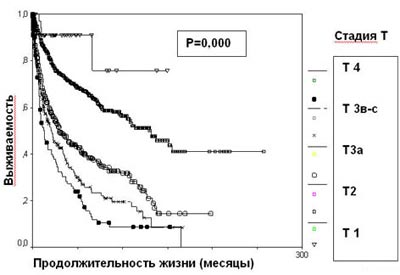
Рисунок 3. Выживаемость 2507 больных раком почки в зависимости от стадии Т
Стадия T
5-летняя выживаемость (%)
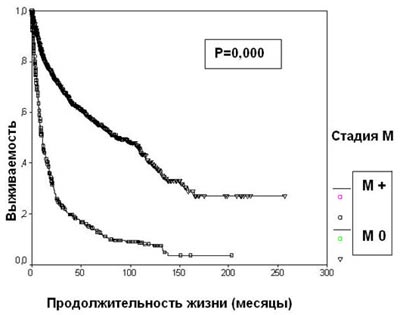
Рисунок 4. Выживаемость 2507 больных раком почки в зависимости от стадии N
Появление отдаленных метастазов резко ухудшает прогноз при раке почки. 5-летняя выживаемость больных диссеминированным раком почки составляет 14,6%, что достоверно меньше, чем в группе пациентов с локализованной опухолью (57,3%) (р=0,0000) (рисунок 5). При наличии отдаленных метастазов стадия Т почечно-клеточного рака прогностического значения не имеет.
Большая продолжительность жизни при диссеминированном почечно-клеточном раке наблюдается при метахронном появлении метастазов и солитарных опухолевых очагах, локализующихся в одном органе. Одним из наиболее важных прогностических факторов является возможность радикального удаления всех определяемых метастазов.
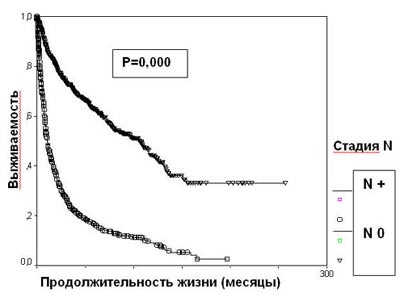
Рисунок 5. Выживаемость 2507 больных раком почки в зависимости от стадии М
Гистопатоморфологические признаки
Большинство современных гистологических классификаций принимает во внимание морфологические признаки клеточного ядра, которые являются независимыми факторами прогноза, занимающими второе место по значимости после стадии заболевания. 5-летняя выживаемость пациентов с опухолями GI составляет 76%, GII – 72%, GIII – 51%, GIV – 35%.
Плоидность ДНК коррелирует с целлюлярной кинетикой почечно-клеточного рака: в диплоидных опухолях отмечается более низкий уровень фракции клеток, находящихся в S-фазе, а также более продолжительное время удвоения опухоли, чем в анеуплоидных клонах, что ассоциировано с благоприятным прогнозом .
На выживаемость больных раком почки влияет митотический индекс. Выявлено, что при наличии менее 1 фигуры митоза на 10 полей зрения при малом увеличении 10-летняя выживаемость составляет 67%, более 1 – 16%.
Генетические факторы
Как было отмечено выше, современные классификации рака почки учитывают не только морфологические, но и цитогенетические особенности опухоли, обуславливающие различное клиническое течение.
Традиционный (не папиллярный) рак составляет 75% всех эпителиальных опухолей почки и характеризуется наличием делеции хромосомы 3р. Только в опухолях данного типа имеет место мутация гена VHL. Данный тип рака почки имеет более высокий метастатический потенциал и отличается худшей выживаемостью по сравнению с папиллярной и хромофобной формами.
При папиллярной форме рака почки обычно выявляется комбинация трисомий по 7,17,3q,8,12,16 и 20 хромосомам, а также утрата Y хромосомы. Папиллярная карцинома часто бывает двухсторонней и мультифокальной, ассоциирована с лучшей выживаемостью, чем традиционный, но худшей, чем хромофобный тип опухоли (рисунок 6).
Для хромофобного рака характерно уменьшение количества хромосом в сочетании с гетерозиготностью по хромосомам 1,2,6,10,13,17,21,X и гипоплоидным содержанием ДНК. Данная форма почечно-клеточного рака имеет низкий метастатический потенциал. Выживаемость больных хромофобными опухолями больше, чем в группе пациентов с папиллярной и традиционной формами рака почки.
Рак собирательных протоков является редкой опухолью, составляющей 1%-2% всех случаев почечно-клеточного рака. Рак собирательных протоков является очень агрессивной опухолью с высоким метастатическим потенциалом.
Таким образом, генетические альтерации детерминируют туморогенез и степень злокачественности опухолевого процесса при различных формах почечно-клеточного рака.
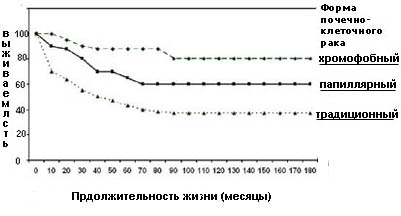
Рисунок 6. Выживаемость больных в зависимости от формы почечно-клеточного рака
Факторы регуляции клеточного цикла
В ряде исследований отмечено прогностическое значение изменений, происходящих в системе регуляции клеточного цикла в процессе развития опухоли. Система регуляции клеточного цикла представлена протеинами, такими как циклины, циклин-зависимые киназы (CDK), CDK-ингибиторы и специфические фосфорилированные и нефосфорилированные субстраты. Белки-регуляторы клеточного цикла являются продуктами экспрессии протоонкогенов. Трансформация протоонкогена в онкоген является одной из ключевых аберраций туморогенеза, приводящей к нарушению регуляции клеточного цикла, обуславливающему повреждение механизмов контроля за клеточным ростом, пролиферацией и апоптозом.
Факторы ангиогенеза
Ангиогенез является важнейшим фактором, определяющим прогрессию опухоли и оказывающим существенное влияние на прогноз больных почечно-клеточным раком. Увеличение новообразования более чем на 1 мм требует появления новых сосудов. Существенную роль в туморогенезе играет сосудистый эндотелиальный фактор роста (VEGF). В настоящее время проводятся исследования, посвященные изучению прогностической роли других факторов (фактора некроза опухоли (TNF-?), основного фактора роста фибробластов (bFGF)) и ингибиторов ангиогенеза (ангиостатина, фактора некроза опухоли (TNF-?)).
Клинические проявления рака почки
Классическая триада симптомов, описываемая ранее при раке почки у 15% больных (боль, макрогематурия и пальпируемая опухоль), в настоящее время встречается редко. В большинстве случаев заболевание протекает бессимптомно.
Клинические проявления возникают в основном при поздних стадиях. Среди местных симптомов наиболее часто отмечаются боль и гематурия. Боли в пояснице и животе возникают при инвазии или компрессии растущей опухолью окружающих структур, а также при почечной колике, обусловленной окклюзией мочеточников сгустками крови. Острая боль может быть следствием кровоизлияния в опухоль или ее разрыва с формированием забрюшинной гематомы. Прощупываемая опухоль – третий местный симптом рака почки, бывает положительным у 12-15% на момент установления диагноза. Появление варикоцеле отмечают до 3.3% больных .
Артериальная гипертензия - непостоянный симптом, (вызываемый сдавлением сегментарных артерий, окклюзией мочеточника, метастазами в головной мозг, формированием артерио-венозных шунтов, или повышенной секрецией опухолью ренина) наблюдается у 15% больных раком почки.
Синдром сдавления нижней полой вены (НПВ) (отеки ног, варикоцеле, расширение подкожных вен живота, тромбоз глубоких вен нижних конечностей, протеинурия) развивается у 50% больных при опухолевом тромбозе НПВ или при компрессии НПВ опухолью и увеличенными лимфатическими узлами.
Рак почки характеризуется большим разнообразием паранеопластических синдромов, наблюдаемых более чем у половины больных. Одной из функций нормальной почечной паренхимы является продукция различных биологически активных веществ (эритропоэтин, ренин, простагландины, простациклины, тромбоксаны, образование активной формы витамина D). Наличие опухоли может приводить к повышенной секреции вышеуказанных субстанций, либо к продукции других гормонов, таких как паратгормон, инсулин, глюкагон, человеческий хорионический гонадотропин. В результате у пациентов может отмечаться артериальная гипертензия, эритроцитоз, гиперкальциемия, гипертермия и др. Появление вышеуказанных симптомов может быть единственным проявлением заболевания и должно настораживать врача в отношении возможного опухолевого поражения почек. После радикального удаления опухоли паранеопластические проявления, как правило, исчезают, но могут возникнуть вновь при развитии местного рецидива или отдаленных метастазов. Таким образом, последние могут быть использованы для мониторинга заболевания.
Редкой формой паранеопластического синдрома является амилоидоз (1.7%). Сохраняющий после нефрэктомии амилоидоз является крайне неблагоприятным фактором прогноза.
До сих пор непонятным остается возникновение в ряде случаев печеночной недостаточности при отсутствии ее метастатического поражения. При этом у больных раком почки отмечается гипоальбуминемия, повышение щелочной фосфатазы, лейкопения, лихорадка, возможно появление очагов некроза печеночной паренхимы (синдром Штафера). Восстановление функции печени после нефрэктомии является благоприятным прогностическим признаком.
Особенное место в клинической картине рака почки занимают симптомы, обусловленные метастазированием, так как более 25% больных имеют отдаленные метастазы на момент установления диагноза. Первым проявлением поражения легких являются кашель и кровохарканье. Костные метастазы могут манифестировать болевым синдромом, развитием патологических переломов, компрессией спинного мозга, появлением пальпируемой опухоли. Поражение головного мозга сопровождается быстрым появлением и нарастанием неврологической симптоматики. Множественные метастазы в печень могут проявляться желтухой.
Такие общие симптомы, как анемия, высокая СОЭ, потеря аппетита, похудание, слабость являются признаками поздних стадий.
Читайте также:

