Пролиферативный рак молочной железы
Здесь речь пойдет о трудностях дифференциального диагноза между протоковым раком in situ и протоковым пролиферативным фиброаденоматозом. Но сначала нужно условиться о том, что следует понимать под названием протокового рака in situ. Казалось бы, этот термин пояснений не требует. Но эта ясность обманчива. Во-первых, то, что называют в практике протоковым раком, далеко не всегда им является в действительности.
Дело в том, что концевые отделы молочной железы, преобразовавшись в раковые, в состоянии достигать размеров среднего или даже крупного протока.
Каждый раз производить окраску на эластику и выискивать существующие или отсутствующие следы стенки предсуществовавшего протока в ежедневной работе лаборатории вряд ли возможно.
Поэтому понятие о протоковом раке стало суммарным — этим термином патологоанатомы обозначают и истинно протоковые раки, и альвеолярные, но достигшие удивительно крупных размеров.
Второе замечание еще более существенно. Имея дело с внутрипротоковым раком без видимого инвазивного роста, никогда нельзя быть уверенным в том, что это действительно рак in situ. Отсутствие инвазивного роста в изучаемых препаратах еще не гарантирует от того, что инвазивного роста нет и в других участках молочной железы.
Скорее наоборот — чем больше изготовлять срезов, тем больше шансов найти участки инвазии. Иными словами, всякий протоковый рак in situ подозрителен на рак инвазивный.
Внутрипротоковые пролифераты, как и любые другие, нельзя изучать без учета всей гистологической обстановки в данной молочной железе. Вряд ли существуют случаи изолированного поражения протоков как раком, так и фиброаденоматозом.
Естественно, что при наличии фокусов инвазивного роста уже не приходится ломать себе голову над определением биологической сущности процесса. Но иначе обстоит дело, если фон представлен той или другой формой фиброаденоматоза.
Выше, при описании лобулярного рака in situ и долькового пролиферативного фиброаденоматоза, уже обращалось внимание на поразительное сходство гистоархитектоники того и другого; дифференциальный диагноз основывался на цитологических, а не гистологических особенностях. Все это можно повторить и относительно протокового рака in situ и протокового пролиферативного фиброаденоматоза.
Сходство может оказаться настолько далеко идущим, что при рассматривании препаратов под малым увеличением дифференциальный диагноз нередко оказывается невозможным, тем более на замороженных срезах. В самом деле, дисгормональные внутрипротоковые пролифераты могут быть солидными, криброзными, сосочковыми, спицеобразными, и все эти гистологические структуры могут повторяться в ином, раковом качестве. Остановлюсь на всех этих вариантах подробнее.
На фоне спокойного фиброаденоматоза с его фиброзной основой, содержащей включения жировой ткани, кисты различных размеров, выстланные бледным или темным эпителием, дольки в состоянии расцвета или атрофии, виден среднего калибра проток, просвет которого нацело закупорен солидной эпителиальной пробкой.
Молочная железа

Внутрипротоковый эпителиальный пролиферат. Дисгормональная
гиперплазия? Рак? (Х200).
Это солидное гнездо — дисгормональной или раковой природы? Такой вопрос возникает перед исследователем часто.
Ориентироваться приходится, как только что подчеркивалось, не на гистоархитектонику, а на цитологию. В пользу дисгормональной природы клеток свидетельствует их функциональное разнообразие, иными словами — дисгормональный полиморфизм (разумеется, при отсутствии патологических митозов и прочих безусловных признаков гистологической злокачественности).
Дисгормональный полиморфизм возникает в силу того, что клетки еще не приобрели опухолевой автономии и еще чувствительны по отношению к гормональным воздействиям.
Поскольку последние утратили свой нормальный характер, клетки отвечают на гормональные стимулы странным, хотя и не раковым ростом. Так, например, по периферии солидного дисгормонального гнезда клетки могут быть значительно темнее остальных и располагаются в виде бордюра, а в центре гнезда одни клетки мелкие и темные, другие — крупные и светлые.
Фиброаденоматоз молочной железы

Протоковый пролиферативный фиброаденоматоз молочной железы (Х400).
Разумеется, на рисунке представлен только один из примемеров дисгормонального полиморфизма; количественные и пространственные соотношения между различными клеточными формами могут быть самыми различными, общими являются только их неравноценность, отсутствие мономорфизма.
При резко выраженном уродстве клеток диагноз внутрипротокового рака затруднений не представляет. Но не всегда раковые изменения в солидном внутрипротоковом гнезде идут по пути атипии и полиморфизма.
Рак молочной железы

Внутринротоковый солидный мономорфноклеточный рак
молочной железы (X 200).
В некоторых случаях раковые клетки предельно упрощают свое строение и становятся похожими одна на другую, настолько сходными, что картина, на первый взгляд, кажется даже спокойнее, чем при дисгормональном полиморфизме. Раковые гнезда такого строения часто дают повод к диагностическим недоразумениям.
Итак, солидные внутрипротоковые гнезда при фиброаденоматозе бывают трех видов: дисгормональные, раковые полиморфноклеточные и раковые мономорфноклеточные. Первые характеризуются функциональным полиморфизмом и могут быть ошибочно приняты за раковые.
Вторые, полиморфноклеточные раковые, диагностических затруднений не представляют. Третьи, мономорфноклеточные раковые, могут быть неправильно расценены как дисгормональные.
Криброзные гнезда формально являются теми же солидными, но снабженными множеством мелких кругловатых отверстий. Однако этими, чисто внешними, особенностями различия между солидными и криброзными гнездами не исчерпываются.
Если рассматривать дисгормональную перестройку молочной железы как своего рода подготовительную работу для ракового роста, то наличие дисгормональных криброзных гнезд свидетельствует о том, что предраковая подготовка зашла дальше, чем в тех случаях, когда дисгормональная пролиферация исчерпывается образованием солидных гнезд.
Об этом свидетельствует то обстоятельство, что криброзные дисгормональные гнезда значительно чаще соседствуют с инвазивным раком, чем только солидные. Отчетливо эта закономерность вырисовывается при изучении многочисленных, а не единичных срезов.
Доброкачественные заболевания ткани молочной железы у женщин с каждым годом встречаются все чаще и чаще. В отличие от опухолевых патологий груди, такие болезни обычно очень длительное время протекают бессимптомно и выявляются только при развитии дискомфорта, боли в молочных железах или же случайно при осмотре врачом. Однако именно эти изменения под действием нарушенного гормонального фона, по данным разных ученных, повышают риск развития рака груди от 3 до 30 раз. Каждой женщине важно понимать, почему развиваются такие доброкачественные изменения в ее молочных железах. Это знание поможет не только понять, что делать при возникновении того или иного симптома, но и позволят предупредить развитие более тяжелой патологии, в первую очередь, рака груди.

Мастопатия обычно выявляется у пациенток в период после 30 лет и до момента наступления менопаузы (45-50 лет). Это процесс патологического замещения нормальной ткани молочной железы на участки разрастания соединительной ткани и видоизмененных железистых клеток органа. Заболевание может принимать несколько морфологических форм (диффузная, узловая или очаговая), которые отражают стадию прогрессирования заболевания и зависят не только от причины болезни, но и от индивидуальных особенностей молочной железы пациентки.
В отличие от клинической классификации заболевания, патанатомами, гистологами и онкологами (которые рассматривают некоторые виды мастопатии как предраковый процесс) принято делить патологию на непролиферативную и пролиферативную формы. К непролиферативному типу мастопатии относят процессы в молочной железе, которые приводят к разрастанию соединительной ткани (фиброзу) и формированию кист в пределах одной протоково-дольковой морфологической единицы. Стенки таких кист выстланы эпителиальными клетками, которые могут подвергаться процессам метаплазии (смены изначального гистологического типа). Это может инициировать процесс сосочковых разрастаний внутри кисты.
Пролиферативная мастопатия
Пролиферативная мастопатия – это патологический процесс разрастания клеток молочной железы путем их активного размножения. Принято выделять следующие формы такого заболевания:
1. Эпителиальная форма пролиферации клеток.
2. Миоэпителиальная форма пролиферации клеток.
3. Фиброэпителиальная форма пролиферации клеток.
По тому, как активно происходит размножение клеток, пролиферативная мастопатия делится на 3 степени, что позволяет оценить потенциальную тяжесть протекания заболевания у конкретной пациентки:
· 1 степень. Мастопатия без гистологических признаков пролиферации эпителиальных клеток.
· 2 степень. Патологические изменения железистой ткани с наличием пролиферации эпителиальной ткани без признаков атипии и метаплазии.
· 3 степень. Мастопатия молочных желез, которая сопровождается пролиферацией атипичного эпителия. Именно эта степень рассматривается как облигатный предрак и представляет наибольшую онкологическую опасность.


Отметим, что рак груди как раз и характеризуется тем, что в ткани молочной железы возникает очаг размножения клеток, которые не могут быть дифференцированы как нормальные клетки человеческого организма. Их принято обозначать термином атипичные клетки.
Пролиферация любой ткани в организме является как нормальным компенсаторным процессом, так и может возникать под действием патологического фактора (воспаления, нарушения гормонального фона, ишемии и т.д.). В случае мастопатии такой процесс размножения клеток вызывается высоким уровнем гормона эстрогена или пролактина на фоне гипоэстрогенемии. В сочетании с другими неблагоприятными факторами (наследственностью, стрессами, токсическим и лучевым воздействием на организм и др.) может развиваться патологическая пролиферация клеточных структур долек и протоков молочной железы.
Поэтому пролиферативную мастопатию 2 и 3-й степени развития принято относить к предраковым формам заболевания . Однако статистический анализ заболеваемости и исходов этой патологии указывает на то, что даже непролиферативные формы мастопатии в ряде случаев приводили к возникновению малигнизации (озлакочествления процесса) и становились основой развития рака груди. Также установлено, что вероятность возникновения онкологического процесса на фоне такого заболевания не одинакова для пациенток, а зависит от ряда сопутствующих факторов:

1. Срок течения мастопатии и длительность наблюдения у врача. Процент возникновения случаев малигнизации процесса выше при длительно текущей патологии, которая не сопровождалась лечением и медицинским наблюдением.
2. Данные результатов гистологических исследований при сомнительной клинической картине. Довольно часто результаты биопсии не могут точно дать ответ на вопрос – трактовать гистологическую картину в пользу рака или нет. Такая ситуация может наблюдаться не только при невыраженном патологическом процессе, но и при получении участка железы вне очага заболевания и т.д. Однако гистологическое исследование в сравнении с другими методами обладает наибольшей диагностической точностью.
3. Индивидуальные особенности организма пациентки (наследственные и генетические факторы, состояние иммунной системы, гормональных процессов и др.).

К сожалению, установить точный тип клеточно-тканевых изменений при мастопатии в молочной железе можно, только проведя биопсию пораженного участка ткани (что не совсем просто при диффузной форме, т.к. сложно выявить очаг наибольших патологических изменений) и дальнейшем внимательном гистологическом и цитологическом исследовании. Но зачастую большое число пациенток в процессе диагностики и лечения, либо самостоятельно игнорируют данное обследование (ссылаясь на его травматичность, дискомфортные ощущения во время процедуры и т.д.), либо оно не возможно из-за несовершенства лечебно-диагностической базы медицинских учреждений.
В любом случае постановка диагноза в большинстве случаев опирается лишь на клиническую форму болезни (диффузная или узловая), которая помогает врачу определиться с тактикой лечения заболевания. Гистологическое подтверждение болезни и ее классификация используется уже на стадии подозрения онкологического процесса у пациентки.
Диагностика заболевания

Пролиферативная мастопатия требует довольно широкого спектра лабораторных и инструментальных обследований. Однако только так можно достоверно определить тип и степень клеточных изменений в груди, что поможет дать пациентке относительно точный прогноз ее состояния и определиться с дальнейшей диагностическо-лечебной тактикой.
Женщинам не стоит забывать о том, что они сами могут довольно точно и быстро определить изменения в своей груди при самоосмотре даже на ранних стадиях мастопатии. Не стоит скептически относиться к такому мероприятию и думать, что невозможно самостоятельно ощутить изменения в ткани органа. При правильном проведении данной процедуры, Вы сможете не только вовремя заподозрить неладное, но и с высокой точностью оценить реакцию областей изменения в груди на пальпацию, консистенцию и эластичность образований и т.д. Такая информация может быть очень важная для врача. О том, как правильно проводить самостоятельный осмотр своих молочных желез, любая женщина может узнать у лечащего врача гинеколога, маммолога или хирурга.

Современная медицина предлагает следующий перечень необходимых исследований для постановки точного диагноза любой формы мастопатии:
1. Осмотр и пальпация молочной железы. Это необходимая процедура, поскольку врач визуально не только выявит грубую патологию, но и сможет определить изменения консистенции железы, наличие болезненности в определенных участках, патологических выделений из сосков. Также специалист задаст ряд вопросов для уточнения общего гинекологического статуса, состояния органа в разные периоды менструального цикла , наличия сопутствующих заболеваний. Часто именно четко указанные жалобы самой пациенткой дают незаменимую информацию для врача и помогают ему более точно определиться с диагностикой заболевания.
3. УЗИ груди и подмышечных лимфатических узлов. Такой вид исследования дает возможность на основании косвенных признаков оценить морфологию молочных желез, а также близлежащих лимфатических узлов, которые могут поражаться при онкологическом процессе. Сочетание маммографии и УЗИ дает максимальную диагностическую информацию о том, как патологический процесс повлиял на морфологическую структуру органа. Также УЗИ может применяться у пациенток, которые по различным причинам не могут переносить процедуру маммографии. Ультразвуковое сканирование считается предпочтительным в молодом возрасте, а маммография – у женщин старше 40 лет.
4. Биопсия зоны патологически измененной ткани груди. Такую процедуру проводят либо специальными иглами, которые берут частичку железы для дальнейшего гистологического исследования, либо в процессе оперативного удаления узлов и очагов мастопатии. Цитологической и гистологическое исследования пунктата – это самый точный, современный метод определения, имеет ли место пролиферативная мастопатия, рак молочной железы и другие заболевания у пациентки.
Отдельной диагностической линией врач пытается установить причину, которая спровоцировала такой патологический процесс, как мастопатия. Для этого изучается общий гормональный фон женщины (с акцентом на уровень половых гормонов), исключаются гинекологические заболевания, поражения щитовидной железы, опухоли гипофиза и т.д. Могут применяться дополнительные УЗ-исследования, КТ, МРТ, а также специфические анализы для оценки иммунного, эндокринологического статуса пациентки и оцениваться маркеры онкологических процессов.
Лечение заболевания
Пролиферативная мастопатия требует комплексного подхода в лечении. Тактика выбора терапии заболевания основывается на том, какая клиническая форма патологии наблюдается у конкретной пациентки.

Общими рекомендациями по лечению любого типа мастопатии являются:
1. Нормализация образа жизни, питания, сна и отдыха.
2. Отказ от вредных привычек.
3. Лечение хронической гинекологической патологии.
4. Избегание стрессов, нервного и психического перенапряжения.
5. Устранение влияния негативных факторов окружающей среды (радиации, токсинов и т.д.).

Диффузный тип мастопатии успешно поддается консервативному лечению у большинства пациенток. Для этого применяют препараты, которые снижают уровень и активность избытка эстрогена или пролактина. Если у женщины точно определена причина, которая привела к избыточной выработке гормонов и нарушения гормонального фона, врачи пытаются воздействовать и на нее.
Узловая и очаговая форма мастопатии помимо консервативного лечения зачастую требуют оперативного вмешательства. Эта необходимость связана не только с эстетическими требованиями, но и также с тем, что такие патологические образования в молочной железе служат с большой долей вероятности очагом развития рака груди при неблагоприятном стечении факторов. Хирург, удалив патологический очаг, отправляет его на гистологическое и цитологическое исследование, где в лаборатории определяется тип и степень прогрессирования болезни, а также дается ответ о наличии возможного онкологического процесса. Профилактика мастопатии >>>
Маркер Ki-67 – один из важнейших показателей ракового процесса при обследовании. Уникальный белок – антиген – показывает деление клеток, которые в состоянии покоя не приводят к образованию вещества. Если при тесте на Ki-67 обнаруживается активность клеток, врачи могут диагностировать степень развития карциномы.
Что такое индекс пролиферации

Индекс выявляется при исследовании Ki-76 на экспрессию – это цифровой показатель активности опухолевых клеток. Если уровень экспрессии Ki-67 опухолевых клеток равен 22, это означает 22% активность. Чем выше показатель, тем активнее происходит размножение атипичных клеток и, следовательно, развитие рака.
При раке молочной железы маркер Ki-67 обнаруживается в тканях, взятых с помощью биопсии или в ходе операции по удалению опухоли. С его помощью оценивается геномная активность. Чаще всего этот протеин применяется для уточнения диагноза карциномы молочной железы. Однако использовать он может и для диагностики злокачественных процессов в других органах.
Показания и противопоказания

Обследование на Ки-67 при раке молочных желез назначают в таких случаях:
- имеется подозрение на агрессивное развитие новообразования;
- требуется определить эффективную методику карциномы;
- нужно выявить эффективность лечения, а также риски рецидива после проведенной терапии;
- нужно определить вторичные очаги в лимфатических узлах и органах;
- требуется определить гормональный статус новообразования;
- в организме обнаружены другие онкологические процессы.
У иммуногистохимии отсутствуют абсолютные противопоказания. Проводить процедуру нельзя только при острых состояниях, когда у пациентов увеличивается температура.
Особенности проведения ИГХ-исследования для выявления маркера
Чтобы выполнить исследование Ki-67 при раке молочной железы у женщин и определить, в норме ли показатели, потребуется образец ткани. Его забирают с помощью специальных инструментов из подозрительного участка груди, используя следующие методы:
- Аспирация иглой. Применяется очень тонкий инструмент, введение которого почти не чувствуется и процедуру выполняют без обезболивания.
- Вакуумная биопсия. Врач применяет местный анестетик, вырезает микроскопический кусочек кожи и вводит зонд. Через разрез специалист получает несколько видов материала.
- Эксцизионная биопсия. Для процедуры используется игла с большим диаметром, ткань берут цилиндрической формы под местным обезболиванием.
- Хирургическая биопсия. При выполнении операции удаляется аномальная зона, часть полученного материала направляется на гистологическое исследование.
Результат анализов пациент получает уже через 10-12 суток.
Метод проведения биопсии не может выбираться пациенткой. Способ определяется исключительно врачом и стоит доверять ему без лишних вопросов.
Польза определения индекса Ki-67
Главная задача маркера Ki-67 – определить точный показатель выживаемости. Он успешно с этим справляется, так как точно определяется количество делящихся раковых клеток в опухоли. При высоком уровне можно говорить о стремительном делении клеток, что будет положительно оценено с точки зрения химиотерапии. Если же эти клетки делятся медленно, терапия не даст существенных результатов.
Методы определения значения маркера
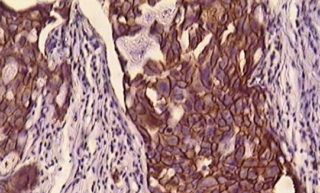
Маркер Ki-67 хорошо выявляет особенности опухолевого процесса. Проводят его на тканях опухоли при обязательном гистологическом исследовании обнаруженных новообразований. Также тест на маркер назначают при агрессивном увеличении опухолей.
Пациентки должны понимать, что положительные показатели Ki-67 указывают на высокий риск рецидива и худшую выживаемость даже на ранних стадиях патологии.
Для оценки результатов взятой биопсии применяют несколько методов исследования:
- окрашивание клеток антигена Ki-67 – световые микроскопы помогают оценить визуально количество активных частиц;
- применение антитела MIB1 для маркировки злокачественных клеток;
- положительно окрашенные клетки опухолей среди общего числа позволяют сопоставить их процент относительно здоровых клеток;
- результаты подсчитывают, учитывая все разделы опухоли.
Исследование маркера Ki-67 – это сложная диагностическая процедура. Иногда на биопсии у пациента берут несколько образцов, что позволяет точно определить уровень активности и количество атипичных опухолевых клеток. Для этого используются разные методы оценки.
Прогноз и сопоставление процентного соотношения
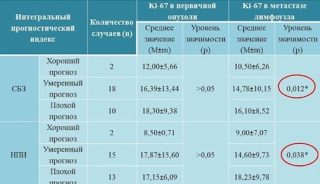
Результаты анализа пациенту выдаются обычно в определенном процентном соотношении. Оно указывает на содержание белка, с помощью которого можно определить тактику лечения. В норме Ki-67 не должен превышать 15%, тогда пациенту ставится благоприятный диагноз и шанс выживания свыше 90%. Чем выше процент Ki-67, тем хуже обстоят дела:
- если Ki-67 равен 10% и меньше, то в 95% случаев после операции срок выживаемости будет более 10 лет;
- при показателе Ki-67 15% в 95% случаев женщины проживают больше 5 лет, в России этот показатель может быть равен 85% случаев;
- при Ki-67 в 20% устанавливается рак молочной железы с активностью новообразования, если лечение начать сразу же, прогноз будет благоприятным, при отказе высок риск прогрессирования болезни и сокращения жизни до 3-5 лет;
- если Ki-67 равен 30% — это указывает на активное развитие и увеличение карциномы в размерах, однако она хорошо будет поддаваться химиотерапии;
- если Ki-67 равен 90%, врачи могут отказаться от лечения – выживаемость в течение 5 лет равна нулю.
При самом высоком показателе Ki-67 женщины, как правило, редко живут дольше 3 лет.
Рак молочной железы с повышенной гормональной зависимостью – очень распространенное заболевание. Оно складывается из ряда факторов, провоцирующих болезнь: беременность, половое созревание, кормление грудью, а затем и предклиматерический период связаны с сильным колебанием гормонов. Прогестероны и эстрогены колоссальным образом воздействуют на женский организм, способствуя неблагоприятному состоянию.
Спровоцировать изменение в груди могут и другие факторы: лечение гормональными средствами в больших дозировках, отсутствие беременностей в течение жизни или бесплодие. Однако это не значит, что рак у нерожавших женщин случается чаще. Прямой связи с беременностями или их отсутствием не существует.
Что делать при плохом диагнозе

При выдаче результатов на руки специалисты лаборатории не дают никаких рекомендаций и пояснений. Однако женщины выясняют значение анализов в интернете. Затем диагноз подтверждается врачом. Далеко не все случаи считаются пригодными для лечения. Это вызывает огромный стресс и тревогу у женщин.
Важно понимать, что даже при обнаружении последней стадии рака молочной железы жизнь не заканчивается в эту же секунду. Многие люди живут больше 1-2 лет. И это время следует потратить на любимых людей, если остаются силы и вера.
Очень важна поддержка близких в этот период, а также контакты с женщинами в таком же состоянии. Нередко группы поддержки тяжелобольных помогают справиться с высоким уровнем тревоги, проработать страхи и подготовиться к окончанию жизненного пути.
При получении плохого результата важно помнить, что высокий уровень экспрессии указывает на то, что опухоль будет хорошо поддаваться химиотерапии. Если сразу же начать лечение и потом пройти повторную диагностику, есть все шансы на существенное улучшение состояния. Результаты тестов на Ки-67 иногда не могут быть интерпретированы точно, если патология связана с положительными лимфатическими узлами.
Определение маркера Ki-67 назначается в спорных случаях, когда есть все причины предполагать наличие рака у пациентки. Также обследование проводят, когда рак установлен, но нужно определить его активность и подобрать лучшую тактику терапии.
Рак молочной железы — самое распространенное в мире онкологическое заболевание у женщин. В России этот вид рака составляет 20,9% всех злокачественных болезней. В 2015 году в стране было выявлено более 66 600 новых случаев возникновения рака молочной железы, а заболеваемость составила 49,75 на 100 000 населения.
Развитие хирургии, фармакологии, методов диагностики и появление новых знаний о раке молочной железы увеличили шансы обнаружить опухоль на ранней стадии. Благодаря этому хирургическое лечение болезни с сохранением молочных желез стало встречаться гораздо чаще. Меняется и тактика обследования пациенток после первичного лечения — теперь она помогает наиболее эффективно и оперативно выявлять возможные рецидивы.
Количество пациенток, прошедших первичное лечение и находящихся на динамическом контроле, увеличивается с каждым годом. Именно поэтому рецидив рака молочной железы и методы его предупреждения становятся все более обсуждаемыми медицинскими темами.
Повторное развитие болезни необходимо диагностировать на ранней стадии. Активное наблюдение пациентов помогает снизить риск рецидива и найти наиболее эффективный метод лечения, если он все же произойдет. Кроме того, повторное возникновение болезни можно предупредить грамотной профилактикой.
Наблюдение после лечения рака молочной железы
В первые 5 лет после первичного лечения онкологии риск возникновения рецидива наиболее велик. Поэтому в этот период необходимо посещать онколога от 1 до 4 раз в год (в зависимости от конкретной клинической ситуации). Во время приема врач осматривает пациентку и выявляет возможные жалобы. По прошествии 5 лет к специалисту советуют обращаться раз в год, если, конечно, нет никаких жалоб на состояние.
Во время приема онколог помимо осмотра назначит проведение инструментальных методов исследования, которые позволят своевременно обнаружить рецидив рака молочной железы или прогрессирование заболевания:
- двустороннюю (в случае органосохранной операции) или контралатеральную маммографию в сочетании с УЗИ региональных зон и области послеоперационного рубца — раз в год;
- сцинтиграфию костей скелета, УЗИ органов брюшной полости и малого таза, рентгенографию органов грудной клетки — по назначению онколога.
Кроме того, женщины, принимающие тамоксифен адъювантно при наличии сохранной матки, должны ежегодно проходить плановый осмотр у гинеколога. Дело в том, что препарат может вызывать развитие гиперплазии эндометрия, а специалист вовремя это заметит.
Женщинам, длительно принимающим ингибиторы ароматазы, рекомендуют ежегодное прохождение денситометрии. Этот метод диагностики помогает оценить плотность костной ткани и риск развития остеопороза.
Почему развиваются рецидивы после мастэктомии
Рецидив рака молочной железы в послеоперационном рубце может возникнуть как следствие некачественного лечения, химиотерапии или неполноценного удаления опухоли.
Наиболее опасными для развития местных рецидивов считаются первые 10 лет после первичного лечения. Причем больше половины случаев повторного заболевания происходят в первые 5 лет. Задача пациенток в этот период — при наличии каких-либо подозрений на рецидив сразу же обратиться к онкологу. Необходимо проводить самостоятельное обследование молочной железы и послеоперационного рубца, а также знать свою группу риска и основные симптомы рецидивов.
Вероятность развития рецидива рака молочной железы зависит от следующих факторов:
- Наличие метастазов в регионарных лимфоузлах;
- Молекулярно-генетический профиль опухоли (наличие рецепторов к эстрогенам и эпидермальному фактору роста HER/2neu);
- Размеры первичной опухоли;
- Возраст пациентки. Рецидив РМЖ чаще развивается у молодых пациенток.
В этой связи выделяют 3 группы риска.
- метастазы в 1-3 лимфатических узлах при отсутствии гиперэкспрессии HER2/neu в опухоли;
- метастазы в 1-3 лимфатических узлах при наличии гиперэкспрессии;
- HER2/neu в опухоли;
- метастазы в 4 лимфатических узлах и более.
Отсутствие метастазов в лимфатических узлах в сочетании хотя бы с одним из перечисленных признаков:
- размер опухоли более 2 см;
- степень злокачественности 2-3;
- наличие инвазии сосудов;
- наличие гиперэкспрессии HER2/neu в опухоли;
- возраст менее 35 лет.
Отсутствие метастазов в лимфатических узлах в сочетании со всеми следующими признаками:
- размер опухоли менее 2 см;
- степень злокачественности опухоли 1 (низкая);
- нет инвазии в сосуды;
- нет гиперэкспрессии HER2/neu;
- возраст более 35 лет.
Симптомы рецидива
Для своевременного выявления рецидива рака молочной железы необходимо регулярно посещать онколога и проходить обследования. Однако не менее важно самостоятельно следить за состоянием грудной клетки и молочных желез.
Симптомы повторного развития рака могут казаться неочевидными. Регулярный осмотр груди и понимание ее нормального состояния поможет выявить нежелательные изменения как можно раньше и приступить к лечению.
Среди наиболее частых симптомов, которыми проявляется рецидив рака молочной железы:
- появление уплотнения под кожей молочной железы (при органосохранной операции) или в зоне послеоперационного рубца;
- изменение структуры тканей молочной железы (при органосохранной операции);
- рецидив рака молочной железы в послеоперационном рубце может давать изменение окраски кожи в зоне шрама (покраснение).
Если вы обнаружили признаки рецидива рака молочной железы, следует безотлагательно обратиться к онкологу.
Диагностика при подозрении на рецидив рака груди
При подозрении на развитие рецидива необходимо немедленно обратиться к врачу. Специалист проведет диагностику: осмотр, пальпацию, маммографию, назначит УЗИ послеоперационного рубца и региональных зон и морфологическое (цитологическое и гистологическое) исследование.
Морфологическое исследование рецидивной опухоли должно проводиться аналогично диагностике первичной опухоли, в том числе с определением рецепторов эстрогенов (РЭ), рецепторов прогестерона (РП), HER2/neu, Ki67. Исходя из полученных данных, будет определяться дальнейшая тактика и методы лечения. При необходимости онколог назначит дополнительные исследования и анализы.
Профилактика повторного возникновения болезни
- комплексное лечение в соответствии с мировыми стандартами;
- при гормонопозитивном раке длительный прием тамоксифена/ ингибиторов ароматазы;
- динамическое наблюдение после завершения основного этапа лечения;
- профилактика средствами на основе индол-3-карбинола и эпигаллокатехин-3-галата (Промисан) для восстановления активности опухоль-подавляющих генов (ген, продукт которого обеспечивает профилактику опухолевой трансформации клеток) и белков BRCA.

Препарат Промисан выступает своеобразным помощником, усиливающим действие химиопрепаратов, так как блокирует ряд факторов роста и формирования гормональных метаболитов, которые участвуют в процессе роста опухоли.
Читайте также:

