Причины в12 фолиево рефрактерной анемии
Из-за наследственного дефекта ферментов, участвующих в синтезе гемма, либо из-за их инактивации.


Отличия Fe-дефицитной и Fe-рефрактерной анемии: по содержанию сывороточного Fe.
Fe в плазме меньше Fe в плазме больше
4. B12, B9 – дефицитная анемия
При недостатке в организме витамина B12 и фолиевой кислоты.
--алиментарный дефицит (при полном длительном вегетарианстве)
--при нарушении всасывания этих витаминов в желудке. Для их всасывания необходим гликопротеид – внутренний фактор Кастла. Он синтезируется париетальными клетками желудка. Его дефицит наблюдается при аутоиммунном гастрите, резекции желудка, раке желудка.
--нарушение всасывания витаминов в кишечнике при резекции, колитах и раке.
--при конкурентном потреблении B12 бактериями и гельминтами (при гельминтозах, декомпенсированных дисбактериозах).
B12, B9 необходимы для образования нуклеиновых кислот, входящих в состав ДНК, поэтому при их дефиците нарушается пролиферация всех быстроделящихся клеток, меняется темп кроветворения на мегалобластический (в место нормальных эритроцитов образуются крупные клетки, похожие на эмбриональные эритроциты, получившие название мегалоцитов, мегалобластов)
Клетки делятся медленноà их мало, но они содержат много Hb из-за крупных размеровà цветной показатель увеличивается.
Уменьшается количество эритроцитов, Hb, цветовой показатель увеличивается (гиперхромная анемия).
Уменьшается количество ретикулоцитов (гипорегенераторная), тромбоцитов, лейкоцитов, наблюдаются мегалоциты, мегалобласты.
5. B12,B9-рефрактерная анемия
При наследственном дефекте или при инактивации ферментов, участвующих в синтезе нуклеиновых кислот, либо при отсутствии белка транскобаламина.
Проявляется так же как дефицитная анемия, но имеет тяжелое, злокачественное течение, не поддающееся лечению препаратами витаминов.
Гипопластическая анемия
Из-за нарушения выработки эритропоэтина почками
Причина: заболевание почек (почечная недостаточность, гломерулонефрит, пиелонефрит, опухоли, нефросклероз и т.д.)
Гемограмма: уменьшение количества эритроцитов, Hb, ретикулоцитов, цветной показатель в норме.
Метапластическая анемия
Из-за вытеснения нормальных ростков кроветворения опухолевыми клетками при лейкозах и гемобластозах.
Гемограмма: угнетение всех нормальных ростков кроветворения на фоне признаков лейкоза, вызвавшего данную анемию.
Гемолитическая анемия
Из-за повышенного разрушения эритроцитов.
Гемолиз:
1-внутриклеточный: эритроциты разрушаются МФ селезенки, при этом в кровь выделяется не конъюгированный билирубин, что приводит к развитию гемолитической желтухи.
2-внутрисосудистый( острая гемолитическая анемия- ОГА):возникает вследствие разрушения эритроцитов непосредственно в сосудах, в крови появляется Hb,что проявляется ложной гиперхромией (цветной показатель резко увеличивается), это не связано с повышенным содержанием Hb в эритроцитах, а связано с тем, что Hb находится в плазме. Данный Hb выводится почками, часто закупоривая почечные канальцы, вызывая гематурию и острую почечную недостаточность.
Для всех гемолитических анемий характерен макроцитоз, т.к перед гемолизом эритроциты набухают.
Острая гемолитическая анемия протекает в 2 стадии:
1) стадия ложной гиперхромии. В гемограмме: эритроциты ↓, Hb в норме, ц. п. ↑, макроцитоз.
2) элиминация растворенного Hb. В гемограмме : эритроциты ↓, Hb ↓, ц. п. в норме, рет ↑, лейкоциты ↑, сдвиг лейкоцитораной формулы влево.
Классификация гемолитических анемий:
Возникают при нарушении образования эритроцитов и синтеза гемоглобина в красном костном мозге. Являются гипо или арегенераторными.
Классификация
1. Железодефицитная и железорефрактерная анемии (обусловлены нарушением синтеза гемоглобина)
2. В12, фолиево дефицитные и рефрактерные (обусловлены нарушением синтеза ДНК и РНК)
3. Апластические, гипопластические, метапластические (обусловлены нарушением пролиферации клеток красного костного мозга)
Железодефицитная анемия (ЖДА) – клинико-гематологический синдром, характеризующийся нарушением синтеза гемоглобина вследствие дефицита железа в организме и проявляющейся анемией и сидеропенией.
Причины железодефицитной анемии:
--нарушение поступления Fe в организм (алиментарный дефицит, либо нарушение всасывания при заболеваниях ЖКТ).
--повышенная потеря Fe из организма (хроническая кровопотеря по 5-10 мл/сут при маточных, носовых, геморроидальных, желудочно-кишечных и др. кровотечениях.
Данная форма носит название хронической постгеморрагической анемии и на нее приходится 80-90% случаев, среди всех железодефицитных анемий.
--повышенный расход Fe (у беременных, в период грудного вскармливания, в период интенсивного роста, при хронических инфекционных заболеваниях).
Патогенез: Fe входит в состав гемма, который необходим для синтеза Hb. При дефиците Fe замедляется процесс деления и созревания эритроцитов, поэтому снижается их содержание в крови. В эритроцитах содержится мало Hb, поэтому их размер уменьшен (микроцитоз, анизоцитоз). Изменяется их форма (пойкилоцитоз).
Для ЖДА характерны следующие синдромы:
Сидеропенический синдром обусловлен дефицитом железа в тканях, что приводит к нарушению синтеза некоторых содержащих железо ферментов (цитохромов). Проявляется сухостью кожи, ломкостью ногтей, волос.
Синдром анемической гипоксии– проявляется генерализованной гипоксией с поражением ЦНС (головокружение, потемнение и мушки перед глазами)
Синдром метаболической интоксикации - проявляется нарушениями в иммунной системе, астенией, утомляемостью)
Гемограмма: уменьшается количество эритроцитов и Hb, цветовой показатель
В12, фолиево дефицитная анемия
Развивается при дефиците витамина В12 и/или фолиевой кислоты необходимых для синтеза нуклеиновых кислот входящих в состав ДНК и РНК.
Причины дефицита витаминов В12 и/или фолиевой кислоты:
--алиментарный дефицит (при полном длительном вегетарианстве)
--при недостатке внутреннего фактора Кастла, который необходим для связывания и всасывания этих витаминов в кишечнике. Фактор Кастла синтезируется париетальными клетками желудка, его дефицит наблюдается при аутоиммунном гастрите типа А, при раке и резекции желудка.
--нарушение всасывания витаминов в кишечнике при его резекции, колитах и раке.
-- конкурентное потребление B12 и фолиевой кислоты бактериями и гельминтами при декомпенсированных дисбактериозах и гельминтозах
B12 и B9 необходимы для образования нуклеиновых кислот, входящих в состав ДНК и РНК, поэтому при их дефиците нарушается пролиферация клеток, меняется тип кроветворения на мегалобластический (вместо нормальных эритроцитов образуются крупные клетки, похожие на эмбриональные эритроциты, получившие название мегалобластов и мегалоцитов)
Клетки редко делятся и замедленно созревают, часто останавливаясь на стадии мегалолобласта и не достигая стадии мегалоцита. Они крупного размера и содержат много Hb, поэтому ЦП увеличивается.
При B12 дефицитной анемии развивается характерная триада синдромов:
Анемический синдром (Гемограмма:)
Уменьшается количество эритроцитов и Hb, ЦП увеличивается (гиперхромная анемия)
Уменьшается количество ретикулоцитов (гипорегенераторная или арегенераторная анемия), уменьшается количество тромбоцитов и лейкоцитов, присутствуют мегалоциты и мегалобласты.
Желудочно-кишечный синдром возникает из-за нарушения пролиферации клеток эпителия ЖКТ (атрофия слизистой, глоссит, ахлоргидрия)
Неврологический синдром проявляется дегенерацией аксонов, нарушение миелинизации.
В12, фолиево рефрактерная анемия
Развивается при наследственном дефекте ферментов, участвующих в синтезе нуклеиновых кислот, либо при отсутствии белка транскобаламина III, осуществляющего транспорт В12 в красный костный мозг. Проявляется так же, как В12, фолиево дефицитная анемия, но имеет тяжелое, злокачественное течение, резистентное к лечению витаминами В12 ифолиевой кислотой.
Апластическая анемия
Возникает в результате наследственных дефектов стволовых клеток, либо из-за гибели стволовых клеток под действием ионизирующей радиации, цитостатиков, бензола. При этом, из-за поражения стволовых клеток происходит нарушение всех видов кроветворения, что проявляется панцитопенией, которая характеризуется развитием анемического синдрома, геморрагического синдрома и инфекционного синдрома.
В гемограмме: снижен Нв и эритроциты, отсутствуют ретикулоциты (арегенераторная анемия), ЦП в норме (нормохромная анемия), наблюдается лейкопения, тромбоцитопения.
Гипопластическая анемия
Возникает при нарушении выработки эритропоэтина почками, что наблюдается при хронической почечной недостаточности, гломерулонефрите, пиелонефрите, опухолях почек. В гемограмме: снижены гемоглобин, эритроциты, ретикулоциты, ЦП в норме, лейкоциты и тромбоциты в норме.
Метапластическая анемия
Развивается из-за вытеснения нормальных ростков кроветворения опухолевыми клетками при лейкозах и гемобластозах.
Гемограмма: угнетение всех нормальных ростков кроветворения на фоне признаков лейкоза, вызвавшего данную анемию.
ГЕМОЛИТИЧЕСКИЕ АНЕМИИ – группа врожденных или приобретенных заболеваний крови, возникающих вследствие повышенного распада эритроцитов (гемолиза)
Гемолиз бывает двух видов: внутриклеточный – осуществляется макрофагами селезёнки, при этом в крови повышается концентрация неконъюгированного билирубина, что проявляется гемолитической желтухой и внутрисосудистый – характеризуется распадом эритроцитов в сосудах, выходом в плазму гемоглобина. В первую стадию острой гемолитической анемии при внутрисосудистом гемолизе наблюдается ложная гиперхромия, ЦП увеличен за счёт внеэритроцитарного гемоглобина, попавшего в плазму из гемолизированных эритроцитов. Гемоглобин выводится почками, что может вызвать закупорку и повреждение почечных канальцев, приводящую к острой почечной недостаточности.
Для всех гемолитических анемий характерен ретикулоцитоз, из-за повышенного образования эритроцитов в красном костном мозге (гиперрегенераторные анемии). Кроме этого наблюдается макроцитоз из-за набухания эритроцитов, которое предшествует гемолизу.
Заболевания крови составляют многочисленную и разнообразную группу синдромов, формирующихся при нарушениях качественного и количественного состава крови. Все они систематизируются, исходя из поражения какого-либо компонента крови. Гематологические заболевания делят на три основные группы:
- патологии, характеризующиеся снижением уровня гемоглобина;
- гемобластозы;
- гемостазиопатии.
Рефрактерная анемия – одна из разновидностей малокровия, отличающаяся нарушением созревания клеток красного ростка.
Миелодиспластический синдром – это что?
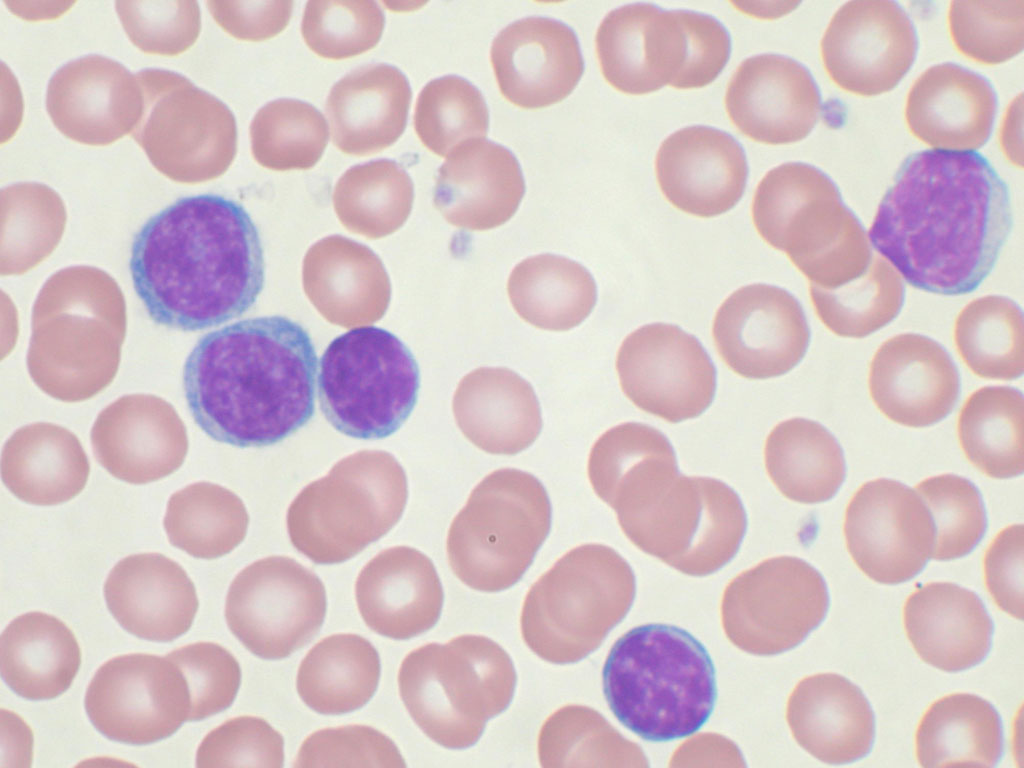
Группу заболеваний и состояний с нарушением процесса образования эритроцитов, моноцитов, тромбоцитов, гранулоцитов в миелоидной ткани (миелоидное кроветворение) с высокой вероятностью развития опухолевого поражения кроветворной системы в медицине именуют миелодиспластическим синдромом (МДС).
Одно из заболеваний группы миелодиспластического синдрома – рефракторная анемия. Данная патология, как и все остальные, объединенные МДС, относится к гематологическим заболеваниям, характеризующимися цитопенией (снижением уровня определенного вида клеток в крови) и патологическими изменениями костного мозга.
Классификация миелодиспластического синдрома
В международную классификацию болезней были внесены некоторые изменения, которые коснулись и гематологических заболеваний. Систематизация схожа с предложенной ранее ВОЗ, но отличается от FAB количеством вариантов определения заболеваний:
- D46.0 - рефрактерная анемия без сидеробластов.
- D46.1 - РА с кольцевыми сидеробластами. Незрелые кровяные клетки в крови не обнаруживаются.
- D46.2 - рефракторная анемия с избытком бластов 1. В анализе крови цитопения, превышение уровня моноцитов, тельца Ауэра отсутствуют.
- D46.3 - рефракторная анемия (РА) со множеством бластов с трансформацией.
- D46.4 - РА неуточненная.
- D46.5 - рефракторная цитопения со многолинейной дисплазией.
- D46.6 - миелодиспластический синдром, ассоциированный с делецией 5q.
- D46.7 - другие миелодиспластические синдромы.
- D46.9 - миелодиспластический синдром неуточненный.
Особенности рефрактерной анемии
Refractorius в переводе с латыни означает "невосприимчивый", "трудноизлечимый". Заболевание относится к гематологическим и характеризуется нарушением развития эритроцитного ростка в крови, продуцируемого костным мозгом. При синдроме рефрактерной анемии сначала снижается содержание эритроцитов в крови, а потом и остальных клеток, поражается орган кроветворной системы, отвечающий за гемопоэз.
Основная опасность патологии заключается в том, что она не поддается лечению, основанному на применении железосодержащих препаратов. Данный вид анемии часто протекает практически бессимптомно и выявляется при диагностике других патологий. Болезнь быстро прогрессирует и ведет к развитию острого лейкоза.
Рефракторная анемия с избытком бластов
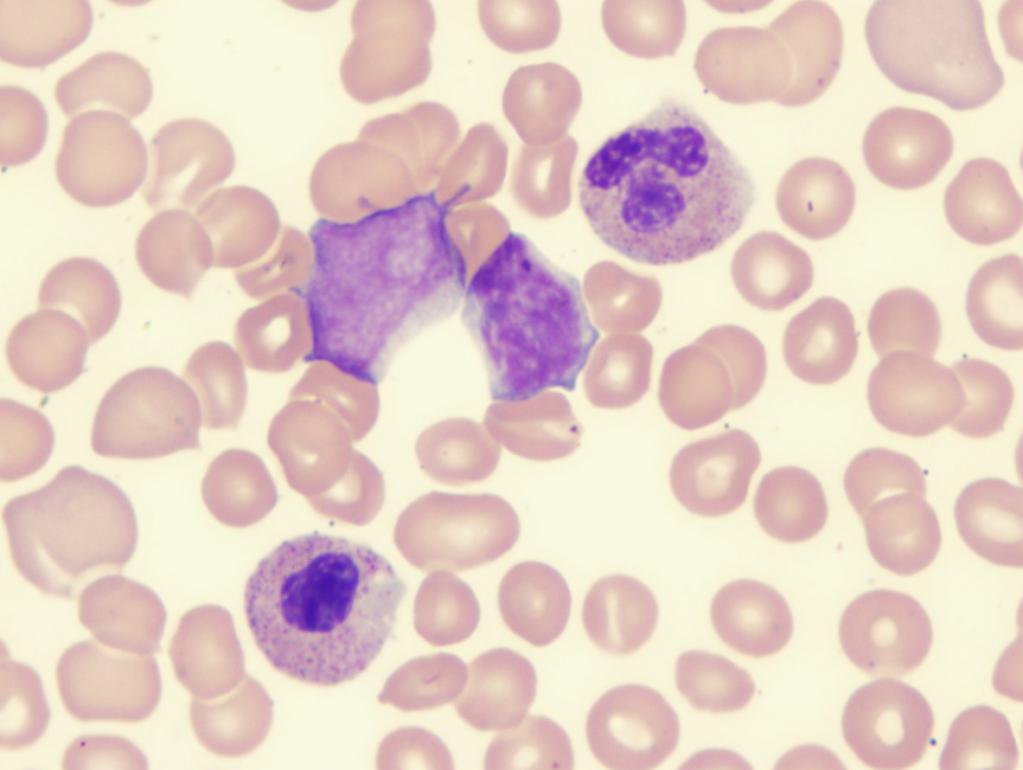
Исходя из статистических данных, людей с подобным диагнозом около 1 015 000. Заболевание чаще всего встречается у мужчин 75-80 лет, а у женщин в возрасте 73-79 лет. Патологию делят на два типа:
- РАИБ-1 – характеризуется цитопенией, увеличением числа моноцитов в крови. Палочковидные красные белковые включения в цитоплазме моноцитов (тельца Ауэра) не обнаруживаются. В костном мозге наблюдается дисплазия одной клеточной линии, бластов (незрелые кровяные клетки) около 5-19 %.
- РАИБ с трансформацией – анализ крови показывает повышенное содержание моноцитов, выявляются тельца Ауэра. Содержание бластов около 30 %. В костном мозге обнаруживаются дисплазии сразу нескольких клеточных линий. Подобная картина способствует развитию острого миелолейкоза.
Смертность от данной патологии составляет около 11 %.
Причины возникновения патологии
Точные причины развития заболевания до сих пор не выявлены. Разделяют два типа синдрома, и по каждому из них установлены факторы риска.
Первичный (идеопатический) выявляется в почти 90 % случаев. Факторы риска:
- Курение.
- Превышенный уровень радиации.
- Проживание в неблагоприятной экологической зоне.
- Регулярное вдыхание паров бензина, органических растворителей, пестицидов.
- Врожденный нейрофиброматоз Реклингхаузена (развитие опухолей из нервной ткани).
- Наследственная анемия Фанкони.
- Синдром Дауна.
Вторичный тип рефрактерной анемии (МДС) наблюдается в 20 % случаев, может развиваться в любом возрасте. Основные причины развития:
- Химиотерапия или радиотерапия.
- Долговременное применение некоторых групп лекарственных средств: циклофосфаты, антрациклины, ингибиторы топоизомеразы, подофиллотоксины.
Вторичный вариант отличается высокой резистентностью к терапии и большой вероятностью формирования острого лейкоза и, как следствие, неблагоприятным прогнозом.
По каким признакам определить заболевание?

Часто патология развивается без каких-либо симптомов, что мешает начать лечение на ранних этапах и в мягких формах. Как правило, диагностируется рефрактерная анемия в тяжелой степени при плановом обследовании пациента.
Но выявить заболевание на ранних этапах все же можно. Первые его признаки имеют много общего с проявлениями, возникающими при патологиях печени, аутоиммунных заболеваниях и любой другой анемии. К ним относятся:
- Бледность, прозрачность кожи, в особенности на лице.
- Чрезмерное утолщение рогового слоя эпидермиса на локтях и коленях.
- Образование гематом, которые долго проходят.
- Постоянные трещины на слизистой рта.
- Ломкость ногтей.
- Изменение обоняния и вкуса: пристрастие к резким запахам, желание есть землю, мел.
- Быстрая утомляемость.
- Частые ОРВИ с тяжелым течением.
При обнаружении подобных симптомов следует обратиться к врачу.
Клинические проявления тяжелой степени патологии

Клиническая картина анемии состоит из двух фаз: хроническая гемодепрессия и тяжелая (финальная) стадия.
При гемодепрессии наблюдаются следующие проявления:
- Значительное повышение температуры, лихорадка.
- Резкий упадок сил.
- Общее плохое самочувствие.
- Снижение веса.
- Увеличение внутренних органов: селезенки, печени.
- Увеличение и болезненность лимфатических узлов.
Подобные состояния затяжные, с периодами ремиссии.
Симптомы тяжелой степени рефрактерной анемии (миелодиспластический синдром) такие же, как при остром лейкозе. Болезнь развивается стремительно. Одной из ее особенностей является обнаружение бластов в анализе крови. Заболевание сопровождается следующими симптомами:
- Гематомы, даже при незначительных ушибах.
- Кровоточивость десен.
- Гингивит.
- Бинокулярное смещение глазного яблока.
- Упорные повторные воспалительные процессы в носоглотке.
- Нагноение царапин, небольших ран.
- Боли в области позвоночника.
У пациентов пожилого возраста возникают вторичные заболевания, чаще поражается сердечно-сосудистая система. Пациенты испытывают боли при ходьбе в нижних конечностях.
Диагностические мероприятия
При первых подозрительных симптомах необходимо обратиться к доктору. Диагноз "миелодиспластический синдром" или "рефрактерная анемия с избытком бластов" ставится только после прохождения ряда лабораторных исследований. Они включают:
- Клинический анализ периферической крови.
- Цитологические исследования аспирата костного мозга.
- Трепанобиопсия заключается во взятии биоматериала из костного мозга путем прокола большеберцовой кости.
- Цитогенетический тест. Анализ выявляет хромосомные нарушения, является обязательным.
В зависимости от клинической картины заболевания могут быть назначены дополнительные диагностические мероприятия:
- УЗИ брюшной полости.
- Эзофагогастродуоденоскопия желудочно-кишечного тракта.
- Анализ на специфические онкомаркеры.
Методы терапии
Выбор способа лечения рефрактерной анемии обусловлен выраженностью клинических проявлений и результатами лабораторных исследований. Схемы терапии довольно сложны и определяются врачом. Пациенты с небольшим количеством бластов находятся в группе низкого риска. Они получают заместительное и поддерживающее лечение и могут вести практически обычный образ жизни. Приблизительная схема лечения такова:
Прогнозирование
Прогноз рефрактерной анемии (миелодиспластический синдром) зависит от клинической картины, ответной реакции организма на терапию, своевременности обращения за медицинской помощью. Исход заболевания обусловлен выраженностью дефицита определенных клеток, наличие и профиль хромосомных отклонений, количество бластов и их тенденцию к развитию в крови и костном мозге.
Профилактика

Ввиду того что сущность, обстоятельства и механизмы развития патологии до конца еще не исследованы, то и действенные профилактические методы назвать практически невозможно. Врачи советуют придерживаться следующих рекомендаций по сохранению здоровья:
- Правильно сбалансировано питаться.
- Включать в рацион продукты с высоким содержанием железа.
- Чаще совершать прогулки на свежем воздухе.
- Отказаться от вредных привычек, в частности курения.
- При работе с пестицидами или органическими растворителями применять средства защиты.
Рефракторная анемия – опасное гематологическое заболевание, переходящее в онкологию. Чтобы избежать тяжелых стадий заболевания и серьезных последствий, необходимо регулярно проводить плановый осмотр. При обнаружении патологии необходимо полностью пройти курс терапии, многим пациентам это помогло не только улучшить, но и продлить жизнь.
В12 фолиеводефицитная анемия (пернициозная, мегалобластная) – болезнь, сопровождающаяся патологическими отклонениями в процессах кроветворения. Обусловлено состояние нехваткой витамина В12 (кобаламина). Выражается в значительной нехватке красных кровяных клеток (эритроцитов), железосодержащего белка, поражении ЦНС и ЖКТ. Болезнь диагностируется относительно редко и чаще всего выявляется у пожилых людей. Встречается у беременных женщин. Проходит самостоятельно после родоразрешения.
Что такое b12 дефицитная анемия

В12-дефицитная анемия входит в группу мегалобластных состояний. Для нее типично снижение гемоглобина, объема эритроцитов из-за недостаточного поступления, быстрого расходования витамина В12, фолиевой кислоты.
Дефицит химических соединений провоцирует поражение костного мозга. Патологический процесс захватывает нервные ткани. Заболевание опасно не только гипоксией тканей органов. Оно способно вызывать тяжелые поражения головного мозга.
Патология была впервые диагностирована английским медиком Томасом Аддисоном. Но название дано по фамилии немецкого врача Антона Бирмера, описавшего клиническую симптоматику состояния.
Дефицит В12 и фолиевой кислоты провоцирует серьезные отклонения в процессе образования ДНК, что вызывает нарушения процесса продуцирования клеток красных кроветворных ростков. Состояние сопровождается признаками нарушения эритрогенеза: диагностическим путем фиксируется снижение числа эритроцитов и гемоглобина. Данный тип анемии нередко сопровождается развитием тромбоцитопении и нейтропении.
Причины В12 фолиеводефицитной анемии
Причины В12 дефицитной анемии разнообразны. Таковыми выступают:
- нехватка поступающих витаминов;
- синдром мальабсорбции;
- усиленное расходование имеющихся резервов кобаламина;
- наследственные патологии, характеризующиеся нарушениями обменных процессов В12.
Организм не приспособлен к самостоятельному продуцированию кобаламина. Восполнение запасов происходит за счет его поступления вместе с едой. Основным источником служат мясная, рыбная продукция, кисломолочные продукты.

Приготовление продуктов путем термической обработки витамин В12 частично уничтожает и это также необходимо учитывать при составлении рациона. Причиной дефицита становится соблюдение принципов вегетарианства и злоупотребление спиртосодержащими напитками.
Вторая вероятная причина – нарушение процессов усвоения кобаламина слизистыми ЖКТ, обусловленные воспалением слизистой оболочки кишечника (тонкого отдела), паразитарные инфекции и нарушения процесса формирования фактора Касла.
Фактор Касла – обязательное условие полноценного усвоения кобаламина. В противном случае всасывания фолиевой кислоты становится невозможным, она выводится вместе с каловыми массами.
Провоцировать нехватку внутреннего фактора Касла способны следующие патологии.
- Заболевания желудочно-кишечного тракта, в частности, воспаление слизистой желудочного мешка, протекающее в атрофической и аутоиммунной форме. В первом случае фиксируется уменьшение его размера и нарушение функциональных возможностей, во втором – происходит нарушение иммунной функции.
- Злокачественное образование желудка.
- Удаление желудка (гастрэктомия).
- Врожденная нехватка фактора Касла. Обусловлена дефектом гена, что способствует нарушению продуцирования секрета желудочными клетками.
Усвоение витамина осуществляется через слизистые тонкого кишечника. Нарушать причины способны следующие патологии:
- энтериты;
- опухолевые новообразования;
- резекция части тонкого кишечника;
- причиной выступают паразитарные инфекции.
Активное потребление кобаламина происходит в следующих случаях:
- во время беременности;
- при гипертиреозе (повышенной активности щитовидной железы);
- из-за наличия злокачественных опухолей.
Нарушать обменные процессы могут наследственные патологии, в частности, наследственный дефицит транскобаламина II, синдром Имерслунд-Гресбека и другие.
Патогенез

Поступление витамина В12 возможно исключительно с белковой пищей. Соединившись в желудочном мешке с внутренним фактором Касла, попадая в кишечник, он успешно усваивается слизистой тонкого отдела ЖКТ. При нарушении его всасывания формируется В12 дефицитная анемия, поскольку кишечный тракт расщепляет пищевой ком и выводит витамин вместе с каловыми массами.
Состояние становится причиной нарушения функций кроветворения, Характеризуется падением числа эритроцитов и гемоглобина. Витамин В12 транспортируется в костный мозг, где участвует в процессе создания эритроцитов. При его дефиците отмечается нехватка красных кровяных телец.
При развитии мегалобластной анемии отмечаются значительные нарушения гемопоэза, что сопровождается характерными изменениями структуры клеток красной и белой крови. Меняется тип кроветворения (нормобластическое увеличение ретикулоцитов характерно для полностью здорового человека). Клетки костного мозга имеют молодое ядро в сочетании со старой цитоплазмой. Регистрируется большое количество базофильных мегалобластов.
Симптомы b12 дефицитной анемии
Симптомы В12-дефицитной анемии способны проявиться спустя несколько лет после формирования патологического состояния. Заболевание прогрессирует медленно и среди его первых признаков стоит выделить:
- слабость;
- утомляемость.
По мере дестабилизации положения формируется характерная клиническая картина. К основным симптомам относят:
- нарушения процесса эритропоэза;
- поражение ЖКТ;
- отклонения в работе центральной и периферической нервной системы.
Для В12-фолиеводефицитной анемии характерно уменьшение уровня эритроцитов. Типичными признаками нарушения кроветворения становятся ниже приведенные.
- Бледность, желтушность кожного покрова, слизистых оболочек – состояние формируется медленно, на протяжении нескольких месяцев, обусловлено нехваткой гемоглобина и повышенным содержанием билирубина.
- Тахикардия – вызвана гипоксией органов.
- Сердечные боли, вызванные активной работой миокарда на фоне нехватки кислорода.
- Негативная реакция на физические нагрузки – быстрая утомляемость, головокружение и т.д.;
- Головокружения, регулярные обмороки – провоцируются кислородным голоданием головного мозга;
- Мелькание мушек в поле зрения;
- Увеличение размера селезенки, обусловленное закупоркой капилляров органа большими по размерам эритроцитами.
Во время заболевания может диагностироваться хроническое легочное сердце – комплексное нарушение гемодинамики. Встречается редко.

Нарушения деятельности пищеварительной системы – один из ранних симптомов анемического состояния. Признаками можно прочитать ниже.
- Сложности с пищеварением, обусловленные нехваткой пищеварительных соков и ферментов.
- Нарушения стула – наблюдается чередование запоров с поносами.
- Ухудшение аппетита – объясняется сниженной секрецией желудочного сока из-за формирования атрофического гастрита.
- Потеря веса – вызвана развитием частичной/полной анорексии и нарушениями процесса переваривания пищевого кома.
- Изменение формы и цвета языка – он получает яркий малиновый оттенок и становится совершенно гладким.
- Нарушение вкусовосприятия.
- Регулярные воспаления слизистой ротовой полости – стоматит, глоссит, гингивит.
- Болезненность и ощущение жжения во рту – спровоцированы поражением нервных окончаний.
- Боли в животе, формирующиеся после еды.
- Заболевания кишечника (целиакия).
Симптоматика неспецифична и способна сопровождать иные патологии.
Поражения центральной нервной системы объясняются непосредственным участием кобаламина в продуцировании миелиновых оболочек. Нарушение процессов провоцирует развитие симптоматики неврологического характера.
Поражается мозг, клинические проявления будут следующими:
- нарушение чувствительности – формируется на любых участках тела;
- парестезии (мурашки);
- отсутствие согласованности в работе мышц – проявляется в потере равновесия, неуклюжести и т.д.;
- снижение мышечной силы – выражается атрофии мышечного корсета;
- проблемы с опорожнением кишечника и мочевого пузыря – проявляются задержкой либо недержанием;
- психические отклонения – бессонница, депрессивные состояния, тяжелые психозы, галлюцинации.
Неврологические симптомы формируются последовательно. Первыми поражаются ноги, далее живот и тело, следующими – пальцы рук, шея, лицо и голова. Самыми последними развиваются расстройства психического характера.
В12-дефицитная анемия для ребенка – у детей и взрослых она сопровождается одинаковыми симптомами – представляет особую опасность.
Диагностика
Диагностика В12 дефицитной анемии включает следующие мероприятия.
- Сбор жалоб.
- Физикальный осмотр.
- Анализ крови. Выявляется уменьшение количества ретикулоцитов, красных кровяных клеток (эритроцитов). Патология сопровождается малокровием.
- Исследование мочи.
- Биохимия крови. Помогает определить уровень холестерола, глюкозы, мочевой кислоты, креатина и т.д. Для заболевания типичен повышенный уровень билирубина.
- Анализ костного мозга. Исследование пунктата дает возможность получить достоверные признаки заболевания: ускоренное формирование красных кровяных клеток, мегалобластический тип кроветворения.
- ЭКГ. Определяет частотность сокращений миокарда.
При диагностировании В12-дефицитной анемии больному в случае необходимости назначается консультация врача общей практики.
Лечение

Лечение В12-дефицитной анемии предусматривает сочетанный подход, поскольку медикам необходимо восстановить функциональность сразу трех систем.
Медикаментозное лечение b12-дефицитной анемии – получение пациентом дефицитного витамина искусственным путем. Показанием к терапии витамином В12 признается подтвержденный диагноз и наличие четкой клинической картины анемического состояния.
Кобаламин предпочтительно вводить внутримышечным путем, но допускается прием его таблетированной формы. Последний вариант используется, если доказана нехватка элемента из-за плохого питания.
Схему лечения В12 подбирают индивидуально. В начале это 500,0 – 1000,0 мг, вводимых внутримышечным способом один раз в сутки. Затем дозы витамина В12 при анемии пересматриваются.
Общая продолжительность лечения достигает 6 недель. После этого пациент получает поддерживающую дозу. Он будет получать по 200 – 400 мг препарата (две – четыре инъекции в месяц). Иногда на протяжении все жизни.
Принимая кобаламин, необходимо контролировать эффективность лечебного протокола. Для этого больной должен два – четыре раза в неделю сдавать кровь для проверки эффективности и коррекции терапии. После восстановления показателей выполняется перевод на поддерживающую терапию. Сдача крови выполняется только единожды в месяц.
При диагностировании дефицита цианокобаламина практикуется гемотрансфузия. Но предпочтительнее переливать эритроцитарную массу. Реализуется методика только при тяжелом течении анемии, существующей угрозе жизни человека.
Показанием становится снижение уровня гемоглобина ниже 70 г/л. Гемотрансфузия практикуется при наличии симптомов прекоматозного состояния или впадения больным в анемическую кому. После стабилизации состояния переливания прекращаются.
Важным этапом терапии становится коррекция действующего рациона. Дефицит кобаламина на начальных стадиях развития успешно лечится путем соблюдения принципов диетического питания. Состав дневного меню должен включать:
- сливовый сок;
- овощи зеленого цвета;
- зерновые;
- масло;
- сливки;
- мясо;
- помидоры;
- морковь;
- свеклу;
- кукурузу;
- субпродукты – печень и сердце;
- рыбу – треска, скумбрия, карп;
- мясо кролика.
Эти продукты содержат большой процент фолиевой кислоты, витамина В12.
Составлением диетического меню при диагностировании анемического состояния должен заниматься специалист, исходя из текущей симптоматики и имеющихся нарушений здоровья. Учитывается восприимчивость организмом различных продуктовых групп.
Профилактика b12 дефицитной анемии
Профилактика б12-дефицитной анемии включает несколько мероприятий.
- Включение в рацион продуктов, содержащих большое количество кобаламина.
- Своевременное лечение патологий, способствующих формированию анемического состояния, в частности, глистных инвазий.
- Назначение поддерживающих дозировок кобаламина в течение послеоперационного периода по поводу резекции желудка/кишечника.
При выявленном дефиците витамина В12 крайне важно соблюдать все рекомендации лечащего доктора. При раннем диагностировании анемической патологии и своевременно начатом лечении прогноз исхода заболевания благоприятный. Стабилизация состояния наблюдается через месяц после начала терапии.
Читайте также:

