При остром недифференцированном лейкозе в крови преобладают
Недифференцированная (острая) форма лейкоза, именуемая ранее гемоцитобластозом, характеризуется глубокими поражениями кроветворной ткани с появлением в крови и увеличением в кроветворных органах недифференцированных клеток. Исходя из этого, достоверный диагноз может быть поставлен только путем морфологических исследований. Острый лейкоз в большинстве своем приводит к тотальному замещению опухолевыми клетками костного мозга, к распространению их в селезенке, лимфатических ушах, печени и других органах. Исходя из этого, зачастую невозможно установить стадийность течения данного заболевания. При локальном поражении происходит обсеменение других органов бластными клетками с последующим выходом их в периферическую кровь. При генерализованном же течении бластные клетки обнаруживают почти одновременно во всех пораженных кроветворных и негемопоэтических органах.
У людей острые лейкозы подразделены на ряд вариантов в зависимости от преимущественного поражения клеток того пли иного ростка гемопоэза (миелобластный, промислоцитарный, лимфобластный, монобластный и др.). У крупного рогатого скота была дифференцирована в основном лимфобластная форма лейкоза, так как при этой форме в крови и кроветворных органах превалируют в основном лимфоидные клетки разной степени зрелости. В нашей работе недифференцированные клетки были представлены в макро-, мезо- и микрогенерации, что и обусловливало характер течения болезни. При классическом варианте болезни, когда задержка дифференциации клеток происходит за счет макро- и мезогенерации, наблюдается острое и подострое течение процесса Микроклеточный вариант протекает по типу хронического лимфолейкоза.
Острое течение болезни отмечается у животных молодого возраста (до 3 лет) с продолжительностью болезни в несколько месяцев, подостpoe — у коров в возрасте 4—5 лет с нарастанием патологических изменений в течение 1—3 лет. Микроклеточный вариант протекает хронически (в течение 3—6 лет) с обострением процесса в конце болезни.
Периферическая кровь характеризуется сублейкемическим и лейкемическим уровнем лейкоцитоза с пределами колебания от 15,6 до 308,8 тыс/мкл лейкоцитов. Лишь у одного теленка был установлен алейкемический состав крови на всем протяжении болезни. Уровень лейкоцитоза зависел от характера течения процесса. При быстром течении болезни с короткой ее продолжительностью количество родоначальник клеток не достигало больших величии. При подостром течения с пролиферацией недифференцированных клеток макро- и мезогенерации, а также лимфоидных клеток разной степени зрелости количество лейкоцитов, постепенно увеличиваясь, достигает лейкемического уровня. При хроническом течении процесса с превалированием недифференцированных клеток микрогенерации количество лейкоцитов, прогрессивно нарастая, достигает до сотен тысяч в 1 мкл крови.
Количество эритроцитов и уровень гемоглобина у исследованных нами животных составили в среднем 4,3 млн/мкл и 7,6 г% с пределами колебания соответственно от 2,8 до 5,8 млн/мкл и от 4,8 до 10,0 г%. Сильная анемия отмечалась на поздних стадиях болезни и зависела от степени подавления эритробластического ростка костного мозга.
При микроклеточном варианте количество лейкоцитов в крови было увеличено за счет лимфоцитоподобных клеток. Они имели размер среднего лимфоцита (7—8 мкм в диаметре), округлую форму, узкую цитоплазму, центральное расположение ядра, нежно-сетчатую или извилисто-петлистую структуру хроматина ядра с наличием одной большой или 2—3 мелких нуклеолей. При этом варианте болезни число клеток микрогенерации в среднем по группе животных было 73,89% с пределами колебания от 18 до 91%, а макрогенерации — 5—10%. При классическом вариантe недифференцированного лейкоза число молодых клеток макро- и мезогенерации, а также пролимфоцитов и лимфобластов составило в среднем 13,78% с пределами колебания от 4,5 до 80,0%. Чем больше таких клеток в крови, тем тяжелее и острее протекал процесс.
Наряду с увеличением в крови вышеуказанных видов клеток отмечается значительное уменьшение относительного и абсолютного содержания базофилов, эозинофилов, нейтрофилов и моноцитов. Однако в ряде случаев абсолютное количество тех или других видов клеток остается в пределах нормы. Это объясняется тем, что данный росток костного мозга не подавлен и процесс дифференциации клеток в этом направлении остается не нарушенным.
Клинические симптомы и патологоанатомические изменения также зависят от характера течения болезни. При хроническом течении на ранних стадиях ее развития клинические симптомы и патологоанатомические изменения отсутствуют. На поздних стадиях, при подостром и остром течении, отмечаются увеличение размеров селезенки (в 87,5% случаев) и лимфатических узлов (в 54,2% случаен), бледность видимых слизистых оболочек с желтушным оттенком. Опухолевые разрастания во внутренних органах (сердце, легкие и др.) и увеличение размеров печени, наблюдаемые в редких случаях, обусловливают появление неспецифических клинических симптомов (нарушение деятельности сердца, желудочно-кишечного тракта и др.).
Цитоморфологические изменения в кроветворных и других пораженных органах выражаются в значительном повышении числа недифференцированных элементов при уменьшении промежуточных форм между зрелыми и родоначальными клетками. В связи с этим в мазках обнаруживается широкий спектр цитоморфологических изменений. Часто отмечается параллелизм между изменениями в периферической крови и костном мозге. Степень этих изменений зависит от характера течения болезни и популяции клеточных элементов.
Нарушение костномозгового кроветворения проявляется подавлением функции миело- и эритропоэза па фоне размножения недифференцированных клеток. Количество миелобластических и эритробластических клеток в миелограммах уменьшается соответственно от 46,4 до 6,9 и от 50,2 до 6,2%. Почта полное подавление белого ростка отмечали в 33%, а красного — в 25% случаев из числа больных животных. При классическом варианте болезни число клеток макро- и мезогенерации увеличивалось до 54,5%, а пролимфоцитов и лимфобластов — до 31,9%. В ряде случаев наблюдали почта тотальную пролиферацию молодых клеток с подавлением всех ростков костномозгового кроветворения. При микроклеточном варианте число молодых и лимфоидных клеток всех степеней зрелости достигало 91,5%.
Изменение количественного соотношения остальных видов клеток в миелорамме не имеет патогномоничного значения в патологии этой формы лейкоза. Увеличение фигур митоза и амитоза наблюдается при одновременном повышении числа недифференцированных клеток.
Клеточные изменения в мазках из пунктатов селезенки и лимфатических узлов также зависят от формы течения острого лейкоза. При классическом варианте и чрезмерном увеличении размеров органов превалирует число крупных клеток с нежно-сетчатым хроматином ядра, лимфобластов и пролимфоцитов за счет полного или частичного вытеснения зрелых лимфоцитов. В мазках из пунктатов они располагаются равномерно, а в мазках-отпечатках образуют обширные скопления, занимающие несколько полей зрения.
На ранних стадиях болезни и при микроклеточном варианте повышено число лимфоцитоподобных клеток с нежной структурой ядра и наличием ядрышек. Наряду с этим до 10—15% клеточных элементов составляют крупные генерации, пролимфоциты и лимфобласты. Степень омоложения клеток зависит от продолжительности и тяжести болезни, объема увеличенного органа. По мере прогрессирования болезни повышается число митотически (при классическом варианте) и амитотически (при микроклеточном варианте) делящихся клеток.
Гистологически в срезах селезенки выявляется выраженная гиперплазия фолликулов с увеличением их центров размножения. В ткани селезенки происходит старание границ белой и красной пульпы. В срезах из лимфоузлов установлено, что пролиферация молодых клеток начинается обычно с межфолликулярных участков. В зависимости от тяжести процесса границы коркового и мозгового слоев, а также очертания фолликулов в центре размножения имеют ту или иную степень выраженности.
Другие органы (печень, почки, сердце и др.) при их поражении были инфильтрированы теми же молодыми недифференцированными клетками всех трех генераций, число которых зависело от степени поражения органа. Эта инфильтрация приводила к резкому нарушению их структуры и дистрофическим изменениям.
Таким образом, при остром лейкозе происходит нарушение дифференциации родоначальных клеток. Это приводит к повышению их количества в пораженных органах и поступлению в периферическую кровь.
Острый лейкоз крови – что это такое? Под данным диагнозом подразумевают онкологическое заболевание, при котором у пациента нарушается состав крови. Это приводит к кислородному голоданию органов и тканей, а также к критическому снижению иммунитета: для жизни больного с острой лейкемией угрозу представляет даже обычное ОРЗ или ОРВИ.
Как возникает острая лейкемия
Механизм развития патологии следующий. В норме клетки крови созревают из стволовых клеток. На определенной стадии они дифференцируются, то есть, их развитие идет по одному из путей. Из таких клеток вырастают либо эритроциты, либо тромбоциты, либо лейкоциты, либо лимфоциты.
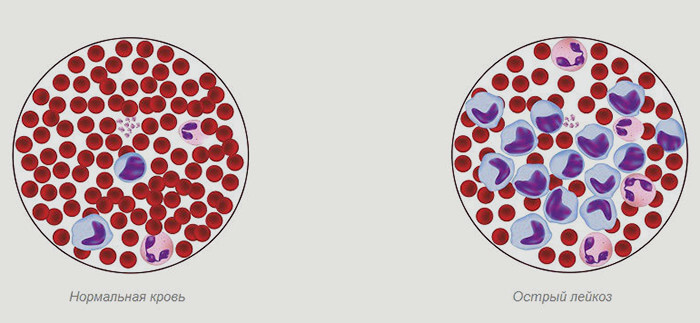
При остром лейкозе крови стволовые клетки мутируют на самых ранних стадиях развития, еще незрелыми. В результате такой мутации они не могут развиваться по здоровому алгоритму. Далее атопичные бластные клетки начинают активно делиться, попадают в большом количестве в кровеносное русло человека и постепенно замещают собой нормальные клетки. Результатом становятся неполноценное функционирование органов и тканей, нарушение свертываемости крови и снижение защитных сил организма.
По приблизительной статистике (точных данных по России на сегодняшний день нет) острая лейкемия диагностируется ежегодно у 4500-5000 пациентов. Среди них как взрослые, так и дети. Среди первых мужчины более склонны к развитию патологии, нежели женщины. Кроме того, особенно подверженными болезни считаются взрослые старше 60-65 лет. Что касается детей, чаще болеют раком крови дошкольники, среди младших школьников и подростков заболевание встречается реже.
Причины острого лейкоза крови
В онкологии и гематологии рассматривают, скорее, не причины, а факторы риска, которые могут спровоцировать старт онкопатологии. По результатам многолетних исследований генетика – основная причина острого лейкоза. Именно наследственным фактором обусловлен наибольший процент этого онкологического заболевания. Незрелая клетка мутирует по причине ошибки в ДНК, то есть, эта мутация присутствует в организме еще до рождения. Все остальные причины лишь способствуют запуску процесса.
Именно поэтому врач всегда старается тщательно изучить семейный анамнез пациента. Чем больше в его истории родственников с аналогичным диагнозом, особенно, близких единокровных, тем выше риск заболевания у обследуемого.
Существуют также заболевания генетической природы, повышающие вероятность развития острого лейкоза. Это в частности:
- синдром Дауна;
- болезнь Клайнфельтера;
- синдромы Вискотта-Олдрича и Луи-Барра;
- анемии Фанкони и прочие.
Данное обстоятельство также учитывается лечащим врачом при диагностике острой лейкемии.

Среди причин возникновения острого лейкоза в качестве провоцирующих факторов выделяют:
- воздействие промышленных канцерогенов – бензолов, силикатов, аминов, диоксинов, свинца, асбеста, мышьяка и других;
- регулярное длительное воздействие ультрафиолетового излучения;
- значительная разовая или длительная доза радиоактивного облучения;
- продолжительный прием некоторых лекарственных препаратов, например, цитостатиков при химиотерапии;
- лучевая терапия;
- тяжелые инфекционные заболевания – туберкулез, гепатит, СПИД, сифилис, прочие;
- вирусы, угнетающие имунную систему, например, Т-лимфотропный вирус и вирус Эпштейна-Барра.
Также существуют исследования, доказывающие, что причиной возникновения острой лейкемии, точнее, предпосылкой к манифесту заболевания, могут стать табакокурение, неумеренное употребление жареных блюд и промышленных полуфабрикатов с высоким индексом канцерогенности.
Виды острого лейкоза
Все острые лейкемии подразделяют на две группы: острые лимфобластные лейкозы и острые нелимфобластные или миелоидные лейкозы.
Лимфобластные формы, в свою очередь, делят на:
- пре-В-форму, при которой преобладают предшественники B-лимфобластов;
- В-форму – если в крови преобладают B-лимфобласты;
- пре-Т-форму, когда среди атопичных клеток преобладают предшественники Т-лимфобластов;
- Т-форму, при которой преобладают Т-лимфобласты.
Острый лимфобластный рак крови вначале поражает костный мозг, затем распространяется на лимфатические узлы, вилочковую железу и селезенку. Такая онкология крови считается не слишком благоприятной с точки зрения дальнейших прогнозов.

Нелимфобластные лейкозы классифицируют следующим образом:
- острый миелобластный лейкоз с большим количеством клеток-предшественников гранулоцитов;
- острый монобластный, а также миеломонобластный лейкозы – их диагностируют в том случае, если в организме пациента наблюдается активное деление монобластов;
- острый эритробластный лейкоз – в анализах обнаруживается высокий уровень эритробластов;
- острый мегакариобластный лейкоз – характеризуется активным делением клеток-предшественников тромбоцитов.
При остром нелимфобластном лейкозе прогноз является более благоприятным, нежели в предыдущем случае.
Если же определить форму заболевания достоверно не удается, врачи ведут речь об остром недифференцированном лейкозе.
Симптомы острого лейкоза
Все клинические признаки этого заболевания можно разделить на четыре группы:
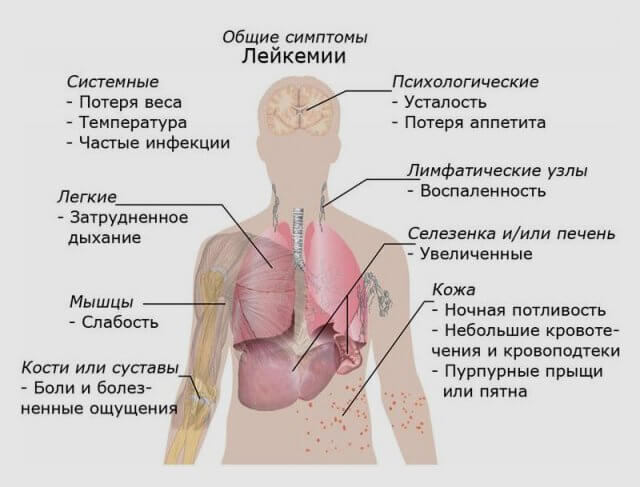
- анемические симптомы острого лейкоза проявляются в виде одышки при минимальных нагрузках и в состоянии покоя, учащенного сердцебиения, бледности кожных покровов, быстрой утомляемости, сонливости. Анализ периферической крови в этом случае показывает снижение уровня гемоглобина;
- инфекционно-токсическая группа признаков заболевания представлена развитием таких сопутствующих патологий как ангина, стоматит, остеомиелит, бронхит, пневмония, различные абсцессы и флегмоны, а также потеря аппетита и снижение веса, слабость, повышенное потоотделение, повышение температуры тела. У больного могут наблюдаться костные и суставные боли разной локализации – от позвоночника до фаланг пальцев;
- к геморрагическим симптомам острой лейкемии относят подкожные кровоподтеки разных размеров, внутренние и наружные кровотечения, обусловленные снижением уровня тромбоцитов в крови. Для острого промиелоцитарного лейкоза характерен также ДВС-синдром – нарушение свертываемости крови, вызванное повышенным тромбообразованием;
- пролиферативные признаки заболевания включают в себя увеличение лимфоузлов, печени и селезенки. На поздних стадиях при остром лейкозе часто развиваются так называемые лейкемиды. Это скопления лейкоцитов, выступающие над уровнем кожи в виде опухолей.
Определить манифест заболевания, ориентируясь только на жалобы больного, сложно. Большинство симптомов могут указывать на наличие целого ряда патологий, к тому же, зачастую на начальных стадиях острого лейкоза они бывают слабовыраженными. Поэтому установить точный диагноз можно только после полного обследования пациента.
Для начала врач опрашивает пациента и собирает анамнез. В нем указываются, помимо наследственной предрасположенности, обстоятельства, которые с той или иной степенью вероятности могли привести к возникновению заболевания. В основном это влияние факторов окружающей среды и особенности образа жизни пациента.
На следующем этапе больному назначаются следующие лабораторные и аппаратные диагностические процедуры:
- общий и биохимический анализ крови;
- спинальная пункция с последующим исследованием клеток костного мозга;
- рентгенография костей и суставов;
- УЗИ печени, селезенки, лимфоузлов.
На основании такой диагностики острого лейкоза врач получает возможность с высокой степенью достоверности определиться с диагнозом. Наиболее показательной процедурой в этом плане является биопсия костного мозга.
Кроме того, для оценки тяжести сопутствующих патологий рекомендуется осмотр смежными специалистами – неврологом, гастроэнтерологом, кардиологом, стоматологом и другими.
Лечение заболевания осуществляется исключительно в условиях стационара. Основным методом является химиотерапия препаратами-цитостатиками. Как правило, она проходит в два этапа. На первом этапе, который называют индукцией ремиссии, воздействие направлено на максимально возможное уменьшение количества бластных клеток. Второй этап – консолидация – предполагает уничтожение оставшихся злокачественных клеток.
Количество сеансов химиотерапии, а также дозы препаратов подбираются индивидуально, с учетом возраста больного, стадии заболевания, наличия и тяжести сопутствующих патологий.
Наиболее эффективным подходом является лечение острого лейкоза посредством трансплантации костного мозга. В результате такой процедуры пациент получает здоровые стволовые клетки, которые начинают делиться и таким образом запускают процесс восстановления кроветворной системы. Однако такой метод сопряжен с рядом сложностей:
- необходимо найти максимально совместимого донора;
- перед процедурой пациент получает иммуносупрессивную терапию. Она направлена на уничтожение поврежденных лейкозных клеток и практически полное подавление иммунитета. В этот период организм больного становится восприимчивым даже к малейшим инфекциям;
- после пересадки важно, чтобы организм пациента не отторгнул донорский костный мозг.
В силу вышеперечисленного трансплантация костного мозга доступна далеко не всем.
В период пребывания на стационарном лечении больной раком крови должен находиться в абсолютно стерильных условиях. Контакты с посетителями следует исключить либо свести к минимуму. Если пациент лежачий, важно уделять должное внимание профилактике пролежней и гипостатической пневмонии.
Прогноз при этом заболевании относят к условно позитивным. По данным медицинской статистики добиться стойкой ремиссии можно в 80% случаев. Длительной считается ремиссия сроком более 5 лет. В 20% случаев врачи говорят о полном выздоровлении пациента.
У детей с острым лейкозом, получающих адекватное лечение, перспективы является более благоприятными, нежели у взрослых. Наиболее осторожно врачи прогнозируют будущее тех, кто заболел в возрасте старше 60 лет. Это связано с наличием сопутствующих патологий и тяжелыми реакциями на химиотерапию.
Частота рецидивов заболевания зависит от его формы. Как уже было сказано ранее, лимфобластные лейкозы хуже поддаются лечению, чем нелимфобластные. Прогноз по первым также менее благоприятен, а рецидивы происходят чаще, чем при второй форме. Наиболее опасным среди нелимфобластных лейкемий считается острый миелобластный лейкоз.
По патогенетическому принципу, исходя из особенностей морфологической характеристики лейкозных клеток, лейкозы подразделяют на острые и хронические. К острым лейкозам относят опухоли с полной остановкой дифференпировки родоначальных кроветворных клеток на каком-то уровне созревания; субстрат опухоли составляют клетки II, III и IV классов по современной схеме кроветворения (см. рис. 64). В группу хронических лейкозов входят опухоли с частичной задержкой созревания клеток и накоплением клеток определенной степени зрелости.
Острые лейкозы.
Гематологическая картина в развернутой стадии, заболевания характеризуется классической триадой - лейкоцитозом, появлением в крови большого числа бластных клеток и так называемым лейкемическим зиянием (hiatus leukaemicus), когда в периферической крови преобладают бластные клетки, имеется небольшой процент зрелых лейкоцитов и практически отсутствуют промежуточные формы созревания. Уже на ранних стадиях болезни отмечаются нормохромная анемия и тромбоцитопения, развитие которых обусловлено угнетением нормального гемопоэза вследствие лейкемической трансформации кроветворения.
Составляющие субстрат опухоли бластные клетки при различных вариантах острого лейкоза морфологически трудно различимы, но могут быть дифференцированы с помощью цитохимических методов по разнице в содержании ферментов (рис. 69). Исходя из особенностей цитохимических свойств лейкозных клеток, в большинстве современных классификаций острые лейкозы подразделяют на миелобластный, лимфобластный, промиелоцитарный (Термин "острый промиелоцитарный лейкоз" в значительной мере является условным, поскольку опухоль состоит не из промиелоцитов, а из атипичных бластных клеток (миелобластов), цитоплазма которых богата крупной зернистостью), монобластный, эритромиелоз, мегакариобластный и недифференцированный (табл. 26). Выделенные нозологические формы различаются также по клиническим признакам и, что особенно важно, по ответу на цитостатическую медикаментозную терапию. У взрослых больных чаще встречаются миелобластный и лимфобластный, у детей - лимфобластный и (реже) недифференцированный варианты острого лейкоза.
Острый миелобластный лейкоз.
Представляет собой опухоль, исходящую из клетки-предшественницы миелопоэза и состоящую преимущественно из родоначальных клеток гранулоцитарного ряда - миелобластов.
Острый лимфобластный лейкоз.
Это опухоль, возникающая из клеткипредшественницы лимфопоэза. Поверхностные мембраны составляющих субстрат опухоли бластных клеток у одной трети больных несут маркеры Т-клеток (Т-клеточный вариант), однако чаще всего поверхностные Т- и В-маркеры при остром лимфобластном лейкозе не обнаруживаются (не Т-, не В-форма или 0-бластный вариант).
У 50 % взрослых больных с острым миелобластным лейкозом и у 80 % детей с острым лимфобластным лейкозом обнаруживаются бластные клетки с аномальным кариотипом (анэуплоидия, изменения структуры хромосом).
Острый недифференцированный лейкоз.
Морфологический субстрат опухоли представлен клетками II - III классов по современной схеме кроветворения; морфологически они напоминают лимфобласты, но отличаются цитохимической интактностью.
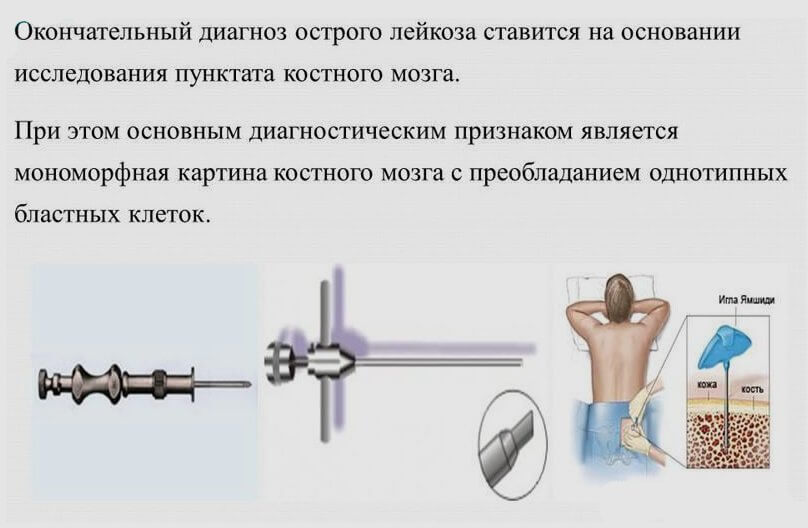
Окончательный диагноз острого лейкоза (особенно в тех случаях, когда лейкемические клетки не выходят в периферическую кровь) должен ставиться на основании исследования пунктата костного мозга. При этом основным диагностическим признаком является мономорфная картина костного мозга с преобладанием однотипных бластных клеток. Морфологические критерии последних очень изменчивы; как и все опухолевые клетки, лейкемические бласты атипичны, отличаются прогрессирующей анаплазией. По мере прогрессирования заболевания вследствие опухолевой прогрессии и под влиянием цитостатической терапии бластные клетки могут до неузнаваемости изменять свою морфологию, утрачивать ферментную специфичность.
Хронические лейкозы.
В несколько упрощенном виде классификацию хронических лейкозов можно представить в следующем виде: хронический миелолейкоз, хронический моноцитарный лейкоз, эритремия, хронический лимфолейкоз, миеломная болезнь, макроглобулинемия Вальденстрема.
Хронический миелолейкоз.
Одно из самых частых заболеваний в группе лейкозов; опухоль, исходящая из клетки-предшественницы миелопоэза. Морфологическим субстратом хронического миелолейкоза являются зрелые и созревающие клетки гранулоцитарного ростка кроветворения. В типичном случае (наличие Рр'-хромосомы в кроветворных клетках костного мозга) характерен нейтрофильный лейкоцитоз с выраженным ядерным сдвигом влево: обнаруживаются единичные миелобласты, промиелоциты, миелоциты, метамиелоциты, палочко- и сегментоядерные формы гранулоцитов. Как правило, развивается гипертромбоцитоз. У детей чаще наблюдается ювенильная (Рh-негативная) форма хронического миелолейкоза, характеризующаяся высоким моноцитозом и тромбоцитопенией. Весьма частым признаком хронического миелолейкоза, особенно у детей, является увеличение числа базофилов и эозинофилов (базофильно-эозинофильная ассоциация). Важным диагностическим признаком заболевания является увеличение селезенки и печени, что связано с лейкозной инфильтрацией и появлением очагов миелоидного кроветворения в этих органах.
Развернутая стадия хронического миелолейкоза закономерно переходит в терминальную фазу, характеризующуюся так называемым "бластным кризом" (появление в костном мозге и в периферической крови значительного числа бластных клеток), прогрессирующей цитопениеи (анемия, лейко- и тромбоцитопения), возникновением лейкемических инфильтратов в коже, лимфоузлах, миокарде и других органах. При кариологическом исследовании выявляется поликлоновость патологических клеток (анэуплоидия), которая является основным признаком терминальной стадии - новым этапом опухолевой прогрессии.
Хронический лимфолейкоз.
Представляет собой опухоль иммунокомпетентной ткани, состоящую преимущественно из зрелых лимфоцитов, представленных в большинстве случаев В-клетками (Хронический лейкоз, представленный Т-лимфоцитами, встречается приблизительно в 5% случаев). Характерен лейкоцитоз; в мазках крови преобладают зрелые узкоцитоплазменные лимфоциты, содержание которых может доходить до 80 % и более. Важным признаком является появление теней Гумпрехта (раздавленные при приготовлении мазков неполноценные лимфоциты). Количество лимфоцитов в костном мозге составляет не менее 50 % всех миелокариоцитов. Разрастание лимфоидной ткани имеет место в лимфатических узлах, селезенке и печени, что сопровождается увеличением указанных органов.
Функциональная неполноценность образующих опухоль лимфоцитов приводит к нарушению иммунологического гомеостаза у больных, что, в свою очередь, становится причиной аутоиммунных конфликтов (аутоиммунные гемолитические анемии и тромбоцитопении); инфекционных осложнений (вследствие нарушения антителообразования) и т. д.
В отличие от хронического миелолейкоза, бластные кризы наблюдаются крайне редко, не развивается также вторичная резистентность к цитостатическим препаратам.
Эритремия (истинная полицитемия, болезнь Вакеза).
Заболевание опухолевой природы, характеризующееся относительно доброкачественным течением. Источником роста опухоли является клетка - предшественница миелопоэза, основной субстрат опухоли - эритроциты. Наиболее характерны изменения со стороны периферической крови: количество эритроцитов достигает 6-12 x 10 12 /л, уровень гемоглобина - 160-200 г/л, показатель гематокрита увеличивается до 0,60-0,80 г/л. Уровень эритропоэтина в крови и моче, в отличие от симптоматических эритроцитозов, понижен. Имеются лейко- и тромбоцитоз, уменьшается СОЭ, возрастает вязкость крови. Важным диагностическим признаком является увеличение массы циркулирующих эритроцитов.
Миеломная болезнь (плазмоцитома). Макроглобулинемия Вальденстрема.
Заболевания из группы парапротеинемических гемобластозов - опухолей из иммунокомпетентных клеток (плазматические и В-лимфоциты), синтезирующих гомогенные (моноклональные) иммуноглобулины.
Общие нарушения в организме при лейкозах проявляются в виде ряда синдромов: анемического, геморрагического, инфекционного, метастатического и интоксикационного.
Анемический синдром.
Связан с угнетением эритроидного ростка костного мозга.
Геморрагический синдром (кровотечения из десен, носа, кишечника; возможны кровоизлияния в жизненно важные органы). Обусловлен снижением продукции тромбоцитов.
Инфекционный синдром.
Причиной его является функциональная неполноценность лейкемических лейкоцитов (снижение способности к фагоцитозу, нарушение ферментного гомеостаза, угнетение синтеза антител в лимфоцитах и т. д.).
Метастатический синдром.
Проявляется нарушением функции различных органов и систем вследствие появления в них лейкемических инфильтратов.
Интоксикационный синдром.
Связан с наводнением организма нуклеопротеидами - токсическими продуктами, образующимися при распаде (гибели) лейкемических клеток.
Используемые в терапии лейкозов цитостатические лекарственные препараты могут вызвать целый комплекс побочных эффектов со стороны нормальных органов и систем организма, объединенных термином "цитостатическая болезнь". Особенно высокую чувствительность к токсическому действию противолейкозных препаратов проявляют нормальные быстро обновляющиеся клеточные системы: костный мозг, лимфоидные органы, эпителий желудочно-кишечного тракта, кожа, волосяные фолликулы, активно пролиферирующие ткани репродуктивных органов. В связи с этим под влиянием применяемой терапии клинические и морфологические проявления того или иного вида лейкоза могут существенно изменяться.
Причинами смерти при лейкозах являются резкое малокровие и тяжелая общая интоксикация, поражение жизненно важных органов (лейкозная инфильтрация, обширные кровоизлияния). Непосредственной причиной смерти больных могут стать инфекционные осложнения (пневмонии, сепсис, перитонит).
Острый недифференцируемый лейкоз

Шатохин Юрий Васильевич — заведующий отделением, доктор медицинских наук, профессор, врач высшей категории.

Снежко Ирина Викторовна — кандидат медицинских наук, врач-гематолог высшей категории, доцент кафедры.

Турбеева Елизавета Андреевна — редактор страницы.

Острый недифференцируемый лейкоз
Исходным элементом для острого недифференцируемого лейкоза являются клетки морфологически неидентифицируемые, клетки-предшественницы второго или третьего класса. Такие опухолевые клетки не дифференцируются. В их цитоплазме отсутствуют признаки принадлежности к тому или иному ряду (А. И. Воробьев, М. Д. Бриллиант, 1976).
Эти клетки обладают большим полиморфизмом, встречаются их макро- и мезогенерации, в связи с чем ядерно-цитоплазматическое отношение различное. В крупных клетках наблюдают широкий ободок цитоплазмы с большим, расположенным в центре круглым ядром, с нежнопетлистой хроматиновой структурой.
Ядро имеет 1—2 нуклеолы. Реже ядра приобретают моноцитоидную, бобовидную или перекрученную форму. В ядрах этих клеток нуклеолы обычно не обнаруживаются, цитоплазма голубая или интенсивно голубая. Иногда по периферии клетки наблюдается темно-синий ободок.
Мезоформы имеют небольшой ободок цитоплазмы и более компактную структуру ядер. Зернистость в цитоплазме этих клеток отсутствует (В. Т. Морозова, 1977); Подобные бластные элементы цитохимически не типируются, так как, возникнув из клеток 2—3 классов, они не дифференцируются в более зрелые.
Острый недифференцируемый лейкоз диагностируют у 2—3 % больных, преимущественно молодого возраста (Bernard et al., 1965). У детей его выделяют как исключительно редкую форму (В. П. Шапетько, 1974). Однако, по нашим данным, в результате тщательного цитохимического исследования, его можно выделить у детей более часто, до 10 % случаев.
Сравнительно недавно мы стали цитохимически шире типировать острые лейкозы, и в 1978—1979 гг. наблюдали семь случаев недифференцируемого лейкоза у детей 3—14 лет (пять мальчиков и две девочки). У девочек лейкоз протекал бурно, с большой генерализацией опухоли, у мальчиков с осложнением септикопиемией и септицемией, у одного из них была семейная форма лейкоза.
Приводим наше наблюдение недифференцируемого лейкоза, протекавшего с бурной генерализацией процесса.
С. Л., 10 лет, находилась в детском гематологическом отделений с 17 по 26.07.78 г. Девочка от первых родов, развивалась нормально, ничем ранее не болела. Заболела остро. Повысилась температура до 38 , появились головная боль, слабость, головокружение, боли в горле.
Лечилась по поводу катаральной ангины на участке! На 8-е сутки увеличились шейные и подчелюстные лимфоузлы, в результате чего с подозрением на эпидемический паротит направлена в инфекционную больницу, а оттуда в детский хирургический центр с подозрением на гнойный лимфоаденит.
В подчелюстной области появились конгломераты: слева — 8X6 см, справа — 2,5×2 см, болезненные. После консультации гематолога переведена в наше отделение. Состояние тяжелое: выражены бледность, полиморфная геморрагическая сыпь, гематома в области предплечья, печень выступает на 2 см ниже края реберной дуги, селезенка на уровне пупка, плотные, безболезненные.
Анализ крови от 17.07: эритроциты — 2,3 • 106 в 1 мкл, гемоглобин — 68 г/л, цветовой показатель — 0,89, ретикулоциты — 6 %„, тромбоциты — 5,1 • 104 в 1 мкл, лейкоциты — 18 • 103 в 1 мкл, бластные клетки — 75 %, лимфоциты — 22 %, СОЭ — 60 мм/ч.
В пунктате костного мозга от 17.07 оказалось 88 % властных клеток, не содержащих зернистости, с отрицательной реакцией на пероксидазу, фосфолипиды, гликоген и неспецифическую эстеразу. Это позволило установить диагноз недифференцируемого лейкоза. На фоне цитостатической терапии по программе ЦВАМП, антибиотико- и витаминотерапии, а также гемотрансфузий состояние больной не улучшилось, и вскоре она погибла.
Патологоанатомический диагноз: острый недифференцируемый лейкоз, распространенная лейкозная инфильтрация в печени, селезенке, висцеральных лимфатических узлах, множественные геморрагии в серозных оболочках. Еще более злокачественным и бурным оказалось течение заболевания у другой больной.
П. Н., 7 лет, находилась в гематологическом отделении с 21 по 24.05.78 г. За 10 дней до поступления пожаловалась на боли в животе, появились тошнота, рвота; при обследовании обнаружены плотные опухолевые образования в брюшной полости, выпот в плевральной полости.
На томограмме определена тень в средостении, заподозрена гематосаркома. Анализ крови от 21.05: эритроциты — 3,3 • 106 в 1 мкл, гемоглобин— 113 г/л, цветовой показатель—1,0, лейкоциты — 72 • 103 в 1 мкл, властные клетки—11 %. миелоциты—14%, эозинофилы — 12%, палочкоядерные—19%, сегментоядерные — 33%, лимфоциты — 16 %, моноциты — 3 %, СОЭ — 7 мм/ч.
Миелограмма от 21.05: властные клетки — 64,5%, нейтрофильные миелоциты— 1 %, нейтрофильные метамиелоциты— 1 %, палочкоядерные — 1,5 %, сегментоядерные — 5,5 %, эозинофилы — 0,5 %, лимфоциты — 6,5%, ретикулярные клетки—16%, плазматические клетки — 2%, нормоциты—1,5%, клетки тромбоцитарного ряда встречаются в достаточном количестве, нарушено созревание и отторжение тромбоцитов.
Властные клетки с ярко-голубой цитоплазмой, почти все вакуолизированные, в основном цитоплазма. Встречаются бласты двух- и трехъядерные; реакции на пероксидазу, гликоген и неспецифическую эстеразу отрицательные.
Диагноз: недифференцируемый лейкоз, стадия разгара.
Состояние прогрессивно ухудшалось, нарастали явления легочно-сердечной недостаточности, и больная скончалась.
Патологоанатомический диагноз: острый недифференцируемый лейкоз с множественными опухолевыми разрастаниями в переднем средостении, правом легком, желчном пузыре, тонком кишечнике, желудке, обоих яичниках. Нашей больной ЦОАП-терапия была только начата.
Однако, как указывает Л. Г. Ковалева (1978), в случае диффузной лейкозной инфильтрации во внутренних органах при недифференцируемом лейкозе обнаруживается резистентность к проводимой противолейкозной терапии. Больные умирают в результате прогрессирования основного заболевания и присоединения инфекционных осложнений.
Читайте также:

