При опухоли клеток островков лангерганса

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Эпидемиология
- Патогенез
- Где болит?
- Формы
- Что нужно обследовать?
- Как обследовать?
- Какие анализы необходимы?
- К кому обратиться?
Опухоли островков Лангерганса морфологам были известны еще в начале XX в.
Описание же эндокринных синдромов стало возможным лишь с открытием гормонов поджелудочной железы и желудочно-кишечного тракта.

[1], [2], [3], [4], [5], [6]
Эпидемиология
Для суждения о распространенности островково-клеточных опухолей точных данных нет. Патологоанатомы одну аденому находят на каждые 1000-1500 вскрытий. В учреждениях широкого профиля соотношение больных с функциионирующей опухолью островков Лангерганса к госпитализированным составляет) 1 /50 тыс. Около 60 % всех эндокринных опухолей поджелудочной железы - инсулиносекретирующие.

[7], [8], [9], [10], [11], [12], [13], [14], [15]
Патогенез
Опухоли из островковых клеток встречаются значительно реже других панкреатических опухолей. Их классификация базируется на тех клинических проявлениях, развитие которых они обусловливают, и на типе клеток и гормонов, идентифицирующихся в них, особенно иммуногистохимически. Значительная часть этих опухолей вырабатывает множество гормонов, которые обнаруживаются в различных опухолевых клетках, но клиническая симптоматика обычно обусловлена одним гормоном, биологически активным и вырабатываемым в наибольшем количестве Более того, метастазы в случае злокачественной опухоли могут состоять только из одного типа клеток, даже при первично поликлональной опухоли. Наряду с этим встречаются опухоли из одного типа клеток, вырабатывающие разнообразные пептиды. В ряде случаев клиническая и гормональная картина обусловлены множественными эндокринными опухолями поджелудочной железы и/или гиперплазией островковых клеток одного или разных типов.
Предполагается существование двух источников происхождения эндокринных опухолей: островкового, откуда и произошло их название - инсуломы, и протокового - из мультипотентных стволовых клеток в протоковом эпителии (незидаобластов), которые могут пролиферировать и дифференцироваться в клетки, продуцирующие различные пептиды. Эти опухоли нередко являются источником эктопического образования гормонов. Чаще всего они возникают у взрослых в любой части поджелудочной железы, редко имеют собственную капсулу (особенно небольшие). Неинкапсулированные опухоли обладают так называемым зигзагообразным ростом, сходным с инфильтративнык. По цвету и виду могут напоминать добавочную селезенку из-за необычайно богатой васкуляризациц j поверхность разреза гомогенная, серовато-розового или вишневого цвета, изредка выявляются кровоизлияния и кистозные участки. При выраженном фиброзе стромы с отложением солей извести инсуломы обретают хрящевидную плотность. Размеры автономных опухолей варьируют от 700 мкм до нескольких сантиметров в диаметре. Опухоли, диаметром 2 см, как правило, доброкачественные, а более 6 см - злокачественные.
Солитарные или даже множественные опухоли нередко сопровождаются развитием в окружающей их панкреатической ткани гиперплазии и/или гипертрофии островкового аппарата, прежде всего за счет бета-клеток (при инсулиномах).
Островковые опухоли - это прежде всего аденомы и реже - аденокарциномы. По размеру и форме опухолевые клетки сходны с соответствующими клетками нормальных островков: полигональные или призматические, редко - веретеновидные. В одних клетках цитоплазма эозинофильная, в других - базофильная, в третьих - светлая, а объем ее варьирует от скудной до обильной. Ядерный полиморфизм - довольно частое явление. Более чем в половине опухолей строма в различной степени фиброзирована, гиалинизирована и кальцифицирована. Примерно в 30 % наблюдается отложение амилоида в строме. В 15 % случаев выявляются псаммомные тела, количество которых варьирует. В 2/3 от общего числа опухолей встречаются протоковые структуры и переходные от протоковых к опухолевым. Последние формируют анастомозирующие тяжи, гнезда, розетки, альвеолы, папиллярные структуры, разделенные многочисленными тонкостенными сосудами. В зависимости от преобладающей структуры различают три типа опухолей:
- I - солидный, называемый еще диффузным;
- II - медуллярный, часто называемый трабекулярным (этот тип строения чаще встречается в инсулиномах и глюкагономах);
- III - железистый (альвеолярный или псевдоацинарный). Этот тип чаще встречается в гастриномах и при синдроме Вернера. Все типы строения могут быть в одной опухоли в различных ее участках.
Бета-клеточные опухоли (инсулиномы) - наиболее часто встречаемые островковые опухоли, 90 % из которых - доброкачественные. Около 80 % из них - солитарные. В 10 % случаев гипогликемя обусловлена множественными опухолями, 5 % из них - злокачественные, а 5 % - незидиоблао тоз, для которого характерны гиперплазия островков за счет их новообразования из протоковых клеток, гипертрофия островков, обусловленная гиперплазией и/или гипертрофией формирующих его клеток, главным образом бета-клеток. Термин незидиобластоз введен G. F. Laidlaw в 1938 г. Он характеризуется также явлениями ацино-инсулярной трансформации. Между клиническими проявлениями инсулином и их размерами существует определенная взаимосвязь. Иммуногистохимически в инсулиномах могут обнаруживаться А- и/или D-клетки, редко ЕС-клетки.
Одним из значительных достижений двух последних десятилетий в области гистохимии и эндокринологии является разработка APUD (Amine Precursor Uptake and Decarboxylation) - концепции, которая позволила объяснить секрецию, в частности островково-клеточными новообразованиями поджелудочной железы, многих гормонов, не свойственных ее физиологической функции, поэтому неудивительны сообщения последних лет о способности этих опухолей секретировать, помимо уже названных гормонов, такие как хорионический гонадотропин, кальцитонин, различные простагландины, гормон роста, антидиуретический гормон, самостоятельная роль которых в формировании каких-либо эндокринных синдромов окончательно не доказана, однако не исключено, что дальнейшие исследования в этом направлении позволят установить причинную связь между некоторыми даже известными заболеваниями желудочно-кишечного тракта и опухолями поджелудочной железы.

[16], [17], [18], [19], [20], [21], [22], [23], [24], [25], [26]
ОПУХОЛИ ИЗ ОСТРОВКОВЫХ КЛЕТОК ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Эндокринология – CureMed.ru
С открытием гормонов поджелудочной железы и желудочно-кишечного тракта появилась возможность описания островково – клеточные опухоли поджелудочной железы (опухоли островков Лангерганса).
Функционирующие опухоли поджелудочной железы делятся на две группы:
- ортоэндокринные, секретирующие гормоны, свойственные физиологической функции островков;
- параэндокринные, выделяющие гормоны, не свойственные им
К ортоэндокринным относятся новообразования клеток: глюкагонома, инсулинома, сомастинома и ППома. Клеточное происхождение параэндокринных опухолей не установлено, к ним относятся новообразования, выделяющие гастрин (гастринома), вазоактивный интестинальный пептид (випома), кортикотропинома, опухоли с карциноидным синдромом.
К параэндокринным опухолям относятся и редкие опухоли, секретирующие другие пептиды и простагландины.
Предполагается существование двух источников происхождения эндокринных опухолей: островкового, откуда произошло их название – инсуломы, и протокового – из мультипотентных стволовых клеток в протоковом эпителии (незидиобластов). Чаще опухоли возникают у взрослых в любой части поджелудочной железы, редко имеет собственную капсулу (особенно небольшие). При выраженном фиброзе стромы с отложением солей извести, инсуломы обретают хрящевидную плотность. Размеры автономных опухолей варьируют от 700 мкм до нескольких сантиметров в диаметре. Опухоли, диаметром до 2 см, как правило, доброкачественные, а более 6 см – злокачественные.
Островковые опухоли – это, прежде всего аденомы и реже - аденокарциномы. По размеру и форме опухолевые клетки сходны с соответствующими клетками нормальных островков: полигональные или призматические, редко – веретеновидные.
- Ортоэндокринные опухоли.
- Глюкагонома – опухоль островков Лангерганса, секретирующая глюкагон, что приводит к развитию сложного симптомокомплекса, Наблюдаются: диабет, анемию и похудание, реже отмечаются диарея, поражение слизистых оболочек, тромбозы и эмболии, доминируют кожные проявления - дерматит. Чаще дерматит развивается на нижних конечностях, в паховой области, промежности, перианальной области, нижней части живота, на лице. Поражение слизистых оболочек при глюкагономе – стоматит, гингивита, глоссита, язык характерный – большой, мясистый, красный со сглаженными сосочками. Диабет при синдроме глюкагономы у 75% больных легкий (для которых достаточна диета), четверть больных нуждаются в инсулинотерапии. Выраженные катаболические изменения при глюкагономе являются причиной похудания, потеря массы тела в отсутствие анорексии. Анемия - нормохромная и нормоцитарная. Глюкагономы обычно больших размеров и составляет до 10 см и выше, в большинстве случаев новообразования злокачественные. 85% больных имеют возраст более 50 лет, реже больных до 30 лет. Лечение – хирургическое и химиотерапевтическое.
- Инсулинома – опухоль, секретирующая избыточное количество инсулина, что проявляется гипогликемическим симпомокомплексом. Опухоль встречается во всех возрастных группах – от новорожденных до престарелых, чаще поражает от 30 до 55 лет, детей составляет около 5%. Клиническое проявление инсулиномы связано с ее гормональной активностью. Гиперинсулинизм является основным патогенетическим механизмом, от которого зависит весь симптомокомплекс заболевания. При снижении уровня глюкозы до гипогликемии включаются механизмы, направленные на гликогенолиз, глюконеогенез, мобилизацию свободных жирных кислот, кетогенез. Характерно наличие нервно-психический нарушений. Развитие гипогликемии в утренние часы и при пропуске очередного приема пищи, при физических и психических напряжениях, у женщин накануне месячных говорит в пользу инсулиномы. В диагностике могут возникнуть трудности при применении больным препаратом инсулина. Радикальный метод лечения – хирургический.
- Соматостатинома – представление о симптомокомлексе, еще не сформировано. Наряду с холелитиазом обнаруживается сахарный диабет, диарея или стеаторея, гипохлоргидрия, анемия, похудание. По характеру секреции соматостатиномы – полигормональные.
- ППома – панкреатический пептид секретируется F-клетками поджелудочной железы. Пептид снижает сократительную функцию желчного пузыря, повышает тонус общего желчного протока и тормозит эндокринную функцию поджелудчной железы, повышенное содержание панкреатического пептида в периферческой крови. Опухоли проявляются случайно при операциях на желудке, кишечнике, желчном пузыре.
- Параэндокринные опухоли.
- Гастринома – ульцерогенный синдром язвенного диатеза (синдром Золлигера – Эллисона) – это сочетание тяжелого течения язвенной болезни двенадцатиперстной кишки при опухоли поджелудочной железы. В основе заболевания лежит гипергастринемия, которая вызывает постоянную стимуляцию функцию обкладочных клеток желудка. Желудочная гиперсекреция с очень высокой концентрацией соляной кислоты обуславливает большинство проявлений синдрома и в первую очередь – изъязвление слизистой оболочки желудочно-кишечного тракта. Язва локализуется чаще в постбульбарном отделе двенадцатиперстной кишки, язвы могут быть множественными, чаще, чем при обычной язвенной болезни – кровотечения, перфорация, стеноза, болевой синдром. Лечение хирургическое.
- Випома – синдром водной диареи с опухолью поджелудочной железы. Причиной клинического проявления – секреция вазоактивного интенстинального пептида (ВИП). У более 70% больных ВИПом – злокачественные, у 20% - симптокомплекс - результат гиперплазии островкового аппарата. Избыточная секреция ВИП стимулирует выраженную экскреции тонкой кишкой и поджелудочной железой жидкости и электролитов, которые не успевают всасываться в толстой кишке. Это выражается профузными поносами, что приводит к дегидрадации. Потеря калия, бикарбонатов и магния приводит к развитию ацидоза, выраженной слабости и тетанических судорог, в последствие – азотемия.
- Кортикотропинома – выражается глюкокортикоидным гиперкортицизмом. Кортикотропинома выявляется уже в стадии метастазирования, поэтому лечение хирургическое.
- Паратиренома – гиперкальциемия, как ведущий признак эндокринных опухолей поджелудочной железы. Гиперкальциемия может быть результатом местастического процесса в кости.
- Опухоли поджелудочной железы с карциноидным синдромом. Обнаруживаются в кишечнике и даже в бронхах. Карциноид поджелудочной железы способен секретировать практически все пептиды, свойственные орто- и параэндокринным заболеваниям.
Медикаментозное лечение имеет положительный эффект от применения соматостатина.
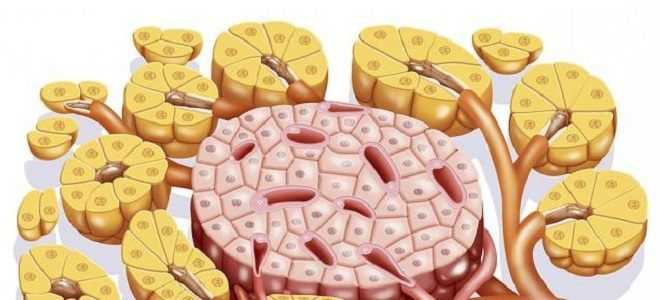
Ткань поджелудочной железы представлена двумя видами клеточных образований: ацинус, вырабатывающий ферменты и участвующий в пищеварительной функции, и островок Лангерганса, основная функция которого — синтезировать гормоны.
В самой железе островков немного: они составляют 1—2% от всей массы органа. Клетки островков Лангерганса разнятся между собой по строению и функциям. Имеется 5 их видов. Они секретируют активные вещества, регулирующие углеводный обмен, пищеварение, могут участвовать в ответе на стрессовые реакции.
Что такое островки Лангерганса?
Островки Лангерганса (ОЛ) — это полигормональные микроорганы, состоящие из эндокринных клеток, расположенных по всей протяженности паренхимы ПЖ, выполняющей экзокринные функции. Их основная масса локализуется в хвостовой части. Размер островков Лангерганса составляет 0,1—0,2 мм, общее их количество в ПЖ человека составляет от 200 тыс. до 1,8 млн.
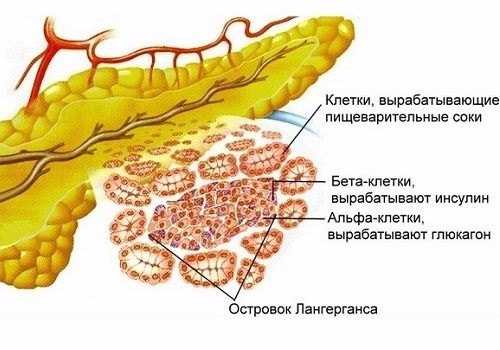
Клетки образуют отдельные группы, между которыми проходят капиллярные сосуды. От железистого эпителия ацинусов они отграничены соединительнотканными и проходящими там же волокнами нервных клеток. Эти элементы нервной системы и клетки островка образуют нейроинсулярный комплекс.
Структурные элементы островков — гормоны — выполняют внутрисекреторные функции: регулируют углеводный, липидный обмен, процессы пищеварения, метаболизм. У ребенка в железе имеется 6% этих гормональных образований от общей площади органа. У взрослого человека эта часть ПЖ значительно уменьшена и составляет 2% от поверхности железы.
Скопления клеток, отличающиеся по своему виду и морфологическому строению от основной ткани железы и располагающиеся небольшими группами преимущественно в хвосте ПЖ, впервые обнаружил в 1869 году немецкий патологоанатом Пауль Лангерганс (1849—1888 гг.).
На основании ее работ в 1889—1892 гг. в Германии О. Минковский и Д. Меринг установили, что при удалении ПЖ развивается сахарный диабет, который можно устранить, проведя подсадку части здоровой ПЖ под кожу прооперированному животному.
Отечественный ученый Л.В. Соболев (1876—1921 гг.) одним из первых на основании проведенных исследовательских работ показал значение островков, открытых Лангергансом и названных его именем, в продуцировании вещества, имеющего отношение к возникновению сахарного диабета.
В дальнейшем благодаря большому количеству исследований, проведенных физиологами в России и других странах, были открыты новые научные данные об инкреторной функции ПЖ. В 1990 г. впервые проведена трансплантация островков Лангерганса человеку.
Типы островковых клеток и их функции
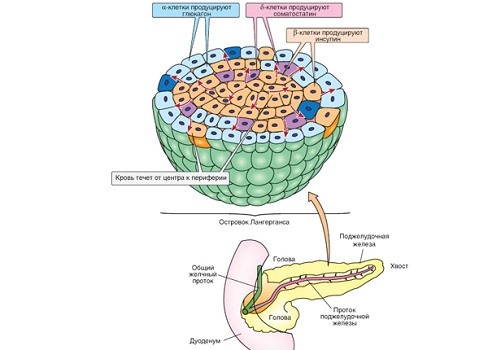
Клетки ОЛ отличаются морфологическим строением, выполняемыми функциями, локализацией. Внутри островков они имеют мозаичное расположение. Каждый островок имеет упорядоченную организацию. В центре находятся клетки, которые выделяют инсулин. По краям – периферийные клетки, количество которых зависит от размеров ОЛ. В отличие от ацинусов, ОЛ не содержит своих протоков – гормоны поступают сразу в кровь через капилляры.
Выделяют 5 основных видов клеток ОЛ. Каждый из них синтезирует определенный вид гормона, регулируя пищеварение, углеводный и белковый обмен:
- α-клетки,
- β-клетки,
- δ-клетки,
- РР-клетки,
- эпсилон-клетки.
Альфа-клетки занимают четверть площади островка (25%), являются вторыми по значимости: вырабатывают глюкагон — антагонист инсулина. Он контролирует процесс расщепления липидов, способствует повышению уровня сахара в крови, участвует в снижении уровня кальция и фосфора в крови.
Бета-клетки составляют внутренний (центральный) слой дольки и являются основными (60%). Они отвечают за выработку инсулина и амилина — компаньона инсулина в регуляции глюкозы крови. Инсулин выполняет несколько функций в организме, главная — нормализация уровня сахара. Если нарушается его синтез, развивается сахарный диабет.
Дельта-клетки (10%) образуют внешний слой в островке. Они продуцируют соматостатин — гормон, значительная часть которого синтезируется в гипоталамусе (структуре головного мозга), а также обнаруживается в желудке и кишечнике.
Функционально он тесно связан также с гипофизом, регулирует работу определенных гормонов, которые вырабатываются этим отделом, а также подавляет образование и выделение гормонально-активных пептидов и серотонина в желудке, кишечнике, печени и самой поджелудочной железе.
РР-клетки (5%) располагаются по периферии, их численность примерно составляет 1/20 части островка. Они могут секретировать вазоактивный интестинальный полипептид (ВИП), панкреатический полипептид (ПП). Максимальное количество ВИП (вазоинтенсивного пептида) встречается в пищеварительных органах и мочеполовой системе (в мочеиспускательном канале). Он влияет на состояние пищеварительного тракта, выполняет много функций, в том числе обладает спазмолитическими свойствами в отношении гладкой мускулатуры желчного пузыря и сфинктеров органов пищеварения.
Самые редкие из входящих в состав ОЛ — эпсилон-клетки. При микроскопическом анализе препарата из дольки ПЖ можно определить, что их число от общего состава составляет меньше 1%. Клетки синтезируют грелин. К наиболее изученной среди его многочисленных функций относится возможность влиять на аппетит.
Какие патологии возникают в островковом аппарате?
Поражение клеток ОЛ приводит к тяжелым последствиям. При развитии аутоиммунного процесса и выработке антител (АТ) к клеткам ОЛ, количество всех перечисленных структурных элементов резко снижается. Поражение 90% клеток сопровождается резким уменьшением синтеза инсулина, что приводит к сахарному диабету. Выработка антител к островковым клеткам поджелудочной железы происходит в основном у людей молодого возраста.
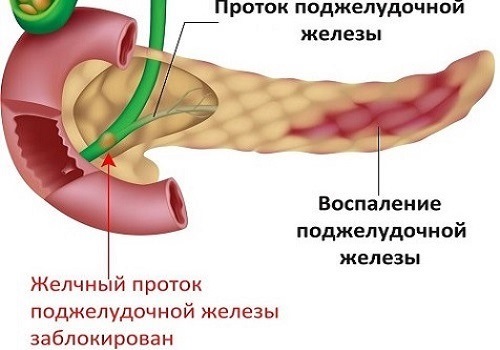
К серьезным последствиям в связи с повреждением островков приводит панкреатит — воспалительный процесс в тканях ПЖ. Нередко он протекает в тяжелой форме в виде панкреонекроза, при котором происходит тотальная гибель клеток органа.
Определение антител к островкам Лангерганса
Если в организме по каким-то причинам произошел сбой в организме, и началась активная выработка антител против собственных тканей, это приводит к трагичным последствиям. Когда воздействию антител подвергаются бета-клетки, развивается сахарный диабет I типа, связанный с недостаточной выработкой инсулина. Каждый вид образующихся антител действует против определенного вида белка. В случае с островками Лангерганса — это структуры бета-клеток, отвечающие за синтез инсулина. Процесс протекает прогрессивно, клетки полностью погибают, нарушается углеводный обмен и при нормальном питании больной может умереть от голода из-за необратимых изменений в органах.
Разработаны диагностические методы определения наличия антител к инсулину в организме человека. Показаниями к такому исследованию являются:
- ожирение с учетом семейного анамнеза,
- любая патология ПЖ, включая перенесенные травмы,
- тяжелые инфекции: в основном вирусные, которые могут стать толчком к развитию аутоиммунного процесса,
- тяжелые стрессы, психическое перенапряжение.
Существует 3 типа антител, благодаря которым диагностируется сахарный диабет I типа:
- к декарбоксилазе глутаминовой кислоты (одна из заменимых аминокислот в организме),
- к вырабатывающемуся инсулину,
- к клеткам ОЛ.
Это своеобразные специфические маркеры, которые необходимо включать в план обследования пациентов с имеющимися факторами риска. Из перечисленного объема исследований выявление антител к компоненту глутаминовой аминокислоты является ранним диагностическим признаком СД. Они появляются, когда клинические признаки болезни еще отсутствуют. Определяются в основном в молодом возрасте и могут быть использованы для выявления людей с предрасположенностью к развитию болезни.
Трансплантация островковых клеток
Трансплантация клеток ОЛ является альтернативой пересадке поджелудочной железы или ее части, а также установке искусственного органа. Связано это с высокой чувствительностью и нежностью тканей ПЖ к любым воздействиям: она легко травмируется и с трудом восстанавливает свои функции.
Пересадка островков сегодня дает возможность лечить сахарный диабет I типа в тех случаях, когда инсулинзамещающая терапия достигла пределов и становится малоэффективной. Метод впервые применен канадскими специалистами и заключается во введении пациенту при помощи катетера здоровых эндокринных донорских клеток в воротную вену печени. Он направлен на то, чтобы заставить работать и сохранившиеся собственные бета-клетки.
За счет функционирования пересаженных постепенно синтезируется необходимое для поддержания нормального уровня глюкозы крови количество инсулина. Эффект наступает быстро: при удачно проведенной операции через две недели состояние больного начинает улучшаться, заместительная терапия сходит на нет, ПЖ начинает самостоятельно синтезировать инсулин.
Опасность операции заключается в отторжении пересаженных клеток. Используются трупные материалы, которые тщательно подбираются по всем параметрам совместимости тканей. Поскольку таких критериев существует около 20, антитела, присутствующие в организме, могут привести к разрушению тканей поджелудочной железы. Поэтому важную роль играет правильное медикаментозное лечение, направленное на снижение иммунных реакций. Препараты подбираются таким образом, чтобы избирательно блокировать некоторые из них, влияющие на выработку антител, к клеткам пересаженных островков Лангерганса. Это позволяет до минимума снизить риск для поджелудочной железы.
На практике пересадка клеток ПЖ при сахарном диабете I типа показывает хорошие результаты: зафиксированных смертельных случаев после такой операции не отмечалось. Определенное количество больных значительно снизило дозу инсулина, а часть прооперированных пациентов перестала в нем нуждаться. Восстановились и другие нарушенные функции органа, улучшилось самочувствие. Значительная часть вернулась к нормальному образу жизни, что позволяет надеяться на дальнейший благоприятный прогноз.
Как и при пересадке других органов, операция на ПЖ, помимо отторжения, опасна другими побочными явлениями за счет нарушения разной степени секреторной деятельности поджелудочной железы. В тяжелых случаях это приводит:
- к панкреатическим поносам,
- к тошноте и рвоте,
- к выраженному обезвоживанию,
- к другим диспепсическим явлениям,
- к общему истощению.

После проведенной процедуры на протяжении всей жизни пациент должен непрерывно получать иммуносупрессорные препараты, чтобы предотвратить отторжение чужеродных клеток. Действие этих лекарств направлено на снижение иммунных реакций — выработку антител. В свою очередь, отсутствие иммунитета увеличивает риск развития любой, даже простой инфекции, которая может осложниться и вызвать серьезные последствия.
Продолжаются исследования по пересадке ПЖ от свиньи — ксенотрансплантация. Известно, что анатомия железы и свиной инсулин наиболее приближены к человеческим и отличаются от него одной аминокислотой. До открытия инсулина в лечении тяжелого сахарного диабета использовался экстракт из поджелудочной железы свиньи.
Поврежденные ткани ПЖ не восстанавливаются. В случаях осложненного сахарного диабета, когда пациент находится на высоких дозах инсулина, такое оперативное вмешательство спасает больного, дает шанс на восстановление структуры бета-клеток. В ряде клинических исследований больным пересаживались эти клетки от доноров. В результате восстанавливалась регуляция углеводного обмена. Но притом пациентам приходится проводить мощную иммуносупрессивную терапию, чтобы не произошло отторжение донорских тканей.
Не всем пациентам с сахарным диабетом I типа показана трансплантация клеток. Существуют строгие показания:
- отсутствие результатов от применяемого консервативного лечения,
- резистентность к инсулину,
- выраженные метаболические нарушения в организме,
- тяжелые осложнения болезни.
Процедуру замещения островков Лангерганса широко проводят в США — таким образом лечат диабет любого типа на ранних стадиях. Этим занимается один из институтов по диабетическим исследованиям в Майами. Полностью вылечить СД таким способом не удается, но достигается хороший терапевтический эффект, притом риски тяжелых осложнений сводятся к минимуму.
Цена такого вмешательства составляет порядка 100 тыс. $. Послеоперационная реабилитация и проведение иммунодепрессивной терапии составляет от 5 до 20 тыс. $. Стоимость этого лечения после проведения операции зависит от реакции организма на пересаженные клетки.
Практически сразу после проведенной манипуляции ПЖ начинает нормально функционировать самостоятельно, и постепенно ее работа улучшается. Процесс восстановления занимает примерно 2 месяца.
Профилактика: как сохранить островковый аппарат?
Так как функция островков Лангерганса поджелудочной железы − вырабатывать важные для человека вещества, то для сохранения здоровья этой части ПЖ необходима модификация образа жизни. Основные пункты:
- отказ от алкоголя и курения,
- исключение вредной пищи,
- физическая активность,
- сведение к минимуму острых стрессов и нервно-психических перегрузок.
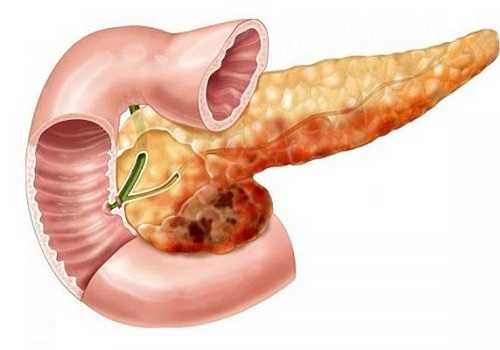
Наибольший вред поджелудочной железе приносит алкоголь: он разрушает ткани ПЖ, приводит к панкреонекрозу — тотальной гибели всех видов клеток органа, которые восстановить невозможно.
К аналогичным последствиям приводит излишнее употребление жирной и жареной пищи, особенно если это происходит натощак и регулярно. Нагрузка на ПЖ значительно возрастает, количество ферментов, которые необходимы для переваривания большого количества жиров, увеличивается и истощает орган. Это приводит к фиброзу и изменениям в остальных клетках железы.
Поэтому при малейших признаках нарушения пищеварительных функций рекомендуется обратиться к гастроэнтерологу или терапевту с целью своевременной коррекции изменений и ранней профилактики осложнений.
Что такое опухоли островков Лангерганса?
Опухоли из клеток островков Лангерганса представляют собой скопление патологических (злокачественных) клеток в эндокринной (вырабатывающей гормоны) части поджелудочной железы. Опухоли из клеток островков могут быть как доброкачественными так и злокачественными (рак). Рак клеток островков поджелудочной железы встречается редко.
Поджелудочная железа представляет собой грушеподобный орган до 6 дюймов в длину, расширенный на одном из концов и суженный на другом. Поджелудочная железа размещается позади желудка, внутри петли, которую формирует тонкий кишечник. Более широкий конец поджелудочной железы называется головкой. Средняя часть органа носит название тела поджелудочной, узкий левый конец называют хвостом.
Поджелудочная железа выполняет две основные задачи в организме. Она продуцирует пищеварительный сок, способствующий перевариванию пищи и гормоны (такие как инсулин), регулирующие способность тела сохранять и использовать питательные вещества. Часть железы, отвечающую за выработку пищеварительных соков, называют экзокринной частью поджелудочной железы. Около 95% всех злокачественных новообразований развиваются именно здесь. В гормоно-продуцирующей части поджелудочной находятся специальные клетки, формирующие так называемые островки и эту часть железы называют эндокринной. В этой части органа возникает до 5% всех злокачественных новообразований поджелудочной железы (опухоли из клеток островков поджелудочной).
Клетки островков поджелудочной железы синтезирует большое количество гормонов, в том числе инсулин, помагающий организму хранить и использовать сахар. При озлакачествлении клеток этих островков они могут продуцировать избыток гормонов. Злокачественные новообразования из клеток островков поджелудочной железы способствуют синтезу большого количества гормонов и называются функционирующими опухолями. Другие опухолевые клетки островков могут не вырабатывать такого количества гормонов и называются нефункционирующими опухолями. Клетки опухолей, не распространяющихся на другие органы и ткани также могут быть обнаружены в островках поджелудочной железы. Такие опухоли называются доброкачественными и не являются раком. Врачу необходимо выяснить является ли опухоль доброкачественной или злокачественной природы.
При появлении болей в брюшной полости, поноса, болей в желудке, постоянного чувства усталости, необоснованной потере или увеличении веса без переедания следует немедленно обратиться к врачу.
При наличии клинических симптомов врач назначает определенные анализы крови и мочи для определения содержания гормонов в организме. Возможно также придется выполнить рентгенографическое исследование и специальное сканирование.
Шанс выздоровления (прогноз) зависит от типа опухоли островков поджелудочной железы, распространенности процесса и общего состояния пациента.
Стадии опухолей из клеток островков Лангерганса (апудом)
При обнаружении опухоли островков поджелудочной железы необходимо провести дополнительные исследования для определения степени распространенности процесса на другие органы и ткани (стадирование заболевания). Лечение опухолей островков Лангерганса зависит от стадии процесса и возраста пациента, а также его общего состояния. Данные опухоли подразделяются на три основные группы:
Лечение опухолей из клеток островков Лангерганса зависит от типа опухоли, стадии процесса, общего состояния пациента.
Существуют следующие разновидности опухолей островков поджелудочной железы:
Опухоль состоит из злокачественных клеток, вырабатывающих излишек гормона под названием гастрин, способствующий выделению соляной кислоты в желудке. В условиях избытка кислоты в желудке на его слизистой могут образовываться язвенные дефекты.
Опухоль продуцирует огромное количество гормона инсулина, что способствует накоплению сахара в организме вместо его утилизации в энергию. Такое состояние сопровождается низким уровнем сахара в крови и называется гипогликемией.
Опухоль синтезирует слишком много гормона под названием глюкагон, что способствует повышению уровня сахара в крови. Такое состояние называют гипергликемией.
Другие виды опухолей из клеток островков Лангерганса могут поражать поджелудочную железу и/или тонкий кишечник. Каждый вид опухоли продуцирует определенный тип гормонов, что обуславливает разнообразную клиническую симптоматику.
Рецидив заболевания означает повторное возникновение опухоли после проведенного лечения. Злокачественный процесс может возникнуть повторно в поджелудочной железе или в любых других органах и тканях.
Как лечат опухоли из клеток островков Лангерганса
Для лечения опухолей из клеток островков поджелудочной существуют различные методы лечения. Некоторые подходы считаются стандартами терапии (лечение, существующее на сегодняшний день), некоторые – исследуются в клинических испытаниях. Клинические испытания проводятся для усовершенствования существующих методов терапии или для получения данных об эффективности новых подходов. Если по результатам таких исследований доказано преимущество изучаемых методов лечения, они могут стать новым стандартом лечения. Многие пациенты могут обсуждать с врачом участие в клинических исследованиях. В некоторые испытания продолжается набор пациентов, еще не получавших лечение.
Существует три вида стандартной терапии:
Наиболее частым методом лечения рака островков поджелудочной железы является хирургический. Врач может удалить опухоль и большую часть поджелудочной железы. Иногда операцию дополняют удалением желудка (гастерэктомией) в связи с язвенными дефектами. Можно также удалить соседние лимфатические узлы для изучения их под микроскопом на предмет наличия опухолевых клеток.
Химиотерапия – это метод лечения рака с помощью цитостатических препаратов, действие которых направлено на уничтожение опухолевых клеток или замедление злокачественного роста. При приеме химиопрепаратов внутрь, введение внутривенно или внутримышечно лекарство поступает в общий кровоток, уничтожая циркулирующие по организму опухолевые клетки (системная химиотерапия).
Гормональная терапия основана на приеме гормонов, действие которых направлено на остановку росту опухолевых клеток и уменьшения симптомов заболевания, вызванных опухолью.
Печеночная артериальная окклюзия или эмболизация основана на применение препаратов или других веществ, действие которых направлено на уменьшение или прекращение поступления крови к печени для остановки роста злокачественных клеток в печени.
Методы лечения, которые продолжают изучаться в клинических исследованиях
Для некоторых пациентов участие в клинических исследованиях может быть лучшим выбором метода лечения. Клинические испытания являются частью процесса изучения рака. Они проводятся для того, чтобы определить являются ли новые методы лечения опухоли эффективными и безопасными, и насколько они превосходят стандартные подходы к терапии.
Большинство сегодняшних стандартов лечения злокачественных новообразований основаны на предыдущих клинических испытаниях. Пациенты, принимающие участие в исследованиях, могут получать стандартную терапию или быть одними из первых, кто получает новое лечение.
Больные, участвующие в клинических исследованиях, также влияют на усовершенствование методов лечения рака в будущем. Даже, если клиническое испытание не приводит к открытию новых эффективных методов борьбы с заболеванием, очень часто на основании полученных результатов можно дать ответы на важнейшие вопросы и помочь в дальнейшем изучении проблемы.
Принять участие в клинических испытаниях можно до, во время или после противоопухолевого лечения.
Читайте также:

