Структура злокачественных новообразований в россии
Ниже представлена структура заболеваемости злокачественными новообразованиями в России. Ведущими локализациями в общей (оба пола) структуре заболеваемости злокачественными новообразованиями населения России являются:
- Рак кожи (12,6%, с меланомой – 14,0%)
- Рак молочной железы (11,1%)
- Рак трахеи, рак бронхов, рак легких (10,7%)
- Рак желудка (7,3%)
- Рак ободочной кишки (6,5%)
- Рак предстательной железы (5,1%)
- Рак прямой кишки, рак ректосигмоидного соединения и рак ануса (4,9%)
- Рак лимфатической и кроветворной ткани (4,7%)
- Рак тела матки (3,8%)
- Рак почки (3,8%)
- Рак поджелудочной железы (2,9%)
- Рак шейки матки (2,8%)
- Рак мочевого пузыря (2,6%)
- Рак яичников (2,5%)
Первые места в структуре заболеваемости злокачественными новообразованиями мужского населения России распределены следующим образом:
- Опухоли трахеи, бронхов, легкого (18,9%)
- Опухоли предстательной железы (11,9%)
- Опухоли кожи (10,1%, с меланомой – 11,5%)
- Опухоли желудка (9,1%)
- Опухоли ободочной кишки (5,8%)
- Значителен удельный вес злокачественных новообразований прямой кишки, ректосигмоидного соединения, ануса (5,2%)
- Опухоли лимфатической и кроветворной ткани (5,0%)
- Опухоли мочевого пузыря (4,5%)
- Опухоли почки (4,5%)
- Опухоли поджелудочной железы (3,1%)
- Опухоли гортани (2,6%)
- Значимую по удельному весу группу у мужчин формируют злокачественные опухоли органов мочеполовой системы, составляя 21,7% всех злокачественных новообразований
Первые места в структуре заболеваемости злокачественными новообразованиями женского населения России распределены следующим образом:
- Злокачественные опухоли молочной железы (20,4%) являются ведущей онкологической патологией у женского населения
- Нвообразования кожи (14,7%, с меланомой – 16,6%)
- Новообразования тела матки (7,4%)
- Новообразования ободочной кишки (7,0%)
- Новообразования желудка (5,8%)
- Новообразования шейки матки (5,3%)
- Новообразования прямой кишки, ректосигмоидного соединения, ануса (4,7%)
- Новообразования яичника (4,6%)
- Новообразования лимфатической и кроветворной ткани (4,4%)
- Новообразования трахеи, бронхов, легкого (3,8%)
Максимальное число заболеваний приходится на возрастную группу 70-74 года:
- У мужчин − 18,2%
- У женщин - 16,3%
Данная статистика позволяет четче представлять наиболее распространённые онкозаболевания среди различных возрастных групп у мужчин и женщин. А это, в свою очередь, дает информацию для принятия решения о прохождении скрининговых или диагностических программ, онко-чекапов. Беспечность в отношении некоторых симптомов просто недопустима, а уверенность в состоянии Вашего здоровья и здоровья Ваших близких – обоснованная жизненная необходимость.
Злокачественные новообразования имеют социальную значимость, так как показатели их распространенности, заболеваемости, смертности довольно высоки, а прогнозы выживаемости в ряде случаев крайне неблагоприятны. При этом стоит отметить, что большая часть пациентов, согласно статистике злокачественных новообразований, находится в возрасте старше 60 лет. Хотя процент заболевших и среди детей и лиц трудоспособного возраста остается на высоком уровне.
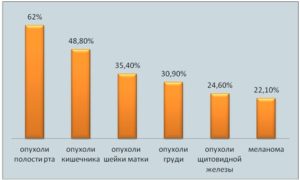
Статистика злокачественных новообразований и контингент больных
По данным статистики, на конец 2014 года на учете в онкологических учреждениях состояло более 3 291 000 пациентов. из них 20% сельских жителей, при этом примерно 1 724 000 больных с новообразованиями наблюдались у специалистов в течение 5 лет и более, что составляет 52,4%. По статистике злокачественных новообразований, наибольшую значимость в структуре заболеваемости среди контингента больных играют следующие формы патологии:
- Опухоль молочных желез -18,2%;
- Опухоль кожи -12%;
- Опухоли матки – 7,1%;
- Опухоли кишечника – 5,7%;
- Опухоли крови – 5,6%;
- Опухоли шейки матки – 5,3%;
- Опухоли простаты – 5,2%;
- Опухоли щитовидной железы – 4,3%;
- Опухоли почки – 4,3%;
- Опухоли желудка – 4,2%;
- Опухоли легких – 4%.
Распространенность злокачественных новообразований в 2014 году достигла 2 257,2 на 100 000 населения, показатель за 10-летний период вырос на 38,8%. Увеличение показателя связано не только с ростом заболеваемости, но и с улучшением диагностики и прогнозов выживаемости больных с онкопатологией. Согласно статистике злокачественных новообразований в России, уровень показателя в разных регионах варьирует; максимальные значения зарегистрированы в Курске -3086, Калужской области – 2779,7, Московской – 2718,9, Орловской – 2716; минимальные в Дагестане – 739, Тыве – 753, Ингушетии – 817, Чечне – 1080.
Стоит отметить, что 1% пациентов, состоявших на учете, из-за переезда в другие районы были сняты с учета и больше не регистрировались, у 0,7% пациентов с подозрением на онкопатологию диагноз был не подтвержден и 1,5% больных снято учета через 5 лет после терапии. Вследствие этого, по статистике, 8,2 человека на каждые 100 умерших от злокачественных новообразований не были зарегистрированы в специализированных учреждениях, и диагноз был установлен посмертно. При этом показатель в разных регионах варьирует от 0 до 27 пациентов на каждые 100 онкологических пациентов.
Статистика злокачественных новообразований, выявленных активно
Показатель активного выявления злокачественных новообразований в 2014 году составил 18,7%, за последние годы он значительно вырос, что говорит об улучшении качества и доступности медицинской помощи. При этом из числа пациентов, выявленных активно, примерно у 74% опухоль находилась на 1-2 стадии развития, что заметно увеличило прогнозы их выживаемости. Доля выявленных больных на профилактических осмотрах составила 25%. Стоит отметить, что этот показатель варьирует в разных регионах России, его анализ свидетельствует об отсутствии диспансеризации и скрининговых профилактических исследований в некоторых областях. К тому же в ряде городов имеется неблагоприятная тенденция выявления новообразований репродуктивной системы.
Статистка злокачественных новообразований в России по стадиям развития
Прогнозы выживаемости при наличии онкологической патологии зависят от множества факторов, но в большей степени на показатель влияет стадия заболевания. Согласно статистике, злокачественные новообразования на 1 стадии были зарегистрированы у 26,7% пациентов, 2 стадии – у 25,3%, 3 стадии – 20,6%. В некоторых случаях (6,7%) стадию процесса выявить не удалось.
Основной критерий оценки методов диагностики – процент запущенных случаев. По данным статистики, злокачественные новообразования при наличии отдаленных метастазов зафиксированы у 20,7% первичных пациентов. К тому же следует учесть новообразования визуальных локализаций в 3 и 4 стадии, на момент первичного посещения их доля составила 27,3%. Показатели несвоевременной диагностики отличаются по регионам и формам:
- Опухоли поджелудочной железы выявляются в запущенной форме в Алтае (практически 100%), Башкирии (82%), Ингушетии (80%);
- Опухоли полости рта запущенных форм диагностированы в Сахалине (75%), Москве (72%), Чувашии (71%), Омске (70%);
- Опухоли легких – в Иркутске (60%), на Чукотке (58%), Калмыкии (58%).
Статистика злокачественных новообразований запущенных форм довольно неблагоприятная и негативно отражается на прогнозах выживаемости.
Структура несвоевременной диагностики по формам патологии
Несмотря на усовершенствование методов обследования, рост диагностических возможностей, высокую оснащенность учреждений, статистка злокачественных новообразований в России в отношении ранней диагностики неблагоприятна. Доля пациентов с запущенными формами достаточно велика, особенно при визуальных локализациях. Все это говорит о низком качестве и недоступности специализированной помощи и халатности пациентов по отношению к своему здоровью.
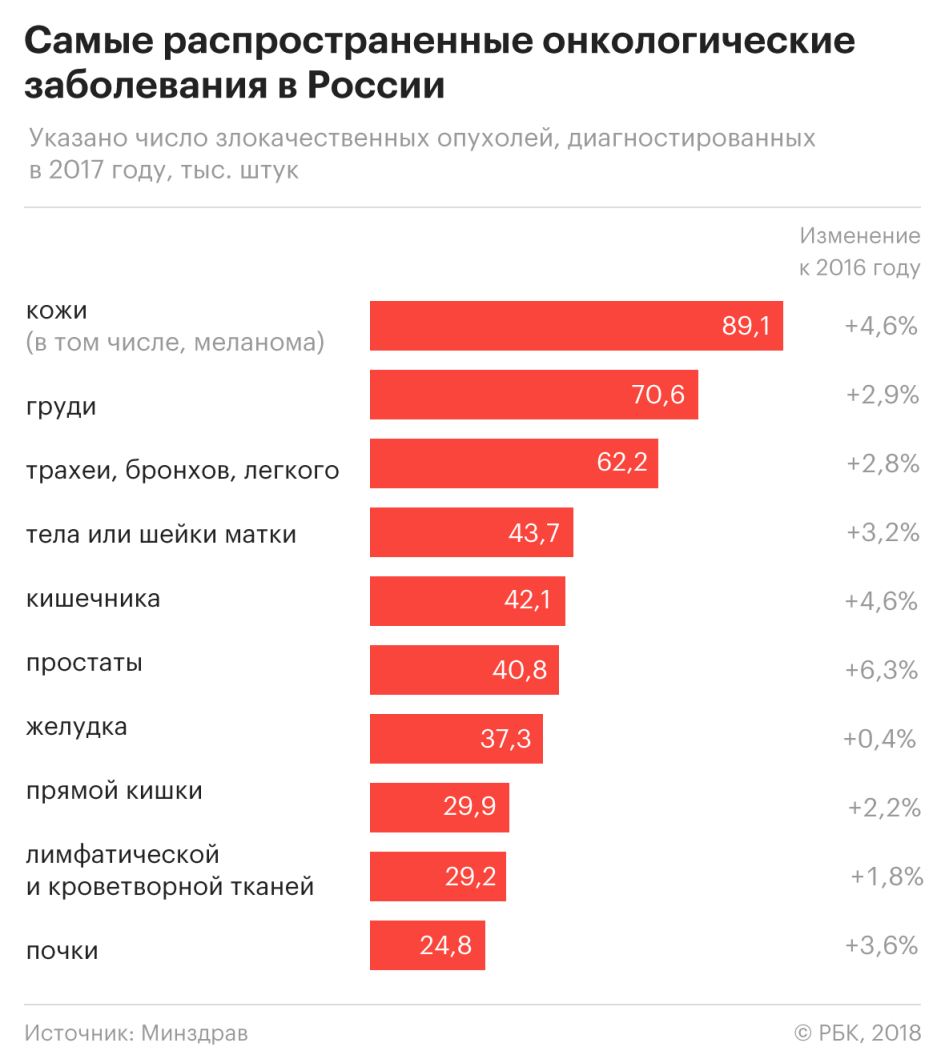
Самое распространенное онкологическое заболевание в России в 2017 году — рак кожи, следует из данных, опубликованных в ежегодном статистическом сборнике Министерства здравоохранения.
При этом общее количество диагнозов по онкологическим заболеваниям в 2017-м увеличилось год к году на 3%, с 599,3 тыс. до 617,2 тыс. случаев (Минздрав с 2011 года учитывает не число пациентов, а количество обнаруженных заболеваний).
Новообразования кожи помимо меланомы были обнаружены в прошлом году у 78 тыс. россиян, меланома — еще у 11,2 тыс., всего более 89 тыс. случаев онкологических заболеваний кожи. Тот же диагноз — новообразования кожи — был самым распространенным и в 2014–2016 годах. В 2016-м рак кожи обнаружили у 74,7 тыс. человек, меланому — у 10,5 тыс. человек.
На втором месте по частоте обнаружения — рак груди. В 2017 году этот диагноз поставили 70,6 тыс. раз. За последние пять лет такие новообразования стали выявлять на 16,2% чаще.
На третьем месте — рак трахеи, бронхов и легких: в 2017 году диагностировано 62,2 тыс. случаев.
Можно ли избежать
Рак кожи — общемировая проблема, отметил в разговоре с РБК директор Национального медицинского исследовательского центра онкологии им. Н.Н. Петрова Алексей Беляев. Но это заболевание достаточно легко лечится и не вызывает метастазов, главное — обнаружить его на ранней стадии, заметил эксперт. Меланома сложнее в лечении и вызывает метастазы. Для профилактики этих заболеваний Беляев рекомендует избегать долгого пребывания на солнце и отказаться от использования солярия.
Онкологию все реже указывают в качестве причины смерти людей, у которых была злокачественная опухоль, следует из данных сборника Минздрава. В 2017 году в 30% случаев, когда умирал человек с онкологическим заболеванием, в качестве причины смерти не указывался рак, в 2013-м этот показатель составлял 23,6%, в 1993 году — 11,6%. Иными словами, 25 лет назад 88% умерших, имевших злокачественное новообразование, умирали именно от него, а в 2017 году онкологическое заболевание оказалось причиной смерти для 70% умерших.
Выявляемость и смертность
Число умерших от злокачественных новообразований россиян в 2017 году составило 274,2 тыс. человек — почти столько же, сколько в 2015-м, когда в России был поставлен рекорд смертности от рака за 11-летний период. 22,5% пациентов, у которых впервые диагностировали злокачественное новообразование, умерли в первый же год после диагностики. Доля таких пациентов уменьшается: десять лет назад их было почти 30%, 20 лет назад — более 36%. Злокачественные новообразования на первой и второй стадиях стали выявлять на 1,5% чаще, чем в 2016 году.
По сравнению с 2016 годом в России стали чаще выявлять рак тестикул — на 13,2% случаев больше в 2017-м и пениса — на 7,4% больше.
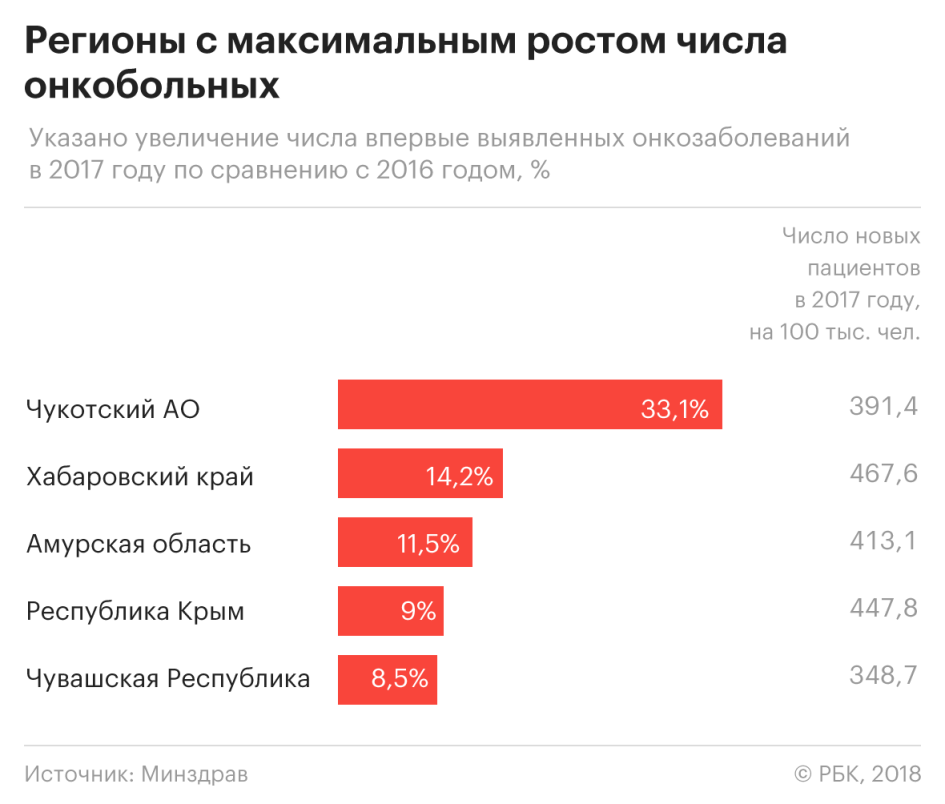
Выявляемость в регионах
Самый большой рост числа новых пациентов с онкологическими заболеваниями зафиксирован в Хабаровском крае — 6,2 тыс. впервые выявленных злокачественных новообразований. Это на 14% больше, чем годом ранее.
Много новых пациентов также в Амурской области — там рост числа выявленных заболевших составил 11%. Реже, чем в 2016 году, стали выявлять злокачественные новообразования в Ленинградской области (на 9,7%) и в Адыгее (на 9,6%).
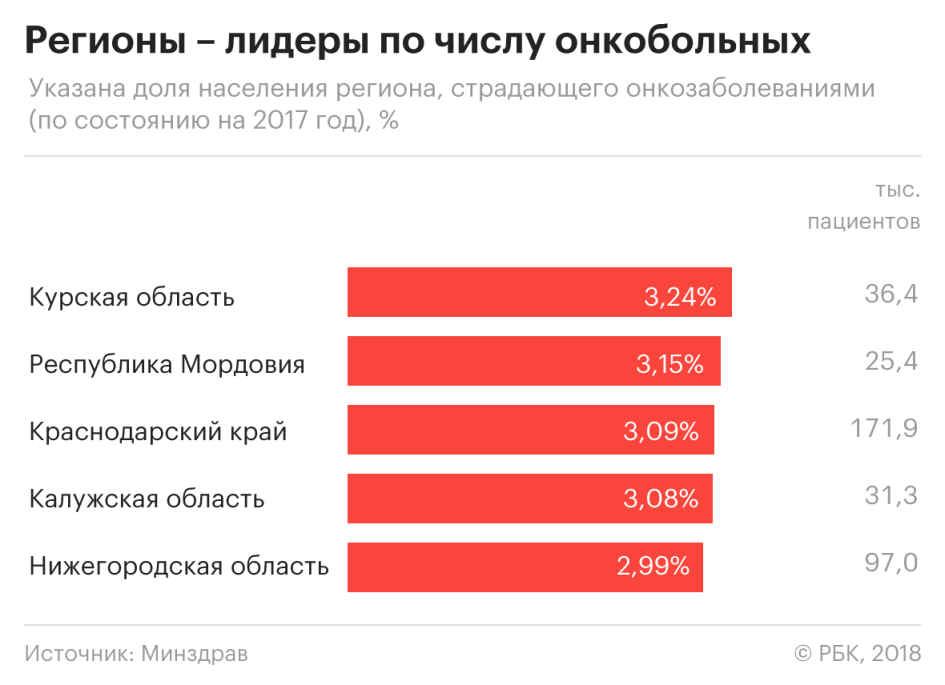
Самый высокий уровень онкологических заболеваний в 2017 году был в Курской области. Под диспансерным наблюдением в онкоцентрах там находятся 32,4 тыс. человек на миллион, то есть более 3% населения. Такая же ситуация была и в 2016 году. Более 3% населения состоит на учете в онкодиспансерах в Краснодарском крае и Мордовии. В Ингушетии число находящихся под диспансерным наблюдением в онкоцентрах увеличилось по сравнению с 2016-м почти на 11%.
В Севастополе зафиксировано самое существенное по России уменьшение доли населения, находящегося под наблюдением в онкодиспансерах, — с 3,2% в 2016 году до 2,8% в 2017-м.
Ведущими локализациями в структуре заболеваемости населения России злокачественными новообразованиями являются: новообразования трахеи, бронхов, легкого (15,3%), желудка (11,9%), кожи (10,4%, с меланомой - 11,7%), молочной железы (9,4%), ободочной кишки (5,5%), прямой кишки, ректосигмоидного соединения и ануса (4,5%), лимфатической и кроветворной ткани (4,4%), тела матки (3,3%), поджелудочной железы (3,0%), шейки матки (2,8%), почек (2,7%), яичников (2,6%), мочевого пузыря (2,6%).
Первые десять мест в структуре заболеваемости мужского населения России злокачественными новообразованиями распределены следующим образом: первое место - новообразования трахеи, бронхов, легкого (26,1%), второе - злокачественные опухоли желудка (13,9%), третье - новообразования кожи (8,3%), кожа с меланомой (9,3%), четвертое - опухоли ободочной кишки (4,6%). Значителен удельный вес злокачественных новообразований лимфатической и кроветворной ткани (4,6%), прямой кишки, ректосигмоидного соединения, ануса (4,3%), предстательной железы (4,3%), мочевого пузыря (4,2%), гортани (3,4%), поджелудочной железы (3,1%). Значимую по удельному весу группу у мужчин формируют злокачественные опухоли органов мочеполовой системы, составляя 12,2% от числа всех злокачественных новообразований.
Злокачественные опухоли молочной железы (18,4%) являются ведущей онкологической патологией у женщин. Доля новообразований кожи (12,5%, с меланомой - 14,1%) у женщин выше, а опухолей желудка (9,9%) - ниже, чем у мужчин. Далее (в порядке убывания распространенности) следуют: новообразования тела матки (6,5%), ободочной кишки (6,5%), шейки матки (5,4%), яичников (5,1%), трахеи, бронхов, легкого (4,8%), прямой кишки, ректосигмоидного соединения и ануса (4,7%), лимфатической и кроветворной ткани (4,2%). Таким образом, наибольший удельный вес в структуре онкологической заболеваемости женщин имеют злокачественные новообразования органов репродуктивной системы (свыше 35,4%), при этом опухоли половых органов составляют 17,0% всех злокачественных новообразований у женщин.
Удельный вес злокачественных новообразований органов системы пищеварения у женщин (28,8%) значительно ниже аналогичного показателя (36,5%) в структуре заболеваемости мужского населения, что отражает различную степень подверженности органоспецифическим канцерогенным факторам. Каждая третья злокачественная опухоль, диагностируемая у мужчин, локализуется в органах системы дыхания, в то время как у женщин процентная доля опухолей органов системы дыхания почти в 6 раз ниже.
Этиология и патогенез новообразований
Изучение этиологии болезней занимает важное место в медицинской науке вообще, и в частности, онкологии. Выявление этиологических факторов опухолей человека является необходимой предпосылкой для их профилактики. Адекватная и эффективная профилактика может быть осуществлена лишь на основании научно-обоснованных фактов об этиологии опухолей человека.
Многовековой опыт изучения этиологии болезней показал, что причина далеко не всегда реализуется в следствие, то есть причинный фактор не всегда приводит к болезни, и, что все поныне известные этиологические или причинные факторы имеют характер "вероятностной", а не так называемой "строгой" причинности. Для реализации причины в следствие необходим ряд дополнительных факторов и условий.
Еще римский врач Клавдий Галей, внесший важный вклад в развитие теории причинности в медицине, считал, что ни одна причина не может вызвать заболевания без соответствующей восприимчивости организма. Поразительной по современности ее звучания является теория, сформулированная Абу-Али-Ибн-Сина в XI веке: "Не всякая причина, достигающая тела, оказывает на него действие, иногда при этом нужны еще три вещи: сила, исходящая из активной силы, сила, исходящая из предрасполагающей силы тела, а также возможность встречи одной из этих с другой на время, достаточное, чтобы проявилось данное действие причины". В контексте причинно- следственных связей в онкологии, можно сказать, что действие канцерогенного вещества на человека, и риск развития опухоли, зависит от: а) дозы канцерогена; б) комплекса эндогенных факторов, определяющих предрасположенность организма к влиянию канцерогена, в) длительности воздействия канцерогенного фактора.
Концепция вероятностной причинности получила развитие в связи с разработкой теории вероятности и квантовой механики. Квантово-механические процессы обладают принципиально-статистическими свойствами, поэтому в пределах наблюдаемого нами мира вероятностно-статистический характер квантово-механических основ может вносить в конечном итоге момент неопределенности в любые процессы.
Вышесказанное говорит о том, что "строгая" причинность, то есть когда причина всегда реализуется в эффект, в результат, не единственная форма причинно-следственной связи. Она соседствует с "вероятностной" причинностью и последняя, по-видимому, является доминирующей формой причинно-следственной связи, как во всем объективном мире, так и в патологии.
Вероятностные процессы имеют статистический характер. "Результаты таких процессов, как правило, не могут быть предсказуемы однозначно. Каждое отдельное взаимодействие в статистически детерминированном процессе относительно случайно. Характерной особенностью подобного процесса является то, что он имеет место в дискретных системах, состоящих из большого числа элементов, относительно независимых друг от друга".
Концепция вероятностно-статистической причинности чрезвычайно важна для правильного понимания, трактовки и оценки как новых, так и старых научных факторов о причинах болезней. Отсутствие "строгой" причинно- следственной связи между фактором и болезнью, то есть то, что причина не всегда реализуется в болезнь, часто приводит к неправильному отрицанию таковой как причины.
Аналогичная ситуация имеет место и в онкологии. Введение химических канцерогенных веществ приводит к возникновению опухоли далеко не у всех лабораторных животных в экспериментальной группе. Курение, которое, как известно, является канцерогенным фактором для человека, вызывает рак далеко не у всех курильщиков, хотя, около 90% всех случаев рака легкого вызваны курением.
Показано, что ряд химических веществ и производственных процессов, ионизирующее и ультрафиолетовое облучение, курение, а также, возможно, некоторые экзогенные вирусы, являются этиологическими факторами опухолей человека, которые, однако, имеют вероятностно-статистический характер. Это означает, что экспозиция к вышеуказанным факторам не равнозначна заболеванию злокачественными опухолями. Для реализации эффекта канцерогенного фактора, будь то химическое вещество или вирус, необходимы ряд дополнительных влияний, и конечный результат взаимодействия канцероген - организм зависит от взаимодействия ряда известных и неизвестных экзогенных и эндогенных факторов.
Ряд унаследованных характеристик внутренней среды организма как то способность метаболизировать канцерогены и проканцерогены, несомненно, имеет важное значение в том, кто из экспонированных заболеет раком. От цвета кожи человека, например, зависит чувствительность к канцерогенному действию ультрафиолетовых лучей.
Степень выраженности вероятностно-статистической причинности в медицине, а, в частности, в онкологии, различна. Имеются примеры, когда вероятностно-статистическая причинность приближается к "строгой" причинности. то есть причинности, следствие которой высоко предсказуемо. Примером вышеуказанному является высокая вероятность развития злокачественных опухолей у людей с генетическими синдромами, такими как атаксия - телеангиоэктазия, анемия Фанкони, пигментная ксеродерма, синдром Блюма, семейный полипоз и синдром Гарднера, нейрофиброматоз. Высокая вероятность развития злокачественных опухолей у людей с вышеуказанными генетическими синдромами, может быть объяснена тем, что эти синдромы, как и, по-видимому, связанные с ними злокачественные опухоли, обусловлены наследованием определенной генетической информации, а наследование генетической информации ввиду своей высокой стабильности и предсказуемости приближается к так называемой "строгой" детерминации.
На понятии вероятностно-статистической причинности основана концепция факторов риска, получившая распространение в современной эпидемиологии.
Для практических целей эпидемиологам и было предложено ввести в научный лексикон понятия "достаточной" или "полной" причины, которой "достаточно" для возникновения заболевания, и причины, которая является частью "полной" причины или "частичной" причины, которая лишь увеличивает вероятность развития заболевания. Причинные факторы, изучаемые в эпидемиологии, являются "частичной" причиной. Несмотря на то, что экспозиция к последней недостаточна для возникновения болезни, ее изъятие или блокирование может привести к тому, что "полная" причина станет "неполной", недостаточной для возникновения болезни, по крайней мере, в пределах одного определенного патогенетического механизма.
Поэтому с точки зрения практической эпидемиологии, а прежде всего, с позиции профилактики, знания о вероятностно-статистических этиологических факторах опухолей человека чрезвычайно важны, так как манипуляция этими факторами может привести к значительному снижению заболеваемости злокачественными опухолями.
В эпидемиологии, как и во всех других научных дисциплинах, первым этапом исследования является наблюдение и формулировка гипотезы. Гипотезы об этиологических факторах той или иной болезни эпидемиологическая наука черпает чаще всего из клинической практики и данных о распространении болезни у человека: о распространении географическом, этническом, в различных религиозных группах, концентрации того или иного заболевания в различных населенных пунктах, вокруг тех или иных предприятий, у работников различных профессий, у лиц с различными бытовыми привычками, в определенных семьях, у людей, болевших теми или иными болезнями и т.д.
Эпидемиология неинфекционных болезней, частью которой является онкоэпидемиология, оперирует рядом специфических методов, разработанных специально для изучения этиологических факторов болезней человека. К ним относятся методы описательные, аналитические и экспериментальные.
Описательная эпидемиология изучает распространение отдельных форм злокачественных опухолей в человеческом обществе в отдельных группах населения. Целью описательной эпидемиологии является описание особенностей распространения злокачественных опухолей. Ее предметом является изучение заболеваемости и смертности в различных географических регионах, населенных пунктах, среди различных групп населения. Кроме того, описательная эпидемиология изучает связь (ассоциацию) между различными характеристиками данного региона, населенного пункта или населения, например, факторами окружающей среды или образа жизни и показателями частоты злокачественных опухолей. Этот тип эпидемиологического исследования принято называть корреляционным или экологическим. С помощью этого метода можно определить корреляцию между степенью выраженности в данном регионе или среди данного населения того или иного фактора, в том числе факторов окружающей среды и быта, и заболеваемостью и смертностью от злокачественных опухолей. Однако, возможности корреляционного метода в изучении причинно-следственных связей ограничены. Корреляционный метод может выявить связь между экспозицией к тому или иному фактору и частотой болезни в данном населении, но не способен выявить связь между экспозицией и индивидуальным риском болезни.
Дальнейшим шагом в изучении этиологического фактора является попытка “сужения” ассоциации от ассоциации между экспозицией и населением к ассоциации между экспозицией и индивидуальным человеком, который заболеет и заболел раком, так как, несомненно, что высокая частота этиологического фактора в населении не означает, что частота экспозиции к данному этиологическому фактору выше среди людей, которые заболеют или заболели раком, чем у другой части данного населения.
Такого рода подход к изучению этиологических факторов возможен с помощью методов аналитической эпидемиологии.
К методам аналитической эпидемиологии относятся:
1.Проспективное или когортное исследование;
2. Ретроспективное исследование методом случай-контроль. С помощью этих методов можно выявить ассоциацию (связь) между экспозицией к изучаемому этиологическому фактору и конкретным заболеванием.
Результаты этих исследований обычно выражаются в показателях относительного риска, которые представляют собой соотношение заболеваемости группы экспонированного населения к заболеваемости группы неэкспонированного населения или соотношение заболеваемости населения с более выраженной экспозицией к заболеваемости населения с менее выраженной экспозицией. Показатели относительного риска являются математическим выражением степени вероятности заболеть той или иной болезнью по причине экспозиции к определенному фактору.
Проспективное или когортное и ретроспективное исследование методом случай-контроль отличаются друг от друга тем, что в первом здоровое население, включенное в когорту для проспективного наблюдения, классифицируется в зависимости от того экспонированы они или нет к интересующему исследователей этиологическому фактору или в зависимости от степени выраженности экспозиции. В то время как в ретроспективном исследовании методом случай-контроль изучаемая группа населения классифицируется на основании присутствия или отсутствия болезни, а не экспозиции. Обычно в исследование включаются больные, и к ним из той же группы населения отбирается контрольная группа.
Экспозиция к тому или иному фактору, степень ее выраженности может быть охарактеризована как на основании уже имеющихся гигиенических данных, так и с помощью ее измерения. Часто для оценки экспозиции применяется анкетный метод.
Экспериментальные эпидемиологические методы или, так называемые, интервенционные методы предполагают постановку эксперимента среди людей. В них обычно изучается эффект, разумеется, удаления или снижения экспозиции к предполагаемому этиологическому фактору на заболеваемость и смертность от опухоли, этиологически связанной с вышеуказанным фактором . Имеется другой вид интервенционных исследований , когда включенные в исследование лица подвергаются воздействию факторов с предположительно ингибирующим действием. За последние годы распространение получили интервенционные методы исследования, в которых изучается роль витаминов, как ингибиторов канцерогенеза у человека.
Таким образом, эпидемиология, как всякая другая научная дисциплина, имеет в своем арсенале как эмпирические, так и экспериментальные методы исследования, целью которых является выявление вероятностных причин или этиологических факторов опухолей человека. Фактор, будь то экзогенный или эндогенный, можно называть этиологическим только тогда, когда эпидемиологически доказана причинно-следственная связь между экспозицией к фактору и болезнью.
Необходимо отметить, что грубой методологической ошибкой является отнесение к этиологическим связям связей ассоциативных. Выявление ассоциативных связей может привести к формулировке гипотезы о возможной этиологической роли того и иного фактора, но не может служить ее доказательством. Как бы прочна не была ассоциация, она всегда будет коренным образом отличаться от причинных отношений.
Несмотря на ограниченность методологических подходов в изучении вероятностных причин и их ограничения от связей ассоциативных, эпидемиология выработала ряд формальных критериев, на основании которых можно дифференцировать причинно-следственные связи от ассоциативных связей.
Необходимым условием для определения причинно-следственной связи является последовательность в действии причины и ее следствия; действия причины или экспозиции к причинному фактору должна предшествовать следствию или заболеванию.
Одним из главных показателей возможной причинно-следственной связи принято считать выраженность ассоциации между фактором и болезнью. Выраженность ассоциации или связи определяется величиной относительного риска. Вероятность того, что выраженная ассоциация имеет причинно- следственный характер больше, чем вероятность причинно-следственного характера слабой ассоциации, последняя, вероятно, более часто носит случайный характер.
Существенным критерием причинно-следственной связи является количественная связь между причиной и следствием по типу “доза-эффект”, то есть от дозы (уровня и длительности экспозиции) зависит частота болезни. Однако, на практике не все причинно-следственные связи могут быть охарактеризованы соответственной кривой “доза-эффект” прежде всего потому, что экспозиция к ним может быть одинаково высокой или одинаково низкой для всего изучаемого населения.
Очень важно, чтобы полученные сведения о рассматриваемом этиологическом факторе не противоречили тому, что известно о биологии и патологии данного заболевания. Кроме того, желательно, чтобы данные, полученные в результате изучения болезни у человека, были подкреплены результатами экспериментальных исследований у лабораторных животных.
При отсутствии эпидемиологических данных химические вещества, для которых имеются достаточно обоснованные данные об их канцерогенности у лабораторных животных, с практической точки зрения должны рассматриваться как представляющие канцерогенную опасность и для человека.
В сентябре Международное агентство по изучению рака (МАИР) [1] выпустило обновление GLOBOCAN [2] – онлайн-инструмента, содержащего полную информацию о заболеваемости и смертности 36 видами злокачественных новообразований в 185 странах мира. МАИР является частью Всемирной организации здравоохранения (ВОЗ), и его миссия заключается в координации и проведении исследований причин возникновения опухолей у человека, механизмов канцерогенеза и разработке научно-обоснованных стратегий противораковой борьбы.
Согласно опубликованным данным, в 2018 году ожидается 18,1 миллионов новых случаев и 9,6 млн. смертей от злокачественных новообразований [3]. Отмечается быстрый рост абсолютных показателей заболеваемости и смертности злокачественными новообразованиями в мире (в 2012 году они составляли 14,1 и 8,2 миллионов, соответственно [4]). Причины этого сложны, они отражают как старение и рост численности населения, так и изменения в распространенности и распределении основных факторов риска развития рака, часть из которых связаны с социально-экономическим развитием. Во всем мире общее число людей, живущих в течение 5 лет после постановки онкологического диагноза, оценивается в 43,8 миллиона человек [5]. С учетом кумулятивных рисков в мире для обоих полов развития рака 21,4% и смерти от злокачественного заболевания 17,7% до достижения 75 лет, при условии отсутствия других причин смерти, один из 5 мужчин и одна из 6 женщин заболеет, а один из 8 мужчин и одна из 10 женщин умрет от онкологического заболевания.
Рак легкого, рак молочной железы у женщин и рак толстой кишки лидируют по заболеваемости и входят в топ-5 по смертности (первое, пятое и второе места, соответственно). Совместно эти три типа злокачественных опухолей составляют порядка трети всех случаев онкологической заболеваемости и смертности в мире. Однако наиболее часто выявляемые злокачественные образования и лидирующие причины смерти среди онкологических заболеваний значимо различаются в разных странах и внутри каждой страны в зависимости от уровня экономического развития и связанных с этим социальных факторов и образа жизни.
Согласно последним опубликованным данным МНИОИ им. П.А. Герцена, в 2017 г. в России впервые в жизни выявлено 617,2 тыс. случаев злокачественных новообразований. Прирост данного показателя по сравнению с 2016 г. составил 3% [6]. Онкологические заболевания занимают второе место среди причин смерти населения России, в 2017 году от злокачественных новообразований умерло 290,7 тыс. больных, что составляет 15,9% в общей структуре смертности. В 2017 г. кумулятивный риск, т. е. риск развития злокачественного заболевания, которому подверглось бы лицо в течение жизни до 75 лет при условии отсутствия всех причин смерти, составил 26,5% (в 2007 г. – 23,4%): для мужчин – 31,3% (в 2007 г. – 28,3%), для женщин – 23,8% (2007 г. – 20,5%).
Около 40% впервые выявленных злокачественных новообразований в России имели III-IV стадию заболевания, что обуславливает достаточно высокий показатель одногодичной летальности (22,5%, по альтернативной оценке, может превышать 26%). Почти 2 миллиона пациентов (1 958 223) или 53,9% всех больных со злокачественными новообразованиями под наблюдением онкологических учреждений состояли на учете 5 и более лет (для сравнения в 2016 г. этот показатель составлял 53,3%) [7].
На первом месте по заболеваемости населения России среди мужчин стоят опухоли трахеи, бронхов, легкого (17,4%), среди женщин – рак молочной железы (21,1%). В структуре смертности от злокачественных новообразований лидируют опухоли органов дыхания (трахеи, бронхов, легкого), толстой кишки, желудка, молочной железы, поджелудочной железы [6].
Последние исследования в странах с высоким уровнем дохода показывают, что от одной трети до двух пятых новых случаев онкологических заболеваний можно избежать, устранив или снизив подверженность известным факторам риска, связанным с образом жизни или окружающей средой. Это говорит о важности внедрения и продвижения первичной профилактики на международном уровне, повышения информированности о пользе профилактических программ.
Важно отметить, что высококачественные данные канцер регистра – основа планирования и внедрения доказательных программ противораковой борьбы – недоступны в большинстве стран с низким и средним уровнем доходов. Данные смертности доступны для большинства стран через ВОЗ, хотя степень детализации и качество данных (как точность записанной причины смерти, так и полнота регистрации) значимо различаются; в настоящее время только около 1 из 5 стран может предоставить отчеты о регистрации смертей высокого качества [3].
Читайте также:


