Позитронная эмиссионная томография при раке молочной железы
ЗАПИСЬ НА ПЭТ/КТ
Единый центр записи на ПЭТ/КТ в городах РФ.
Платно или по ОМС (только в Москве).
Все виды: глюкоза, холин, метионин, галлий.


ЕДИНЫЙ ЦЕНТР ЗАПИСИ НА ПЭТ/КТ
+7 (499) 753-77-85
Бесплатное ПЭТ/КТ по квоте (по ОМС) - делается только в Москве и только с глюкозой по направлению из онкодиспансера по месту жительства или от врача-онколога государственной больницы.
ПЭТ/КТ с глюкозой делается в 15 городах России на платной основе и СРОЧНО!
ПЭТ с холином делается только на платной основе. В трех городах: Москва, Санкт-Петербург, Уфа. Стоимость 45 000 - 85 000 рублей. Можно сделать СРОЧНО!
ПЭТ с галлием проводится Санкт-Петербурге и Екатеринбурге. По ОМС не делается, только на платной основе. Стоимость: 45 000 - 85 000 рублей. Можно сделать СРОЧНО!
ПЭТ с метионином делается только на платной основе и только в Санкт-Петербурге.
ПЭТ с тирозином делается только на платной основе и только в Уфе.
Помимо ПЭТ, всем нашим пациентам мы можем предложить эффективное лечение: пересмотр гистологии, лечение в ведущих клиниках Москвы и за границей.

- Цена
- Где сделать
- Отзывы
- Фото
- Видео

20 интересных фактов о ПЭТ/КТ
1. Первые упоминания о ПЭТ появились в 50-х годах XX века.
2. Уже в 1972 году этот вид диагностики получил широкое распространение в США.
3. В России первое обследование ПЭТ было проведено в 1997 году.

20 интересных фактов о ПЭТ/КТ
4. Точность полученной при сканировании информации достигает 99%, тогда как при КТ и МРТ этот показатель в среднем составляет 70-85%.
5. В Европе лидер по ПЭТ/КТ исследованиям — Германия, где свыше 100 клиники имеет соответствующее оборудование, тогда как в России их число не превышает 30.

20 интересных фактов о ПЭТ/КТ
6. Результаты ПЭТ/КТ используют три отрасли медицины — онкология, кардиология, неврология.
7. Доза радиации при ПЭТ/КТ обследовании не превышает облучения при обычном рентгене.
8. Некоторые виды ПЭТ/КТ в России не проводятся. Например, обследование с галлием 68.

20 интересных фактов о ПЭТ/КТ
9. Диагностика ПЭТ/КТ выявляет опухоли на более ранних стадиях, чем КТ или МРТ, потому что метаболические нарушения можно зафиксировать тогда, когда структурные изменения еще отсутствуют.
10. В большинстве случаев информативность полученных снимков оказывается выше, чем у проведенной биопсии пораженного болезнью органа. Особенно это справедливо для обследования головного мозга с метионином.

20 интересных фактов о ПЭТ/КТ
12. Методика позволяет обнаружить патологии размером до 1 мм.

20 интересных фактов о ПЭТ/КТ
13. В России ПЭТ/КТ есть только в 9 городах: Москве, Санкт-Петербурге, Воронеже, Екатеринбурге, Уфе, Курске, Орле, Тамбове, Липецке. Стоимость такого обследования в нашей стране намного дешевле, чем в Европе. Поэтому нет смысла ехать в Германию и Израиль где процедура стоит намного дороже.
14. с 2016 года в России ПЭТ КТ можно сделать бесплатно по полису ОМС. Для этого нужно получить соответствующее направление от врача и записаться на обследование в одной из клиник, где доступна эта услуга.

20 интересных фактов о ПЭТ/КТ
15. После ПЭТ/КТ нет необходимости в других видах диагностики — обычно это исследование дает ответы на все вопросы.
16. Ошибки при ПЭТ/КТ связаны только с человеческим фактором: неверной трактовкой результатов, неправильной подготовкой к обследованию, нарушением технологии сканирования и др.

20 интересных фактов о ПЭТ/КТ
17. Большинство опухолей активно питается глюкозой, поэтому для обследования чаще всего используют РФП 18F-фтордезоксиглюкозу — она накапливается в онкологическом очаге. Однако этот РФП не подходит для исследования головного мозга, который всегда активно поглощает это вещество.
18. Единственное абсолютное противопоказание для обследования — беременность. Остальные входят в разряд относительных.

20 интересных фактов о ПЭТ/КТ
19. В некоторых случаях проводят ПЭТ/КТ с контрастом — помимо радиоферментов пациенту вводят контрастное йодсодержащее вещество, повышающее точность и информативность обследования.
20. От качества подготовки к ПЭТ/КТ зависит и точность полученных данных. Пациенту предписывают соблюдать специальную диету и не перенапрягаться за 2-3 дня до сканирования.
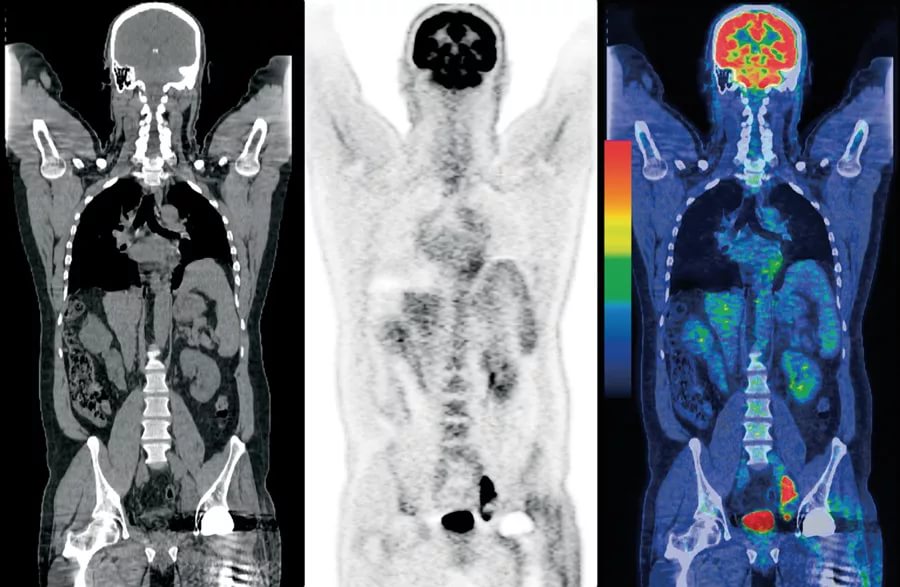
Позитронно-эмиссионная томография (ПЭТ) в последнее время становится все более популярным методом исследования, используемым для обнаружения, стадирования и контроля различных злокачественных опухолей. Метод основан на регистрации гамма-излучения, испускаемого радиоактивными элементами (радионуклидами), которые вводятся в организм человека в составе специальных меченых веществ — радиофармпрепаратов (РФП). При совмещении ПЭТ-сканера с компьютерным томографом (КТ) говорят о комбинированной позитронно-эмиссионной и компьютерной томографии (ПЭТ-КТ).
В чем разница КТ и ПЭТ-КТ при раке груди
В основе таких методов, как КТ и МРТ, лежит визуализация анатомических структур с целью выявления патологических изменений у пациенток с раком молочной железы, стадирования и контроля. В то же время, позитронно-эмиссионная томография (ПЭТ) позволяет обнаружить патологические измененения метаболизма 18-фтор-2-дезокси-D-глюкозы (ФДГ), что делает возможным получение качественной информации о ее накоплении в опухоли, и является критичным моментом при постановке диагноза и при контрольных исследованиях. Комбинация ПЭТ-КТ имеет преимущества перед изолированным использованием ПЭТ, поскольку появляется возможность более точной привязки очагов повышенного захвата ФДГ к определенным анатомическим областям. Кроме того, при этом методе уменьшается время исследования. Также ПЭТ-КТ позволяет частично преодолеть ограниченную специфичность ПЭТ, при которой могут обнаруживаться очаги гиперметаболизма глюкозы в доброкачественных опухолях и воспалительно измененных тканях (например, при туберкулезе). Необходимым условием информативности метода является достоверная оценка изображений опытным радиологом, иногда с применением Второго мнения.
Ранняя диагностика рака молочной железы
Рак молочной железы является самой распространенным новообразованием у женщин во всем мире и ведущей причиной женской смертности в результате рака. Во всем мире каждый год насчитывается примерно 1,38 миллионов вновь возникших случаев заболевания, а также 458 тысяч летальных исходов в течение года, обусловленных этой болезнью. Многие факторы риска хорошо известны. Тем не менее, точные причины возникновения рака молочной железы не определены. Например, наличие заболевания у родственников и предков является хорошо известным фактором риска: при нем вероятность развития рака возрастает в два или три раза. Также предполагается, что мутации в гене BRCA (1 и 2) и мутации белка p53 в значительной степени повышают риск развития опухоли. Ранняя диагностика является основополагающим способом контроля, так как определяет способ лечения, а также прогноз и шансы пациентки на выживание.
Как обнаружить рак груди
К методам диагностики, основанным на обнаружении анатомических изменений, относятся маммография, ультразвуковое исследование (УЗИ), компьютерная (КТ) и магнитно-резонансная томография (МРТ). Они широко используются в клинической практике для выявления первичной опухоли и определения стадии рака молочной железы. Эти методы диагностики постоянно улучшаются, кроме того, в практику также внедряются новые способы исследования молочных желез: оптическая маммография, однофотонная эмиссионная томография (ОФЭКТ) и позитронно-эмиссионная томография (ПЭТ), которые позволяют перенести информацию относительно анатомических изменений, функции, метаболизма с макроскопического на молекулярный уровень.
В сочетании с традиционными методами лучевой диагностики, радионуклидные методы исследования, позволяющие визуализировать биологические процессы, позволили сделать шаг вперед в обнаружении рака. И теперь новыми целями использования радионуклидных методов является разделение различных биохимических изменений в тканях.
Оценка первичной опухоли
Возможность обнаружения рака молочной железы посредством ПЭТ зависит от размера и тканевого строения опухоли. Сообщается, что чувствительность ПЭТ составляет 68% для малых опухолей (меньше 2 см), и 92% для опухолей большего размера (2-5 см), однако, общая точность при выявлении рака in situ является низкой (чувствительность составляет 2-25%). Таким образом, главным фактором, ограничивающим использование ПЭТ при визуализации молочной железы, является низкий уровень обнаружения маленьких опухолей и неинвазивного рака.
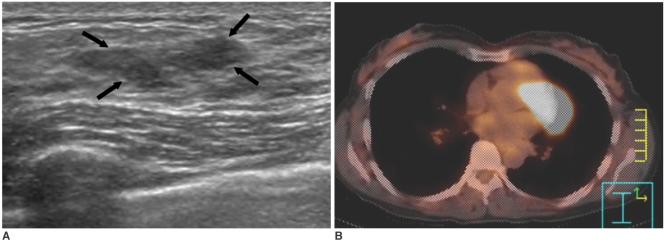
Протоковый рак in situ у 49-летней женщины. А: на УЗИ определяется гипоэхогенное объемное образование размером 2,5 см с нечеткими краями, расположенное в верхних отделах левой молочной железы (отмечено стрелками). В: на ПЭТ-КТ скане не выявлено признаков повышенного захвата ФДГ в левой молочной железе. При оперативном вмешательстве подтвердился неинвазивный протоковый рак.
Тем не менее, метод играет важную роль для некоторых групп пациенток, например, с плотными молочными железами либо с наличием имплантов. Позитронно-эмиссионная томография используется для определения множественности опухолевого поражения; для выявления локализации первичной опухоли у пациенток с метастазами, когда маммография неинформативна; а также у тех пациенток, которым противопоказана биопсия. ПЭТ-КТ имеет потенциальные преимущества перед изолированной ПЭТ при оценке поражений малого размера, в которых может быть выявлен пониженный захват ФДГ вследствие эффекта частичного объема при ПЭТ, так как гиперметаболизм глюкозы может быть характерен и для патологических, и для нормальных анатомических структур.

Инвазивный рак молочной железы у 57-летней женщины. А: на скрининговой рентгенограмме левой молочной железы в косой медиолатеральной проекции определяется объемное образование со спикулообразными краями, размером около 1,1 см (отмечено стрелкой). В: при ПЭТ обнаружен очаг слабо выраженного гиперметаболизма ФДГ (стандартизированный уровень накопления = 1,2) в левой молочной железе. Очаг поражения сложно обнаружить в результате эффекта частичного объема. С: на ПЭТ-КТ определяется очаг гиперметаболизма ФДГ на ограниченном участке (отмечен стрелкой) в левой молочной железе.
Оценка вторичного поражения лимфатических узлов
Вторая задача метода — это обнаружение метастазов рака молочной железы в лимфатических узлах. Метастатическое поражение подмышечных лимфоузлов является важным фактором, определяющим прогноз. У пациенток, страдающих раком молочной железы, при вторичном поражении четырех и большего количества лимфоузлов подмышечной группы, имеется значительно более высокий риск рецидива. Сообщается о чувствительности ПЭТ при визуализации подмышечных лимфоузлов у пациенток с раком молочной железы в пределах 79-94%, и специфичности 86-92%. При ПЭТ-КТ можно точно определить местоположение и отличить друг от друга лимфатические узлы, вторично пораженные опухолью, и реактивно измененные (незлокачественные) лимфоузлы, в то время как на КТ будут обнаруживаться лишь множественные увеличенные лимфоузлы подмышечной группы без четких дифференциальных признаков.
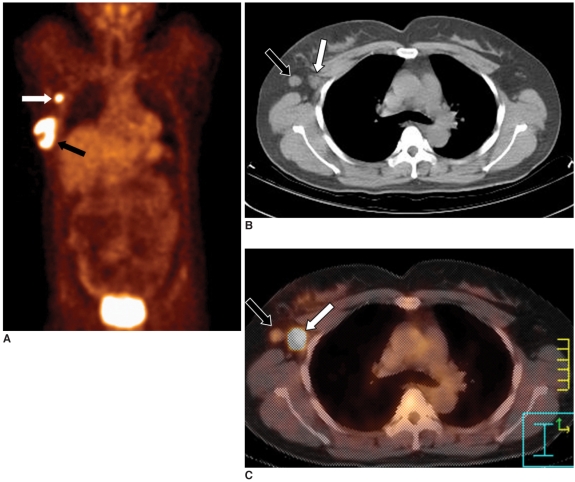
Метастазы в подмышечные лимфатические узлы у 45-летней женщины с инвазивным протоковым раком молочной железы. А: на ПЭТ визуализируется очаг гиперметаболизма ФДГ в правой железе (черная стрелка) и в подмышечной области (белая стрелка). В: на КТ определяются два увеличенных подмышечных лимфоузла справа (отмечены стрелками). С: ПЭТ-КТ позволяет определить точную локализацию лимфоузлов, вторично пораженных опухолью (белая стрелка, стандартизированный уровень накопления РФП = 9,9), визуализируется также реактивно измененный лимфоузел (черная стрелка). Среди 21 лимфоуза, удаленного во время операции, метастазы были выявлены только в одном.
Метастазы рака молочной железы во внутригрудные или медиастинальные лимфоузлы часто клинически ничем себя не проявляют. Количество обнаруживаемых патологических изменений со стороны внутригрудных или медиастинальных узлов (у пациенток с метастатическим либо рецидивным раком молочной железы) при ПЭТ почти в два раза больше по сравнению с традиционной КТ. Кроме того, ПЭТ-КТ выглядит более применимой по сравнению с КТ для оценки внутригрудных лимфатических узлов и лимфоузлов средостения, поскольку возможности КТ в обнаружении метастазов в лимфоузлы малого размера довольно ограничены.
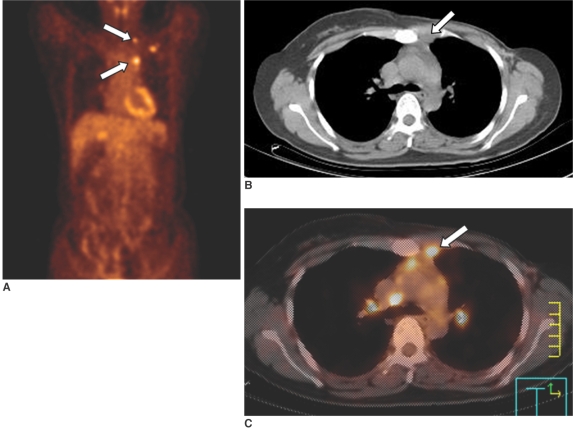
Метастазы в лимфоузлы средостения у женщины, 10 месяцев назад перенесшей модифицированную радикальную левостороннюю мастэктомию. А: на ПЭТ определяются множественные участки гиперметаболизма РФП в верхних отделах грудной клетки слева. В: на КТ визуализируется небольшой участок мягкотканной плотности в переднем средостении (отмечен стрелкой). В: на ПЭТ-КТ обнаружено, что мяготканный участок в переднем средостении, выявленный при КТ, соотносится с зоной гиперметаболизма ФДГ, что позволяет предположить метастазы во внутригрудные лимфатические узлы.
Оценка отдаленных метастазов
Рак молочной железы часто дает отдаленные метастазы в легкие, печень и кости. Преимуществом ПЭТ всего тела перед традиционными методами диагностики, такими как рентгенография органов грудной клетки, сцинтиграфия скелета и УЗИ органов брюшной полости, является возможность обнаружения отдаленных метастазов в различных областях тела и органах во время одного исследования. Было обнаружено (Moon et al.), что ПЭТ всего тела обладает высокой диагностической точностью в отношении пациенток, у которых имеется подозрение на рецидив рака или на метастатическое поражение. На основании количества обнаруженных очагов чувствительность метода в обнаружении отдаленных метастазов составила 85%, а специфичность 79%.
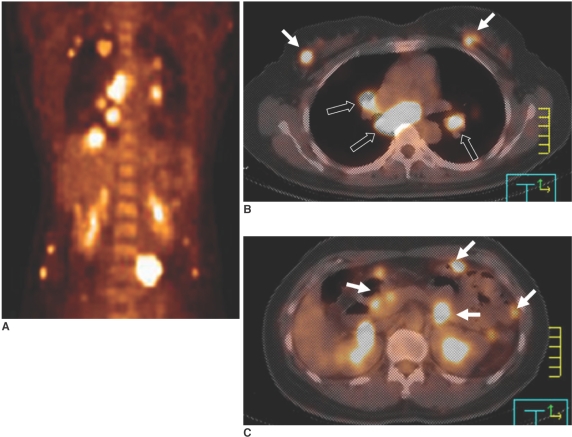
Множественные отдаленные метастазы у 44-летней пациентки, страдающей раком обеих желез. А: на ПЭТ определяются множественные зоны гиперметаболизма ФДГ в грудной клетке и брюшной полости. B, C: на ПЭТ обнаружены также зоны гиперметаболизма ФДГ в обеих молочных железах (отмечены белыми стрелками на томограмме B), в лимфоузлах средостения (отмечены черными стрелками на томограмме B), и во внутренних органах (отмечены стрелками на томограмме C).
В исследовании (Cook et al.) было обнаружено, что ПЭТ превосходит сцинтиграфию скелета при выявлении остеолитических метастазов рака молочной железы. И, наоборот, остеобластические метастазы характеризуются низкой метаболической активностью и часто не обнаруживаются посредством ПЭТ. Однако ПЭТ-КТ позволяет преодолеть это ограничение: остеобластические метастазы, даже если они не видны на ПЭТ, будут визуализироваться на КТ-сканах.
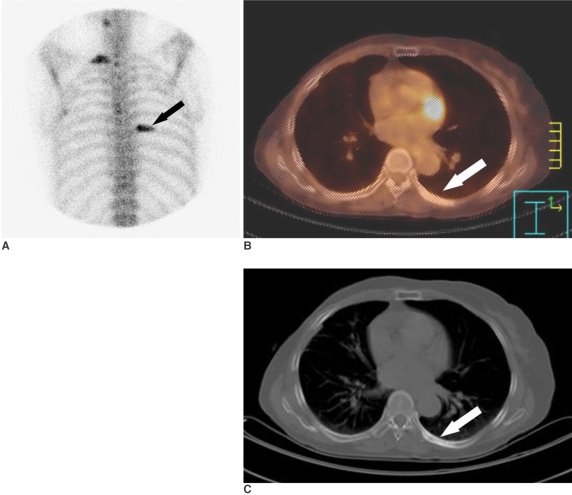
Метастазы в кости у 64-летней женщины, которой была выполнена правосторонняя модифицированная радикальная мастэктомия 36 месяцев назад. A: при сцинтиграфии скелета обнаруживаются очаги гиперфиксации ФДГ в первом ребре справа и седьмом ребре слева (стрелки), которые, скорее всего, связаны с метастатическим поражением ребер. B: на ПЭТ-КТ не определяется гиперметаболизма ФДГ в седьмом ребре слева (стрелка). C: на КТ определяется остеобластическое поражение седьмого ребра слева (стрелка).
Лечение рака молочной железы
Для лечения пациенток, у которых опухоль имеет большой размер, либо наблюдается ее локальное распространение, используется неоадъювантная химиотерапия с целью уменьшения стадии первичной опухоли перед оперативным вмешательством и устранения метастазов. Кроме того, в нескольких исследованиях было продемонстрировано, что выживаемость пациенток с резистентными опухолями может увеличиваться при использовании альтернативной химиотерапии и (или) при удлинении курсов химиотерапии. Так как химиотерапия имеет побочные эффекты, необходимо как можно скорее выделить пациенток, которые не получают эффекта от применяемого лечения.
В настоящее время лучевые методы диагностики часто используются для определения ответа на терапию путем оценки изменений размеров опухоли. Тем не менее, последовательные измерения размера опухоли во многих случаях не позволяют сделать вывод о наличии раннего ответа. Эффективность ПЭТ при оценке ответа на терапию была подтверждена для различных типов новообразований. В исследовании (Smith et al.) было показано, что средняя редукция захвата ФДГ после первого курса химиотерапии была в большей степени выражена в очагах, для которых макроскопически был обнаружен частичный или полный ответ, или полный ответ при микроскопическом исследовании, по сравнению с резистентными поражениями при гистопатологическом исследованиях. По данным (Rose et al.) после единственного курса химиотерапии при помощи позитронно-эмиссионной томографии было возможно спрогнозировать полный ответ на терапию при патогистологическом исследовании, чувствительность при этом составляла 90%, а специфичность 74%. Если принять степень снижения захвата ФДГ меньше 55% от первоначального значения за пороговое значение, свидетельствующее о наличии реакции на лечение, изменения на ПЭТ у всех респондентов в данном исследовании были корректны и подтвердились патогистологически (100% чувствительность и 85% специфичность).
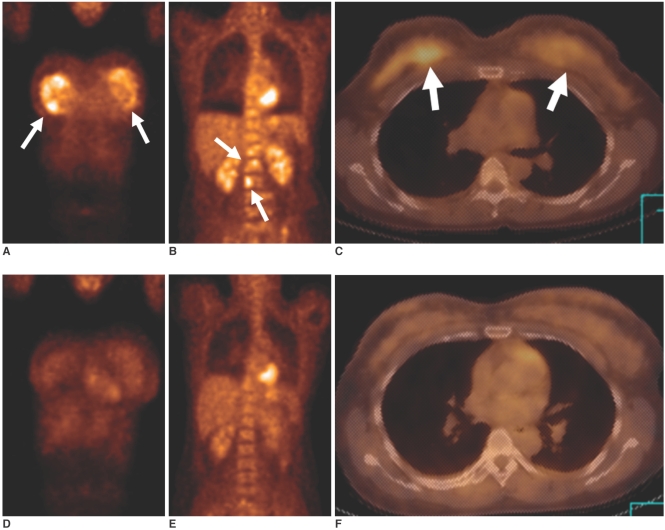
Изображения иллюстрируют контроль химиотерапии у 35-летней пациентки, страдающей раком молочной железы с метастазами в кости. A-C: на ПЭТ, выполненной изначально (A, B) и ПЭТ-КТ (C) определяется в значительной степени выраженный гиперметаболизм ФДГ в обоих молочных железах и во многих позвонках. D-F: на контрольной ПЭТ (D, E) и ПЭТ-КТ (F), выполненных спустя три курса химиотерапии, определяется существенное снижение гиперметаболизма ФДГ в обоих молочных железах и позвонках.
ПЭТ-КТ также играет роль для лучевой терапии, т. к. позволяет точно оценить распространенность опухоли.
Контроль рецидива опухоли
Раннее распознавание рецидива опухоли является важным моментом, улучшающим выживаемость, поскольку подталкивает клиницистов к использованию различных способов лечения. Однако отличить истинный рецидив от постоперационных и лучевых изменений сложно при использовании лишь традиционных методов лучевой диагностики. При ограниченном, регионарном рецидиве преимущественно поражается молочная железа, кожа, подмышечные и надключичные лимфоузлы, а также грудная стенка.
Было обнаружено, что чувствительность и специфичность ПЭТ при обнаружении рецидива составляет 84% и 78% соответственно, в то время как чувствительность и специфичность традиционных методов исследования 63% и 61% соответственно. Предполагается, что ПЭТ является более эффективным методом оценки рецидива рака молочной железы по сравнению с традиционными методами визуализации в плане обнаружения изменений всего тела. Данные КТ, полученные при ПЭТ-КТ, позволяют установить соответствие анатомических структур и очагов гиперметаболизма ФДГ.
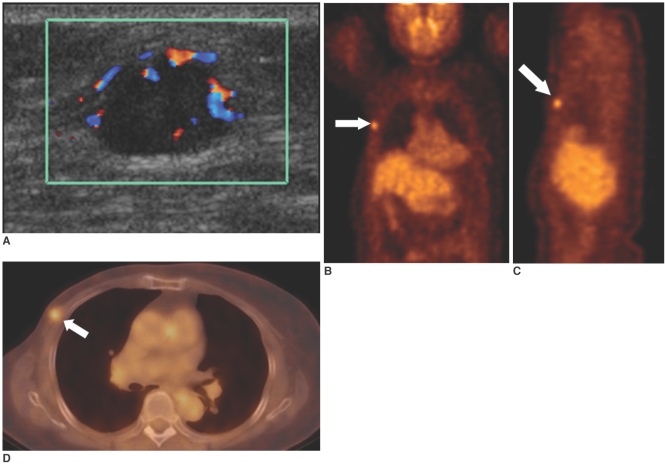
Локальный рецидив опухоли у 74-летней женщины, которой была выполнена модифицированная правосторонняя радикальная мастэктомия 8 лет назад. А: на УЗИ выявлено объемное образование овоидной формы, 1,4 см, с усиленным кровотоком, расположенный в правой грудной мышце в зоне мастэктомии. B, C: на ПЭТ определяется ограниченный очаг гиперметаболизма ФДГ (стандартизированный уровень накопления = 3,3) (стрелки) в правой половине грудной клетки. D: на ПЭТ-КТ определяется очаг гиперметаболизма ФДГ (стрелка) в правой грудной мышце, в то время как при использовании только ПЭТ определение точной локализации очага является затруднительным.
Расшифровка ПЭТ-КТ при раке молочной железы
В ряде случаев для повышения достоверности оценки результатов ПЭТ-КТ рекомендуется получить второе мнение специализированного радиолога. Это бывает необходимо при сомнительных или неоднозначных результатах первичного прочтения снимков. Второе мнение по ПЭТ-КТ помогает решить следующие задачи: снижение риска врачебной ошибки, более достоверная оценка первичной опухоли, уточнение стадии заболевания, достоверное исключение признаков метастатического поражения костей, печени или легких. Кроме того, в результате такой консультации онколог получает более подробное описание исследования, что помогает ему выбрать наиболее подходящий протокол лечения.
Заключение
ПЭТ/КТ играет важную роль в диагностике рака молочной железы, которая заключается в обнаружении и определении местоположения метастазов, контроле лечения и раннем выявлении рецидивов. Тем не менее, ограничивающим фактором ПЭТ/КТ в выявлении рака молочной железы является недостаточная способность обнаруживать опухоли малого размера.
Василий Вишняков, врач-радиолог
При подготовке текста использованы материалы:

Строяковский Даниил Львович
Руководитель химиотерапевтического отделения
Городской онкологической больницы №62,
член правления RUSSCO, кандидат медицинских наук,
Москва
Выражаю исключительно свое собственное мнение, основанное на каждодневной работе и постоянном просмотре дисков КТ, ПЭТ-КТ, МРТ и других рентгенологических исследований, во время консультаций пациентов.
На мой взгляд, сегодня независимо от нозологии выполнение ПЭТ-КТ исследования без введения внутривенного (в/в) контрастирования делает это исследование неполноценным. Без в/в контрастирования зачастую сложно оценить размер патологических образований и, самое главное, это исследование невозможно использовать в дальнейшем для оценки динамики процесса при сравнении с КТ исследованием. Если сделано ПЭТ-КТ без в/в контраста, то пациенту необходимо делать еще одно исследование – КТ с в/в контрастированием 3 зон (грудная клетка, брюшная полость и малый таз), чтобы дальше можно было оценивать эффективность лечения с помощью КТ. Если сделано сразу ПЭТ-КТ исследование с в/в контрастированием, то КТ-часть этого исследования с в/в контрастированием отлично подходит для оценки эффективности при дальнейшем использовании КТ. На мой взгляд, ПЭТ-КТ без в/в контраста должно быть очень редким исследованием и проводиться только при наличии жестких противопоказаний для введения в/в контраста (например, аллергическая реакция на йод или тяжелая почечная недостаточность). Не должно быть так, что ПЭТ-КТ исследование делают без в/в контраста из-за того, что тариф ОМС при добавлении стоимости контрастного вещества делает исследование менее прибыльным (к сожалению, сегодня это распространенная практика). Как результат – скупой платит дважды: пациенту приходится делать еще одно исследование – КТ с в/в контрастом.
Для чего нужно делать более углубленные методы исследований при онкологических заболеваниях, такие как КТ, МРТ, ПЭТ-КТ? Углубленное исследование практически может привести к повышению стадии заболевания или, крайне маловероятно, к снижению стадии. Всегда ли это необходимо? Это необходимо делать в том случае, если дополнительные знания о наличии метастатических очагов (регионарных или метастатических), которые не были видны при рутинном обследовании, приведут к изменению тактики лечения. Данное изменение тактики лечения должно быть более благоприятно для лечения пациента, как с точки зрения прогноза и выбора метода, так и последовательности лечения. Если углубленное исследование не приводит к изменению тактики лечения или может создать дополнительные сложности в принятии решения, за которыми не стоит реальное излечение или увеличение продолжительности жизни пациента, то проведение подобного исследования может носить негативный характер.
Местнораспространенный рак молочной железы: IIB-III стадии. Более сложная проблема. Здесь очень много факторов влияют на выбор тактики лечения. Основные: биологический тип опухоли, возраст и сопутствующая патология.
Если у больной Her2 позитивный вариант рака молочной железы, то предоперационная химиотаргетная терапия с очень высокой вероятностью перекрывает отсутствие информации о возможных клинически незначимых метастазах, пропущенных при рутинном обследовании. На мой взгляд, лучше лечить пациентку как с III стадией, проводить интенсивное лечение, т.к. это подразумевает куративный (а не паллиативный) подход. Получается, что у ПЭТ-КТ задача: перевести пациентку с III стадией в IV стадию, т.к. будут визуализированы субклинические очаги! А надо ли это? При использовании химиотерапии, с двойной таргетной блокадой, у больной имеются высокие шансы (50-75%) достичь полного лечебного патоморфоза первичной опухоли и л/у (pCR), как суррогат элиминации микрометастазов. При этом понятно, что дистанция между микрометастазами, которые мы еще не видим, и мелкими видимыми метастазами, которые начинаем видеть, очень эфемерная. Соответственно, маленькие, подозрительные или слегка видимые метастазы будут также уничтожены эффективным системным лечением. Лучше для больной и для врачей не знать об их наличии и не сомневаться в необходимости использования эффективной программы для IIB-III стадии. Если мы по какой-то причине решим, что выявленные изменения по КТ или ПЭТ-КТ являются отдаленными метастазами (неважно, так это на самом деле или нет), то терапия будет деэскалирована, хирургический компонент может быть отменен, лучевая терапия отменена, таргетная терапия будет проводиться до прогрессирования или токсичности (а она практически нетоксична) и лечение с паллиативным настроем будет проводиться бесконечно (или очень долго). Причем никто не знает, как долго ее проводить!
Но у больных преклонного возраста с выраженной сопутствующей патологией имеет смысл уточнить стадию процесса, так как данная категория больных с трудом может перенести всю программу радикального лечения, и риск осложнений может превышать потенциальную пользу. В этом случае ПЭТ-КТ может помочь избежать ненужной агрессии, если мы сразу поймем, что имеем дело с IV стадией болезни, и далее безопасно, но при этом достаточно эффективно, длительно лечить пациентку с помощью лекарственной терапии. Но если с помощью ПЭТ-КТ (или КТ) подтвердилась III стадия, то тогда у врачей имеется четкое обоснование для радикального подхода к лечению больной.
Если у пациентки агрессивный вариант трижды-негативного рака. Базальный подтип
Еще одна, самая многочисленная группа – гормонопозитивный, Her2 негативный вариант. Очень гетерогенная группа.
Пациентки с ранними формами, их много, не нуждаются в углубленном дообследовании. Шансы найти отдаленные метастазы и повысить стадию малы. У больных с местнораспространенным раком шансы найти отдаленные метастазы довольно большие – примерно 20-25%. У молодых и/или у пациентов без существенной сопутствующей патологии нет смысла усугублять стадию с помощью ПЭТ-КТ. Это лишает пациенток радикального подхода к лечению. Конечно, у значительной доли больных с течением времени реализуются отдаленные метастазы. Но это может быть через 3-5-10 лет. Зачем об этом знать с самого начала? Это вопрос спорный. С одной стороны, ранняя информация о наличии бессимптомной метастатической болезни не увеличивает продолжительность жизни (сегодня пока так), просто пациентка живет с информацией о неизлечимости болезни и о том, что лечение (гормонотерапия, химиотерапия и т.д.) будут проводиться всю оставшуюся жизнь, а это многие-многие годы. С другой стороны, если у пациентки изначально 4 стадия, то 1 год жизни (неоадъювантная химиотерапия, операция, лучевое лечение) она потратит на агрессивное лечение, которое не приведет к увеличению общей выживаемости, при этом снизит качество жизни (удаление молочной железы, полгода токсичной химиотерапии, лучевое лечение). Не все пациентки этого бы хотели, и эти обсуждения, безусловно, должны приниматься совместно с пациенткой и, в том числе, в зависимости от ее настроя. Надо объяснить, что мы ждем от ПЭТ-КТ и какие изменения тактики могут быть.
Опять стоит задуматься о больных преклонного возраста и/или с сопутствующей патологией. В этом случае конверсия стадии из III в IV позволяет избежать избыточного химиотерапевтического и локального лечения, которое входит в программу лечения местнораспространенных стадий. В этом случае мы основной упор делаем на гормонотерапию +/- ингибиторы CDK 4/6. И лечение может быть очень эффективным. Долгие годы метастатический процесс контролируется с помощью минимально токсичного лечения. В этой группе знание – сила.
Также стоит отметить, что такие спорные обсуждения и индивидуальные решения не могут быть масштабированы или применяться рутинно вне экспертных центров.
Теперь о метастатическом раке молочной железы. Надо ли делать ПЭТ-КТ и отслеживать эффективность по ПЭТ-КТ? Возникает вопрос: а что такого может дополнительно дать ПЭТ-КТ в сравнении с КТ с контрастом? КТ хорош тем (сейчас практически все КТ мультиспиральные), что воспроизводим, не очень дорог, видит очевидную патологию, удобен для динамического контроля, много аппаратов. Может ли информация о каком-либо дополнительным очаге или группе очагов, которые пропущены на КТ трех зон, поменять тактику лечения? Мой ответ – в небольшом проценте случаев может, так как ПЭТ-КТ делается всего тела (а не только 3-х зон). На ПЭТ-КТ видна голова, проксимальная часть рук и ноги: можно увидеть там какие-либо изменения. Например, увидеть подозрительный бессимптомный очаг в головном мозге, врач направит на МРТ, и если окажется метастаз, то будет проведен гамма-нож (например). Но много ли таких случаев в рутинной клинической практике? Мой опыт говорит, что не более 3-5%, это я сужу по своим ощущениям. Статистику не делал. Может быть, раз в месяц или два вижу подобные находки благодаря ПЭТ-КТ, которые меняют мой подход к выбору лечения. Может ли накопление радиофармпрепарата (SUV) диктовать мне необходимость каких-либо действий, если нет явного очага? КТ тем и хорош, что видит явный очаг (плюс ткань), пропускает клинически незначимые малые очаги (которые практически всегда бессимптомные). Врачу-клиницисту не нужна избыточная и бессмысленная информация, это мешает, создает информационный шум, мешает увидеть главное. Те врачи-клиницисты, кто регулярно смотрит КТ и ПЭТ-КТ, все время видят, что нет совершенного метода, который может со 100% вероятностью отличить онкопатологию от воспаления или неспецифики.
Терапия метастатического рака молочной железы требует видения проблемы болезни и пациентки в целом, и очень редко детализации. На продолжительность и качество жизни практически не влияет, на 1-2 мм больше метастаз или меньше, стал ли немного больше SUV или чуть уменьшился. Для оценки эффективности химиотерапии метастатического рака молочной железы отлично подходит КТ с контрастом. ПЭТ-КТ с контрастом может быть на старте (обезопасить себя, что не прозевали метастаз в мозг или диафиз бедренной кости, например), а затем отслеживать динамику стоит на основании КТ трех зон с в/в контрастом. Некоторые формы метастатического рака молочной железы, например, дольковый рак, вообще плохо видны на ПЭТ-КТ с точки зрения SUV. На фоне гормонотерапии изменения в костных метастазах происходят небыстро, и может быть симптом вспышки (как при сканировании костей), когда на фоне эффективной гормонотерапии сначала SUV может вырасти. При этом структура метастазов начинает меняться в сторону склерозирования, что отражает положительную динамику на фоне лечения (я очень много видел формальных заключений ПЭТ-КТ о прогрессировании на основании роста SUV, тогда как по КТ части исследования и клинически была явная положительная динамика, и вынужден брать на себя ответственность, успокаивать пациентку и продолжать лечение без изменений). Проведение ПЭТ-КТ исследования может быть оправданно, если у больной мы видим олигометастатическую болезнь и задумали какое-то локальное лечение (например, удалить единственный метастаз), тут ПЭТ-КТ очевидный помощник в принятии решения.
В целом, при метастатическом раке молочной железы ПЭТ-КТ практически не имеет преимуществ в сравнении с качественным КТ. Может быть, оправдан на старте терапии. Но не в оценке динамики. Лишь в отдельных случаях, на усмотрение клинициста, ПЭТ-КТ может дать дополнительную ценную информацию.
Категорически нет. Также как и КТ, МРТ, УЗИ, маркеры, анализы крови и т.д. Раннее выявление бессимптомных метастазов не приводит к увеличению продолжительности жизни. Это не то же самое, что рано выявить первичную опухоль. Это – рано выявить фактически IV и неизлечимую стадию. При отсутствии симптоматики не нужно искать метастазы – это несет вред в большинстве случаев. Иногда, правда, можно случайно выявить другую опухоль ранней стадии (например, рак толстой кишки) и тогда вовремя прооперируют, но это все как случайный выстрел, который попал в десятку (в жизни все бывает). Не стоит заниматься скринингом с помощью ПЭТ-КТ. А что делать? Только маммографию неудаленной железы или обеих, если была органосохранная операция. Почему? Потому что у больных, перенесших рак молочной железы, повышается риск повторного первичного рака молочной железы. И лучше его выявить раньше. Повторная радикальная терапия локальной стадии имеет практически такой же шанс на успех, как и предыдущая.
У ПЭТ-КТ есть ограниченная роль в лечении рака молочной железы. Назначение ПЭТ-КТ должно быть инициировано врачом-клиницистом, который реально разбирается во всех тонкостях болезни и понимает, для чего ему будет нужна потенциально новая информация. Ни в коем случае нельзя делать ПЭТ-КТ по требованию пациентки или ее родственников (сегодня медицина зачастую работает по принципу: чего изволите-с). ПЭТ-КТ не должно быть заменой КТ только потому, что проще направить и быстрее сделают, так как на КТ очередь, а ПЭТ-КТ оплачивает ОМС.
Читайте также:

