Печеночно клеточный рак гистология
Печеночно-клеточный рак печени (гепатоцеллюлярная карцинома) – самая распространённая первичная онкоопухоль секреторного органа. Этот диагноз ставится примерно в 85% клинических случаев поражения печени. Заболевание может развиваться у людей любой возрастной категории, но у детей встречается сравнительно редко.
Злокачественный процесс, провоцирующий развитие онкоопухоли такого типа, начинается вследствие трансформации гепатоцитов (клеток печёночной паренхимы). Аномальные нарушения в клеточном строении в достаточно короткие сроки приводят к озлокачествлению эпителиальные ткани секреторного органа.
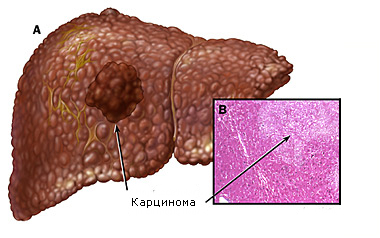
Печеночно-клеточный рак печени, называемый иначе гепатоцеллюлярный рак или гепатома, имеет несколько отличительных особенностей:
У этой разновидности злокачественных новообразований имеется один подтип – фиброламеллярная карцинома. Печеночно-клеточный рак печени, развивающийся по фиброламеллярному типу, поражает людей молодого возраста, не имеющих патологических изменений печёночной паренхимы. У этой разновидности патологического процесса более благоприятные прогнозы, так как онкоопухоль не склонна к повышенной агрессии и хорошо реагирует на проводимые терапевтические мероприятия.
Классификация онкоопухоли
Чтобы правильно поставить диагноз и подобрать наиболее адекватный протокол лечения, в онкологии принято классифицировать злокачественные новообразования.
Печеночно-клеточный рак печени по макроскопическим признакам подразделяется специалистами на несколько форм:
- Узловая. В паренхиме секреторного органа, одной или обеих его долях, локализовано несколько некрупных, имеющих практически одинаковые размеры, узелков. Центральная их часть всегда подвержена некрозу.
- Массивная. Такая опухоль в печени выглядит как один крупный узел, зачастую гигантских, размеров, имеющий в непосредственной близости несколько проросших из него дочерних узелков.
- Диффузная. Эта форма рака печени встречается сравнительно редко и представляет собой слившиеся в единый конгломерат узлы, занимающие по площади всю печёночную паренхиму.
Гистологическая классификация заключается в подразделении аномальных новообразований на трабекулярный, скиррозный, компактный и псевдожелезистый типы. Каждый из них имеет специфическое клеточное строение и требует своего подхода к выбору терапевтического воздействия.
Важно! Когда у пациента выявляется печеночно-клеточный рак печени, лечение может быть назначено только после определения её типа. Единого подхода к терапии всех видов рака не существует – в каждом конкретном случае необходим индивидуальный подход, имеющий непосредственную связь с характером и степенью агрессии первичной онкоопухоли.
Причины возникновения печеночно-клеточного рака печени
Этиология появления в крупнейшей пищеварительной железе генной мутации клеток, провоцирующей начало процесса малигнизации, до сих пор остаётся до конца невыясненной. Но учёные давно обнаружили несколько негативных факторов, способных спровоцировать печеночно-клеточный рак.
Исходя из результатов их исследований, гепатологи ориентируют своих пациентов на следующие причины печеночно-клеточной карциномы:
- Наличие в анамнезе человека острых и хронических форм гепатитов В и С. Риск развития возрастает не только при активных формах этой болезни, но и в тех случаях, когда человек является носителем вируса.
- Цирроз любой этиологии. Патологическое состояние сопровождается замещением нормальных печёночных клеток на соединительную ткань, что приводит к началу их мутации.
- Употребление пищи, содержащей афлотоксины, ядовитые вещества, появляющиеся в некоторых продуктах питания из-за неправильного их хранения.
- Наследственный фактор. Печеночно-клеточный рак печени чаще всего поражает тех людей, кровные родственники которых имели в анамнезе онкологические заболевания.
Важно! Онкологи предупреждают, что атипичные клетки, склонные к активной злокачественной трансформации, могут появиться в печёночных тканях вследствие ведения человеком неправильного образа жизни. Значительное влияние на изменение клеточной структуры оказывают длительное курение, злоупотребление спиртными напитками, нарушения пищевого рациона с преобладанием в нём канцерогенов (жареная и жирная пища, фаст-фуд), частые стрессы и бесконтрольный приём многих лекарственных средств.
Печеночно-клеточный рак печени: симптомы и проявление
Клиническая картина при печеночно-клеточном раке имеет прямую зависимость от места локализации и размеров опухолей, а также наличия или отсутствия в печёночной паренхиме цирротических повреждений. Если новообразование имеет небольшие размеры, специфическая симптоматика практически полностью отсутствует, а обнаружение его бывает случайной находкой при прохождении ультразвукового исследования по другому поводу. Только после того, как онкоопухоль начнёт разрастаться, у человека появляются некоторые тревожные признаки, на которые необходимо обратить внимание и срочно обратиться за консультацией к гепатологу.
Специалисты выделяют следующие симптомы печеночно-клеточнго рака печени:
- диспепсические расстройства (постоянное подташнивание, частая рвота, диарея);
- повышенная утомляемость, снижение работоспособности и постоянная усталость;
- появление в подреберье немотивированных болезненных ощущений;
- потеря аппетита и резкое снижение веса.
Стоит знать! Если проигнорировать появление вышеперечисленных симптомов и не начать лечить рак печени, заболевание начинает активно прогрессировать и в короткие сроки переходит в запущенную неоперабельную стадию, сопровождающуюся обширным метастазированием. В этом случае у онкобольного появляется выраженная желтушность кожных покровов, спровоцированная сдавливанием желчных протоков, а также боли в костях и грудной клетке, вызываемые активным разрастанием вторичных аномальных очагов.
Стадии злокачественного процесса
Начинается развитие злокачественного процесса с так называемого предракового состояния, при котором в гепатоцитах только появляются зачатки патологических изменений. Предрак не имеет никакой симптоматики и если не будет выявлен случайно, через короткое время в клеточных структурах печёночной паренхимы начнётся процесс активной малигнизации. Специалистами отмечается 3 излечимых стадии печеночно — клеточного рака печени.
Недуг, обнаруженный на одном из этих этапов, в большей или меньшей степени поддаётся излечению, а у пациента появляются шансы на значительное продление жизни с сохранением её качества:
- Печеночно-клеточный рак печени на 1 стадии — чаще всего это одиночная опухоль, которая имеет сравнительно небольшие размеры – её диаметр не превышает 2 см. Она не сдавливает окружающие ткани, поэтому человек не ощущает какого-либо дискомфорта и болезненности. Также отсутствуют прорастания в сосудистые стенки и лимфатические узлы. Прогнозы излечения такого новообразования самые благоприятные – при проведении адекватной терапии у многих пациентов имеются шансы не просто достигнуть длительной ремиссии, а полностью забыть про опасную болезнь.
- Печеночно-клеточный рак печени на 2 стадии характеризуется появлением множественных очагов, достигающих в диаметре 5 см, и вовлечением в патологический процесс сосудистых стенок. Онкобольной начинает ощущать негативную симптоматику, которая с каждым днём усиливается. На этом этапе всё ещё возможно полное излечение, хотя в клинической практике оно отмечается редко.
- На 3 стадии печеночный рак печени проходит через 3 подстадии – A, B, и C. Они имеют небольшие различия, заключающиеся в степени метастатического процесса. На подстадии A происходит разрушение аномальными клетками стенок кровеносных сосудов, но они ещё не попадают в кровоток и не разносятся по организму, B — опухолевая структура прорастает в брюшную полость и поражает находящиеся в непосредственной близости органы, C — появляются метастазы в регионарных лимфоузлах.
- Если онкопроцесс не обнаружен на этих этапах развития, он переходит в заключительную, не поддающуюся излечению 4 стадию. Симптомы печеночно-клеточного рака печени становятся очень мучительными, поэтому для улучшения качества жизни последних месяцев или недель пациентам проводят курсы паллиативной терапии.
Диагностика печеночно-клеточного рака печени
Успех терапии зависит от того, насколько своевременно было обнаружено заболевание и как правильно поставлен окончательный диагноз. Первые признаки, которыми сопровождается практически любая онкология печени, опытный гепатоонколог может определить уже на первичном осмотре при проведении пальпации. Заподозрить печеночно-клеточный рак позволяет наличие прощупываемых в области секреторного органа неспецифических для него уплотнений и наличие на сильно увеличенном животе явно выраженных кровеносных сосудов.
Если у человека помимо тревожной симптоматики присутствуют и эти признаки, ему сразу же назначается специфическая диагностика, состоящая из ряда исследований:
- Лабораторные анализы. У пациента берут кровь на онкомаркеры, а также проводят биохимическое её исследование. Наличие в биологической жидкости специфического белка, являющегося продуктом жизнедеятельности аномальных клеток печёночной паренхимы, подтверждает, что в ней начала развиваться онкология.
- Аппаратные визуальные исследования. ПЭТ, МРТ, КТ и УЗИ позволяют оценить размеры онкоопухоли, и определить степень её распространения. Кроме этого с помощью данных диагностических методик достаточно хорошо обнаруживаются вторичные злокачественные очаги.
- Гистология. Изучение под микроскопом биопсийного материала (тончайшего среза с подозрительного участка печёночной паренхимы) окончательно подтверждает предполагаемый диагноз.
Дополнительные диагностические методики применяются для уточнения степени метастазирования. С этой целью используют рентгенографию грудной клетки, выявляющую метастазы в лёгких, сцинтиграфию, обнаруживающую костные поражения и контрастную ангиографию, изучающую сосудистую сетку на предмет вторичных злокачественных очагов.
Лечение печеночно-клеточного рака печени
Терапевтические мероприятия, направленные на разрушение печеночно-клеточного рака, должны быть только комплексными. Применение какого-либо одного метода терапии при этом заболевании не даёт положительных результатов, так как не позволяет полностью уничтожить аномальные клетки секреторного органа. Основное лечение печеночно — клеточной карциномы печени заключается в применении хирургического вмешательства. Оно считается предпочтительнее противоопухолевой медикаментозной терапии, так как позволяет кардинально решить проблему онкоопухоли. Операционное лечение проводится одним из двух способов – частичная резекция пораженного опухолевой структурой участка печёночной паренхимы или трансплантация органа.
Одновременно с операцией пациентам назначаются следующие виды терапии:
- Химиотерапия. При локализации злокачественных новообразований в секреторном органе применяется прямой (внутриартериальный) способ введения лекарственных препаратов. Преимуществом его является воздействие ядовитых средств непосредственно на аномальные клеточные структуры без повреждения здоровых. Это позволяет избежать большого количества побочных эффектов, сопровождающих системную (пероральную и внутривенную) химию.
- Лучевая терапия. Проведение её до последнего времени считалось неперспективным и даже опасным из-за высокой чувствительности здоровых гепатоцитов к облучению, но с появлением новейших методик ионизирующее излучение стало всё чаще применяться в гепатоонкологической практике.
На последних стадиях болезни, когда онкоопухоль переходит в категорию неоперабельных, специалисты используют исключительно паллиативное лечение. Оно имеет одну цель – купировать мучительные симптомы печеночно — клеточного рака печени и улучшить качество жизни пациента.
Метастазы и рецидив
В случае, когда лечение печеночно-клеточного рака печени началось несвоевременно или было недостаточным, у значительной части онкобольных развивается обширный метастатический процесс. В связи с тем, что опухоль печени метастазирует преимущественно гематогенным путём, вторичные поражения обнаруживаются в самых отдалённых участках организма. Чаще всего метастазы из печёночной паренхимы проникают в лёгкие, позвоночник и рёбра. В некоторых случаях их выявляют и в головном мозге. Из-за склонности первичной онкоопухоли секреторного органа к раннему метастазированию повышаются риски развития рецидива опасного заболевания, и уменьшаются шансы на благоприятный терапевтический прогноз.
Сколько живут пациенты с печеночно-клеточным раком в печени?
Прогнозы печеночно-клеточного рака по большей части считаются неутешительными, так как его очень сложно выявить на начальных стадиях, когда онкоопухоль достаточно хорошо реагирует на терапевтические мероприятия. Чаще всего у пациентов диагностируется низкодифференцированная g3 гепатоцеллюлярная карцинома, при которой любые терапевтические мероприятия, направленные на выздоровление человека, становятся бесперспективными. Именно на этой стадии развития развивается обширный метастатический процесс, который затрагивает самые отдалённые участки организма.
В онкологической статистике имеются следующие прогностические данные по пятилетней выживаемости недуга:
Стоит знать! Опаснее всего печеночно-клеточный рак печени на 4 стадии. Прогноз при выявлении болезни на этом этапе самый плохой – у пациентов остаётся несколько недель или месяцев жизни, причём на всём их продолжении обязательно проведение паллиативных курсов химии и облучения. Только при таком терапевтическом подходе возможно устранение мучительной симптоматики и поддержание более-менее нормального качества жизни.
СМОТРЕТЬ ДРУГИЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
Год утверждения 2018
Профессиональные ассоциации:
- Ассоциация онкологов России
- Российское общество клинических онкологов
Оглавление
1. Общая информация
Печеночно–клеточный рак (гепатоцеллюлярная карцинома – ГЦК, или гепатоцеллюлярный рак – ГЦР) – злокачественная опухоль, исходящая из гепатоцита.
- холангиокарциномы (ХК, или холангиоцеллюлярный рак, ХЦР) - злокачественная опухоль из эпителия внутрипеченочных желчных протоков;
- смешанные гепатохолангиокарциномы;
- фиброламеллярная карцинома (ФЛК) формально классифицируется как вариант ГЦК.
- хроническое воспаление (вирусные гепатиты В и С, алкогольный и первичный билиарный и криптогенный цирроз),
- неалкогольный стеатогепатит,
- аутоиммунный гепатит,
- экзогенные токсические повреждения печени (афлотоксины, винилхлорид, стероиды),
- наследственные заболевания (дефицит альфа 1-антитрипсина, тирозинемия и гемохроматоз),
- нарушения иммунной системы с исходом в хронический гепатит и цирроз.
Менее 10% ГЦР развивается на фоне здоровой ткани печени.
В 2014 году в России:
- 7 252 ГЦР и рака внутрипеченочных желчных протоков,
- 9 268 больных умерло.
С22 Злокачественное новообразование печени и внутрипеченочных желчных протоков
С22.0 Печеночно-клеточный рак. Гепатоцеллюлярный рак. Гепатома.
С22.1 Рак внутрипеченочного желчного протока. Холангиокарцинома.
С22.3 Ангиосаркома печени
С22.4 Другие саркомы печени
С22.7 Другие уточненные раки печени
С22.9 Злокачественное образование печени неуточненное
Эпителиальные гепатоцеллюлярные доброкачественные опухоли:
- Гепатоцеллюлярная аденома 8170/0;
- Фокальная нодулярная гиперплазия 8170/0
Предраковые или ассоциированные со злокачественными новообразования
- Крупноклеточные изменения
- Мелкоклеточные изменения
- Диспластические узлы
- Низкой степени злокачественности
- Высокой степени злокачественности
Злокачественные гепатоцеллюлярные опухоли:
- гепатоцеллюлярный рак 8170/3;
- гепатоцеллюлярный рак (фиброламеллярный вариант) 8171/3
- гепатобластома, эпителиальные варианты 8171/3;
- недифференцированный рак 8020/3.
Мезенхимальные опухоли:
- Ангиомиолипома (PECома) 8860/0 гемангиома;
- Кавернозная гемангиома 9131/0
- Инфантильная гемангиома 9131/0
- Воспалительная псевдоопухоль
- Лимфангиома 9170/0
- Мезенхмальная гамартома
- Солитарная фиброзная опухоль 8815/0
Злокачественные опухоли
- Ангиосаркома 9120/3
- Эмбриональная саркома 8991/3
- Эпителиоидная гемангиоэндотелиома 9133/3
- Саркома Капоши 9140/3
- Лейомиосаркома 8890/3
- Рабдомиосаркома 8900/3
- Синовильная саркома 9040/3
Смешанные злокачественные опухоли неясного происхождения
- смешанный гепатохолангиоцеллюлярный рак 8180/3;
- карциносаркома 8980/3
Герминогенные опухоли
Лимфомы
Метастатические опухоли.
Барселонская система учитывает:
- распространенность опухолевого процесса,
- функциональное состояния печени,
- объективное состояния больного,
- предполагаемую эффективность лечения.
Стадия BCLC, прогноз и тактика лечения изменяются при прогрессировании заболевания
2. Диагностика печеночно–клеточного рака
Выявление факторов, которые могут повлиять на выбор тактики лечения.
У большинства развитие ГЦР связано с фоновой патологией печени:
- вирусные гепатиты,
- цирроз печени любой этиологии,
- неалкогольный стеатогепатит,
- аутоиммунный гепатит,
- токсический гепатит,
- наследственные заболевания.
Стандартный физикальный осмотр.
Оценка нутритивного статуса.
- Развернутый клинический анализ крови.
- Развернутый БАК (+альбумин).
- Онкомаркер альфа-фетопротеин (АФП).
- Исследование свёртывающей системы крови.
- Общий анализ мочи.
При сопутствующем хроническом вирусном гепатите:
антитела к HBsAg и HCV;
при HBsAg+:
- HBeAg,
- HBeAb,
- количественное ДНК HBV.
При подозрении на острый вирусный гепатит необходим анализ на HBcAb IgG.
Оценка функционального статуса печени по критериям Child-Pugh (СР):
- 5–6 баллов - цирроз класса А
- 7–9 баллов – цирроз класса В
- 10–15 баллов - цирроз класса C
УЗИ органов брюшной полости и забрюшинного пространства:
- на этапе скрининга,
- для чрескожной биопсии и интервенционных вмешательств,
- иногда мониторинг эффективности лечения,
- чувствительность невысока для обнаружения узлов малого размера.
4-фазная КТ (нативная, артериальная, венозная и отсроченная венозная фазы) и/или динамическая МРТ органов брюшной полости с в/в контрастированием.
Обоснованный диагноз ГЦР без морфологической верификации - в цирротически измененной печени независимо КТ и МРТ выявляют типичную васкуляризацию в опухоли.
МРТ с гепатотропным контрастом для дифференциальной диагностики ГЦР от другой опухоли.
МРТ органов брюшной полости с гадоксетовой кислотой:
- первично выявленные новообразования печени неустановленной природы (для уточнения характера и количества);
- цирроз печени – для оценки состояния паренхимы и дифференциальной диагностики регенераторных узлов и ГЦР;
- при первичном или метастатическом ГЦР на фоне цирроза – оценка эффективности химио- и локо-регионарной терапии;
- при гепатоцеллюлярных аденомах – динамическая оценка выявленных опухолевых узлов.
Рентгенография грудной клетки либо КТ.
ЭГДС для выявления степени выраженности варикозного расширения вен пищевода.
ЭКГ.
Остеосцинтиграфия при подозрении на метастатическое поражение костей скелета.
Биопсия под контролем УЗИ/КТ при подозрении на метастазы по КТ или МРТ, когда подтверждение принципиально меняет тактику лечения.
КТ-ангиография печени для определения возможности:
- трансартериальной эмболизации,
- объема и характера планируемого интервенционного вмешательства.
ПЭТ-КТ с холином при подозрении на отдаленные метастазы по КТ или МРТ, если подтверждение принципиально меняет тактику лечения.
МРТ или КТ головного мозга с в/в контрастированием при подозрении на метастазы.
Дополнительное обследование при подготовке к хирургическому лечению:
- ЭХОКГ,
- холтеровское мониторирование,
- исследование ФВД,
- УЗДГ сосудов шеи и нижних конечностей,
- консультации специалистов по показаниям.
Пункционная биопсия (кор-биопсия) опухоли печени:
- при малом размере опухоли (
- нетипичная васкуляризация узла >2 см;
- расхождения контрастных динамических исследований при норме или незначительном повышении АФП;
- выявление любого опухолевого образования в нецирротической печени.
Не требуется биопсия образования в цирротической печени:
1. не планируется лечения из-за декомпенсированного цирроза и/или другой тяжелой патологии;
2. планируется резекция печени;
3. при циррозе мультифазная на КТ и МРТ c контрастом специфичные для ГЦР признаки.
Отрицательный результат биопсии не снимает диагноза злокачественной опухоли печени и предполагает дальнейшее наблюдение.
3. Лечение печеночно–клеточного рака
Хирургическое вмешательство - основной метод радикального лечения при учёте:
- наличия и степени цирроза,
- распространенности опухолевого процесса,
- функциональных резервов печени,
- объективного состояния больного,
- прогноза основного и фонового заболевания печени.
Ранний ГЦР
Резекция печени с учетом функциональной состоятельности остающейся части печени - при очень ранней стадии ГЦР (BCLC 0):
- без сопутствующего цирроза;
- с компенсированным циррозом (при сохранной функции, нормальном билирубине, без портальной гипертензии).
Для резекции размер опухоли и множественное внутриорганное поражение не абсолютное противопоказание.
Ортотопическая трансплантация печени при раннем ГЦР:
- при невозможности резекции из-за билобарного поражения;
- при декомпенсированном циррозе СР В/С, BCLCА.
- размер единственной опухоли не более 5 см
- или до 3-х очагов с диаметром наибольшего узла до 3 см и отсутствием инвазии в сосуды.
- неоадъювантная ХТ,
- РЧА,
- трансартериальная (химио)эмболизация,
- резекция печени,
- химиотерапия сорафенибом.
- увеличение вероятности выполнения трансплантации печени,
- селекция и исключение агрессивных случаев ГЦР.
При раннем ГЦР (BCLC A) и противопоказаниях к трансплантации применение методов локальной деструкции опухоли.
Показания для РЧА:
- неоперабельный ГЦР;
- в сочетании с резекцией печени;
- в период ожидания трансплантации;
- при рецидиве после резекции печени;
- солитарный или единичные опухолевые узлы до 3 см в диаметре.
Противопоказания для РЧА:
- множественное поражение печени,
- большие размеры опухоли >3 см в диаметре,
- декомпенсированный цирроз (Child-Pugh C),
- внепеченочные проявления заболевания,
- портальный шунт,
- не смещаемое прилежание опухолевого узла к органам и крупным желчным протокам.
Стереотаксическая лучевая терапия при раннем ГЦР (BCLC A) и противопоказаниях к трансплантации:
- при единичных (№1-3) опухолевых узлах в печени.
Промежуточная стадия ГЦР
При BCLC трансартериальная химиоэмболизация (ТАХЭ) в качестве первой линии:
- при нерезектабельном/неоперабельном процессе без инвазии/тромбоза магистральных печеночных сосудов и без внепеченочных проявлений заболевания,
- в период ожидания трансплантации в комбинации с другими методами локального и системного воздействия.
Повторные сеансы ТАХЭ:
1. при объективном и стойком (>6 мес.) эффекте первичной ТАХЭ
2. в отсутствие внепеченочных метастазов
3. при сохранной функции печени.
- отсутствие объективного эффекта по критериям mRECIST;
- появление новых опухолевых очагов в зоне ТАХЭ после технически эффективной 1-2 кратной эмболизации.
При неэффективности ТАХЭ возможна системная терапия.
Противопоказания к системной терапии:
- декомпенсированный цирроз (CP C),
- тромбоз магистральных ветвей или ствола воротной вены,
- ЖК-кровотечение,
- портальный шунт,
- внепеченочное распространение заболевания,
- не купируемый асцит,
- тяжелые нарушения свертывающей системы крови.
При не подходящих под другие варианты лечения ранней и промежуточной стадии ГЦР (BCLC А/В) - конформная 3D ДГТ с СОД на опухоль 30–60 Гр:
- без цирроза,
- без опухолевой инвазии в нижнюю полую вену, портальную вену и ее ветви.
После радикального хирургического лечения адъювантная терапия не рекомендуется, так как не снижает риск рецидива и не продлевает жизни.
Системная лекарственная терапия:
- при локализованном ГЦР (BCLC A/B) bridge-терапия в сочетании с методами локального воздействия;
- при распространенном ГЦР (BCLC C) с внепеченочными метастазами,
- прогрессирование процесса в печени после локальных методов лечения.
В первую очередь рассматривается возможность лечения в рамках клинических исследований.
При суб- и декомпенсированном циррозе (класс Child-Pugh В или С) цитотоксическое лечение, как правило, не проводится.
При распространенном ГЦР (BCLC C) в первой линии сорафениб, достоверно увеличивающий продолжительность жизни больных ГЦР.
- нет предикторов эффективности;
- начальная доза 800 мг/сутки;
- при циррозе СР В и для ослабленных – 400 мг/сутки с эскалацией до 800 мг/сутки при удовлетворительной переносимости;
- при выраженной (≥ 2 степени) токсичности возможно снижение до 600/400/200 мг в сутки, возможен временный перерыв в приеме препарата;
- при токсичности 3–4 степени перерыв в приеме на 1 неделю и активная симптоматическая терапия, с возобновлением приема в редуцированной дозе и на фоне симптоматической терапии при уменьшении токсичности
- отмена терапии при непереносимой токсичности на 200 мг через день;
- начальная доза 400 мг/сутки при прогрессирующем после трансплантации ГЦР на фоне иммуносупрессивной терапии вследствие более выраженной токсичности, с последующей ступенчатой эскалацией до 800 мг/сутки при хорошей переносимости;
- опухолевый тромбоз магистральных сосудов не противопоказание для приема.
Полихимиотерапия при неэффективности/непереносимости сорафениба при распространенном ГЦР (BCLC C) без цирроза:
- эффективность менее 20%;
- не увеличивает продолжительности жизни;
- только регорафениб достоверно увеличивает выживаемость.
Вторая линия возможна у больных в удовлетворительном состоянии и при компенсированной функции печени.
Монохимиотерапия:
- Сорафениб 400 мг х 2 р/сутки длительно.
- Доксорубицин 75 мг/м2 в 1-й день. Интервал – 3 недели.
- Гемцитабин 1000 мг/м2 в 1,8,15-й дни. Интервал – 4 недели.
- Регорафениб 160 мг/сут 1-21 день. Интервал – 4 недели.
- Гемцитабин 1000 мг/м2 + Цисплатин 25-30 мг/м2, 1 и 8 дни, интервал 3 недели
- Гемцитабин 1000 мг/м2 + Оксалиплатин 85 мг/м2, 1 и 15 дни, интервал 2 недели
- FOLFOX4 (Оксалиплатин 85 мг/м2 2-часовая инфузия в 1 день + ЛВ 200 мг/м2 в/в 2-часовая инфузия в 1 и 2 дни + 5-ФУ 400 мг/м2 в/в струйно в 1 и 2 дни + 22-часовая инфузия 5-ФУ 600 мг/м2 в 1 и 2 дни). Интервал 2 недели.
- XELOX (Оксалиплатин 130 мг/м2 в 1 день + капецитабин 2000 мг/м2 в сутки 1-14 дни) Интервал 3 недели.
- по критериям RECIST 1.1 и/или mRECIST (при циррозе);
- КТ и/или МРТ с контрастным усилением каждые 2–3 месяца;
- АФП в динамике при исходно высоком показателе (самостоятельного значения не имеет).
При ГЦР с хроническим вирусным гепатитом В проводится терапия аналогами нуклеозидов (например, энтекавир 0,5 или 1 мг/сут) вне зависимости от выраженности цитолитического синдрома и количества копий вируса все время ХТ.
Хронический гепатит С:
- чаще всего не влияет на возможность проведения ПХТ;
- не проводится специфическая противовирусная терапия интерфероновыми режимами;
- неизвестно влияние безинтерфероновых режимов на течение ГЦР.
При локальном и/или системном лечении ГЦР на фоне цирроза на всем протяжении лечения проводится подробное обследование для уточнения выраженности цирроза.
При варикозном расширении вен пищевода/желудка II–III степени:
- первичная профилактика кровотечения неселективными β-адреноблокаторами;
- лигирование варикозно-расширенных вен при неэффективности медикаментозного лечения, угрозе кровотечения и для вторичной профилактики рецидивного кровотечения.
При снижении уровня альбумина плазмы
Для коррекции цирротического асцита - адекватная диуретическая терапия (верошпирон до 400 мг/д, фуросемид) под контролем электролитов крови.
При терминальной стадии ГЦР и цирроза печени (Child-Pugh С, BCLC D) проводится симптоматическая терапия и коррекция осложнений цирроза печени, болевого синдрома
4. Реабилитация печеночно–клеточного рака
По общим принципам реабилитации после хирургических вмешательств, трансартериальной химиоэмболизации и/или химиотерапии.
5. Профилактика и диспансерное наблюдение при печеночно–клеточном раке
Наблюдение после радикального лечения физикальный осмотр и сбор жалоб:
- каждые 3-6 месяца 2 года,
- 1 раз в 6-12 месяцев с 3-го года.
1. Анамнез и физикальное обследование;
2. АФП при исходном повышении каждые 3-6 месяцев 2 года, далее каждые 6-12 мес.
3. УЗИ органов брюшной полости каждые 3-6 мес.
4. КТ или МРТ органов брюшной полости с в/в контрастированием каждые 3-6 мес.
5. Рентгенография органов грудной клетки каждые 12 мес.
При противоопухолевом лечении обследование каждые 2 - 3 месяцев:
1. Анамнез и физикальное обследование;
2. Развернутый клинический анализ крови с формулой и тромбоцитами;
3. БАК: мочевина, креатинин, альбумин, глюкоза, АСТ, АЛТ, щелочная фосфатаза;
4. Коагулограмма (МНО);
5. АФП каждые 3-4 мес.;
6. УЗИ органов брюшной полости каждые 2-3 мес.;
7. ЭГДС каждые 6 мес.;
8. Мультифазная КТ и/или МРТ органов брюшной полости с в/в контрастированием каждые 3-4 мес.;
9. Рентгенография органов грудной клетки каждые 6 мес.
10. Сцинтиграфия скелета – по показаниям.
Задача наблюдения - раннее выявление прогрессирования с целью:
- раннего хирургического лечения резектабельных метастазов,
- аблации и/или химиоэмболизации рецидивных опухолей,
- лекарственного противоопухолевого лечения.
Читайте также:

