Опухоли роль факторы химические и физические характера
Причинами развития опухолей являются различные факторы, способные вызвать превращение нормальной клетки в опухолевую. Они называются канцерогенными или бластомогеннами. Это агенты химической, физической и биологической природы, а главным условием, способствующим реализации их действия (фактором риска), является снижение эффективности механизмов противоопухолевой защиты организма. В значительной мере это определяется генетической предрасположенностью. Свойствами канцерогенных факторов, обеспечивающими опухолевую трансформацию клеток, являются мутагенность (способность прямо или косвенно влиять на геном клетки, что в итоге приводит к мутациям), способность к проникновению через внешние и внутренние барьеры и дозированность действия, которая обеспечивает незначительное повреждение клетки, что позволяет ей выжить.
Наряду с канцерогенными факторами, существует целый ряд веществ, которые не вызывая сами мутаций, являются обязательными участниками канцерогенеза - коканцерогены и синканцерогены. Коканцерогены - немутагенные факторы (промоторы), усиливающие эффект канцерогенных агентов. Коканцеогенез – усиление мутагенного действия канцерогена соединениями, которые стимулируют пролиферацию клеток, инактивируя белки-продукты антионкогенов или усиливая передачу ростостимулирующих сигналов. Синканцерогены – канцерогенные факторы, вызывающие усиленное образование опухолей при комбинированном действии нескольких известных концерогенов.
По данным ВОЗ, более 75% случаев злокачественных опухолей человека вызвано воздействием химических факторов внешней среды. Потенциально канцерогенные вещества сами по себе не вызывают опухолевого роста. Поэтому их называют проканцерогенами, или преканцерогенами. В организме они подвергаются физико-химическим превращениям, в результате которых становятся истинными, конечными канцерогенами. Конечными канцерогенами являются алкилирующие соединения, эпоксиды, диолэпоксиды, свободнорадикальные формы ряда веществ.
К возникновению опухолей приводят преимущественно факторы сгорания табака (примерно 40%); химические агенты, входящие в состав пищи (25—30%) и соединения, используемые в различных сферах производства (около 10%). Известно более 1500 химических соединений, обладающих канцерогенным эффектом. Из них не менее 20 определённо являются причиной опухолей у человека. Наиболее опасные канцерогены относятся к нескольким классам химических веществ (рис. 1).
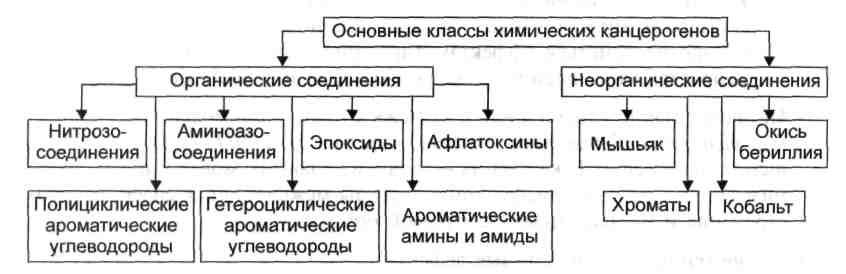
Рис. 1 Основные классы химических канцерогенов.
Органические химические канцерогены
• Полициклические ароматические углеводороды.
Наибольшей канцерогенной активностью среди них обладают 3,4-бензпирен, 20-метилхолантрен, диметилбензантрацен. Ежегодно в атмосферу промышленных городов выбрасываются сотни тонн этих и подобных им веществ.
• Гетероциклические ароматические углеводороды.
В эту группу входят дибензакридин, дибензкарбазол и другие соединения.
• Ароматические амины и амиды.
К ним относятся 2-нафтиламин, 2-аминофлюорен, бензидин и др.
• Нитрозосоединения. Наиболее опасные среди них — диэтилнитрозамин, ди-метилнитрозамин, нитрозометилмочевина.
Высокоэффективными канцерогенами среди них считаются 4-диметилами-ноазобензол и ортоаминоазотолуол.
• Афлатоксины — продукты метаболизма (производные кумаринов) плесневых грибов, в основном аспергилл Aspergillus flavus (отсюда название производимых ими веществ).
• Прочие органические вещества с канцерогенной активностью: эпоксиды, пластмассы, уретан, четырёххлористый углерод, хлорэтиламины и другие.
Поскольку лишь около 10% опухолей человека можно связать с наследственным фактором, соответственно более 90% опухолей либо возникают спонтанно, либо индуцированы какими-либо канцерогенными факторами. Разделяют физический, химический и вирусный канцерогенез.
Физический канцерогенез
Основными физическими канцерогенами являются ультрафиолетовое и ионизирующие излучения.
Ультрафиолетовое излучение (УФ)с длиной волны 240-330 нм в больших дозах вызывает рак кожи и наружных слизистых оболочек, поскольку обладает высокой проникающей способностью и мутагенным действием на клетки эпидермиса и дермы. Поэтому длительный прием солнечных ванн, особенно в периоды высокой солнечной активности, может спровоцировать развитие рака кожи. Мутагенный эффект усиливается химическими канцерогенами, а также при действии фотосенсибилизаторов, которыми могут быть различные вещества (описано мощное фотосенсибилизирующее действие духов и другой парфюмерии).
Ионизирующее излучение (гамма - лучи, рентгеновские лучи, нейтронное излучение и пр.) обладают мощным мутагенным действием. Около 3% всех опухолей человека можно связать с мутагенным воздействием радиации. Если принять риск возникновения спонтанных опухолей за единицу, то после радиационного воздействия он возрастает в 20 раз, хотя эта закономерность имеет нелинейный характер. Существует избирательная чувствительность органов к радиации. Наиболее чувствительной тканью является кроветворная: после общего облучения резко увеличивается частота лейкозов. Очень чувствительны к воздействию радиации щитовидная железа и молочные железы. Известно, что женщины, болеющие туберкулезом легких, и вследствие этого проходившие частые рентгеноскопические исследования, имели и более высокую частоту развития опухолей молочной железы. Необходимо отметить, что женщины более чувствительны к воздействию радиации, так радиационно-индуцированные опухоли щитовидной железы чаще возникают именно у женщин. Несмотря на высокую частоту спонтанно развивающихся опухолей матки и яичников, действие радиации на эти органы не приводит к индукции опухолевого роста.
Степень канцерогенности зависит от вида радиации. Например, нейтронное поражение более мутагенно, чем g - излучение. Важное значение имеет возраст, в котором произошло воздействие радиации: максимальная частота развития опухолей молочной железы отмечается после радиационного поражения, полученного в возрасте 10-20 лет; при облучении в более молодом или старшем возрасте риск развития опухоли уменьшается.
Механические факторы. Известно, что сильная травма, ушиб могут спровоцировать развитие саркомы кости. Если вживить инородное тело в ткань, например под кожу, и при этом вызывать индукцию опухоли канцерогенными веществами, то скорость возникновения опухолей будет выше, чем при индукции теми же канцерогенами, но без влияния инородного тела. Опухоли могут возникать при длительном существовании язвы, например малигнизация язвы желудка, после заживления ожогов и т.д., хотя однозначно оценить роль травмы как причины малигнизации клеток нельзя и, по-видимому, механический фактор является дополнительным условием, но не причиной развития опухолей.
Вирусный канцерогенез
У человека опухоли вызываются в основном ДНК - содержащими вирусами, однако, несмотря на множество предположений и статистических данных, однозначного мнения о роли вирусов в канцерогенезе у человека нет. Существуют отдельные опухоли у человека в развитии которых в достаточной степени доказана роль вирусов. Было установлено, что хронические вирусные инфекции являются причинными факторами развития опухолевого процесса в 8-17 % всех случаев. Канцерогенез, связанный с инфекцией является комплексным процессом. С начала 60-х годов прошлого века были установлены следующие шесть вирусов, ассоциированных с опухолевыми заболеваниями, а именно, вирус Эпштейн-Барра (ЕВV) связан с лимфомой Беркита, Ходжскинской лимфомой, вирус папилломы человека (HPV) с раком шейки матки, половых органов, а также ротоглотки, вирусы гепатита B (HBV) и гепатита С (HCV) ассоциированы с гепатоцеллюлярной карциномой, Т-клеточный лимфотропный вирус человека (HTLV) - с Т-клеточной лимфомой, а также ассоциированный с саркомой Капоши вирус (KSHV) инициирует саркому Капоши.
ДНК- содержащие вирусы
Вирус папилломы человека. Известно больше 60 типов вирусов папилломы человека. Некоторые типы: 1, 2, 4, 7 - вызывают доброкачественную опухоль кожи - папиллому. Типы 16 и 18, реже 31, 33, 35, 51 являются причиной 85% карцином шейки матки, полового члена и прямой кишки. Однако, вирус-индуцированное опухолевое перерождение клетки in vitro не является полным. Таким образом, на развитие опухоли, по-видимому, влияют и другие факторы, в частности, другие вирусы (например вирус герпеса II типа).
Вирус герпеса II типа. Считается одним из факторов, являющихся причиной развития рака шейки матки у человека. При этом в большинстве случаев предполагается синергическое действие вирусов папилломы и герпеса, приводящее к опухолевому перерождению клеток.
Цитомегаловирус. Возможна его роль в развитии саркомы Капоши, однако, наиболее часто эта опухоль наблюдается при ВИЧ-инфекции, т.е. на фоне выраженного иммуннодефицита, поэтому роль цитомегаловируса в механизме канцерогенеза не окончательно ясна.
Вирус Эпштейна-Барра. Доказана роль этого вируса в развитии нескольких типов опухолей человека:
· лимфомы Беркитта (африканский тип)
· В-клеточной лимфомы в условиях иммунодефицита (часто развивается при ВИЧ-инфекции, трансплантации органов)
Вирус поражает В-лимфоциты и клетки эпителия носоглотки, вызывая их малигнизацию. Однако, этот вирус также не единственная причина перечисленных опухолей. Несмотря на повсеместное распространение вируса, четкая связь его с лимфомой Беркита прослеживается лишь в Африке, в других регионах только 15-20% лимфом Беркитта связано с вирусом. Таким образом, поражение клетки этим вирусом является всего лишь одним из механизмов канцерогенеза. В частности, в регионах, где есть лимфома Беркитта очень высока частота хронической малярии. Назофарингеальная карцинома встречается в южных районах Китая, в Африке и у эскимосов в Гренландии и на Аляске. Однако, учитывая столь ограниченные регионы встречаемости, вероятно, что генетические особенности, а также особенности окружающей среды являются важными.
Вирус гепатита В. Этот вирус может являться причиной развития рака печени, причем вероятнее всего в сочетании с химическими канцерогенами, например афлатоксином. Поэтому связь этого вируса с раком печени можно проследить лишь на Дальнем Востоке и в Африке, что связано с высоким содержанием афлатоксина в пищевых продуктах в этих регионах.
РНК-содержащие вирусы
Вирус Т-клеточного лейкоза. Как и вирус иммунодефицита человека этот вирус поражает СD4 + лимфоциты, передается половым путем и при переливании крови. Опухоль развивается только у 1% инфицированных через 20-30 лет после инфицирования. Инфицированые вирусом клетки усиленно синтезируют ИЛ-2 и рецепторы к нему, а также КСФ-ГМ. Заболевание встречается в некоторых регионах Японии и Карибского бассейна.
Механизм развития опухолей под действием вирусов связан с тем, что онковирусы содержат гены, встраивание которых в ДНК хозяина вызывает опухолевое перерождение клетки. Вирусные гены, способствующие развитию опухолей, называются вирусными онкогенами.
Бактерии и паразиты также обусловливают появление опухолей. Так, при инфицирование Helicobacter pylori повышает риск аденокарциномы желудка. Хотя, при условии, что 50% населения планеты имеет эту инфекцию, ее значение в развитии опухолей относительно условно. Паразитарная инвазия Schistosoma haematobium и Clonorchis sinensis способствует развитию, соответственно, рака мочевого пузыря и холангиокарциномы.
Химический канцерогенез
Первое описание связи между возникновением опухоли и действием химических веществ принадлежит Джону Хиллу, который в 1761 году описал рак слизистой оболочки полости носа у людей, постоянно применявших нюхательный табак. В 1775 Персиваль Потт отметил частое развитие рака кожи мошонки у трубочистов, которые имели эту профессию с детства. Эти наблюдения имели, безусловно, описательный характер. Прямая связь между действием химических веществ и развитием опухолей была отмечена лишь через сто лет при исследовании высокой частоты развития рака легких у рабочих урановых рудников.
В настоящее время химическим канцерогенам уделяется пристальное внимание. Все химические вещества, существующие в природе, делят на 3 группы по степени опасности:
1. Вещества - опасные канцерогены, т.е. вещества, канцерогенные свойства которых доказаны для человека.
2. Вещества с возможными канцерогенными свойствами:
а) с более высокой степенью доказанности
б) с низкой степенью доказанности
3. Вещества, не являющиеся канцерогенными.
Канцерогенность химических веществ нередко выявляется случайно и их опасность для человека оценивается либо на основании экспериментальных данных, либо с помощью статистических исследований. Так, в свое время было отмечено, что у лиц, работающих с анилиновыми красителями, рак мочевого пузыря возникает в 33 раза чаще, чем в остальной популяции, что в последствии привело к обнаружению использующихся в этом производстве химических веществ, обладающих канцерогенным действием.
Классификация канцерогенных веществ. Существуют различные классификации канцерогенных веществ, основанные на их химическом строении, происхождении, механизме действия и т.д. Выделяют экзогенные и эндогенные канцерогены, вызывающие развитие опухолей у животных.
Экзогенные канцерогенные вещества:
1) Полициклические ароматические углеводороды, ПАУ (бензпирен, метилхолантрен) вызывают опухоли кожи, молочной железы, мышечной, соединительной тканей.
2) Ароматические амины: 2-нафтиламин, бензидил, аминоазобензол, аминоазотолуол (вызывают опухоли печени, молочной железы, мочевого пузыря).
3) Нитрозосоединения (нитрозамины, нитрозамиды): нитрозодиметиламин, нитрозомочевина (вызывают опухоли печени, легких, почек, мозга, органов желудочно-кишечного тракта).
4) Неорганические вещества
· асбест (вызывает развитие мезотелиом).
· металлы и их соли: бериллий, никель, хром (вызывают развитие рака кожи).
5) Природные: афлатоксин, вырабатываемый грибом Aspergillus flavum (вызывает развитие рака печени).
6) Противоопухолевые препараты, особенно из группы алкилирующих соединений (цисплатин, циклофосфамид).
Эндогенные канцерогены. Ряд веществ, являющихся естественными метаболитами в организме человека и животных способствует или ускоряет развитие опухолей. Так, доказана роль эстрогенов в развитии гормоно-зависимых опухолей, таких как рак молочной железы и опухоли гонад, желчные кислоты и метаболиты триптофана способствуют развитию рака толстой кишки.
Механизмы повреждающего действия канцерогенов
Экзогенные канцерогенные вещества поступают в организм через желудочно-кишечный тракт с пищей, через легкие, через кожу; эндогенные вырабатываются в самом организме. Они легко проникают через клеточную мембрану и включаются в метаболизм клетки. Канцерогены по механизму действия делятся на генотоксические, т.е. влияющие на геном клетки и эпигенетические, т.е. не влияющие на геном клетки. Генотоксические канцерогены в свою очередь разделяются на непрямые (или проканцерогены) и прямые канцерогены.
Непрямые канцерогены подвергаются метаболизму в различных клетках, в частности, по механизму микросомального окисления с участием фермента цитохрома Р-450. Образовавшиеся при этом промежуточные метаболиты являются более активными, чем исходные продукты, и способны реагировать с ДНК клетки (наиболее частый механизм повреждения - метилирование ДНК). К таким веществам относятся, например, ПАУ и нитрозамины. Аналогичный процесс метилирования ДНК происходит и спонтанно, увеличиваясь с возрастом человека, что объясняет высокую частоту развития опухолей у лиц старческого и пожилого возраста. Прямые канцерогены, например нитрозамиды и неорганические канцерогены, непосредственно повреждают ДНК при попадании в клетку.
Эпигенетические канцерогены (к ним, например, относятся эндогенные канцерогены и вещества с возможными канцерогенными свойствами) стимулируют клеточную пролиферацию или способствуют развитию иммуносупрессии, что может ускорять малигнизацию клеток.
Химические канцерогены имеют важное значение в развитии опухолей у человека, поскольку предполагается, что основная масса развивающихся опухолей у человека связана с поступлением химических канцерогенов в связи с вредными привычками, при контакте с ними на производстве, с пищей и т.д. Так, по некоторым данным до 30% опухолей у человека можно связать с курением, 35% опухолей могут быть связаны с особенностями питания и около 4% - с производственными вредностями.
Курение - один из наиболее изученных факторов риска развития опухолей, особенно опасными является курение с детского возраста и большой стаж курения. В табачном дыму содержатся ПАУ, нитрозосоединения, ароматические амины и другие химические канцерогены. Кроме опухолей легких канцерогены, поступающие с табачным дымом, уменьшают выработку пролактина, лютеинизирующего и других гормонов, что приводит к дисгормонозу и предрасположенности к раку молочной железы.
Особенности питания. Канцерогенным действием обладает этиловый спирт, злоупотребление которым является фактором риска онкологических заболеваний верхних отделов пищеварительного тракта. Так, употребляющие 120 и более граммов этанола в сутки имеют в 20 раз большую вероятность развития рака пищевода по сравнению с лицами, употребляющими менее 40 г/сутки.
Важное значение имеют пищевые нитраты, поступающие в основном с овощами, а также с некоторыми деликатесными продуктами, например копчеными колбасами. Повышенные дозы нитратов увеличивают риск развития рака желудка. Пищевые нитраты всасываются в желудочно-кишечном тракте, а затем с кровью попадают в слюнные железы, откуда со слюной снова поступают в желудок в течение нескольких часов. Около 20% нитратов превращается в нитриты под действием микрофлоры полости рта, а другая часть нитратов переходит в нитриты в желудке. Эта реакция протекает особенно быстро в щелочной или нейтральной среде желудка, например при гипоацидных состояниях. Из нитритов в желудке в свою очередь образуются нитрозамины, являющиеся генотоксическими канцерогенами.
Увеличенное потребление с пищей животных жиров является фактором риска развития рака толстой кишки. Это связано с тем, что пищевые жиры стимулируют желчеобразование и желчевыделение, а следовательно, значительная часть желчных кислот не успевает всасываться и поступает в толстую кишку. Дезоксихолевая кислота вызывает стимуляцию пролиферации эпителия толстой кишки, что является фоном, на котором не успевает происходить репарация ДНК при повреждении генома клетки.
Важную роль в канцерогенезе может играть дефицит поступающих с пищей веществ, таких как витамины А, Е, С, а также некоторых микроэлементов, например селена, поскольку они уменьшают мутагенное действие химических канцерогенов.
ЭТИОЛОГИЯ ОПУХОЛЕЙ.
Этиология опухолей изучена не до конца. В данный момент ведущей считается мутационная теория канцерогенеза. Ниже перечислены основные исторически сложившиеся теории.
1) Вирусно-генетическая теория решающую роль в развитии опухолей отводит онкогенным вирусам, к которым относят: герпесоподобный вирус Эпштейна-Барр (лимфома Беркитта), вирус герпеса (лимфогранулематоз, саркома Капоши, опухоли головного мозга), папилломавирус (рак шейки матки, бородавки обыкновенные и ларингеальные), ретровирус (хронический лимфолейкоз), вирусы гепатитов B и C (рак печени). Согласно вирусно-генетической теории интеграция генома вируса с генетическим аппаратом клетки может привести к опухолевой трансформации клетки. При дальнейшем росте и размножении опухолевых клеток вирус перестает играть существенную роль.
2) Физико-химическая теория основной причиной развития опухолей считает воздействие различных физических и химических факторов на клетки организма (рентгеновское и гамма-излучение, канцерогенные вещества), что приводит к их онкотрансформации. Помимо экзогенных химических канцерогенов рассматривается роль в возникновении опухолей эндогенных канцерогенов (в частности, метаболитов триптофана и тирозина) путем активации этими веществами протоонкогенов, которые посредством синтеза онкобелков приводят к трансформации клетки в опухолевую.
3) Теория дисгормонального канцерогенеза рассматривает в качестве причины возникновения опухолей различные нарушения гормонального равновесия в организме.
4) Дизонтогенетическая теория причиной развития опухолей считает нарушения эмбриогенеза тканей, что под действием провоцирующих факторов может привести к онкотрансформации клеток ткани.
5) Теория четырёхстадийного канцерогенеза объединяет все вышеперечисленные теории
Канцерогенные факторы
- Химические факторы
Вещества ароматической природы (полициклические и гетероциклические ароматические углеводороды, ароматические амины), некоторые металлы и пластмассы обладают выраженным канцерогенным свойством благодаря их способности реагировать с ДНК клеток, нарушая ее структуру (мутагенная активность). Канцерогенные вещества в больших количествах содержатся в продуктах горения автомобильного и авиационного топлива, в табачных смолах. При длительном контакте организма человека с этими веществами могут возникнуть такие заболевания, как рак легкого, рак толстого кишечника и др. Известны также эндогенные химические канцерогены(ароматические производные аминокислоты триптофана), вызывающие гормонально зависящие опухоли половых органов.
- Физические факторы
Солнечная радиация (в первую очередь ультрафиолетовое излучение) и ионизирующее излучение также обладает высокой мутагенной активностью. Так, послеаварии Чернобыльской АЭС отмечено резкое увеличение заболеваемости раком щитовидной железы у людей, проживающих в зараженной зоне. Длительное механическое или термическое раздражение тканей также является фактором повышенного риска возникновения опухолей слизистых оболочек и кожи (рак слизистой рта, рак кожи, рак пищевода). Также есть давнее мнение А.А. Белостоцкого, что чисто механические факторы могут быть причиной почти любого вида рака. Избыточное или наоборот, недостаточное, механическое воздействие на ткани могло бы приводить к изменениям в тканях (изменения во взаимодействии клетки с другими клетками и с внеклеточным матриксом), которые и приводят к канцерогенезу
- Биологические факторы
Доказана канцерогенная активность вируса папилломы человека в развитии рака шейки матки, вируса гепатита B в развитии рака печени, ВИЧ — в развитии саркомы Капоши. Попадая в организм человека, вирусы активно взаимодействуют с его ДНК, что в некоторых случаях вызывает трансформацию собственных протоонкогенов человека в онкогены. Геном некоторых вирусов (ретровирусы) содержит высокоактивные онкогены, активирующиеся после включения ДНК вируса в ДНК клеток человека.
- Наследственная предрасположенность
Изучено более 200 наследственных заболеваний, характеризующихся повышенным риском возникновения опухолей различной локализации. Развитие некоторых типов опухолей связывают с врожденным дефектом системы репарации ДНК (пигментная ксеродерма)
Предопухолевые состояния (предраки)
Предраковое состояние характеризуется развитием атрофических и пролиферативных процессов с высоким риском малигнизации и трансформации в злокачественную опухоль. При этих заболеваниях совсем не обязательна трансформация в злокачественную опухоль, однако высокий риск злокачественного перерождения при предраковом состоянии всегда существует.
К данной категории заболеваний относятся все неспецифические и специфические хронические длительные воспаления, дистрофии, дисплазии, метаплазии, гиперпролиферации тканей, различные иммунодефициты. Например, фактором повышенного риска малигнизации является хронический гастрит, хроническая бронхопневмония, хронический аднексит и другие воспаления.
Этиология опухолей. Определяющие факторы и внешние этиологические факторы. Канцерогенез.
1) определяющие – оказывают постоянное влияние на организм (пол, возраст, этническая принадлежность, наследственность):
- рак молочной железы встречается у женщин в 100 раз чаще, чем у мужчин, а рак щитовидной железы – в 5 раз чаще.
- рак легкого в 10 раз чаще возникает у мужчин и т. д.
- мутации генов BRCA-1 и BRCA-2 (2-3% рака молочной железы). Наличие мутаций приводит к риску РМЖ 50-80%.
- семейные опухолевые синдромы (Li-Fraumeni - множественные семейные опухоли различных локализаций; Gorlin - базалиома, медуллобластома; MEN-IIA, MEN-IIB – рак щитовидной железы, феохромоцитома, опухоль паращитовидных желез)
- в процессе деления в каждой клетке человека возникает 5000 спонтанных повреждений ядерной и митохондриальной ДНК; спонтанная нестабильность генома в 1 млн раз превышает индуцированную
2) модифицирующие (внешние) – не влияют на организм постоянно (место жительства, условия труда и быта, вредные привычки и т. д.):
- неправильное питание – 35%
- репродуктивный статус – 7%
- профессиональные вредности – 5%
- генетические дефекты – 4%
- геофизические факторы – 3%
Канцерогенез (основные этапы воздействия канцерогена на организм):
1. Воздействие канцерогенного вещества на человека, которое характеризуется:
а) наружной дозой – конценрацией канцерогена в окружающей среде
б) внутренней дозой – концентрацией канцерогена во внутренней среде организма (кровь, моча, ткани и т. д.)
в) биологически эффективной дозой – количеством экзогенного канцерогена или его метаболита, которое связывается с ДНК или белками.
2. Ранний биологический эффект: повреждение генетического аппарата клетки, активация онкогенов и инактивация генов-супрессоров с появлением хромосомных аберраций, микроядер и др.
3. Клиническое проявление злокачественной опухоли.
В реализации всех этих этапов важное значение имеют особенности генетической / метаболической репарации ДНК, иммунный статус, питание и ряд других факторов.
А) Инфекционные факторы (вирусы, микроорганизмы и паразиты)
- вирус Эпштейн-Барра (EBV) вызывает лимфому Беркита, рак носоглотки, опухоль Ходжкина. Мишень – В-лимфоцит.
- вирус HTLV - T-клеточный лимфолейкоз. Мишень – Т-лимфоцит.
- вирус HPV – рак шейки матки. Мишень – многослойный плоский эпителий.
- вирус гепатита B (HBV) – рак печени (у носителей антигена HBs рак печени бывает в 15-20 раз чаще)
- ВИЧ-1 – саркома Капоши.
- Helicobacter pylori – рак желудка
- гемолитическая шистосома – рак мочевого пузыря
Б) Физические факторы:
- УФО - рак кожи и меланома
- радиация – рак щитовидной железы, легкого, гемобластозы, рак кожи
- термический фактор – рак кожи, слизистой рта
- СВЧ и микроволновое излучение – рак почки, гемобластозы, опухоли ЦНС
В) механические факторы:
- меланома кожи в 50% наблюдений развивается из поврежденных невусов
- опухоли яичка у наездников
Г) Химические факторы: мышьяк и его производные; асбест; бензидин; хром и его производные; изопропиловый спирт; иприт; сажа, смолы, минеральное масло; винилхлорид; производство кожи, ремонт обуви; деревообработка; эстрогены; циклофосфан; афлотоксин; бензпирен; бериллий и его соединения; оральные контрацептивы; никель и его соединения; ДДТ; кадмий и его производные; адриамицин; цисплатин; хлороформ; гербициды с феноксиуксусной кислотой.
Самый сильный химический канцероген – Тринитробензантрон, полученный в дизельных выбросах.
· Экзогенные канцерогены: хроматы, мышьяк и его соединения, кобальт, окись бериллия, асбест и ряд других. Эндогенные канцерогены. Эти соединения образуются в организме в результате физико-химической модификации продуктов нормального обмена веществ. Полагают, что такими потенциально канцерогенными веществами являются жёлчные кислоты, эстрогены, некоторые аминокислоты (тирозин, триптофан), липопе-роксидные соединения.
· Радиационный канцерогенез относится к числу стохастических эффек тов. Основной причиной злокачественной трансформации облученной клетки являются нелетальные повреждения генетического материала. На первых порах исследования радиационного канцерогенеза господствова ло представление о том, что прямой причиной злокачественной транс формации клетки является мутация, возникшая в результате поглощения порции энергии излучения соответствующим участком генома клетк
Вирусная и вирусо-генетическая теории этиологии опухолевого роста. Механизмы действия онковирусов на клетку. Понятие об онкогенах и антионкогенах, их роль в онкогенезе.
· Вирусно-генетическая теория отводит решающую роль в развитии неоплазм онкогенным вирусам. Сущность вирусно-генетической теории заключается в представлении об интеграции геномов вируса и нормальной клетки, т. е. в объединении нуклеиновой кислоты вируса с генетическим аппаратом клетки, которая превратится в опухолевую. Онкогенные вирусы могут быть ДНК- и РНК-содержащими (онкорнавирусы). Среди экзогенных вирусов (ДНК- и РНК-содержащих) в этиологии опухолей человека имеют значение герпесоподобный вирус Эпстайна - Барра (развитие лимфомы Беркитта), вирус герпеса (рак шейки матки), вирус гепатита В (рак печени) и некоторые другие. Наряду с экзогенными в настоящее время обнаружены и эндогенные онкогенные вирусы, относящиеся к онкорнавирусам. Эти вирусы в обычных условиях составляют интегральную часть клеточного генома, однако при определенных воздействиях они способны вызывать опухоли у человека. Согласно вирусно-генетической теории, процесс канцерогенеза распадается на две фазы, в которых роль вируса различна. Первая фаза - поражение вирусами клеточного генома и трансформация клеток в опухолевые. Опухолеродные ДНК-геномные вирусы и РНК-геномные ретровирусы, подобно возбудителям вирусных инфекций,- циклические внутриклеточные паразиты. Для размножения им необходимо извне проникнуть в клетку и встроить свой геном в ее геном. При первом попадании в клетку опухолеродные вирусы включают свой геном в ту часть генома клетки, где находится онкоген (протоонкоген), который представляет собой нормальные последовательности нуклеотидов клеточной ДНК (протоонкогены входят в состав генома каждой нормальной клетки и участвуют в регуляции ее деления и дифференцировки). Дочерние вирусы, уже содержащие онкоген, попадают затем в клетки-мишени. Онкоген, входящий в состав вирусного генома, активируется и трансформирует клетку в опухолевую. Вторая фаза - размножение образовавшихся опухолевых клеток, при котором вирус не играет существенной роли.
· Опухолевый супрессор, антионкоген, ген-супрессор опухолевого роста - (tumor suppressor, cancer susceptibility gene, antioncogene, лат. suppressio — подавление) - ген, продукт которого в норме оказывает негативное влияние на клеточный цикл, препятствуя этим образованию опухоли. Мутации в антионкогенах (точечные мутации, делеции или блокирование экспрессии) приводят к развитию опухоли.
· Онкоге́н — это ген, продукт которого может стимулировать образование злокачественной опухоли. Мутации, вызывающие активацию онкогенов, повышают шанс того, что клетка превратится в раковую клетку. Считается, что гены-супрессоры опухолей (ГСО) предохраняют клетки от ракового перерождения, и, таким образом, рак возникает либо в случае нарушения работы генов-супрессоров опухолей, либо при появлении онкогенов (в результате мутации или повышения активности протоонкогенов, см. ниже)[1].
Стадии онкогенеза, их механизм. Роль иммунного надзора и неиммунных факторов резистентности организма в онкогенезе. Предраковые состояния. Понятия: доброкачественная и злокачественная опухоль.
78. Стадии онкогенеза, их механизм. Роль иммунного надзора и неиммунных факторов резистентности организма в онкогенезе. Предраковые состояния. Понятия: доброкачественная и злокачественная опухоль.
в процессе онко-генеза можно условно выделить несколько общих этапов.
5. • На первом этапе происходит взаимодействие канцерогенов химической, физической и биологической природы с протоонкогенами и антионкогенами (онкосупрессорами) генома нормальной клетки.
6. • В результате такого взаимодействия на втором этапе канцерогенеза подавляется активность онкосупрессоров, а также происходит трансформация протоонкогенов в онкогены. Экспрессия онкогена — необходимое и достаточное условие для трансформации нормальной клетки в опухолевую.
7. • В результате подавления активности онкосупрессоров и экспрессии онкогенов на третьем этапе синтезируются и реализуют свои эффекты (непосредственно или с участием клеточных факторов роста и рецепторов к ним) он-кобелки. С этого момента генотипически изменённая клетка приобретает опухолевый фенотип.
8. • На четвёртом этапе опухолевая клетка начинает бесконтрольно проли-ферировать, что ведёт к формированию новообразования (опухолевого узла).
Неиммунные механизмы.Эти механизмы осуществляют надзор за сохранением нормального (индивидуального и однородного) клеточного состава организма. Реализуют эти механизмы как клетки, так и гуморальные факторы.
Иммунные механизмы. Эти механизмы реализуют клеточное и гуморальное звенья иммунитета.
Доброкачественные опухоли. Клетки доброкачественной опухоли морфологически идентичны или похожи на нормальные клетки—предшественники и формируют характерные — высокодифференцированные для данной ткани структуры. Такие опухоли растут медленно, не метастазируют и с клинической и прогностической точек зрения их расценивают как доброкачественные.
Злокачественные опухоли. Клетки злокачественной опухоли морфологически отличаются от нормальной клетки—предшественника, соседних опухолевых клеток и образуют искажённые тканевые структуры (или вовсе их не образуют) — низкодифференцированные, анапластические. Эти опухоли растут быстро, прорастают в соседние структуры, а отдельные опухолевые клетки формируют близко расположенные или отдалённые точки роста — метастазы.С клинической и прогностической точек зрения такие опухоли расценивают как злокачественные.
79. Нарушение всасывания углеводов пищи. Нарушение синтеза, депонирования, расщепления гликогена. Нарушения транспорта углеводов в клетке и их усвоения. Галактоземия, фруктозурия, пентозурия, гликогенозы, агликогеноз.
80. Гипогликемические состояния, их виды и механизм. Патогенез гипогликемической комы и ее проявления.
Гипогликемии — состояния, характеризующиеся снижением уровня глюкозы плазмы крови (ГПК) ниже нормы (менее 65 мг%, или 3,58 ммоль/л). В норме ГПК натощак колеблется в диапазоне 65—110 мг%, или 3,58—6,05 ммоль/л.
Причины Гипогликемии.
Патология печени.Наследственная и приобретённая патология печени — одна из наиболее частых причин гипогликемии. К гипогликемии приводят нарушения транспорта глюкозы из крови в гепатоциты, снижение активности гликогенеза в них и отсутствие (или малое содержание) депонированного гликогена. Гипогликемия развивается также при длительном голодании, а также может развиться при значительной активации жизнедеятельности организма (например, при физической нагрузке или стрессе).
Нарушения пищеварения. Нарушения пищеварения — полостного переваривания углеводов, а также их пристеночного расщепления и абсорбции — приводят к развитию гипогликемии. Гипогликемия развивается также при хронических энтеритах, алкоголь ном панкреатите, опухолях поджелудочной железы, синдромах нарушенного всасывания.
Патология почек. Гипогликемия развивается при нарушении реабсорбции глюкозы в проксимальных канальцах нефрона почек.
Эндокринопатии. Основные причины развития гипогликемии при эндокринопатиях: недостаток гипергликемизирующих факторов или избыток инсулина.
Углеводное голодание. Углеводное голодание наблюдается в результате длительного общего голодания, в том числе углеводного. Дефицит в пище только углеводов не приводит к гипогликемии в связи с активацией глюконеогенеза (образование углеводов из неуглеводных веществ).
Длительная значительная гиперфункция организма при физической работе. Гипогликемия развивается при длительной и значительной физической работе в результате истощения запасов гликогена, депонированного в печени и скелетных мышцах.
Последствия гипогликемии: гипогликемическая реакция, синдром и кома.
Гипогликемическая реакция — острое временное снижение ГПК до нижней границы нормы (как правило, до 80—70 мг%, или 4,0—3,6 ммоль/л).
Гипогликемический синдром — стойкое снижение ГПК ниже нормы (до 60— 50 мг%, или 3,3—2,5 ммоль/л), сочетающееся с расстройством жизнедеятельности организма.
Гипогликемическая кома — состояние, характеризующееся падением ГПК ниже нормы (как правило, менее 40—30 мг%, или 2,0—1,5 ммоль/л), потерей сознания, значительными расстройствами жизнедеятельности организма.
81. Гипергликемические состояния, их виды, этиология. Патогенные последствия острой и хронической гипергликемии. Гипергликемическая кома.
Гипергликемии.
Гипергликемии — состояния, характеризующиеся увеличением ГПК выше нормы (более 120 мг%, или 6,05 ммоль/л натощак).
Причины гипергликемии: эндокринопатии, неврологические и психогенные расстройства, переедание, патология печени.
Эндокринопатии.Эндокринопатии — наиболее частая причина гипергликемии. Основные причины развития гипергликемии при эндокринопатиях: избыток гипергликемизирующих факторов и дефицит инсулина.
Неврологические и психогенные расстройства. Нейро- и психогенные расстройства характеризуются активацией симпатико-адреналовой, гипоталамо-гипофизарно-надпочечниковой и тиреоидной систем. Гормоны этих систем вызывают ряд эффектов, приводящих к значительной гипергликемии.
Переедание. Переедание— одна из причин гипергликемии. Глюкоза быстро всасывается в кишечнике. ГПК повышается и превышает возможность гепатоцитов включать её в процесс гликогенеза. Кроме того, избыток углеводсодержащей пищи в кишечнике стимулирует гликогенолиз в гепатоци-тах, потенцируя гипергликемию.
Патология печени. При печёночной недостаточности может развиваться преходящая гипергликемия в связи с тем, что гепатоциты не способны трансформировать глюкозу в гликоген. Обычно это наблюдается после приёма пищи.
Последствия гипергликемии: гипергликемический синдром и гипергликемическая кома.
Гипергликемический синдром — состояние, характеризующееся значительным и относительно длительным увеличением ГПК выше нормы (до 190—210 мг%, т.е. 10,5-11,5 ммоль/л и более), сочетающееся с расстройством жизнедеятельности организма.
В развитии гипергликемической комы, различают два периода, по аналогии с гипогликемической комой: прекома и гипергликемическая кома. Но, время на их развитие измеряется не десятками минут, а днями.
При развитии гипергликемической прекомы, больного беспокоят:
Затем, по мере нарастания кетоновых тел, присоединяется тошнота и рвота. Причем, рвота не приносит облегчения. Часто отмечаются боли в животе. В критический момент, когда гипергликемия и кетоз (наличие кетоновых тел в крови) достигают значительных цифр, появляется спутанность сознания, увеличение частоты дыхания, которое становится шумным.
Кома имеет ряд особенных признаков, кроме потери сознания, что отличает ее от подобных состояний:
· кожа сухая, холодная на ощупь. Отмечается ее повышенное шелушение.
· дыхание частое, поверхностное и шумное. При этом, от больного исходит запах ацетона.
Скорость развития комы зависит от индивидуальных особенностей, но, в среднем, стадия прекомы длится 1-3 дня. А сама кома, без лечения, приводит к смерти не более чем за сутки. Хотя, может отмечаться и больший срок. К тому же, ряд клиницистов, выделяют промежуточную стадию - начинающейся комы, время которой исчисляется несколькими часами.
. С 82 ПО 85, ВОПРОСЫ ПО САХАРНЫЙ ДИАБЕТ, ВСЕ ЗДЕСЬ.
82. Этиология и патогенез сахарного диабета 1 типа. Роль вирусов и аутоиммунных процессов в механизмах развития СД 1 типа. Стадии течения СД 1 типа.
САХАРНЫЙ ДИАБЕТ - заболевание, которое характеризуется нарушением всех видов метаболизма и расстройством жизнедеятельности организма; развивается в результате гипоинсулинизма (т.е. абсолютной или относительной инсулиновой недостаточности).
Первичные формы сахарного диабета. Первичные формы СД характеризуются отсутствием у пациента каких-либо определённых заболеваний, вторично приводящих к развитию диабета. Выделяют две разновидности первичного СД:
• инсулинзависимый сахарный диабет (ИЗСД);
• инсулиннезависимый сахарный диабет (ИНСД).

Вторичные формы сахарного диабета. Вторичные формы СД характеризуются наличием у пациента какой-либо основной болезни или патологического состояния, повреждающих поджелудочную железу, а также действие на неё физических или химических факторов. Это приводит к возникновению СД. К таким болезням, патологическим состояниям и факторам относятся:
• Заболевания, поражающие ткань поджелудочной железы (например, панкреатит).
• Другие болезни эндокринной системы (например, семейный полиэндокринный аденоматоз).
• Воздействие на поджелудочную железу химических или физических агентов.
Сахарный диабет типов I и II
В более ранних классификациях выделяли СД типов I и II. Эти обозначения вначале применяли как синонимы ИЗСД и ИНСД соответственно. Современные специалисты считают такой подход не совсем корректным. Это объясняется тем, что, например, больные с ИНСД также могут приобрести зависимость от инсулина. При его недостатке у них развивается кетоацидоз, чреватый коматозным состоянием (например, это наблюдается у многих пациентов без ожирения, имеющих в крови AT.
Этиология.
СД развивается вследствие либо дефицита инсулина (ИЗСД), либо недостаточности его эффектов (ИНСД).
· Дефицит инсулинаможет возникнуть под влиянием факторов биологической, химической, физической природы, а также при воспалительных процессах поджелудочной железы
· Воспалительные процессы, возникающие в поджелудочной железе под действием факторов биологической (главным образом, микроорганизмов), химической и физической природы. Хронические панкреатиты примерно в 30% случаев являются причиной инсулиновой недостаточности.
· Недостаточность эффектов инсулинаразвивается под влиянием причин нейро- или психогенной природы, контринсулярных факторов, а также вследствие дефектов инсулиновых рецепторов и пострецепторных нарушений в клетках-мишенях.
При дефиците инсулина происходит: повреждение и гибель р-клеток островков Лангерханса, уменьшение суммарной массы β-клеток, подавление синтеза и выделения в кровь инсулина из повреждённых β-клеток.
Дата добавления: 2018-08-06 ; просмотров: 694 ;
Читайте также:

