Опухоль по левому краю
Патологическое деление клеток в ускоренном темпе приводит к разрастанию тканей. В зависимости от их структуры образуется доброкачественная или злокачественная опухоль почки. Симптомы и лечение, сколько живут при каждом из заболеваний - все зависит от конкретного случая. Разберем основные типы опухолей почек, особенности их проявления и применяемой терапии.
Причины развития
В организме здорового человека каждую минуту погибают клетки, которые затем заменяются новыми. Это нормальный процесс, происходящий под контролем иммунной системы. Когда возникает сбой, клетки начинают делиться несоразмерно. В итоге образуются лишние структуры, мешающие работоспособности органа.
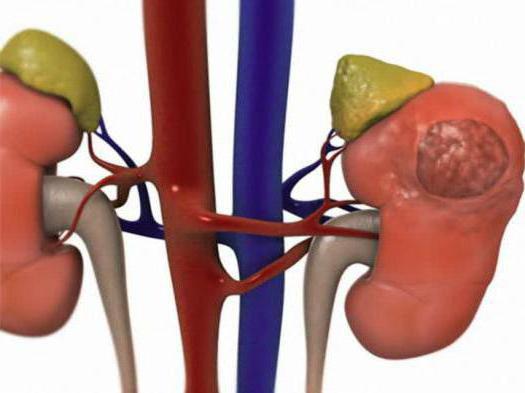
Основными причинами, способствующими развитию опухолей почек, являются:
- пожилой возраст (70 и более лет);
- пагубное влияние химических и токсичных веществ;
- радиоактивное и ультрафиолетовое излучение;
- генетические аномалии;
- наследственный фактор;
- заболевания иммунной системы.
Немаловажную роль в появлении доброкачественных и злокачественных образований играет длительный воспалительный процесс или хроническая болезнь.
Доброкачественная опухоль почки: симптомы и лечение, сколько живут
Доброкачественное образование менее агрессивно. Порой оно настолько незначительно, что даже не вызывает дискомфорта и не нарушает привычную жизнедеятельность органа. Опухоль характеризуется медленным ростом, при ее развитии не нарушается структура ткани и не образуются метастазы.
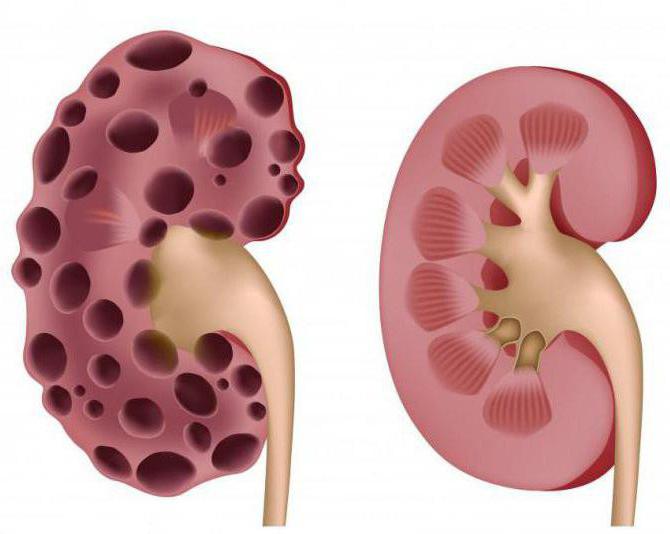
Пациент с подозрением на доброкачественное образование в почке обычно жалуется на:
- слабость и общее недомогание;
- боли в пояснице;
- кровь в моче;
- отечность ног;
- незначительное повышение температуры тела;
- потерю веса.
Врач при осмотре и пальпации может также обнаружить увеличение органа, прощупать образование неясного характера и отметить явное увеличение брюшной полости больного. Для установления более точной клинической картины назначается обследование в виде УЗ и лабораторной диагностики.
Лечение доброкачественной опухоли почки чаще всего сводится к наблюдению и поддержанию нормального функционирования органа. К хирургическому удалению прибегают лишь в некоторых случаях, когда польза от планируемого вмешательства значительно превосходит риски. Исход болезни обычно благоприятный, с большой продолжительностью жизни.
Типы доброкачественных образований в почках
Аденома и онкоцитома
Это наиболее часто встречающееся патологическое разрастание железистой ткани почки. Характеризуется медленным темпом роста, а также маленькими размерами образований. В настоящий момент врачи не могут объяснить причины ее появления в организме человека.
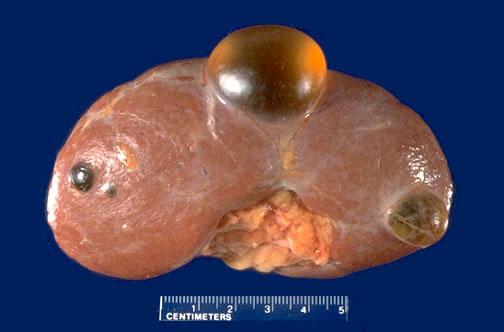
Обычно болезнь протекает бессимптомно. Лишь в случаях значительного увеличения в размерах можно заподозрить рак почки в связи со схожестью клинических признаков. Многие врачи-диагносты считают аденому предвестником злокачественной опухоли, которая дает зачатки для развития более серьезного заболевания.
Онкоцитома чаще встречается у мужчин и выявляется случайно. В отличие от аденомы, размеры ее более внушительны. По микроскопическому строению клетки онкоцитомы схожи с раковыми, что дает основание считать ее опухолью с высоким уровнем малигнизации.
Ангимиолипома и фиброма
Это достаточно редкий вид доброкачественной опухоли почки, к образованию которой ведет врожденная мутация генов. Заболеванию в почти 80% случаев сопутствует туберозный склероз. Как и другие липомы почек, ангимиолипома поражает жировую ткань почки - именно здесь клетки начинают бесконтрольно делиться.
Образование может встречаться и в качестве одиночной болезни. Наиболее подвержены риску его развития женщины среднего возраста. Обычно опухоль бывает незначительных размеров и мало беспокоит пациента. Это обуславливает тот факт, что диагностируют ее чаще всего случайно.
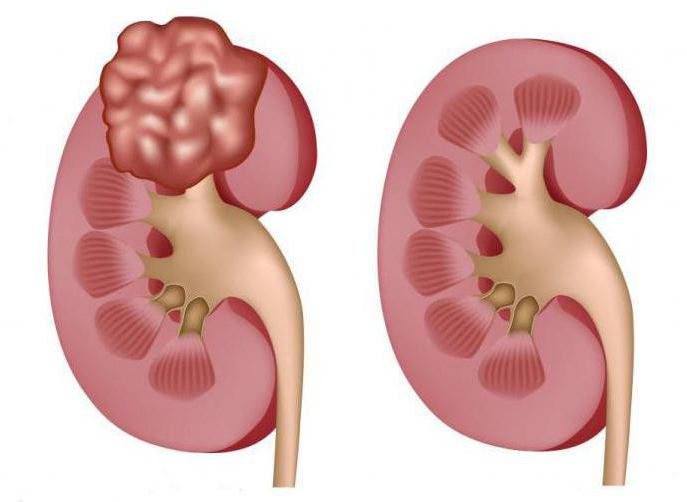
Фиброма образуется за счет избытка клеток фиброзной ткани почки. Опухоль при этом располагается внутри или снаружи органа. Заболеванию больше подвержены женщины. Прежде чем клинически проявить себя, фиброма разрастается на периферии почки.
Разновидности злокачественных новообразований почки
Рак почки – онкологическое заболевание, которое в большинстве случаев поражает эпителиальную ткань органа. Риску подвержены мужчины и женщины 40–70 лет. Заядлые курильщики увеличивают свои шансы развития новообразования в 2–4 раза.
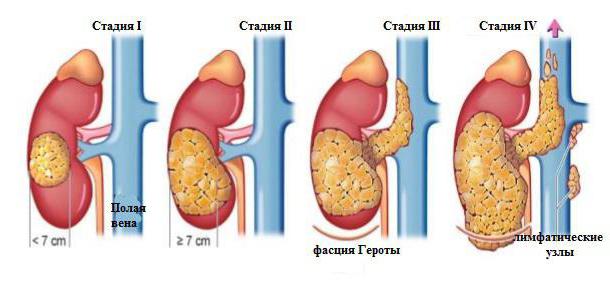
Как и поражения других органов, злокачественная опухоль почки развивается по разным сценариям, т. е. имеет разновидности. Среди них в 85% случаев диагностируют почечно-клеточный рак, который локализируется в эпителиальной ткани почечных трубочек. Кроме него встречаются злокачественные опухоли:
- Переходно-клеточная – на ее долю приходится 5–10% заболеваемости. Место поражения – лоханка почки. Заболевание имеет схожую клиническую картину с раком мочевого пузыря. Прогноз в 90% случаев благоприятный.
- Нефробластома – развивается преимущественно в детском возрасте. Редкий вид новообразования, встречающийся приблизительно в 8% случаев возникновения опухолей почек.
- Саркома – поражает соединительную ткань. Такой диагноз ставят очень редко. Это агрессивный тип опухоли, для которого характерно метастазирование и быстрый рост.
Удаление опухоли почки злокачественной природы - неминуемый этап лечения. Оперативное вмешательство в совокупности с терапевтическим воздействием максимально продлевает срок и качество жизни пациента.
Злокачественная опухоль почки: симптомы и лечение, сколько живут
Клинические признаки разных форм рака почки схожи, что затрудняет первичную диагностику. За профессиональной медицинской помощью людей побуждают обратиться такие тревожные признаки, как:
- кровь в моче;
- варикоцеле;
- болезненность и опухоли поясничного отдела позвоночника;
- чрезмерная утомляемость, слабость, усталость;
- гипертония;
- отечность ног;
- быстрая потеря веса;
- лихорадка.
Большинство симптомов напрямую указывают на заболевания мочевыделительной системы, но определить точный диагноз, основываясь только на жалобах пациента, практически невозможно.
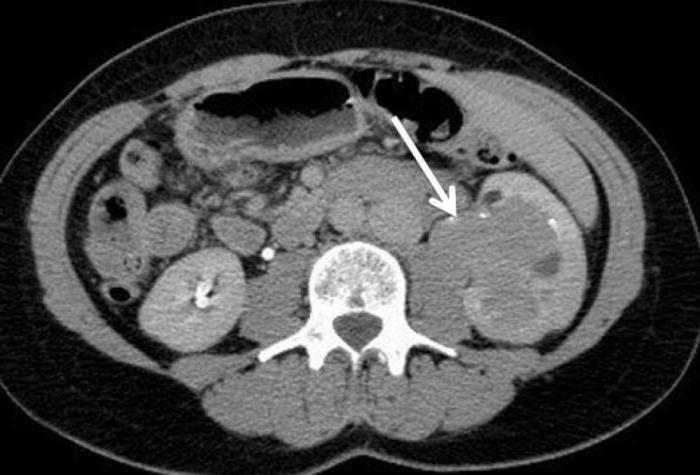
Прохождение процедуры УЗИ, КТ или МРТ, а также лабораторных анализов прояснит ситуацию.
Методы лечения
Злокачественная опухоль почки, последствия бесконтрольного развития которой крайне печальны, с успехом лечится. При своевременной диагностике пациент в 90% случаев может рассчитывать на положительный исход. Методы лечения зависят от конкретной ситуации. Чаще всего в роли главного лекарства выступает хирургическое вмешательство.
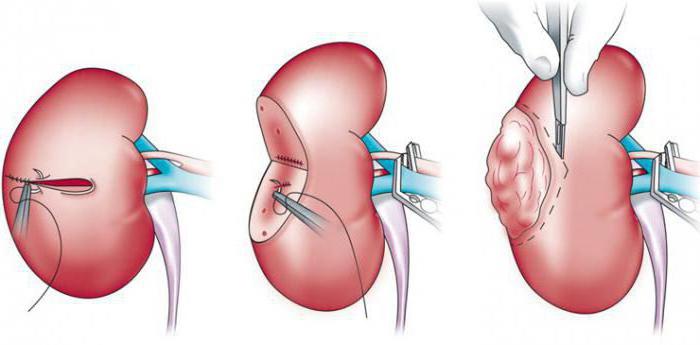
Как и любая болезнь, доброкачественные или злокачественные образования напрямую зависят от индивидуальных характеристик здоровья человека. Для разных индивидов по-своему будет проявляться опухоль почки, симптомы и лечение. Сколько живут пациенты с таким диагнозом? Все опять же сводится к конкретным данным. Доброкачественные опухоли обычно совсем не мешают жить полноценно и долго. Злокачественные опухоли без метастазов излечиваются в 90% случаев.
Первые признаки опухоли головного мозга легко спутать с симптомами других, менее опасных заболеваний. Поэтому и пропустить начало развития онкологии мозга очень легко. Рассказываем, как этого не допустить.

В России ежегодно выявляют около 34 000 случаев опухоли головного мозга. Как и прочие заболевания, оно молодеет. Дело в том, что первые признаки опухоли головного мозга напоминают усталость, депрессию и тревожные расстройства. А при жалобах на головную боль, бессонницу и потерю внимания обычно советуют взять отпуск, а не сделать МРТ, особенно в молодом возрасте. Именно поэтому так легко пропустить начало болезни.
Первые симптомы новообразований
Первые признаки болезни не дают чёткой картины — очень уж сильно они схожи с симптомами многих других заболеваний:
- тошнота. Она будет присутствовать независимо от того, когда вы последний раз принимали пищу. И, в отличие от отравления, самочувствие после рвоты не улучшится;
- сильная головная боль, усиливающаяся при движении и ослабевающая в вертикальном положении;
- судороги и эпилептические припадки;
- нарушение внимания и ослабление памяти.
О наличии опухоли говорит совокупность этих симптомов. Конечно, есть вероятность, что они появятся по другим причинам независимо друг от друга, но встречается такое достаточно редко.
Именно на этой стадии вылечить опухоль проще всего. Но, к сожалению, редко кто принимает подобные симптомы всерьёз.
Первые общемозговые симптомы опухоли
Когда наступает вторая стадия развития заболевания, возбуждаются мозговые оболочки и повышается внутричерепное давление. В результате наступают общемозговые изменения.
Опухоль давит на мозг, влияя на его работу.
В это время лечение ещё успешно, но проходит дольше и сложнее. Симптомы второй стадии уже не так легко спутать с симптомами других болезней:
- теряется чувствительность на отдельных участках тела;
- случаются внезапные головокружения;
- ослабевают мышцы, чаще на одной стороне тела;
- наваливается сильная усталость и сонливость;
- двоится в глазах.
Вместе с тем, общее самочувствие портиться, продолжается утренняя тошнота. Всё это проявляется у больного независимо от того, в какой части мозга находится новообразование.
Однако, спутать симптомы всё-таки можно — они примерно такие же, как и при эпилепсии, нейропатии или гипотонии. Так что если вы обнаружили у себя эти симптомы, не спешите впадать в панику. Но к врачу обязательно сходите — неизвестность ещё никому не шла на пользу. Да и с такими симптомами не стоит шутить.
Очаговые признаки опухолей на ранних стадиях
Если общемозговые симптомы проявляются из-за поражения всего головного мозга и влияют на самочувствие всего организма, то очаговые зависят от участка поражения. Каждый отдел мозга отвечает за свои функции. В зависимости от местонахождения опухоли поражаются различные отделы. А значит и симптомы болезни могут быть разными:
- нарушение чувствительности и онемение отдельных участков тела;
- частичная или полная потерей слуха или зрения;
- ухудшение памяти, спутанность сознания;
- изменение интеллекта и самосознания;
- спутанность речи;
- нарушение гормонального фона;
- частая смена настроения;
- галлюцинации, раздражительность и агрессия.
Симптомы могут подказать, в какой части мозга располагается опухоль. Так, параличи и судороги характерны для поражения лобных долей, потеря зрения и галлюцинации — затылочных. Поражённый мозжечок приведёт к расстройству мелкой моторики и координации, а опухоль в височной доле приведёт к утрате слуха, потере памяти и эпилепсии.
Диагностика при подозрении на опухоль головного мозга
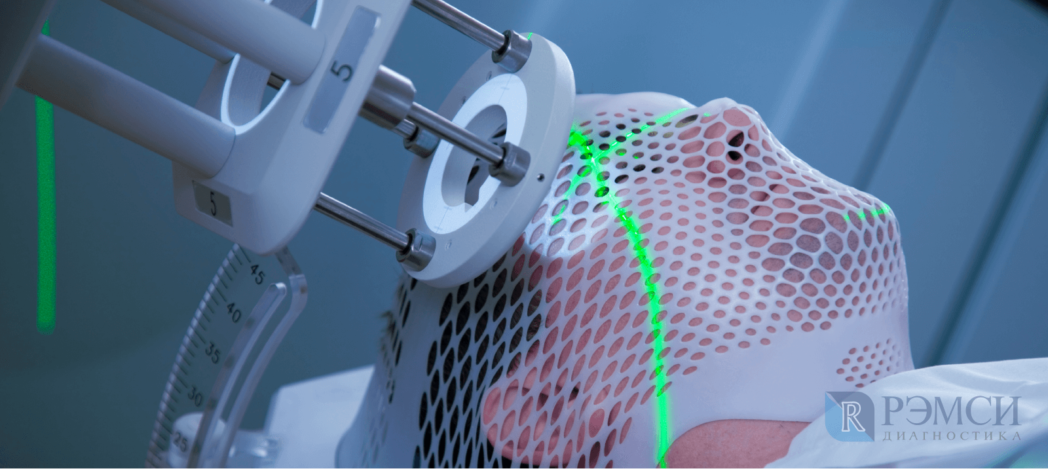
На наличие опухоли могут косвенно указывать даже общий или биохимический анализ крови. Однако, если есть подозрения на новообразование, назначают более точные анализы и исследования:
- электроэнцефалография покажет наличие опухолей и очагов судорожной активности коры мозга;
- МРТ головного мозга покажет очаги воспаления, состояние сосудов и самые мелкие структурные изменения головного мозга;
- КТ головного мозга, особенно с применением контрастной жидкости, поможет определить границы поражения;
- анализ ликвора — жидкости из желудочков мозга — покажет количество белка, состав клеток и кислотность;
- исследование спинномозговой жидкости на наличие раковых клеток;
- биопсия опухоли поможет понять, доброкачественное это или злокачественное новообразование.
Когда бить тревогу?
Так как первые признаки опухоли головного мозга могут встречаться даже для относительно здоровых людей, следует отнестись к ним разумно: не игнорировать, но и не паниковать раньше времени. К врачу следует обратиться в любом случае, но особенно важно это сделать, если у вас:
- есть все ранние симптомы новообразования (усталость, головная боль и т. д.);
- была черепно-мозговая травма или инсульт;
- отягощённая наследственность: некоторые родственники страдали от онкологических заболеваний.
В ходе осмотра, любой врач может направить вас к неврологу, заподозрив опухоль по косвенным признакам. Офтальмолог, проверяя внутричерепное давление, а эндокринолог — после анализа крови на гормоны. Внимательный врач обратит внимание даже на речь и координацию. Не игнорируйте такие советы: лучше посетить невролога и убедиться, что вы здоровы, чем пропустить развитие заболевания.
Наиболее сложными вопросами определения операбельности больного при левосторонних торакотомиях является диагностика поражения анатомических образований "аортального окна", нисходящего отдела аорты, легочных вен, а также как и при правосторонних операциях — пищевода.
Распространение опухоли по левому главному бронху или наличие метастазов в области "аортального окна"могут явиться причинами опухолевого поражения внелегочных анатомических образований этого отдела средостения.
Внутрисредостенная часть левого главного бронха и многочисленные расположенные здесь трахеобронхиальные и пароаортальные лимфатические узлы находятся в сложных и весьма тесных взаимоотношениях с рядом важных анатомических образований. Это, прежде всего, дуга аорты и начальный отдел ее нисходящей части, левая легочная артерия, блуждающий нерв и отходящий от него возвратный гортанный нерв, пищевод и грудной лимфатический проток.
Дуга аорты ограничивает доступ к левому трахеобронхальному углу и в начальном отделе своей нисходящей части интимно связана с задней стенкой левого главного бронха фиброзными тяжами, так называемыми "аорто-бронхиальными связками Жилетта"(Бежан Л., Зитти Е.Гр. 1981; Надь Д., 1959).
В области дуги аорты, в непосредственном соприкосновении с верхне-задней стенкой левого главного бронха, располагаются бронхиальные артерии, повреждение которых может осложниться трудно останавливаемым кровотечением. Обычно они 3— стволиками отходят от задней поверхности исходящего отдела аорты, на уровне IV — VIII грудных позвонков, направляясь к главным бронхам (Травин А.А. с соавт., 1981; Уткин В.В., Озолис А.Я., 1978; Колесников И.С. с соавт., 1988). В таких случаях их идентификация и перевязка не представляет больших трудностей. Но, приблизительно, у каждого пятого больного встречаются различные варианты отхождения бронхиальных артерий и даже их общего ствола от задне-нижней поверхности дуги аорты (Бисенков Н.П. с соавт., 1955; Уткин В.В., Озолис А.Я., 1978). Это необходимо помнить при хирургических манипуляциях в области "аортального окна".
При наличии опухоли или конгломерата метастазов в лимфатические узлы, прорастающих медиастинальную плевру в проекции корня легкого, выполняется широкая медиастинотомия и с помощью тщательной препаровки оценивается возможность внеперикардиальной обработки элементов корня легкого. При прорастании перикарда, невозможности выделения достаточных участков легочных сосудов, для обеспечения безопасных условий для их обработки, необходимо переходить к выполнению внутриперикардиальной ревизии.
Своеобразие строения левой легочной артерии — относительно небольшая протяженность, наличие артериальной связки, а также близость к верхнедолевому бронху —определяет нередкое вовлечение ее в опухолевый процесс и особенности хирургической обработки. Левая легочная артерия располагается, в основном, внеперикардиально, задним листком перикарда покрыта только ее передне-нижняя поверхность. Пальпацией через поперечный синус перикарда возможно оценить состояние нижней стенки начального отдела левой легочной артерии и левой боковой стенки легочного ствола.
Выделение легочной артерии при интраперикардиальной ее обработке осуществляют преимущественно комбинируя трансперикардиальный и внеперикардиальный доступы к сосуду. Отдавливая книзу верхнюю легочную вену, обнажают переднюю поверхность легочной артерии. Под контролем зрения, оттягивая свободный листок перикарда, рассекают его до нижнего края стенки артерии в поперечном направлении. Анатомическим ориентиром, соответствующим границе ствола легочной артерии и левой ее ветви со стороны нижней поверхности является латеральный конец остаточной складки перикардиального заворота верхней легочной вены. Отслаивая перикард по передней и нижней поверхности, вскрывают околоартериальный фасциальный футляр, в плоскости которого и производят выделение легочной артерии.
При наличии плотных сращений перикарда или увеличенных лимфатических узлов в области верхней стенки сосуда и нижней поверхности дуги аорты необходимо обязательно, предварительно, рассечь перикард и под контролем зрения произвести их препаровку.
Проведение лигатуры под легочной артерией возможно до и после пересечения артериальной связки, а также дистальнее и проксимальнее ее. Если достаточно хорошо была выделена нижняя поверхность легочной артерии, провизорную лигатуру можно провести проксимальнее связки после рассечения заднего листка перикарда над инструментом, проведенным под легочной артерией, у ее верхнего края. В таких случаях, артериальная связка предотвращает смещение наложенной провизорной лигатуры в проксимальном направлении и дает большую уверенность при проведении препаровки анатомических образований "аортального окна".
При проведении лигатуры дистальнее артериальной связки и высоком распространении опухоли по левой легочной артерии, имеется реальная угроза рассечения сосуда при его перевязке. Короткая, широкая левая легочная артерия фиксирована в дистальных отделах конгломератами лимфатических узлов, в проксимальных — артериальной связкой. Поэтому, в такой ситуации лучше приступать к выделению и пересечению артериальной связки, а в области корня легкого —препаровке левой легочной артерии в пределах пораженных метастазами лимфатических узлов.
В любом случае, при перевязке легочной артерии или прошивании ее с помощью механических сшивающих аппаратов непосредственно по стенке ствола легочной артерии, необходимо предварительно, в намеченном для перевязки уровне пережать сосуд и убедиться, что при этом не наступило тяжелых расстройств кровообращения в связи с сужением легочного ствола.
Интраперикардиальное выделение легочных вен слева технически проще, чем при правосторонних операциях. Длина внутриперикардиальной части легочных вен слева несколько больше, чем справа, и кроме того, они почти по всей своей окружности расположены интраперикардиально, а нижняя легочная вена обладает длинной брыжейкой, образованной задним листком перикарда. Левое предсердие более доступно из левостороннего доступа и значительно легче может быть мобилизовано при необходимости выполнить его резекцию. При массивном поражении опухолью стенки левого предсердия в семи случаях в клинике была выполнена внутрисердечная ревизия стенок левого предсердия через его ушко, по методу, описанному для ревизии правого предсердия и полых вен.
Поражение опухолью стенки аорты значительно увеличивает риск операции и усложняет ее. Как показал опыт оперативных вмешательств, разобраться в истинных размерах и характере прорастания опухолью стенки аорты можно только в процессе оперативной диагностики, путем проведения тщательной препаровки. Нередко, массивный, казалось бы, неподвижный опухолевый конгломерат, окружающий аорту, после его мобилизации со стороны здоровых тканей без особых технических трудностей отделяется от стенки сосуда. Часто, даже в при опухолевом поражении стенки аорты, оно оказывается по размерам значительно меньшим, чем это предполагалось в начале ревизии. Кроме того, прорастание опухолью стенки аорты может ограничиться только ее адвентициальной оболочкой, резекцию которой можно произвести на весьма значительном протяжении.
Препаровку аорты осуществляют по тем же правилам, что и верхней полой вены, со стороны неизмененных ее отделов. После выделения стенки аорты из параканкрозных изменений уточняются истинные размеры опухолевого поражения.
При прорастании опухоли только в адвентициальную оболочку можно определить некоторую подвижность опухолевого конгломерата по отношению к сосуду. В неизмененном участке вскрывают адвентициальную оболочку и постепенно отделяют ее от среднего слоя. При прорастании всех слоев стенки аорты показанием к резекции ее участка мы считаем наличие ограниченного поражения нисходящего отдела, при возможности выполнить краевую резекцию без значительного сужения просвета сосуда после наложения аортального зажима.
При периферических опухолях, локализующихся в верхушке легкого, так называемых "вколоченных", выделение легкого и оценка возможности выполнить операцию, особенно трудны. Грубые манипуляции могут привести к разрыву подключичной артерии и плечеголовной вены. Поэтому, при выделении верхушки легкого всегда необходимо вести препаровку от средостения по ходу сосудов. Выделив справа верхнюю полую вену, продолжают выделение по ходу правой плечеголовной вены, пока у купола гемиторакса отчетливо не ощущатся пульсация подключичной артерии. Смещая артерию вверх, осторожно препарируют ее.
После выделения сосудов, задние отделы верхушки правого легкого выделяются уже более безопасно. Слева — сначала необходимо выделить дугу аорты и отходящую от нее левую подключичную артерию и, продолжая препарировать сосуд, выделить легкое. После выделения левой подключичной артерии до купола гемиторакса, дальнейшее выделение верхушки легкого можно осуществлять более энергично.
Во время выполнения хирургических операций при манипуляциях на большой глубине, что встречается при выделении верхушки легкого, его базальных отделов, нередко возникают трудности с освещением операционного поля. Для решения этой задачи был сконструирован и применяется универсальный инструмент, который сочетает в себе качества зажима, осветителя и наконечника электродиатермии. К прямому зажиму Федорова единым штифтом, соединяющим бранши, прикреплен фиксатор, который фиксирует гибкий светопроводящий кабель из стекловолокна, длиной 1800 мм, диаметром 3,5 мм. Светопроводящий кабель, в свою очередь, подключается к световому прибору 489,10 с входным напряжением 6 В (0,8 А). Светопроводящий кабель и световой прибор используется от бронхоскопа Фриделя типа 441 производства ГДР (применение световода и светового прибора не исключает их применения при бронхоскопиях).
Разработано два варианта фиксаторов: пружинный и винтовой.
Универсальный зажим используется нами в качестве рабочего инструмента для выделения легкого из спаек, сращений, удаления патологически измененных лимфатических узлов средостения в условиях узкого операционного поля при плохой его освещенности основным источником света. При выполнении операций на легких с использованием универсального зажима значительно улучшается обзор операционного поля, сокращается время операции, повышается ее безопасность.
Прорастание опухоли в диафрагму, как правило, не считается противопоказанием к выполнению резекции легкого, если в опухолевый процесс не вовлечены органы поддиафрагмального пространства. Высокая эластичность диафрагмы позволяет выполнить ее резекцию в значительных пределах до 10 — см. Рассечение диафрагмы и выполнение резекции пораженного ее участка лучше осуществлять на заключительном этапе операции. Только в отдельных случаях, при наличии подозрения на возможность поражения органов брюшной полости, предварительно выполняется диафрагмотомия и проводится ревизия поддиафрагмального пространства.
Таким образом, интраоперационная диагностика с точки зрения технических возможностей и обоснованности выполнения оперативного вмешательства, осуществляемая в ранних стадиях развития рака легкого, иногда, за считанные минуты, при распространенном опухолевом процессе требует от хирурга большого опыта и высокого хирургического мастерства. Принимая окончательное решение о выполнении намеченного объема операции, он должен полностью представлять характер и распространенность опухолевого поражения, быть уверенным в технических возможностях осуществления, в крайнем случае, паллиативного вмешательства.
Бисенков Л.Н., Гришаков С.В., Шалаев С.А.
Распад опухоли — это закономерное следствие слишком активного роста ракового узла по периферии или осложнение избыточно высокой реакции распространённого злокачественного процесса на химиотерапию.
Не каждому пациенту доводится столкнуться с тяжелой проблемой распада ракового процесса, но при любой интенсивности клинических проявлений инициируемое распадом злокачественной опухоли состояние непосредственно угрожает жизни и радикально меняет терапевтическую стратегию.

Распад опухоли: что это такое?
Распад — это разрушение злокачественного новообразования, казалось бы, что именно к распаду необходимо стремиться в процессе противоопухолевой терапии. В действительности при химиотерапии происходит уничтожение раковых клеток, только убийство органичное и не массовое, а единичных клеток и небольших клеточных колоний — без гибели большого массива ткани с выбросами в кровь из распадающихся клеток токсичного содержимого.
Под действием химиотерапии клетки рака приходят не к распаду, а к процессу апоптоза — программной смерти. Останки раковых клеток активно утилизируются фагоцитами и уносятся прочь от материнского образования, а на месте погибших возникает нормальная рубцовая ткань, очень часто визуально не определяющаяся.
Регрессия злокачественного новообразования в форме апоптоза происходит медленно, если наблюдать за новообразованием с перерывами в несколько дней, то заметно, как по периферии раковый узел замещается совершенно нормальной тканью и сжимается в размере.
При распаде раковый конгломерат не замещается здоровыми клетками соединительной ткани, мертвые клеточные пласты формируются в очаг некроза, отграничивающийся от остальной раковой опухоли мощным воспалительным валом. Внутри злокачественного новообразования некроз не способен организоваться и заместиться рубцом, он только увеличивается, захватывая новые участки ракового узла, походя разрушая опухолевую сосудистую сеть. Из мертвого очага в кровь поступают продукты клеточного гниения, вызывая интоксикацию.
Массированный выброс клеточного субстрата становится причиной тяжелейшей интоксикации, способной привести к смерти.
Причины распада злокачественной опухоли
Инициируют распад ракового образования всего только две причины: сама жизнедеятельность клеток злокачественной опухоли и химиотерапия.
Первая причина спонтанного — самопроизвольного распада характерна для солидных новообразований, то есть рака, сарком, злокачественных опухолей головного мозга и меланомы. Вторая причина распада типична для онкогематологических заболеваний — лейкозов и лимфом, при онкологических процессах встречается чрезвычайно редко.

Второй вариант распада, типичный для онкогематологических заболеваний, можно констатировать по клиническим симптомам тяжелейшей интоксикации с осложнениями — тумор-лизис-синдрому (СОЛ) и биохимическим анализам крови, где резко повышена концентрация мочевой кислоты, калия и фосфора, но существенно снижен кальций. Конкретная побудительная причина для развития СОЛ — обширное злокачественное поражение с очень высокой чувствительностью к химиотерапии.
При онкологических процессах — раках, саркомах, меланоме реакция на цитостатики преимущественно умеренная и не столь стремительная, поэтому СОЛ принципиально возможен только в исключительных случаях мелкоклеточного, недифференцированного или анаплазированного злокачественного процесса.
Симптомы распада злокачественной опухоли
Клиническим итогом спонтанного распада раковой опухоли становится хроническая интоксикация, нередко сочетающаяся с симптомами генерализованного воспаления вследствие образования гнойного очага. Симптомы разнообразны, но у большинства отмечается прогрессивно нарастающая слабость, повышение температуры от субфебрильной до лихорадки, сердцебиение и даже аритмии, изменение сознания — оглушенность, нарушение аппетита и быстрая потеря веса.
Локальные проявления спонтанного разрушения раковой опухоли определяются её локализацией:
- рак молочной железы, меланома и карцинома кожи, опухоли ротовой полости — гнойная, обильно секретирующая открытая язва с грубыми подрытыми краями, часто источающая гнилостный запах;
- распадающаяся карцинома легкого — при прободении некротической полости в крупный бронх возникает приступообразный кашель с гнойной мокротой, нередко с прожилками крови, иногда случается обильное легочное кровотечение;
- разрушение новообразования органов желудочно-кишечного тракта — развитие локального перитонита при прободении ракового конгломерата в брюшную полость, кровотечение с чёрным стулом и рвотой кофейной гущей;
- распадающаяся карцинома матки — интенсивные боли внизу живота, нарушение мочеиспускания и дефекации при образование гнойных свищей.
Синдром опухолевого лизиса при лейкозах и лимфомах потенциально смертельное состояние, приводящее:
- в первую, очередь к осаждению кристаллов мочевой кислоты в почечных канальцах с выключением функции и острой почечной недостаточностью;
- дополнительно повреждает почки быстрое закисление крови — лактатацидоз;
- снижение уровня кальция и повышение фосфатов инициирует судорожный синдром, дополняемый неврологическими проявлениями вследствие выброса цитокинов;
- повышения калия негативно отражается на сердечной деятельности;
- выброс биологически-активных веществ из клеток приводит к повышению проницаемости мелких кровеносных сосудов, что снижает уровень белков и натрия крови, уменьшает объем циркулирующей плазмы, клинические проявляется падением давления и усугублением поражения почек;
- обширные и глубокие нарушения метаболизма во всех системах органов с исходом в полиорганную недостаточность.
Лечение распада опухоли
Формально при распадающейся опухоли невозможна радикальная операция, зачастую заболевание считается неоперабельным, но химиотерапия и облучение исключаются из программы, потому что способны усугубить некроз. Отчаянное положение пациента и вероятность массированного кровотечения из изъеденного раком крупного сосуда оправдывает выполнение паллиативной операции, основная цель которой — удаление очага хронического воспаления и интоксикации.
Синдром лизиса опухоли лечится многочасовыми капельными вливаниями при усиленном диурезе — выведении мочи, связыванием мочевой кислоты специальными лекарствами. Одновременно поддерживается работа сердечно-сосудистой системы, купируется интоксикация и воспаление. При развитии острой почечной недостаточности проводится гемодиализ.
Синдром лизиса опухоли сложно лечить, но можно предотвратить или хотя бы уменьшить его проявления. Профилактика начинается за несколько дней до курса химиотерапии и продолжается не менее трёх суток после завершения цикла. Кроме специальных препаратов, выводящих мочевую кислоту, назначаются продолжительные капельницы, вводятся недостающие микроэлементы, а избыточные выводятся или связываются другими лекарствами.
Профилактика лизиса опухоли стала стандартом лечения онкогематологических больных, чего нельзя сказать об онкологических пациентах с распадающимися злокачественными процессами, которым очень сложно найти хирурга, готового выполнить паллиативную операцию. Во вмешательстве по санитарным показаниям отказывают из-за сложности выхаживания тяжелого больного после обширного хирургического вмешательства. В нашей клинике никому не отказывают в помощи.
Читайте также:

