Нейроэндокринные опухоли забрюшинного пространства
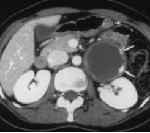
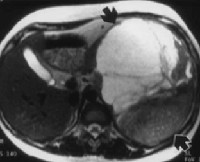
Внеорганные забрюшинные опухоли – группа злокачественных и доброкачественных новообразований мезодермального, нейрогенного и эмбриогенного происхождения, локализующихся в забрюшинном пространстве. Характерно длительное бессимптомное течение. При забрюшинных опухолях большого размера наблюдаются диспепсические расстройства, нарушения мочеиспускания, одышка, неврологические симптомы и отеки нижних конечностей. При злокачественных поражениях на поздних стадиях выявляются признаки раковой интоксикации. Диагноз выставляется с учетом данных КТ, МРТ, УЗИ, биопсии и других исследований. Лечение – операция, радиотерапия, химиотерапия.
- Классификация забрюшинных опухолей
- Причины развития забрюшинных опухолей
- Симптомы забрюшинных опухолей
- Диагностика забрюшинных опухолей
- Лечение и прогноз при забрюшинных опухолях
- Цены на лечение
Общие сведения
Внеорганные забрюшинные опухоли – группа новообразований, происходящих из тканей забрюшинного пространства, в том числе из жировой, мышечной, соединительной и нервной ткани, лимфоузлов, лимфатических и кровеносных сосудов и эмбриональных элементов. Группа забрюшинных опухолей не включает в себя онкологические процессы в органах, расположенных в данном пространстве, а также метастатические поражения забрюшинных лимфоузлов при опухолях других локализаций. Причинами объединения столь разнородных заболеваний в одну группу являются сходные особенности клинического течения, общие методы диагностики и терапии.
Забрюшинные опухоли могут быть как злокачественными, так и доброкачественными. Встречаются редко, по различным данным составляют от 0,03 до 0,3% от общего количества онкологических заболеваний. Некоторые специалисты полагают, что эта цифра занижена из-за диагностических затруднений при выявлении данной патологии. Обнаруживаются преимущественно в возрасте 50 лет и старше. Представители обоих полов страдают одинаково часто. Лечение осуществляют специалисты в области онкологии, неврологии и сосудистой хирургии.

Классификация забрюшинных опухолей
Забрюшинным пространством называют пространство между задним листком брюшины, диафрагмой, мышцами спины, позвоночником и мышцами, выстилающими дно малого таза. В этой анатомической зоне локализуются поджелудочная железа, почки, надпочечники, мочеточники, часть двенадцатиперстной кишки и часть толстого кишечника. Пространство между органами заполнено клетчаткой, в которой располагаются нервные сплетения, лимфоузлы, лимфатические и кровеносные сосуды. Забрюшинная клетчатка разделена фасциями на несколько отделов.
Внеорганными забрюшинными опухолями считаются любые узлы, расположенные в данном пространстве за исключением новообразований, происходящих из перечисленных выше органов, а также метастатических поражений лимфоузлов и опухолей, прорастающих в забрюшинное пространство из других анатомических зон (например, из брюшной полости). В основе наиболее популярной классификации забрюшинных опухолей, созданной Аккерманном в 1954 году, лежат гистогенетические особенности неоплазий. Согласно этой классификации различают три больших подгруппы таких новообразований: мезодермальные, нейрогенные и происходящие из элементов эмбриональных тканей.
Мезодермальные забрюшинные опухоли:
- Происходящие из жировой ткани: липомы (доброкачественные) и липосаркомы (злокачественные).
- Происходящие из гладкомышечной ткани: лейомиомы (доброкачественные) и лейомиосаркомы (злокачественные).
- Происходящие из поперечно-полосатой мышечной ткани: рабдомиомы (доброкачественные) и рабдомиосаркомы (злокачественные).
- Происходящие из соединительной ткани: фибромы (доброкачественные) и фибросаркомы (злокачественные).
- Происходящие из кровеносных сосудов: гемангиомы (доброкачественные) и ангиосаркомы (злокачественные), гемангиоперицитомы (доброкачественные и злокачественные).
- Происходящие из лимфатических сосудов: лимфангиомы (доброкачественные) и лимфангиосаркомы (злокачественные).
- Происходящие из остатков первичной мезенхимы: миксомы (доброкачественные) и миксосаркомы (злокачественные).
- Неясного гистогенеза: ксантогранулемы (доброкачественные).
Нейрогенные забрюшинные опухоли:
- Происходящие из оболочек нервов: нейрофибромы (доброкачественные), нейролемоммы (доброкачественные и злокачественные).
- Происходящие из симпатических нервных ганглиев: ганглионевромы (доброкачественные) и ганглионейробластомы (злокачественные).
- Происходящие из хромаффинных и нехромафинных клеток параганглиев и внеогранно расположенных участков ткани надпочечников: параганглиомы (доброкачественные, злокачественные), феохромоцитомы, рак из клеток надпочечников.
Забрюшинные опухоли из эмбриональных остатков: тератомы, хордомы.
Причины развития забрюшинных опухолей
Причины появления забрюшинных опухолей пока не выяснены. Ученые выделяют ряд факторов, способствующих развитию этой патологии. В числе таких факторов – специфические и неспецифические генетические нарушения, воздействие ионизирующего излучения и некоторых химических веществ. На возможную связь с ионизирующим облучением указывает повышенная вероятность возникновения забрюшинных опухолей у пациентов, ранее получавших радиотерапию в процессе лечения других онкологических заболеваний.
Существуют исследования, свидетельствующие о повышении риска развития некоторых видов новообразований данной локализации при воздействии гербицидов и пестицидов, особенно – диоксина и производных феноксиацетоновой кислоты. Механизм стимуляции роста забрюшинных опухолей в подобных случаях пока не выяснен. Есть версии, как о прямом воздействии, так и об опосредованном влиянии в результате подавления иммунитета при токсическом воздействии химикатов.
Симптомы забрюшинных опухолей
Особенностью забрюшинных опухолей является длительное отсутствие клинической симптоматики, обусловленное наличием большого количества рыхлой клетчатки и относительной подвижностью соседних органов. Некоторые новообразования достигают огромных размеров, не вызывая нарушений функций пищеварительной и мочевыводящей системы. В литературе встречаются описания отдельных узлов массой от 13 до 51 кг.
Еще одним типичным признаком забрюшинных опухолей является отсутствие специфических симптомов. Клиническая картина заболевания обусловлена не видом новообразования, а его локализацией (в нижней, верхней или боковой части забрюшинного пространства), близостью тех или иных органов и анатомических образований (кровеносных сосудов, нервов, лимфатических протоков). Пациенты с забрюшинными опухолями обычно впервые обращаются к врачу в связи с постоянными болями в животе. При пальпации у 80% больных определяются узлы различного размера и консистенции. В половине случаев прощупывание забрюшинной опухоли сопровождается болью различной интенсивности.
Возможны жалобы на тошноту, рвоту, преждевременное появление чувства насыщения и нарушения стула. При новообразованиях, локализующихся в нижней части забрюшинного пространства, могут наблюдаться расстройства мочеиспускания, вызванные сдавлением мочевого пузыря. При высоко расположенных забрюшинных опухолях иногда развивается одышка, обусловленная давлением на диафрагму. На ранних стадиях у многих больных выявляются гипотермия и гипергидроз нижней конечности на стороне поражения. На поздних этапах болезни гипотермия конечности сменяется гипертермией. Развитие этого симптома при забрюшинных опухолях обусловлено начальным раздражением и последующим параличом симпатического нерва.
При сдавлении крупных вен, расположенных в забрюшинном пространстве, наблюдаются отеки и варикоз в области нижних конечностей. У 25-30% пациентов выявляются неврологические расстройства. При злокачественных забрюшинных опухолях на поздних стадиях отмечаются снижение веса, потеря аппетита, лихорадка неясного генеза и общая гипертермия. Новообразования данной локализации часто рецидивируют, но редко метастазируют. Характерно метастатическое поражение печени и легких. Реже встречаются вторичные опухоли в яичниках и лимфоузлах.
Диагностика забрюшинных опухолей
Диагноз устанавливается на основании жалоб, результатов внешнего осмотра и дополнительных исследований. Пациентов с подозрением на забрюшинную опухоль направляют на УЗИ, КТ и МРТ органов брюшной полости и забрюшинного пространства. Перечисленные диагностические методы позволяют определить структуру и локализацию новообразования, оценить степень вовлеченности близлежащих органов и выявить отдаленные метастазы в печени. Учитывая ряд признаков (форма, плотность, наличие или отсутствие капсулы, уровень гомогенности, степень васкуляризации), после проведения УЗИ, МРТ и КТ специалист может оценить злокачественность забрюшинной опухоли и выдвинуть обоснованные предположения о типе новообразования.
Для оценки состояния пищеварительной и мочевыводящей системы применяют рентгенконтрастные методы (ирригоскопию и экскреторную урографию). Для выявления герминогенных новообразований назначают тесты на определение альфа-фетопротеина и хорионического гонадотропина. Поскольку основным методом лечения забрюшинных опухолей является их радикальное удаление, биопсию обычно не проводят из-за высокого риска обсеменения и недостаточной целесообразности исследования. Исключением являются ситуации, когда забор материала осуществляется для планирования операции, определения резектабельности новообразования или исключения метастатического характера онкологического поражения.
Лечение и прогноз при забрюшинных опухолях
Единственным радикальным способом лечения является оперативное вмешательство. В зависимости от локализации удаление забрюшинной опухоли производят с использованием бокового доступа, срединной лапаротомии или торакоабдоминального доступа. Более чем у половины пациентов операция включает в себя резекцию близлежащих органов: почки, поджелудочной железы, двенадцатиперстной кишки или толстой кишки. Эффективность пред- и послеоперационной радиотерапии и химиотерапии при забрюшинных опухолях пока остается под сомнением. Показанием к использованию этих лечебных методик является доказанная злокачественность новообразования при наличии сомнений в его операбельности.
Данные об операбельности забрюшинных опухолей сильно различаются. В литературе встречаются указания как на 25%, так и на 95% резектабельность подобных новообразований. Послеоперационная летальность при удалении забрюшинных опухолей составляет около 5%, вероятность развития местных рецидивов в отдаленном периоде – около 50%. До 5 лет с момента операции доживает менее 10% пациентов, страдающих злокачественными новообразованиями. При доброкачественных забрюшинных опухолях прогноз более благоприятный, однако, высокая вероятность рецидивирования обуславливает необходимость большого количества повторных хирургических вмешательств.
Нейроэндокринные опухоли органов брюшной полости и забрюшинного пространства (клиника, диагностика, лечение, прогноз)
Нейроэндокринные опухоли (НЭО) представляют собой группу злокачественных новообразований, происходящих из нейроэндокринных клеток, находящихся в любой части тела, характеризующихся положительной иммуногистохимической реакцией со специфическими маркерами (хромогранин А — ХрА, синаптофизин — Син), сродством к серебру, способностью вырабатывать различные пептидные гормоны и биогенные амины, которые вызывают типичные гормональные синдромы [1].
Стандартизованные показатели заболеваемости НЭО в разных странах варьируют в пределах 0,71–1,36 на 100 000 человек в год. Большинство исследователей отмечают увеличение частоты заболеваемости за последние 30 лет с ежегодным приростом заболеваемости на 3 % [2].
НЭО органов брюшной полости и забрюшинного пространства составляют до 20 % всех новообразований желудочно-кишечного тракта (ЖКТ), поджелудочной железы и других органов и около 2 % всех злокачественных новообразований другого генеза. Наиболее частой их локализацией является ЖКТ (73,7 %) и бронхолегочная система (25,1 %). В пределах ЖКТ большинство опухолей локализуются в тонкой кишке (28,7 %), червеобразном отростке (18,9 %) и прямой кишке (12,6 %). Общая 5-летняя выживаемость больных НЭО независимо от локализации составляет 67,2–82 % [3].
Чаще при НЭО клинические симптомы отсутствуют до возникновения осложнений или до развития карциноидного синдрома (КС). Поэтому в большинстве случаев диагностика первичной опухоли и метастазов затруднена.
При морфологическом исследовании НЭО часто возникают большие трудности в их точной верификации и определении принадлежности к этому типу опухоли. Точная гистогенетическая диагностика НЭО и установление степени их злокачественности возможны с помощью методов электронной микроскопии (ЭМИ) и иммуногистохимии (ИГХ).
Есть основание предполагать, что степень дифференцировки опухолевых апудоцитов, их функциональная активность и синтез того или иного гормона оказывают влияние на скорость и характер роста опухоли, определяют способность к метастазированию, рецидивированию и инвазии.
ИГХ-исследования показывают, что НЭО могут давать положительную реакцию на серотонин, вазоактивный интестинальный полипептид и многие другие гормоны и биогенные амины. На основании ультраструктурного типа эндокринных гранул (форма, размер и внутреннее строение) и ИГХ-идентификации синтезируемого ими гормона можно точно определить функциональный профиль НЭО, что важно для понимания клинического проявления заболевания [4].
Для течения НЭО определены несколько независимых прогностических параметров: размер, локализация, характер роста, гистологический тип опухоли, степень атипии, гормональная зависимость.
Существуют различные методы диагностики НЭО: компьютерная томография (КТ), ультразвуковая томография (УЗТ), сцинтиграфический метод определения рецепторов соматостатина, эндоскопические исследования, но до сих пор не определено, какие из них наиболее информативны для визуализации первичных опухолей или метастазов в печени, а также для выявления внепеченочного и экстраабдоминального распространения опухоли.
Хирургический метод лечения НЭО органов брюшной полости и забрюшинного пространства является основным. Большинство авторов считают, что: при опухолях 0,05).
По локализации опухоли больные распределились следующим образом: желудок — 50 (16,2 %) наблюдений, тонкая кишка — 36 случаев (11,7 %), червеобразный отросток — 25 (8,1 %), ободочная кишка — 23 (7,5 %), прямая кишка — 24 (7,9 %), поджелудочная железа — 46 (14,9 %), печень — 16 (5,2 %) наблюдений, надпочечники — 26 (8,4 %) случаев, внеорганные забрюшинные опухоли — 18 (5,8 %), яичники — 12 (3,9 %), почка — 9 (2,9 %) и метастазы НЭО без выявленного первичного очага — 23 (7,5 %) наблюдения.
Частота карциноидного синдрома составила 15,6 % (48 пациентов), при этом его развитие в начале заболевания наблюдалось в 32 случаях (10,4 %) и в 16 (5,2 %) — при прогрессировании опухолевого процесса.
Первично-множественные НЭО выявлены у 29 больных (9,4 %): 13 (44,8 %) синхронных и 16 (55,2 %) метахронных опухолей. Из метахронных опухолей наиболее часто встречались рак молочной железы и меланома кожи (3 и 2 наблюдения соответственно); из синхронных — рак толстой кишки и НЭО других локализаций (по 4 наблюдения соответственно).
Наиболее часто первично-множественные опухоли развивались при НЭО яичников — 4 (33,3 %) и тонкой кишки — 7 (19,4 %).
Для выявления локализации первичной опухоли использовались как неинвазивные: рентгенография, УЗТ, КТ, гастроскопия, колоноскопия, ректороманоскопия, так и инвазивные методы исследования: РПХГ, ангиография. Наиболее часто для диагностики НЭО использовались УЗТ органов брюшной полости и забрюшинного пространства (50,6 %), КТ (36,7 %), ангиография (30,8 %) и гастроскопия (29,9 %). Частота применения метода менялась в зависимости от локализации опухоли. Для визуализации опухолей желудка основными методами диагностики являлись гастроскопия и рентгенография желудка, толстой кишки — колоноскопия и ирригография; поджелудочной железы, тонкой кишки, надпочечников и опухолей забрюшинного пространства — УЗТ, КТ и ангиография.
Противоопухолевое лечение получили 304 пациента (98,7 %). Из них только хирургическое 214 больных (70,1 %), у 60 (20,1 %) операция дополнялась химиотерапией, у 10 операция сочеталась с лучевой терапией (3,3 %), у 6 пациентов в послеоперационном периоде проводилась химиолучевая терапия (2,0 %). Консервативное лечение получили 14 пациентов (4,9 %): химиотерапию — 13 больных (4,6 %), из них у 2 она сочеталась с химиоэмболизацией печени, и у 1 пациента (0,3 %) проведена только лучевая терапия. Симптоматическую терапию получили 4 пациента (1,3 %).
Радикальные операции выполнены 201 больному (65,3 %), паллиативные — в 34 (11,0 %), диагностические — в 33 (10,7 %), пробные — в 23 наблюдениях (7,5 %), и в 2 случаях оперативное лечение выполнялось по другому поводу (0,7 %) и НЭО выявлена интраоперационно.
Отдаленные результаты оценивались на 01.01.2008 года. На момент оценки отдаленных результатов лечения 216 больных живы (70,1 %), 50 умерли (16,2 %) и 42 вышли из-под наблюдения (13,6 %). Метастазы развились у 153 пациентов (49,7 %): одиночные — в 98 наблюдениях (64,0 %), множественные — в 55 (36,0 %). Наиболее часто диссеминированный опухолевый процесс отмечался при локализации опухоли в тонкой кишке (20,0 %), поджелудочной железе (17,5 %), желудке (16,3 %) и ободочной кишке (15,0 %), а наименьший процент диссеминированных опухолей отмечен для червеобразного отростка (2,5 %) и надпочечников (3,8 %).
Метастазы на момент постановки диагноза выявлены у 61 (21,4 %) пациента. При этом на момент постановки диагноза 52,2 % больных с опухолью ободочной кишки, 44,4 % — с опухолью тонкой кишки и только 2 % пациентов с опухолью червеобразного отростка имели диссеминированное заболевание. Рецидивные опухоли выявлены у 27 больных (8,8 %).
В послеоперационном периоде с целью верификации диагноза производилось гистологическое исследование удаленной опухоли или биопсийного материала. Гистологический диагноз НЭО подтвержден у 300 (97,4 %) пациентов; у 8 (2,6 %) больных диагноз верифицирован только при цитологическом исследовании.
По гистологическому строению опухоли представляли собой: карциноиды — 229 наблюдений (76,9 %), феохромоцитомы (ФХ) — 26 (7,5 %) наблюдений, параганглиомы (ПГ) — 18 (4,9 %), в 4-ю группу вошли опухоли, которые на светооптическом уровне было трудно дифференцировать между раком и карциноидом, — 22 (7,8 %) и 5-ю группу составили опухоли диморфного строения (рак + карциноид) — 9 наблюдений (2,9 %).
В случае возникновения трудностей диагностического плана, а также для решения поставленных задач, связанных с изучением степени ультраструктурной дифференцировки опухоли, оценкой пролиферативной активности и установлением гистогенетической принадлежности опухоли было использовано ЭМИ. Материалом для ЭМИ послужили 84 (27,3 %) наблюдения. Анализ проводили на основании ранее разработанной ультраструктурной классификации опухолей человека (Н.Т. Райхлин, 1991).
Для уточнения диагноза и учитывая диагностические трудности, возникшие при светооптическом исследовании НЭО, проводилось ИГХ-определение иммунофенотипа опухолевых клеток. ИГХ-исследование проводилось на 37 опухолях (12,0 %), наиболее сложных в плане дифференциальной диагностики. Для этой цели была использована панель моноклональных и поликлональных антител: маркеры нейроэндокринной дифференцировки — синаптофизин, хромогранин А, СD56; широкий спектр цитокератинов (ЦК) — (А1/А3), ЦК 7, ЦК 19 и ЦК 20; эпителиально-мембранный антиген (ЭМА), виментин (Вим), антитела к гормонам — инсулину, глюкагону, соматостатину, гастрину, серотонину, панкреатическому полипептиду, кальцитонину и адренокортикотропному гормону (АКТГ). Гистогенез опухоли установлен во всех случаях.
Определение индекса пролиферации Ki 67 и индекса PCNA вычислялось как среднее от числа меченых на 100 учтенных ядер (при подсчете 500–1000 опухолевых клеток).
Клиническая лабораторная диагностика НЭО основывается на изучении уровня серотонина, гистамина в крови и 5-оксииндолуксусной кислоты (5-ОИУК) в моче. Концентрации гистамина и серотонина определены у 65 пациентов (24,1 %), экскреция 5-ОИУК в суточной моче определена у 34 (12,6 %) пациентов. Экскреция адреналина, норадреналина (НА) и дофамина (ДОФА) в суточной моче определена у 32 (84,2 %) пациентов с катехоламинсекретирующими опухолями.
Определение содержания VEGF (фактор роста эндотелия сосудов), TNF- b (фактор некроза опухоли) и эндостатина в сыворотке крови проводили иммуноферментным методом при использовании реактивов фирмы R&D (США) для VEGF и эндостатина, и Bender MedSystems (Австрия) для TNF- b.
Определение концентрации VEGF, эндостатина и TNF- b в сыворотке крови выполнено у 20 больных НЭО органов брюшной полости и забрюшинного пространства. В контрольную группу вошли 25 практически здоровых испытуемых.
Статистическая обработка материала производилась при помощи компьютерных программ Excel, SAS (версия 11.0, Чикаго, штат Иллинойс), на основе созданной базы данных Paradox. Анализ кривых выживаемости проводился методом Kaplan — Meier, сравнение кривых выживаемости проводилось методом log-rank. Достоверными считались различия с вероятностью не менее 95 % (р 100 нг/мл и TNF- b Список литературы
1. Кушлинский Н.Е., Бритвин Т.А., Казанцева И.А. и др. Интерлейкин-6 в сыворотке крови больных с опухолями надпочечников // Бюллетень экспериментальной биологии и медицины. — 2004. — Т. 137, № 3. — С. 309-312.
2. Бритвин Т.А., Кушлинский Н.Е., Казанцева И.А. и др. Сравнительное исследование уровней интерлейкина-6 в сыворотке больных с опухолями надпочечников // Вестник РОНЦ им. Н.Н. Блохина РАМН. — 2005. — № 1–2. — С. 17-20.
3. Пирогова М.С., Поликарпова С.Б. Результаты хирургического лечения эндокринно-клеточных опухолей желудочно-кишечного тракта // Вестник РГМУ. — 2008. — № 2 (61). — С. 132.
4. Поликарпова С.Б., Кушлинский Н.Е., Любимова Н.В. и др. VEGF, эндостатин, TNF- b в сыворотке крови больных нейроэндокринными опухолями органов брюшной полости // Вопросы биологической, медицинской и фармацевтической химии. — 2009. — № 6. — С. 21-24.
- Причины развития
- Особенности нейроэндокринных опухолей
- Классификация нейроэндокринных опухолей
- Виды нейроэндокринных опухолей и их симптоматика
- Диагностика заболевания
- Лечение
- Прогноз выживаемости
Нейроэндокринные опухоли (НЭО) образуются из апудоцитов, или APUD-клеток. Эти клетки разбросаны по всему организму и составляют самую древнюю часть эндокринной системы. Они одновременно похожи на нервные клетки и клетки желез внутренней секреции, так как могут реагировать на сигналы извне или изменения состояния организма, способны производить гормоны, выполняющие разные функции.
Опухоли APUD-системы встречаются редко, и их бывает сложно диагностировать. Чаще всего они возникают в желудочно-кишечном тракте, но могут поражать и другие органы. Особенность нейроэндокринных новообразований в том, что опухолевые клетки производят повышенное количество гормонов, и из-за этого могут возникать определенные симптомы.
Согласно данным американского реестра SEER, в 2004 году заболеваемость нейроэндокринными опухолями в США составила 5 случаев на 100 тысяч населения. В России статистика, к сожалению, отсутствует, но, вероятно, заболеваемость находится на аналогичном уровне.
По данным американских экспертов, распространенность нейроэндокринных опухолей ежегодно растет. В первую очередь это связывают с изменениями в характере питания, неблагоприятной экологической обстановкой.
По данным все того же реестра SEER, новообразования APUD-системы часто диагностируются на поздних стадиях: в 50% случаев опухоль успевает распространиться на окружающие ткани, в регионарные лимфоузлы, дать отдаленные метастазы.
Причины развития
У некоторых людей нейроэндокринные опухоли возникают в результате генетических заболеваний:
- Множественная эндокринная неоплазия (МЭН, MEN) вызвана мутацией в гене MEN, RET или CDKN1B. У больных может развиваться множество нейроэндокринных новообразований и опухолей в железах внутренней секреции. Некоторые из этих опухолей доброкачественные, некоторые — злокачественные. Выделяют четыре типа множественной эндокринной неоплазии: MEN1, MEN2A, MEN2B и MEN4. При MEN1 чаще всего возникают нейроэндокринные опухоли в паращитовидных железах, поджелудочной железе, гипофизе, иногда в пищеварительном тракте и легких. У большинства пациентов с MEN2A и MEN2B обнаруживают медуллярные карциномы (разновидность опухоли щитовидной железы), в некоторых случаях — аденомы паращитовидных желез, феохромоцитому. При MEN4 чаще всего встречаются аденомы гипофиза и паращитовидных желез.
- Болезнь Гиппеля-Линдау возникает при мутации в гене VHL. У больных в разных частях тела развиваются кисты и опухоли. Среди этих опухолей встречаются нейроэндокринные, в том числе НЭО поджелудочной железы, феохромоцитома.
- Нейрофиброматоз I типа вызван мутацией в гене NF1. Некоторые люди получают эту мутацию от родителей, у других она возникает спонтанно. Основное проявление заболевания — множество доброкачественных новообразований нервов и кожи. Повышен риск развития опухолей APUD-системы в желудочно-кишечном тракте, поджелудочной железе, феохромоцитомы.
- Туберозный склероз приводит к возникновению доброкачественных новообразований в разных органах, включая кожу, глаза, головной мозг, сердце, легкие, почки. Повышен риск развития НЭО.
У людей, которые не являются носителями этих мутаций, нейроэндокринные новообразования тоже могут возникать. Причины до конца не известны. Многие исследования показали, что одним из важнейших факторов риска является наследственность. Если в семье есть люди, у которых была обнаружена нейроэндокринная опухоль, то у остальных членов риски тоже повышены, особенно у ближайших родственников больных (родителей, детей, сестер и братьев). Кроме того, риск опухолей APUD-системы повышен в семьях с отягощенным анамнезом по раку толстой кишки, молочной железы, легкого.
Известны и другие факторы риска, но их роль нельзя считать полностью доказанной:
- Курение может способствовать развитию нейроэндокринных опухолей в легких, желудке, тонкой кишке и поджелудочной железе.
- Хронический атрофический гастрит, как показали некоторые исследования, способствует развитию НЕО в желудке.
- Сахарный диабет связывают с возникновением новообразований APUD-системы в поджелудочной железе, желудке.
Ученые пока не могут сказать, повышаются ли риски при частом употреблении алкоголя, нездоровом питании (много животных жиров), у людей с лишним весом. Нужны дополнительные исследования.
Особенности нейроэндокринных опухолей
Нейроэндокринные клетки не привязаны к какому-либо конкретному органу. Они разбросаны по всему организму. Хотя опухоли чаще всего и возникают в пищеварительном тракте, в более редких случаях они обнаруживаются и в других местах. В 15% случаев найти первичную опухоль не удается.
Нейроэндокринные опухоли могут производить гормоны, которые вызывают в органах определенные эффекты, и из-за этого пациент испытывает те или иные симптомы. Такие новообразования называют функционирующими. Если гормоны не вырабатываются — это нефункционирующая опухоль.
Классификация нейроэндокринных опухолей
Существуют разные классификации нейроэндокринных опухолей. Ниже в таблице представлены основные группы:
Стадию нейроэндокринных опухолей определяют в соответствии с общепринятой системой TNM:
- T — размер первичной опухоли, ее прорастание в окружающие ткани.
- N — поражение регионарных (близлежащих по отношению к опухоли) лимфатических узлов.
- M — наличие отдаленных метастазов.
Классификация по стадиям различается в зависимости от того, в каком органе находится нейроэндокринное новообразование. Например, стадию опухоли APUD-системы в легком определяют так же, как для немелкоклеточного рака легкого. Для нейроэндокринных новообразований в желудке, тонкой кишке, червеобразном отростке, ободочной, прямой кишке и поджелудочной железе разработаны собственные системы классификации по стадиям.
Виды нейроэндокринных опухолей и их симптоматика
Так как существуют разные типы нейроэндокринных опухолей, и они могут находиться в разных органах, то и симптомы различаются. Можно выделить три основные группы проявлений. Первая — это общие симптомы, характерные для любого типа рака: слабость, повышенная утомляемость, снижение аппетита, потеря веса без видимой причины.

Вторая группа симптомов связана с локализацией опухоли и ее размерами, сдавлением анатомических структур и нарушением функции пораженного органа. Беспокоят боли в определенной части тела, тошнота, упорный хронический кашель, расстройства стула, мочеиспусканий, кровотечения, необычные выделения. При поражении печени, желчных протоков, поджелудочной железы развивается механическая желтуха.
Третья группа симптомов вызвана гормонами, которые продуцируют нейроэндокринные клетки:
- диарея — жидкий стул более трех раз в сутки;
- постоянная жажда, голод, частые мочеиспускания, — признаки повышения уровня глюкозы в крови;
- повышенная утомляемость, раздражительность, дрожь, головокружение, судороги, потери сознания — признаки снижения уровня глюкозы в крови;
- язвенная болезнь, которая не поддается лечению;
- тревожность;
- сыпь на коже.
Желудочно-кишечный тракт — наиболее распространенное место локализации нейроэндокринных опухолей. Такие новообразования часто называют карциноидными опухолями. Частота поражения разных отделов пищеварительного тракта:
- тонкая кишка — 39%;
- прямая кишка — 15%;
- червеобразный отросток (аппендикс) — 7%;
- толстая кишка — 5–7%;
- желудок — 2–4%.
Опухоли в пищеварительном тракте вызывают классический карциноидный синдром. Он проявляется в виде покраснения и ощущения тепла в области лица, диареей, одышкой, симптомами, напоминающими бронхиальную астму, слабостью, учащенным сердцебиением, увеличением веса без видимой причины, высоким артериальным давлением, его частыми колебаниями.
Вторым по частоте местом локализации опухолей APUD-системы после НЭО ЖКТ являются легкие. Примерно в 30% случаев нейроэндокринное новообразование возникает в бронхиальной системе.
Феохромоцитома — опухоль надпочечников (иногда в других частях тела), которая вырабатывает гормоны стресса: адреналин и норадреналин. В результате избыточного уровня гормонов возникают приступы (кризы), во время которых человек испытывает беспокойство, страх, озноб, дрожь, головную боль и боль в грудной клетке, его кожа становится бледной, учащается сердцебиение, возникают экстрасистолы, тошнота, рвота.
Рак из клеток Меркеля — злокачественная опухоль кожи. Она встречается очень редко, но отличается высокой агрессивностью, рано распространяется в лимфатические узлы, метастазирует. Патология проявляется в виде одного или нескольких узелков на коже красного и синюшного цвета. Они могут изъязвляться. Рак из клеток Меркеля сложно диагностировать, зачастую его выявляют уже на поздних стадиях.
Диагностика заболевания
В большинстве случаев нейроэндокринные новообразования обнаруживаются случайно, когда человек проходит обследование по другому поводу. Опухоль можно обнаружить с помощью таких методов диагностики, как:
- Ультразвуковое исследование.
- Эндоскопические исследования: гастроскопия, колоноскопия, бронхоскопия.
- Рентгенография с контрастным усилением. Перед исследованием пациенту дают выпить раствор, который помогает четко увидеть контуры желудка, кишечника.
Диагноз подтверждается с помощью биопсии. Обнаружив патологическое образование, врач удаляет из него фрагмент ткани и отправляет в лабораторию для исследования под микроскопом. Если опухоль предположительно является феохромоцитомой, к биопсии прибегают только в крайних случаях, так как она сопряжена с серьезными рисками.
Компьютерная томография и МРТ помогают обнаружить опухоль, оценить ее размеры, локализацию, степень распространения в организме, обнаружить метастатические очаги. Для поиска метастазов применяют ПЭТ-сканирование. Врач может назначить анализы, которые помогают обнаружить гормоны, вырабатываемые опухолью, например, исследование мочи на 5-HIAA — продукт обмена серотонина. Определение уровня хромогранина А в крови помогает контролировать эффективность лечения.
Лечение
Выбор лечения зависит от типа опухоли, ее локализации, степени злокачественности, стадии. В некоторых случаях, если нейроэндокринное новообразование является высокодифференцированным и практически не растет, врач назначает активное наблюдение. Нужно периодически являться на осмотры, проходить КТ, МРТ, сдавать анализы крови. Как только появляются признаки роста или распространения в организме, начинают активное лечение.
В большинстве случаев нейроэндокринные новообразования успешно лечатся хирургическим путем. Во время операции удаляют саму опухоль и некоторое количество окружающих тканей. Затем удаленный материал изучают в лаборатории. Если получен негативный край резекции, это означает, что опухолевая ткань удалена полностью.
Если радикальное вмешательство невозможно, может быть выполнена циторедуктивная операция, во время которой стараются удалить как можно большее количество опухолевой ткани.
Если у пациента имеются признаки карциноидного синдрома, есть риск, что его состояние во время операции может сильно ухудшиться. Врач-анестезиолог должен быть осведомлен о такой возможности и принять необходимые меры.
При неоперабельных опухолях назначают медикаментозное лечение, лучевую терапию. Применяют различные виды химиопрепаратов, таргетные препараты, иммунотерапию. Терапия аналогами соматостатина помогает справиться с симптомами и замедлить рост опухоли.
Если нейроэндокринные опухолевые очаги имеются в печени, может быть проведена радиочастотная аблация, эмболизация артерии, питающей опухоль. Врачи Европейской клиники обладают большим опытом в проведении таких вмешательств.
Прогноз выживаемости
Прогноз зависит от того, какой вид опухоли был диагностирован, насколько она агрессивна, на какой стадии находится. Лечение преследует одну из двух целей:
- Полностью удалить опухолевые очаги. Если по результатам обследований не выявляются признаки присутствия опухоли в организме, констатируют ремиссию.
- Избавить пациента от симптомов и сдержать рост новообразования. При этом больной может прожить довольно долго.
Стоит поговорить с врачом перед началом лечения, спросить, какой будет цель, какого результата можно ожидать, и что планируется делать в случае, если ситуация ухудшится, опухоль рецидивирует.
Читайте также:

